Л28_ Электрохимия_ПМ_2015.pptx
- Количество слайдов: 26
 Электрохимические методы анализа Лекция 29. Потенциометрический метод анализа Лектор к. х. н. , доцент Ю. Ю. Петрова
Электрохимические методы анализа Лекция 29. Потенциометрический метод анализа Лектор к. х. н. , доцент Ю. Ю. Петрова
 Мембранный потенциал Ем + а 2 – внутренний раствор + + Е 2 + М + + + Е 1 а 1 – анализируемый раствор Активность ионов А+ во внутреннем растворе постоянна, поэтому:
Мембранный потенциал Ем + а 2 – внутренний раствор + + Е 2 + М + + + Е 1 а 1 – анализируемый раствор Активность ионов А+ во внутреннем растворе постоянна, поэтому:
 Селективность мембранного электрода Любая мембрана в той или иной мере проницаема для всех ионов одного вида, находящихся в растворе, и поэтому необходимо учитывать влияние посторонних ионов, например В+, на потенциал электрода. Ионы В+ проникают в фазу мембраны в результате реакции обмена: Константа равновесия этой реакции (константа обмена, КА-В) зависит от природы мембраны и природы иона В+.
Селективность мембранного электрода Любая мембрана в той или иной мере проницаема для всех ионов одного вида, находящихся в растворе, и поэтому необходимо учитывать влияние посторонних ионов, например В+, на потенциал электрода. Ионы В+ проникают в фазу мембраны в результате реакции обмена: Константа равновесия этой реакции (константа обмена, КА-В) зависит от природы мембраны и природы иона В+.
 Селективность мембранного электрода n Потенциал мембранного электрода в растворе, содержащем кроме определяемого иона А посторонние ионы В, С и другие, описывается модифицированным уравнением Нернста (уравнением Никольского): n n n где z. A — целое число, по знаку и величине равное заряду иона А (зарядовое число); z. B, zc — то же, для ионов В и С; kпот — потенциометрический коэффициент селективности; const включает значения потенциалов внешнего и внутреннего электродов сравнения и зависит от природы мембраны, поскольку включает величину граничного потенциала на внутренней стороне мембраны.
Селективность мембранного электрода n Потенциал мембранного электрода в растворе, содержащем кроме определяемого иона А посторонние ионы В, С и другие, описывается модифицированным уравнением Нернста (уравнением Никольского): n n n где z. A — целое число, по знаку и величине равное заряду иона А (зарядовое число); z. B, zc — то же, для ионов В и С; kпот — потенциометрический коэффициент селективности; const включает значения потенциалов внешнего и внутреннего электродов сравнения и зависит от природы мембраны, поскольку включает величину граничного потенциала на внутренней стороне мембраны.
 Потенциометрический коэффициент селективности: отражает относительное влияние ионов А и В на величину мембранного потенциала и характеризует способность мембраны различать ионы А и В, А и С и т. д. u. A и uв - подвижности ионов А и В в фазе мембраны.
Потенциометрический коэффициент селективности: отражает относительное влияние ионов А и В на величину мембранного потенциала и характеризует способность мембраны различать ионы А и В, А и С и т. д. u. A и uв - подвижности ионов А и В в фазе мембраны.
 Основными характеристиками ионселективного электрода являются: n электродная функция, n селективность, n время отклика.
Основными характеристиками ионселективного электрода являются: n электродная функция, n селективность, n время отклика.
 Электродная функция Электрод имеет нернстовскую электродную функцию в интервале активности (концентрации), где зависимость потенциала от р. А (-lga. A ) линейна и имеет угловой коэффициент 59, 16/z. A м. В (25 °С). Протяженность этого интервала зависит от природы мембраны.
Электродная функция Электрод имеет нернстовскую электродную функцию в интервале активности (концентрации), где зависимость потенциала от р. А (-lga. A ) линейна и имеет угловой коэффициент 59, 16/z. A м. В (25 °С). Протяженность этого интервала зависит от природы мембраны.
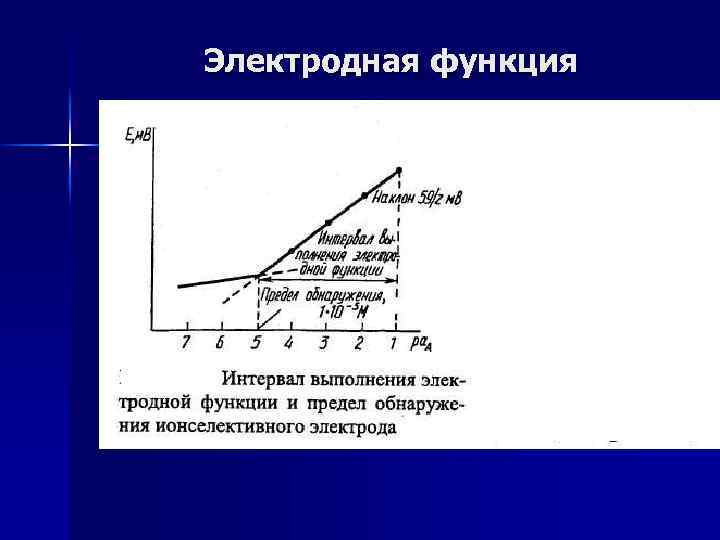 Электродная функция
Электродная функция
 Селективность электрода определяется величиной k пот. А. В Если величина kпот. А. В < 1 электрод селективен относительно ионов А. n Чем меньше числовая величина kпот. А. В тем выше селективность. n
Селективность электрода определяется величиной k пот. А. В Если величина kпот. А. В < 1 электрод селективен относительно ионов А. n Чем меньше числовая величина kпот. А. В тем выше селективность. n
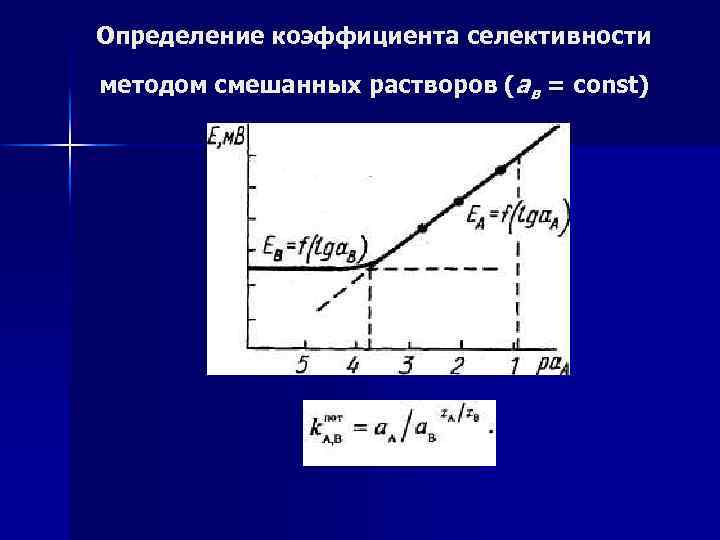 Определение коэффициента селективности методом смешанных растворов (ав = const)
Определение коэффициента селективности методом смешанных растворов (ав = const)
 Время отклика (время установления стационарного потенциала) определяют по зависимости потенциала электрода от времени с момента погружения в анализируемый раствор. В зависимости от природы мембраны время отклика может колебаться от нескольких секунд до нескольких минут.
Время отклика (время установления стационарного потенциала) определяют по зависимости потенциала электрода от времени с момента погружения в анализируемый раствор. В зависимости от природы мембраны время отклика может колебаться от нескольких секунд до нескольких минут.
 Классификация ионселективных электродов 1) первичные ионселективные электроды — 2) электроды с подвижными носителями — 3) сенсибилизированные (активированные) электроды с кристаллическими мембранами, электроды с жесткой матрицей (стеклянные); положительно заряженными, отрицательно заряженными, незаряженными (с «нейтральными переносчиками» ); электроды — газочувствительные, ферментные.
Классификация ионселективных электродов 1) первичные ионселективные электроды — 2) электроды с подвижными носителями — 3) сенсибилизированные (активированные) электроды с кристаллическими мембранами, электроды с жесткой матрицей (стеклянные); положительно заряженными, отрицательно заряженными, незаряженными (с «нейтральными переносчиками» ); электроды — газочувствительные, ферментные.
 1. Электроды с кристаллическими мембранами Кристаллические гомогенные мембраны изготовляют из индивидуального кристаллического соединения (La. F 3, Ag 2 S, Ag. Cl) или гомогенной смеси кристаллических веществ (Ag 2 S + Ag. Cl, Ag 2 S + Cu. S, Ag 2 S + Cd. S).
1. Электроды с кристаллическими мембранами Кристаллические гомогенные мембраны изготовляют из индивидуального кристаллического соединения (La. F 3, Ag 2 S, Ag. Cl) или гомогенной смеси кристаллических веществ (Ag 2 S + Ag. Cl, Ag 2 S + Cu. S, Ag 2 S + Cd. S).
 1. Электроды с кристаллическими мембранами Электрическая проводимость этих мембран обусловлена способностью иона решетки с наименьшим радиусом и зарядом перемещаться по вакансиям решетки. Для кристаллических мембран характерна высокая специфичность. Низкая растворимость материала мембраны (La. F 3, Ag 2 S + Cu. S) позволяет достигать очень низких пределов обнаружения.
1. Электроды с кристаллическими мембранами Электрическая проводимость этих мембран обусловлена способностью иона решетки с наименьшим радиусом и зарядом перемещаться по вакансиям решетки. Для кристаллических мембран характерна высокая специфичность. Низкая растворимость материала мембраны (La. F 3, Ag 2 S + Cu. S) позволяет достигать очень низких пределов обнаружения.
 F - - селективный электрод
F - - селективный электрод
 1. Электроды с жесткой матрицей Стеклянные мембраны изготовляют из специальных стекол, подбирая их состав так, чтобы мембрана проявляла повышенную селективность к определенному иону и позволяла определять его в присутствии других. Первым ионселективным электродом был стеклянный электрод для измерения р. Н.
1. Электроды с жесткой матрицей Стеклянные мембраны изготовляют из специальных стекол, подбирая их состав так, чтобы мембрана проявляла повышенную селективность к определенному иону и позволяла определять его в присутствии других. Первым ионселективным электродом был стеклянный электрод для измерения р. Н.
 Стеклянный электрод для измерения р. Н Главной частью электрода является тонкая р. Н-чувствительная мембрана. Обычно ее изготовляют из стекла, содержащего 22% оксида натрия, 6% оксида кальция и 72% оксида кремния. Внутренним раствором служит 0, 1 М раствор соляной кислоты, насыщенный хлоридом серебра. Чувствительностью к ионам водорода обладает только хорошо вымоченная мембрана.
Стеклянный электрод для измерения р. Н Главной частью электрода является тонкая р. Н-чувствительная мембрана. Обычно ее изготовляют из стекла, содержащего 22% оксида натрия, 6% оксида кальция и 72% оксида кремния. Внутренним раствором служит 0, 1 М раствор соляной кислоты, насыщенный хлоридом серебра. Чувствительностью к ионам водорода обладает только хорошо вымоченная мембрана.
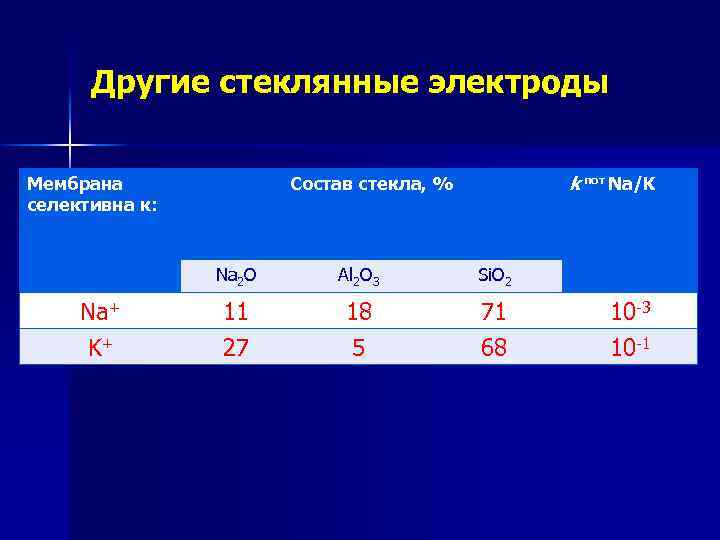 Другие cтеклянные электроды Мембрана селективна к: k пот Na/K Состав стекла, % Na 2 O Al 2 O 3 Si. O 2 Na+ 11 18 71 10 -3 K+ 27 5 68 10 -1
Другие cтеклянные электроды Мембрана селективна к: k пот Na/K Состав стекла, % Na 2 O Al 2 O 3 Si. O 2 Na+ 11 18 71 10 -3 K+ 27 5 68 10 -1
 Стеклянный электрод для измерения р. Н
Стеклянный электрод для измерения р. Н
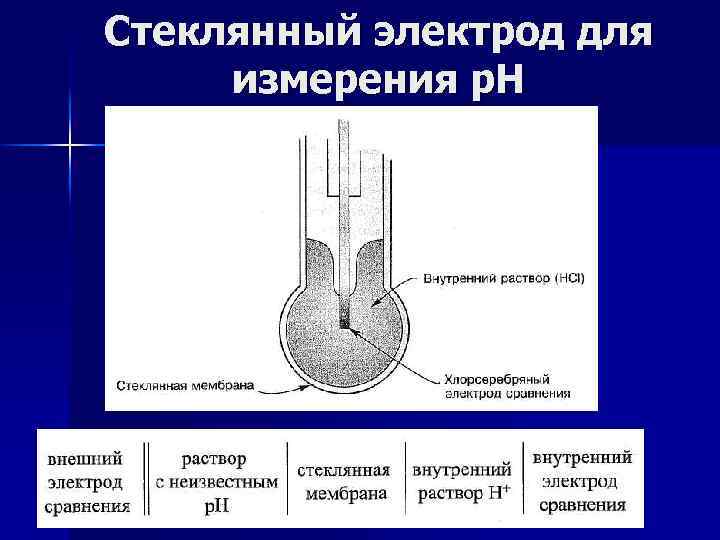 Стеклянный электрод для измерения р. Н
Стеклянный электрод для измерения р. Н
 В гидратированном слое на внешней поверхности мембраны ионы Na+ замещаются ионами Н+ из раствора:
В гидратированном слое на внешней поверхности мембраны ионы Na+ замещаются ионами Н+ из раствора:
 Стеклянный электрод для измерения р. Н Потенциал хорошо вымоченного стеклянного электрода описывается уравнением n т. е. электрод обладает водородной функцией. В слагаемое const входят величины потенциалов внешнего и внутреннего электродов сравнения и j-потенциал асимметрии.
Стеклянный электрод для измерения р. Н Потенциал хорошо вымоченного стеклянного электрода описывается уравнением n т. е. электрод обладает водородной функцией. В слагаемое const входят величины потенциалов внешнего и внутреннего электродов сравнения и j-потенциал асимметрии.
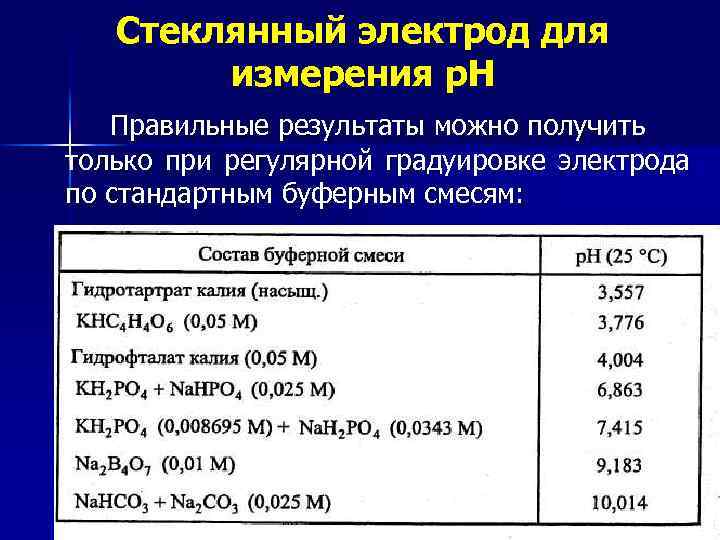 Стеклянный электрод для измерения р. Н Правильные результаты можно получить только при регулярной градуировке электрода по стандартным буферным смесям:
Стеклянный электрод для измерения р. Н Правильные результаты можно получить только при регулярной градуировке электрода по стандартным буферным смесям:
 Стеклянный электрод для измерения р. Н Стеклянный электрод пригоден для правильного измерения р. Н в ограниченном интервале р. Н, зависящем от состава стекла. Предполагается, что неправильные результаты в сильнокислых растворах обусловлены разрушением стекла. Знак погрешности измерения р. Н в щелочных растворах указывает на то, что электрод реагирует не только на ионы Н+, но и на ионы К+ и других щелочных металлов.
Стеклянный электрод для измерения р. Н Стеклянный электрод пригоден для правильного измерения р. Н в ограниченном интервале р. Н, зависящем от состава стекла. Предполагается, что неправильные результаты в сильнокислых растворах обусловлены разрушением стекла. Знак погрешности измерения р. Н в щелочных растворах указывает на то, что электрод реагирует не только на ионы Н+, но и на ионы К+ и других щелочных металлов.
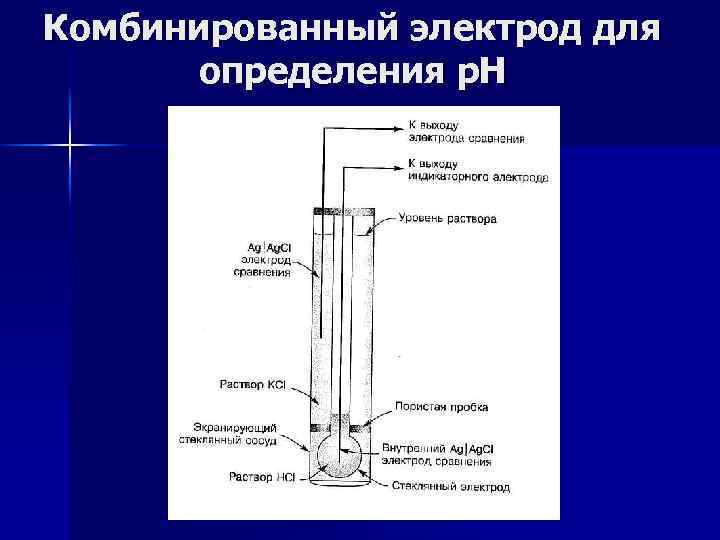 Комбинированный электрод для определения р. Н
Комбинированный электрод для определения р. Н
 Стандартный р. Н-метр (Denver Instrument Company)
Стандартный р. Н-метр (Denver Instrument Company)


