Электрохимические методы.pptx
- Количество слайдов: 52
 ЭЛЕКТРОХИМИЧЕСКИЕ МЕТОДЫ АНАЛИЗА 1. Классификация электрохимических методов анализа 2. Общая характеристика и виды электродов. 3. Потенциометрический метод анализа
ЭЛЕКТРОХИМИЧЕСКИЕ МЕТОДЫ АНАЛИЗА 1. Классификация электрохимических методов анализа 2. Общая характеристика и виды электродов. 3. Потенциометрический метод анализа
 ВОПРОС 1. Классификация электрохимиченских методов анализа.
ВОПРОС 1. Классификация электрохимиченских методов анализа.
 Достоинства электрохимических методов: 1. Высокая чувствствительность (полярография, кулонометрия), 2. Широкий интервал определяемых концентраций (1 - 10 -9 моль/л), 3. Избирательность и экспрессность (ионометрия, электрогравиметрия), 4. Относительная простота выполнения и невысокая стоимость аппаратуры (кондуктометрия, потенциометрия), 5. Возможность концентрирования в рамках самого метода (инверсионная вольтамперометрия) или в сочетании с другими методами (например, с хроматографией, экстракцией), 6. Легкость автоматизации.
Достоинства электрохимических методов: 1. Высокая чувствствительность (полярография, кулонометрия), 2. Широкий интервал определяемых концентраций (1 - 10 -9 моль/л), 3. Избирательность и экспрессность (ионометрия, электрогравиметрия), 4. Относительная простота выполнения и невысокая стоимость аппаратуры (кондуктометрия, потенциометрия), 5. Возможность концентрирования в рамках самого метода (инверсионная вольтамперометрия) или в сочетании с другими методами (например, с хроматографией, экстракцией), 6. Легкость автоматизации.
 КЛАССИФИКАЦИЯ по измеряемому электрическому параметру 1. Полярография – основана на получении и использовании зависимости между силой постоянного тока и напряжением, подаваемым на электроды. В качестве индикаторного электрода используют ртутный капающий электрод. 2. Потенциометрия – основана на измерении потенциала индикаторного электрода в зависимости от концентрации определяемого иона. 3. Кулонометрия – основана на измерении количества электричества, израсходованного на электролиз определяемого вещества. , 4. Кондуктометрия – основана на изучении зависимости между электропроводностью раствора и концентрацией в нем ионов.
КЛАССИФИКАЦИЯ по измеряемому электрическому параметру 1. Полярография – основана на получении и использовании зависимости между силой постоянного тока и напряжением, подаваемым на электроды. В качестве индикаторного электрода используют ртутный капающий электрод. 2. Потенциометрия – основана на измерении потенциала индикаторного электрода в зависимости от концентрации определяемого иона. 3. Кулонометрия – основана на измерении количества электричества, израсходованного на электролиз определяемого вещества. , 4. Кондуктометрия – основана на изучении зависимости между электропроводностью раствора и концентрацией в нем ионов.
 1. 2. 3. КЛАССИФИКАЦИЯ ПО ЭЛЕКТРОДНЫМ ПРОЦЕССАМ методы, основанные на протекании электродной реакции (потенциометрия, , кулонометрия и др. ) методы, не связанные с протеканием электродной реакции (кондуктометрия). КЛАССИФИКАЦИЯ ПО СПОСОБУ ВЫПОЛНЕНИЯ АНАЛИЗА: прямые методы (прямая потенциометрия, ионометрия, кулонометрия, вольтамперометрия и др. ); косвенные методы (инструментальное титрование); инверсионные методы (инверсионная вольтамперометрия и др. ).
1. 2. 3. КЛАССИФИКАЦИЯ ПО ЭЛЕКТРОДНЫМ ПРОЦЕССАМ методы, основанные на протекании электродной реакции (потенциометрия, , кулонометрия и др. ) методы, не связанные с протеканием электродной реакции (кондуктометрия). КЛАССИФИКАЦИЯ ПО СПОСОБУ ВЫПОЛНЕНИЯ АНАЛИЗА: прямые методы (прямая потенциометрия, ионометрия, кулонометрия, вольтамперометрия и др. ); косвенные методы (инструментальное титрование); инверсионные методы (инверсионная вольтамперометрия и др. ).
 Электрический потенциал- это работа по перемещению единичного положительного заряда из данной точки пространства в бесконечность. Абсолютное значение потенциала электрода определить нельзя. Можно лишь сравнивать потенциалы различных электродов друг с другом объединив два электрода в электрохимическую цепь.
Электрический потенциал- это работа по перемещению единичного положительного заряда из данной точки пространства в бесконечность. Абсолютное значение потенциала электрода определить нельзя. Можно лишь сравнивать потенциалы различных электродов друг с другом объединив два электрода в электрохимическую цепь.
 Схематически такую цепь изображают следующим образом: Индикаторный Анализируемый Солевой Электрод электрод сравнения раствор мостик Солевой мостик служит для предотвращения смешивания анализируемого раствора и раствора электрода сравнения. В качестве солевого мостика используют насыщенные растворы солей KCl, КNО 3 и других с близкими значениями подвижностей катиона и аниона. Это позволяет снизить диффузионный потенциал Едиф жидкостного соединения практически до нуля.
Схематически такую цепь изображают следующим образом: Индикаторный Анализируемый Солевой Электрод электрод сравнения раствор мостик Солевой мостик служит для предотвращения смешивания анализируемого раствора и раствора электрода сравнения. В качестве солевого мостика используют насыщенные растворы солей KCl, КNО 3 и других с близкими значениями подвижностей катиона и аниона. Это позволяет снизить диффузионный потенциал Едиф жидкостного соединения практически до нуля.
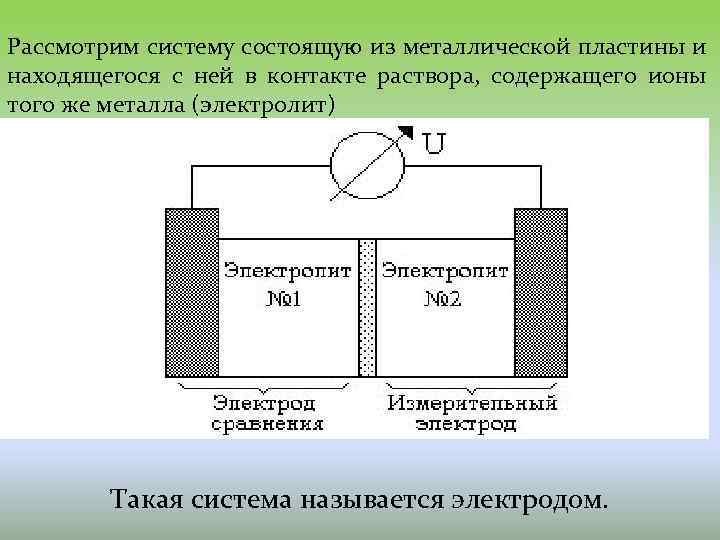 Рассмотрим систему состоящую из металлической пластины и находящегося с ней в контакте раствора, содержащего ионы того же металла (электролит) Такая система называется электродом.
Рассмотрим систему состоящую из металлической пластины и находящегося с ней в контакте раствора, содержащего ионы того же металла (электролит) Такая система называется электродом.
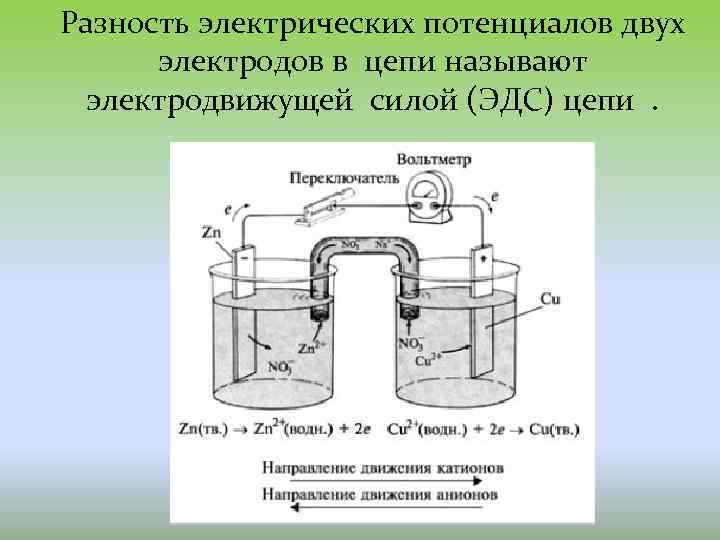 Разность электрических потенциалов двух электродов в цепи называют электродвижущей силой (ЭДС) цепи .
Разность электрических потенциалов двух электродов в цепи называют электродвижущей силой (ЭДС) цепи .
 УРАВНЕНИЕ НЕРНСТА. Электродное равновесие имеет вид: Окисленная форма + nё = восстановленная форма Е- равновесный стандартный потенциал; Е 0 – стандартный потенциал данной редоксипары; R = 8, 314 Дж/моль. К- универсальная газовая постоянная; Т- абсолютная температура в растворе; n- число электронов; F- постоянная, число Фарадея (9648 Кл/моль). В уравнение Нернста не входят концентрации твёрдых веществ! Например: Аg+ + 1ё = Аg 0 (тв. ) Е= E°Ag+/Ae+ 0, 059 lg. C(Ag+), Где ЕAg+/Ag — стандартный потенциал электрода, В; 0, 059 — чистовой коэффициент, В (при 25 °С); C(Ag+) — молярная концентрация ионов Ag+, моль/л.
УРАВНЕНИЕ НЕРНСТА. Электродное равновесие имеет вид: Окисленная форма + nё = восстановленная форма Е- равновесный стандартный потенциал; Е 0 – стандартный потенциал данной редоксипары; R = 8, 314 Дж/моль. К- универсальная газовая постоянная; Т- абсолютная температура в растворе; n- число электронов; F- постоянная, число Фарадея (9648 Кл/моль). В уравнение Нернста не входят концентрации твёрдых веществ! Например: Аg+ + 1ё = Аg 0 (тв. ) Е= E°Ag+/Ae+ 0, 059 lg. C(Ag+), Где ЕAg+/Ag — стандартный потенциал электрода, В; 0, 059 — чистовой коэффициент, В (при 25 °С); C(Ag+) — молярная концентрация ионов Ag+, моль/л.
 Виды электродов
Виды электродов
 ВОПРОС 2 Общая характеристика и виды электродов.
ВОПРОС 2 Общая характеристика и виды электродов.
 Электроды первого рода Электроды, состоящие из металлической пластинки, погруженной в раствор соли того же металла. При обратимой работе элемента, в который включен электрод, на металлической пластинке идет процесс перехода катионов из металла в раствор либо из раствора в металл. Т. о. , электроды первого рода обратимы по катиону и их потенциал связан уравнением Нернста с концентрацией катиона Электроды второго рода Электроды, в которых металл покрыт малорастворимой солью этого металла и находится в растворе, содержащем другую растворимую соль с тем же анионом. Электроды этого типа обратимы относительно аниона и зависимость их электродного потенциала от температуры и концентрации аниона может быть записана в следующем виде:
Электроды первого рода Электроды, состоящие из металлической пластинки, погруженной в раствор соли того же металла. При обратимой работе элемента, в который включен электрод, на металлической пластинке идет процесс перехода катионов из металла в раствор либо из раствора в металл. Т. о. , электроды первого рода обратимы по катиону и их потенциал связан уравнением Нернста с концентрацией катиона Электроды второго рода Электроды, в которых металл покрыт малорастворимой солью этого металла и находится в растворе, содержащем другую растворимую соль с тем же анионом. Электроды этого типа обратимы относительно аниона и зависимость их электродного потенциала от температуры и концентрации аниона может быть записана в следующем виде:
 Также электроды подразделяются: Индикаторные электроды - Электроды сравнения - электрод, потенциал которого зависит от которого концентрации постоянные при определяемых ионов работе с ними и при в растворе. хранении.
Также электроды подразделяются: Индикаторные электроды - Электроды сравнения - электрод, потенциал которого зависит от которого концентрации постоянные при определяемых ионов работе с ними и при в растворе. хранении.
 Электрод, относительно которого производится измерение потенциала, называется электродом сравнения. Кроме водородного, в качестве электродов сравнения используют хлорсеребряный, каломельный и др. Во всех случаях потенциал электрода сравнения принимается равным нулю.
Электрод, относительно которого производится измерение потенциала, называется электродом сравнения. Кроме водородного, в качестве электродов сравнения используют хлорсеребряный, каломельный и др. Во всех случаях потенциал электрода сравнения принимается равным нулю.
 ЭЛЕКТРОДЫ СРАВНЕНИЯ: 1. Водородный электрод. 2. Каломельный электрод. 3. Хлорсеребряный электрод.
ЭЛЕКТРОДЫ СРАВНЕНИЯ: 1. Водородный электрод. 2. Каломельный электрод. 3. Хлорсеребряный электрод.
 Водородный электрод представляет собой платиновую пластинку, омываемую газообразным водородом, погруженную в раствор, содержащий ионы водорода. Схематически его изображают : Рt, Н 2 / Н+ Электрохимическое равновесие на электроде можно рассматривать в следующем виде: 2 Н+ + 2 е- ––> Н 2 Потенциал водородного электрода зависит от активности ионов Н+ в растворе и давления водорода; потенциал стандартного водородного электрода (с активностью ионов Н+ 1 моль/л и давлением водорода 101. 3 к. Па) принят равным нулю. Поэтому для электродного потенциала нестандартного водородного электрода можно записать:
Водородный электрод представляет собой платиновую пластинку, омываемую газообразным водородом, погруженную в раствор, содержащий ионы водорода. Схематически его изображают : Рt, Н 2 / Н+ Электрохимическое равновесие на электроде можно рассматривать в следующем виде: 2 Н+ + 2 е- ––> Н 2 Потенциал водородного электрода зависит от активности ионов Н+ в растворе и давления водорода; потенциал стандартного водородного электрода (с активностью ионов Н+ 1 моль/л и давлением водорода 101. 3 к. Па) принят равным нулю. Поэтому для электродного потенциала нестандартного водородного электрода можно записать:
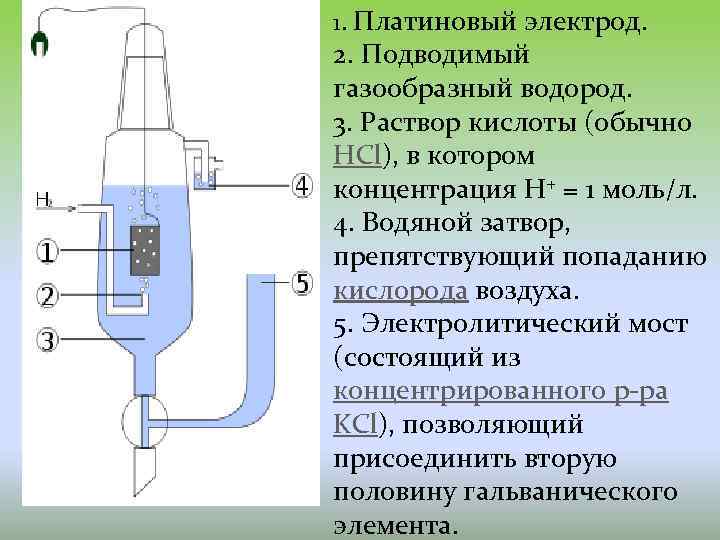 1. Платиновый электрод. 2. Подводимый газообразный водород. 3. Раствор кислоты (обычно HCl), в котором концентрация H+ = 1 моль/л. 4. Водяной затвор, препятствующий попаданию кислорода воздуха. 5. Электролитический мост (состоящий из концентрированного р-ра KCl), позволяющий присоединить вторую половину гальванического элемента.
1. Платиновый электрод. 2. Подводимый газообразный водород. 3. Раствор кислоты (обычно HCl), в котором концентрация H+ = 1 моль/л. 4. Водяной затвор, препятствующий попаданию кислорода воздуха. 5. Электролитический мост (состоящий из концентрированного р-ра KCl), позволяющий присоединить вторую половину гальванического элемента.
 Каломельный электрод более простой в обращении, величина электродного потенциала относительно стандартного водородного электрода точно известна и зависит только от температуры. Каломельный электрод состоит из ртутного электрода, помещенного в раствор КСl определенной концентрации и насыщенный каломелью Hg 2 Сl 2: Нg / Нg 2 Сl 2, КСl Каломельный электрод обратим относительно анионов хлора и уравнение Нернста для него имеет вид:
Каломельный электрод более простой в обращении, величина электродного потенциала относительно стандартного водородного электрода точно известна и зависит только от температуры. Каломельный электрод состоит из ртутного электрода, помещенного в раствор КСl определенной концентрации и насыщенный каломелью Hg 2 Сl 2: Нg / Нg 2 Сl 2, КСl Каломельный электрод обратим относительно анионов хлора и уравнение Нернста для него имеет вид:
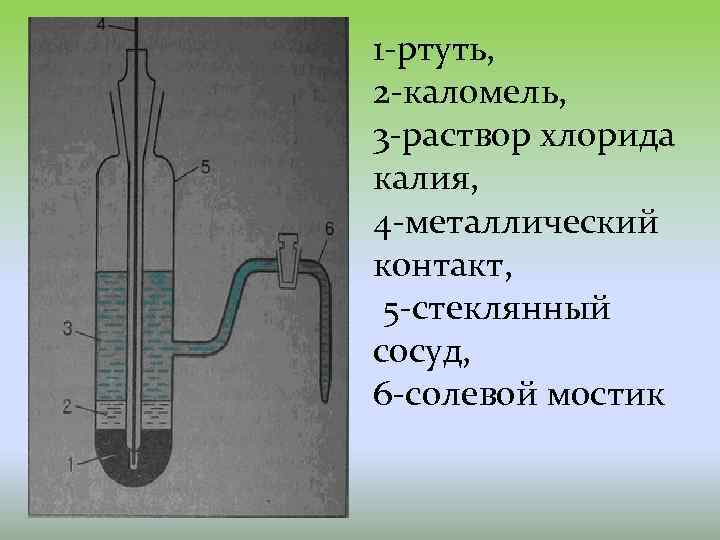 1 -ртуть, 2 -каломель, 3 -раствор хлорида калия, 4 -металлический контакт, 5 -стеклянный сосуд, 6 -солевой мостик
1 -ртуть, 2 -каломель, 3 -раствор хлорида калия, 4 -металлический контакт, 5 -стеклянный сосуд, 6 -солевой мостик
 Хлорсеребряный электрод второго рода, представляет собой серебряную проволоку, покрытую хлоридом серебра и помещённую в раствор хлорида калия. Хлорсеребряный электрод обратим относительно анионов хлора: Аg / Аg. Сl, КСl В отличие от каломельного, он устойчив при повышенных температурах и применим как в водных, так и во многих неводных средах. Величина потенциала хлорсеребряного электрода зависит от активности ионов хлора; данная зависимость имеет следующий вид:
Хлорсеребряный электрод второго рода, представляет собой серебряную проволоку, покрытую хлоридом серебра и помещённую в раствор хлорида калия. Хлорсеребряный электрод обратим относительно анионов хлора: Аg / Аg. Сl, КСl В отличие от каломельного, он устойчив при повышенных температурах и применим как в водных, так и во многих неводных средах. Величина потенциала хлорсеребряного электрода зависит от активности ионов хлора; данная зависимость имеет следующий вид:
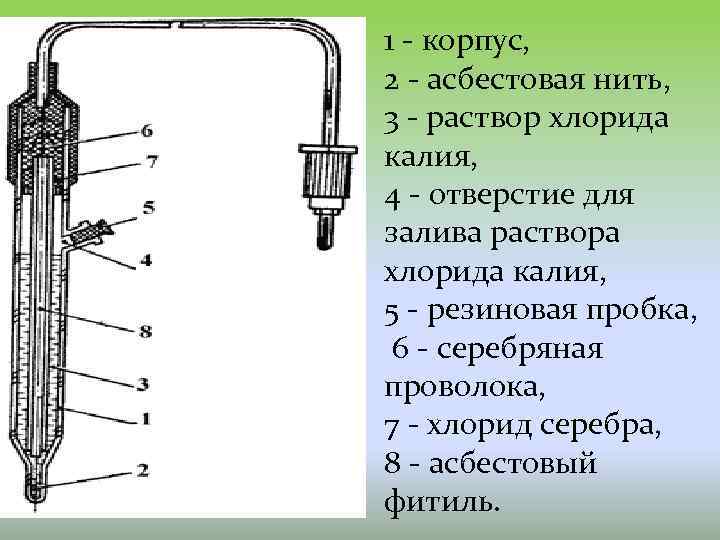 1 - корпус, 2 - асбестовая нить, 3 - раствор хлорида калия, 4 - отверстие для залива раствора хлорида калия, 5 - резиновая пробка, 6 - серебряная проволока, 7 - хлорид серебра, 8 - асбестовый фитиль.
1 - корпус, 2 - асбестовая нить, 3 - раствор хлорида калия, 4 - отверстие для залива раствора хлорида калия, 5 - резиновая пробка, 6 - серебряная проволока, 7 - хлорид серебра, 8 - асбестовый фитиль.
 ИНДИКАТОРНЫЕ ЭЛЕКТРОДЫ
ИНДИКАТОРНЫЕ ЭЛЕКТРОДЫ
 Индикаторные электроды Электроды, обратимые относительно иона водорода, используются на практике для определения р. Н раствора и последующим расчетом р. Н по уравнению Нернста. В качестве индикаторного электрода может использоваться и водородный электрод, однако работа с ним неудобна.
Индикаторные электроды Электроды, обратимые относительно иона водорода, используются на практике для определения р. Н раствора и последующим расчетом р. Н по уравнению Нернста. В качестве индикаторного электрода может использоваться и водородный электрод, однако работа с ним неудобна.
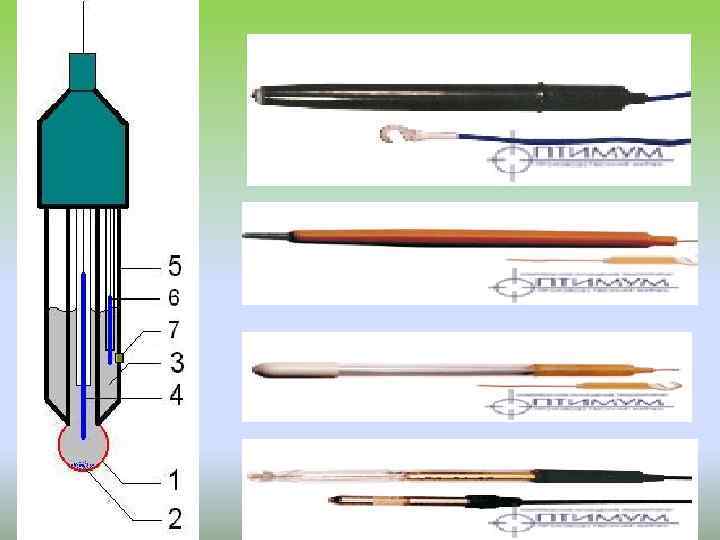
 Стеклянный электрод относится к т. н. ионоселективным или мембранным электродам. В основе работы таких электродов лежат ионообменные реакции, протекающие на границах мембран с растворами электролитов; ионоселективные электроды могут быть обратимы как по катиону, так и по аниону. При соответствующем составе и строении мембраны её потенциал зависит только от активности иона. Необходимо отметить, что стандартный потенциал ε°ст для каждого электрода имеет свою величину, которая со временем изменяется; поэтому стеклянный электрод перед каждым измерением р. Н калибруется по стандартным буферным растворам с точно известным р. Н. Потенциал стеклянного электрода с водородной функцией (т. е. обратимого по отношению к иону Н+) выражается уравнением:
Стеклянный электрод относится к т. н. ионоселективным или мембранным электродам. В основе работы таких электродов лежат ионообменные реакции, протекающие на границах мембран с растворами электролитов; ионоселективные электроды могут быть обратимы как по катиону, так и по аниону. При соответствующем составе и строении мембраны её потенциал зависит только от активности иона. Необходимо отметить, что стандартный потенциал ε°ст для каждого электрода имеет свою величину, которая со временем изменяется; поэтому стеклянный электрод перед каждым измерением р. Н калибруется по стандартным буферным растворам с точно известным р. Н. Потенциал стеклянного электрода с водородной функцией (т. е. обратимого по отношению к иону Н+) выражается уравнением:
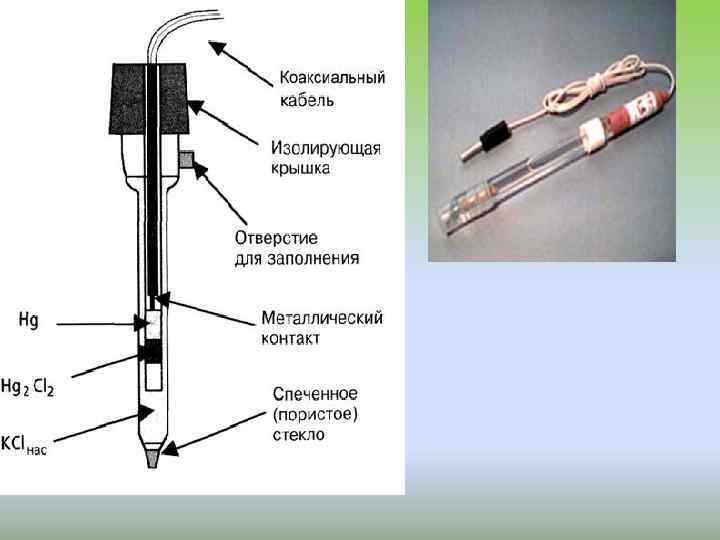
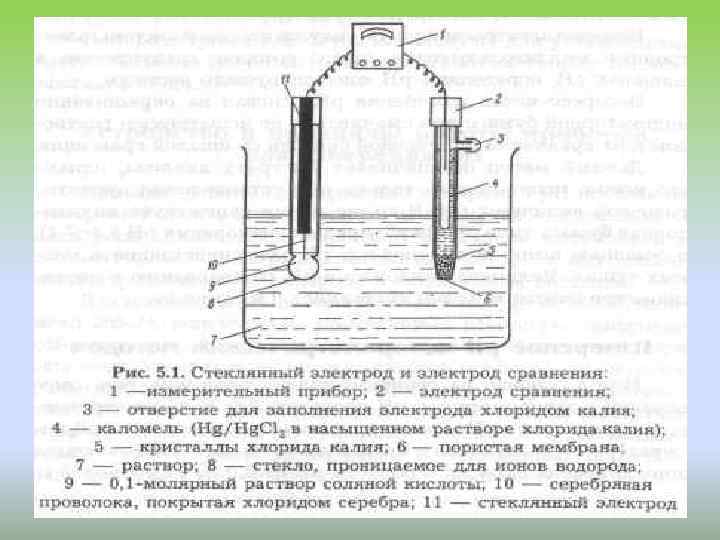
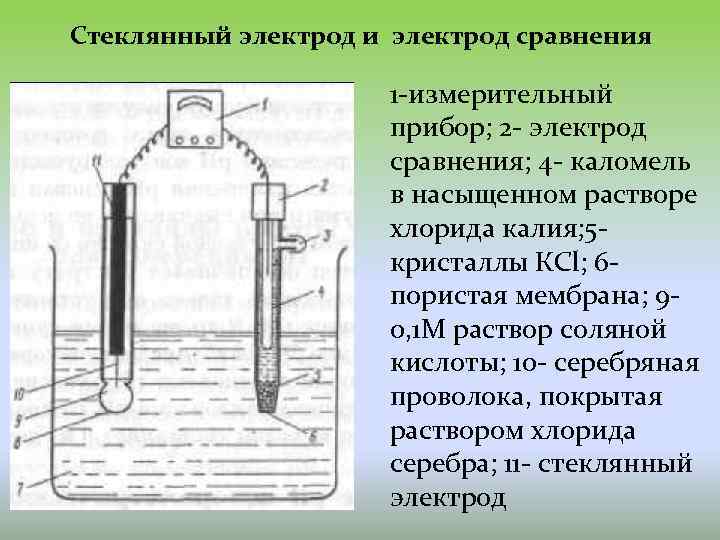 Стеклянный электрод и электрод сравнения 1 -измерительный прибор; 2 - электрод сравнения; 4 - каломель в насыщенном растворе хлорида калия; 5 - кристаллы КСl; 6 пористая мембрана; 9 - 0, 1 М раствор соляной кислоты; 10 - серебряная проволока, покрытая раствором хлорида серебра; 11 - стеклянный электрод
Стеклянный электрод и электрод сравнения 1 -измерительный прибор; 2 - электрод сравнения; 4 - каломель в насыщенном растворе хлорида калия; 5 - кристаллы КСl; 6 пористая мембрана; 9 - 0, 1 М раствор соляной кислоты; 10 - серебряная проволока, покрытая раствором хлорида серебра; 11 - стеклянный электрод
 Стеклянный электрод Потенциал стеклянного электрода с водородной функцией (т. е. обратимого по отношению к иону Н+) выражается уравнением:
Стеклянный электрод Потенциал стеклянного электрода с водородной функцией (т. е. обратимого по отношению к иону Н+) выражается уравнением:
 ИНДИКАТОРНЫЕ ЭЛЕКТРОДЫ ИЗ БЛАГОРОДНЫХ МЕТАЛЛОВ (ПЛАТИНА, ПАЛЛАДИЙ, ЗОЛОТО) являются индикаторными для окислительновосстановительных систем. В этом случае металлы являются лишь переносчиками электронов от восстановленной формы к окисленной. Электроды из платины (и золота) используют при потенциометрическом окислительно-восстановительном титровании. Эти электроды используются для измерения p. H в средах, когда не возможно использовать стеклянный электрод, на пример в средах фтороводородной кислоты или в средах с грубыми частицами.
ИНДИКАТОРНЫЕ ЭЛЕКТРОДЫ ИЗ БЛАГОРОДНЫХ МЕТАЛЛОВ (ПЛАТИНА, ПАЛЛАДИЙ, ЗОЛОТО) являются индикаторными для окислительновосстановительных систем. В этом случае металлы являются лишь переносчиками электронов от восстановленной формы к окисленной. Электроды из платины (и золота) используют при потенциометрическом окислительно-восстановительном титровании. Эти электроды используются для измерения p. H в средах, когда не возможно использовать стеклянный электрод, на пример в средах фтороводородной кислоты или в средах с грубыми частицами.
 Ионоселективные электроды Ионоселективным электродом называется индикаторный или измерительный электрод с относительно высокой специфичностью к отдельному иону. В зависимости от типа мембраны ионоселективные электроды подразделяются на следующие группы: 1. Твердые электроды; 2. Жидкостные электроды; 3. Газовые электроды 4. Энзимные электроды
Ионоселективные электроды Ионоселективным электродом называется индикаторный или измерительный электрод с относительно высокой специфичностью к отдельному иону. В зависимости от типа мембраны ионоселективные электроды подразделяются на следующие группы: 1. Твердые электроды; 2. Жидкостные электроды; 3. Газовые электроды 4. Энзимные электроды
 Твёрдые электроды Это электроды с твердыми мембранами гомогенные, гетерогенные, на основе ионообменных смол, стекол, осадков, моно- и поликристаллов. 1. Сульфидсеребряные электроды 2. Галогенсеребряные и некоторые другие электроды на основе серебра 3. Электроды на основе сульфидов (халькогенидов) некоторых двузарядных ионов металлов
Твёрдые электроды Это электроды с твердыми мембранами гомогенные, гетерогенные, на основе ионообменных смол, стекол, осадков, моно- и поликристаллов. 1. Сульфидсеребряные электроды 2. Галогенсеребряные и некоторые другие электроды на основе серебра 3. Электроды на основе сульфидов (халькогенидов) некоторых двузарядных ионов металлов
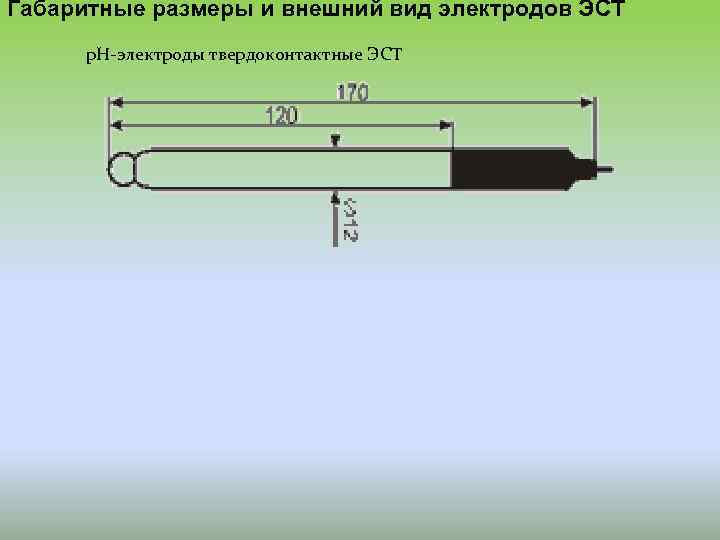 Габаритные размеры и внешний вид электродов ЭСТ р. Н-электроды твердоконтактные ЭСТ
Габаритные размеры и внешний вид электродов ЭСТ р. Н-электроды твердоконтактные ЭСТ
 Жидкостные электроды на основе жидких ионитов хелатов - нейтральных переносчиков, биологически активных веществ. Жидкая мембрана - это слой растворителя, который не должен растворяться в исследуемом растворе. • Электроды на основе жидких катионитов (Кальций - селективный электрод; Электрод, селективный по отношению к сумме катионов кальция и магния) • Электроды на основе жидких анионитов (Нитрат - селективный электрод, Фосфат селективный электрод)
Жидкостные электроды на основе жидких ионитов хелатов - нейтральных переносчиков, биологически активных веществ. Жидкая мембрана - это слой растворителя, который не должен растворяться в исследуемом растворе. • Электроды на основе жидких катионитов (Кальций - селективный электрод; Электрод, селективный по отношению к сумме катионов кальция и магния) • Электроды на основе жидких анионитов (Нитрат - селективный электрод, Фосфат селективный электрод)
 НИТРАТ-СЕЛЕКТИВНЫЙ ЭЛЕКТРОД
НИТРАТ-СЕЛЕКТИВНЫЙ ЭЛЕКТРОД
 Газовые электроды Газовый электрод включает ионоселективный электрод и сравнительный электрод, контактирующие с небольшим объемом вспомогательного раствора, который отделен от исследуемого раствора газовой прослойкой или гидрофобной газопроницаемой мембраной. Самыми распространёнными являются электроды с чувствительным элементом на аммиак; оксиды азота; и угарный, углекислый газы.
Газовые электроды Газовый электрод включает ионоселективный электрод и сравнительный электрод, контактирующие с небольшим объемом вспомогательного раствора, который отделен от исследуемого раствора газовой прослойкой или гидрофобной газопроницаемой мембраной. Самыми распространёнными являются электроды с чувствительным элементом на аммиак; оксиды азота; и угарный, углекислый газы.
 3. Вопрпос Потенциометрический метод анализа
3. Вопрпос Потенциометрический метод анализа
 Потенциометрический метод анализа основан на использовании зависимости электрического сигнала (потенциала) специального датчика, называемого измерительным электродом, от состава анализируемого раствора. В идеальном случае измерительный электрод избирательно (селективно) реагирует на определенный ион (или группу ионов), а его потенциал зависит от содержания этих ионов в растворе и подчиняется уравнению Нернста.
Потенциометрический метод анализа основан на использовании зависимости электрического сигнала (потенциала) специального датчика, называемого измерительным электродом, от состава анализируемого раствора. В идеальном случае измерительный электрод избирательно (селективно) реагирует на определенный ион (или группу ионов), а его потенциал зависит от содержания этих ионов в растворе и подчиняется уравнению Нернста.
 Потенциал электрода E связан с активностью (концентрацией) веществ, участвующих в электродном процессе, уравнением Нернста: Подставляя T=298, 15 и числовые значения констант в уравнение, получаем для 25 °C:
Потенциал электрода E связан с активностью (концентрацией) веществ, участвующих в электродном процессе, уравнением Нернста: Подставляя T=298, 15 и числовые значения констант в уравнение, получаем для 25 °C:
 Потенциометрические методы: 1. прямая потенциометрия (ионометрию); 2. потенциометрическое титрование. Прямая потенциометрия основана на применении уравнения Нернста для нахождения активности или концентрации участника электродной реакции по экспериментально измеренной ЭДС цепи или потенциалу соответствующего электрода. При потенциометрическом титровании точку эквивалентности определяют по резкому изменению (скачку) потенциала вблизи точки эквивалентности.
Потенциометрические методы: 1. прямая потенциометрия (ионометрию); 2. потенциометрическое титрование. Прямая потенциометрия основана на применении уравнения Нернста для нахождения активности или концентрации участника электродной реакции по экспериментально измеренной ЭДС цепи или потенциалу соответствующего электрода. При потенциометрическом титровании точку эквивалентности определяют по резкому изменению (скачку) потенциала вблизи точки эквивалентности.
 При потенциометрическом титровании регистрируют изменение потенциала индикаторного электрода в процессе титрования исследуемого раствора стандартным раствором реагента в зависимости от объема последнего. Потенциометрическое титрование проводят с использованием различных реакций: кислотно-основного и окислительно-восстановительного взаимодействий, осаждения и комплексообразования.
При потенциометрическом титровании регистрируют изменение потенциала индикаторного электрода в процессе титрования исследуемого раствора стандартным раствором реагента в зависимости от объема последнего. Потенциометрическое титрование проводят с использованием различных реакций: кислотно-основного и окислительно-восстановительного взаимодействий, осаждения и комплексообразования.
 Для потенциометрического титрования собирают цепь из индикаторного электрода в анализируемом растворе и электрода сравнения (каломельный или хлорсеребряный электроды). Тип применяемого индикаторного электрода зависит от свойств титриметрической смеси и ее взаимодействия с электродом. В кислотно-основном титровании используют стеклянный электрод, в окислительно-восстановительном - инертный (платиновый) электрод или электрод, обратимый по отношению к одному из ионов, содержащихся в титриметрической смеси; в осадительном – серебряный электрод; в комплексонометрическом - металлический электрод, обратимый к титруемому иону металла.
Для потенциометрического титрования собирают цепь из индикаторного электрода в анализируемом растворе и электрода сравнения (каломельный или хлорсеребряный электроды). Тип применяемого индикаторного электрода зависит от свойств титриметрической смеси и ее взаимодействия с электродом. В кислотно-основном титровании используют стеклянный электрод, в окислительно-восстановительном - инертный (платиновый) электрод или электрод, обратимый по отношению к одному из ионов, содержащихся в титриметрической смеси; в осадительном – серебряный электрод; в комплексонометрическом - металлический электрод, обратимый к титруемому иону металла.
 Потенциометрическое титрование основано на определении точки эквивалентности по результатам потенциометрических измерений. Вблизи точки эквивалентности происходит резкое изменение (скачок) потенциала индикаторного электрода. Это наблюдается лишь тогда, когда хотя бы один из участников реакции титрования является участником электродного процесса. Так, например, титрование по методу кислотно-основного взаимодействия может быть выполнено со стеклянным электродом. Определение хлорида - с хлорсеребряным и т. д.
Потенциометрическое титрование основано на определении точки эквивалентности по результатам потенциометрических измерений. Вблизи точки эквивалентности происходит резкое изменение (скачок) потенциала индикаторного электрода. Это наблюдается лишь тогда, когда хотя бы один из участников реакции титрования является участником электродного процесса. Так, например, титрование по методу кислотно-основного взаимодействия может быть выполнено со стеклянным электродом. Определение хлорида - с хлорсеребряным и т. д.
 Рис. 2. Кривые потенциометрического титрования: а - интегральная кривая титрования; б - дифференциальная кривая титрования; в - кривая титрования Грана
Рис. 2. Кривые потенциометрического титрования: а - интегральная кривая титрования; б - дифференциальная кривая титрования; в - кривая титрования Грана
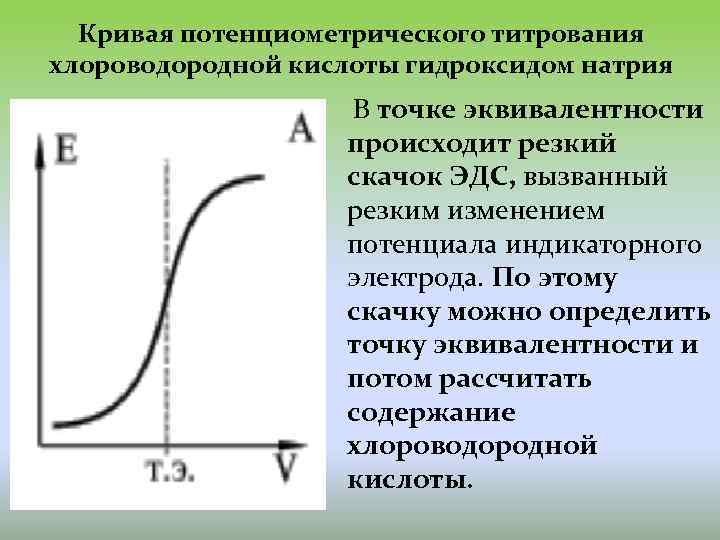 Кривая потенциометрического титрования хлороводородной кислоты гидроксидом натрия В точке эквивалентности происходит резкий скачок ЭДС, вызванный резким изменением потенциала индикаторного электрода. По этому скачку можно определить точку эквивалентности и потом рассчитать содержание хлороводородной кислоты.
Кривая потенциометрического титрования хлороводородной кислоты гидроксидом натрия В точке эквивалентности происходит резкий скачок ЭДС, вызванный резким изменением потенциала индикаторного электрода. По этому скачку можно определить точку эквивалентности и потом рассчитать содержание хлороводородной кислоты.
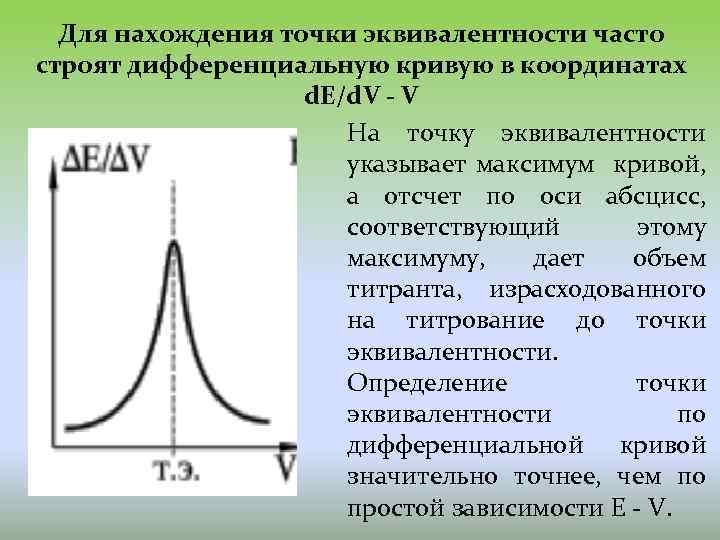 Для нахождения точки эквивалентности часто строят дифференциальную кривую в координатах d. E/d. V - V На точку эквивалентности указывает максимум кривой, а отсчет по оси абсцисс, соответствующий этому максимуму, дает объем титранта, израсходованного на титрование до точки эквивалентности. Определение точки эквивалентности по дифференциальной кривой значительно точнее, чем по простой зависимости E - V.
Для нахождения точки эквивалентности часто строят дифференциальную кривую в координатах d. E/d. V - V На точку эквивалентности указывает максимум кривой, а отсчет по оси абсцисс, соответствующий этому максимуму, дает объем титранта, израсходованного на титрование до точки эквивалентности. Определение точки эквивалентности по дифференциальной кривой значительно точнее, чем по простой зависимости E - V.
 В потенциометрическом анализе измерительный приборам — потенциометр. Он предназначен для измерения ЭДС электродной системы. Так как ЭДС зависит от активности соответствующих ионов в растворе, многие потенциометры позволяют непосредственно измерять также величину р. Х – отрицательный логарифм активности иона Х. Такие потенциометры в комплекте с соответствующим ионоселективным электродом носят название иономеров. Если потенциометр и электродная система предназначены для измерения активности только водородных ионов, прибор называется р. Нметром.
В потенциометрическом анализе измерительный приборам — потенциометр. Он предназначен для измерения ЭДС электродной системы. Так как ЭДС зависит от активности соответствующих ионов в растворе, многие потенциометры позволяют непосредственно измерять также величину р. Х – отрицательный логарифм активности иона Х. Такие потенциометры в комплекте с соответствующим ионоселективным электродом носят название иономеров. Если потенциометр и электродная система предназначены для измерения активности только водородных ионов, прибор называется р. Нметром.
 р. Н-МЕТР (ИОНОМЕР)
р. Н-МЕТР (ИОНОМЕР)
 Прибор мультитест позволяют измерять значение ЭДС (Eh, redox, окислительно-восстановительного потенциала) и температуру.
Прибор мультитест позволяют измерять значение ЭДС (Eh, redox, окислительно-восстановительного потенциала) и температуру.
 НИТРАТ-ТЕСТЕР
НИТРАТ-ТЕСТЕР
 ЛАБОРАТОРНЫЙ НИТРАТОМЕР
ЛАБОРАТОРНЫЙ НИТРАТОМЕР


