Лекция_1_Термод&кинет.ppt
- Количество слайдов: 46
 Электрохимическая термодинамика и кинетика 1
Электрохимическая термодинамика и кинетика 1
 A. J. Bard, L. R. Faulkner “Electrochemical Methods: Fundamentals and Applications” J. Wang “Analytical Electrochemistry” E. Barsoukov, J. R. Macdonald “Impedance Spectroscopy Theory, Experiment, and Applications” C. Gabrielli “Identification of Electrochemical Processes by Frequency Response Analysis” 2
A. J. Bard, L. R. Faulkner “Electrochemical Methods: Fundamentals and Applications” J. Wang “Analytical Electrochemistry” E. Barsoukov, J. R. Macdonald “Impedance Spectroscopy Theory, Experiment, and Applications” C. Gabrielli “Identification of Electrochemical Processes by Frequency Response Analysis” 2
 Electroanalysis: • widest dynamic range (down to a single molecule detection) • less sensitive to matrix effects (insensitive to color, turbidity etc. ) • the cheapest equipment 3
Electroanalysis: • widest dynamic range (down to a single molecule detection) • less sensitive to matrix effects (insensitive to color, turbidity etc. ) • the cheapest equipment 3
 Электрохимия Химия посредством электричества Электричество посредством химии 4
Электрохимия Химия посредством электричества Электричество посредством химии 4
 Дополнительная степень свободы Химия хим. состав, температура, давление Электрохимия хим. состав, температура, давление + электричество 5
Дополнительная степень свободы Химия хим. состав, температура, давление Электрохимия хим. состав, температура, давление + электричество 5
 Первый закон термодинамики в химии (изобарно-изотермический потенциал) U=Q–A A = p∆ V Q = T ∆S ∆H = ∆U +p∆ V ∆G = ∆H - T∆S = ∆U +p∆ V- T∆S ∆G = 0 ∆ 6
Первый закон термодинамики в химии (изобарно-изотермический потенциал) U=Q–A A = p∆ V Q = T ∆S ∆H = ∆U +p∆ V ∆G = ∆H - T∆S = ∆U +p∆ V- T∆S ∆G = 0 ∆ 6
 Первый закон термодинамики в электрохимии (изобарно-изотермический потенциал) U=Q–A A = p∆ V+q∆E Q = T ∆S ∆H = ∆U +p∆ V ∆G = ∆H - T∆S = ∆U +p∆ V- T∆S = - q∆E q=n. F ∆G = -n. F∆E ∆ 7
Первый закон термодинамики в электрохимии (изобарно-изотермический потенциал) U=Q–A A = p∆ V+q∆E Q = T ∆S ∆H = ∆U +p∆ V ∆G = ∆H - T∆S = ∆U +p∆ V- T∆S = - q∆E q=n. F ∆G = -n. F∆E ∆ 7
 Ток – кинетический параметр 8
Ток – кинетический параметр 8
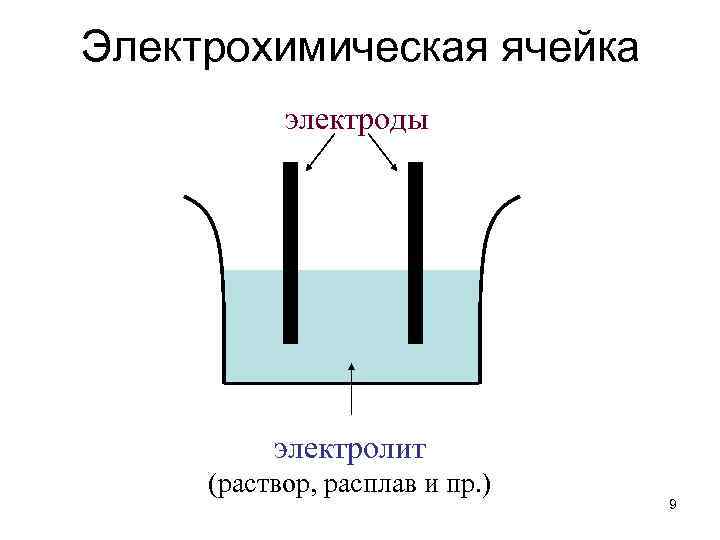 Электрохимическая ячейка электроды электролит (раствор, расплав и пр. ) 9
Электрохимическая ячейка электроды электролит (раствор, расплав и пр. ) 9
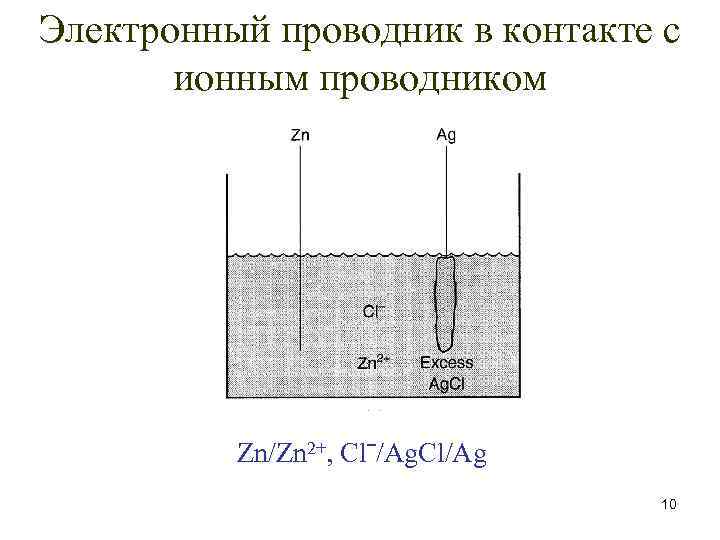 Электронный проводник в контакте с ионным проводником Zn/Zn 2+, Сlˉ/Ag. Cl/Ag 10
Электронный проводник в контакте с ионным проводником Zn/Zn 2+, Сlˉ/Ag. Cl/Ag 10
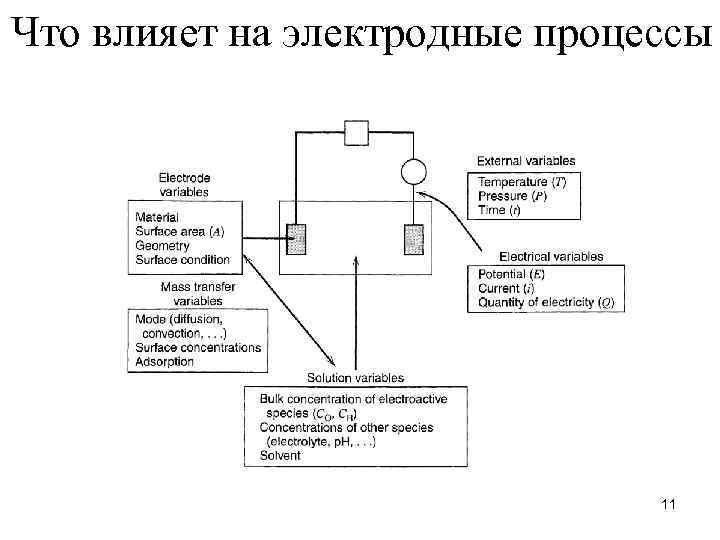 Что влияет на электродные процессы 11
Что влияет на электродные процессы 11
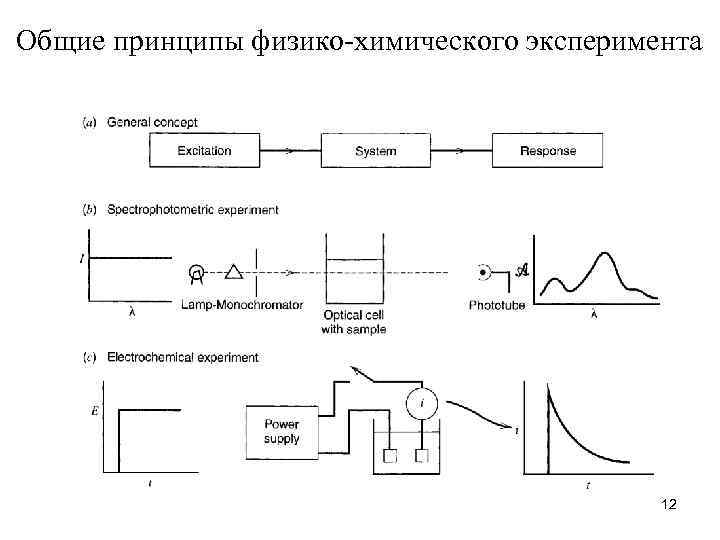 Общие принципы физико-химического эксперимента 12
Общие принципы физико-химического эксперимента 12
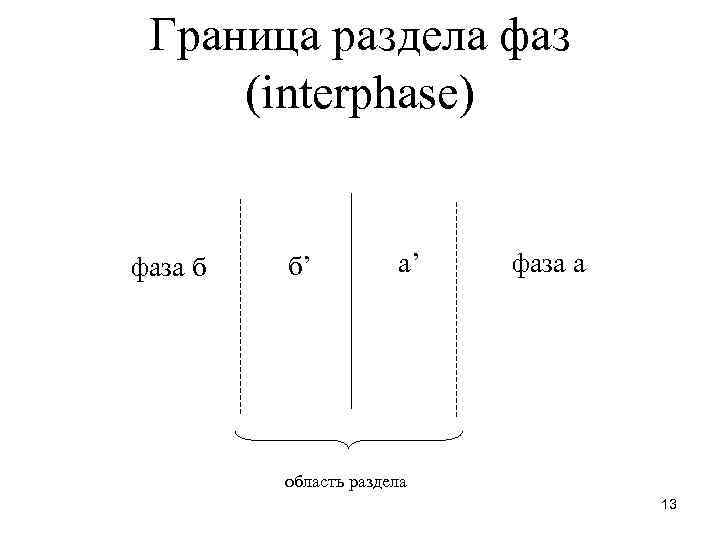 Граница раздела фаз (interphase) фаза б б’ а’ фаза а область раздела 13
Граница раздела фаз (interphase) фаза б б’ а’ фаза а область раздела 13
 Определения Поляризация –смещение потенциала относительно его равновесного (стационарного) значения под действием тока. Катод – электрод с отрицательной поляризацией. Анод – электрод с положительной поляризацией. 14
Определения Поляризация –смещение потенциала относительно его равновесного (стационарного) значения под действием тока. Катод – электрод с отрицательной поляризацией. Анод – электрод с положительной поляризацией. 14
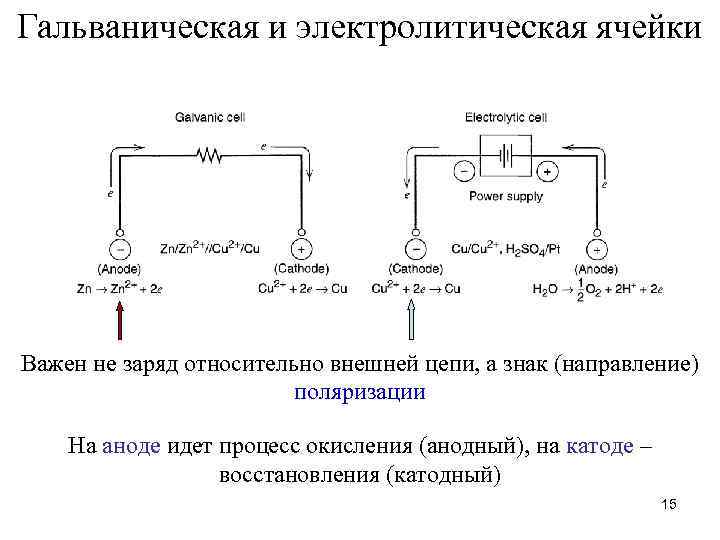 Гальваническая и электролитическая ячейки Важен не заряд относительно внешней цепи, а знак (направление) поляризации На аноде идет процесс окисления (анодный), на катоде – восстановления (катодный) 15
Гальваническая и электролитическая ячейки Важен не заряд относительно внешней цепи, а знак (направление) поляризации На аноде идет процесс окисления (анодный), на катоде – восстановления (катодный) 15
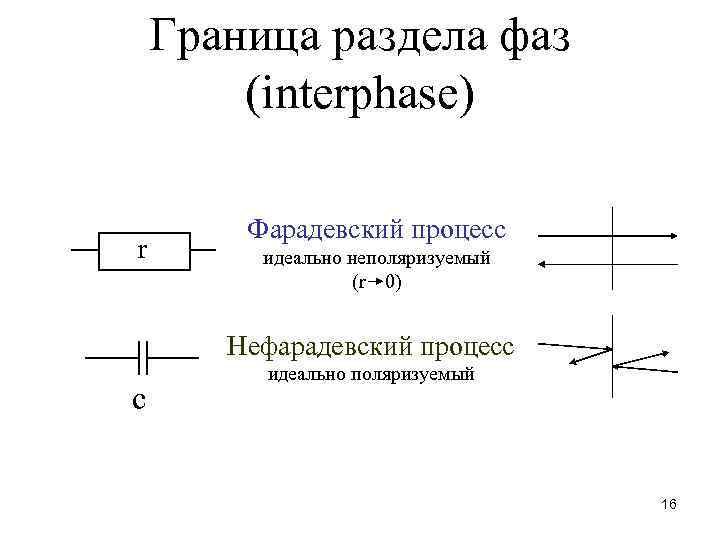 Граница раздела фаз (interphase) r Фарадевский процесс идеально неполяризуемый (r 0) Нефарадевский процесс c идеально поляризуемый 16
Граница раздела фаз (interphase) r Фарадевский процесс идеально неполяризуемый (r 0) Нефарадевский процесс c идеально поляризуемый 16
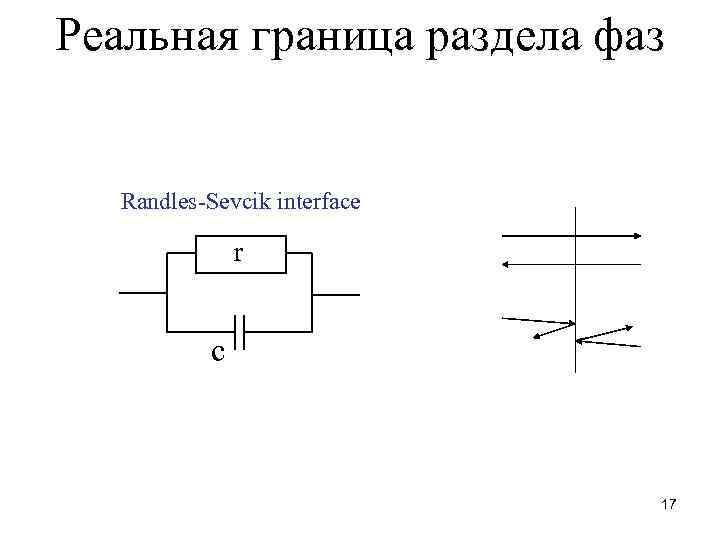 Реальная граница раздела фаз Randles-Sevcik interface r c 17
Реальная граница раздела фаз Randles-Sevcik interface r c 17
 Электрохимическая термодинамика 18
Электрохимическая термодинамика 18
 Термодинамика электродной реакции Q 233 k. J/mol r 233 k. J/mol 190 k. J/mol 43 k. J/mol 19
Термодинамика электродной реакции Q 233 k. J/mol r 233 k. J/mol 190 k. J/mol 43 k. J/mol 19
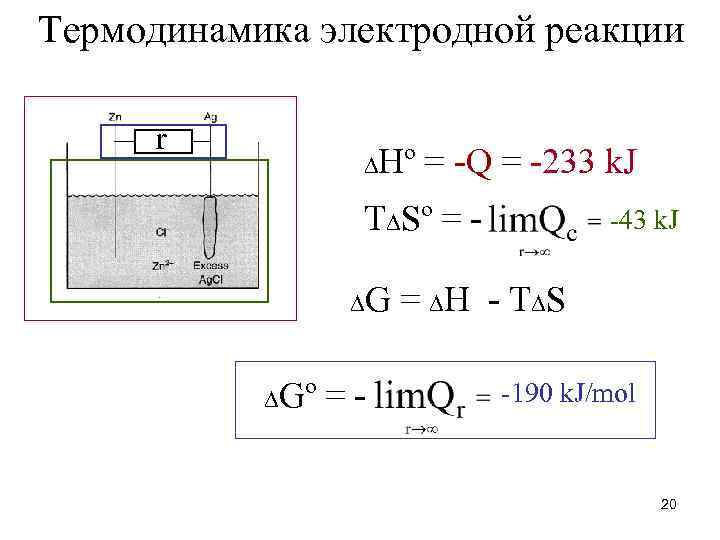 Термодинамика электродной реакции r ∆Hº = -Q = -233 k. J T∆Sº = ∆G ∆Gº =- -43 k. J = ∆H - T ∆S -190 k. J/mol 20
Термодинамика электродной реакции r ∆Hº = -Q = -233 k. J T∆Sº = ∆G ∆Gº =- -43 k. J = ∆H - T ∆S -190 k. J/mol 20
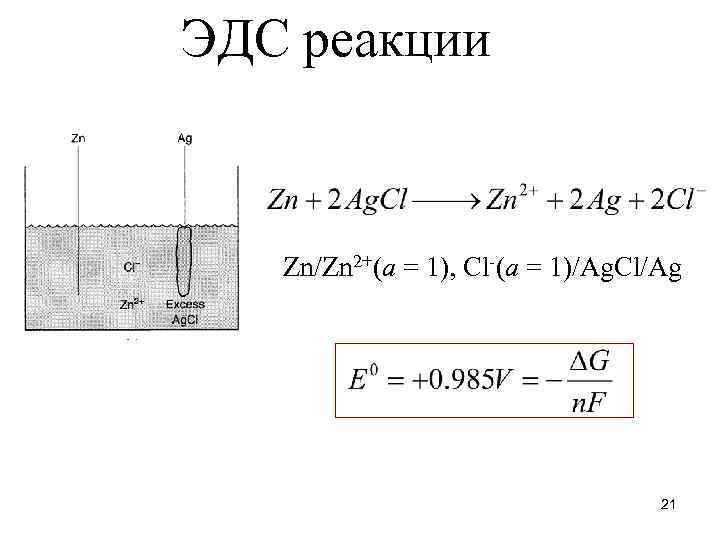 ЭДС реакции Zn/Zn 2+(a = 1), Cl-(a = 1)/Ag. Cl/Ag 21
ЭДС реакции Zn/Zn 2+(a = 1), Cl-(a = 1)/Ag. Cl/Ag 21
 Полуреакции и восстановительные потенциалы Pt/H+(a = 1)/H 2(a = 1) NHE Ag+(a = 1)/Ag 0. 779 V vs NHE 22
Полуреакции и восстановительные потенциалы Pt/H+(a = 1)/H 2(a = 1) NHE Ag+(a = 1)/Ag 0. 779 V vs NHE 22
 ЭДС и концентрация Nernst уравнение для потенциала электрода 23
ЭДС и концентрация Nernst уравнение для потенциала электрода 23
 Формальные потенциалы E 0’ 24
Формальные потенциалы E 0’ 24
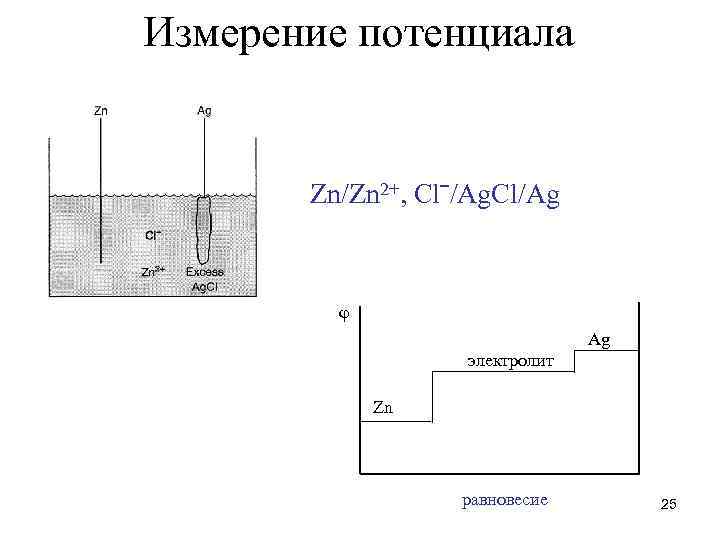 Измерение потенциала Zn/Zn 2+, Сlˉ/Ag. Cl/Ag φ Ag электролит Zn равновесие 25
Измерение потенциала Zn/Zn 2+, Сlˉ/Ag. Cl/Ag φ Ag электролит Zn равновесие 25
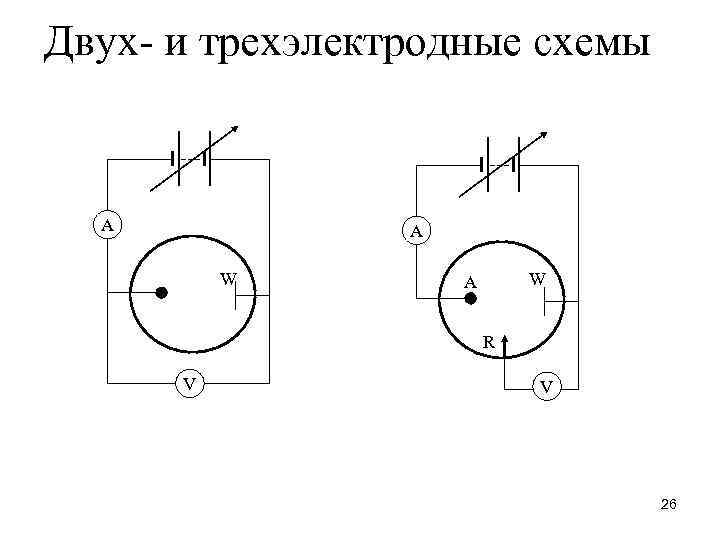 Двух- и трехэлектродные схемы A A W W A R V V 26
Двух- и трехэлектродные схемы A A W W A R V V 26
 Электрохимический потенциал для незаряженных частиц для равновесия между фазами α и 27
Электрохимический потенциал для незаряженных частиц для равновесия между фазами α и 27
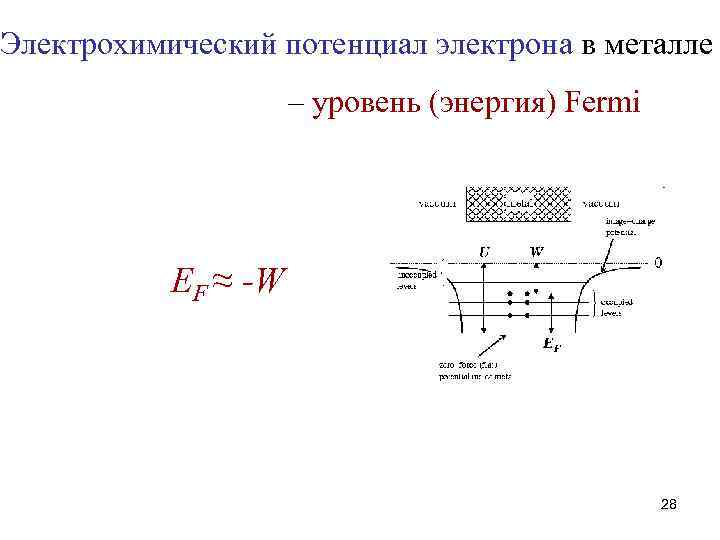 Электрохимический потенциал электрона в металле – уровень (энергия) Fermi EF ≈ -W 28
Электрохимический потенциал электрона в металле – уровень (энергия) Fermi EF ≈ -W 28
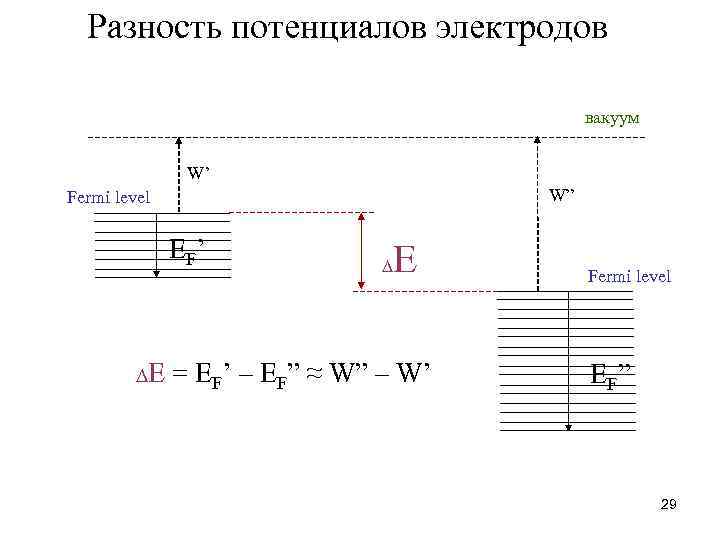 Разность потенциалов электродов вакуум W’ W” Fermi level E F’ ∆E ∆ E = EF’ – EF” ≈ W” – W’ Fermi level E F” 29
Разность потенциалов электродов вакуум W’ W” Fermi level E F’ ∆E ∆ E = EF’ – EF” ≈ W” – W’ Fermi level E F” 29
 Абсолютная шкала потенциалов 30
Абсолютная шкала потенциалов 30
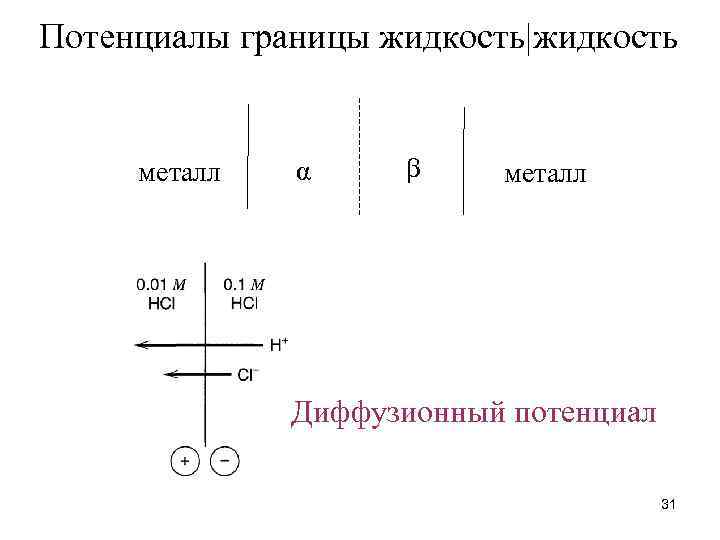 Потенциалы границы жидкость|жидкость металл α металл Диффузионный потенциал 31
Потенциалы границы жидкость|жидкость металл α металл Диффузионный потенциал 31
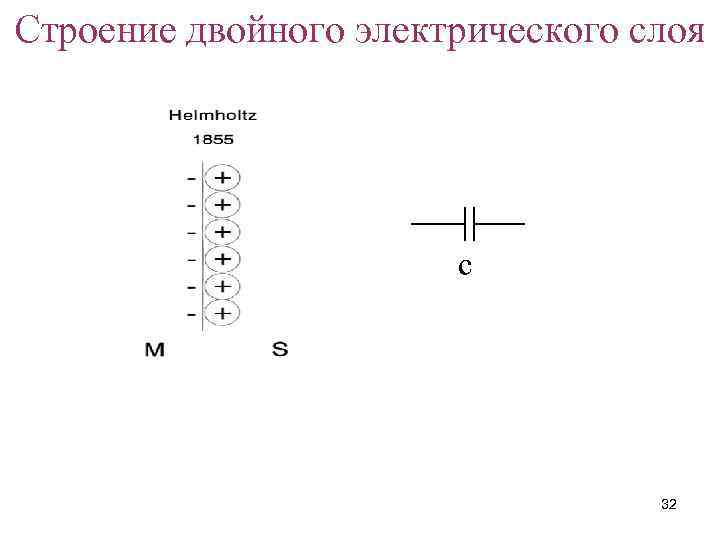 Строение двойного электрического слоя c 32
Строение двойного электрического слоя c 32
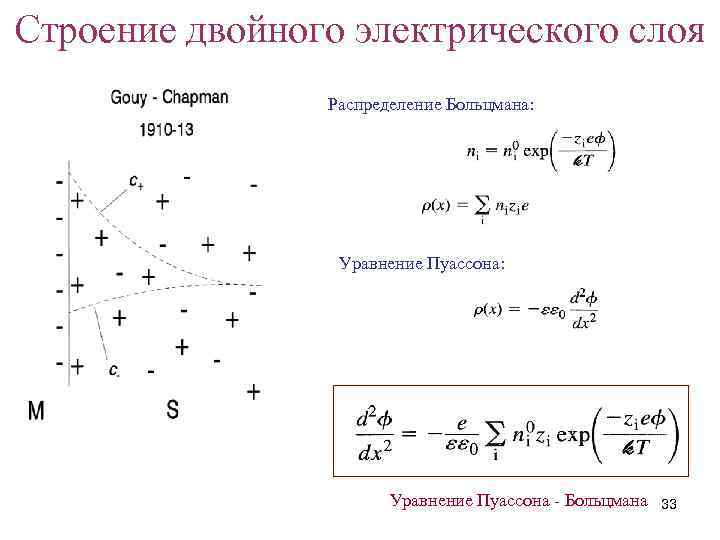 Строение двойного электрического слоя Распределение Больцмана: Уравнение Пуассона - Больцмана 33
Строение двойного электрического слоя Распределение Больцмана: Уравнение Пуассона - Больцмана 33
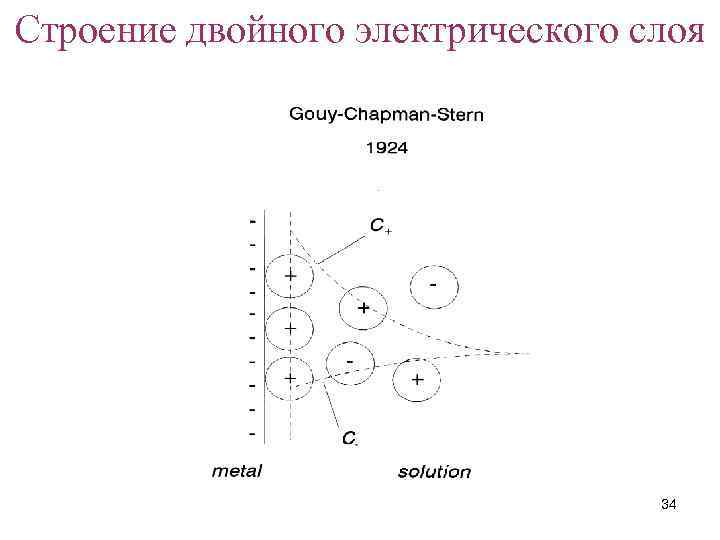 Строение двойного электрического слоя 34
Строение двойного электрического слоя 34
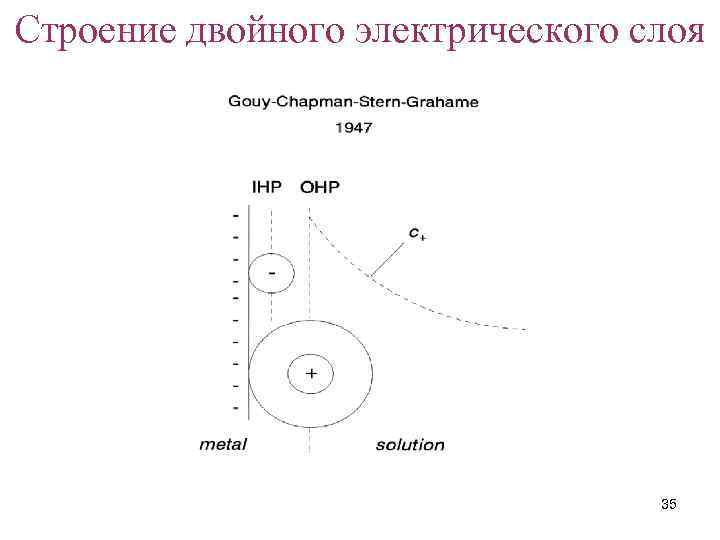 Строение двойного электрического слоя 35
Строение двойного электрического слоя 35
 Электрохимическая кинетика 36
Электрохимическая кинетика 36
 Электрохимические методы: i = f(E, t) i кинетика E = f(i, t) E термодинамика 37
Электрохимические методы: i = f(E, t) i кинетика E = f(i, t) E термодинамика 37
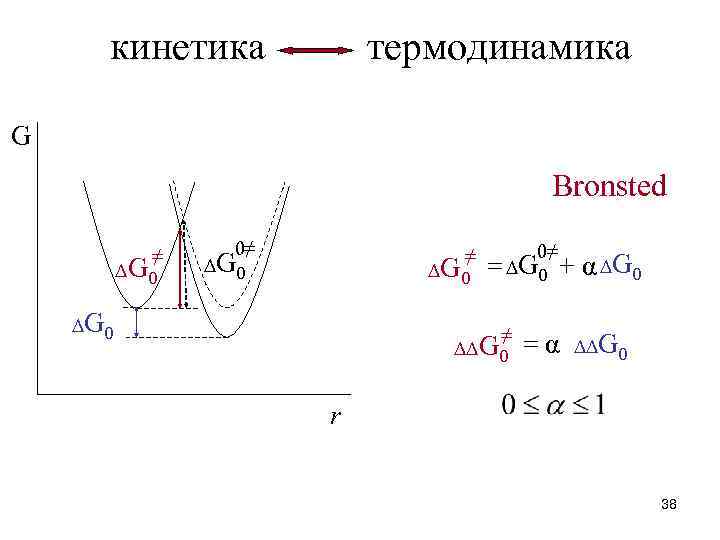 термодинамика кинетика G Bronsted ≠ ∆ G 0 0≠ ≠ ∆ G 0 0≠ = ∆ G 0 + α ∆ G 0 ≠ ∆∆G 0 =α ∆∆G 0 r 38
термодинамика кинетика G Bronsted ≠ ∆ G 0 0≠ ≠ ∆ G 0 0≠ = ∆ G 0 + α ∆ G 0 ≠ ∆∆G 0 =α ∆∆G 0 r 38
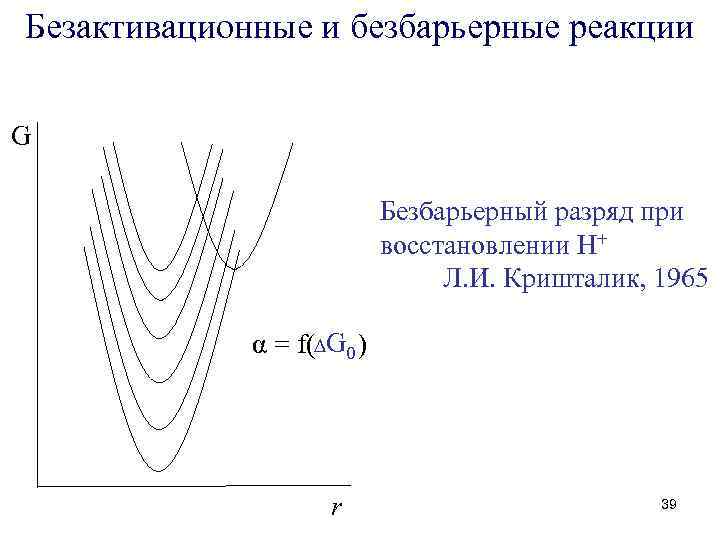 Безактивационные и безбарьерные реакции G Безбарьерный разряд при восстановлении Н+ Л. И. Кришталик, 1965 α = f(∆G 0 ) r 39
Безактивационные и безбарьерные реакции G Безбарьерный разряд при восстановлении Н+ Л. И. Кришталик, 1965 α = f(∆G 0 ) r 39
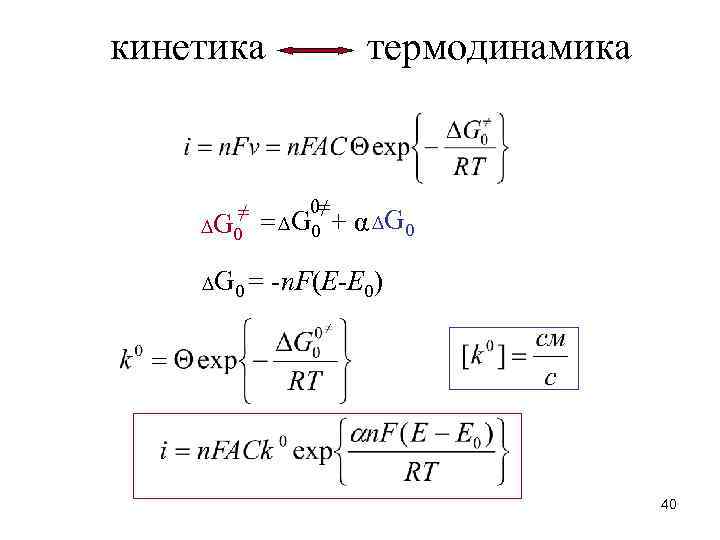 термодинамика кинетика ≠ ∆ G 0 0≠ = ∆ G 0 + α ∆ G 0 = -n. F(E-E 0) 40
термодинамика кинетика ≠ ∆ G 0 0≠ = ∆ G 0 + α ∆ G 0 = -n. F(E-E 0) 40
 Электрохимическая обратимость 41
Электрохимическая обратимость 41
 Уравнение разряда для обратимой реакции Butler-Volmer 42
Уравнение разряда для обратимой реакции Butler-Volmer 42
 Равновесие. Ток обмена. Равновесие: 43
Равновесие. Ток обмена. Равновесие: 43
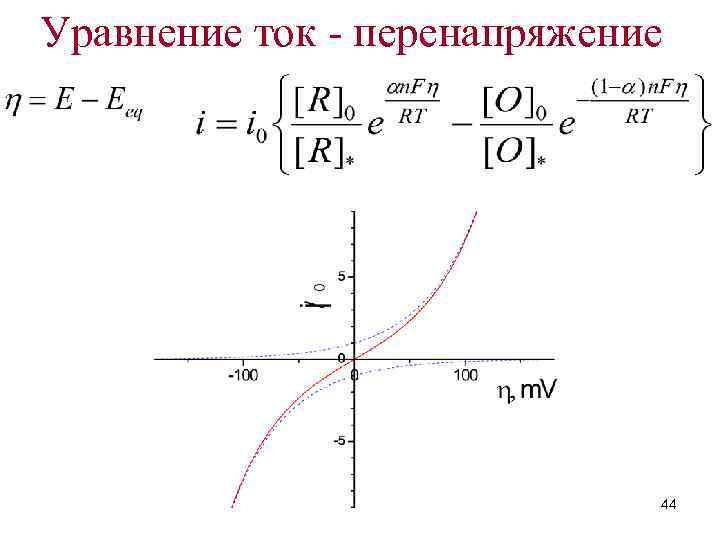 Уравнение ток - перенапряжение 44
Уравнение ток - перенапряжение 44
 Предельные случаи а) отсутствие влияния массопереноса Butler-Volmer а 1) малые перенапряжения RT/F ≈ 25 m. V а 2) большие перенапряжения 45
Предельные случаи а) отсутствие влияния массопереноса Butler-Volmer а 1) малые перенапряжения RT/F ≈ 25 m. V а 2) большие перенапряжения 45
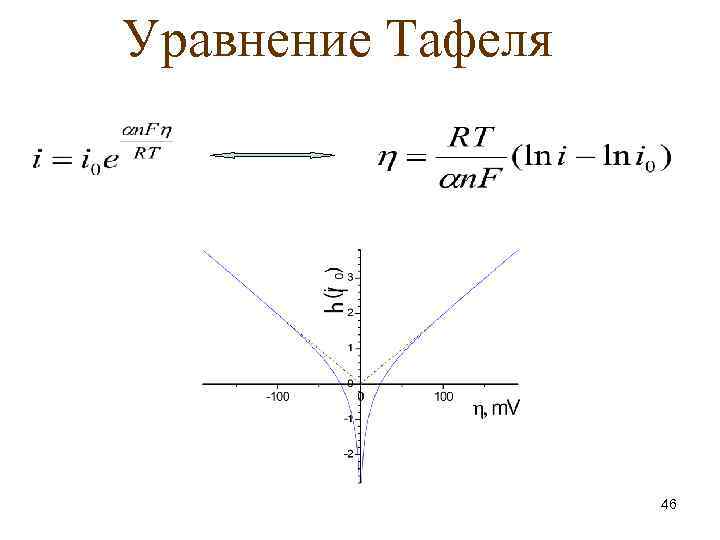 Уравнение Тафеля 46
Уравнение Тафеля 46


