Электрохимическая коррозя металлов Лекция 3.ppt
- Количество слайдов: 16
 Электрохимическая коррозия Плетнев Михаил Андреевич
Электрохимическая коррозия Плетнев Михаил Андреевич
 Введение Электрохимическая коррозия - взаимодействие металла с коррозионной средой (раствором электролита), при котором ионизация атомов металла и восстановление окислительной компоненты коррозионной среды протекают не в одном акте (пространственно разделены) и их скорости зависят от электродного потенциала (ГОСТ 5272 -68) Этот тип коррозии наиболее распространен. Он реализуется при взаимодействии металлических материалов с электролитами: водными растворами солей, кислот, щелочей, расплавами солей и щелочей.
Введение Электрохимическая коррозия - взаимодействие металла с коррозионной средой (раствором электролита), при котором ионизация атомов металла и восстановление окислительной компоненты коррозионной среды протекают не в одном акте (пространственно разделены) и их скорости зависят от электродного потенциала (ГОСТ 5272 -68) Этот тип коррозии наиболее распространен. Он реализуется при взаимодействии металлических материалов с электролитами: водными растворами солей, кислот, щелочей, расплавами солей и щелочей.
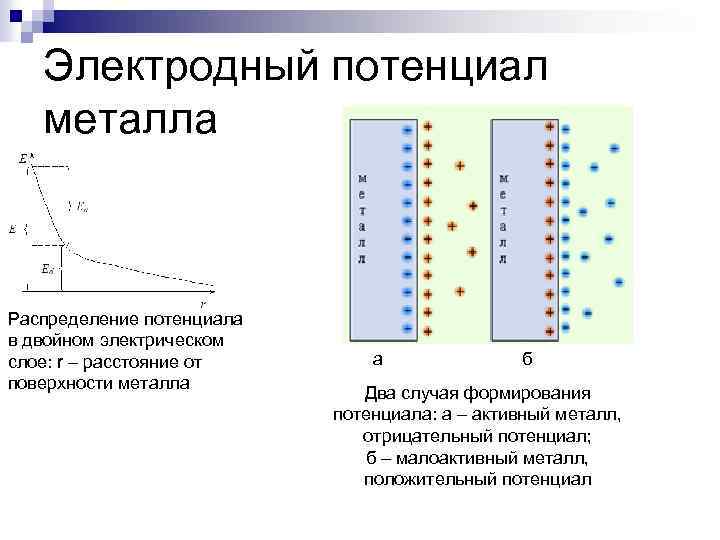 Электродный потенциал металла Распределение потенциала в двойном электрическом слое: r – расстояние от поверхности металла а б Два случая формирования потенциала: а – активный металл, отрицательный потенциал; б – малоактивный металл, положительный потенциал
Электродный потенциал металла Распределение потенциала в двойном электрическом слое: r – расстояние от поверхности металла а б Два случая формирования потенциала: а – активный металл, отрицательный потенциал; б – малоактивный металл, положительный потенциал
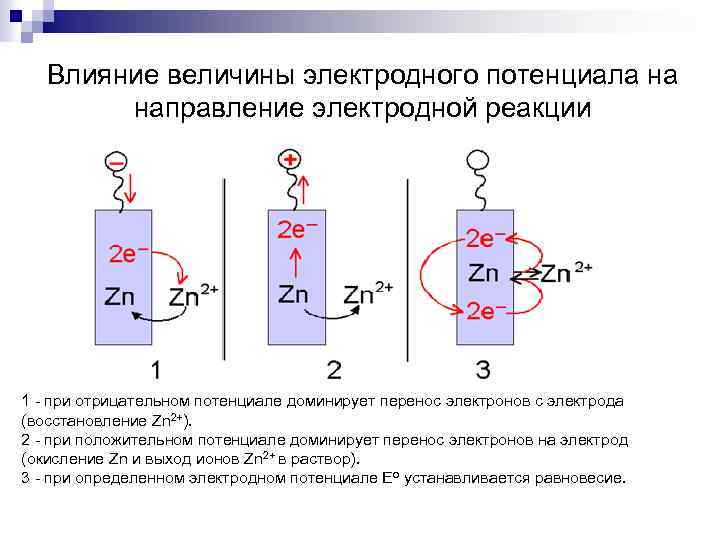 Влияние величины электродного потенциала на направление электродной реакции 1 - при отрицательном потенциале доминирует перенос электронов с электрода (восстановление Zn 2+). 2 - при положительном потенциале доминирует перенос электронов на электрод (окисление Zn и выход ионов Zn 2+ в раствор). 3 - при определенном электродном потенциале Eo устанавливается равновесие.
Влияние величины электродного потенциала на направление электродной реакции 1 - при отрицательном потенциале доминирует перенос электронов с электрода (восстановление Zn 2+). 2 - при положительном потенциале доминирует перенос электронов на электрод (окисление Zn и выход ионов Zn 2+ в раствор). 3 - при определенном электродном потенциале Eo устанавливается равновесие.
 Уравнение Нернста Eме = E 0 ме + (RT/n. F)*lna. Men+, где n -число моль-эквивалентов веществ, участвующих в реакции окисления; a. Men+ - активность ионов металла в растворе; E 0 ме - электродный потенциал металла в стандартных условиях, т. е. при a. Men+, =1; R - универсальная газовая постоянная; F – число Фарадея; Т – температура по шкале Кельвина. Если представить все константы при температуре 298 К (25°С) и выразить зависимость в десятичных логарифмах, введя множитель 2. 303, R =8, 314 (Дж/К. моль), F=96500 К/экв, то Eме = E 0 ме + (0, 059/n)*lga. Men+
Уравнение Нернста Eме = E 0 ме + (RT/n. F)*lna. Men+, где n -число моль-эквивалентов веществ, участвующих в реакции окисления; a. Men+ - активность ионов металла в растворе; E 0 ме - электродный потенциал металла в стандартных условиях, т. е. при a. Men+, =1; R - универсальная газовая постоянная; F – число Фарадея; Т – температура по шкале Кельвина. Если представить все константы при температуре 298 К (25°С) и выразить зависимость в десятичных логарифмах, введя множитель 2. 303, R =8, 314 (Дж/К. моль), F=96500 К/экв, то Eме = E 0 ме + (0, 059/n)*lga. Men+
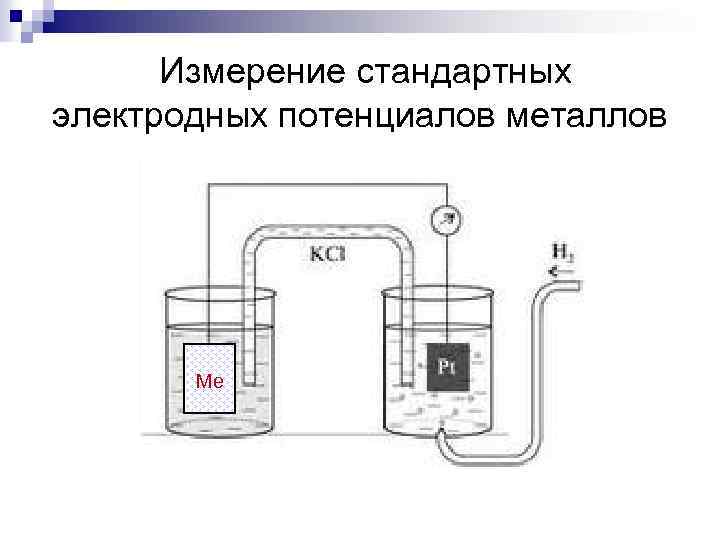 Измерение стандартных электродных потенциалов металлов Ме
Измерение стандартных электродных потенциалов металлов Ме
 Стандартные электродные потенциалы Электродная реакция Нейтральные среды (p. H = 7) Электродная реакция Е 0 Кислые среды (p. H = 0) Е 0 Аl(ОН)3 + 3 е = Аl + 3 ОН - -1, 94 H + + e = ½H 2 0, 000 Zr. O 2+ 2 Н 2 O + 4 е = Zr+ 4 OН - -1, 54 Н + + Н 2 O + 2 е = Н 2 + ОН - -0, 414 Тi. O 2 + 2 Н 2 O + 4 е = Ti + 4 OН - -1, 27 O 2 + 4 H + + 4 e = 2 H 2 O +1, 229 Сr(ОН)3 + 3 е = Сr + 3 ОН - -0, 886 Cr 2 O 72 - + 14 H + + 6 e = 2 Cr 3+ + 7 H 2 O +1, 33 Zn(OH)2 + 2 е = Zn + 2 OН - -0, 83 Щелочные среды (p. H = 14) Fe(OH)2 + 2 е = Fe + 2 OН - -0, 463 Mg(OH)2 + 2 e = Mg + 2 OH - -2, 69 Cd(OH)2 + 2 е = Cd + 2 OН - -0, 395 Mn(OH)2 + 2 e = Mn + 2 OH - -1, 55 Со(OH)2 + 2 е = Со + 2 OН - -0, 316 2 H 2 O + 2 e = H 2 + 2 OH - -0, 828 Ni(OH)2 + 2 е = Ni + 2 OН - -0, 306 O 2 + 2 Н 2 O + 4 e = 4 OH - +0, 401 Pb. O + Н 2 O + 2 е = Pb + 2 OН - -0, 136 Cu(ОН)2 + 2 е = Cu + 2 OН - +0, 19 Ag. Cl + е = Ag + С 1 - +0, 222 Hg 2(Cl 2) + 2 е = 2 Hg + 2 C 1 - +0, 268 O 2 + 2 H + + 4 e = 2 OH - +0, 815 Сl 2 + 2 e = 2 C 1 - +1, 360
Стандартные электродные потенциалы Электродная реакция Нейтральные среды (p. H = 7) Электродная реакция Е 0 Кислые среды (p. H = 0) Е 0 Аl(ОН)3 + 3 е = Аl + 3 ОН - -1, 94 H + + e = ½H 2 0, 000 Zr. O 2+ 2 Н 2 O + 4 е = Zr+ 4 OН - -1, 54 Н + + Н 2 O + 2 е = Н 2 + ОН - -0, 414 Тi. O 2 + 2 Н 2 O + 4 е = Ti + 4 OН - -1, 27 O 2 + 4 H + + 4 e = 2 H 2 O +1, 229 Сr(ОН)3 + 3 е = Сr + 3 ОН - -0, 886 Cr 2 O 72 - + 14 H + + 6 e = 2 Cr 3+ + 7 H 2 O +1, 33 Zn(OH)2 + 2 е = Zn + 2 OН - -0, 83 Щелочные среды (p. H = 14) Fe(OH)2 + 2 е = Fe + 2 OН - -0, 463 Mg(OH)2 + 2 e = Mg + 2 OH - -2, 69 Cd(OH)2 + 2 е = Cd + 2 OН - -0, 395 Mn(OH)2 + 2 e = Mn + 2 OH - -1, 55 Со(OH)2 + 2 е = Со + 2 OН - -0, 316 2 H 2 O + 2 e = H 2 + 2 OH - -0, 828 Ni(OH)2 + 2 е = Ni + 2 OН - -0, 306 O 2 + 2 Н 2 O + 4 e = 4 OH - +0, 401 Pb. O + Н 2 O + 2 е = Pb + 2 OН - -0, 136 Cu(ОН)2 + 2 е = Cu + 2 OН - +0, 19 Ag. Cl + е = Ag + С 1 - +0, 222 Hg 2(Cl 2) + 2 е = 2 Hg + 2 C 1 - +0, 268 O 2 + 2 H + + 4 e = 2 OH - +0, 815 Сl 2 + 2 e = 2 C 1 - +1, 360
 Электроды сравнения
Электроды сравнения
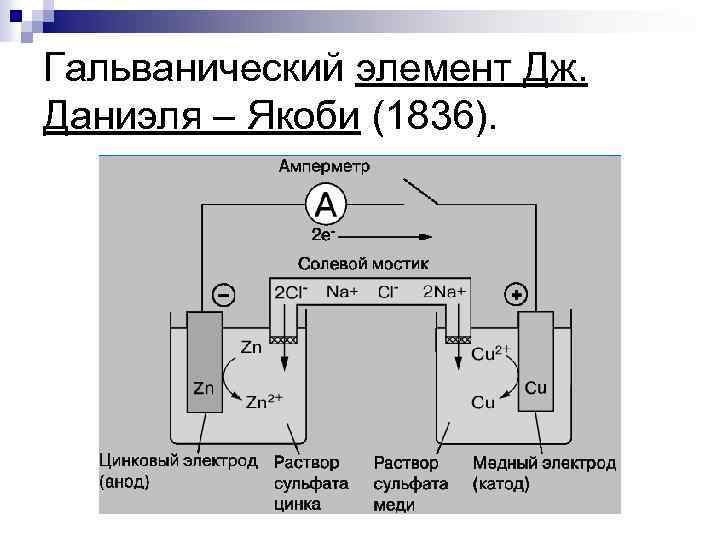 Гальванический элемент Дж. Даниэля – Якоби (1836).
Гальванический элемент Дж. Даниэля – Якоби (1836).
 Гальванические элементы n В элементе происходит переход электронов от восстановителя к окислителю: Zn + Cu. SO 4 = Cu + Zn. SO 4 Окисление Zn: Zn – 2 e = Zn 2+ Восстановление Cu: Cu 2+ + 2 e = Cu n В электрохимических системах процессы окисления и восстановления пространственно разделены, электроны переходят от восстановителя (Zn) к окислителю (Cu) по внешнему проводнику (идет электрический ток).
Гальванические элементы n В элементе происходит переход электронов от восстановителя к окислителю: Zn + Cu. SO 4 = Cu + Zn. SO 4 Окисление Zn: Zn – 2 e = Zn 2+ Восстановление Cu: Cu 2+ + 2 e = Cu n В электрохимических системах процессы окисления и восстановления пространственно разделены, электроны переходят от восстановителя (Zn) к окислителю (Cu) по внешнему проводнику (идет электрический ток).
 При работе ГЭ происходят реакции: Анод: Zn – 2 e = Zn 2+ (окисление) Катод: Cu 2+ + 2 e = Cu (восстановление) Схема записи ГЭ: е- A(–) Zn l Zn. SO 4 ll Cu. SO 4 l Cu (+) K E = φK – φA = 0, 34 – (-0, 76) = 1, 1 В Z n Zn. SO 4 C u Cu. SO 4 Zn окисляется, т. к. его катионы переходят в раствор. Cu восстанавливается, т. к. катионы меди превращаются в металлическую медь
При работе ГЭ происходят реакции: Анод: Zn – 2 e = Zn 2+ (окисление) Катод: Cu 2+ + 2 e = Cu (восстановление) Схема записи ГЭ: е- A(–) Zn l Zn. SO 4 ll Cu. SO 4 l Cu (+) K E = φK – φA = 0, 34 – (-0, 76) = 1, 1 В Z n Zn. SO 4 C u Cu. SO 4 Zn окисляется, т. к. его катионы переходят в раствор. Cu восстанавливается, т. к. катионы меди превращаются в металлическую медь
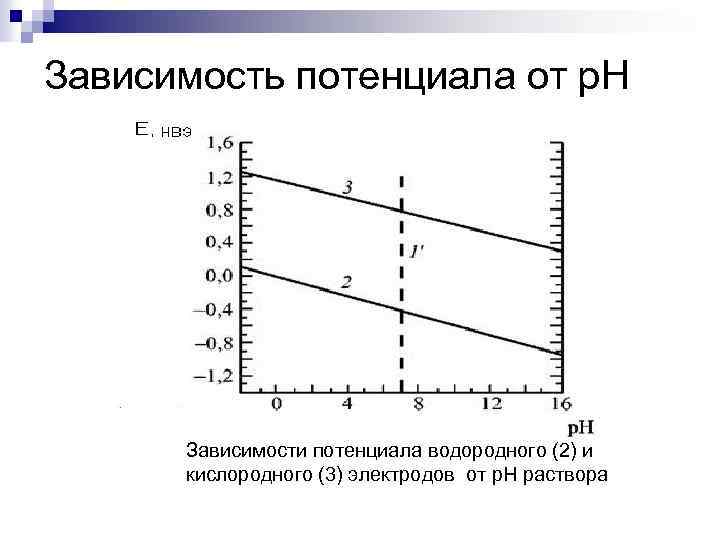 Зависимость потенциала от р. Н Зависимости потенциала водородного (2) и кислородного (3) электродов от р. Н раствора
Зависимость потенциала от р. Н Зависимости потенциала водородного (2) и кислородного (3) электродов от р. Н раствора
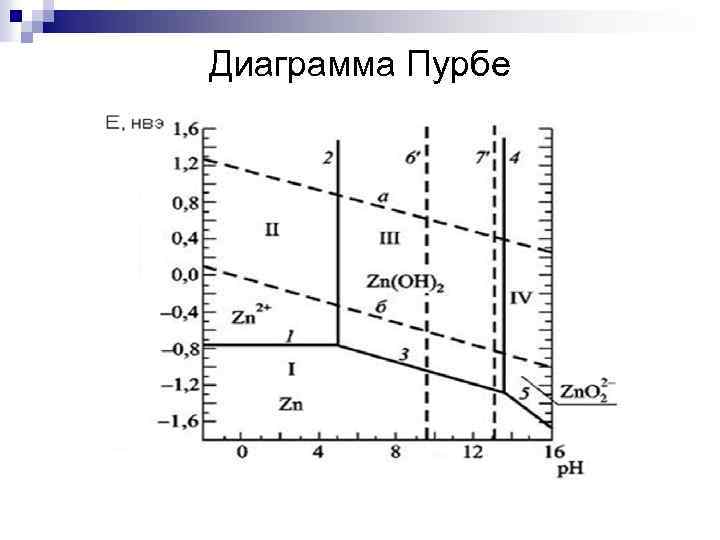 Диаграмма Пурбе
Диаграмма Пурбе
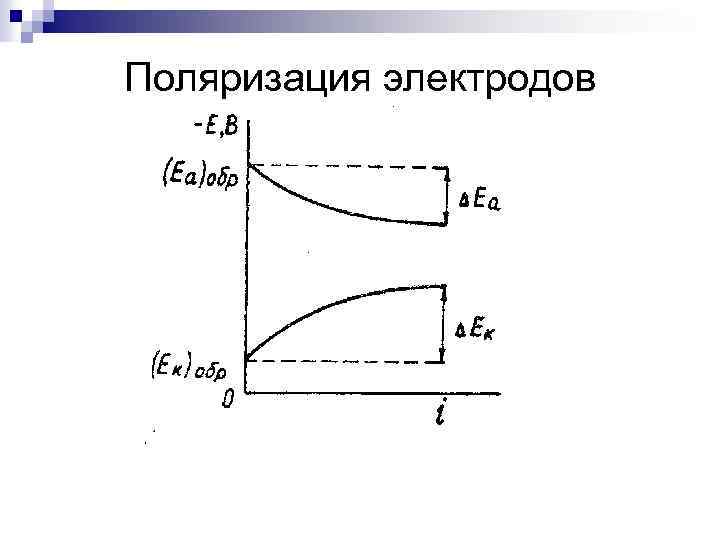 Поляризация электродов
Поляризация электродов
 Катодная деполяризация
Катодная деполяризация



