Электрохимическая коррозия.pptx
- Количество слайдов: 18
 ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ МЕТАЛЛОВ Выполнил: студент группы ТСА-09 Шамсувалеев М. Р. Проверил: Кандидат технических наук Пыхтунова С. В. Магнитогорск, 2012
ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ МЕТАЛЛОВ Выполнил: студент группы ТСА-09 Шамсувалеев М. Р. Проверил: Кандидат технических наук Пыхтунова С. В. Магнитогорск, 2012
 Электрохимическая коррозия металлов представляет собой самопроизвольное разрушение металлических материалов вследствие электрохимического взаимодействия их с окружающей электролитически проводящей средой, при котором ионизация атомов металла и восстановление окислительного компонента коррозионной среды протекают не в одном акте и их скорости зависят от величины электродного потенциала металла. По электрохимическому механизму корродируют металлы в контакте с растворами электролитов (морская вода, растворы кислот, щелочей, солей). В обычных атмосферных условиях и в земле металлы корродируют также по электрохимическому механизму, т. к. на их поверхности имеются капли влаги с растворенными компонентами воздуха и земли. Электрохимическая коррозия является гетерогенным и многостадийным процессом. Ее причиной является термодинамическая неустойчивость металлов в данной коррозионной среде. Примеры электрохимической коррозии металлов: ржавление различных металлических изделий и конструкций в атмосфере(металлических станков и оборудования заводов, стальных мостов, каркасов зданий и др. ), (рис. 1); коррозия наружной металлической обшивки судов в речной и морской воде; ржавление стальных конструкций гидросооружений; ржавление стальных трубопроводов в земле и др. ; Рис. 1 Ржавление зубчатых колес.
Электрохимическая коррозия металлов представляет собой самопроизвольное разрушение металлических материалов вследствие электрохимического взаимодействия их с окружающей электролитически проводящей средой, при котором ионизация атомов металла и восстановление окислительного компонента коррозионной среды протекают не в одном акте и их скорости зависят от величины электродного потенциала металла. По электрохимическому механизму корродируют металлы в контакте с растворами электролитов (морская вода, растворы кислот, щелочей, солей). В обычных атмосферных условиях и в земле металлы корродируют также по электрохимическому механизму, т. к. на их поверхности имеются капли влаги с растворенными компонентами воздуха и земли. Электрохимическая коррозия является гетерогенным и многостадийным процессом. Ее причиной является термодинамическая неустойчивость металлов в данной коррозионной среде. Примеры электрохимической коррозии металлов: ржавление различных металлических изделий и конструкций в атмосфере(металлических станков и оборудования заводов, стальных мостов, каркасов зданий и др. ), (рис. 1); коррозия наружной металлической обшивки судов в речной и морской воде; ржавление стальных конструкций гидросооружений; ржавление стальных трубопроводов в земле и др. ; Рис. 1 Ржавление зубчатых колес.
 Стремлением металлов переходить из металлического состояния в ионное для различных металлов различно. Вероятность такого перехода зависит также от природы коррозионной среды. Такую вероятность можно выразить уменьшением свободной энергии протекании реакции перехода в заданной среде при определенных условиях. Но прямой связи между термодинамическим рядом и коррозией металлов нет. Это объясняется тем, что термодинамические данные получены для идеально чистой поверхности металла, в то время как в реальных условиях корродирующий металл покрыт слоем (пленкой) продуктов взаимодействия металла со средой. Для расчетов изменения свободной энергии реакции при электрохимической коррозии металла используют величины электродных потенциалов. Следовательно, для электрохимического растворения металла необходимо присутствие в растворе окислителя (деполяризатора, который бы осуществлял катодную реакцию ассимиляции электронов), обратимый окислительно - восстановительный потенциал которого положительнее обратимого потенциала металла в данных условиях. Катодные процессы при электрохимической коррозии могут осуществляться различными веществами: 1)ионами 2)молекулами 3)оксидами и гидрооксидами (как правило малорастворимыми продуктами коррозии, образованными на поверхности металлов) 4)органическими соединениями В коррозионной практике в качестве окислителей-деполяризаторов, осуществляющих коррозию, выступают ионы водорода и молекулы растворенного в электролите кислорода. При увеличении активности ионов металла (повышение концентрации ионов металла в растворе), потенциал анода возрастает, что приводит к торможению растворения металла. Понижение активности металла, напротив, способствует растворению металла.
Стремлением металлов переходить из металлического состояния в ионное для различных металлов различно. Вероятность такого перехода зависит также от природы коррозионной среды. Такую вероятность можно выразить уменьшением свободной энергии протекании реакции перехода в заданной среде при определенных условиях. Но прямой связи между термодинамическим рядом и коррозией металлов нет. Это объясняется тем, что термодинамические данные получены для идеально чистой поверхности металла, в то время как в реальных условиях корродирующий металл покрыт слоем (пленкой) продуктов взаимодействия металла со средой. Для расчетов изменения свободной энергии реакции при электрохимической коррозии металла используют величины электродных потенциалов. Следовательно, для электрохимического растворения металла необходимо присутствие в растворе окислителя (деполяризатора, который бы осуществлял катодную реакцию ассимиляции электронов), обратимый окислительно - восстановительный потенциал которого положительнее обратимого потенциала металла в данных условиях. Катодные процессы при электрохимической коррозии могут осуществляться различными веществами: 1)ионами 2)молекулами 3)оксидами и гидрооксидами (как правило малорастворимыми продуктами коррозии, образованными на поверхности металлов) 4)органическими соединениями В коррозионной практике в качестве окислителей-деполяризаторов, осуществляющих коррозию, выступают ионы водорода и молекулы растворенного в электролите кислорода. При увеличении активности ионов металла (повышение концентрации ионов металла в растворе), потенциал анода возрастает, что приводит к торможению растворения металла. Понижение активности металла, напротив, способствует растворению металла.
 При погружении металла в электролит в результате взаимодействия между ними возникает разность электрических потенциалов, что связанно с образованием двойного электрического слоя, т. е. несимметричного распределения заряженных частиц у границы раздела фаз. Причинами возникновения этого скачка потенциала между металлом и электролитом являются: 1) переход заряженных частиц (катионов) из одной фазы в другую ( из металла в электролит или из электролита в металл ) с образованием двойного электрического слоя в пределах этих двух фаз; 2) избирательная адсорбция на поверхности металла частиц из жидкой фазы – ионов или полярных молекул и появление противоположного заряда в близлежащем слое электролита с образованием двойного электрического слоя в пределах одой (жидкой) фазы; 3) образование двойного слоя, обусловленного обеими причинами, т. е. адсорбционно- ионного скачка потенциала на поверхности металла в условиях наличия перехода катионов из металла в электролит или из электролита в металл.
При погружении металла в электролит в результате взаимодействия между ними возникает разность электрических потенциалов, что связанно с образованием двойного электрического слоя, т. е. несимметричного распределения заряженных частиц у границы раздела фаз. Причинами возникновения этого скачка потенциала между металлом и электролитом являются: 1) переход заряженных частиц (катионов) из одной фазы в другую ( из металла в электролит или из электролита в металл ) с образованием двойного электрического слоя в пределах этих двух фаз; 2) избирательная адсорбция на поверхности металла частиц из жидкой фазы – ионов или полярных молекул и появление противоположного заряда в близлежащем слое электролита с образованием двойного электрического слоя в пределах одой (жидкой) фазы; 3) образование двойного слоя, обусловленного обеими причинами, т. е. адсорбционно- ионного скачка потенциала на поверхности металла в условиях наличия перехода катионов из металла в электролит или из электролита в металл.
 Электрохимическое растворение металла- сложный процесс, состоящий из трех основных процессов: 1) анодного процесса- образования гидратированных ионов металла в электролите и некомпенсированных электронов на анодных участках по реакции: 2) процесса протекания электронов по металлу от анодных участков к катодным и соответствующего перемещения катионов и анионов в растворе; 3) катодного процесса- ассимиляции электронов какими-либо ионами или молекулами раствора (деполяризаторами), способны к восстановлению на катодных участках по реакции: D+ne=[D ne]. Таким образом, протекание электрохимического коррозионного процесса аналогично работе короткозамкнутого гальванического элемента. При замыкании в электролите двух электродов с разными потенциалами происходит перетекание электронов от более отрицательного электрода (анода) к менее отрицательному (или более положительному) электроду (катоду). Это перетекание электронов выравнивает значения потенциалов замкнутых электродов. Если бы при этом электродные процессы ( анодный на аноде и катодный на катоде) не протекали, потенциалы электродов сравнялись бы и наступила бы полная поляризация.
Электрохимическое растворение металла- сложный процесс, состоящий из трех основных процессов: 1) анодного процесса- образования гидратированных ионов металла в электролите и некомпенсированных электронов на анодных участках по реакции: 2) процесса протекания электронов по металлу от анодных участков к катодным и соответствующего перемещения катионов и анионов в растворе; 3) катодного процесса- ассимиляции электронов какими-либо ионами или молекулами раствора (деполяризаторами), способны к восстановлению на катодных участках по реакции: D+ne=[D ne]. Таким образом, протекание электрохимического коррозионного процесса аналогично работе короткозамкнутого гальванического элемента. При замыкании в электролите двух электродов с разными потенциалами происходит перетекание электронов от более отрицательного электрода (анода) к менее отрицательному (или более положительному) электроду (катоду). Это перетекание электронов выравнивает значения потенциалов замкнутых электродов. Если бы при этом электродные процессы ( анодный на аноде и катодный на катоде) не протекали, потенциалы электродов сравнялись бы и наступила бы полная поляризация.
 Характерными особенностями электрохимического коррозионного процесса являются: 1) подразделение его на два одновременно протекающих, но в значительной степени независимых электродных процесса: анодный и катодный. 2) зависимость кинетики этих двух электрохимических процессов, а следовательно, и скорости коррозии в соответствии с законами электрохимической кинетики от величины электродного потенциала металла: смещение потенциала металла в положительную сторону (например, в результате поляризации от внешнего источника тока) обычно облегчает анодный процесс и затрудняет катодный; смещение потенциала в отрицательную сторону, наоборот, ускоряет катодный процесс и тормозит анодный; 3) возможность локализации анодного и катодного процессов на различных участках поверхности корродирующего металла, где их протекание облегчено; 4) при локализации электродных процессов реализация материального эффекта коррозии на анодных участках поверхности корродирующего металла.
Характерными особенностями электрохимического коррозионного процесса являются: 1) подразделение его на два одновременно протекающих, но в значительной степени независимых электродных процесса: анодный и катодный. 2) зависимость кинетики этих двух электрохимических процессов, а следовательно, и скорости коррозии в соответствии с законами электрохимической кинетики от величины электродного потенциала металла: смещение потенциала металла в положительную сторону (например, в результате поляризации от внешнего источника тока) обычно облегчает анодный процесс и затрудняет катодный; смещение потенциала в отрицательную сторону, наоборот, ускоряет катодный процесс и тормозит анодный; 3) возможность локализации анодного и катодного процессов на различных участках поверхности корродирующего металла, где их протекание облегчено; 4) при локализации электродных процессов реализация материального эффекта коррозии на анодных участках поверхности корродирующего металла.
 Скорость и характер процесса электрохимической коррозии металла зависят от многих факторов, действующих одновременно. К внутренним факторам электрохимической коррозии металлов относятся факторы, связанные с составом, структурной, состоянием поверхности металла, напряжениями в металле и др. Это следующие факторы: 1) термодинамическая устойчивость металла; 2) положение металла в периодической системе элементов Д. И. Менделеева; 3) состояние поверхности металла; 4) границы устойчивости твердых растворов; 5) структурная гетерогенность сплавов и величина зерна; 6) механический фактор( постоянные напряжения; переменные напряжения; истирающее воздействие; кавитационное воздействие); 7) потенциал нулевого заряда; К внешним факторам, связанным с составом коррозионной среды и условиями коррозии, относят: 1) водородный показатель р. Н раствора; 2) состав и концентрация нейтральных растворов; 3) замедлители (ингибиторы) электрохимической коррозии металлов; 4) ускорители (стимуляторы) электрохимической коррозии металлов; 5) скорость движения электролита; 6) температура и давление; 7) контакт с другими металлами; 8) внешняя поляризация постоянным и переменными токами; 9) электрокоррозия;
Скорость и характер процесса электрохимической коррозии металла зависят от многих факторов, действующих одновременно. К внутренним факторам электрохимической коррозии металлов относятся факторы, связанные с составом, структурной, состоянием поверхности металла, напряжениями в металле и др. Это следующие факторы: 1) термодинамическая устойчивость металла; 2) положение металла в периодической системе элементов Д. И. Менделеева; 3) состояние поверхности металла; 4) границы устойчивости твердых растворов; 5) структурная гетерогенность сплавов и величина зерна; 6) механический фактор( постоянные напряжения; переменные напряжения; истирающее воздействие; кавитационное воздействие); 7) потенциал нулевого заряда; К внешним факторам, связанным с составом коррозионной среды и условиями коррозии, относят: 1) водородный показатель р. Н раствора; 2) состав и концентрация нейтральных растворов; 3) замедлители (ингибиторы) электрохимической коррозии металлов; 4) ускорители (стимуляторы) электрохимической коррозии металлов; 5) скорость движения электролита; 6) температура и давление; 7) контакт с другими металлами; 8) внешняя поляризация постоянным и переменными токами; 9) электрокоррозия;
 Требуемую коррозионную стойкость можно во многих случаях обеспечить правильным выбором металла для изготовления конструкции. В тех случаях, когда не удается подобрать достаточно стойкий в условиях эксплуатации металл с хорошими технико-экономическими показателями, необходимо защищать металл, из которого изготовляют конструкцию, от коррозии. Для защиты металлов от электрохимической коррозии применяют следующие основные методы: 1) легирование; 2) обработку коррозионной среды; 3) защитные покрытия; 4) электрохимическую защиту; 5) рациональное конструирование; В практике приходится использовать не один какой-либо метод защиты, а комбинацию методов, что оказывается экономически более выгодным.
Требуемую коррозионную стойкость можно во многих случаях обеспечить правильным выбором металла для изготовления конструкции. В тех случаях, когда не удается подобрать достаточно стойкий в условиях эксплуатации металл с хорошими технико-экономическими показателями, необходимо защищать металл, из которого изготовляют конструкцию, от коррозии. Для защиты металлов от электрохимической коррозии применяют следующие основные методы: 1) легирование; 2) обработку коррозионной среды; 3) защитные покрытия; 4) электрохимическую защиту; 5) рациональное конструирование; В практике приходится использовать не один какой-либо метод защиты, а комбинацию методов, что оказывается экономически более выгодным.
 Легирование металла другими элементами (металлами и неметаллами) имеет целью повышение его коррозионной стойкости или перевод местной коррозии в менее опасную равномерную коррозию. Повышение коррозионной стойкости. По теории Н. Д. Томашова, повышения коррозионной стойкости металлов можно достигнуть одним из трех основных способов: а) введением компонентов, способствующих образованию более совершенного экранирующего защитного слоя продуктов коррозии на поверхности сплава (повышение коррозионной стойкости меди в атмосферных условиях легированием алюминием ( алюминиевые бронзы ) и цинком (латуни); повышение щелочеупорности сталей и чугунов легированием их никелем); б) введением компонентов, уменьшающих катодную активность сплава (введение компонентов, повышающих перенапряжения катодного процесса на данном сплаве: амальгамированием технического цинка, легированием технического магния марганцем с целью повышения устойчивости в кислотах); в) введением компонентов, уменьшающих анодную активность сплава (введение компонентов, повышающих термодинамическую устойчивость анодной фазы (легирование меди золотом и т. п. ); введением более легкопассивирующихся компонентов (легированием никеля хромом); введением компонентов (активных катодов) в условиях возможного установления пассивного состояния, облегчающих наступление пассивности (введением меди в низколегированную сталь при атмосферной коррозии, легированием коррозионностойких хромистых и хромоникелевых сталей небольшими добавками меди, серебра, палладия или платины ). Уменьшение возможности местной коррозии. Уменьшение возможности местной, в частности наиболее опасной межкристаллической коррозии, достигают: а) устранением причин превращения границ зерен в активные аноды (легированием коррозионностойких хромоникелевых сталей активными карбидообразователями- титаном, ниобием танталом, препятствующими удалению хрома из твердого раствора у границ зерен при нагреве стали в опасном интервале температуры); б) выравниванием значения потенциалов зерен и границ зерен сплава за счет сдвига потенциала зерна в отрицательную сторону, т. е. увеличения анодной активности зерна (легированием дюралюминия магнием).
Легирование металла другими элементами (металлами и неметаллами) имеет целью повышение его коррозионной стойкости или перевод местной коррозии в менее опасную равномерную коррозию. Повышение коррозионной стойкости. По теории Н. Д. Томашова, повышения коррозионной стойкости металлов можно достигнуть одним из трех основных способов: а) введением компонентов, способствующих образованию более совершенного экранирующего защитного слоя продуктов коррозии на поверхности сплава (повышение коррозионной стойкости меди в атмосферных условиях легированием алюминием ( алюминиевые бронзы ) и цинком (латуни); повышение щелочеупорности сталей и чугунов легированием их никелем); б) введением компонентов, уменьшающих катодную активность сплава (введение компонентов, повышающих перенапряжения катодного процесса на данном сплаве: амальгамированием технического цинка, легированием технического магния марганцем с целью повышения устойчивости в кислотах); в) введением компонентов, уменьшающих анодную активность сплава (введение компонентов, повышающих термодинамическую устойчивость анодной фазы (легирование меди золотом и т. п. ); введением более легкопассивирующихся компонентов (легированием никеля хромом); введением компонентов (активных катодов) в условиях возможного установления пассивного состояния, облегчающих наступление пассивности (введением меди в низколегированную сталь при атмосферной коррозии, легированием коррозионностойких хромистых и хромоникелевых сталей небольшими добавками меди, серебра, палладия или платины ). Уменьшение возможности местной коррозии. Уменьшение возможности местной, в частности наиболее опасной межкристаллической коррозии, достигают: а) устранением причин превращения границ зерен в активные аноды (легированием коррозионностойких хромоникелевых сталей активными карбидообразователями- титаном, ниобием танталом, препятствующими удалению хрома из твердого раствора у границ зерен при нагреве стали в опасном интервале температуры); б) выравниванием значения потенциалов зерен и границ зерен сплава за счет сдвига потенциала зерна в отрицательную сторону, т. е. увеличения анодной активности зерна (легированием дюралюминия магнием).
 Уменьшение агрессивности коррозионной среды соответствующей обработкой целесообразно только при ее ограниченном объеме. Защита металлов от коррозии может быть достигнута: 1) уменьшением содержания деполяризатора; 2) введением замедлителей коррозии. Уменьшение содержания деполяризатора Скорость электрохимического коррозионного процесса зависит от концентрации деполяризатора в электролите. Уменьшение содержания деполяризатора в коррозионной среде в ряде случаев является эффективным методом борьбы с коррозией металлов. Примерами такого рода обработки коррозионной среды являются: а) нейтрализации кислых сред, вызывающих коррозию металлов за счет водородной деполяризации б) удалением из воды кислорода ( обескислороживание или деаэрация, когда кислород удаляется вместе с воздухом), который вызывает коррозию металлов в результате протекания кислородной деполяризации. Обескислороживание или деаэрация воды осуществляется различными способами: нагреванием воды (термическая деаэрация), продуванием воды инертным газом (десорбционное обескислороживание), введением в воду восстановителей или пропусканием воды через фильтр со стальными стружками или сульфидом железа (химическое обескислороживание).
Уменьшение агрессивности коррозионной среды соответствующей обработкой целесообразно только при ее ограниченном объеме. Защита металлов от коррозии может быть достигнута: 1) уменьшением содержания деполяризатора; 2) введением замедлителей коррозии. Уменьшение содержания деполяризатора Скорость электрохимического коррозионного процесса зависит от концентрации деполяризатора в электролите. Уменьшение содержания деполяризатора в коррозионной среде в ряде случаев является эффективным методом борьбы с коррозией металлов. Примерами такого рода обработки коррозионной среды являются: а) нейтрализации кислых сред, вызывающих коррозию металлов за счет водородной деполяризации б) удалением из воды кислорода ( обескислороживание или деаэрация, когда кислород удаляется вместе с воздухом), который вызывает коррозию металлов в результате протекания кислородной деполяризации. Обескислороживание или деаэрация воды осуществляется различными способами: нагреванием воды (термическая деаэрация), продуванием воды инертным газом (десорбционное обескислороживание), введением в воду восстановителей или пропусканием воды через фильтр со стальными стружками или сульфидом железа (химическое обескислороживание).
 Введение замедлителей коррозии Кислотные замедлители ( ) коррозии чаще всего применяют при удалении с поверхности стали окалины или ржавчины. В качестве замедлителей коррозии металлов в воде и водных растворах солей находят применение некоторые окислители- пассиваторы (нитриты, хроматы и бихроматы) и плёнкообразователи (фосфаты , полифосфаты, амины). Замедлители атмосферной коррозии можно подразделить на две группы: 1)нелетучие (или контактные) замедлители, действие которых ограниченно местом их соприкосновения с поверхностью металла( ); 2)летучие (или парофазные) замедлители: нитриты замещенных аминов (нитриты дициклогексиламина, диизопропиламина); сложные эфиры карбоновых кислот (моноэтанолбензонат, метиловый эфир коричной кислоты); карбонаты замещенных аминов (карбонаты дициклогексиламина, дибутиламина, бензиламина). Чехлы с заложенными в них летучими замедлителями коррозии для хранения под открытым небом.
Введение замедлителей коррозии Кислотные замедлители ( ) коррозии чаще всего применяют при удалении с поверхности стали окалины или ржавчины. В качестве замедлителей коррозии металлов в воде и водных растворах солей находят применение некоторые окислители- пассиваторы (нитриты, хроматы и бихроматы) и плёнкообразователи (фосфаты , полифосфаты, амины). Замедлители атмосферной коррозии можно подразделить на две группы: 1)нелетучие (или контактные) замедлители, действие которых ограниченно местом их соприкосновения с поверхностью металла( ); 2)летучие (или парофазные) замедлители: нитриты замещенных аминов (нитриты дициклогексиламина, диизопропиламина); сложные эфиры карбоновых кислот (моноэтанолбензонат, метиловый эфир коричной кислоты); карбонаты замещенных аминов (карбонаты дициклогексиламина, дибутиламина, бензиламина). Чехлы с заложенными в них летучими замедлителями коррозии для хранения под открытым небом.
 Самый распространенный метод защиты металлов от коррозии- нанесение различных защитных металлический и неметаллических покрытий или превращение поверхностного слоя металла в химическое соединение, обладающее защитными свойствами. Металлические покрытия Все металлические покрытия по их полярности относительно защищаемого металла подразделяются на катодные, электродный потенциал которых в данных условиях положительнее потенциала защищаемого металла (Au, Ag, Cu, Ni, Cr, Pb и др. на углеродистой или низколегированной стали), и анодные, электродный потенциал которых в данных условиях отрицательнее потенциала защищаемого металла (Zn и Cd на углеродистой или низколегированной стали). Катодные покрытия в обычных условиях защищают основной металл механически, изолируя его от воздействия коррозионной среды. При наличии в покрытии пор, трещин и других несплошностей эти участки при осаждении тонкой пленки влаги или при погружении изделия в электролит будут анодами, а вся остальная поверхность изделия- катодом. Анодные покрытия в обычных условиях защищают покрываемый металл не только механически, изолируя его от воздействия коррозионной среды, но и электрохимически. В случае нарушения сплошности анодного покрытия в образовавшемся гальваническом элементе металл покрытия становится анодом и подвергается коррозии, а обнаженный участок основного металла становится катодом и не корродирует. Металлические покрытия наносятся следующими основными методами: 1) погружением в расплавленный металл; 2) термодиффузионным; 3) напылением (металлизацией); 4) механотермическим (плакированием); 5) гальваническим;
Самый распространенный метод защиты металлов от коррозии- нанесение различных защитных металлический и неметаллических покрытий или превращение поверхностного слоя металла в химическое соединение, обладающее защитными свойствами. Металлические покрытия Все металлические покрытия по их полярности относительно защищаемого металла подразделяются на катодные, электродный потенциал которых в данных условиях положительнее потенциала защищаемого металла (Au, Ag, Cu, Ni, Cr, Pb и др. на углеродистой или низколегированной стали), и анодные, электродный потенциал которых в данных условиях отрицательнее потенциала защищаемого металла (Zn и Cd на углеродистой или низколегированной стали). Катодные покрытия в обычных условиях защищают основной металл механически, изолируя его от воздействия коррозионной среды. При наличии в покрытии пор, трещин и других несплошностей эти участки при осаждении тонкой пленки влаги или при погружении изделия в электролит будут анодами, а вся остальная поверхность изделия- катодом. Анодные покрытия в обычных условиях защищают покрываемый металл не только механически, изолируя его от воздействия коррозионной среды, но и электрохимически. В случае нарушения сплошности анодного покрытия в образовавшемся гальваническом элементе металл покрытия становится анодом и подвергается коррозии, а обнаженный участок основного металла становится катодом и не корродирует. Металлические покрытия наносятся следующими основными методами: 1) погружением в расплавленный металл; 2) термодиффузионным; 3) напылением (металлизацией); 4) механотермическим (плакированием); 5) гальваническим;
 Коррозия металла с анодным и катодным защитными покрытиями. Химические соединения металлов Защитные пленки на металлах могут быть получены путем превращения поверхностного слоя металла воздействием реагентов или электрохимического тока в химические соединения, обладающие защитными свойствами. К ним относят: оксидирование и фосфатирование. Неметаллические покрытия. К ним относят: 1) органические покрытия в виде смазки (различные минеральные масла, растворы парафинов, битумов и др. ), лакокрасочных покрытий, лака, краски, смолы; 2) неорганические покрытия, к которым относят цементные и бетонные покрытия, эмали, керамические кислотоупорные плитки.
Коррозия металла с анодным и катодным защитными покрытиями. Химические соединения металлов Защитные пленки на металлах могут быть получены путем превращения поверхностного слоя металла воздействием реагентов или электрохимического тока в химические соединения, обладающие защитными свойствами. К ним относят: оксидирование и фосфатирование. Неметаллические покрытия. К ним относят: 1) органические покрытия в виде смазки (различные минеральные масла, растворы парафинов, битумов и др. ), лакокрасочных покрытий, лака, краски, смолы; 2) неорганические покрытия, к которым относят цементные и бетонные покрытия, эмали, керамические кислотоупорные плитки.
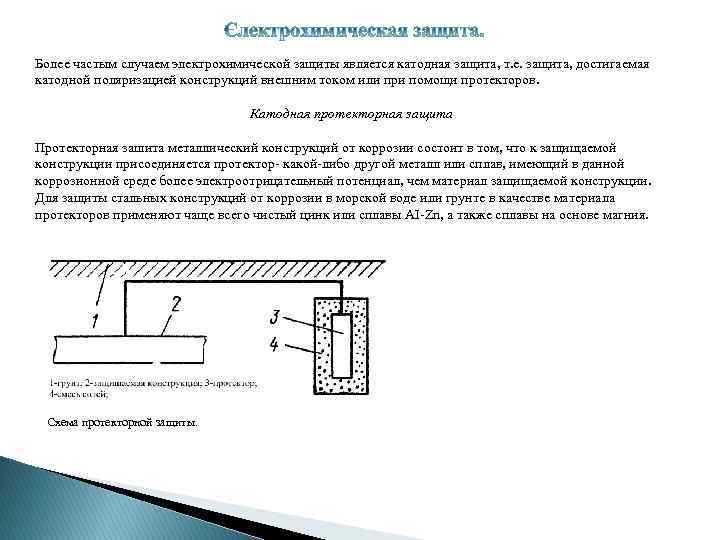 Более частым случаем электрохимической защиты является катодная защита, т. е. защита, достигаемая катодной поляризацией конструкций внешним током или при помощи протекторов. Катодная протекторная защита Протекторная зашита металлический конструкций от коррозии состоит в том, что к защищаемой конструкции присоединяется протектор- какой-либо другой металл или сплав, имеющий в данной коррозионной среде более электроотрицательный потенциал, чем материал защищаемой конструкции. Для защиты стальных конструкций от коррозии в морской воде или грунте в качестве материала протекторов применяют чаще всего чистый цинк или сплавы AI-Zn, а также сплавы на основе магния. Схема протекторной защиты.
Более частым случаем электрохимической защиты является катодная защита, т. е. защита, достигаемая катодной поляризацией конструкций внешним током или при помощи протекторов. Катодная протекторная защита Протекторная зашита металлический конструкций от коррозии состоит в том, что к защищаемой конструкции присоединяется протектор- какой-либо другой металл или сплав, имеющий в данной коррозионной среде более электроотрицательный потенциал, чем материал защищаемой конструкции. Для защиты стальных конструкций от коррозии в морской воде или грунте в качестве материала протекторов применяют чаще всего чистый цинк или сплавы AI-Zn, а также сплавы на основе магния. Схема протекторной защиты.
 Катодная защита внешним током- защита металла от коррозии с помощью постоянного тока от внешнего источника. Она заключается в том, что защищаемый металл присоединяют к отрицательному полюсу внешнего источника тока (т. е. в качестве катода), а к положительному полюсу присоединяют дополнительный электрод, поляризуемый анодно. Таким образом, при пропускании тока поверхность защищаемой металлической конструкции поляризуется катодно, ее потенциал смещается в отрицательную сторону, что приводит к уменьшению или полному прекращению коррозионного разрушения. Активному разрушению при этом подвергается анод, который обычно выполняется из металлического лома, старых труб, рельсов и др. Схема катодной защиты внешним током.
Катодная защита внешним током- защита металла от коррозии с помощью постоянного тока от внешнего источника. Она заключается в том, что защищаемый металл присоединяют к отрицательному полюсу внешнего источника тока (т. е. в качестве катода), а к положительному полюсу присоединяют дополнительный электрод, поляризуемый анодно. Таким образом, при пропускании тока поверхность защищаемой металлической конструкции поляризуется катодно, ее потенциал смещается в отрицательную сторону, что приводит к уменьшению или полному прекращению коррозионного разрушения. Активному разрушению при этом подвергается анод, который обычно выполняется из металлического лома, старых труб, рельсов и др. Схема катодной защиты внешним током.
 В зависимости от природы неметаллические материалы делятся на две группы: а) материалы неорганического происхождения; б) материалы органического происхождения. К материалам неорганического происхождения относятся: 1) горные породы (граниты, андезиты, бештауниты); 2) искусственные силикатные изделия, получаемые плавлением горных пород (каменное литье, плавленый кварц, стекло); 3) керамические изделия, получаемые методом спекания (каменно-керамические изделия, фарфор); 4) вяжущие силикатные материалы (цементы, асбоцемент, бетоны); К материалам органического происхождения относятся: 1) непластичные материалы ( древесина, уголь, графит); 2) пластические массы: конденсационные ( фаолит, текстолит, стеклотекстолит), полимеризационные (винипласт, полиэтилен, полипропилен, полиизобутилен, асбовинил, фторопласты и др. )
В зависимости от природы неметаллические материалы делятся на две группы: а) материалы неорганического происхождения; б) материалы органического происхождения. К материалам неорганического происхождения относятся: 1) горные породы (граниты, андезиты, бештауниты); 2) искусственные силикатные изделия, получаемые плавлением горных пород (каменное литье, плавленый кварц, стекло); 3) керамические изделия, получаемые методом спекания (каменно-керамические изделия, фарфор); 4) вяжущие силикатные материалы (цементы, асбоцемент, бетоны); К материалам органического происхождения относятся: 1) непластичные материалы ( древесина, уголь, графит); 2) пластические массы: конденсационные ( фаолит, текстолит, стеклотекстолит), полимеризационные (винипласт, полиэтилен, полипропилен, полиизобутилен, асбовинил, фторопласты и др. )
 Использованные источники. 1) 2) 3) «Курс коррозии и защиты металлов» Н. П. Жук, М. 1968 http: //www. biohim. ru/corrosion/ http: //www. okorrozii. com/elektrximichiskakorozia. html
Использованные источники. 1) 2) 3) «Курс коррозии и защиты металлов» Н. П. Жук, М. 1968 http: //www. biohim. ru/corrosion/ http: //www. okorrozii. com/elektrximichiskakorozia. html



