стр. атома. лицей.ppt
- Количество слайдов: 71

 Электронные конфигурации атомов и периодичность свойств химических элементов 400 лет до н. э. , Демокрит, греч. философ Вещество можно делить лишь до тех пор, пока не будут получены его наименьшие частицы. Он назвал эти частицы атомами (неделимый).
Электронные конфигурации атомов и периодичность свойств химических элементов 400 лет до н. э. , Демокрит, греч. философ Вещество можно делить лишь до тех пор, пока не будут получены его наименьшие частицы. Он назвал эти частицы атомами (неделимый).
 1808 г. , англ. химик Дальтон сформулировал атомистическую теорию. «Все вещества состоят из атомов, мельчайших неделимых частиц, которые не могут быть ни созданы, ни уничтожены» . 1886 г. Бутлеров А. М. высказал предположение, что может быть атомы ”не неделимы по своей природе, а неделимы только доступными нам ныне средствами” Д. И. Менделеев допускал предположение, “что называемое нами неделимым (атом) неделимо только обычными химическими силами…”
1808 г. , англ. химик Дальтон сформулировал атомистическую теорию. «Все вещества состоят из атомов, мельчайших неделимых частиц, которые не могут быть ни созданы, ни уничтожены» . 1886 г. Бутлеров А. М. высказал предположение, что может быть атомы ”не неделимы по своей природе, а неделимы только доступными нам ныне средствами” Д. И. Менделеев допускал предположение, “что называемое нами неделимым (атом) неделимо только обычными химическими силами…”
 Начало 20 века Фотоэффект – испускание электронов металлами и полупроводниками… Радиоактивность (фр. физик Беккерель) – самопроизвольный распад атомов… U, Th; к 1912 г. их насчитывалось 39 М≥ 209
Начало 20 века Фотоэффект – испускание электронов металлами и полупроводниками… Радиоактивность (фр. физик Беккерель) – самопроизвольный распад атомов… U, Th; к 1912 г. их насчитывалось 39 М≥ 209
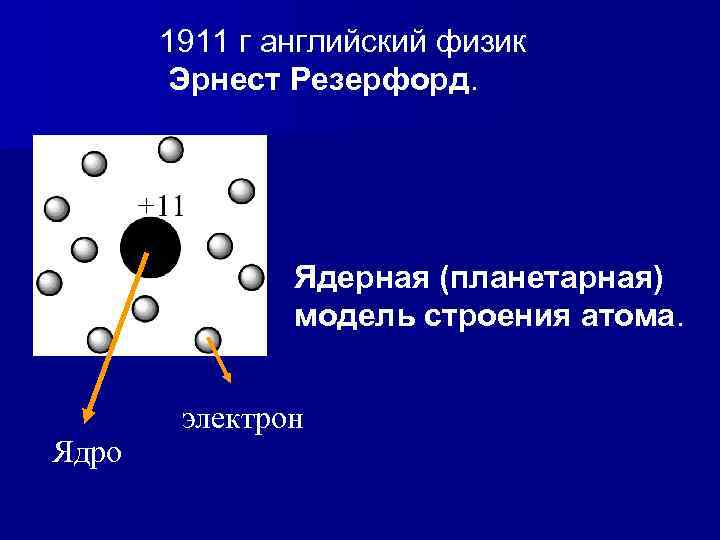 1911 г английский физик Эрнест Резерфорд. Ядерная (планетарная) модель строения атома. Ядро электрон
1911 г английский физик Эрнест Резерфорд. Ядерная (планетарная) модель строения атома. Ядро электрон
 Недостатки планетарной теории Изменяется ли во времени энергия движущегося вокруг ядра электрона? На каких расстояниях от ядра движется электрон? Как объяснить линейный спектр атомов элементов? 20 век; физические методы исследования: рентгеноскопия, спектроскопия, электронография, ПМР, ЯМР …
Недостатки планетарной теории Изменяется ли во времени энергия движущегося вокруг ядра электрона? На каких расстояниях от ядра движется электрон? Как объяснить линейный спектр атомов элементов? 20 век; физические методы исследования: рентгеноскопия, спектроскопия, электронография, ПМР, ЯМР …
 Радиус атома 10 -10 м; радиус ядра 10 -15 м. Масса ядра 1, 67· 10 -27 кг (атом водорода); масса электрона 9, 1· 10 -31 кг. Скорость движения электрона 108 м/с. Электрон в 1835 раз легче ядра. Классическая электромагнитная теория и устойчивость атома
Радиус атома 10 -10 м; радиус ядра 10 -15 м. Масса ядра 1, 67· 10 -27 кг (атом водорода); масса электрона 9, 1· 10 -31 кг. Скорость движения электрона 108 м/с. Электрон в 1835 раз легче ядра. Классическая электромагнитная теория и устойчивость атома
 1913 г Нильс Бор (Дания). «Разрешённые» орбиты. Принцип квантования энергии
1913 г Нильс Бор (Дания). «Разрешённые» орбиты. Принцип квантования энергии
 1924 г французский учёный Луи де Бройль – предположение о волновом характере материи. mv h – постоянная Планка, равная 6, 626∙ 10 -34 Дж∙с
1924 г французский учёный Луи де Бройль – предположение о волновом характере материи. mv h – постоянная Планка, равная 6, 626∙ 10 -34 Дж∙с
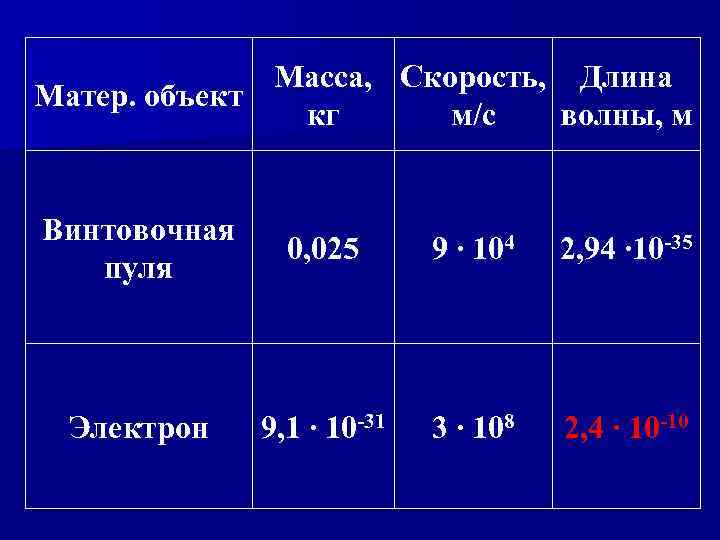 Масса, Скорость, Длина Матер. объект кг м/с волны, м Винтовочная пуля 0, 025 9 ∙ 104 2, 94 ∙ 10 -35 Электрон 9, 1 ∙ 10 -31 3 ∙ 108 2, 4 ∙ 10 -10
Масса, Скорость, Длина Матер. объект кг м/с волны, м Винтовочная пуля 0, 025 9 ∙ 104 2, 94 ∙ 10 -35 Электрон 9, 1 ∙ 10 -31 3 ∙ 108 2, 4 ∙ 10 -10
 Дифракция электронов (впоследствии и нейтронов) Квантовая механика Гейзенберг (нем. уч. , 1926 г. ) Принцип неопределённости: Δp • Δq ≥ h / 2π Δp -… неточность измерения mv Δq -… координаты
Дифракция электронов (впоследствии и нейтронов) Квантовая механика Гейзенберг (нем. уч. , 1926 г. ) Принцип неопределённости: Δp • Δq ≥ h / 2π Δp -… неточность измерения mv Δq -… координаты
 Оценка вероятности… Волновое ур-ие Шрёдингера; 1926 г (Эрвин Шрёдингер - австрийский физик): НΨ=ЕΨ где, Н – оператор Гамильтона Е – энергия электрона. Ψ -… Ψ 2 -. . . Ψ 2 ∆V - …∆V (орбиталь электрона).
Оценка вероятности… Волновое ур-ие Шрёдингера; 1926 г (Эрвин Шрёдингер - австрийский физик): НΨ=ЕΨ где, Н – оператор Гамильтона Е – энергия электрона. Ψ -… Ψ 2 -. . . Ψ 2 ∆V - …∆V (орбиталь электрона).
 Ψ 1, Ψ 2, Ψ 3, …, Е 1, Е 2, Е 3, … , ряд дискретных «разрешённых» энергий (квантование энергии) Ψ – волновая функция, соответствующая амплитуде трёхмерного волнового процесса; Ψ = f(x, y, z). где x, y, z – координаты точки. Результатом решения ур-ия Шрёдингера является комбинация некоторых параметров - набор целых чисел n, l, и ml
Ψ 1, Ψ 2, Ψ 3, …, Е 1, Е 2, Е 3, … , ряд дискретных «разрешённых» энергий (квантование энергии) Ψ – волновая функция, соответствующая амплитуде трёхмерного волнового процесса; Ψ = f(x, y, z). где x, y, z – координаты точки. Результатом решения ур-ия Шрёдингера является комбинация некоторых параметров - набор целых чисел n, l, и ml
 Пространственное движение электрона в атоме может быть описано тремя целыми числами, которые называют квантовыми. n, l, и ml - квантовые числа; определяют геометрические особенности электронного облака - важное следствие теории квантовой механики.
Пространственное движение электрона в атоме может быть описано тремя целыми числами, которые называют квантовыми. n, l, и ml - квантовые числа; определяют геометрические особенности электронного облака - важное следствие теории квантовой механики.
 Характеристика энергии электрона и пространственное распределение вероятности нахождения его в атоме системой квантовых чисел. Квантовые числа n -главное квантовое число; n = 1, 2, 3, …
Характеристика энергии электрона и пространственное распределение вероятности нахождения его в атоме системой квантовых чисел. Квантовые числа n -главное квантовое число; n = 1, 2, 3, …
 Чем ↑ n , тем ↑ энергией обладает электрон, и тем слабее он связан с ядром.
Чем ↑ n , тем ↑ энергией обладает электрон, и тем слабее он связан с ядром.
 Электроны, характеризующиеся одним и тем же значением главного квантового числа, образуют в атоме электронные облака приблизительно одинаковых размеров. Поэтому можно говорить о существовании в атоме энергетических уровней (электронных слоев или оболочек), отвечающих определенным значениям главного квантового числа - n.
Электроны, характеризующиеся одним и тем же значением главного квантового числа, образуют в атоме электронные облака приблизительно одинаковых размеров. Поэтому можно говорить о существовании в атоме энергетических уровней (электронных слоев или оболочек), отвечающих определенным значениям главного квантового числа - n.
 l - орбитальное квантовое число, определяет момент количества движения электрона (векторная величина); форму эл. обл. ; эн. электр. в подуровне l = 0, 1, 2, 3…(n-1); Энергетический подуровень – это совокупность электронных состояний, характеризующихся определенным набором квантовых чисел n и l.
l - орбитальное квантовое число, определяет момент количества движения электрона (векторная величина); форму эл. обл. ; эн. электр. в подуровне l = 0, 1, 2, 3…(n-1); Энергетический подуровень – это совокупность электронных состояний, характеризующихся определенным набором квантовых чисел n и l.
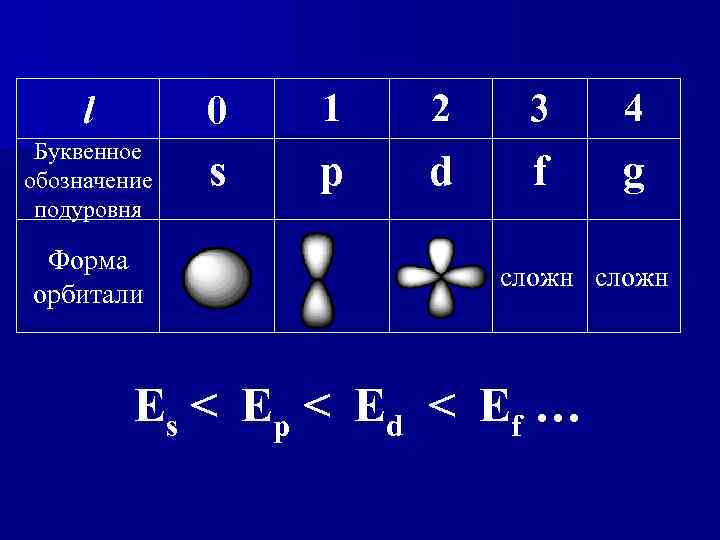 l 0 1 2 3 4 Буквенное обозначение подуровня s p d f g Форма орбитали сложн Es < Ep < E d < Ef …
l 0 1 2 3 4 Буквенное обозначение подуровня s p d f g Форма орбитали сложн Es < Ep < E d < Ef …
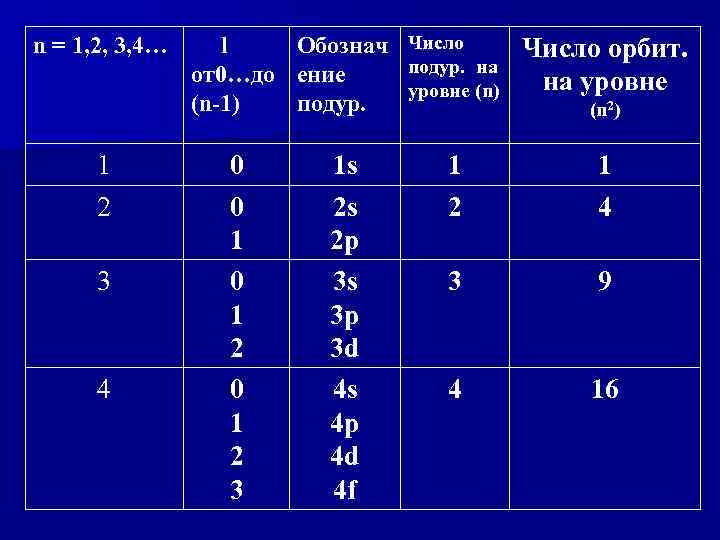 n = 1, 2, 3, 4… 1 2 3 4 l Обознач Число орбит. подур. на от 0…до ение на уровне (n) (n-1) подур. (n 2 ) 0 0 1 2 3 1 s 2 s 2 p 3 s 3 p 3 d 4 s 4 p 4 d 4 f 1 2 1 4 3 9 4 16
n = 1, 2, 3, 4… 1 2 3 4 l Обознач Число орбит. подур. на от 0…до ение на уровне (n) (n-1) подур. (n 2 ) 0 0 1 2 3 1 s 2 s 2 p 3 s 3 p 3 d 4 s 4 p 4 d 4 f 1 2 1 4 3 9 4 16
 ml - магнитное квантовое число Значения ml характеризуют разрешённые ориентации электронного облака в пространстве (ml = -l … 0…+l).
ml - магнитное квантовое число Значения ml характеризуют разрешённые ориентации электронного облака в пространстве (ml = -l … 0…+l).
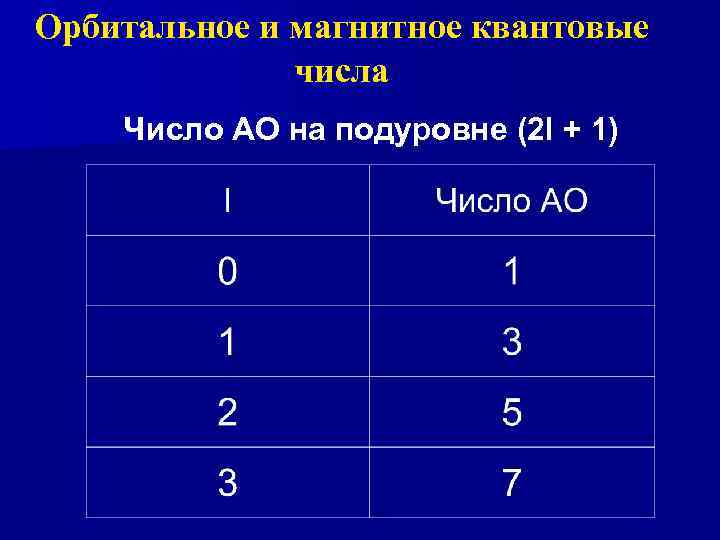 Орбитальное и магнитное квантовые числа Число АО на подуровне (2 l + 1)
Орбитальное и магнитное квантовые числа Число АО на подуровне (2 l + 1)
 Любому значению l соответствует (2 l+1) возможных расположений электронного облака данного типа в пространстве.
Любому значению l соответствует (2 l+1) возможных расположений электронного облака данного типа в пространстве.
 Все орбитали, принадлежащие одному подуровню данного энергетического уровня, имеют одинаковую энергию. Состояние электрона в атоме, характеризующееся определенными значениями чисел n, l, ml называется атомной орбиталью.
Все орбитали, принадлежащие одному подуровню данного энергетического уровня, имеют одинаковую энергию. Состояние электрона в атоме, характеризующееся определенными значениями чисел n, l, ml называется атомной орбиталью.
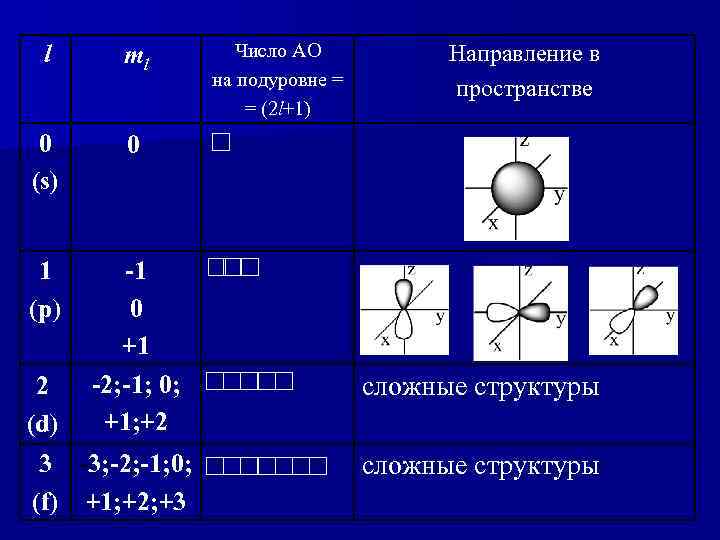 l ml 0 (s) 0 1 (p) -1 0 +1 -2; -1; 0; +1; +2 2 (d) 3 -3; -2; -1; 0; (f) +1; +2; +3 Число АО на подуровне = = (2 l+1) Направление в пространстве сложные структуры
l ml 0 (s) 0 1 (p) -1 0 +1 -2; -1; 0; +1; +2 2 (d) 3 -3; -2; -1; 0; (f) +1; +2; +3 Число АО на подуровне = = (2 l+1) Направление в пространстве сложные структуры
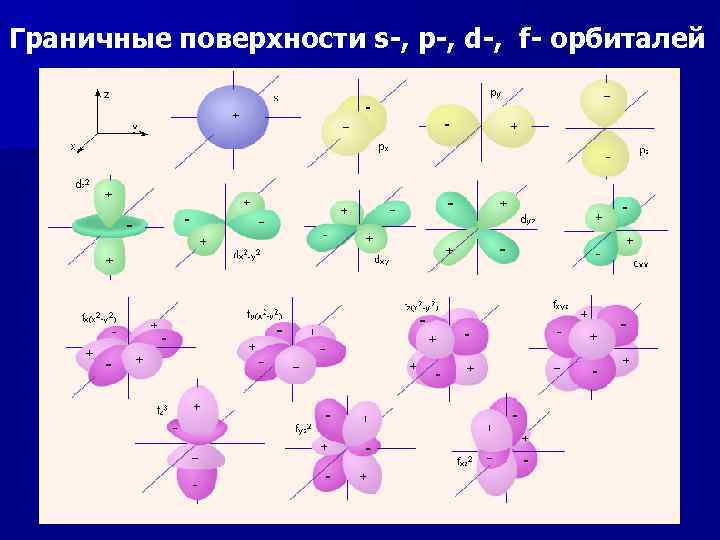 Граничные поверхности s-, p-, d-, f- орбиталей
Граничные поверхности s-, p-, d-, f- орбиталей
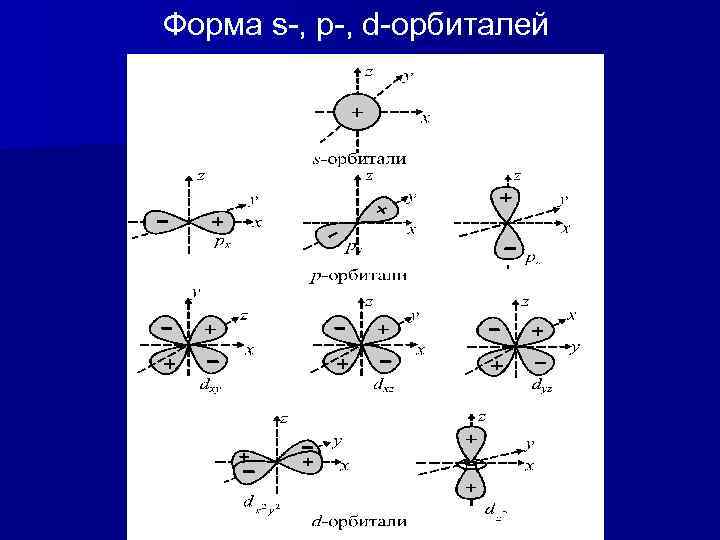 Форма s-, p-, d-орбиталей
Форма s-, p-, d-орбиталей
 ms – спиновое квантовое число характеризует собственный механический момент электрона, связанный с вращением его вокруг своей оси - по часовой стрелке и против часовой стрелки. to spin - вращать Значение + 1/2 ms = +1/2 ( ) + Значение – 1/2 ms = – 1/2 ( ) –
ms – спиновое квантовое число характеризует собственный механический момент электрона, связанный с вращением его вокруг своей оси - по часовой стрелке и против часовой стрелки. to spin - вращать Значение + 1/2 ms = +1/2 ( ) + Значение – 1/2 ms = – 1/2 ( ) –
 Принципы заполнения электронами энергетических уровней и подуровней Принцип минимума полной энергии атома Распр. электр. в атоме Уровни Подуровни Орбитали Z; форм. эл. конф. min Е; max Есв. Реализуется этот принцип, если:
Принципы заполнения электронами энергетических уровней и подуровней Принцип минимума полной энергии атома Распр. электр. в атоме Уровни Подуровни Орбитали Z; форм. эл. конф. min Е; max Есв. Реализуется этот принцип, если:
 Принцип Паули В атоме не может быть двух электронов, у которых все четыре квантовых числа были бы одинаковыми. +1/2 нет -1/2 +1/2 да
Принцип Паули В атоме не может быть двух электронов, у которых все четыре квантовых числа были бы одинаковыми. +1/2 нет -1/2 +1/2 да
 Правило Гунда В пределах одного энергетического подуровня электроны располагаются т. о. , чтобы их суммарный спин был максимальным. px py pz $ # $ -1/2 +1/2 -1/2 spin = 1/2 # -1/2 +1/2 spin = 1/2 нет
Правило Гунда В пределах одного энергетического подуровня электроны располагаются т. о. , чтобы их суммарный спин был максимальным. px py pz $ # $ -1/2 +1/2 -1/2 spin = 1/2 # -1/2 +1/2 spin = 1/2 нет
 px py pz # $ # # $ $ +1/2 -1/2 spin = 3/2 да
px py pz # $ # # $ $ +1/2 -1/2 spin = 3/2 да
 Правила В. М. Клечковского 1) возрастание суммы (n+l); 2) увеличение n.
Правила В. М. Клечковского 1) возрастание суммы (n+l); 2) увеличение n.
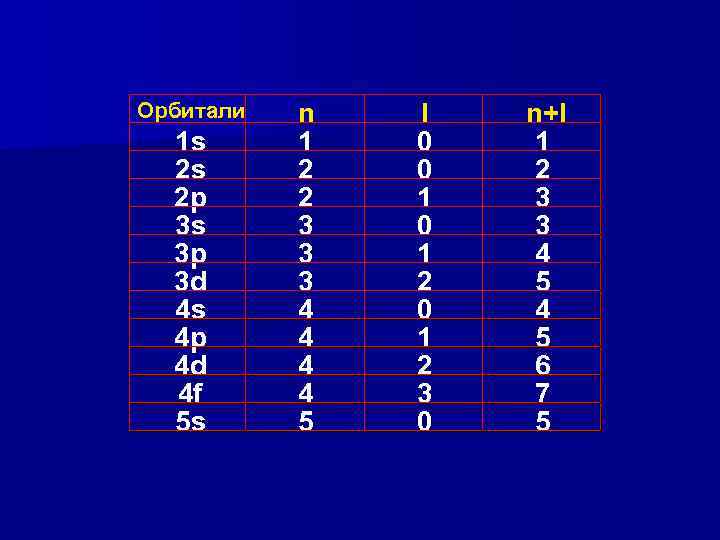 Орбитали 1 s 2 s 2 p 3 s 3 p 3 d 4 s 4 p 4 d 4 f 5 s n 1 2 2 3 3 3 4 4 5 l 0 0 1 2 3 0 n+l 1 2 3 3 4 5 6 7 5
Орбитали 1 s 2 s 2 p 3 s 3 p 3 d 4 s 4 p 4 d 4 f 5 s n 1 2 2 3 3 3 4 4 5 l 0 0 1 2 3 0 n+l 1 2 3 3 4 5 6 7 5
 1 s 22 p 63 s 23 p 64 s 23 d 104 p 65 s 24 d 105 p 66 s 2 4 f 145 d 106 p 67 s 25 f 146 d 107 p 6… 1 s 22 p 63 s 23 p 64 s 23 d 104 p 65 s 24 d 105 p 66 s 2 5 d 14 f 145 d 2 -106 p 67 s 26 d 15 f 146 d 2 -107 p 6…
1 s 22 p 63 s 23 p 64 s 23 d 104 p 65 s 24 d 105 p 66 s 2 4 f 145 d 106 p 67 s 25 f 146 d 107 p 6… 1 s 22 p 63 s 23 p 64 s 23 d 104 p 65 s 24 d 105 p 66 s 2 5 d 14 f 145 d 2 -106 p 67 s 26 d 15 f 146 d 2 -107 p 6…
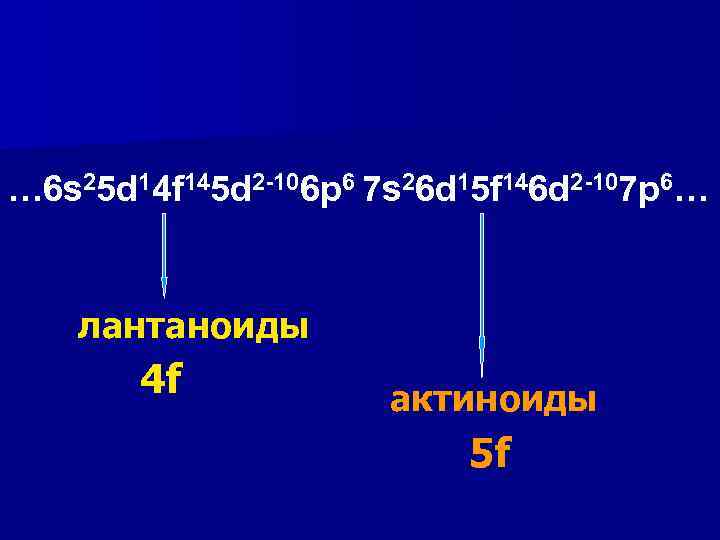 … 6 s 25 d 14 f 145 d 2 -106 p 6 7 s 26 d 15 f 146 d 2 -107 p 6… лантаноиды 4 f актиноиды 5 f
… 6 s 25 d 14 f 145 d 2 -106 p 6 7 s 26 d 15 f 146 d 2 -107 p 6… лантаноиды 4 f актиноиды 5 f
![Малые периоды 11 Na 2 1 s 2 2 s 6 2 p [Ne] Малые периоды 11 Na 2 1 s 2 2 s 6 2 p [Ne]](https://present5.com/presentation/3/-29906771_15817224.pdf-img/-29906771_15817224.pdf-38.jpg) Малые периоды 11 Na 2 1 s 2 2 s 6 2 p [Ne] … 1 3 s
Малые периоды 11 Na 2 1 s 2 2 s 6 2 p [Ne] … 1 3 s
![14 Si 16 S 18 Ar 2 [Ne] 3 s 2 3 p 4 14 Si 16 S 18 Ar 2 [Ne] 3 s 2 3 p 4](https://present5.com/presentation/3/-29906771_15817224.pdf-img/-29906771_15817224.pdf-39.jpg) 14 Si 16 S 18 Ar 2 [Ne] 3 s 2 3 p 4 3 p 6
14 Si 16 S 18 Ar 2 [Ne] 3 s 2 3 p 4 3 p 6
 Большие периоды 19 K 21 Sc 23 V 26 Fe 30 Zn 31 Ga 36 Kr [Ar] [Ar] 1 4 s 2 4 s 2 4 s 1 3 d 3 3 d 6 3 d 10 1 3 d 4 p 10 6 3 d 4 p
Большие периоды 19 K 21 Sc 23 V 26 Fe 30 Zn 31 Ga 36 Kr [Ar] [Ar] 1 4 s 2 4 s 2 4 s 1 3 d 3 3 d 6 3 d 10 1 3 d 4 p 10 6 3 d 4 p
 «Проскок (провал) электрона» Энергет. выгодный «провал» набл. при достройке d-подуровня до пяти (половина макс. ёмкости) или десяти (макс. ёмкость). ns 2 (n-1)d 4 ns 1 (n-1)d 5 ns 2 (n-1)d 9 ns 1 (n-1)d 10
«Проскок (провал) электрона» Энергет. выгодный «провал» набл. при достройке d-подуровня до пяти (половина макс. ёмкости) или десяти (макс. ёмкость). ns 2 (n-1)d 4 ns 1 (n-1)d 5 ns 2 (n-1)d 9 ns 1 (n-1)d 10
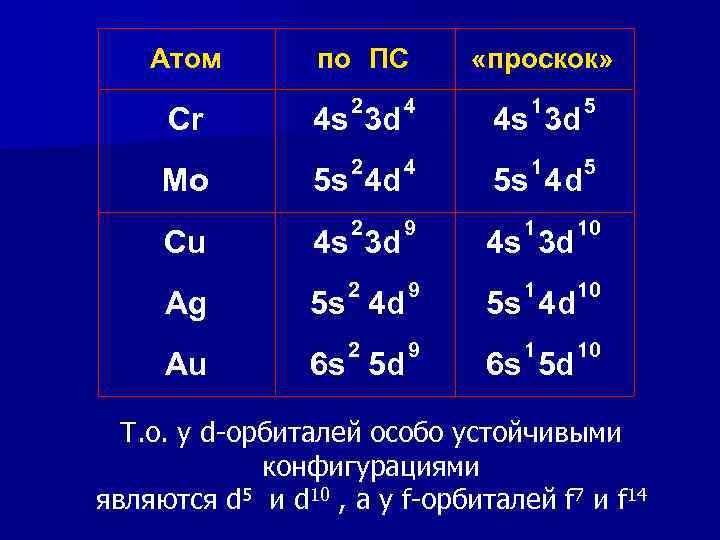 Атом по ПС «проскок» Cr 2 4 s 3 d 4 1 4 s 3 d 5 Mo 2 5 s 4 d 4 1 5 Cu 2 4 s 3 d 9 1 4 s 3 d 10 Ag 2 5 s 4 d 9 1 5 s 4 d 10 Au 2 9 1 10 6 s 5 d 5 s 4 d 6 s 5 d Т. о. у d-орбиталей особо устойчивыми конфигурациями являются d 5 и d 10 , а у f-орбиталей f 7 и f 14
Атом по ПС «проскок» Cr 2 4 s 3 d 4 1 4 s 3 d 5 Mo 2 5 s 4 d 4 1 5 Cu 2 4 s 3 d 9 1 4 s 3 d 10 Ag 2 5 s 4 d 9 1 5 s 4 d 10 Au 2 9 1 10 6 s 5 d 5 s 4 d 6 s 5 d Т. о. у d-орбиталей особо устойчивыми конфигурациями являются d 5 и d 10 , а у f-орбиталей f 7 и f 14
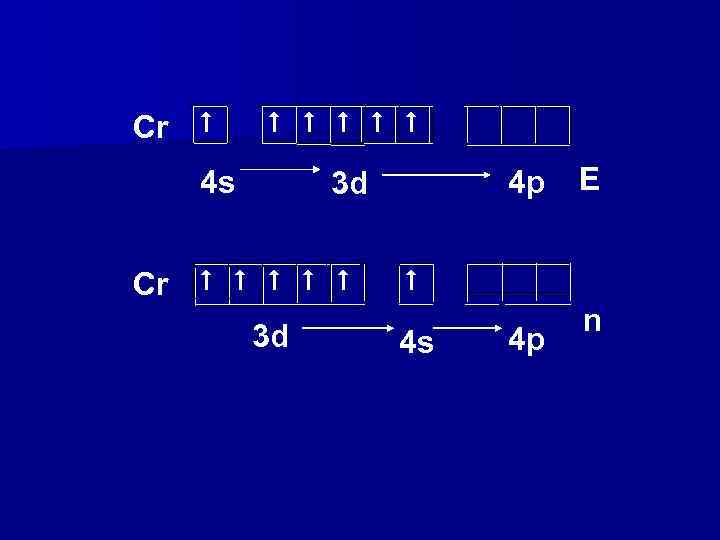 Cr # # # 4 s 4 p 3 d Cr # # # 3 d E # 4 s 4 p n
Cr # # # 4 s 4 p 3 d Cr # # # 3 d E # 4 s 4 p n
 Периодический закон и периодическая система Д. И. Менделеева.
Периодический закон и периодическая система Д. И. Менделеева.
 1869 г. Д. И. Менделеев: свойства простых тел, а также свойства и формы их соединений находятся в периодической зависимости от величины атомных весов. Современная формулировка: свойства химических элементов, а также формы и свойства их соединений находятся в периодической зависимости от величины заряда ядер их атомов в результате периодического повторения электронных конфигураций внешнего энергетического уровня.
1869 г. Д. И. Менделеев: свойства простых тел, а также свойства и формы их соединений находятся в периодической зависимости от величины атомных весов. Современная формулировка: свойства химических элементов, а также формы и свойства их соединений находятся в периодической зависимости от величины заряда ядер их атомов в результате периодического повторения электронных конфигураций внешнего энергетического уровня.
 H 2 O PH 3 H 2 S HCl H 2 Se При определении свойств Д. И. Менделеев пользовался правилом среднего арифметического К дисс. (I) H 2 Se = 1, 7∙ 10 -4 К дисс. (I) H 2 S = 6, 0∙ 10 -8
H 2 O PH 3 H 2 S HCl H 2 Se При определении свойств Д. И. Менделеев пользовался правилом среднего арифметического К дисс. (I) H 2 Se = 1, 7∙ 10 -4 К дисс. (I) H 2 S = 6, 0∙ 10 -8
 Период – ряд элементов, расположенных в порядке возрастания Z, электронная конфигурация внешнего энергет. уровня которых изменяется от ns 1 до ns 2 p 6 (кроме I периода). Элементы – аналоги - расположены в одной подгруппе ПС; имеют одинаковое строение внешних электр. оболочек атомов при различных значениях n и поэтому проявляют сходные хим. св-ва.
Период – ряд элементов, расположенных в порядке возрастания Z, электронная конфигурация внешнего энергет. уровня которых изменяется от ns 1 до ns 2 p 6 (кроме I периода). Элементы – аналоги - расположены в одной подгруппе ПС; имеют одинаковое строение внешних электр. оболочек атомов при различных значениях n и поэтому проявляют сходные хим. св-ва.
 Периодичность изменения радиусов атомов и ионов, энергии ионизации, сродства к электрону и электроотрицательности элементов.
Периодичность изменения радиусов атомов и ионов, энергии ионизации, сродства к электрону и электроотрицательности элементов.
 Атомные и ионные радиусы Радиусы атомов рассчитывают исходя из межъядерных расстояний в твёрдых веществах или молекулах газов. Радиус, нм N+5 0, 015 N 0 0, 071 увеличение N-3 0, 148
Атомные и ионные радиусы Радиусы атомов рассчитывают исходя из межъядерных расстояний в твёрдых веществах или молекулах газов. Радиус, нм N+5 0, 015 N 0 0, 071 увеличение N-3 0, 148
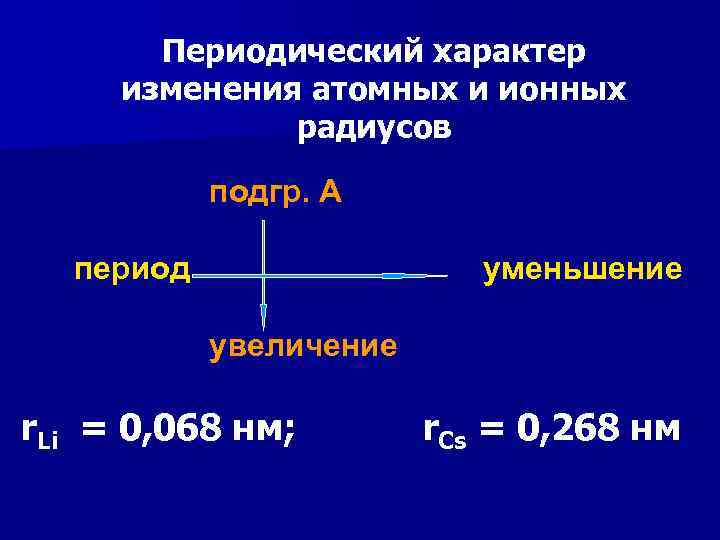 Периодический характер изменения атомных и ионных радиусов подгр. А период уменьшение увеличение r. Li = 0, 068 нм; r. Cs = 0, 268 нм
Периодический характер изменения атомных и ионных радиусов подгр. А период уменьшение увеличение r. Li = 0, 068 нм; r. Cs = 0, 268 нм
 В ряду изоэлектр. катионов (… 2 s 22 p 6): Na+ Mg 2+ Al 3+ 0, 095 0, 065 0, 050 нм уменьшение
В ряду изоэлектр. катионов (… 2 s 22 p 6): Na+ Mg 2+ Al 3+ 0, 095 0, 065 0, 050 нм уменьшение
 Энергия (потенциал) ионизации Li 1 s 22 s 1 I 1 = 520, 0 к. Дж/моль I 2 = 7295, 8 к. Дж/моль 14 I 3 = 11770, 6 к. Дж/моль 23
Энергия (потенциал) ионизации Li 1 s 22 s 1 I 1 = 520, 0 к. Дж/моль I 2 = 7295, 8 к. Дж/моль 14 I 3 = 11770, 6 к. Дж/моль 23
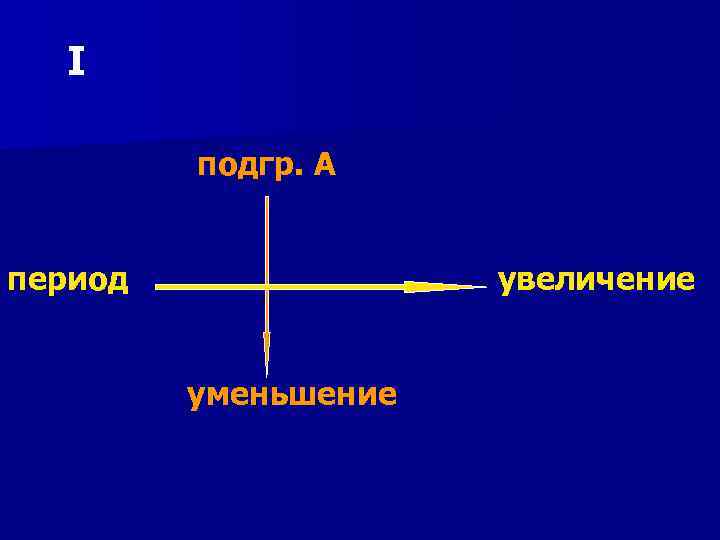 I подгр. А период увеличение уменьшение
I подгр. А период увеличение уменьшение
 Атом I, к. Дж/моль Mg 738, 1 Ba 502, 7 Увеличение восстановительной способности
Атом I, к. Дж/моль Mg 738, 1 Ba 502, 7 Увеличение восстановительной способности
 Энергия сродства к электрону (сродство к электрону Еа) Н 0 + 1 е = Н 1 s 1 1 s 2 Еа(Н) = 73 к. Дж/моль (энергия выделяется)
Энергия сродства к электрону (сродство к электрону Еа) Н 0 + 1 е = Н 1 s 1 1 s 2 Еа(Н) = 73 к. Дж/моль (энергия выделяется)
 Атом Eа, к. Дж/моль Ba -47 Cl 348, 7 Увеличение окислительной способности
Атом Eа, к. Дж/моль Ba -47 Cl 348, 7 Увеличение окислительной способности
 Ea подгр. А период увеличение уменьшение
Ea подгр. А период увеличение уменьшение
 Электроотрицательность ( ) По Малликену: =1/2(I 1 + Ea) По Полингу: Li H 1, 0 2, 1 F 4, 0
Электроотрицательность ( ) По Малликену: =1/2(I 1 + Ea) По Полингу: Li H 1, 0 2, 1 F 4, 0
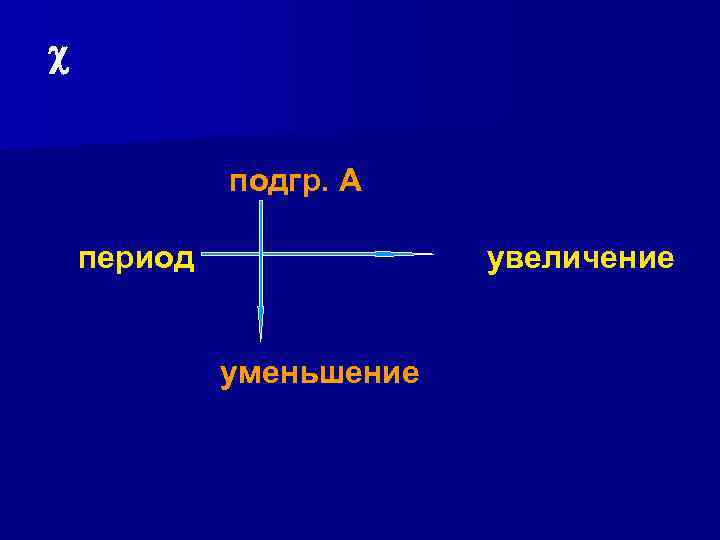 подгр. А период увеличение уменьшение
подгр. А период увеличение уменьшение
 Химическая связь и строение молекул
Химическая связь и строение молекул
 Молекула – это термодинамически устойчивая динамическая система, представляющая собой совокупность ядер и электронов, которая характеризуется минимумом полной энергии системы.
Молекула – это термодинамически устойчивая динамическая система, представляющая собой совокупность ядер и электронов, которая характеризуется минимумом полной энергии системы.
 Термодинамика процесса образования молекулы Образование молекул из атомов – процесс самопроизвольный ΔG < 0 ΔG = ΔН – ТΔS ΔН – энтальпийный фактор; -ТΔS – энтропийный фактор
Термодинамика процесса образования молекулы Образование молекул из атомов – процесс самопроизвольный ΔG < 0 ΔG = ΔН – ТΔS ΔН – энтальпийный фактор; -ТΔS – энтропийный фактор
 энтропия S 2 < S 1 А + В = АВ S 1 S 2 ΔS < 0 -ТΔS>0 ΔН < 0 ΔG < 0 Основная причина образования химических связей между атомами -
энтропия S 2 < S 1 А + В = АВ S 1 S 2 ΔS < 0 -ТΔS>0 ΔН < 0 ΔG < 0 Основная причина образования химических связей между атомами -
 Электрическая природа химической связи ао АО ов ОВ Типы электростатического взаимодействия: 1. Взаимодействия ядро – электрон: Ав способствуют образованию Ва химической связи
Электрическая природа химической связи ао АО ов ОВ Типы электростатического взаимодействия: 1. Взаимодействия ядро – электрон: Ав способствуют образованию Ва химической связи
 2. Межэлектронные взаимодействия : а) притяжение электронов с антипараллельными спинами (+) б) отталкивание электронов с параллельными спинами (-). 3. Межъядерное отталкивание АВ не способствует образованию химической связи.
2. Межэлектронные взаимодействия : а) притяжение электронов с антипараллельными спинами (+) б) отталкивание электронов с параллельными спинами (-). 3. Межъядерное отталкивание АВ не способствует образованию химической связи.
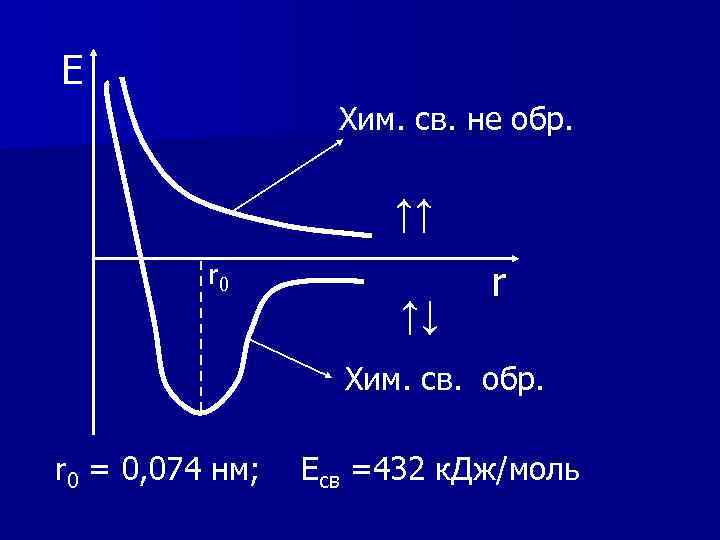 Е Хим. св. не обр. ↑↑ r 0 ↑↓ r Хим. св. обр. r 0 = 0, 074 нм; Есв =432 к. Дж/моль
Е Хим. св. не обр. ↑↑ r 0 ↑↓ r Хим. св. обр. r 0 = 0, 074 нм; Есв =432 к. Дж/моль
 Химическая связь – это совокупность электронно – ядерных взаимодействий, приводящих к минимуиу потенциальной энергии системы. Теории химической связи ВС ММО
Химическая связь – это совокупность электронно – ядерных взаимодействий, приводящих к минимуиу потенциальной энергии системы. Теории химической связи ВС ММО
 Основные положения метода валентных связей 1. Обобществление валентных электронов (двухэлектронная; двухцентровая) 2. неспаренные электроны с антипараллельными спинами (↑↓) 3. Частичное перекрывание атомных орбиталей
Основные положения метода валентных связей 1. Обобществление валентных электронов (двухэлектронная; двухцентровая) 2. неспаренные электроны с антипараллельными спинами (↑↓) 3. Частичное перекрывание атомных орбиталей
 4. Степень перекрывания атомных орбиталей и прочность связи 5. Направление и степень перекрывания электронных облаков
4. Степень перекрывания атомных орбиталей и прочность связи 5. Направление и степень перекрывания электронных облаков
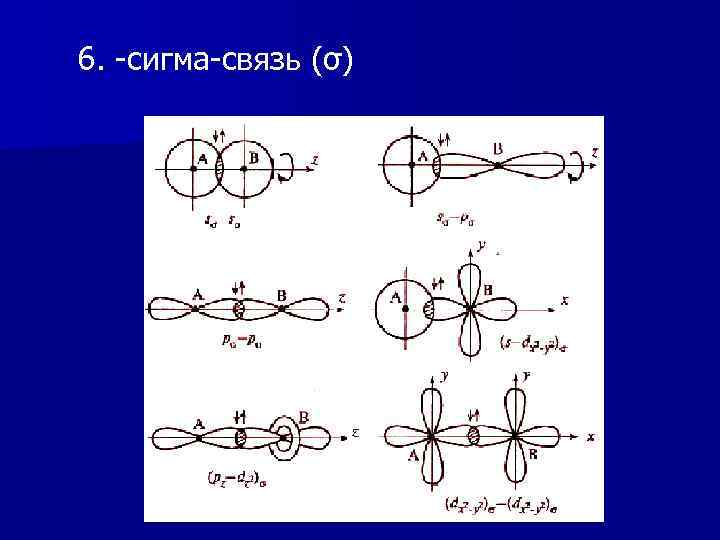 6. -сигма-связь (σ)
6. -сигма-связь (σ)
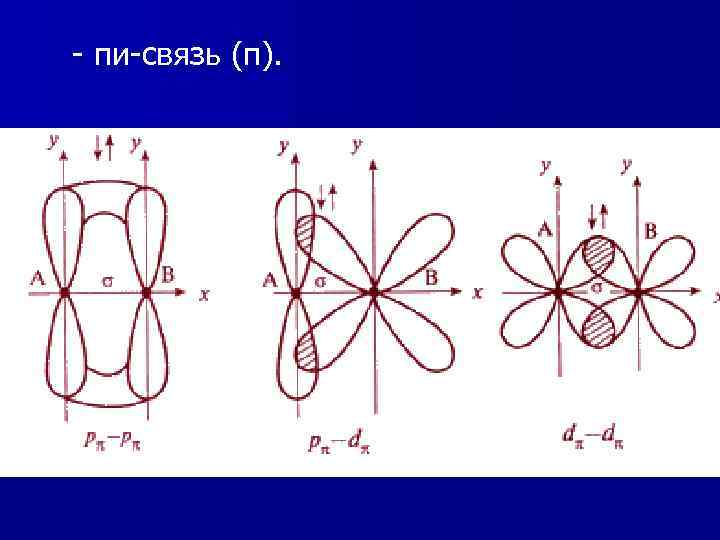 - пи-связь (π).
- пи-связь (π).


