Квант сандары.pptx
- Количество слайдов: 7

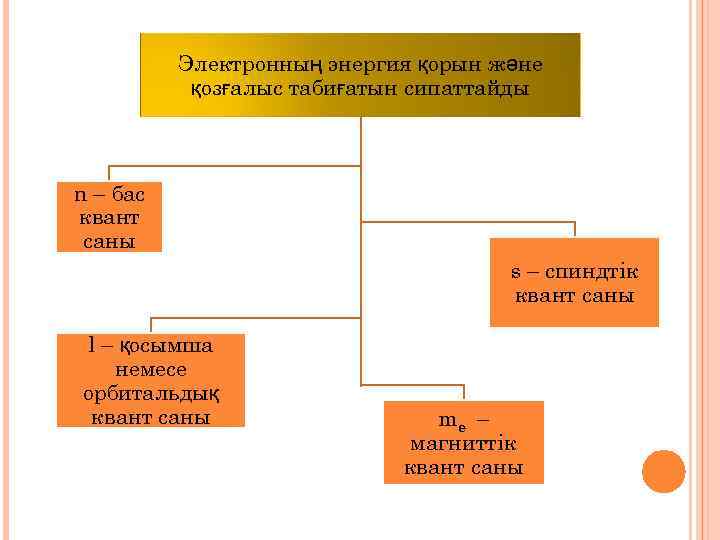
Электронның энергия қорын және қозғалыс табиғатын сипаттайды n – бас квант саны s – спиндтік квант саны l – қосымша немесе орбитальдық квант саны me – магниттік квант саны

ФИЗИКАЛЫҚ МА ҒЫНАСЫ:

Атом орбиталінің мөлшерін, электронның энергия қорын көрсетеді. Бас квант саны бірден басталатын бүтін сандарды қабылдайды, n = 1, 2, 3, 4, оны әріптермен белгілеуге болады, K, L, M, N.

ОРБИТАЛЬДЫҚ КВАНТ САНЫ l - Электронның энергетикалық күйін, және электрондық бұлт пішінін көрсетеді, электронның ядро айналасында қозғалуынан туатын орбитальды магнит моментін анықтайды, оның мәндерін: l = 0, 1, 2, 3. . . (n-1) n = 1 болғанда l = 0 (1 s), s - электрон бұлтының пішіні шар тәріздес болады. n = 2 l =0 (s) 2 s l = 1 (p) 2 p p – гантель пішіндес n = 3 l = 0 (s) – 3 s l = 1 (p) – 3 p l = 2 (d) – 3 d d, f- деңгейшелерінің пішіндері күрделілеу болады.

МАГНИТТІК КВАНТ САНЫ m- Электрон орбиталінің кеңістікте орналасуын көрсетеді, бұл сан – l. . . 0. . . + l аралығындағы бүтін мәндерді қабылдайды, электрон орбиталінің қозғалысының орбитальдық моментінің көрсетілген бағытқа (координат осіне) проекциясының мәнін анықтайды. Энергия шамалары бірдей орбитальді туынды жағдай деп атайды.

СПИН КВАНТ САНЫ s- Электронды сипаттайдын массасы, заряды тәріздес электронның өз осінен айналу бағытын көрсететін шама, ол екі мәнді болады: +½ және - ½. Орбитальдарды кванттық ұяшықтар арқылы белгілесек, әрбір ұяда спиндері қарама-қарсы екі электрон болады. Көп электронды атомдар үшін де Шредингердің толқындық теңдеуін жуықтап шешіп (Томас, Ферми, Хартри, Фок), деңгейлердің энергия қорын және электрон тығыздығының таралуын есептеуге болады, электрондар күйі жоғарыда көрсетілген квант сандарымен сипатталады.
Квант сандары.pptx