 ЭЛЕКТРОННОЕ СТРОЕНИЕ АТОМА Лекция № 4
ЭЛЕКТРОННОЕ СТРОЕНИЕ АТОМА Лекция № 4
 Ранние модели строения атома «Пудинг с изюмом» (1902 -1904 г. Дж. Томсон) «Планетарная» (1907 г. Э. Резерфорд) «Модель Бора» (1913 г. )
Ранние модели строения атома «Пудинг с изюмом» (1902 -1904 г. Дж. Томсон) «Планетарная» (1907 г. Э. Резерфорд) «Модель Бора» (1913 г. )
 Современная модель атома - Квантово-механическая Атом – электронейтральная частица Ядро атома – положительно заряженное Электроны – отрицательно заряженные Электроны вращаются вокруг ядра с определённой скоростью Электроны имеют двойственную природу
Современная модель атома - Квантово-механическая Атом – электронейтральная частица Ядро атома – положительно заряженное Электроны – отрицательно заряженные Электроны вращаются вокруг ядра с определённой скоростью Электроны имеют двойственную природу
 Корпускулярно-волновой дуализм Электрон – частица с массой m = 9, 1*10 -31 кг, скоростью v = 106 м/с, величина заряда электрона 1, 6*10 -19 Кл. Электрон как волна λ = 2, 4*10 -8 м.
Корпускулярно-волновой дуализм Электрон – частица с массой m = 9, 1*10 -31 кг, скоростью v = 106 м/с, величина заряда электрона 1, 6*10 -19 Кл. Электрон как волна λ = 2, 4*10 -8 м.
 Уравнение Планка Е = h ν, Е – энергия кванта; h – постоянная Планка 6, 626∙ 10 -34 Дж∙с; ν–частота колебаний ν = с/λ
Уравнение Планка Е = h ν, Е – энергия кванта; h – постоянная Планка 6, 626∙ 10 -34 Дж∙с; ν–частота колебаний ν = с/λ
 Уравнение Шредингера Описывает движение электрона как волны. Атомная орбиталь – это часть пространства (описывается волновой функцией Шредингера), где вероятность нахождения электрона максимальна.
Уравнение Шредингера Описывает движение электрона как волны. Атомная орбиталь – это часть пространства (описывается волновой функцией Шредингера), где вероятность нахождения электрона максимальна.
 Квантовые числа n – главное квантовое число (характеризует энергию электрона на уровне, показывает размер атомной орбитали) l – орбитальное квантовое число (характеризует энергию электрона на подуровне, показывает форму атомной орбитали) ml – магнитное квантовое число (характеризует пространственную ориентацию электронных облаков) ms – спиновое квантовое число (характеризует величину и ориентацию спина)
Квантовые числа n – главное квантовое число (характеризует энергию электрона на уровне, показывает размер атомной орбитали) l – орбитальное квантовое число (характеризует энергию электрона на подуровне, показывает форму атомной орбитали) ml – магнитное квантовое число (характеризует пространственную ориентацию электронных облаков) ms – спиновое квантовое число (характеризует величину и ориентацию спина)
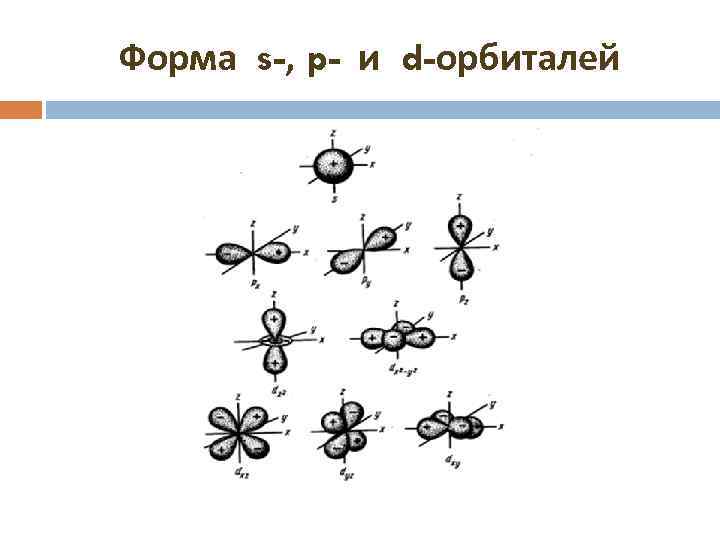 Форма s-, p- и d-орбиталей
Форма s-, p- и d-орбиталей
 Принцип запрета Паули: «В атоме не может быть двух электронов , у которых были бы одинаковыми все четыре квантовых числа» . Правило Клечковского: «Заполнение энергетических уровней происходит в порядке возрастания суммы чисел n + l, а при равных значениях суммы – в порядке возрастания n» . Правило Гунда: «В данном подуровне электроны стремятся занять энергетические состояния таким образом , чтобы суммарный спин был максимальным» .
Принцип запрета Паули: «В атоме не может быть двух электронов , у которых были бы одинаковыми все четыре квантовых числа» . Правило Клечковского: «Заполнение энергетических уровней происходит в порядке возрастания суммы чисел n + l, а при равных значениях суммы – в порядке возрастания n» . Правило Гунда: «В данном подуровне электроны стремятся занять энергетические состояния таким образом , чтобы суммарный спин был максимальным» .
 Электронные семейства элементов s-элементы, если заполняется s-подуровень p-элементы, если заполняется p-подуровень d-элементы, если заполняется d-подуровень f-элементы, если заполняется f-подуровень
Электронные семейства элементов s-элементы, если заполняется s-подуровень p-элементы, если заполняется p-подуровень d-элементы, если заполняется d-подуровень f-элементы, если заполняется f-подуровень





















