охт.pptx
- Количество слайдов: 29
 ЭЛЕКТРОЛИЗ Решение задач Выполнил: Махров П. В. Группа 1 ХТ-49 Д
ЭЛЕКТРОЛИЗ Решение задач Выполнил: Махров П. В. Группа 1 ХТ-49 Д
 Электрохимические процессы взаимного превращения электрической формы энергии в химическую. Электродныйпотенциал– φ– cкачок потенциалов, возникающий на границе раздела металл− раствор за счет процессов растворения-осаждения металла. [φ]= В.
Электрохимические процессы взаимного превращения электрической формы энергии в химическую. Электродныйпотенциал– φ– cкачок потенциалов, возникающий на границе раздела металл− раствор за счет процессов растворения-осаждения металла. [φ]= В.






 Электролиз – это совокупность процессов, протекающих в растворе или расплаве электролита, при пропускании через него электрического тока. Анодом при электролизе называется положительный электрод, катодом — отрицательный. Положительные ионы — катионы — (ионы металлов, водородные ионы, ионы аммония и др. ) — движутся к катоду, отрицательные ионы — анионы — (ионы кислотных остатков и гидроксильной группы) — движутся к аноду.
Электролиз – это совокупность процессов, протекающих в растворе или расплаве электролита, при пропускании через него электрического тока. Анодом при электролизе называется положительный электрод, катодом — отрицательный. Положительные ионы — катионы — (ионы металлов, водородные ионы, ионы аммония и др. ) — движутся к катоду, отрицательные ионы — анионы — (ионы кислотных остатков и гидроксильной группы) — движутся к аноду.
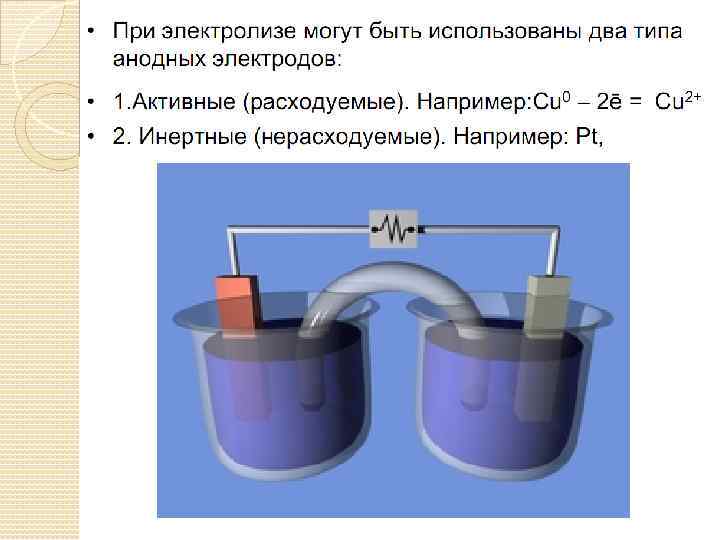







 Выход по току – это выраженное в процентах отношение количества фактически затраченного электричества (Qфакт) к теоретически необходимому(Qтеор): Bт = (Qфакт/ Qтеор)·100% Иногда в задачах используется выход по току, рассчитанный как степень отклонения массы фактически прореагировавшего на электроде вещества (mфакт) к теоретически рассчитанной по закону Фарадея (mтеор): Bт = (mфакт/ mтеор)·100%
Выход по току – это выраженное в процентах отношение количества фактически затраченного электричества (Qфакт) к теоретически необходимому(Qтеор): Bт = (Qфакт/ Qтеор)·100% Иногда в задачах используется выход по току, рассчитанный как степень отклонения массы фактически прореагировавшего на электроде вещества (mфакт) к теоретически рассчитанной по закону Фарадея (mтеор): Bт = (mфакт/ mтеор)·100%
 При электролизе водного раствора Аg. NO 3 с нерастворимым анодом в течение 50 мин. при силе тока в 3, 0 А на катоде выделилось 9, 6 г серебра. Вычислить выход по току. Решение: Выход по току находим как Bт = (mфакт / mтеор)·100% mтеор = Mэ·I·τ / F Совместим обе формулы и проведем вычисление: Bт= (mфакт ·F·100%)/ Mэ·I·τ = 9, 6·96500·100/107, 87·3·3000 = 95, 42%
При электролизе водного раствора Аg. NO 3 с нерастворимым анодом в течение 50 мин. при силе тока в 3, 0 А на катоде выделилось 9, 6 г серебра. Вычислить выход по току. Решение: Выход по току находим как Bт = (mфакт / mтеор)·100% mтеор = Mэ·I·τ / F Совместим обе формулы и проведем вычисление: Bт= (mфакт ·F·100%)/ Mэ·I·τ = 9, 6·96500·100/107, 87·3·3000 = 95, 42%
 Выход по энергии – это количество электрической энергии (выраженное в к. Вт·час), затраченное на весовую единицу полученного продукта: Bэ = (1000·I·τ·U)/m где I – сила тока, А; τ – продолжительность процесса электролиза, ч; U – рабочее напряжение, В; m – масса полученного продукта, г. Толщину слоя металлического покрытия вычисляют по формуле: h = i. К·m. Э·ВТ·τ ·1000/ F·ρ где h – толщина покрытия, мкм; ρ – плотность металла, г/см 3; ВТ – выход металла по току, %; m. Э – молярная масса эквивалента металла, г/моль; F – постоянная Фарадея, Кл или А. ч; τ – продолжительность электролиза, с. или час; i. К – катодная плотность тока, А/см 2.
Выход по энергии – это количество электрической энергии (выраженное в к. Вт·час), затраченное на весовую единицу полученного продукта: Bэ = (1000·I·τ·U)/m где I – сила тока, А; τ – продолжительность процесса электролиза, ч; U – рабочее напряжение, В; m – масса полученного продукта, г. Толщину слоя металлического покрытия вычисляют по формуле: h = i. К·m. Э·ВТ·τ ·1000/ F·ρ где h – толщина покрытия, мкм; ρ – плотность металла, г/см 3; ВТ – выход металла по току, %; m. Э – молярная масса эквивалента металла, г/моль; F – постоянная Фарадея, Кл или А. ч; τ – продолжительность электролиза, с. или час; i. К – катодная плотность тока, А/см 2.
 Пример. Сколько времени нужно пропускать ток силой 2, 0 А через раствор сульфата никеля, чтобы покрыть металлическую пластинку с площадью поверхности равной 200 см 2 слоем никеля, толщиной 0, 01 мм, если плотность никеля 8, 9 г/см 3. Выход по току составляет 90 %. Решение: Объем покрытия: V= S×h = 200 × 0, 001 = 0. 2 см 3 Масса покрытия: mфакт = V×r = 0, 2 × 8, 9 = 1, 78 г. Молярная масса эквивалента никеля Mэ = 29, 345 г/моль. Из уравнения Bт = (mфакт·F·100% )/ Mэ·I·τ выразим время: τ = (mфакт·F·100% )/ Mэ·I·τ·Bт = 1, 78· 96500 ·100 / 29, 345· 2 ·90 = 3251 с = 54, 2 мин
Пример. Сколько времени нужно пропускать ток силой 2, 0 А через раствор сульфата никеля, чтобы покрыть металлическую пластинку с площадью поверхности равной 200 см 2 слоем никеля, толщиной 0, 01 мм, если плотность никеля 8, 9 г/см 3. Выход по току составляет 90 %. Решение: Объем покрытия: V= S×h = 200 × 0, 001 = 0. 2 см 3 Масса покрытия: mфакт = V×r = 0, 2 × 8, 9 = 1, 78 г. Молярная масса эквивалента никеля Mэ = 29, 345 г/моль. Из уравнения Bт = (mфакт·F·100% )/ Mэ·I·τ выразим время: τ = (mфакт·F·100% )/ Mэ·I·τ·Bт = 1, 78· 96500 ·100 / 29, 345· 2 ·90 = 3251 с = 54, 2 мин
 Пример. Определите толщину слоя платины (в миллиметрах), нанесенной на другой металл гальваническим методом. Исходный электролит H 2[Pt. Cl 6]. Площадь поверхности металлической пластинки 250 см 2, плотность пластины 21, 47 г/см 2. Время электролиза 45 мин, ток силой 0, 2 А, выход по току составляет 90%. Решение: Зная выход по току, определяем массу выделенного при электролизе вещества:
Пример. Определите толщину слоя платины (в миллиметрах), нанесенной на другой металл гальваническим методом. Исходный электролит H 2[Pt. Cl 6]. Площадь поверхности металлической пластинки 250 см 2, плотность пластины 21, 47 г/см 2. Время электролиза 45 мин, ток силой 0, 2 А, выход по току составляет 90%. Решение: Зная выход по току, определяем массу выделенного при электролизе вещества:
 η=Gф/Gt=525/555=0. 946
η=Gф/Gt=525/555=0. 946


 Пример 1. При рафинировании меди ток силой в 50 А выделил - за 5 ч чистую медь массой 281 г. Какому выходу по току это соответствует? Решение. По законам Фарадея можно рассчитать теоретическое значение массы выделившейся меди: Выход по току находим по формуле: .
Пример 1. При рафинировании меди ток силой в 50 А выделил - за 5 ч чистую медь массой 281 г. Какому выходу по току это соответствует? Решение. По законам Фарадея можно рассчитать теоретическое значение массы выделившейся меди: Выход по току находим по формуле: .
 Через раствор, содержащий ионы Pb 2+, в течение 5 мин. пропускался ток постоянной силы. За это время масса катода увеличилась на 1, 24 г. Какова сила тока, который был использован для электролиза? Решение. Поскольку нет дополнительных сведений, считаем выход по току 100%-ным. Тогда для расчета силы тока можно воспользоваться законом Фарадея:
Через раствор, содержащий ионы Pb 2+, в течение 5 мин. пропускался ток постоянной силы. За это время масса катода увеличилась на 1, 24 г. Какова сила тока, который был использован для электролиза? Решение. Поскольку нет дополнительных сведений, считаем выход по току 100%-ным. Тогда для расчета силы тока можно воспользоваться законом Фарадея:
 Ток последовательно проходит через два электролизера, в которых содержатся водные растворы: а) Ni. SO 4; б) Fe. Cl 2. Какие количества металлов выделятся на катодах, если известно, что у анода второго электролизера выделилось 1, 4 л хлора? Решение. Воспользуемся законом эквивалентов для расчета массы железа, выделившегося на катоде второго электролизера:
Ток последовательно проходит через два электролизера, в которых содержатся водные растворы: а) Ni. SO 4; б) Fe. Cl 2. Какие количества металлов выделятся на катодах, если известно, что у анода второго электролизера выделилось 1, 4 л хлора? Решение. Воспользуемся законом эквивалентов для расчета массы железа, выделившегося на катоде второго электролизера:
 Переведем объем хлора в массу: Аналогично вычислим массу никеля, выделившегося на катоде первого электролизера:
Переведем объем хлора в массу: Аналогично вычислим массу никеля, выделившегося на катоде первого электролизера:


