Электролитическая диссоциация воды.pptx
- Количество слайдов: 12
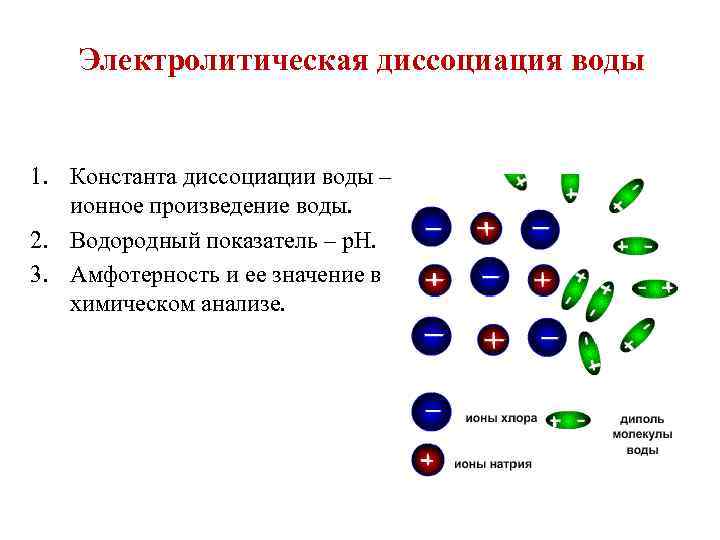 Электролитическая диссоциация воды 1. Константа диссоциации воды – ионное произведение воды. 2. Водородный показатель – р. Н. 3. Амфотерность и ее значение в химическом анализе.
Электролитическая диссоциация воды 1. Константа диссоциации воды – ионное произведение воды. 2. Водородный показатель – р. Н. 3. Амфотерность и ее значение в химическом анализе.
 По уравнению электролитической диссоциации воды видно, что вода типичный электролит, проявляющий амфотерные свойства: Н 2 О ↔ 2 Н+ + ОНион Н+ - носитель кислотных свойств, ион ОН- - обуславливает щелочные свойства воды Как видно из уравнения диссоциации в жидкой воде концентрация ионов водорода приблизительно равна концентрации ионов гидроксила и поэтому можно написать, что в воде [Н+] = [ОН-]
По уравнению электролитической диссоциации воды видно, что вода типичный электролит, проявляющий амфотерные свойства: Н 2 О ↔ 2 Н+ + ОНион Н+ - носитель кислотных свойств, ион ОН- - обуславливает щелочные свойства воды Как видно из уравнения диссоциации в жидкой воде концентрация ионов водорода приблизительно равна концентрации ионов гидроксила и поэтому можно написать, что в воде [Н+] = [ОН-]
![Применив закон действующих масс к равновесной системе электролитической диссоциации воды получим: [Н+][ОН-] / [Н Применив закон действующих масс к равновесной системе электролитической диссоциации воды получим: [Н+][ОН-] / [Н](https://present5.com/presentation/161171421_271237115/image-3.jpg) Применив закон действующих масс к равновесной системе электролитической диссоциации воды получим: [Н+][ОН-] / [Н 2 О] = К, т. е. получаем константу электролитической диссоциации воды. Подобные процессы называют реакциями автопротолиза, в этих реакциях одна молекула амфипротного растворителя ведет себя как кислота, а другая как основание. Вычисления по электрической проводимости показали, что концентрация ионов водорода и гидроксид-ионов в воде оказалась равна 10 -7 моль/л при 220 С. Преобразуя это уравнение, получаем [Н+] • [ОН-] = [Н 2 О] • К. Но степень диссоциации воды очень мала, и концентрацию ее недиссоциированных молекул в любом разбавленном водном растворе можно считать величиной постоянной.
Применив закон действующих масс к равновесной системе электролитической диссоциации воды получим: [Н+][ОН-] / [Н 2 О] = К, т. е. получаем константу электролитической диссоциации воды. Подобные процессы называют реакциями автопротолиза, в этих реакциях одна молекула амфипротного растворителя ведет себя как кислота, а другая как основание. Вычисления по электрической проводимости показали, что концентрация ионов водорода и гидроксид-ионов в воде оказалась равна 10 -7 моль/л при 220 С. Преобразуя это уравнение, получаем [Н+] • [ОН-] = [Н 2 О] • К. Но степень диссоциации воды очень мала, и концентрацию ее недиссоциированных молекул в любом разбавленном водном растворе можно считать величиной постоянной.
![Т. о. в правой части уравнения находятся 2 -ве постоянные величины: [Н 2 О] Т. о. в правой части уравнения находятся 2 -ве постоянные величины: [Н 2 О]](https://present5.com/presentation/161171421_271237115/image-4.jpg) Т. о. в правой части уравнения находятся 2 -ве постоянные величины: [Н 2 О] – концентрация недиссоциированных молекул воды и К – константа диссоциации. Но произведение 2 -х постоянных величин есть также величина постоянная. Поэтому заменив [Н 2 О] • К новой константой, получим [Н+] [ОН-] = КН 2 О. Следовательно, как бы не изменялись концентрации ионов Н+ и ОН- в воде или в разбавленном водном растворе, произведение их остается величиной практически постоянной. Эту величину называют ионным произведением воды. Числовое значение этой константы нетрудно найти, подставив в уравнение значения концентраций водородных и гидроксид-ионов в воде: КН 2 О = [Н+][ОН-] = 10 -7 = 10 -14
Т. о. в правой части уравнения находятся 2 -ве постоянные величины: [Н 2 О] – концентрация недиссоциированных молекул воды и К – константа диссоциации. Но произведение 2 -х постоянных величин есть также величина постоянная. Поэтому заменив [Н 2 О] • К новой константой, получим [Н+] [ОН-] = КН 2 О. Следовательно, как бы не изменялись концентрации ионов Н+ и ОН- в воде или в разбавленном водном растворе, произведение их остается величиной практически постоянной. Эту величину называют ионным произведением воды. Числовое значение этой константы нетрудно найти, подставив в уравнение значения концентраций водородных и гидроксид-ионов в воде: КН 2 О = [Н+][ОН-] = 10 -7 = 10 -14
 Реакцию того или иного раствора принято характеризовать концентрацией водородных ионов, т. к. концентрацию ионов ОН- легко вычислить, исходя из ионного произведения воды. 1. Всякий раствор будет называться нейтральным, если в нем при комнатной температуре [Н+] = [ОН-] = 10 -7 гион/л. 2. Для кислых растворов справедливо условие [Н+]>[ОН-]; [Н+]>10 -7 г-ион/л, [ОН-]<10 -7. 3. Для щелочных растворов справедливо - [Н+]<[ОН-]; [Н+]<10 -7, [ОН]<10 -7 г-ион/л.
Реакцию того или иного раствора принято характеризовать концентрацией водородных ионов, т. к. концентрацию ионов ОН- легко вычислить, исходя из ионного произведения воды. 1. Всякий раствор будет называться нейтральным, если в нем при комнатной температуре [Н+] = [ОН-] = 10 -7 гион/л. 2. Для кислых растворов справедливо условие [Н+]>[ОН-]; [Н+]>10 -7 г-ион/л, [ОН-]<10 -7. 3. Для щелочных растворов справедливо - [Н+]<[ОН-]; [Н+]<10 -7, [ОН]<10 -7 г-ион/л.
 Например, если концентрация ионов водорода в растворе равна 10 -3 г-ион/л, реакция среды кислая, величину [ОН-] в таком растворе можно рассчитать из уравнения ионного произведения воды: [Н+][ОН-] = 10 -14 г-ион/л, следовательно, [ОН-] =10 -14/[Н+] = 10 -14/10 -3=10 -11 г-ион/л.
Например, если концентрация ионов водорода в растворе равна 10 -3 г-ион/л, реакция среды кислая, величину [ОН-] в таком растворе можно рассчитать из уравнения ионного произведения воды: [Н+][ОН-] = 10 -14 г-ион/л, следовательно, [ОН-] =10 -14/[Н+] = 10 -14/10 -3=10 -11 г-ион/л.
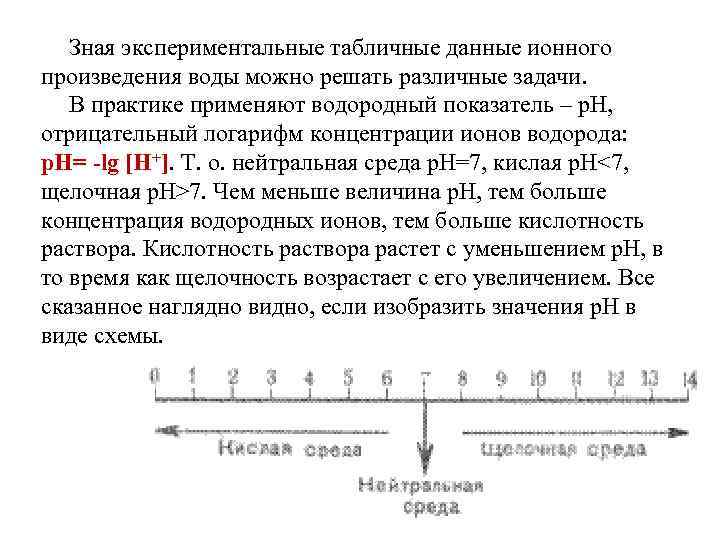 Зная экспериментальные табличные данные ионного произведения воды можно решать различные задачи. В практике применяют водородный показатель – р. Н, отрицательный логарифм концентрации ионов водорода: р. Н= -lg [Н+]. Т. о. нейтральная среда р. Н=7, кислая р. Н<7, щелочная р. Н>7. Чем меньше величина р. Н, тем больше концентрация водородных ионов, тем больше кислотность раствора. Кислотность раствора растет с уменьшением р. Н, в то время как щелочность возрастает с его увеличением. Все сказанное наглядно видно, если изобразить значения р. Н в виде схемы.
Зная экспериментальные табличные данные ионного произведения воды можно решать различные задачи. В практике применяют водородный показатель – р. Н, отрицательный логарифм концентрации ионов водорода: р. Н= -lg [Н+]. Т. о. нейтральная среда р. Н=7, кислая р. Н<7, щелочная р. Н>7. Чем меньше величина р. Н, тем больше концентрация водородных ионов, тем больше кислотность раствора. Кислотность раствора растет с уменьшением р. Н, в то время как щелочность возрастает с его увеличением. Все сказанное наглядно видно, если изобразить значения р. Н в виде схемы.
![Наряду с водородным показателем нередко применяют гидроксильный показатель р. ОН= -lg [ОН-]. Если уравнение Наряду с водородным показателем нередко применяют гидроксильный показатель р. ОН= -lg [ОН-]. Если уравнение](https://present5.com/presentation/161171421_271237115/image-8.jpg) Наряду с водородным показателем нередко применяют гидроксильный показатель р. ОН= -lg [ОН-]. Если уравнение ионного произведения воды [Н+][ОН-] = 10 -14 прологарифмировать, а затем поменять у логарифмов знаки на обратные, то получим р. Н + р. ОН= р. КН 2 О=14, где р. КН 2 О= --lg. КН 2 О=-lg 10 -14=14. Отсюда следует, что в любом водном растворе действительно соотношение р. Н= р. КН 2 О – р. ОН = 14 – р. ОН (при 250 С)
Наряду с водородным показателем нередко применяют гидроксильный показатель р. ОН= -lg [ОН-]. Если уравнение ионного произведения воды [Н+][ОН-] = 10 -14 прологарифмировать, а затем поменять у логарифмов знаки на обратные, то получим р. Н + р. ОН= р. КН 2 О=14, где р. КН 2 О= --lg. КН 2 О=-lg 10 -14=14. Отсюда следует, что в любом водном растворе действительно соотношение р. Н= р. КН 2 О – р. ОН = 14 – р. ОН (при 250 С)
 Используя эти уравнения можно решать различные задачи: вычислять р. Н растворов кислот и оснований, вычислять концентрацию ионов Н+ и ОН- по известным значениям р. Н и обратно. При расчете водородного показателя среды водных растворов сильных кислот и оснований следует учитывать необратимость процесса их электролитической диссоциации (б=1). Концентрация ионов Н+ в растворах одноосновных сильных кислот и концентрация ионов ОН- в растворах одноосновных щелочей численно равна молярности растворов. Например, концентрация ионов Н+ в 0, 001 М растворе НС 1 равна 0, 001 моль/л, а концентрация ОН- в 0, 01 М растворе Nа. ОН равна 0, 01 моль/л.
Используя эти уравнения можно решать различные задачи: вычислять р. Н растворов кислот и оснований, вычислять концентрацию ионов Н+ и ОН- по известным значениям р. Н и обратно. При расчете водородного показателя среды водных растворов сильных кислот и оснований следует учитывать необратимость процесса их электролитической диссоциации (б=1). Концентрация ионов Н+ в растворах одноосновных сильных кислот и концентрация ионов ОН- в растворах одноосновных щелочей численно равна молярности растворов. Например, концентрация ионов Н+ в 0, 001 М растворе НС 1 равна 0, 001 моль/л, а концентрация ОН- в 0, 01 М растворе Nа. ОН равна 0, 01 моль/л.
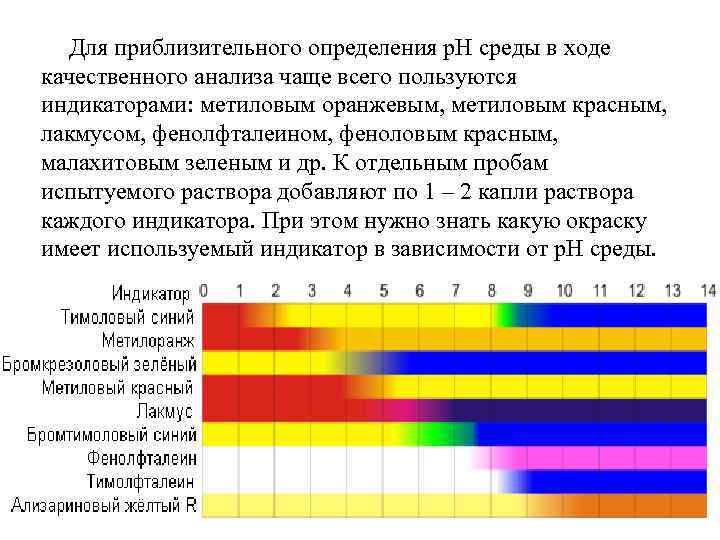 Для приблизительного определения р. Н среды в ходе качественного анализа чаще всего пользуются индикаторами: метиловым оранжевым, метиловым красным, лакмусом, фенолфталеином, феноловым красным, малахитовым зеленым и др. К отдельным пробам испытуемого раствора добавляют по 1 – 2 капли раствора каждого индикатора. При этом нужно знать какую окраску имеет используемый индикатор в зависимости от р. Н среды.
Для приблизительного определения р. Н среды в ходе качественного анализа чаще всего пользуются индикаторами: метиловым оранжевым, метиловым красным, лакмусом, фенолфталеином, феноловым красным, малахитовым зеленым и др. К отдельным пробам испытуемого раствора добавляют по 1 – 2 капли раствора каждого индикатора. При этом нужно знать какую окраску имеет используемый индикатор в зависимости от р. Н среды.
 Буферными системами (буферами) называют растворы, обладающие свойством достаточно стойко сохранять постоянство концентрации ионов водорода как при добавлении кислот или щелочей, так и при разведении. Классификация буферных систем Кислотные – состоят из слабой кислоты и соли этой кислоты, образованной сильным основанием. Ацетатный буфер: Гидрокарбонатный буфер: Аммиачный буфер: Основные – состоят из слабого основания и соли этого основания, образованной сильной кислотой. Фосфатный буфер: Солевые – состоят из роль слабой к-ты гидрофосфата и дигидрофосфата Na или К. СН 3 СООН СН 3 СООNa Н 2 СО 3 Na. HCO 3 NH 4 OH NH 4 Cl Na. H 2 PO 4 Na 2 HPO 4
Буферными системами (буферами) называют растворы, обладающие свойством достаточно стойко сохранять постоянство концентрации ионов водорода как при добавлении кислот или щелочей, так и при разведении. Классификация буферных систем Кислотные – состоят из слабой кислоты и соли этой кислоты, образованной сильным основанием. Ацетатный буфер: Гидрокарбонатный буфер: Аммиачный буфер: Основные – состоят из слабого основания и соли этого основания, образованной сильной кислотой. Фосфатный буфер: Солевые – состоят из роль слабой к-ты гидрофосфата и дигидрофосфата Na или К. СН 3 СООН СН 3 СООNa Н 2 СО 3 Na. HCO 3 NH 4 OH NH 4 Cl Na. H 2 PO 4 Na 2 HPO 4
 Контрольные вопросы 1. Чему равна концентрация ионов водорода и гидроксид-ионов в воде при 220 С? 2. Чему равно ионное произведение воды? 3. Чему равна концентрация ионов водорода и ионов гидроксида в растворе сильных одноосновных кислот и оснований? 4. Дайте определение понятия «буферный раствор» . Д/З конспект, стр. 49, п. 3. 1. 1.
Контрольные вопросы 1. Чему равна концентрация ионов водорода и гидроксид-ионов в воде при 220 С? 2. Чему равно ионное произведение воды? 3. Чему равна концентрация ионов водорода и ионов гидроксида в растворе сильных одноосновных кислот и оснований? 4. Дайте определение понятия «буферный раствор» . Д/З конспект, стр. 49, п. 3. 1. 1.


