 Электролитическая диссоциация.
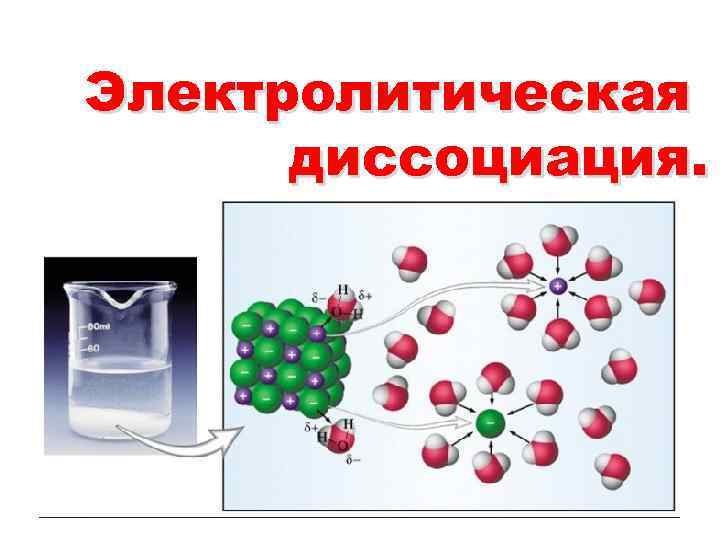
Электролитическая диссоциация.
 Вода Сухой Na. Cl Раствор Na. Cl Прибор для определения электропроводности Электропроводность веществ. wmv
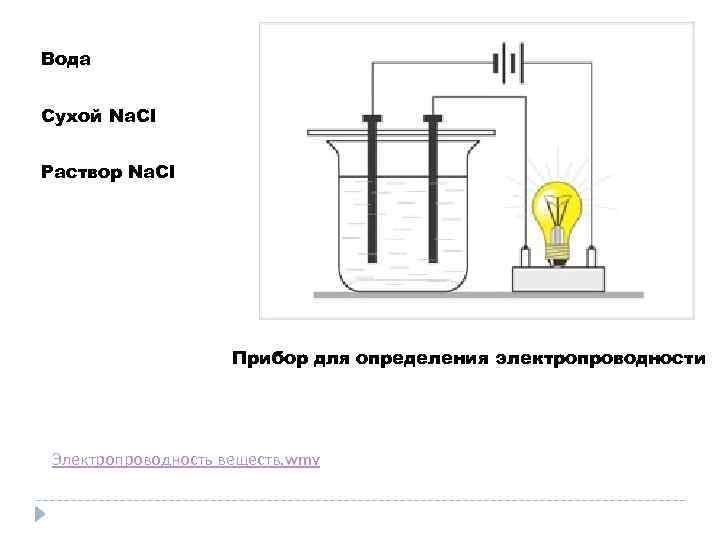
Вода Сухой Na. Cl Раствор Na. Cl Прибор для определения электропроводности Электропроводность веществ. wmv
 Электролитическая диссоциация - это процесс распада электролита на ионы при растворении его в воде или расплавлении. Диссоциация хлорида натрия: Na. Cl = Na⁺ + Cl⁻
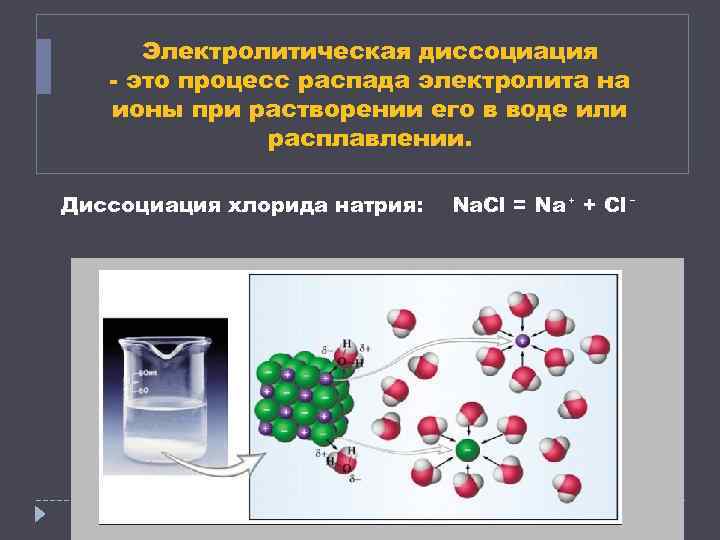
Электролитическая диссоциация - это процесс распада электролита на ионы при растворении его в воде или расплавлении. Диссоциация хлорида натрия: Na. Cl = Na⁺ + Cl⁻
 Электролиты – это вещества, водные растворы или расплавы которых проводят электрический ток.
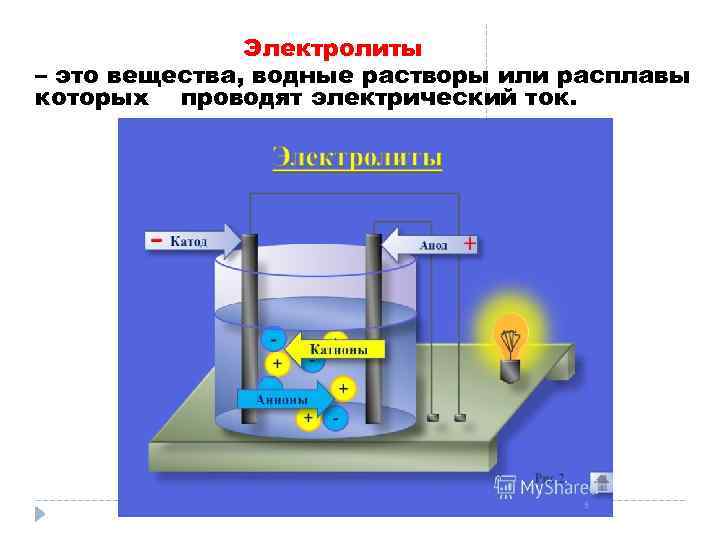
Электролиты – это вещества, водные растворы или расплавы которых проводят электрический ток.
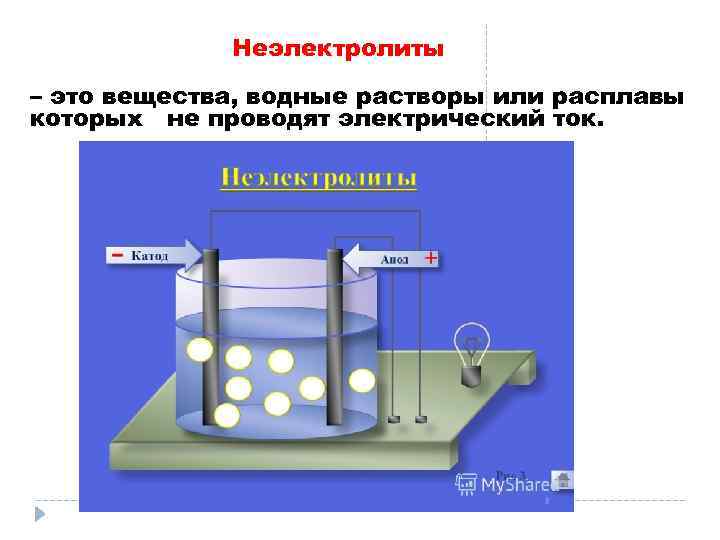 Неэлектролиты – это вещества, водные растворы или расплавы которых не проводят электрический ток.
Неэлектролиты – это вещества, водные растворы или расплавы которых не проводят электрический ток.
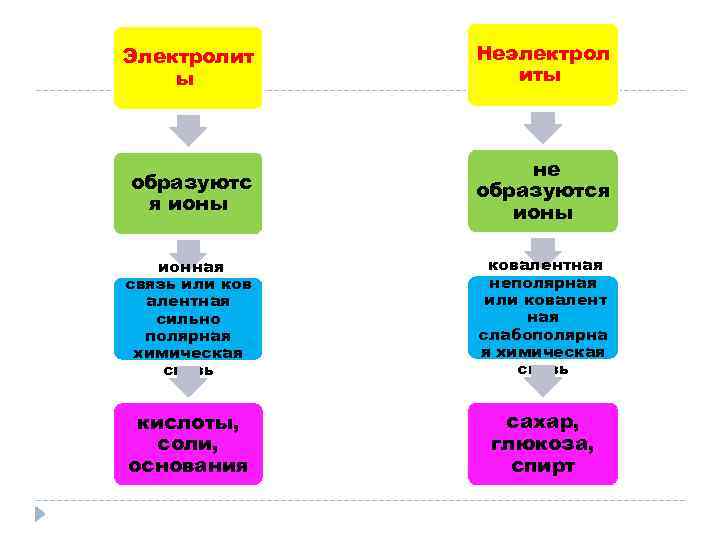 Электролит ы Неэлектрол иты образуютс я ионы не образуются ионы ионная связь или ков алентная сильно полярная химическая связь ковалентная неполярная или ковалент ная слабополярна я химическая связь кислоты, соли, основания сахар, глюкоза, спирт
Электролит ы Неэлектрол иты образуютс я ионы не образуются ионы ионная связь или ков алентная сильно полярная химическая связь ковалентная неполярная или ковалент ная слабополярна я химическая связь кислоты, соли, основания сахар, глюкоза, спирт
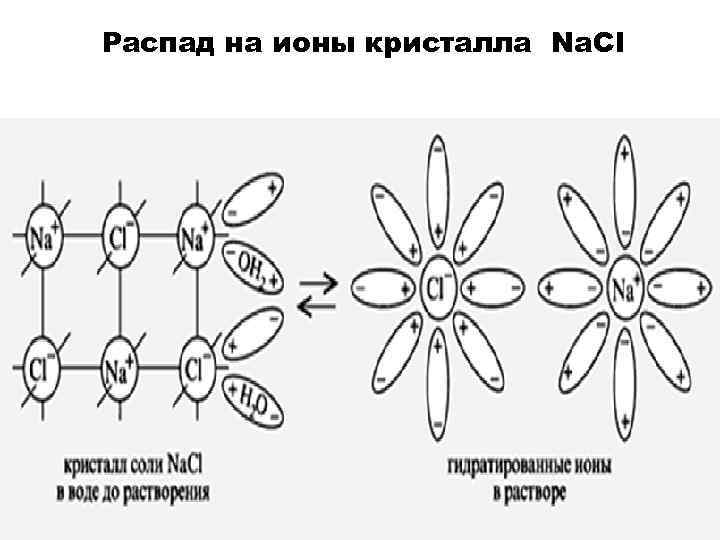 Распад на ионы кристалла Na. Cl
Распад на ионы кристалла Na. Cl
 Диссоциация кислот Кислотами называются электролиты, при диссоциации которых в качестве катионов образуются только катионы водорода (H+). HCl ↔ H+ + Cl HNO 3 ↔ H+ + NO 3 H 2 SO 4 ↔ 2 Н+ + SО 2 -4 Н 3 РО 4 ↔ 3 Н+ + PОЗ-4
Диссоциация кислот Кислотами называются электролиты, при диссоциации которых в качестве катионов образуются только катионы водорода (H+). HCl ↔ H+ + Cl HNO 3 ↔ H+ + NO 3 H 2 SO 4 ↔ 2 Н+ + SО 2 -4 Н 3 РО 4 ↔ 3 Н+ + PОЗ-4
 Диссоциация оснований (щелочей) Основаниями называются электролиты, при диссоциации которых в качестве анионов образуются только гидроксидионы (OH -). KOH ↔ K+ + OH NH 4 OH ↔ NH 4+ + OH Ba(ОН)2 ↔ Ba 2++ 2 OH
Диссоциация оснований (щелочей) Основаниями называются электролиты, при диссоциации которых в качестве анионов образуются только гидроксидионы (OH -). KOH ↔ K+ + OH NH 4 OH ↔ NH 4+ + OH Ba(ОН)2 ↔ Ba 2++ 2 OH
 Диссоциация солей Солями называются электролиты, при диссоциации которых образуются катионы металлов, а также катион аммония (NH 4+) и анионы кислотных остатков. (NH 4)2 SO 4 ↔ 2 NH₄++ SO₄2 -; Na 3 PO 4 ↔ 3 Na+ + PO₄3 -
Диссоциация солей Солями называются электролиты, при диссоциации которых образуются катионы металлов, а также катион аммония (NH 4+) и анионы кислотных остатков. (NH 4)2 SO 4 ↔ 2 NH₄++ SO₄2 -; Na 3 PO 4 ↔ 3 Na+ + PO₄3 -
 ЗАДАНИЕ № 1. Используя таблицу растворимости солей, кислот, оснований напишите уравнения диссоциации следующих веществ: HF, Mg(OH)2, Ca. Cl 2, Zn(NO 3)2, Ba(OH)2, K 2 SO 4, H 2 Si. O 3, Fe. I 3, Ni. Cl 2, H 3 PO 4
ЗАДАНИЕ № 1. Используя таблицу растворимости солей, кислот, оснований напишите уравнения диссоциации следующих веществ: HF, Mg(OH)2, Ca. Cl 2, Zn(NO 3)2, Ba(OH)2, K 2 SO 4, H 2 Si. O 3, Fe. I 3, Ni. Cl 2, H 3 PO 4