Электролитическая диссоциация.ppt
- Количество слайдов: 14

Электролитическая диссоциация. Реакции ионного обмена Тесты
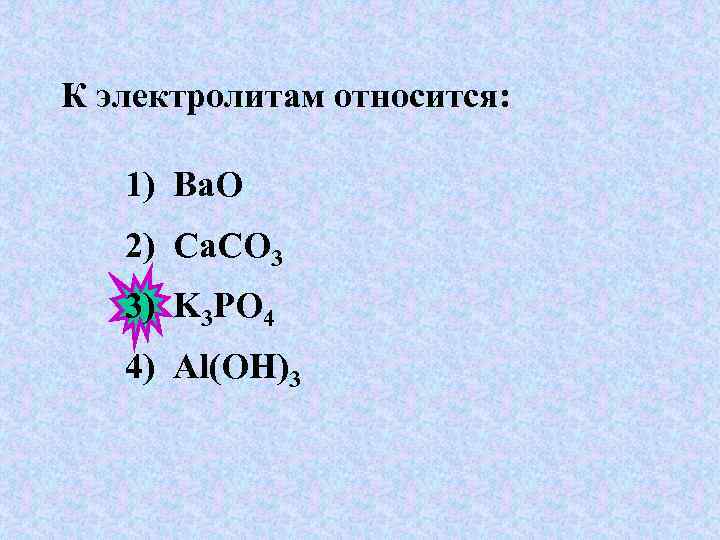
К электролитам относится: 1) Ba. O 2) Сa. СO 3 3) K 3 PO 4 4) Al(OH)3

К электролитам не относится: 1) Ba. Cl 2 2) Zn. SO 4 3) H 2 SO 4 4) CO 2
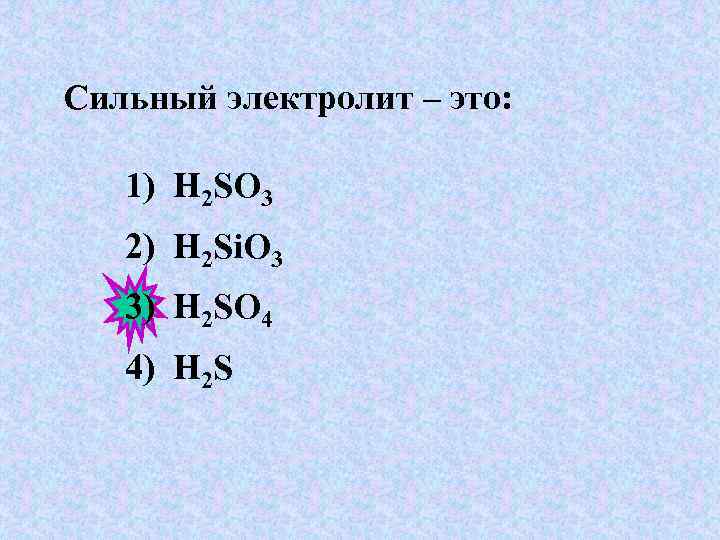
Сильный электролит – это: 1) H 2 SO 3 2) H 2 Si. O 3 3) H 2 SO 4 4) H 2 S

Слабым электролитом является раствор: 1) HI 2) HBr 3) HCl 4) HF

Вещество, при диссоциации которого образуются силикат-ионы, – это: 1) K 2 Si. O 3 2) Si. O 2 3) H 2 Si. O 3 4) Ca. Si. O 3

Вещество, при диссоциации которого образуются катионы цинка, – это: 1) Zn. SO 3 2) Zn. O 3) Zn(OH)2 4) Zn(NO 3)2

При полной диссоциации 1 моль Сa(NO 3)2 общее число моль образующихся ионов равно: 1) 2 2) 3 3) 4 4) 5

При полной диссоциации 1 моль ортофосфата натрия образуется: 1) 2 моль ионов 2) 3 моль ионов 3) 4 моль ионов 4) 5 моль ионов

При полной диссоциации 1 моль Fe 2(SO 4)3 общее число моль образующихся ионов равно: 1) 2 2) 3 3) 4 4) 5

В сокращенном ионном уравнении реакции серной кислоты с гидроксидом натрия сумма коэффициентов равна: 1) 6 2) 5 3) 3 4) 4

Сокращенное ионное уравнение реакции Fe 3+ + 3 OH– = Fe(OH)3 соответствует взаимодействию: 1) железа с гидроксидом натрия 2) железа с водой 3) хлорида железа(III) с гидроксидом меди(II) 4) хлорида железа(III) с гидроксидом натрия

Установите соответствие между сокращенными ионными уравнениями реакций обмена и веществами, вступающими в реакцию. 1) Ca 2+ + CO 32– =Ca. CO 3 А) H 2 SO 4 и Ba. Cl 2 2) H+ + OH– = H 2 O Б) Na 2 CO 3 и Ca. Cl 2 3) Ba 2+ + SO 42– = Ba. SO 4 В) Na. OH и H 2 Si. O 3 Г) Ba(OH)2 и HCl

Установите соответствие между классами исходных веществ, вступающих в реакции обмена, и сокращенными ионными уравнениями этих реакций. 1) Кислота и металл А) OH- + H+ = H 2 O 2) Кислота и основный Б) Zn + 2 H+ = Zn 2+ + H 2 оксид 3) Кислота и основание 4) Кислота и соль B) 2 Na+ + SO 42– = Na 2 SO 4 Г) Ag+ + Cl– = Ag. Cl Д) Сu. O + 2 H+ = Cu 2+ + H 2 O
Электролитическая диссоциация.ppt