15_Электролитическая диссоциация.ppt
- Количество слайдов: 17

Электролитическая диссоциация Лекция 15 по курсу «Общая химия»

Электролиты и неэлектролиты Соли Кислоты Щелочи Простые веществанеметаллы Органические водорастворимые вещества (кроме кислот, аминов, солей)
Две теории растворов «Электролиты в растворах состоят частично из диссоциированных молекул, число которых растет при разбавлении раствора; образующиеся при диссоциации молекул ионы определяют специфические физические и химические свойства растворов электролитов; в бесконечно разбавленных растворах молекулы существуют только в виде ионов; вещество в растворе тем более активно, чем больше оно диссоциировано на ионы» . С. Аррениус «Растворы суть химические соединения, определяемые силами, действующими между растворителем и растворенным веществом» Д. И. Менделеев
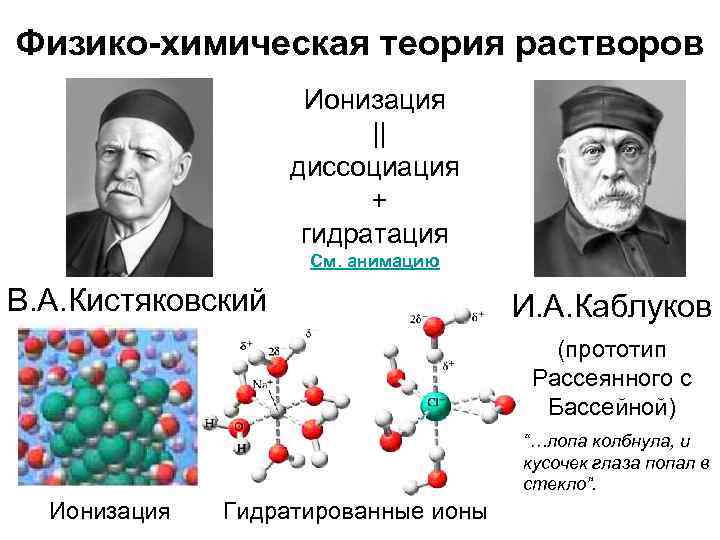
Физико-химическая теория растворов Ионизация || диссоциация + гидратация См. анимацию В. А. Кистяковский И. А. Каблуков (прототип Рассеянного с Бассейной) “…лопа колбнула, и кусочек глаза попал в стекло”. Ионизация Гидратированные ионы
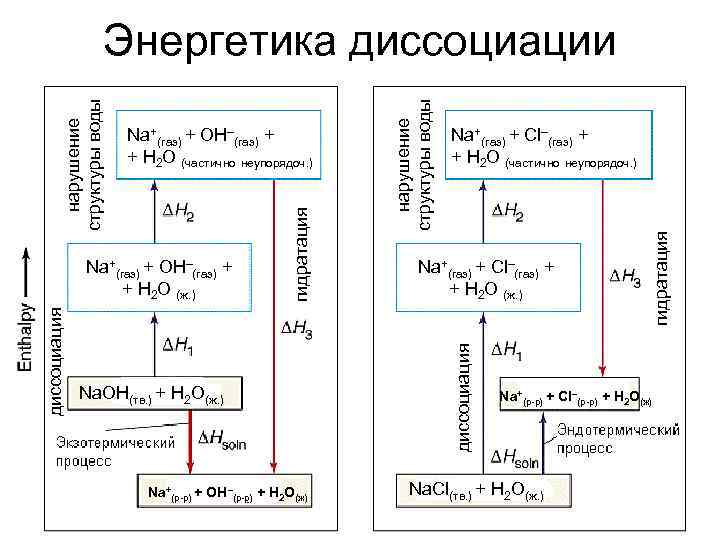
Na. OH(тв. ) + H 2 O(ж. ) Na+(р-р) + OH–(р-р) + H 2 O(ж) Na+(газ) + Cl–(газ) + + H 2 O (ж. ) гидратация Na+(газ) + Cl–(газ) + + H 2 O (частично неупорядоч. ) диссоциация Na+(газ) + OH–(газ) + + H 2 O (ж. ) нарушение структуры воды Na+(газ) + OH–(газ) + + H 2 O (частично неупорядоч. ) гидратация нарушение структуры воды Энергетика диссоциации Na+(р-р) + Cl–(р-р) + H 2 O(ж) Na. Cl(тв. ) + H 2 O(ж. )

Кислоты, основания, соли Кислота: катионы при диссоциации – только H+ Основание: анионы при диссоциации – только OH– Соль: любые другие катионы и анионы H 2 SO 4 = 2 H+ + SO 42– – кислота, НО! KHSO 4 = K+ + H+ +SO 42– – соль Ca(OH)2 = Ca 2+ + 2 OH– – основание НО! Ca(OH)Cl = Ca 2+ + OH– + Cl– – соль
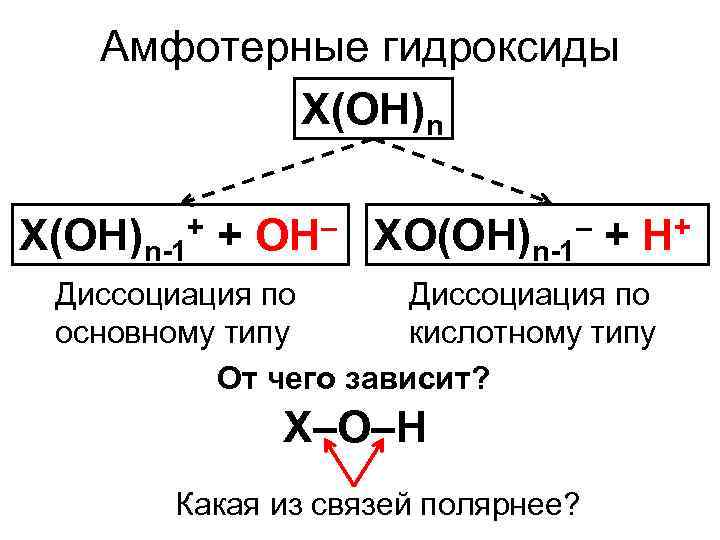
Амфотерные гидроксиды X(OH)n-1+ + OH– XO(OH)n-1– + H+ Диссоциация по основному типу кислотному типу От чего зависит? X–O–H Какая из связей полярнее?

Сильные электролиты Диссоциируют полностью или почти полностью Класс Примеры Соли Основания Практически все Неорганические: гидроксиды металлов групп IA и IIA (кроме Be(OH)2, Mg(OH)2) Органические: четвертичные аммониевые основания R 4 N+OH–, гуанидин (NH 2)2 C=NH Неорганические: HCl. O 4, HCl. O 3, HCl, HBr, HI, HNO 3, HMn. O 4, H 2 SO 4, H 2 Cr 2 O 7 (редкие примеры сильных двухосновных кислот!), все комплексные кислоты ионного строения (HBF 4, HSb. F 6, HAu. Cl 4 и т. д. ) Органические: сульфокислоты RSO 3 H, алкилсульфаты ROSO 3 H Кислоты
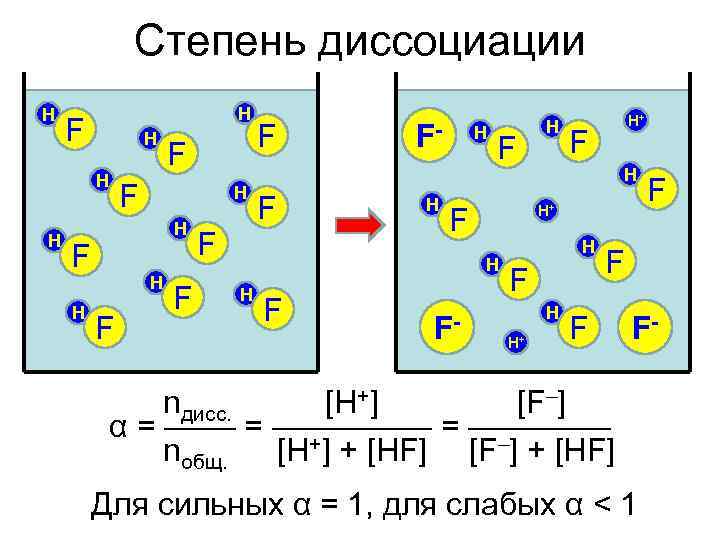
Степень диссоциации H H F H F F FH H F F- H+ F H H+ H H F H H+ F F- nдисс. [H+] [F–] α = ––––––––– = –––– nобщ. [H+] + [HF] [F–] + [HF] Для сильных α = 1, для слабых α < 1

От чего зависит α? 1. Природа растворителя (полярность и др. ) Н 2 О > C 2 H 5 OH > (C 2 H 5)O > C 6 H 6 HCl в безводном эфире не реагирует с Na! 2. Природа электролита Ионная связь – сильные электролиты Ковалентная полярная – сильные и слабые Ковалентная неполярная – неэлектролиты 3. Концентрация Для слабых электролитов – С↑ α↓ 4. Присутствие одноименных ионов α↓ – принцип Ле Шателье 5. Температура Обычно ΔНдисс > 0 с ростом температуры α↑

Закон разбавления Оствальда Только для очень разбавленных растворов слабых электролитов! Kt. An Kt+ + An– α 1/ CKt. An С 0 α 1 К. В. Оствальд HCl – при разбавлении в 10 раз [H+] падает в 10 раз CH 3 COOH – при разбавлении в 10 раз [H+] падает только в 3, 1 раза!

Константа диссоциации HAn H+ + An– – константа диссоциации Для многоосновных кислот – ступенчатая диссоциация H 3 PO 4 H+ + H 2 PO 4– H+ + HPO 42– H+ + PO 43– Чем дальше, тем слабее!

Вывод закона разбавления HAn H+ + An– С 0 СHAn Сравн СHAn – x 0 x Т. к. , то:

Диссоциация воды H 2 O + H + – OH НО! Ионное произведение воды Постоянно для всех разбавленных растворов!
![Водородный показатель (p. H) p. H = –lg[H+] Водородный показатель (p. H) p. H = –lg[H+]](https://present5.com/presentation/3/155114067_41106427.pdf-img/155114067_41106427.pdf-15.jpg)
Водородный показатель (p. H) p. H = –lg[H+]

Значения р. Н некоторых растворов Почему не 13. 0?
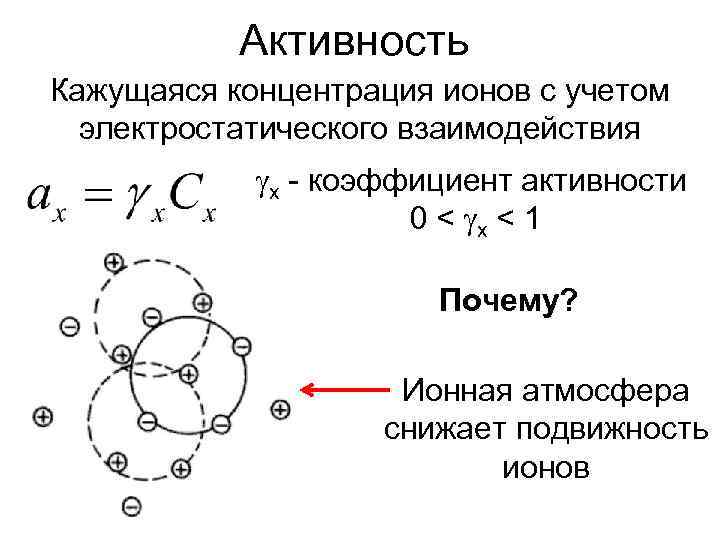
Активность Кажущаяся концентрация ионов с учетом электростатического взаимодействия x - коэффициент активности 0 < x < 1 Почему? Ионная атмосфера снижает подвижность ионов
15_Электролитическая диссоциация.ppt