 Электролитическая диссоциация(ЭД). Теория электролитической диссоциации (ТЭД).
Электролитическая диссоциация(ЭД). Теория электролитической диссоциации (ТЭД).
 Вещества Электропроводность Электролиты Неэлектролиты вещества, растворы и расплавы которых проводят электрический ток вещества, растворы и расплавы которых не проводят электрический ток Ионная или ковалентная сильно полярная связь Ковалентная неполярная или мало полярная связь
Вещества Электропроводность Электролиты Неэлектролиты вещества, растворы и расплавы которых проводят электрический ток вещества, растворы и расплавы которых не проводят электрический ток Ионная или ковалентная сильно полярная связь Ковалентная неполярная или мало полярная связь
 Основные положения ТЭД: 1) При растворении в воде эл-ты диссоциируют (распадаются) на ⊕ и ⊖ ионы. Процесс распада эл-та на ионы называют электролитической диссоциацией (ЭД).
Основные положения ТЭД: 1) При растворении в воде эл-ты диссоциируют (распадаются) на ⊕ и ⊖ ионы. Процесс распада эл-та на ионы называют электролитической диссоциацией (ЭД).
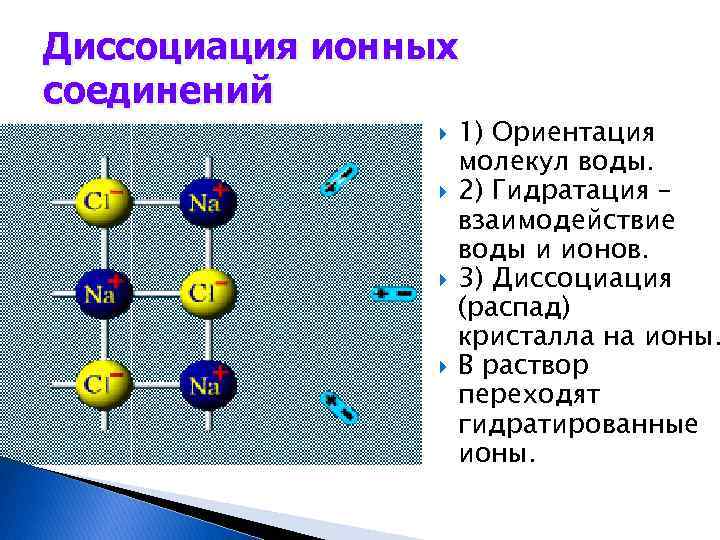 Диссоциация ионных соединений 1) Ориентация молекул воды. 2) Гидратация – взаимодействие воды и ионов. 3) Диссоциация (распад) кристалла на ионы. В раствор переходят гидратированные ионы.
Диссоциация ионных соединений 1) Ориентация молекул воды. 2) Гидратация – взаимодействие воды и ионов. 3) Диссоциация (распад) кристалла на ионы. В раствор переходят гидратированные ионы.
 Диссоциация соединений с ковалентной полярной связью: 1) Ориентация молекул воды вокруг полюсов эл-та. 2) Гидратация – взаимодействие воды молекулы эл-та. 3) Ионизация молекулы эл-та. 4) Диссоциация (распад) молекулы элта на ионы. В раствор переходят гидратированные ионы.
Диссоциация соединений с ковалентной полярной связью: 1) Ориентация молекул воды вокруг полюсов эл-та. 2) Гидратация – взаимодействие воды молекулы эл-та. 3) Ионизация молекулы эл-та. 4) Диссоциация (распад) молекулы элта на ионы. В раствор переходят гидратированные ионы.
 2. Причиной дис-ции эл-та в водном р-ре является его гидратация, т. е. взаимодействие эл-та с молекулами воды и разрыв химической связи в нем. ⇒ по наличию водной оболочки ионы делят на гидратированные и негидратированные. 3. Под действием электрического тока ⊕ заряженные ионы движутся к ⊖ заряженному полюсу – катоду, поэтому называют катионами, ⊖ заряженные ионы движутся к ⊕ заряженному полюсу – аноду, поэтому называются анионами.
2. Причиной дис-ции эл-та в водном р-ре является его гидратация, т. е. взаимодействие эл-та с молекулами воды и разрыв химической связи в нем. ⇒ по наличию водной оболочки ионы делят на гидратированные и негидратированные. 3. Под действием электрического тока ⊕ заряженные ионы движутся к ⊖ заряженному полюсу – катоду, поэтому называют катионами, ⊖ заряженные ионы движутся к ⊕ заряженному полюсу – аноду, поэтому называются анионами.
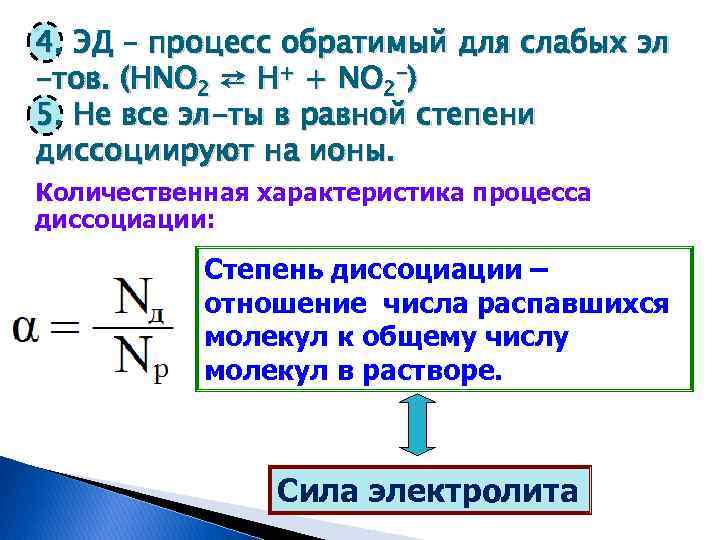 4. ЭД – процесс обратимый для слабых эл -тов. (HNO 2 ⇄ H+ + NO 2 -) 5. Не все эл-ты в равной степени диссоциируют на ионы. Количественная характеристика процесса диссоциации: Степень диссоциации – отношение числа распавшихся молекул к общему числу молекул в растворе. Сила электролита
4. ЭД – процесс обратимый для слабых эл -тов. (HNO 2 ⇄ H+ + NO 2 -) 5. Не все эл-ты в равной степени диссоциируют на ионы. Количественная характеристика процесса диссоциации: Степень диссоциации – отношение числа распавшихся молекул к общему числу молекул в растворе. Сила электролита
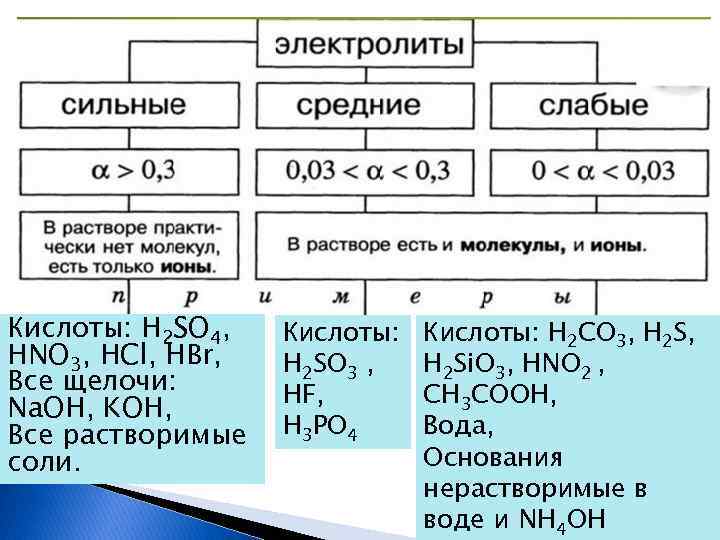 Кислоты: H 2 SO 4, HNO 3, HCl, HBr, Все щелочи: Na. OH, KOH, Все растворимые соли. Кислоты: H 2 SO 3 , HF, H 3 PO 4 Кислоты: H 2 CO 3, H 2 Si. O 3, HNO 2 , CH 3 COOH, Вода, Основания нерастворимые в воде и NH 4 OH
Кислоты: H 2 SO 4, HNO 3, HCl, HBr, Все щелочи: Na. OH, KOH, Все растворимые соли. Кислоты: H 2 SO 3 , HF, H 3 PO 4 Кислоты: H 2 CO 3, H 2 Si. O 3, HNO 2 , CH 3 COOH, Вода, Основания нерастворимые в воде и NH 4 OH
 6. Химические св-ва р-ров эл-тов определяются св-ами тех ионов, которые образуются при дис-ции: ∗ Кислотами называют эл-ты, которые при дис-ции образуют катионы водорода и анионы кислотного остатка: HCl → H+ + Cl Многоосновные кислоты диссоциируют ступенчато: I H 3 PO 4 ⇄ H+ + H 2 PO 4 II H 2 PO 4 - ⇄ H+ + HPO 42 По второй ступени дис-ция происходит слабее, по третьей при обычных условиях не происходит.
6. Химические св-ва р-ров эл-тов определяются св-ами тех ионов, которые образуются при дис-ции: ∗ Кислотами называют эл-ты, которые при дис-ции образуют катионы водорода и анионы кислотного остатка: HCl → H+ + Cl Многоосновные кислоты диссоциируют ступенчато: I H 3 PO 4 ⇄ H+ + H 2 PO 4 II H 2 PO 4 - ⇄ H+ + HPO 42 По второй ступени дис-ция происходит слабее, по третьей при обычных условиях не происходит.
 ∗ Основаниями называют эл-ты, которые при дис-ции образуют катионы металла и гидроксид-анионы: Na. OH → Na+ + OHCa(OH)2 → Ca+ + 2 OH∗ Солями называют эл-ты, которые при дис-ции образуют катионы металла (или аммония NH 4+) и анионы кислотного остатка. В отличие от кислот средние соли диссоциируют полностью и не ступенчато: (NH 4)3 PO 4 → 3(NH 4)+ + PO 43 Na. Cl → Na+ + Cl-
∗ Основаниями называют эл-ты, которые при дис-ции образуют катионы металла и гидроксид-анионы: Na. OH → Na+ + OHCa(OH)2 → Ca+ + 2 OH∗ Солями называют эл-ты, которые при дис-ции образуют катионы металла (или аммония NH 4+) и анионы кислотного остатка. В отличие от кислот средние соли диссоциируют полностью и не ступенчато: (NH 4)3 PO 4 → 3(NH 4)+ + PO 43 Na. Cl → Na+ + Cl-
 Домашнее задание: § 35 -36, № 4, 5, с. 203
Домашнее задание: § 35 -36, № 4, 5, с. 203