bacfde03a593d1fcaf85e7955a1614c2.ppt
- Количество слайдов: 36

Электрофорез и Блоттинг Наталья Володина Молекулярная Биология 12. 02. 2011

Принципы • Нуклеиновые кислоты (ДНК, РНК) двигаются от отрицательного к положительному полюсу в процессе электрофореза в геле • Скорость передвижения зависит от размера молекулы

• Агарозный и акриламидный гель полимер, Акриламид – это синтетический используемый для разделения фрагметов ДНК размером в несколько сотен пар оснований – Вначале его полимеризуют добавляяя специальные компоненты – Получается прозрачный гель, используемый обычно в вертикальном аппарате • Агароза – это полисахарид, используемый для разделения молекул ДНК и РНК размером от нескольких сотен до десятков тысяч пар оснований – Гель создается нагреванием до кипения смеси агарозы и воды до ее растворения и остыванием геля в специальной форме – Получается полупрозрачный гель, обычно используемый в горизонтальном аппарате

Рестрикционные ферменты • Происхождение и природная функция – Некоторые ферменты используются бактериями для защиты от чужеродной (предполагается, что вирусной) ДНК – Бактериальная ДНК может быть метилирована в определенных местах • Рестриктазы не могут порезать последовательность, которая была метилирована • А вирусная ДНК неметелирована и таким образом уничтожается рестриктазами

• Рестриктазы – Обычно бактериального происхождения Ферменты • Но могут происходить от низших эукариот (простейших), и даже вирусов и. т. п. – Режут ДНК в определенных коротких палиндромных последовательностях • Длиной 2 и больше нуклеотидов • До 30 нуклеотидов • В результате получается 5’ фосфат и 3’ гидроксильная группа • Могут получиться одноцепочечные концы или двухцепочечные (затупленные концы) • Места разреза могут быть комплементарно соединены вместе и далее склеены ковалентно ДНК лигазой

• Средний размер фрагмента зависит от количества нуклеотидов в узнаваемой последовательности Размер узнаваемой последовательнос ти 4 5 6 8 Средний размер фрагмента 256 1024 4096 65536
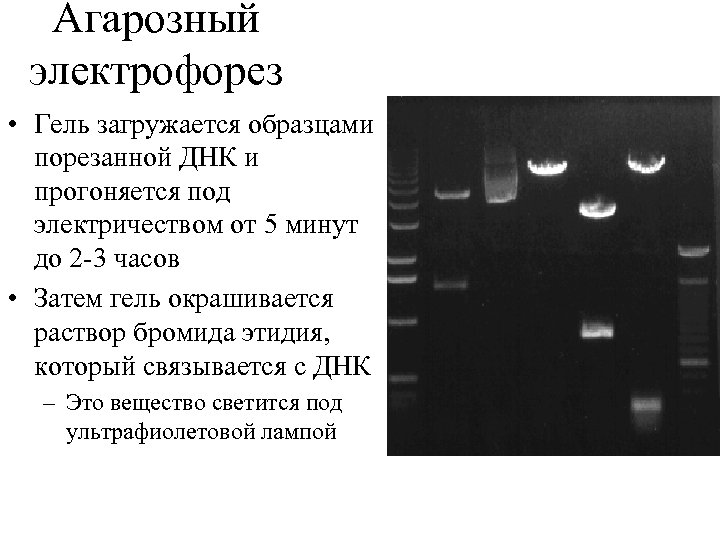
Агарозный электрофорез • Гель загружается образцами порезанной ДНК и прогоняется под электричеством от 5 минут до 2 -3 часов • Затем гель окрашивается раствор бромида этидия, который связывается с ДНК – Это вещество светится под ультрафиолетовой лампой
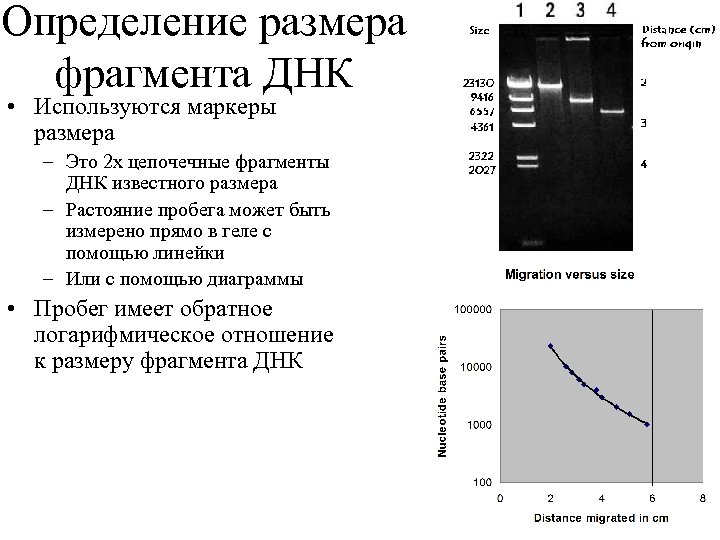
Определение размера фрагмента ДНК • Используются маркеры размера – Это 2 х цепочечные фрагменты ДНК известного размера – Растояние пробега может быть измерено прямо в геле с помощью линейки – Или с помощью диаграммы • Пробег имеет обратное логарифмическое отношение к размеру фрагмента ДНК

Разрезание человеческой хромосомной ДНК • Если используется фермент, узнающий последовательность в 6 п. о. – получается 750 000 фрагментов • На геле получается размазанная дорожка – Средний размер фрагментов от или больше 4096 п. о. – Повторяющиеся последовательности могут не содержать данную последовательность – Если последовательность узнавания находится внутри повторяющихся последовательностей, то появиться отдельный бэнд – полоска на геле в размазанной дорожке
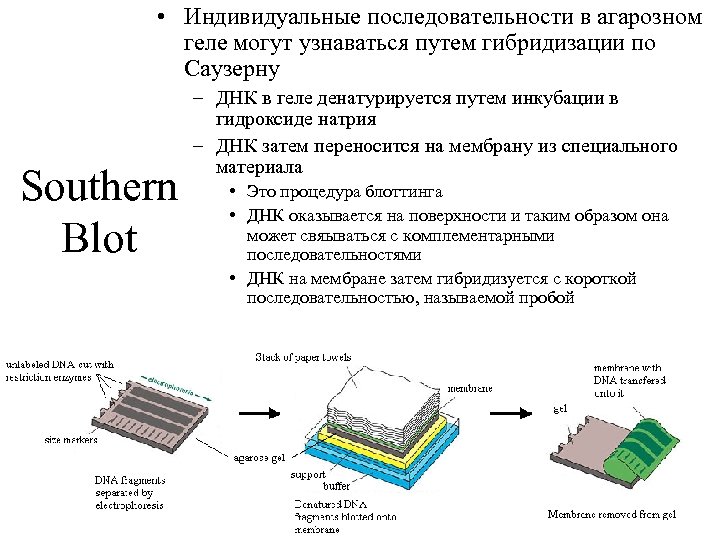
• Индивидуальные последовательности в агарозном геле могут узнаваться путем гибридизации по Саузерну Southern Blot – ДНК в геле денатурируется путем инкубации в гидроксиде натрия – ДНК затем переносится на мембрану из специального материала • Это процедура блоттинга • ДНК оказывается на поверхности и таким образом она может свяываться с комплементарными последовательностями • ДНК на мембране затем гибридизуется с короткой последовательностью, называемой пробой

Проба • Олиго или поли-нуклеотид, представляющий собой известную последовательность – Обычно комплементарна какому-то гену – Либо одноцепочечная с самого начала или двухцепочечная и денатурирована перед употреблением – Помечена радиоактивным изотопом фосфора или флюоресцентной меткой
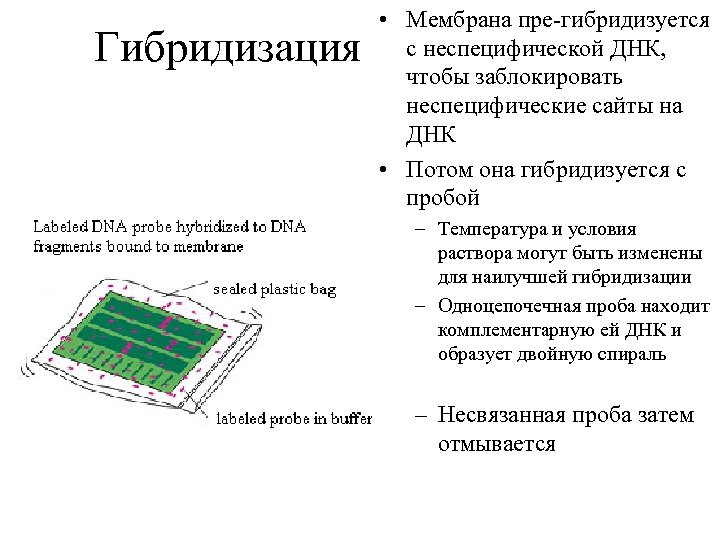
Гибридизация • Мембрана пре-гибридизуется с неспецифической ДНК, чтобы заблокировать неспецифические сайты на ДНК • Потом она гибридизуется с пробой – Температура и условия раствора могут быть изменены для наилучшей гибридизации – Одноцепочечная проба находит комплементарную ей ДНК и образует двойную спираль – Несвязанная проба затем отмывается

Экспозиция на специальную фото пленку в случае радиоактивной метки – Радиоактивная проба засвечивает пленку так как она выделяет электроны – бета частицы – Флюоресцентная проба катализирует реакцию, производящую свечение при добавлении субстрата • Проявление пленки дает ауторадиограмму – Полоски (бэнды) на пленке показывают наличие данной рестрикционного фрагмента с последовательностью, комплементарной пробе.
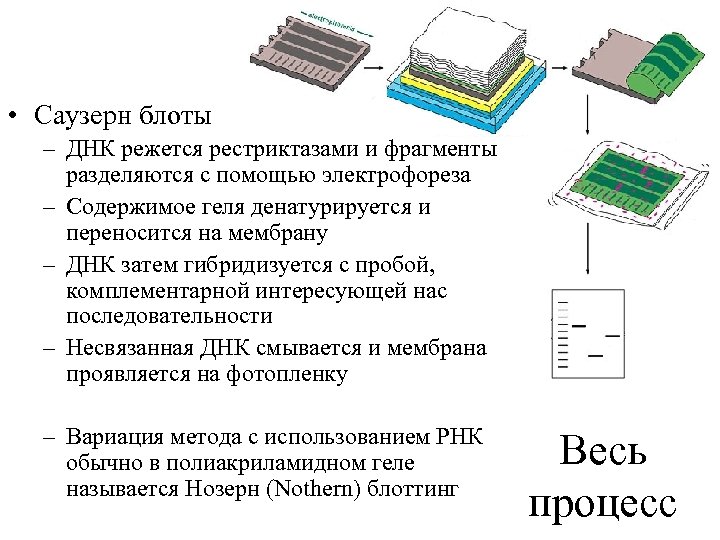
• Саузерн блоты – ДНК режется рестриктазами и фрагменты разделяются с помощью электрофореза – Содержимое геля денатурируется и переносится на мембрану – ДНК затем гибридизуется с пробой, комплементарной интересующей нас последовательности – Несвязанная ДНК смывается и мембрана проявляется на фотопленку – Вариация метода с использованием РНК обычно в полиакриламидном геле называется Нозерн (Nothern) блоттинг Весь процесс

Метод полиморфизма рестрикционных фрагментов • Хромосомная ДНК 2 х разных людей различается случайными полиморфизмами – Существуют миллионы SSP - single nucleotide polymorphisms • Если эти вариации приводят к созданию или разрушению рестрикционного сайта, то и получившиеся фрагменты будут различаться на Саузерн блотах

Пример 1 – точковая мутация • Последовательность содержит 2 Eco R 1 последовательности, разделенные 4000 нуклеотидов • Мутация в одной из 2 х хромосом у одного из сравниваемых людей создала новую Eco R 1 последовательность внутри исследуемого гена – Получилось 2 фрагмента 1500 and 2500 п. о. – Проба комплементарна к последовательности лежащей внутри последовательности длиной 2500 п. о. – Детекция метод Саузерн блота даст 1 фрагмент 4000 п. о. от нормальной хромосомы и 2 фрагмента от мутантной хромосомы
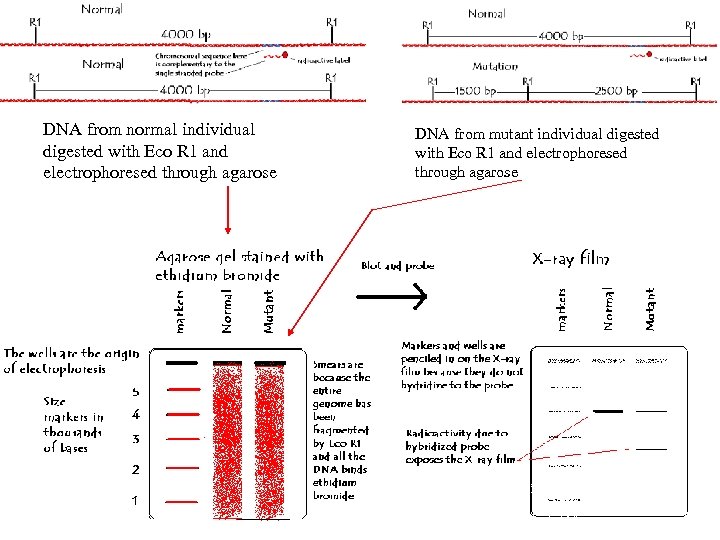
DNA from normal individual digested with Eco R 1 and electrophoresed through agarose DNA from mutant individual digested with Eco R 1 and electrophoresed through agarose
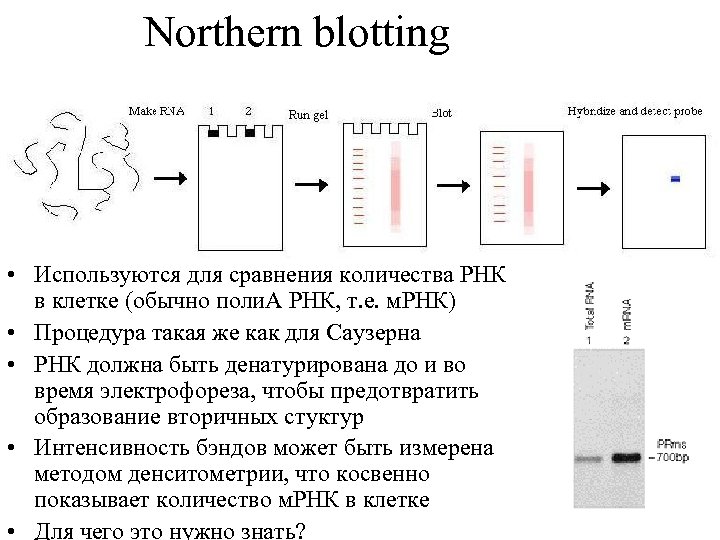
Northern blotting • Используются для сравнения количества РНК в клетке (обычно поли. А РНК, т. е. м. РНК) • Процедура такая же как для Саузерна • РНК должна быть денатурирована до и во время электрофореза, чтобы предотвратить образование вторичных стуктур • Интенсивность бэндов может быть измерена методом денситометрии, что косвенно показывает количество м. РНК в клетке • Для чего это нужно знать?

Электрофорез белков • Белки не имеют постоянную величину отношения размера и заряда – Метод электрофореза заставляет белки принять постоянные величины размера и заряда

SDS-полиакриламидный гель для электрофореза белков • Белковый экстракт, выделенный из клеток, кипятится 3 минуты в растворе детергента SDS и бета меркаптоэтанола, который разрывает дисульфидные связи. – Детергент разрывает третичную и вторичную структуру – Детергент, который имеет негативный заряд, вытягивает и покрывает молекулы белка своим слоем – Таким образом молекулы белка мигрируют в геле от отрицательного полюса к положительному в соответствии со своим размером, который может быть определен с помощью маркеров – см. пример
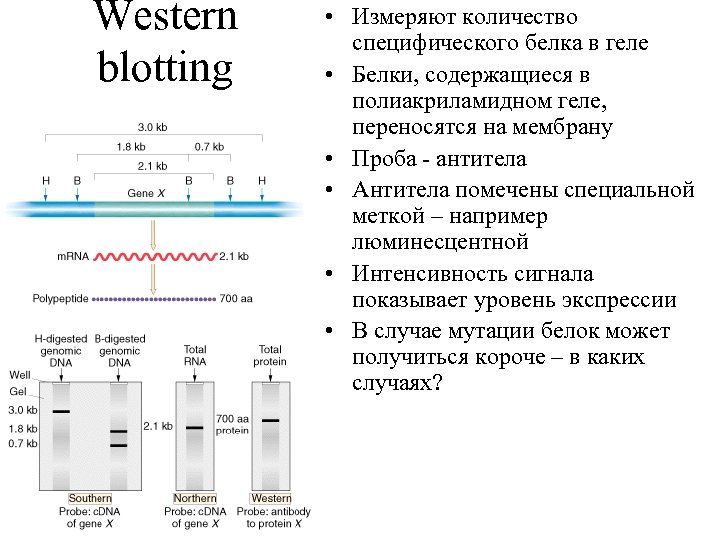
Western blotting • Измеряют количество специфического белка в геле • Белки, содержащиеся в полиакриламидном геле, переносятся на мембрану • Проба - антитела • Антитела помечены специальной меткой – например люминесцентной • Интенсивность сигнала показывает уровень экспрессии • В случае мутации белок может получиться короче – в каких случаях?
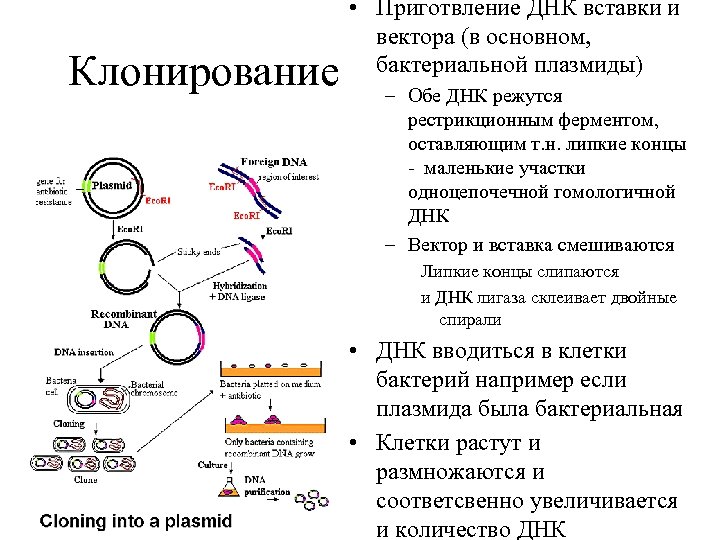
Клонирование • Приготвление ДНК вставки и вектора (в основном, бактериальной плазмиды) – Обе ДНК режутся рестрикционным ферментом, оставляющим т. н. липкие концы - маленькие участки одноцепочечной гомологичной ДНК – Вектор и вставка смешиваются Липкие концы слипаются и ДНК лигаза склеивает двойные спирали • ДНК вводиться в клетки бактерий например если плазмида была бактериальная • Клетки растут и размножаются и соответсвенно увеличивается и количество ДНК

Зачем клонировать? • Аналитические цели – Последовательность ДНК и структура и функция гена и производного белка могут быть изучены если этот ген изолирован из контекста целого генома и клонирован • Практические цели – Изолированный ген может быть экспрессирован in vivo или in vitro – Коммерческие цели – Терапевтические цели – Примеры? • Манипуляции, чтобы изменить структуру белка Какие? – Получить много идентичных копий одного и того же гена

Реагенты для клонирования • Ферменты и буферные растворы – Рестрикционные ферменты – Лигаза – Иногда в случае клонов к. ДНК – обратная транскриптаза • Что такое к. ДНК и зачем она нужна? См. ниже • Векторы • Принимающие клетки
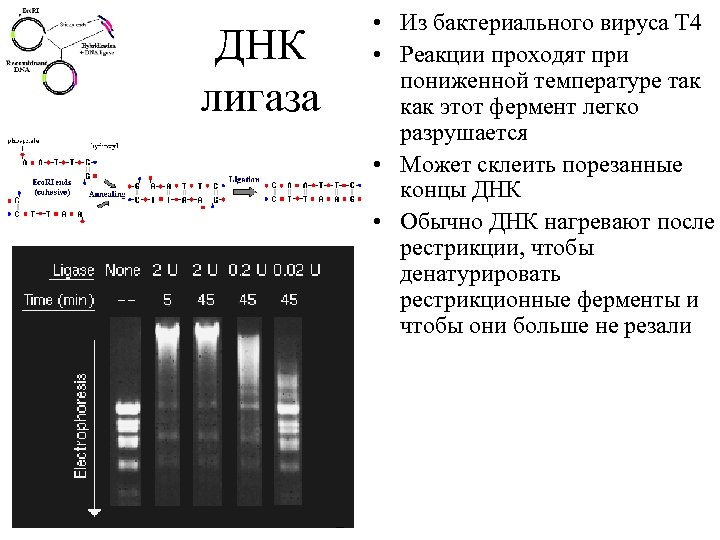
ДНК лигаза • Из бактериального вируса T 4 • Реакции проходят при пониженной температуре так как этот фермент легко разрушается • Может склеить порезанные концы ДНК • Обычно ДНК нагревают после рестрикции, чтобы денатурировать рестрикционные ферменты и чтобы они больше не резали
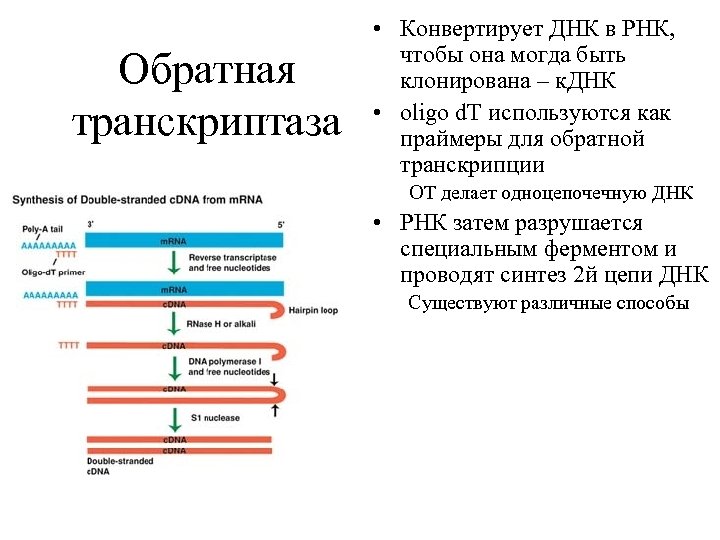
Обратная транскриптаза • Конвертирует ДНК в РНК, чтобы она могда быть клонирована – к. ДНК • oligo d. T используются как праймеры для обратной транскрипции ОТ делает одноцепочечную ДНК • РНК затем разрушается специальным ферментом и проводят синтез 2 й цепи ДНК Существуют различные способы

Векторы • ДНК с независимым ориджином репликации (про- и/или эукариотическим) и маркерами селекции и экспрессии – Маркер селекции позволяет клетке выжить в летальных условиях, например – в присутствии антибиотиков – Маркер экспрессии позволяет увидеть наличие гена например GFP – green fluorescent protein! – Плазмиды, вирусы или искусственные хромосомы
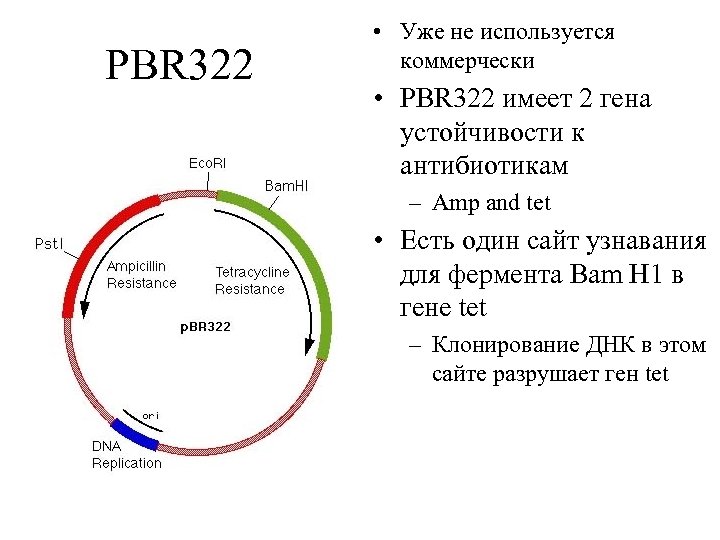
PBR 322 • Уже не используется коммерчески • PBR 322 имеет 2 гена устойчивости к антибиотикам – Amp and tet • Есть один сайт узнавания для фермента Bam H 1 в гене tet – Клонирование ДНК в этом сайте разрушает ген tet
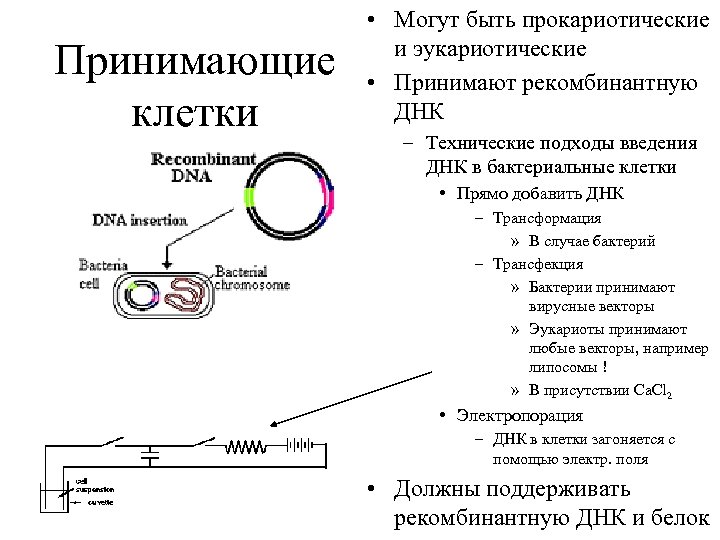
Принимающие клетки • Могут быть прокариотические и эукариотические • Принимают рекомбинантную ДНК – Технические подходы введения ДНК в бактериальные клетки • Прямо добавить ДНК – Трансформация » В случае бактерий – Трансфекция » Бактерии принимают вирусные векторы » Эукариоты принимают любые векторы, например липосомы ! » В присутствии Ca. Cl 2 • Электропорация – ДНК в клетки загоняется с помощью электр. поля • Должны поддерживать рекомбинантную ДНК и белок
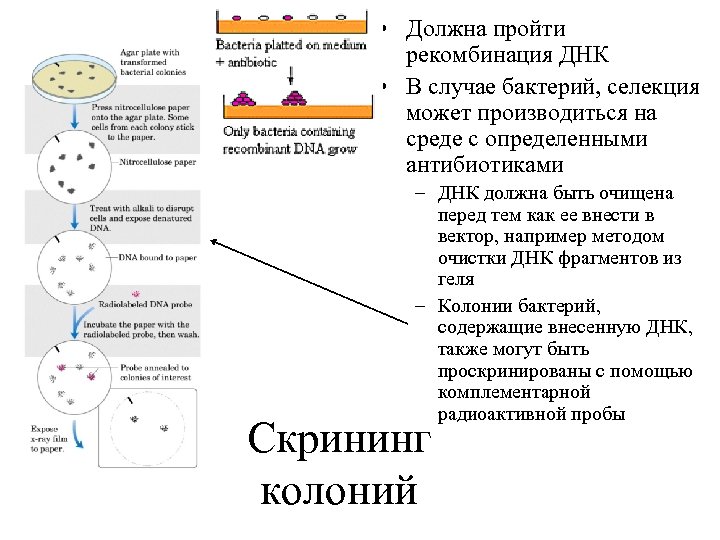
• Должна пройти рекомбинация ДНК • В случае бактерий, селекция может производиться на среде с определенными антибиотиками – ДНК должна быть очищена перед тем как ее внести в вектор, например методом очистки ДНК фрагментов из геля – Колонии бактерий, содержащие внесенную ДНК, также могут быть проскринированы с помощью комплементарной радиоактивной пробы Скрининг колоний

Что делать с ДНК? Принимающие клетки могут быть размножены и ДНК таким образом амплифицирована • Секвенировать – Может быть сделано прямо на очищенной ДНК • Экспрессировать – Можно наработать много белка • Мутировать – Возможно внести специфические мутации, например методом ПЦР мутагенеза • Можно изучать функции разных доменов получившегося белка • Можно изучать различные промоторы и энхансеры

Примеры медицинской значимости • Диабет (особенно Инсулино-зависимый) – Когда существует дефект клеток, производящих инсулин – Требуется искусственный инсулин • Инсулин, выделенный из других животных, может вызвать иммунную реакцию • Человеческий инсулин был клонирован и экспрессирован вначале в бактериях – Но проблема в том, что бактерии не поддерживают посттрансляционной модификации про-инсулина http: //www. diabetesdaily. com/wiki/images/2/25/Insulinpath. png

В настоящее время • Полная последовательность к. ДНК клонирована в дрожжах (простейших эукариотах) • Дрожжи – это одноклеточные эукариоты и следовательно они содержат ЭР и сигнальную пептидазу и они были генетически модифицированы, чтобы содержать пептидазу, отрезающюю С-пептид

Какие следующие проблемы на пути доступности инсулина?

FISH • http: //en. wikipedia. org/wiki/Flu orescent_in_situ_hybridization

Ресурсы Интернета http: //www. hhmi. org/biointeractive /vlabs/bacterial_id/index. html http: //www. ornl. gov/sci/techresour ces/Human_Genome/posters/chrom osome/tools. shtml http: //www. ebi. ac. uk/Tools/
bacfde03a593d1fcaf85e7955a1614c2.ppt