ЭХ_03_16.pptx
- Количество слайдов: 32
 Электродные реакции, контролируемые скоростью массопереноса Диффузионная кинетика в том числе в условиях миграции и конвекции. Диффузный и диффузионный слои у поверхности электрода. Стационарная поляризации. диффузия. Полярографическая волна при концентрационной Вращающийся дисковый электрод (ДЭ). Применение ДЭ в АХ и для исследования механизма реакций. Уравнения обратимой и необратимой поляризационной кривой. Классификация сложных электродных процессов. Обозначения. Примеры. Сопряженные с электродной реакцией химические реакции, протекающие в объеме раствора. Вывод зависимости i=i( ): Обратимый электродный процесс, сопряженный с предшествующей равновесной химической реакцией; Обратимый электродный процесс, сопряженный с предшествующей неравновесной химической реакцией; Обратимый электродный процесс, сопряженный с последующей неравновесной химической реакцией; Смешанный (коррозионный, стационарный) потенциал. 1
Электродные реакции, контролируемые скоростью массопереноса Диффузионная кинетика в том числе в условиях миграции и конвекции. Диффузный и диффузионный слои у поверхности электрода. Стационарная поляризации. диффузия. Полярографическая волна при концентрационной Вращающийся дисковый электрод (ДЭ). Применение ДЭ в АХ и для исследования механизма реакций. Уравнения обратимой и необратимой поляризационной кривой. Классификация сложных электродных процессов. Обозначения. Примеры. Сопряженные с электродной реакцией химические реакции, протекающие в объеме раствора. Вывод зависимости i=i( ): Обратимый электродный процесс, сопряженный с предшествующей равновесной химической реакцией; Обратимый электродный процесс, сопряженный с предшествующей неравновесной химической реакцией; Обратимый электродный процесс, сопряженный с последующей неравновесной химической реакцией; Смешанный (коррозионный, стационарный) потенциал. 1
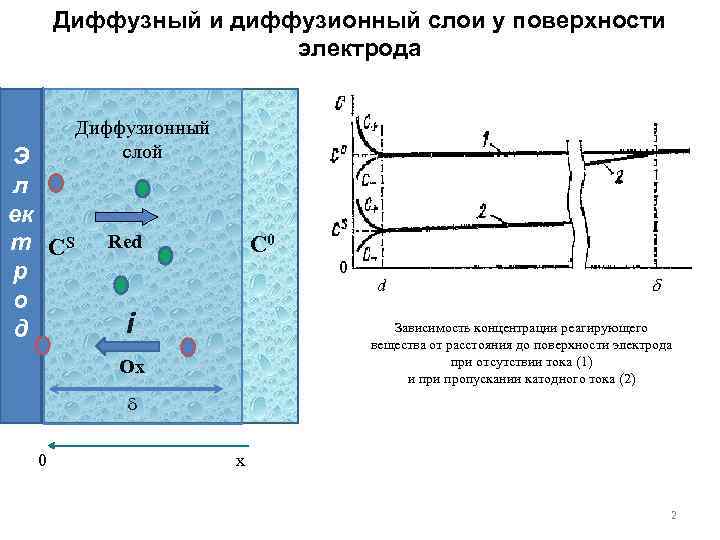 Диффузный и диффузионный слои у поверхности электрода Э л ек т СS р о д Диффузионный слой Red С 0 i 0 d Зависимость концентрации реагирующего вещества от расстояния до поверхности электрода при отсутствии тока (1) и пропускании катодного тока (2) Ox 0 x 2
Диффузный и диффузионный слои у поверхности электрода Э л ек т СS р о д Диффузионный слой Red С 0 i 0 d Зависимость концентрации реагирующего вещества от расстояния до поверхности электрода при отсутствии тока (1) и пропускании катодного тока (2) Ox 0 x 2
 Стационарная дифузия 3
Стационарная дифузия 3
 4
4
 Потенциал полуволны 5
Потенциал полуволны 5
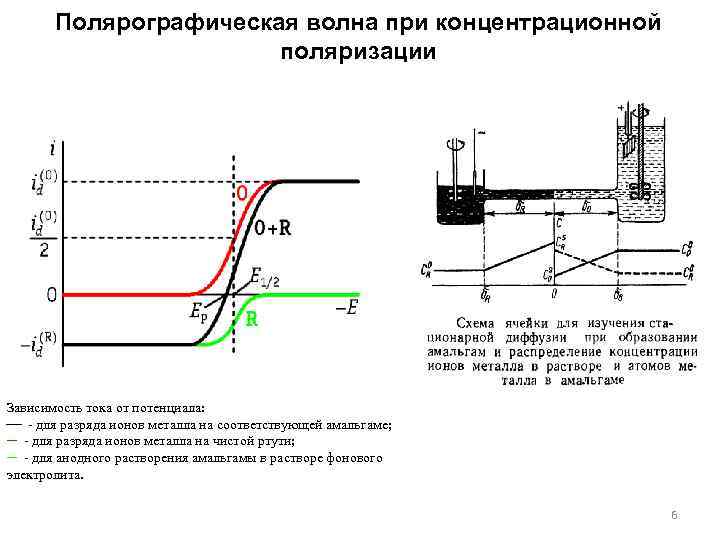 Полярографическая волна при концентрационной поляризации Зависимость тока от потенциала: для разряда ионов металла на соответствующей амальгаме; ─ для разряда ионов металла на чистой ртути; ─ для анодного растворения амальгамы в растворе фонового электролита. 6
Полярографическая волна при концентрационной поляризации Зависимость тока от потенциала: для разряда ионов металла на соответствующей амальгаме; ─ для разряда ионов металла на чистой ртути; ─ для анодного растворения амальгамы в растворе фонового электролита. 6
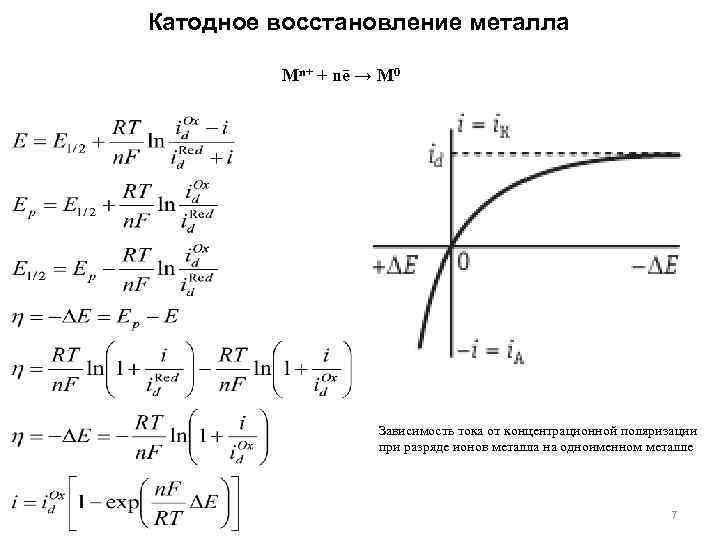 Катодное восстановление металла Mn+ + nē → M 0 Зависимость тока от концентрационной поляризации при разряде ионов металла на одноименном металле 7
Катодное восстановление металла Mn+ + nē → M 0 Зависимость тока от концентрационной поляризации при разряде ионов металла на одноименном металле 7
 Миграция в процессах массопереноса. Диффузия плюс миграция в стационарных условиях Суммарный процесс диффузии и миграции описывается уравнением вида: 8
Миграция в процессах массопереноса. Диффузия плюс миграция в стационарных условиях Суммарный процесс диффузии и миграции описывается уравнением вида: 8
 Разряд катионов Ag+ на серебряном электроде в бинарном растворе Ag. NO 3 Ag+ + ē → Ag 0 9
Разряд катионов Ag+ на серебряном электроде в бинарном растворе Ag. NO 3 Ag+ + ē → Ag 0 9
 Разряд катионов Ag+ на серебряном электроде из смешанного раствора Ag. NO 3 + KNO 3 Ag+ + ē → Ag 0 10
Разряд катионов Ag+ на серебряном электроде из смешанного раствора Ag. NO 3 + KNO 3 Ag+ + ē → Ag 0 10
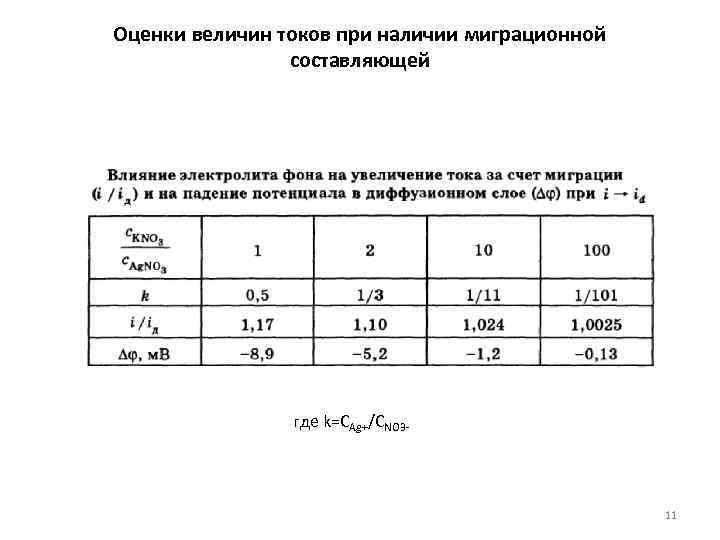 Оценки величин токов при наличии миграционной составляющей где k=CAg+/CNO 3 11
Оценки величин токов при наличии миграционной составляющей где k=CAg+/CNO 3 11
 Конвективная диффузия и метод вращающегося дискового электрода • Размешивание раствора ускоряет процесс массопереноса реагентов и продуктов реакции за счет того, что уменьшается толщина диффузионного слоя, возрастают градиенты концентрации этих веществ у поверхности электрода и их потоки диффузии. • Впервые решение задачи проведено Нернстом (1904 г. ) при условии, что толщина диффузионного слоя и неперемешиваемого слоя совпадают. • в условиях размешивания диффузия реагентов к электроду и продуктов реакции от элек трода происходит в движущихся слоях, причем приближе нии к электроду скорость движения раствора относительно поверхности уменьшается. Это обстоя тельство сильно осложняет решение за дачконвективной диффузии. • Задача существенно упрощается для вращающегося дискового электрода. 12
Конвективная диффузия и метод вращающегося дискового электрода • Размешивание раствора ускоряет процесс массопереноса реагентов и продуктов реакции за счет того, что уменьшается толщина диффузионного слоя, возрастают градиенты концентрации этих веществ у поверхности электрода и их потоки диффузии. • Впервые решение задачи проведено Нернстом (1904 г. ) при условии, что толщина диффузионного слоя и неперемешиваемого слоя совпадают. • в условиях размешивания диффузия реагентов к электроду и продуктов реакции от элек трода происходит в движущихся слоях, причем приближе нии к электроду скорость движения раствора относительно поверхности уменьшается. Это обстоя тельство сильно осложняет решение за дачконвективной диффузии. • Задача существенно упрощается для вращающегося дискового электрода. 12
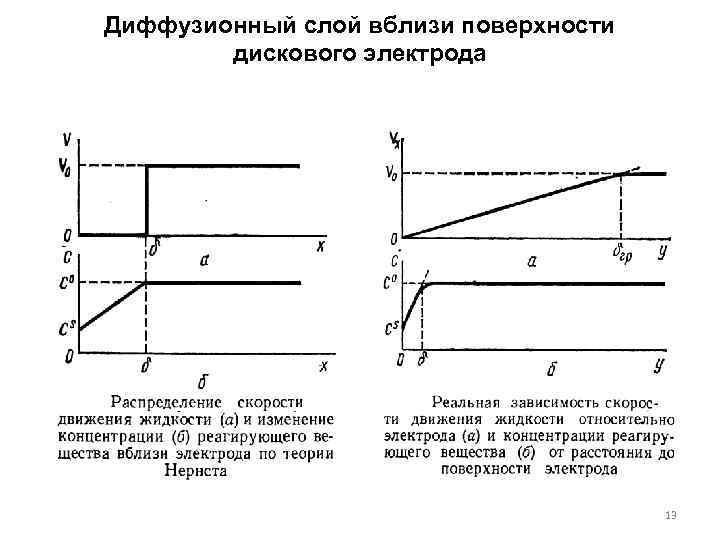 Диффузионный слой вблизи поверхности дискового электрода 13
Диффузионный слой вблизи поверхности дискового электрода 13
 Уравнение Левича 14
Уравнение Левича 14
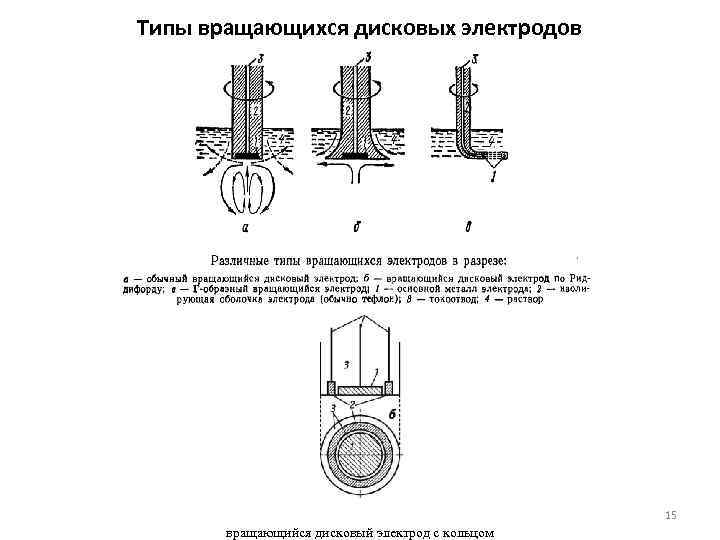 Типы вращающихся дисковых электродов 15 вращающийся дисковый электрод с кольцом
Типы вращающихся дисковых электродов 15 вращающийся дисковый электрод с кольцом
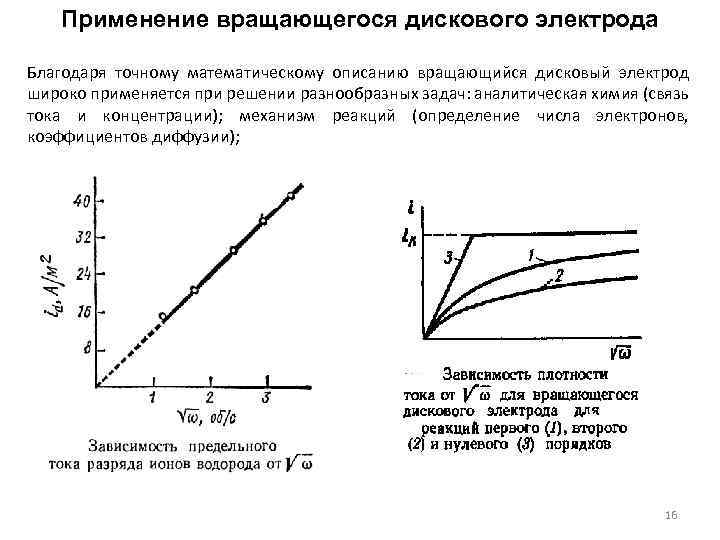 Применение вращающегося дискового электрода Благодаря точному математическому описанию вращающийся дисковый электрод широко применяется при решении разнообразных задач: аналитическая химия (связь тока и концентрации); механизм реакций (определение числа электронов, коэффициентов диффузии); 16
Применение вращающегося дискового электрода Благодаря точному математическому описанию вращающийся дисковый электрод широко применяется при решении разнообразных задач: аналитическая химия (связь тока и концентрации); механизм реакций (определение числа электронов, коэффициентов диффузии); 16
 Условия, положенные в осно ву полученного выше решения диффузионной задачи в , реальных системах обычно не выполняются. Тем не ме нее выведенные уравнения связывающие зависимость тока от потенциала оказываются справедливыми для многих, в том числе практически важных, случаев ограничения скорости электродных процессов диффузией (если только в эти уравнения подставить соответствующие ре альным системам выражения для предельных диффузионных то ков d. Ox и id. Red)). i Они вы полняются также и для нестационарной диффузии к электродам разного типа (плоские, в форме неподвижной или расширяющей ся сфер) при различных E = const, но при условии, что толщина диффузионного слоя на этих электродах значительно меньше их геометрических размеров. 17
Условия, положенные в осно ву полученного выше решения диффузионной задачи в , реальных системах обычно не выполняются. Тем не ме нее выведенные уравнения связывающие зависимость тока от потенциала оказываются справедливыми для многих, в том числе практически важных, случаев ограничения скорости электродных процессов диффузией (если только в эти уравнения подставить соответствующие ре альным системам выражения для предельных диффузионных то ков d. Ox и id. Red)). i Они вы полняются также и для нестационарной диффузии к электродам разного типа (плоские, в форме неподвижной или расширяющей ся сфер) при различных E = const, но при условии, что толщина диффузионного слоя на этих электродах значительно меньше их геометрических размеров. 17
 Уравнение обратимой поляризационной кривой Oxz + ne Redz–n Стационарная диффузия. Граничные условия: при x = 0 (на поверхности электрода) концентрация равна С(0); при x = δ (в объеме раствора) концентрация равна C*. Ox и Red растворимы, при t=0, CRed=0 18
Уравнение обратимой поляризационной кривой Oxz + ne Redz–n Стационарная диффузия. Граничные условия: при x = 0 (на поверхности электрода) концентрация равна С(0); при x = δ (в объеме раствора) концентрация равна C*. Ox и Red растворимы, при t=0, CRed=0 18
 Уравнение обратимой поляризационной кривой 19
Уравнение обратимой поляризационной кривой 19
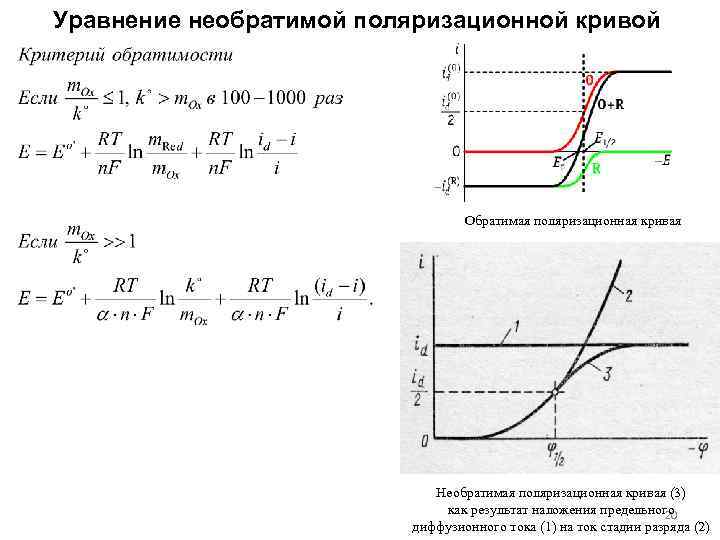 Уравнение необратимой поляризационной кривой Обратимая поляризационная кривая Необратимая поляризационная кривая (3) как результат наложения предельного 20 диффузионного тока (1) на ток стадии разряда (2)
Уравнение необратимой поляризационной кривой Обратимая поляризационная кривая Необратимая поляризационная кривая (3) как результат наложения предельного 20 диффузионного тока (1) на ток стадии разряда (2)
 Классификация сложных электродных процессов Подход учитывает положение химической стадии в реакционной схеме относительно стадии переноса заряда. Обозначения: C – “chemical” химическая стадия процесса; E – “electrochemical” электродная стадия процесса; r – “reversible” обратимая стадия; i – “irriversible” необратимая стадия. СЕ–процесс: электро активное вещество образуется из исходного неактивного соединения. Такая стадия называется также предшествующей. +n ē A ↔ O↔ R Пример: В водном растворе формальдегид присутствует в виде двух таутомерных форм H 2 C(OH)2 = H 2 CO + H 2 O Карбонильная форма электрохимически более активна. Предельный ток электродной реакции определяется объемной химической реакцией дегидратации. H 2 O +n ē H 2 C(OH)2 ↔ H 2 CO ↔ R ЕC –процесс: химическая реакция следует за реакцией переноса электрона +n ē O ↔ R↔ B 2 Hадс →H 2 21
Классификация сложных электродных процессов Подход учитывает положение химической стадии в реакционной схеме относительно стадии переноса заряда. Обозначения: C – “chemical” химическая стадия процесса; E – “electrochemical” электродная стадия процесса; r – “reversible” обратимая стадия; i – “irriversible” необратимая стадия. СЕ–процесс: электро активное вещество образуется из исходного неактивного соединения. Такая стадия называется также предшествующей. +n ē A ↔ O↔ R Пример: В водном растворе формальдегид присутствует в виде двух таутомерных форм H 2 C(OH)2 = H 2 CO + H 2 O Карбонильная форма электрохимически более активна. Предельный ток электродной реакции определяется объемной химической реакцией дегидратации. H 2 O +n ē H 2 C(OH)2 ↔ H 2 CO ↔ R ЕC –процесс: химическая реакция следует за реакцией переноса электрона +n ē O ↔ R↔ B 2 Hадс →H 2 21
 ЕC–процесс: Продукт электродной стадии расходуется при химической реакции, в результате чего падает его концентрация на поверхности электрода. Окисление или восстановление многих органических соединений сопровождается реакциями протонирования, взаимодействия с растворителем или димеризации: HO C 6 H 4 NH 2 → O=C 6 H 4=NH + 2 H+ +2ē O=C 6 H 4=NH + H 2 O → O=C 6 H 4=O + NH 3 Также выделяют более сложные процессы например ЕСЕС. Восстановление кислорода до H 2 O 2: О 2 + ē → O 2 ─ E O 2 ─ + H 3 O+ → HO 2 + H 2 O C HО 2 + ē → HO 2 ─ E HO 2 ─ + H 3 O+ → H 2 O 2 + H 2 O C H 2 О 2 + 2ē + 2 H 3 O+ → 4 H 2 O 22
ЕC–процесс: Продукт электродной стадии расходуется при химической реакции, в результате чего падает его концентрация на поверхности электрода. Окисление или восстановление многих органических соединений сопровождается реакциями протонирования, взаимодействия с растворителем или димеризации: HO C 6 H 4 NH 2 → O=C 6 H 4=NH + 2 H+ +2ē O=C 6 H 4=NH + H 2 O → O=C 6 H 4=O + NH 3 Также выделяют более сложные процессы например ЕСЕС. Восстановление кислорода до H 2 O 2: О 2 + ē → O 2 ─ E O 2 ─ + H 3 O+ → HO 2 + H 2 O C HО 2 + ē → HO 2 ─ E HO 2 ─ + H 3 O+ → H 2 O 2 + H 2 O C H 2 О 2 + 2ē + 2 H 3 O+ → 4 H 2 O 22
 Пример каталитических процессов К химическим реакциям, сопровождающим электродный процесс, относятся каталитические процессы, общую схему которых можно записать в виде: +n ē A + B Ox R B + C Существуют случаи, когда химическая реакция с участием продукта электродной реакции приводит к полной или частичной регенерации исходного вещества. Восстановление U(VI) в минеральной кислоте: U(VI) + ē → U(V) 2 U(V) → U(VI) + U(IV) 23
Пример каталитических процессов К химическим реакциям, сопровождающим электродный процесс, относятся каталитические процессы, общую схему которых можно записать в виде: +n ē A + B Ox R B + C Существуют случаи, когда химическая реакция с участием продукта электродной реакции приводит к полной или частичной регенерации исходного вещества. Восстановление U(VI) в минеральной кислоте: U(VI) + ē → U(V) 2 U(V) → U(VI) + U(IV) 23
 Обратимый электродный процесс, сопряженный с предшествующей равновесной стадией Cr. Er-процесс Наиболее простой случай, который реализуется при электроосаждении металлов из растворов металлокомплексов, а также в полярографическом анализе. MLp Mn+ + p. L, Mn+ + nē (Hg) M 0(Hg). 24
Обратимый электродный процесс, сопряженный с предшествующей равновесной стадией Cr. Er-процесс Наиболее простой случай, который реализуется при электроосаждении металлов из растворов металлокомплексов, а также в полярографическом анализе. MLp Mn+ + p. L, Mn+ + nē (Hg) M 0(Hg). 24
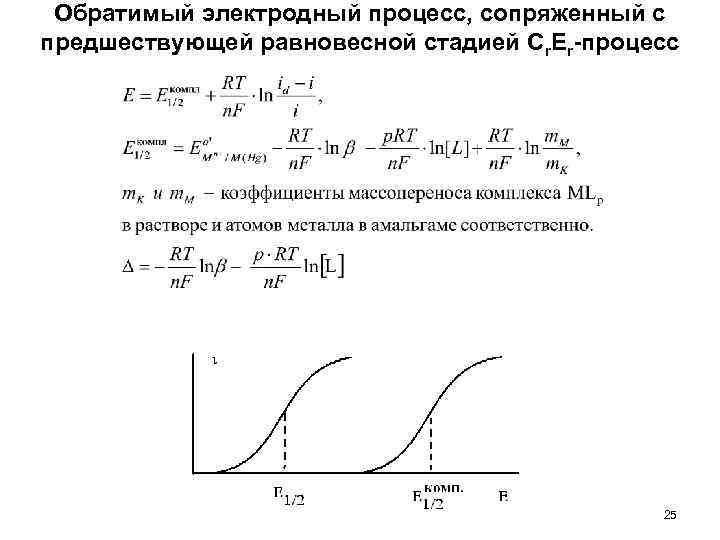 Обратимый электродный процесс, сопряженный с предшествующей равновесной стадией Cr. Er-процесс 25
Обратимый электродный процесс, сопряженный с предшествующей равновесной стадией Cr. Er-процесс 25
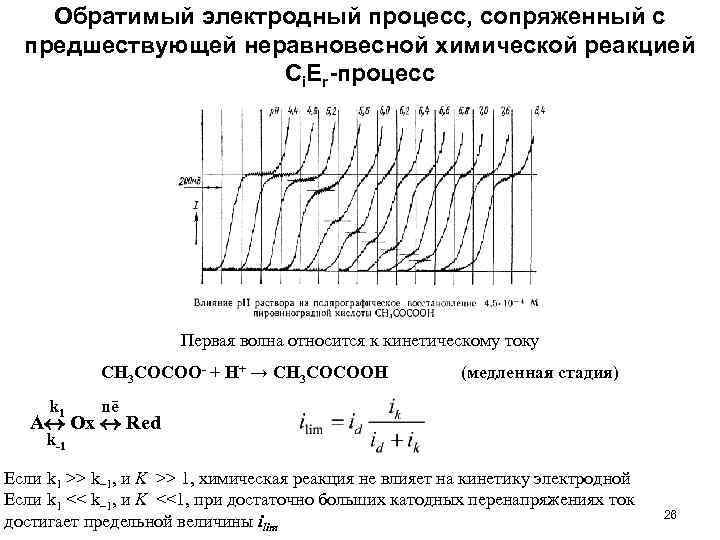 Обратимый электродный процесс, сопряженный с предшествующей неравновесной химической реакцией Ci. Er-процесс Первая волна относится к кинетическому току СH 3 COCOO + H+ → СH 3 COCOOH k 1 (медленная стадия) nē A Ox Red k 1 Если k 1 >> k– 1, и K >> 1, химическая реакция не влияет на кинетику электродной Если k 1 << k– 1, и K <<1, при достаточно больших катодных перенапряжениях ток достигает предельной величины ilim 26
Обратимый электродный процесс, сопряженный с предшествующей неравновесной химической реакцией Ci. Er-процесс Первая волна относится к кинетическому току СH 3 COCOO + H+ → СH 3 COCOOH k 1 (медленная стадия) nē A Ox Red k 1 Если k 1 >> k– 1, и K >> 1, химическая реакция не влияет на кинетику электродной Если k 1 << k– 1, и K <<1, при достаточно больших катодных перенапряжениях ток достигает предельной величины ilim 26
 Ci. Er-процесс. Концепция реакционного слоя Р. Брдичка и К. Визнер 1947 г. k 1 nē A Ox Red k 1 x Зависимость концентрации вещества A, участвующего в медленной гомогенной химической реакции, от расстояния до поверхности электрода по теории Брдички Визнера. (Пунктиром показана истинная зависимость СА от х). Согласно концепции реакционного слоя в объеме раствора равновесие химической реакции не нарушается, тогда как вблизи поверхности электрода в реакционном слое толщиной концентрации A и Ox отличны от равновесных вследствие протекания электродной реакции. Ток определяется числом электрохимически активных частиц Ox (HA), которые образуются в пределах реакционного слоя в единицу времени. - скорость химической реакции; S – площадь поверхности электрода ; толщина реакционного слоя ; i – кинетическая плотность тока ; ik – предельная кинетическая плотность тока. 27
Ci. Er-процесс. Концепция реакционного слоя Р. Брдичка и К. Визнер 1947 г. k 1 nē A Ox Red k 1 x Зависимость концентрации вещества A, участвующего в медленной гомогенной химической реакции, от расстояния до поверхности электрода по теории Брдички Визнера. (Пунктиром показана истинная зависимость СА от х). Согласно концепции реакционного слоя в объеме раствора равновесие химической реакции не нарушается, тогда как вблизи поверхности электрода в реакционном слое толщиной концентрации A и Ox отличны от равновесных вследствие протекания электродной реакции. Ток определяется числом электрохимически активных частиц Ox (HA), которые образуются в пределах реакционного слоя в единицу времени. - скорость химической реакции; S – площадь поверхности электрода ; толщина реакционного слоя ; i – кинетическая плотность тока ; ik – предельная кинетическая плотность тока. 27
 Кинетический ток Толщину реакционного слоя можно приближенно оценить по формуле Энштейна – Смолуховского как среднее расстояние которое проходит частица за время её жизни t. Среднее время существования частиц Ox в реакционном слое обратно пропорционально k-1: tср. 1/k-1. За это время в соответствии с формулой Эйнштейна Смолуховского частица может пройти расстояние (2 Dtср. )½. Реакционный слой можно определить как такой слой раствора из которого все частицы Ox за среднее время своей жизни успевают подойти к поверхности и разрядиться. Точный математический анализ показывает, что толщина такого слоя должна быть (Dtср. )½, так как некоторые частицы движутся параллельно поверхности или в сторону от нее. Тогда 28
Кинетический ток Толщину реакционного слоя можно приближенно оценить по формуле Энштейна – Смолуховского как среднее расстояние которое проходит частица за время её жизни t. Среднее время существования частиц Ox в реакционном слое обратно пропорционально k-1: tср. 1/k-1. За это время в соответствии с формулой Эйнштейна Смолуховского частица может пройти расстояние (2 Dtср. )½. Реакционный слой можно определить как такой слой раствора из которого все частицы Ox за среднее время своей жизни успевают подойти к поверхности и разрядиться. Точный математический анализ показывает, что толщина такого слоя должна быть (Dtср. )½, так как некоторые частицы движутся параллельно поверхности или в сторону от нее. Тогда 28
 Обратимый электродный процесс, сопряженный с последующей необратимой химической реакцией Er. Ci-процес k Ox+ne Red → P Протекание последующей химической реакции не влияет на массоперенос Ox к поверхности электрода. Отвод Red от поверхности электрода происходит как за счет диффузии, так и за счет химической реакции, которая в соответствии с рассматриваемой концепцией протекает в реакционном слое толщиной , где концентрация Red не равна нулю за счет осуществления электродной реакции. Если при t=0 C*Red=0, то плотность измеряемого тока: 29
Обратимый электродный процесс, сопряженный с последующей необратимой химической реакцией Er. Ci-процес k Ox+ne Red → P Протекание последующей химической реакции не влияет на массоперенос Ox к поверхности электрода. Отвод Red от поверхности электрода происходит как за счет диффузии, так и за счет химической реакции, которая в соответствии с рассматриваемой концепцией протекает в реакционном слое толщиной , где концентрация Red не равна нулю за счет осуществления электродной реакции. Если при t=0 C*Red=0, то плотность измеряемого тока: 29
 Смешанный (коррозионный, стационарный) потенциал. Zn + 2 HCl →Zn. Cl 2 + H 2 Поляризационные кривые разряда и ионизации цинка (1) и водо рода(2) Zn 2+ + 2ē Zn H 3 O+ + ē 1/2 H 2 + H 2 O 30
Смешанный (коррозионный, стационарный) потенциал. Zn + 2 HCl →Zn. Cl 2 + H 2 Поляризационные кривые разряда и ионизации цинка (1) и водо рода(2) Zn 2+ + 2ē Zn H 3 O+ + ē 1/2 H 2 + H 2 O 30
 Cтационарный и равновесный потенциалы • • • Равновесный потенциал отвечает равенству скоростей реакций с участием окисленной и восстановленной форм одного и того же вещества, а стационарный потенциал — равенству суммар ных скоростей катодных и анодных реакций для нескольких различных систем. При равновесном потенциале состав фаз постоянен. При ста ционарном потенциале химический состав системы постепен ноизменяется. Например, при растворении цинка концент рация ионов цинка в растворе растет, концентрация ионов водорода уменьшается и одновременно накапливается газообразный водород. Так как скорости процессов зависят от концентраций компонентов раствора, то в принципе стационарный потенциал должен меняться во времени, хотя это из менениеможет быть и очень медленным. Равновесный потенциал не зависит от состояния поверхности электрода, например от способа предварительной обработки поверхности и ее кристаллографической ориентации, состава адсорбционного слоя и т. д. Необходимо только учитывать, что при сильном уменьшении тока обмена начинает сказываться присутствие в растворе различных примесей, способных окис ляться или восстанавливаться и тем самым вызывать отклоне ниепотенциала системы от равновесного значения. Напомним также, что окислительно восстановительные потенциалы не зависят от природы материа ла электрода, если он непо средственно не участвует в установлении равновесия. Стационарный потенциал в принципе зависит от всех тех факторов, которые влия ютна скорость электродных процессов. Поэтому стацио нарные потенциалы часто плохо воспроизводимы. 31
Cтационарный и равновесный потенциалы • • • Равновесный потенциал отвечает равенству скоростей реакций с участием окисленной и восстановленной форм одного и того же вещества, а стационарный потенциал — равенству суммар ных скоростей катодных и анодных реакций для нескольких различных систем. При равновесном потенциале состав фаз постоянен. При ста ционарном потенциале химический состав системы постепен ноизменяется. Например, при растворении цинка концент рация ионов цинка в растворе растет, концентрация ионов водорода уменьшается и одновременно накапливается газообразный водород. Так как скорости процессов зависят от концентраций компонентов раствора, то в принципе стационарный потенциал должен меняться во времени, хотя это из менениеможет быть и очень медленным. Равновесный потенциал не зависит от состояния поверхности электрода, например от способа предварительной обработки поверхности и ее кристаллографической ориентации, состава адсорбционного слоя и т. д. Необходимо только учитывать, что при сильном уменьшении тока обмена начинает сказываться присутствие в растворе различных примесей, способных окис ляться или восстанавливаться и тем самым вызывать отклоне ниепотенциала системы от равновесного значения. Напомним также, что окислительно восстановительные потенциалы не зависят от природы материа ла электрода, если он непо средственно не участвует в установлении равновесия. Стационарный потенциал в принципе зависит от всех тех факторов, которые влия ютна скорость электродных процессов. Поэтому стацио нарные потенциалы часто плохо воспроизводимы. 31
 Уравнение описывающее стационарный потенциал 32
Уравнение описывающее стационарный потенциал 32


