Электродные потенциалы.ppt
- Количество слайдов: 27
 Электродные потенциалы. Химические источники тока
Электродные потенциалы. Химические источники тока
 • Двойной электрический слой – тонкий слой из пространственно разделённых электрических зарядов, образующийся на границе раздела двух фаз • Электроды – электронно-проводящая фазы (металлы или полупроводники), контактирующие с ионным проводником • Электродный потенциал – разность электростатических потенциалов между электродом и находящимся с ним в контакте электролитом
• Двойной электрический слой – тонкий слой из пространственно разделённых электрических зарядов, образующийся на границе раздела двух фаз • Электроды – электронно-проводящая фазы (металлы или полупроводники), контактирующие с ионным проводником • Электродный потенциал – разность электростатических потенциалов между электродом и находящимся с ним в контакте электролитом
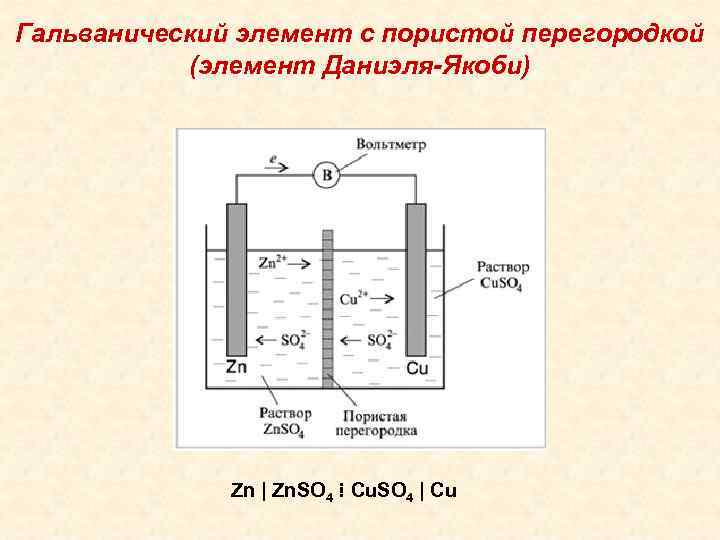 Гальванический элемент с пористой перегородкой (элемент Даниэля-Якоби) Zn | Zn. SO 4 ⁞ Cu. SO 4 | Cu
Гальванический элемент с пористой перегородкой (элемент Даниэля-Якоби) Zn | Zn. SO 4 ⁞ Cu. SO 4 | Cu
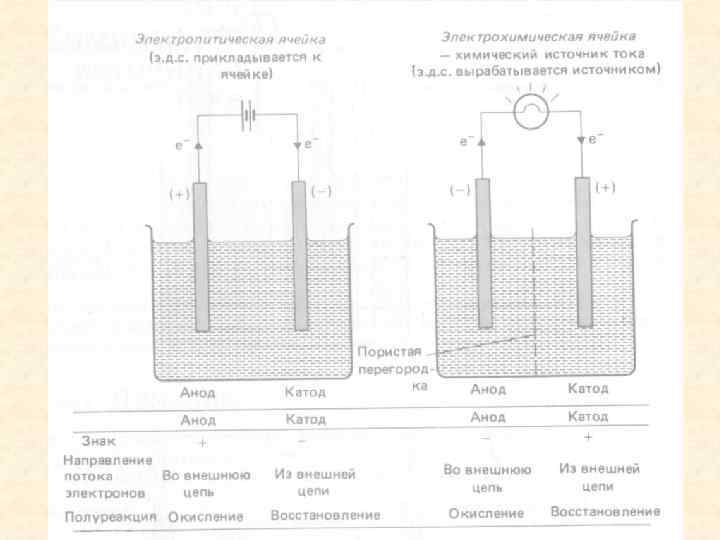
 • Электрохимические цепи – системы, состоящие из двух электродов, помещённых в раствор электролита или в два разных раствора, находящихся в контакте друг с другом • Гальванические элементы – электрохимические цепи, способные вырабатывать электрическую энергию • Электродвижущая сила (ЭДС) – разность потенциалов между электродами: катодом (процесс восстановления, «+» ) и анодом (процесс окисления, «–» )
• Электрохимические цепи – системы, состоящие из двух электродов, помещённых в раствор электролита или в два разных раствора, находящихся в контакте друг с другом • Гальванические элементы – электрохимические цепи, способные вырабатывать электрическую энергию • Электродвижущая сила (ЭДС) – разность потенциалов между электродами: катодом (процесс восстановления, «+» ) и анодом (процесс окисления, «–» )
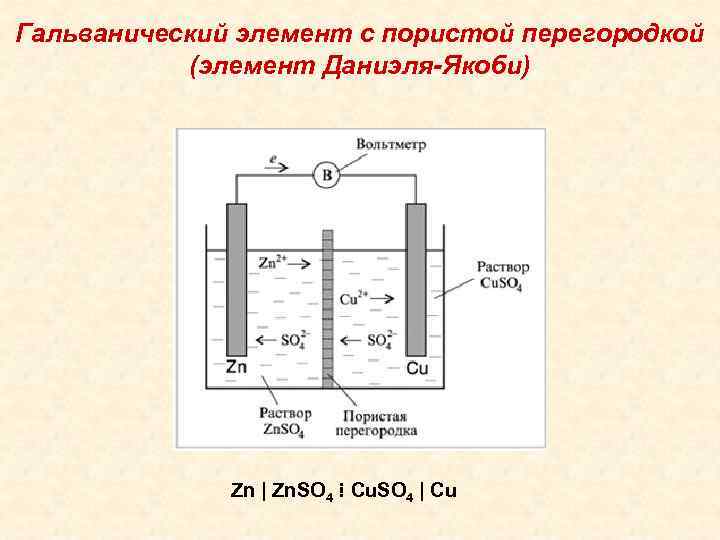 Гальванический элемент с пористой перегородкой (элемент Даниэля-Якоби) Zn | Zn. SO 4 ⁞ Cu. SO 4 | Cu
Гальванический элемент с пористой перегородкой (элемент Даниэля-Якоби) Zn | Zn. SO 4 ⁞ Cu. SO 4 | Cu
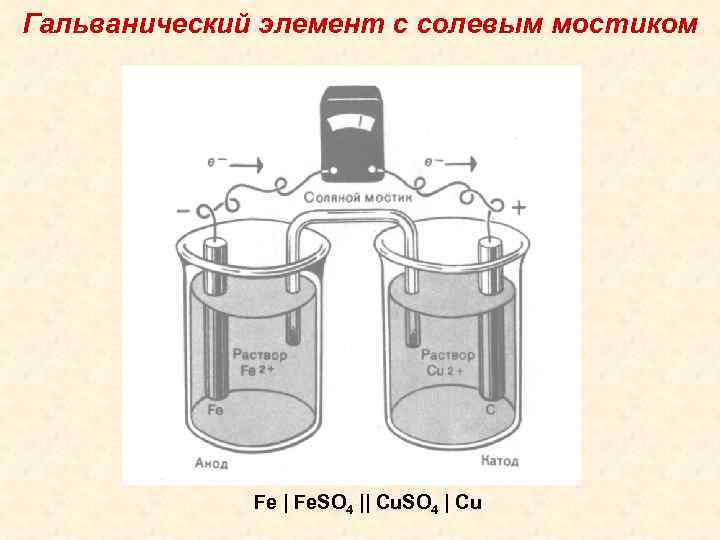 Гальванический элемент с солевым мостиком Fe | Fe. SO 4 || Cu. SO 4 | Cu
Гальванический элемент с солевым мостиком Fe | Fe. SO 4 || Cu. SO 4 | Cu
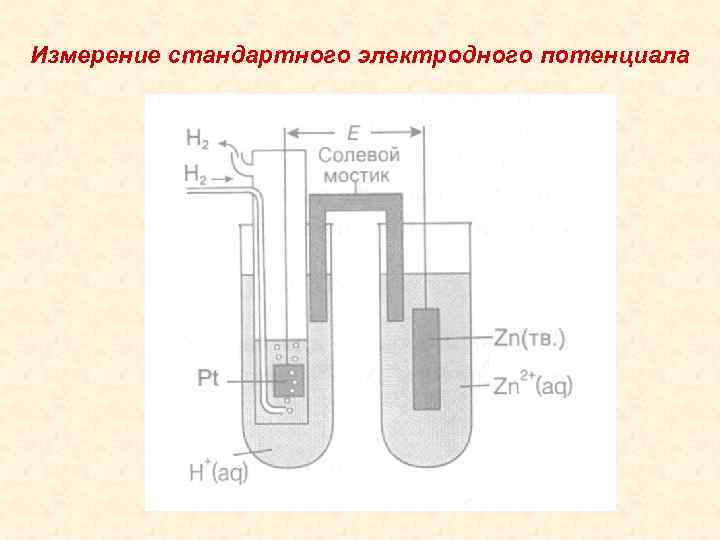 Измерение стандартного электродного потенциала
Измерение стандартного электродного потенциала
 • Стандартный электродный потенциал – электродный потенциал, измеренный по отношению к водородному электроду в стандартных условиях
• Стандартный электродный потенциал – электродный потенциал, измеренный по отношению к водородному электроду в стандартных условиях
 Гальванические элементы • Химические – источником электрической энергии является энергия Гиббса протекающей в системе окислительно-восстановительной (“токообразующей”) химической реакции • Концентрационные – состоят из одинаковых электродов с различной концентрацией веществ, участвующих в окислительно-восстановительных процессах.
Гальванические элементы • Химические – источником электрической энергии является энергия Гиббса протекающей в системе окислительно-восстановительной (“токообразующей”) химической реакции • Концентрационные – состоят из одинаковых электродов с различной концентрацией веществ, участвующих в окислительно-восстановительных процессах.
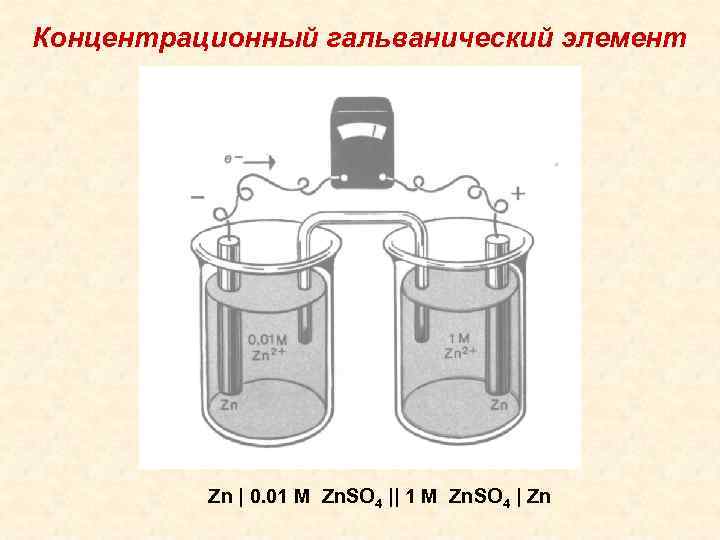 Концентрационный гальванический элемент Zn | 0. 01 M Zn. SO 4 || 1 M Zn. SO 4 | Zn
Концентрационный гальванический элемент Zn | 0. 01 M Zn. SO 4 || 1 M Zn. SO 4 | Zn
 • Потенциометрия – метод физико-химического анализа, основанный на экспериментальном определении электродных потенциалов с помощью измерения ЭДС соответствующих гальванических элементов • С помощью потенциометрии можно определять термодинамические характеристики токообразующих реакций (изменение энергии Гиббса, константу равновесия), коэффициенты активности электролитов, р. Н растворов и пр.
• Потенциометрия – метод физико-химического анализа, основанный на экспериментальном определении электродных потенциалов с помощью измерения ЭДС соответствующих гальванических элементов • С помощью потенциометрии можно определять термодинамические характеристики токообразующих реакций (изменение энергии Гиббса, константу равновесия), коэффициенты активности электролитов, р. Н растворов и пр.
 Химические источники тока • Гальванические элементы (первичные элементы) – источники тока одноразового действия • Электрические аккумуляторы (вторичные элементы) – источники тока многократного действия • Топливные элементы – источники тока непрерывного действия
Химические источники тока • Гальванические элементы (первичные элементы) – источники тока одноразового действия • Электрические аккумуляторы (вторичные элементы) – источники тока многократного действия • Топливные элементы – источники тока непрерывного действия
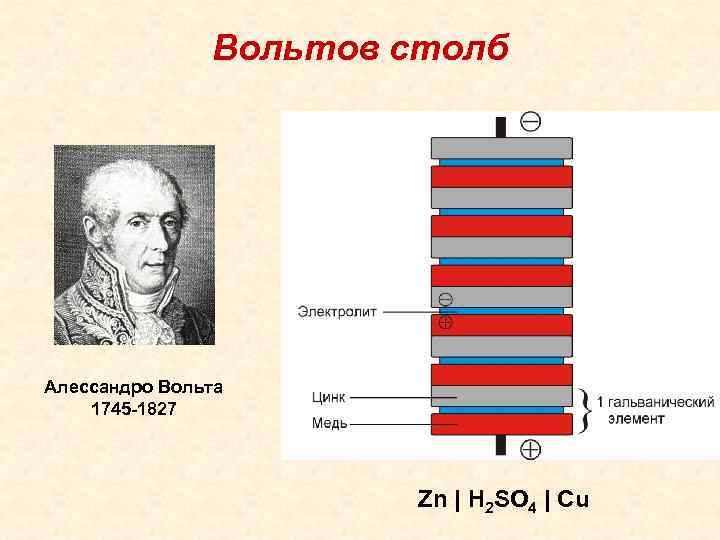 Вольтов столб Алессандро Вольта 1745 -1827 Zn | H 2 SO 4 | Cu
Вольтов столб Алессандро Вольта 1745 -1827 Zn | H 2 SO 4 | Cu
 Василий Владимирович Петров 1761 -1834
Василий Владимирович Петров 1761 -1834
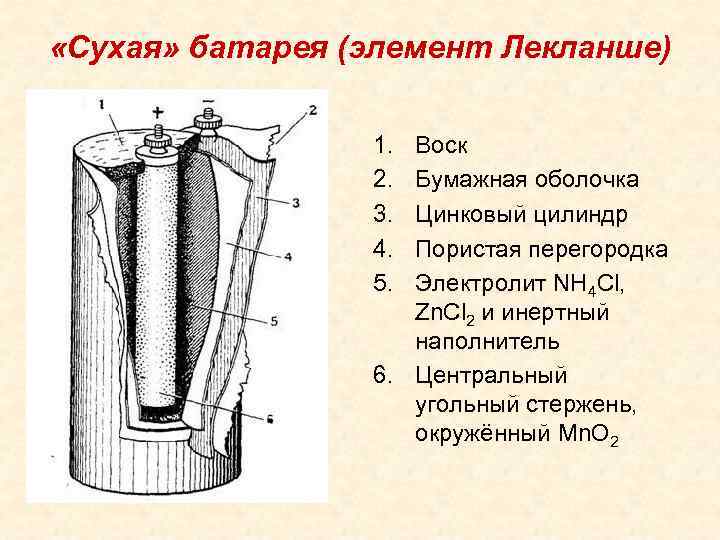 «Сухая» батарея (элемент Лекланше) 1. 2. 3. 4. 5. Воск Бумажная оболочка Цинковый цилиндр Пористая перегородка Электролит NH 4 Cl, Zn. Cl 2 и инертный наполнитель 6. Центральный угольный стержень, окружённый Mn. O 2
«Сухая» батарея (элемент Лекланше) 1. 2. 3. 4. 5. Воск Бумажная оболочка Цинковый цилиндр Пористая перегородка Электролит NH 4 Cl, Zn. Cl 2 и инертный наполнитель 6. Центральный угольный стержень, окружённый Mn. O 2
 Свинцовый аккумулятор Изобретён в 1859 г. французским физиком Г. Планте Pb | H 2 SO 4 | Pb. O 2 | Pb
Свинцовый аккумулятор Изобретён в 1859 г. французским физиком Г. Планте Pb | H 2 SO 4 | Pb. O 2 | Pb
 Литий-ионный аккумулятор В настоящее время это самый популярный тип аккумуляторов в таких устройствах как сотовые телефоны, ноутбуки, цифровые фотоаппараты, электромобили. Первый литиево-ионный аккумулятор разработала корпорация Sony в 1991 г. • • Принцип действия анод: Li. Co. O 2 – n ē = Li 1 -n. Co. O 2 + n. Li+ катод: С + n. Li+ + n ē = C Lin • • • Потребительские характеристики Энергетическая плотность: 110 … 200 Вт*ч/кг Внутреннее сопротивление: 150 … 250 м. Ом (для батареи 7, 2 В) Число циклов заряд/разряд до потери 20% ёмкости: 500— 1000 Время быстрого заряда: 2 -4 часа Допустимый перезаряд: очень низкий Саморазряд при комнатной температуре: 5 -10% в месяц Напряжение максимальное: 4, 18. . 4, 20 В (полностью заряжен) Напряжение минимальное: 2, 5. . 2, 75 В(полностью разряжен) Диапазон рабочих температур: − 20 — +60 °C Оптимальные условия: при 40%-ом заряде от ёмкости аккумулятора «Стареют» при хранении
Литий-ионный аккумулятор В настоящее время это самый популярный тип аккумуляторов в таких устройствах как сотовые телефоны, ноутбуки, цифровые фотоаппараты, электромобили. Первый литиево-ионный аккумулятор разработала корпорация Sony в 1991 г. • • Принцип действия анод: Li. Co. O 2 – n ē = Li 1 -n. Co. O 2 + n. Li+ катод: С + n. Li+ + n ē = C Lin • • • Потребительские характеристики Энергетическая плотность: 110 … 200 Вт*ч/кг Внутреннее сопротивление: 150 … 250 м. Ом (для батареи 7, 2 В) Число циклов заряд/разряд до потери 20% ёмкости: 500— 1000 Время быстрого заряда: 2 -4 часа Допустимый перезаряд: очень низкий Саморазряд при комнатной температуре: 5 -10% в месяц Напряжение максимальное: 4, 18. . 4, 20 В (полностью заряжен) Напряжение минимальное: 2, 5. . 2, 75 В(полностью разряжен) Диапазон рабочих температур: − 20 — +60 °C Оптимальные условия: при 40%-ом заряде от ёмкости аккумулятора «Стареют» при хранении
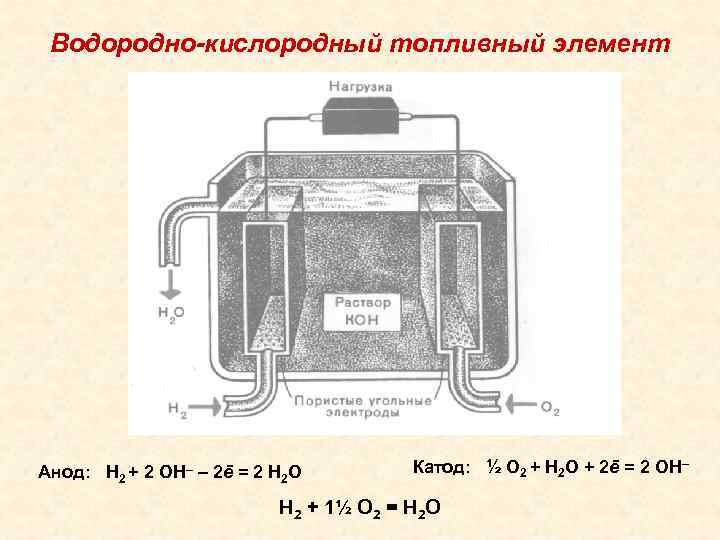 Водородно-кислородный топливный элемент Анод: Н 2 + 2 ОН– – 2ē = 2 Н 2 О Катод: ½ О 2 + Н 2 О + 2ē = 2 ОН– H 2 + 1½ O 2 = H 2 O
Водородно-кислородный топливный элемент Анод: Н 2 + 2 ОН– – 2ē = 2 Н 2 О Катод: ½ О 2 + Н 2 О + 2ē = 2 ОН– H 2 + 1½ O 2 = H 2 O
 Метаноловый топливный элемент Анод: CH 3 OH + H 2 O – 6ē = CO 2 + 6 H+ Катод: 1½ O 2 + 6 H+ + 6ē =3 H 2 O CH 3 OH + 1½ O 2 = CO 2 + 2 H 2 O
Метаноловый топливный элемент Анод: CH 3 OH + H 2 O – 6ē = CO 2 + 6 H+ Катод: 1½ O 2 + 6 H+ + 6ē =3 H 2 O CH 3 OH + 1½ O 2 = CO 2 + 2 H 2 O
 2009. 12. 26, 14: 27 Новостная служба Ferra Японская корпорация Panasonic объявила о разработке системы прямого метанольного топливного элемента (Direct Methanol Fuel Cell System), чей средний показатель выхода мощности может достигать 20 ватт. Прямой метанольный топливный элемент отличается тем, что топливо (метанол) в нем предварительно не разлагается с выделением водорода, а используется напрямую. Используя данную технологию, Panasonic ставит перед собой цель разработать 100 -ваттный портативный генератор и приступить к его испытаниям не позднее марта 2012 г. Такие метанольные топливные элементы большой мощности могут применяться, к примеру, для питания функциональных ноутбуков с относительно высоким энергопотреблением. Новая система топливных элементов отличается достаточной надежностью и долговечностью, а срок ее службы составляет 5000 часов при перемежающемся использовании в течение 8 часов в день. Следует отметить, что именно малая долговечность ранее была основным препятствием на пути коммерческого применения топливных элементов, поскольку из-за износа электродов падала их мощность.
2009. 12. 26, 14: 27 Новостная служба Ferra Японская корпорация Panasonic объявила о разработке системы прямого метанольного топливного элемента (Direct Methanol Fuel Cell System), чей средний показатель выхода мощности может достигать 20 ватт. Прямой метанольный топливный элемент отличается тем, что топливо (метанол) в нем предварительно не разлагается с выделением водорода, а используется напрямую. Используя данную технологию, Panasonic ставит перед собой цель разработать 100 -ваттный портативный генератор и приступить к его испытаниям не позднее марта 2012 г. Такие метанольные топливные элементы большой мощности могут применяться, к примеру, для питания функциональных ноутбуков с относительно высоким энергопотреблением. Новая система топливных элементов отличается достаточной надежностью и долговечностью, а срок ее службы составляет 5000 часов при перемежающемся использовании в течение 8 часов в день. Следует отметить, что именно малая долговечность ранее была основным препятствием на пути коммерческого применения топливных элементов, поскольку из-за износа электродов падала их мощность.
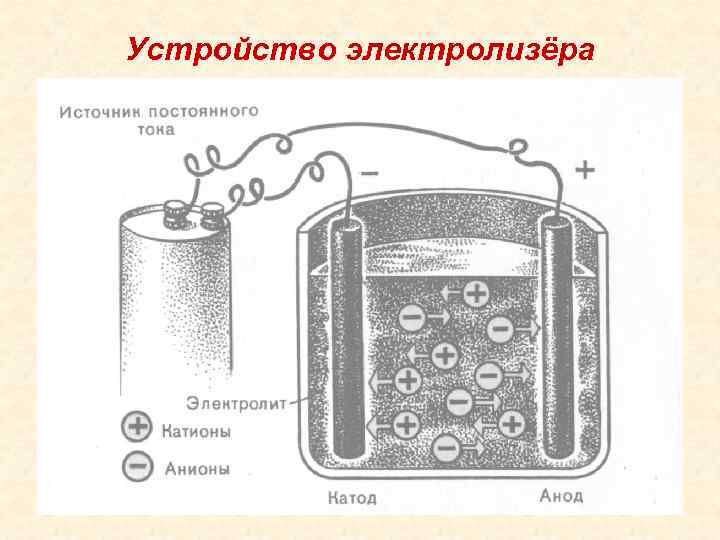 Устройство электролизёра
Устройство электролизёра
 Законы электролиза 1. Масса вещества, образующегося при электролизе в результате катодной или анодной реакции, пропорциональна количеству электричества, прошедшего через электролитическую ячейку. Майкл Фарадей 1791 -1867 2. Массы различных веществ, образующиеся при пропускании одного и того же количества электричества, пропорциональна эквивалентным массам этих веществ.
Законы электролиза 1. Масса вещества, образующегося при электролизе в результате катодной или анодной реакции, пропорциональна количеству электричества, прошедшего через электролитическую ячейку. Майкл Фарадей 1791 -1867 2. Массы различных веществ, образующиеся при пропускании одного и того же количества электричества, пропорциональна эквивалентным массам этих веществ.
 Электролиз
Электролиз
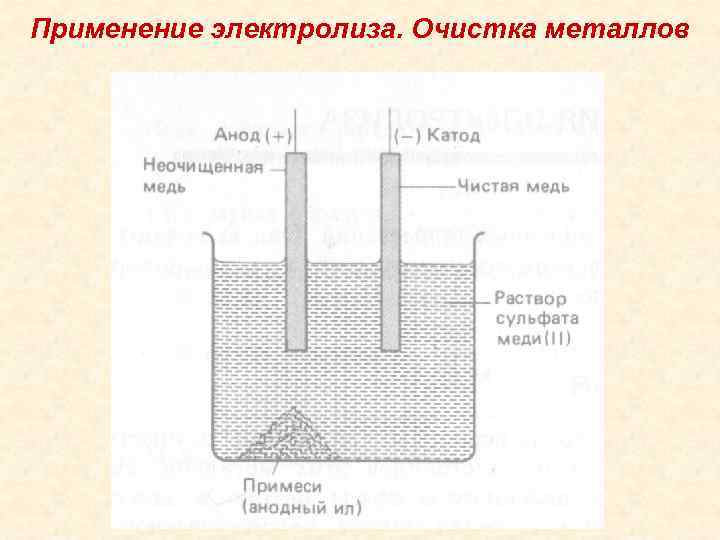 Применение электролиза. Очистка металлов
Применение электролиза. Очистка металлов

 Литий-ионный аккумулятор Первый литиево-ионный аккумулятор разработала корпорация Sony в 1991 году. Потребительские характеристики • Энергетическая плотность: 110 … 200 Вт*ч/кг • Внутреннее сопротивление: 150 … 250 м. Ом (для батареи 7, 2 В) • Число циклов заряд/разряд до потери 20% ёмкости: 500— 1000 • Время быстрого заряда: 2 -4 часа • Допустимый перезаряд: очень низкий • Саморазряд при комнатной температуре: 5 -10% в месяц • Напряжение максимальное: 4, 18. . 4, 20 В (полностью заряжен) • Напряжение минимальное: 2, 5. . 2, 75 В(полностью разряжен) • Диапазон рабочих температур: − 20 — +60 °C Принцип действия • анод: Li. Co. O 2 → Li 1 -x. Co. O 2 + x. Li+ + xe− • катод: С + x. Li+ + xe− → CLix • Оптимальные условия хранения Li-ion-аккумуляторов достигаются при 40%-ом заряде от ёмкости аккумулятора
Литий-ионный аккумулятор Первый литиево-ионный аккумулятор разработала корпорация Sony в 1991 году. Потребительские характеристики • Энергетическая плотность: 110 … 200 Вт*ч/кг • Внутреннее сопротивление: 150 … 250 м. Ом (для батареи 7, 2 В) • Число циклов заряд/разряд до потери 20% ёмкости: 500— 1000 • Время быстрого заряда: 2 -4 часа • Допустимый перезаряд: очень низкий • Саморазряд при комнатной температуре: 5 -10% в месяц • Напряжение максимальное: 4, 18. . 4, 20 В (полностью заряжен) • Напряжение минимальное: 2, 5. . 2, 75 В(полностью разряжен) • Диапазон рабочих температур: − 20 — +60 °C Принцип действия • анод: Li. Co. O 2 → Li 1 -x. Co. O 2 + x. Li+ + xe− • катод: С + x. Li+ + xe− → CLix • Оптимальные условия хранения Li-ion-аккумуляторов достигаются при 40%-ом заряде от ёмкости аккумулятора


