Электрический ток в жидкостях.ppt
- Количество слайдов: 9

Электрический ток в жидкостях Работу выполнили Ученики 10 б класса Воробьев Денис, Махмутова Ирина, Чижова Анастасия

Внутреннее строение в-ва для данной среды Электролит - это проводящая жидкость (растворы кислот , щелочей, солей и расплавленные соли). В растворах и расплавах электролитов (солей, кислот и щёлочей) перенос зарядов под действием электрического поля, осуществляется “+” и “-” ионами, которые движутся в противоположных направлениях.
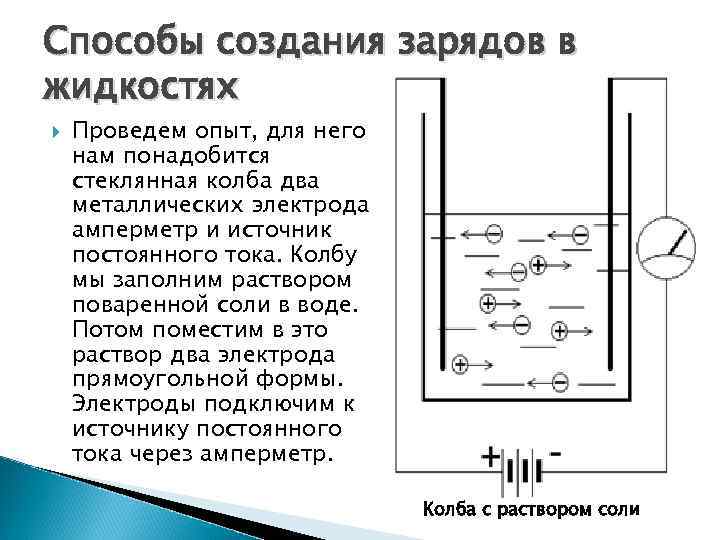
Способы создания зарядов в жидкостях Проведем опыт, для него нам понадобится стеклянная колба два металлических электрода амперметр и источник постоянного тока. Колбу мы заполним раствором поваренной соли в воде. Потом поместим в это раствор два электрода прямоугольной формы. Электроды подключим к источнику постоянного тока через амперметр. Колба с раствором соли

Законы Фарадея 1. Масса вещества, выделяемого на электроде, прямо пропорциональна электрическому заряду, прошедшему через электролит. где m - масса вещества, выделяющегося на электроде, k - электрохимический эквивалент, q - заряд, прошедший через электролит.

Законы Фарадея 2. Электрохимический эквивалент вещества прямо пропорционален его химическому эквиваленту. где М- молярная масса вещества, Fпостоянная Фарадея, z - валентность иона. Постоянная Фарадея численно равна заряду, который должен пройти через электролит, чтобы выделить из него массу вещества, численно равную химическому эквиваленту.

Объединенный закон Фарадея.
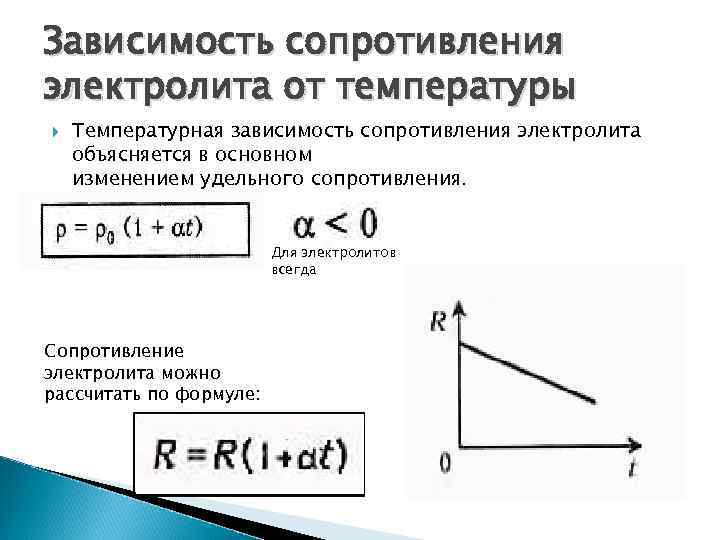
Зависимость сопротивления электролита от температуры Температурная зависимость сопротивления электролита объясняется в основном изменением удельного сопротивления. Для электролитов всегда Сопротивление электролита можно рассчитать по формуле:
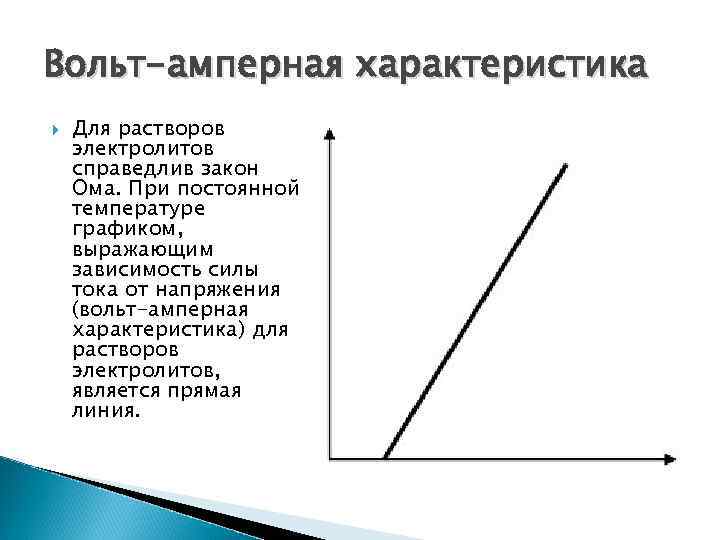
Вольт-амперная характеристика Для растворов электролитов справедлив закон Ома. При постоянной температуре графиком, выражающим зависимость силы тока от напряжения (вольт-амперная характеристика) для растворов электролитов, является прямая линия.

Применение электролиза а) электролитический метод получения чистых металлов (рафинирование). б) посредством электролиза можно покрыть металлические предметы слоем другого металла. в) гальванопластика- изготовление рельефной копии предмета. г) получение оксидных защитных пленок на металлах (анодирование) д) электрохимическая обработка поверхности металлического изделия (полировка) е) электрохимическое окрашивание металлов (медь, латунь, цинк) ж) очистка воды – удаление из нее растворимых примесей, в результате получается так называемая мягкая вода з) электрохимическая заточка режущих инструментов (хирургические ножи, бритвы)
Электрический ток в жидкостях.ppt