ЭМД в онкологии Ботк1 июнь 2012.ppt
- Количество слайдов: 102
 Экстракорпоральная детоксикация в онкологии Д. м. н. ГРОМОВА Е. Г.
Экстракорпоральная детоксикация в онкологии Д. м. н. ГРОМОВА Е. Г.
 • • • Причины развития органной недостаточности у онкологических больных Исходные нарушения гомеостаза (↓иммунитета, анемия, ↓алиментация, ↓кровоснабжение/нарушенный отток, и т. п. ) Предшествовавшие лучевая, гормональная, ПХТ →к макс. хир. радикализму→мультиорганные резекции Хирургическая травма: – Гипоксия (компрессия сосудов, массивная кровопотеря, гипотензия, отёк , краевой некроз по линии резекции…) – Повреждение критических органов-мишеней – Формирование органной недостаточности и СПОН – Сепсис Сопутствующая патология • соматическая • паранеопластический синдром
• • • Причины развития органной недостаточности у онкологических больных Исходные нарушения гомеостаза (↓иммунитета, анемия, ↓алиментация, ↓кровоснабжение/нарушенный отток, и т. п. ) Предшествовавшие лучевая, гормональная, ПХТ →к макс. хир. радикализму→мультиорганные резекции Хирургическая травма: – Гипоксия (компрессия сосудов, массивная кровопотеря, гипотензия, отёк , краевой некроз по линии резекции…) – Повреждение критических органов-мишеней – Формирование органной недостаточности и СПОН – Сепсис Сопутствующая патология • соматическая • паранеопластический синдром
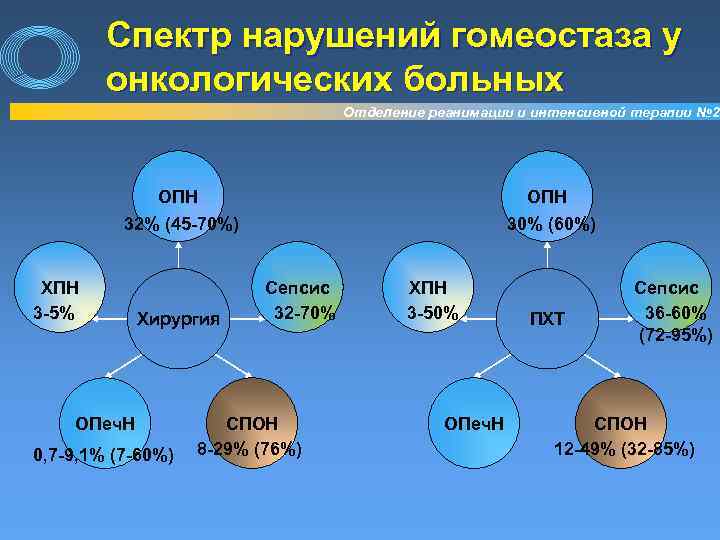 Спектр нарушений гомеостаза у онкологических больных Отделение реанимации и интенсивной терапии № 2 ОПН 32% (45 -70%) 30% (60%) ХПН 3 -5% Хирургия ОПеч. Н 0, 7 -9, 1% (7 -60%) Сепсис 32 -70% СПОН 8 -29% (76%) ХПН 3 -50% ОПеч. Н ПХТ Сепсис 36 -60% (72 -95%) СПОН 12 -49% (32 -85%)
Спектр нарушений гомеостаза у онкологических больных Отделение реанимации и интенсивной терапии № 2 ОПН 32% (45 -70%) 30% (60%) ХПН 3 -5% Хирургия ОПеч. Н 0, 7 -9, 1% (7 -60%) Сепсис 32 -70% СПОН 8 -29% (76%) ХПН 3 -50% ОПеч. Н ПХТ Сепсис 36 -60% (72 -95%) СПОН 12 -49% (32 -85%)
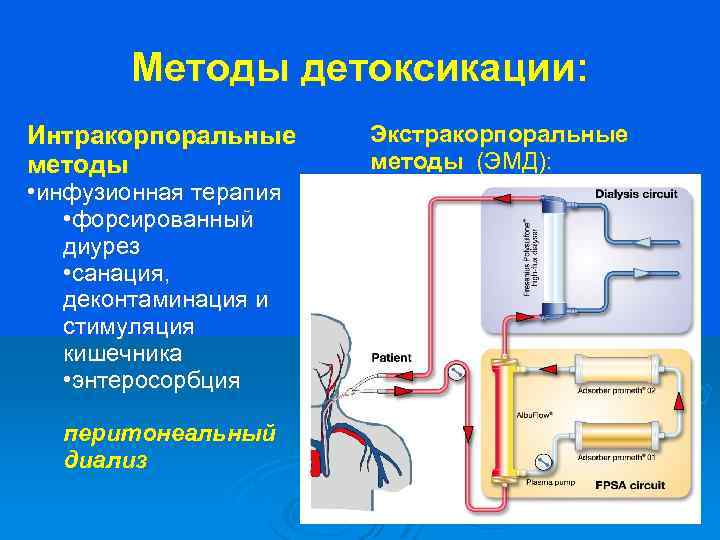 Методы детоксикации: Интракорпоральные методы • инфузионная терапия • форсированный диурез • санация, деконтаминация и стимуляция кишечника • энтеросорбция перитонеальный диализ Экстракорпоральные методы (ЭМД): количественное и качественное изменение • клеточного, • белкового, • водно-электролитного, ферментного, • газового состава крови путём обработки её вне организма
Методы детоксикации: Интракорпоральные методы • инфузионная терапия • форсированный диурез • санация, деконтаминация и стимуляция кишечника • энтеросорбция перитонеальный диализ Экстракорпоральные методы (ЭМД): количественное и качественное изменение • клеточного, • белкового, • водно-электролитного, ферментного, • газового состава крови путём обработки её вне организма
 Основные технологии ЭМД • • • Мембранные (ГД, и. УФ, ГДФ, ПФ, гемоксигенация) Центрифужные (ПА, ЛАФ, Тр. АФ, Эр. АФ) Сорбционные (ГС, ПС, ЛС, ксеноперфузия) Преципитационные (кислотная гепариновая преципитация, криоплазмосорбция, термопреципитация, термоплазмосорбция) Электромагнитные (фотомодификация, магнитная обработка, рентгеновское облучение) Электрохимические (непрямое ЭХО, озонирование)
Основные технологии ЭМД • • • Мембранные (ГД, и. УФ, ГДФ, ПФ, гемоксигенация) Центрифужные (ПА, ЛАФ, Тр. АФ, Эр. АФ) Сорбционные (ГС, ПС, ЛС, ксеноперфузия) Преципитационные (кислотная гепариновая преципитация, криоплазмосорбция, термопреципитация, термоплазмосорбция) Электромагнитные (фотомодификация, магнитная обработка, рентгеновское облучение) Электрохимические (непрямое ЭХО, озонирование)
 Основная суть медицины – в добавлении недостающего и изъятии избыточного. И тот, кто это делает наилучшим образом – лучший врач. Традиционно удаление • • • избыточного решалось на основе эмпирического опыта Хирургическое удаление Кровопускание Слабительные Рвотные Стимуляция потоотделения Сорбенты Изобрёл для пациентов свой фильтр для воды ( «Гиппократов рукав» ) - мешковину, через которую пропускалась кипячёная вода
Основная суть медицины – в добавлении недостающего и изъятии избыточного. И тот, кто это делает наилучшим образом – лучший врач. Традиционно удаление • • • избыточного решалось на основе эмпирического опыта Хирургическое удаление Кровопускание Слабительные Рвотные Стимуляция потоотделения Сорбенты Изобрёл для пациентов свой фильтр для воды ( «Гиппократов рукав» ) - мешковину, через которую пропускалась кипячёная вода
 Немного истории Если слепить из окажется воска сосуд и , пресной, ибо заткнув его землеобразное горлышко так , вещество, чья чтобы вода не примесь проникала создаёт внутрь , солёность, опустить в море , отделяется, то влага , словно через просочившаяся цедилку… в сосуд сквозь восковые стенки , Соч. , т. 3, с 486 Аристотель, 384 -322 до н. э.
Немного истории Если слепить из окажется воска сосуд и , пресной, ибо заткнув его землеобразное горлышко так , вещество, чья чтобы вода не примесь проникала создаёт внутрь , солёность, опустить в море , отделяется, то влага , словно через просочившаяся цедилку… в сосуд сквозь восковые стенки , Соч. , т. 3, с 486 Аристотель, 384 -322 до н. э.
 Немного истории Томас Грэхем (1805 -1869) шотландский химик труд «Осмотическая сила» Заложил в 1861 г. физические основы ГД Впервые описал способ изготовления полупроницаемых мембран из специально обработанного пергамента. Сконструировал диализатор в форме обруча С помощью данного метода стало возможно разделение коллоидных и кристаллоидных растворов. Процесс диффузии кристаллоидных растворов через пергаментную бумагу назвал диализом. Доказал связь размеров молекулы и скорости диффузии. Чем молекула больше, тем скорость диффузии ↓
Немного истории Томас Грэхем (1805 -1869) шотландский химик труд «Осмотическая сила» Заложил в 1861 г. физические основы ГД Впервые описал способ изготовления полупроницаемых мембран из специально обработанного пергамента. Сконструировал диализатор в форме обруча С помощью данного метода стало возможно разделение коллоидных и кристаллоидных растворов. Процесс диффузии кристаллоидных растворов через пергаментную бумагу назвал диализом. Доказал связь размеров молекулы и скорости диффузии. Чем молекула больше, тем скорость диффузии ↓
 Спустя 50 лет… • Создал первый аппарат для удаления растворенных в крови веществ. • Исследования проводил на бинефрэктомированных собаках. • Доказал возможность эффективного удаления из крови не связанных с белками азотистых соединений. • Малая площадь фильтрующей мембраны у аппарата не позволяла эффективно применять его для очищения крови у людей. Антикоагулянт - гирудин. • Но! низкая эффективность гирудина→ тромбоэмболические осложнения John Jacob Abel (1857 - 1938) (Abel J. , Rowntree L. , Turner B. , 1913)
Спустя 50 лет… • Создал первый аппарат для удаления растворенных в крови веществ. • Исследования проводил на бинефрэктомированных собаках. • Доказал возможность эффективного удаления из крови не связанных с белками азотистых соединений. • Малая площадь фильтрующей мембраны у аппарата не позволяла эффективно применять его для очищения крови у людей. Антикоагулянт - гирудин. • Но! низкая эффективность гирудина→ тромбоэмболические осложнения John Jacob Abel (1857 - 1938) (Abel J. , Rowntree L. , Turner B. , 1913)
 Прошло ещё 20 лет… Германия, октябрь 1924 г. Георг Хаас (1886 -1971) • Выполнил первый ГД больному с уремией. • В качестве антикоагулянта использовал очищенный гирудин, антигенные свойства которого не позволяли проводить диализ более 30 -60 минут. • 1927 г. -произвёл первую партию гепарина и впервые использовал его по время гемодиализа. • Разработал диализатор с большой S мембраны (1, 5 -2, 1 м 2) и адекватным распределением крови • Стал применять насос по крови и очищенную форму гепарина.
Прошло ещё 20 лет… Германия, октябрь 1924 г. Георг Хаас (1886 -1971) • Выполнил первый ГД больному с уремией. • В качестве антикоагулянта использовал очищенный гирудин, антигенные свойства которого не позволяли проводить диализ более 30 -60 минут. • 1927 г. -произвёл первую партию гепарина и впервые использовал его по время гемодиализа. • Разработал диализатор с большой S мембраны (1, 5 -2, 1 м 2) и адекватным распределением крови • Стал применять насос по крови и очищенную форму гепарина.
 И ещё почти 20 лет: первый успешный опыт гемодиализа • 1943 г. : первое клиническое Willem Johan Kolff (1911 -2009), Голландия применение диализа • 1944 г. : опыт лечения 16 больных с ОПН. • 1945 г: первый успешный результат с восстановлением почечной функции - у больного с ОПН п /S-амидов по поводу крупозной пневмонии (ОПН разрешилась п/1 ГД). • 1 -я больная, спасённая с помощью аппарата «искусственная почка» (1945 год) - 67 -летняя заключённая конц. лагеря с о. холециститом и ОПН (Ur=67 ммоль/л, t´ ГД =11 часов, восстановление ОПН – ч/з 7 дней, смерть от другой причины – ч/з 6 лет.
И ещё почти 20 лет: первый успешный опыт гемодиализа • 1943 г. : первое клиническое Willem Johan Kolff (1911 -2009), Голландия применение диализа • 1944 г. : опыт лечения 16 больных с ОПН. • 1945 г: первый успешный результат с восстановлением почечной функции - у больного с ОПН п /S-амидов по поводу крупозной пневмонии (ОПН разрешилась п/1 ГД). • 1 -я больная, спасённая с помощью аппарата «искусственная почка» (1945 год) - 67 -летняя заключённая конц. лагеря с о. холециститом и ОПН (Ur=67 ммоль/л, t´ ГД =11 часов, восстановление ОПН – ч/з 7 дней, смерть от другой причины – ч/з 6 лет.
 Первый аппарат для гемодиализа • 1943 г. : Кольф создал аппарат с большой поверхностью мембраны, пригодный для клинического применения. • Аппарат представлял собой цилиндрический барабан, на который наматывали целлофановую трубку длиной 3040 м. Нижняя часть вращающегося в горизонтальной плоскости барабана погружалась в стационарный резервуар, содержащий 70 л (позднее 100 л) диализирующего раствора.
Первый аппарат для гемодиализа • 1943 г. : Кольф создал аппарат с большой поверхностью мембраны, пригодный для клинического применения. • Аппарат представлял собой цилиндрический барабан, на который наматывали целлофановую трубку длиной 3040 м. Нижняя часть вращающегося в горизонтальной плоскости барабана погружалась в стационарный резервуар, содержащий 70 л (позднее 100 л) диализирующего раствора.
 Технический прогресс 1945 -1999
Технический прогресс 1945 -1999
 Современное оборудование для ЭКД
Современное оборудование для ЭКД
 Современные технологии ЭКД Толщина стенки 35µм Размер пор: 0, 1 - 0, 3 нм 1µм внутренний слой стенки Внутренний диаметр 185µм Устройства для селективной сорбции
Современные технологии ЭКД Толщина стенки 35µм Размер пор: 0, 1 - 0, 3 нм 1µм внутренний слой стенки Внутренний диаметр 185µм Устройства для селективной сорбции
 Начало эпохи хронического гемодиализа 1. 2. 3. 1960 год: Белдинг Скрибнер и Вейн Квинтон: артерио-венозный шунт. имплантация в лучевую артерию и подкожную вену двух тонкостенных тефлоновых трубок, соединенных с трубками из силиконизированной резины, расположенных частично подкожно, а частично снаружи. Наружные концы трубок соединялись изогнутым тефлоновым трубчатым переходником, который на время проведения ГД удалялся, а к трубкам подключался диализатор. 1970 г: следующий шаг (нефрологи Чимино и Брешиа - авторство оспаривается) - артериовенозная фистула, которая по настоящее время считается самым надежным видом сосудистого доступа
Начало эпохи хронического гемодиализа 1. 2. 3. 1960 год: Белдинг Скрибнер и Вейн Квинтон: артерио-венозный шунт. имплантация в лучевую артерию и подкожную вену двух тонкостенных тефлоновых трубок, соединенных с трубками из силиконизированной резины, расположенных частично подкожно, а частично снаружи. Наружные концы трубок соединялись изогнутым тефлоновым трубчатым переходником, который на время проведения ГД удалялся, а к трубкам подключался диализатор. 1970 г: следующий шаг (нефрологи Чимино и Брешиа - авторство оспаривается) - артериовенозная фистула, которая по настоящее время считается самым надежным видом сосудистого доступа
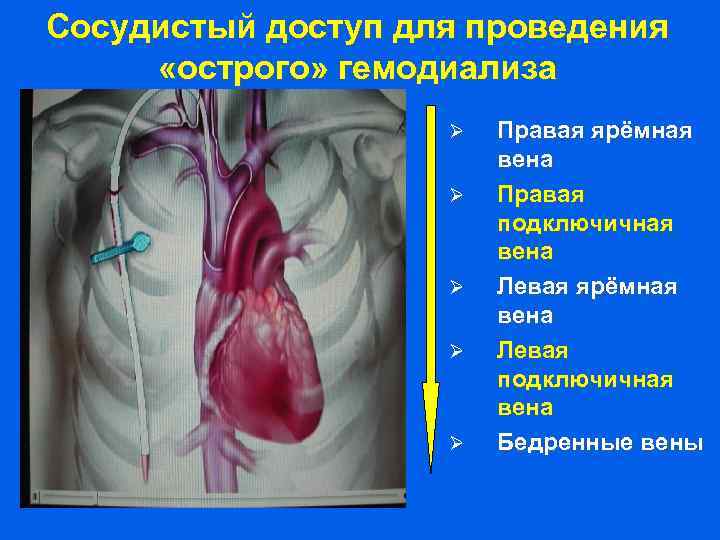 Сосудистый доступ для проведения «острого» гемодиализа Правая ярёмная вена Правая подключичная вена Левая ярёмная вена Левая подключичная вена Бедренные вены
Сосудистый доступ для проведения «острого» гемодиализа Правая ярёмная вена Правая подключичная вена Левая ярёмная вена Левая подключичная вена Бедренные вены
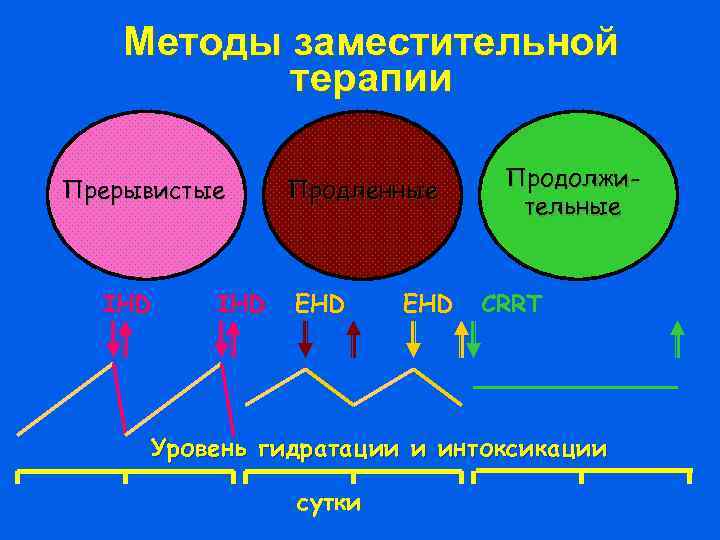 Методы заместительной терапии Прерывистые IHD Продленные EHD Продолжительные CRRT Уровень гидратации и интоксикации сутки
Методы заместительной терапии Прерывистые IHD Продленные EHD Продолжительные CRRT Уровень гидратации и интоксикации сутки
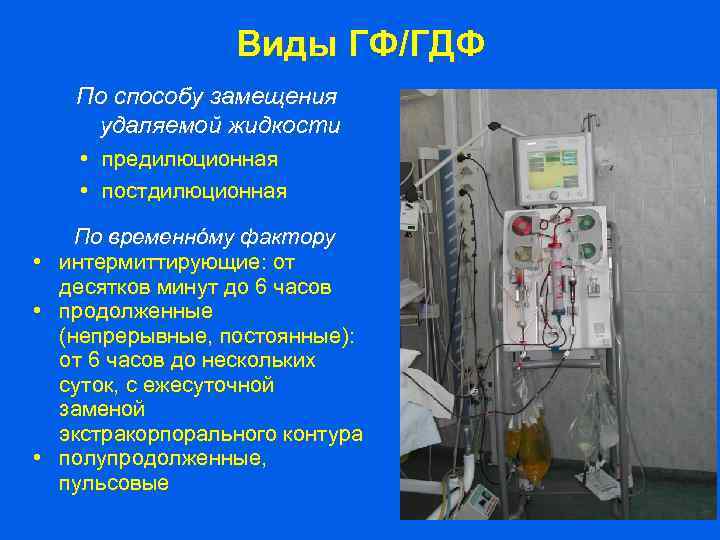 Виды ГФ/ГДФ По способу замещения удаляемой жидкости • предилюционная • постдилюционная По временнóму фактору • интермиттирующие: от десятков минут до 6 часов • продолженные (непрерывные, постоянные): от 6 часов до нескольких суток, с ежесуточной заменой экстракорпорального контура • полупродолженные, пульсовые
Виды ГФ/ГДФ По способу замещения удаляемой жидкости • предилюционная • постдилюционная По временнóму фактору • интермиттирующие: от десятков минут до 6 часов • продолженные (непрерывные, постоянные): от 6 часов до нескольких суток, с ежесуточной заменой экстракорпорального контура • полупродолженные, пульсовые
 Острая почечная недостаточность
Острая почечная недостаточность
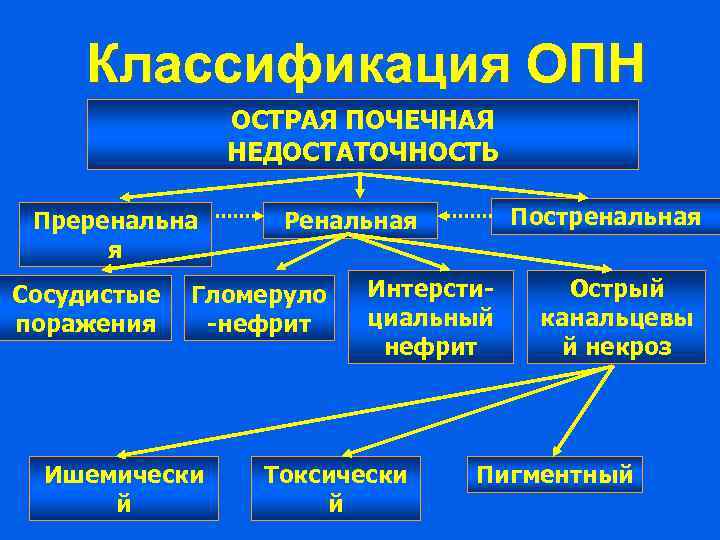 Классификация ОПН ОСТРАЯ ПОЧЕЧНАЯ НЕДОСТАТОЧНОСТЬ Преренальна я Сосудистые поражения Гломеруло -нефрит Ишемически й Постренальная Ренальная Интерстициальный нефрит Токсически й Острый канальцевы й некроз Пигментный
Классификация ОПН ОСТРАЯ ПОЧЕЧНАЯ НЕДОСТАТОЧНОСТЬ Преренальна я Сосудистые поражения Гломеруло -нефрит Ишемически й Постренальная Ренальная Интерстициальный нефрит Токсически й Острый канальцевы й некроз Пигментный
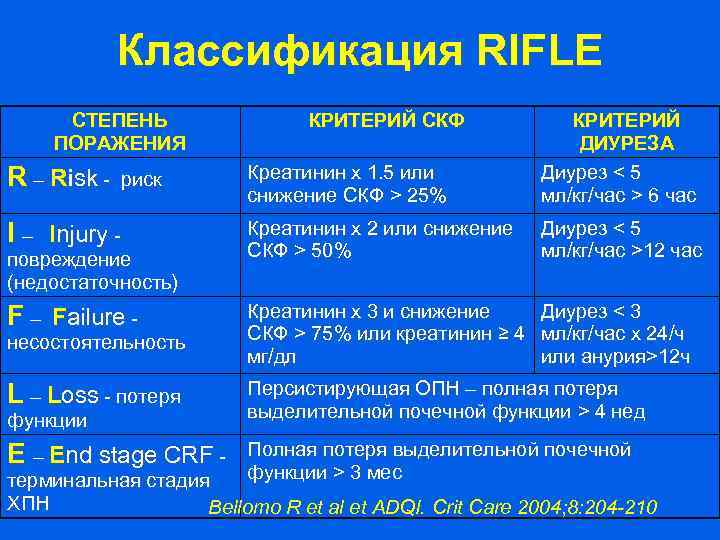 Классификация RIFLE СТЕПЕНЬ ПОРАЖЕНИЯ Креатинин х 1. 5 или снижение СКФ > 25% КРИТЕРИЙ ДИУРЕЗА Диурез < 5 мл/кг/час > 6 час I – Injury - Креатинин х 2 или снижение СКФ > 50% Диурез < 5 мл/кг/час >12 час F – Failure - несостоятельность Креатинин х 3 и снижение Диурез < 3 СКФ > 75% или креатинин ≥ 4 мл/кг/час х 24/ч мг/дл или анурия>12 ч L – Loss - потеря Персистирующая ОПН – полная потеря выделительной почечной функции > 4 нед E – End stage CRF - Полная потеря выделительной почечной функции > 3 мес R – Risk - риск повреждение (недостаточность) функции КРИТЕРИЙ СКФ терминальная стадия ХПН Bellomo R et al et ADQI. Crit Care 2004; 8: 204 -210
Классификация RIFLE СТЕПЕНЬ ПОРАЖЕНИЯ Креатинин х 1. 5 или снижение СКФ > 25% КРИТЕРИЙ ДИУРЕЗА Диурез < 5 мл/кг/час > 6 час I – Injury - Креатинин х 2 или снижение СКФ > 50% Диурез < 5 мл/кг/час >12 час F – Failure - несостоятельность Креатинин х 3 и снижение Диурез < 3 СКФ > 75% или креатинин ≥ 4 мл/кг/час х 24/ч мг/дл или анурия>12 ч L – Loss - потеря Персистирующая ОПН – полная потеря выделительной почечной функции > 4 нед E – End stage CRF - Полная потеря выделительной почечной функции > 3 мес R – Risk - риск повреждение (недостаточность) функции КРИТЕРИЙ СКФ терминальная стадия ХПН Bellomo R et al et ADQI. Crit Care 2004; 8: 204 -210
 Острая почечная недостаточность Частота ОПН: 5 -10% пациентов ОИТ с ОПН нуждаются в ЗПТ Летальность=60, 3%-71, 6% Диализная зависимость – у 13, 8% выписанных больных • США: 1 -5% от всех госпитализированных (50. 000/год); • 7 -23% пациентов ОРИТ (Let→ 86%) Uchino S, Kellum JA, Bellomo R, et. al. , 2005 • Европа: 52 -203/млн Weisbord SD, Palevsky PM. 2006 населения/год Soubrier S, Leroy O, Devos P, et al. 2006 • Россия: сводных данных нет; • Москва: 172/млн населения/год
Острая почечная недостаточность Частота ОПН: 5 -10% пациентов ОИТ с ОПН нуждаются в ЗПТ Летальность=60, 3%-71, 6% Диализная зависимость – у 13, 8% выписанных больных • США: 1 -5% от всех госпитализированных (50. 000/год); • 7 -23% пациентов ОРИТ (Let→ 86%) Uchino S, Kellum JA, Bellomo R, et. al. , 2005 • Европа: 52 -203/млн Weisbord SD, Palevsky PM. 2006 населения/год Soubrier S, Leroy O, Devos P, et al. 2006 • Россия: сводных данных нет; • Москва: 172/млн населения/год
 Летальность при ОПН Летальность больных с ОПН=25 -80% и не снижается за последние 30 лет q Факторы, определяющие летальность: q • • Мужской пол Олигурия Механическая вентиляция Острый инфаркт миокарда Инсульт Хроническая иммуносупрессия Предшествующие нарушения питания Гипоальбуминемия Возраст Летальность гематологических больных, нуждающихся в ЗПТ, коррелирует с числом поражённых органов от 36% при недостаточности 1 органа до 83% при поражении 3 органов. •
Летальность при ОПН Летальность больных с ОПН=25 -80% и не снижается за последние 30 лет q Факторы, определяющие летальность: q • • Мужской пол Олигурия Механическая вентиляция Острый инфаркт миокарда Инсульт Хроническая иммуносупрессия Предшествующие нарушения питания Гипоальбуминемия Возраст Летальность гематологических больных, нуждающихся в ЗПТ, коррелирует с числом поражённых органов от 36% при недостаточности 1 органа до 83% при поражении 3 органов. •
 Необходимость в Гемодиализе у онкологических больных Проспективное 56 -недельное иссл. в Национальном институте рака (n=975): у 32 % онкологических больных (солидные/гематологические=3/1), поступающих в ОИТ, развивается ОПН. Из них 32 % требуется ЗПТ. Диализная зависимость – у 6% больных Полное восстановление функции почек -у 82%, частичное - у 12%, Márcio Soares, Jorge I. F. Salluh, Marilia S. et al. , 2006 1997 -2002 г. , из 222 онкогематологических пациентов ОРИТ 22, 5% нуждались в ЗПТ. D. Benoit et al. , 2005, Gent, Belg. Летальность=50 -51, 3% Darmon M, Thiery G, Ciroldi M, et al. 2007
Необходимость в Гемодиализе у онкологических больных Проспективное 56 -недельное иссл. в Национальном институте рака (n=975): у 32 % онкологических больных (солидные/гематологические=3/1), поступающих в ОИТ, развивается ОПН. Из них 32 % требуется ЗПТ. Диализная зависимость – у 6% больных Полное восстановление функции почек -у 82%, частичное - у 12%, Márcio Soares, Jorge I. F. Salluh, Marilia S. et al. , 2006 1997 -2002 г. , из 222 онкогематологических пациентов ОРИТ 22, 5% нуждались в ЗПТ. D. Benoit et al. , 2005, Gent, Belg. Летальность=50 -51, 3% Darmon M, Thiery G, Ciroldi M, et al. 2007
 Преренальные причины ОПН в онкологии • • • Гиповолемия/критическая гипотензия (кровотечение, экстраренальные потери при рвоте/диарее, экстравазация жидкости: асцит, перитонит, панкреатит) Периферическая вазодилатация: сепсис, анафилаксия, анестетики, интра- и п/о шок Низкий сердечный выброс : сдавление опухолью извне (ЛГМ, опухоли средостения), гидроторакс, гидро- и гемоперикард, ТЭЛА Экстраренальная билатеральная сосудистая окклюзия Функциональные нарушения почечного кровотока: гепато-ренальный синдром, медикаментозное снижение синтеза простагландинов (НПВС)
Преренальные причины ОПН в онкологии • • • Гиповолемия/критическая гипотензия (кровотечение, экстраренальные потери при рвоте/диарее, экстравазация жидкости: асцит, перитонит, панкреатит) Периферическая вазодилатация: сепсис, анафилаксия, анестетики, интра- и п/о шок Низкий сердечный выброс : сдавление опухолью извне (ЛГМ, опухоли средостения), гидроторакс, гидро- и гемоперикард, ТЭЛА Экстраренальная билатеральная сосудистая окклюзия Функциональные нарушения почечного кровотока: гепато-ренальный синдром, медикаментозное снижение синтеза простагландинов (НПВС)
 Ренальные причины ОПН в онкологии Связанные с опухолью: • • Гломерулярные: гломерулонефрит, ГУС Тубулярные: ишемический ОТН, экзогенные нефротоксины (противоопухолевые, а/б, радиоконтрастные препараты, анестетики), Ig-лёгкие цепи, Са, Р, мочевая кислота, ксантин Интерстициальные: лекарственно индуцированные тубулоинтерстициальные нефриты, острый пиелонефрит, инфильтрация почек опухолью (рак почки, лимфома, лейкоз); амилоидоз, лучевая нефропатия Нарушения внутрипочечного кровотока: ДВС, ГУС, злокачественная гипертензия (опухоли надпочечников, феохромоцитома), васкулиты
Ренальные причины ОПН в онкологии Связанные с опухолью: • • Гломерулярные: гломерулонефрит, ГУС Тубулярные: ишемический ОТН, экзогенные нефротоксины (противоопухолевые, а/б, радиоконтрастные препараты, анестетики), Ig-лёгкие цепи, Са, Р, мочевая кислота, ксантин Интерстициальные: лекарственно индуцированные тубулоинтерстициальные нефриты, острый пиелонефрит, инфильтрация почек опухолью (рак почки, лимфома, лейкоз); амилоидоз, лучевая нефропатия Нарушения внутрипочечного кровотока: ДВС, ГУС, злокачественная гипертензия (опухоли надпочечников, феохромоцитома), васкулиты
 Ренальные причины ОПН в онкологии Связанные с противоопухолевым лечением: • • • (би)нефрэктомия/резекция единственной функционирующей почки; Нефротоксичная ПХТ: адриамицин, митомицин, памидронат → прямое повреждающее действие на клубочки; цисплатин, метотрексат, ифосфамид, золедронат → ренотубулярную преципитацию → обструкцию, гломерулярные и микрососудистые нарушения, ОПН п/ЦП дозозависима; характерны гипокалиемия, гипомагниемия, полиурия. Митомицин, флюорурацил, гемцитабин →ГУС (Let при отсутствии ИТ=50 -100%). Антибактериальная/противогрибковая терапия НПВС Гиперосмолярные R-контрастные средства Тубулоинтерстициальные нефриты (при
Ренальные причины ОПН в онкологии Связанные с противоопухолевым лечением: • • • (би)нефрэктомия/резекция единственной функционирующей почки; Нефротоксичная ПХТ: адриамицин, митомицин, памидронат → прямое повреждающее действие на клубочки; цисплатин, метотрексат, ифосфамид, золедронат → ренотубулярную преципитацию → обструкцию, гломерулярные и микрососудистые нарушения, ОПН п/ЦП дозозависима; характерны гипокалиемия, гипомагниемия, полиурия. Митомицин, флюорурацил, гемцитабин →ГУС (Let при отсутствии ИТ=50 -100%). Антибактериальная/противогрибковая терапия НПВС Гиперосмолярные R-контрастные средства Тубулоинтерстициальные нефриты (при
 Постренальные причины ОПН в онкологии Связанные с опухолью: • Обструкция мочевыводящих путей • Высокое внутрибрюшное давление (асцит) Связанные с противоопухолевым лечением: • Нефролитиаз (вследствие гиперкальциемии и гиперурикемии) • Тампонада мочевого пузыря
Постренальные причины ОПН в онкологии Связанные с опухолью: • Обструкция мочевыводящих путей • Высокое внутрибрюшное давление (асцит) Связанные с противоопухолевым лечением: • Нефролитиаз (вследствие гиперкальциемии и гиперурикемии) • Тампонада мочевого пузыря
 Общие критерии начала ЗПТ при ОПН Анурия/Олигурия (< 400 мл/сут) Ureabl > 25 ммоль/л Crсыв > 600 мкмоль/л/ ↑ 100 мкмоль/сут Гиперкалиемия (К+ > 6, 0 ммоль/л+ЭКГ Отек лёгких, резистентный к диуретикам Периферические отёки Метаболический ацидоз: ↓р. Нарт < 7, 2/HCO 3 - <15 Уремическая энцефалопатия Уремический перикардит Дизнатриемия (115>Na>160 ммоль/л) Передозировка диализирующихся лекарственных препаратов • Неконтролируемая гипертермия (Т°>39, 5°) • • •
Общие критерии начала ЗПТ при ОПН Анурия/Олигурия (< 400 мл/сут) Ureabl > 25 ммоль/л Crсыв > 600 мкмоль/л/ ↑ 100 мкмоль/сут Гиперкалиемия (К+ > 6, 0 ммоль/л+ЭКГ Отек лёгких, резистентный к диуретикам Периферические отёки Метаболический ацидоз: ↓р. Нарт < 7, 2/HCO 3 - <15 Уремическая энцефалопатия Уремический перикардит Дизнатриемия (115>Na>160 ммоль/л) Передозировка диализирующихся лекарственных препаратов • Неконтролируемая гипертермия (Т°>39, 5°) • • •
 ОПН после резекции единственной почки Больная С. , 51 год. Ds: Рак правой почки T 4 N 0 M 1, Cостояние после нефрэктомии справа в 1998 г. ХПН I ст. Множественные метастазы в левую почку, правый надпочечник, печень. Варианты лечения Биотерапия? ПХТ? 2. Нефрэктомия → прогр. ГД) 3. Органосохраняющая операция: удаление метастазов с неизбежным развитием п/о ОПН) 1. Решение: Хирургическое лечение Экстракорпоральная резекция единственной почки с аутотрансплантацией в правую подвздошную область, резекция правого надпочечника, овариоэктомии слева, атипичная резекция печени
ОПН после резекции единственной почки Больная С. , 51 год. Ds: Рак правой почки T 4 N 0 M 1, Cостояние после нефрэктомии справа в 1998 г. ХПН I ст. Множественные метастазы в левую почку, правый надпочечник, печень. Варианты лечения Биотерапия? ПХТ? 2. Нефрэктомия → прогр. ГД) 3. Органосохраняющая операция: удаление метастазов с неизбежным развитием п/о ОПН) 1. Решение: Хирургическое лечение Экстракорпоральная резекция единственной почки с аутотрансплантацией в правую подвздошную область, резекция правого надпочечника, овариоэктомии слева, атипичная резекция печени
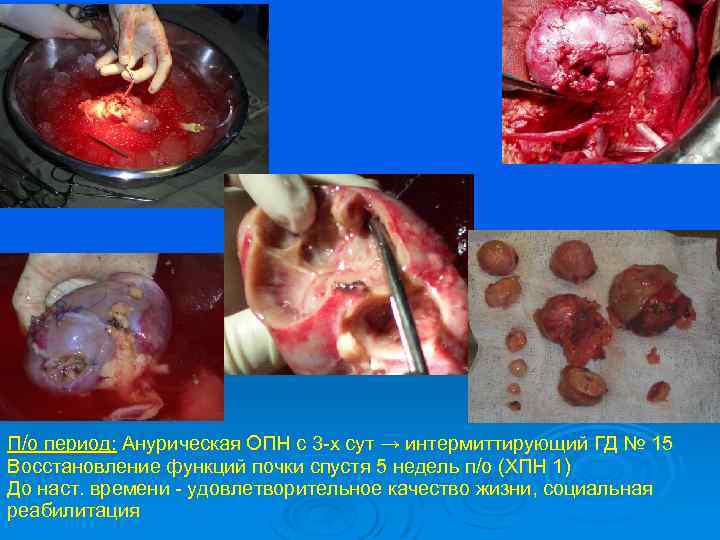 П/о период: Анурическая ОПН с 3 -х сут → интермиттирующий ГД № 15 Восстановление функций почки спустя 5 недель п/о (ХПН 1) До наст. времени - удовлетворительное качество жизни, социальная реабилитация
П/о период: Анурическая ОПН с 3 -х сут → интермиттирующий ГД № 15 Восстановление функций почки спустя 5 недель п/о (ХПН 1) До наст. времени - удовлетворительное качество жизни, социальная реабилитация
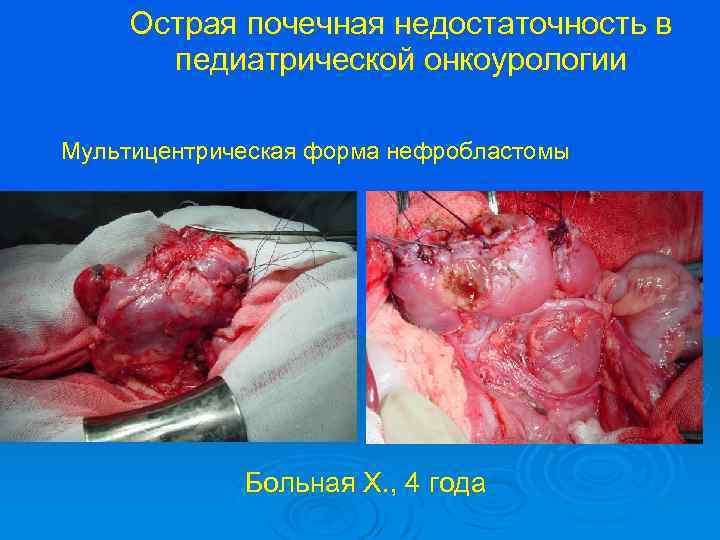 Острая почечная недостаточность в педиатрической онкоурологии Мультицентрическая форма нефробластомы Больная Х. , 4 года
Острая почечная недостаточность в педиатрической онкоурологии Мультицентрическая форма нефробластомы Больная Х. , 4 года
 Острая почечная недостаточность в педиатрической онкоурологии Мультицентрическая форма нефробластомы Больная Х. , 4 года
Острая почечная недостаточность в педиатрической онкоурологии Мультицентрическая форма нефробластомы Больная Х. , 4 года
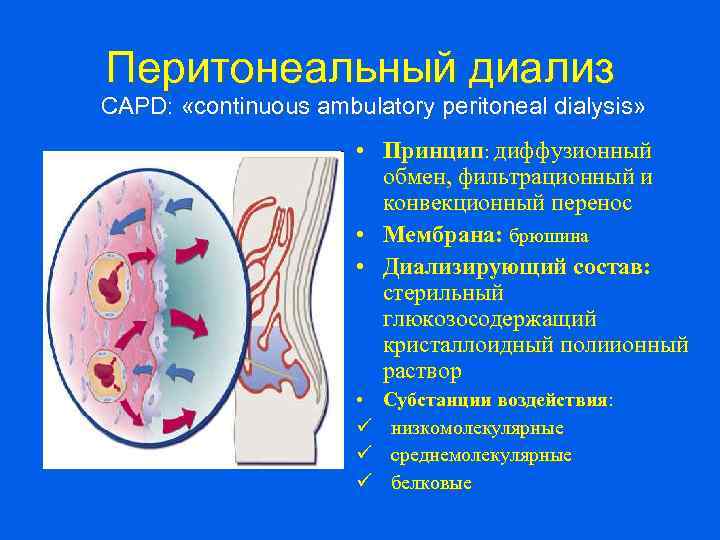 Перитонеальный диализ CAPD: «continuous ambulatory peritoneal dialysis» • Принцип: диффузионный обмен, фильтрационный и конвекционный перенос • Мембрана: брюшина • Диализирующий состав: стерильный глюкозосодержащий кристаллоидный полиионный раствор • ü ü ü Субстанции воздействия: низкомолекулярные среднемолекулярные белковые
Перитонеальный диализ CAPD: «continuous ambulatory peritoneal dialysis» • Принцип: диффузионный обмен, фильтрационный и конвекционный перенос • Мембрана: брюшина • Диализирующий состав: стерильный глюкозосодержащий кристаллоидный полиионный раствор • ü ü ü Субстанции воздействия: низкомолекулярные среднемолекулярные белковые
 За и против ПД + • • Самостоятельность Высвобождение времени Домашние условия Отсутствие необходимости в сосудистом доступе ─ • Перитонит • Неконтролируемое потребление глюкозы • Домашние условия • Невозможность программирования параметров лечения • Меньшая эффективность
За и против ПД + • • Самостоятельность Высвобождение времени Домашние условия Отсутствие необходимости в сосудистом доступе ─ • Перитонит • Неконтролируемое потребление глюкозы • Домашние условия • Невозможность программирования параметров лечения • Меньшая эффективность
 Перитонеальный диализ применяется редко: • эффективность выведения токсинов и жидкости ниже, чем при ГД • ОПН нередко развивается у больных с интраабдоминальной патологией или после хирургических операций на органах брюшной полости • увеличение внутрибрюшного давления при ПД может нарушить функцию легких и, следовательно, ПД опасен при остром повреждении легких • использование концентрированных растворов глюкозы может нарушить метаболические процессы Т. о. , ПД – резервный метод лечения ОПН, при невозможности применения других методов
Перитонеальный диализ применяется редко: • эффективность выведения токсинов и жидкости ниже, чем при ГД • ОПН нередко развивается у больных с интраабдоминальной патологией или после хирургических операций на органах брюшной полости • увеличение внутрибрюшного давления при ПД может нарушить функцию легких и, следовательно, ПД опасен при остром повреждении легких • использование концентрированных растворов глюкозы может нарушить метаболические процессы Т. о. , ПД – резервный метод лечения ОПН, при невозможности применения других методов
 Показания к ЭМД при синдромной патологии с ОПН • • Синдром массивного лизиса опухоли Острый гемолиз Паранеопластический синдром Гипервискозный синдром Гепато-ренальный синдром Сепсис/СПОН Непереносимость/передозировка лекарственных препаратов
Показания к ЭМД при синдромной патологии с ОПН • • Синдром массивного лизиса опухоли Острый гемолиз Паранеопластический синдром Гипервискозный синдром Гепато-ренальный синдром Сепсис/СПОН Непереносимость/передозировка лекарственных препаратов
 Методы ЭКЛ при синдромной ОПН Гемофильтрация Принципы фильтрации и конвекции: перенос воды, низко- и среднемолекулярных (до 50 KD) субстанций из крови через полупроницаемую мембрану с высокой гидравлической проницаемостью, с в/в возмещением ультрафильтрата сбалансированным полиионным раствором. Моделирует процессы фильтрации и реабсорбции, здоровой почки Гемодиафильтрация Сочетание ГД и ГФ. Эффективна при лечении ПН с гиперкатаболизмом. 2 одновременных процесса: 1. диффузия токсических веществ через мембрану в диализирующий раствор по градиенту концентраций; 2. конвективный транспорт воды и растворённых в ней токсических веществ через мембрану
Методы ЭКЛ при синдромной ОПН Гемофильтрация Принципы фильтрации и конвекции: перенос воды, низко- и среднемолекулярных (до 50 KD) субстанций из крови через полупроницаемую мембрану с высокой гидравлической проницаемостью, с в/в возмещением ультрафильтрата сбалансированным полиионным раствором. Моделирует процессы фильтрации и реабсорбции, здоровой почки Гемодиафильтрация Сочетание ГД и ГФ. Эффективна при лечении ПН с гиперкатаболизмом. 2 одновременных процесса: 1. диффузия токсических веществ через мембрану в диализирующий раствор по градиенту концентраций; 2. конвективный транспорт воды и растворённых в ней токсических веществ через мембрану
 Синдром лизиса опухоли обусловлен гибелью большого количества быстро пролиферирующих опухолевых клеток, выходом внутриклеточного содержимого в экстрацеллюлярное пространство с развитием: • гиперурикемии • гиперкалиемии • гиперфосфатемии • вторичной гипокальциемии • метаболического ацидоза, непропорционального ПН • ОПН (как правило, олигурической)
Синдром лизиса опухоли обусловлен гибелью большого количества быстро пролиферирующих опухолевых клеток, выходом внутриклеточного содержимого в экстрацеллюлярное пространство с развитием: • гиперурикемии • гиперкалиемии • гиперфосфатемии • вторичной гипокальциемии • метаболического ацидоза, непропорционального ПН • ОПН (как правило, олигурической)
 Синдром лизиса опухоли Противоопухолевые препараты, ответственные за развитие СЛО Факторы развития СЛО • • Спонтанное ХТ (в т. ч. монотерапия кортикостероидами) Эмболизация сосудов Радиочастотная аблация Моноклональные антитела Интерферон Лучевая терапия ВДХТ с трансплантацией стволовых клеток периферической крови • • • Флюдарабин Митоксантрон 6 -Меркаптопурин Метотрексат Комбинации ХТС
Синдром лизиса опухоли Противоопухолевые препараты, ответственные за развитие СЛО Факторы развития СЛО • • Спонтанное ХТ (в т. ч. монотерапия кортикостероидами) Эмболизация сосудов Радиочастотная аблация Моноклональные антитела Интерферон Лучевая терапия ВДХТ с трансплантацией стволовых клеток периферической крови • • • Флюдарабин Митоксантрон 6 -Меркаптопурин Метотрексат Комбинации ХТС
 Синдром лизиса опухоли Впервые описан у пациентов с лимфомой Бёркитта, внезапно умерших после ХТ. Развивается у больных • Лимфомой Бёркитта (42%) • ОЛЛ (гиперлейкоцитоз!) • Хр лейкозами • Раком желудка • Раком лёгкого (МК/НМК) • Раком молочной железы • Раком яичников • Медуллобластомами Факторы риска • Массивное опухолевое поражение+ожидаемая ↑ чувствительность к лечению • Большие конгломераты л/у • Гиперлейкоцитоз • ОПН/ХПН Предикторы: Уровни ЛДГ, мочевой кислоты, креатинина до начала лечения. ↑ЛДГ+ ↑Р+↓диурез→показание для превентивной ЭКД (Kopecna L. , Dolezel Z. et al. , 2002) Характеристики СЛО: быстрое (< 72 часов) развитие тяжёлое течение летальность 17 -70%
Синдром лизиса опухоли Впервые описан у пациентов с лимфомой Бёркитта, внезапно умерших после ХТ. Развивается у больных • Лимфомой Бёркитта (42%) • ОЛЛ (гиперлейкоцитоз!) • Хр лейкозами • Раком желудка • Раком лёгкого (МК/НМК) • Раком молочной железы • Раком яичников • Медуллобластомами Факторы риска • Массивное опухолевое поражение+ожидаемая ↑ чувствительность к лечению • Большие конгломераты л/у • Гиперлейкоцитоз • ОПН/ХПН Предикторы: Уровни ЛДГ, мочевой кислоты, креатинина до начала лечения. ↑ЛДГ+ ↑Р+↓диурез→показание для превентивной ЭКД (Kopecna L. , Dolezel Z. et al. , 2002) Характеристики СЛО: быстрое (< 72 часов) развитие тяжёлое течение летальность 17 -70%
 Симптомы развивающегося СЛО Неспецифические • • • Тошнота Рвота Мышечная слабость Артралгии Потемнение мочи Обусловленные метаболическими и электролитными нарушениями ССС: гипотензия, брадикардия, аритмии (!внезапная смерть!) Нервная система Н/мышечная раздражимость, судороги→тетания→эпилептиформные припадки; нарушения сознания (кома) ЖКТ: тошнота, рвота, диаррея МВС: ОПН, лактат-ацидоз Органы зрения: отёк диска зрительного нерва, ретробульбарный неврит с потерей зрения
Симптомы развивающегося СЛО Неспецифические • • • Тошнота Рвота Мышечная слабость Артралгии Потемнение мочи Обусловленные метаболическими и электролитными нарушениями ССС: гипотензия, брадикардия, аритмии (!внезапная смерть!) Нервная система Н/мышечная раздражимость, судороги→тетания→эпилептиформные припадки; нарушения сознания (кома) ЖКТ: тошнота, рвота, диаррея МВС: ОПН, лактат-ацидоз Органы зрения: отёк диска зрительного нерва, ретробульбарный неврит с потерей зрения
 Лабораторные ориентиры СЛО • • • повышение уровня мочевой кислоты ≥ 476 мкмоль/л; гиперкалиемия ≥ 6 ммоль/л; гиперфосфатемия ≥ 2, 1 ммоль/л у детей и ≥ 1, 45 ммоль/л у взрослых; гипокальциемия ≤ 1, 75 ммоль/л, либо изменение каждого из показателей на 25% от нормальных значений.
Лабораторные ориентиры СЛО • • • повышение уровня мочевой кислоты ≥ 476 мкмоль/л; гиперкалиемия ≥ 6 ммоль/л; гиперфосфатемия ≥ 2, 1 ммоль/л у детей и ≥ 1, 45 ммоль/л у взрослых; гипокальциемия ≤ 1, 75 ммоль/л, либо изменение каждого из показателей на 25% от нормальных значений.
 Профилактика и консервативная терапия СЛО • • • Гидратация до 3 л/м 2/ сут. ; диурез от 100 мл/ч независимо от применения диуретиков (0, 3 -1 -2 -3 мг/кг в/в каждые 4 -6 час) Ингибиторы ксантин-оксидазы (аллопуринол) 100 -300 (до 900!) мг/сут (алоприм 400 мг/м 2) Алкализация крови в/в введением Na. HCO 3 – до достижения р. Н мочи = 7, 1 -7, 5 Рекомбинантная урат-окидаза/разбуриказа, 200 мг/кг –предупреждение уратной нефропатии Лечение гиперкалиемии (приём ионообменных смол, в/в инсулин, декстроза, глюконат Са) При сочетании гиперфосфатемии и гипокальциемии – Са ацетат или Са бикарбонат per os! (внутривенное введение может вызвать преципитацию фосфата Са!)
Профилактика и консервативная терапия СЛО • • • Гидратация до 3 л/м 2/ сут. ; диурез от 100 мл/ч независимо от применения диуретиков (0, 3 -1 -2 -3 мг/кг в/в каждые 4 -6 час) Ингибиторы ксантин-оксидазы (аллопуринол) 100 -300 (до 900!) мг/сут (алоприм 400 мг/м 2) Алкализация крови в/в введением Na. HCO 3 – до достижения р. Н мочи = 7, 1 -7, 5 Рекомбинантная урат-окидаза/разбуриказа, 200 мг/кг –предупреждение уратной нефропатии Лечение гиперкалиемии (приём ионообменных смол, в/в инсулин, декстроза, глюконат Са) При сочетании гиперфосфатемии и гипокальциемии – Са ацетат или Са бикарбонат per os! (внутривенное введение может вызвать преципитацию фосфата Са!)
 Показания к началу ЗПТ при СЛО Общепринятые для ОПН при отсутствии или меньших значениях общепринятых для ОПН критериев: • ↑ уровень мочевой кислоты ≥ 20 мг/дл • фосфора ≥ 3, 3 ммоль/л (≥ 10, 2 мг/дл), особенно в сочетании с гипокальциемией • Yeung S. C. , Escalante C. , Cancer medicine/ 2003
Показания к началу ЗПТ при СЛО Общепринятые для ОПН при отсутствии или меньших значениях общепринятых для ОПН критериев: • ↑ уровень мочевой кислоты ≥ 20 мг/дл • фосфора ≥ 3, 3 ммоль/л (≥ 10, 2 мг/дл), особенно в сочетании с гипокальциемией • Yeung S. C. , Escalante C. , Cancer medicine/ 2003
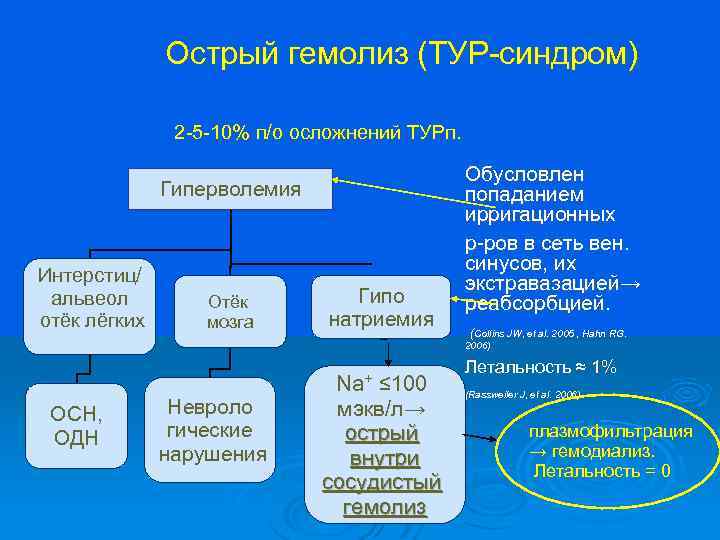 Острый гемолиз (ТУР-синдром) 2 -5 -10% п/о осложнений ТУРп. Гиперволемия Интерстиц/ альвеол отёк лёгких ОСН, ОДН Отёк мозга Невроло гические нарушения Гипо натриемия Na+ ≤ 100 мэкв/л→ острый внутри сосудистый гемолиз • Обусловлен попаданием ирригационных р-ров в сеть вен. синусов, их экстравазацией→ реабсорбцией. (Collins JW, et al. 2005 , Hahn RG. 2006) Летальность ≈ 1% (Rassweiler J, et al. 2006) плазмофильтрация → гемодиализ. Летальность = 0
Острый гемолиз (ТУР-синдром) 2 -5 -10% п/о осложнений ТУРп. Гиперволемия Интерстиц/ альвеол отёк лёгких ОСН, ОДН Отёк мозга Невроло гические нарушения Гипо натриемия Na+ ≤ 100 мэкв/л→ острый внутри сосудистый гемолиз • Обусловлен попаданием ирригационных р-ров в сеть вен. синусов, их экстравазацией→ реабсорбцией. (Collins JW, et al. 2005 , Hahn RG. 2006) Летальность ≈ 1% (Rassweiler J, et al. 2006) плазмофильтрация → гемодиализ. Летальность = 0
 Почечная недостаточность в онкологии и химиотерапия
Почечная недостаточность в онкологии и химиотерапия
 Особенности ОПН при ХТ Цисплатин • Метотрексат • Ифосфамид • Мелфалан Вызывают ренотубулярную преципитацию ксенобиотиков → реноваскулярную обструкцию, гломерулярные и микрососудистые нарушения, тубулоинтерстициальные поражения • ОПН после цисплатина и карбоплатина дозозависима. Характерны гипокалиемия и гипомагниемия Фармацевтические антидоты: Амифостин Тиосульфат натрия Диэтилтиокарбамат • • •
Особенности ОПН при ХТ Цисплатин • Метотрексат • Ифосфамид • Мелфалан Вызывают ренотубулярную преципитацию ксенобиотиков → реноваскулярную обструкцию, гломерулярные и микрососудистые нарушения, тубулоинтерстициальные поражения • ОПН после цисплатина и карбоплатина дозозависима. Характерны гипокалиемия и гипомагниемия Фармацевтические антидоты: Амифостин Тиосульфат натрия Диэтилтиокарбамат • • •
 Химиотерапия у больных с почечной недостаточностью • Риск развития токсических эффектов у онкологических больных, нуждающихся в химиотерапии по поводу опухолевого заболевания и страдающих сопутствующей почечной недостаточностью, возрастает многократно Launay-Vacher V. , Deray G. 2006 • В то же время в случае проведения получающему ЗПТ онкологическому больному ПХТ высокодиализирующимися препаратами необходимо корректирующее ↑ лекарственной дозы для обеспечения адекватного терапевтического эффекта. Tomita M. , Aoki Y. , Tanaka K. Clin Pharmacokinet 2004; 43 (8); 515 -527. Boesler B. , Czock D. , Keller F. et al. Nephrol Dial Transpl 2005 20 (6): 1187 -1191.
Химиотерапия у больных с почечной недостаточностью • Риск развития токсических эффектов у онкологических больных, нуждающихся в химиотерапии по поводу опухолевого заболевания и страдающих сопутствующей почечной недостаточностью, возрастает многократно Launay-Vacher V. , Deray G. 2006 • В то же время в случае проведения получающему ЗПТ онкологическому больному ПХТ высокодиализирующимися препаратами необходимо корректирующее ↑ лекарственной дозы для обеспечения адекватного терапевтического эффекта. Tomita M. , Aoki Y. , Tanaka K. Clin Pharmacokinet 2004; 43 (8); 515 -527. Boesler B. , Czock D. , Keller F. et al. Nephrol Dial Transpl 2005 20 (6): 1187 -1191.
 Способность противоопухолевых препаратов к элиминации посредством ГД (in vitro) 1990 г. Изучение на биологических тест-системах изменения цитотоксичности 20 цитостатиков на экспериментальной модели ГД Высокая Метотрексат Флуорацил Цитарабин Дактиномицин Митомицин Циклофосфамид Ифосфамид Мелфалан Цисплатин Умеренная Доксорубицин Эпирубицин Кармустин Низкая Даунорубицин Винкристин Винбластин Виндезин Этопозид Тенипозид Митоксантрон Дакарбазин Sauer H, . Fuger K. , . Blumenstein M. Cancer Treat Rev 1990 г.
Способность противоопухолевых препаратов к элиминации посредством ГД (in vitro) 1990 г. Изучение на биологических тест-системах изменения цитотоксичности 20 цитостатиков на экспериментальной модели ГД Высокая Метотрексат Флуорацил Цитарабин Дактиномицин Митомицин Циклофосфамид Ифосфамид Мелфалан Цисплатин Умеренная Доксорубицин Эпирубицин Кармустин Низкая Даунорубицин Винкристин Винбластин Виндезин Этопозид Тенипозид Митоксантрон Дакарбазин Sauer H, . Fuger K. , . Blumenstein M. Cancer Treat Rev 1990 г.
 Цисплатин Области применения: • Рак лёгкого • Рак яичников • Рак яичка • Рак мочевого пузыря • Компонент многих схем ПХТ Особенности фармакокинетики: Период полувыведения 12 -49 ׳ быстрое и прочное связывание с тканевыми белками →необходимо ↓ дозы на 50% при т. ХПН. Гемодиализ эффективно выводит дериваты ЦП; выполняется сразу после введения ЦП Tomita M. , Aoki Y. , Tanaka K. Effect of haemodialysis on the pfarmacokinetics of antineoplastic drugs. Clin. Pharmacokinet. 2004
Цисплатин Области применения: • Рак лёгкого • Рак яичников • Рак яичка • Рак мочевого пузыря • Компонент многих схем ПХТ Особенности фармакокинетики: Период полувыведения 12 -49 ׳ быстрое и прочное связывание с тканевыми белками →необходимо ↓ дозы на 50% при т. ХПН. Гемодиализ эффективно выводит дериваты ЦП; выполняется сразу после введения ЦП Tomita M. , Aoki Y. , Tanaka K. Effect of haemodialysis on the pfarmacokinetics of antineoplastic drugs. Clin. Pharmacokinet. 2004
 Этопозид Области применения: Мелкоклеточный рак лёгкого • Лимфомы • Лейкозы • Рак яичка • Особенности фармакокинетики: • 95% прочно связывается с • белками плазмы. • Высокий объём • распределения • Длительный (11 часов, 2 • фазная кривая) Т½. Гемодиализ неэффективен. Больным с т. ХПН необходимо ↓ дозы на 60% от N. Tomita M. , Aoki Y. , Tanaka K. Effect of haemodialysis on the pfarmacokinetics of antineoplastic drugs. Clin. Pharmacokinet. 2004
Этопозид Области применения: Мелкоклеточный рак лёгкого • Лимфомы • Лейкозы • Рак яичка • Особенности фармакокинетики: • 95% прочно связывается с • белками плазмы. • Высокий объём • распределения • Длительный (11 часов, 2 • фазная кривая) Т½. Гемодиализ неэффективен. Больным с т. ХПН необходимо ↓ дозы на 60% от N. Tomita M. , Aoki Y. , Tanaka K. Effect of haemodialysis on the pfarmacokinetics of antineoplastic drugs. Clin. Pharmacokinet. 2004
 Циклофосфамид Области применения: • • • Рак лёгкого Лимфогранулематоз Лейкозы Герминогенные опухоли Множестваенная миелома Рак МПС Рак предстательной железы Рак тела матки Особенности фармакокинетики: 2 -фазная кривая выведения Гемодиализ эффективен, должен начинаться не ранее 12 часов после введения, чтобы избежать избыточной элиминации и ↓ AUC Tomita M. , Aoki Y. , Tanaka K. Effect of haemodialysis on the pfarmacokinetics of antineoplastic drugs. Clin. Pharmacokinet. 2004
Циклофосфамид Области применения: • • • Рак лёгкого Лимфогранулематоз Лейкозы Герминогенные опухоли Множестваенная миелома Рак МПС Рак предстательной железы Рак тела матки Особенности фармакокинетики: 2 -фазная кривая выведения Гемодиализ эффективен, должен начинаться не ранее 12 часов после введения, чтобы избежать избыточной элиминации и ↓ AUC Tomita M. , Aoki Y. , Tanaka K. Effect of haemodialysis on the pfarmacokinetics of antineoplastic drugs. Clin. Pharmacokinet. 2004
 Метотрексат Области применения: Острый лимфобластный Остеогенная саркома лейкоз Рак печени Лимфогранулематоз Рак почечной лоханки Саркома Юинга Рак почки Трофобластическая Рак лёгкого болезнь Рак молочной железы Рак кожи Герминогенные Рак шейки матки опухоли Рак пищевода Опухоли головы и шеи
Метотрексат Области применения: Острый лимфобластный Остеогенная саркома лейкоз Рак печени Лимфогранулематоз Рак почечной лоханки Саркома Юинга Рак почки Трофобластическая Рак лёгкого болезнь Рак молочной железы Рак кожи Герминогенные Рак шейки матки опухоли Рак пищевода Опухоли головы и шеи
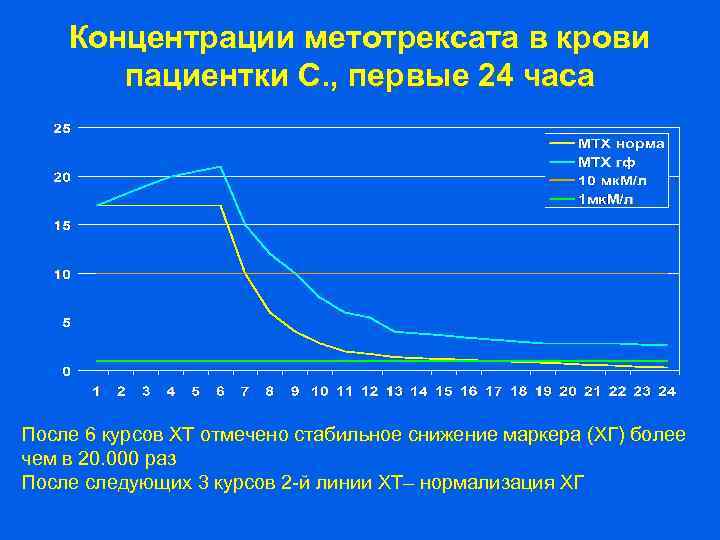 Концентрации метотрексата в крови пациентки С. , первые 24 часа После 6 курсов ХТ отмечено стабильное снижение маркера (ХГ) более чем в 20. 000 раз После следующих 3 курсов 2 -й линии ХТ– нормализация ХГ
Концентрации метотрексата в крови пациентки С. , первые 24 часа После 6 курсов ХТ отмечено стабильное снижение маркера (ХГ) более чем в 20. 000 раз После следующих 3 курсов 2 -й линии ХТ– нормализация ХГ
 Множественная Миелома и острая почечная недостаточность • ОПН – у 18 -56% Sakhuja V. et al. Renal involvement in multiple mieloma, 2000 • Ранняя (в первые 2 мес п/начала лечения) летальность > 30% (Goldschmidt H. , et al. , NDT, 2000) • 9% больных первичных (ММ) пациентов нуждаются в ЗПТ (6 -8 случаев на млн. насел/год) Knudsen. L. , et a. 1994 • Пациенты с ОПН часто исключаются из протоколов высокодозной химиотерапии • Медиана выживаемости: 24 - 44 мес Greip P. , et al. , 2005 • Выживаемость больных ММ на диализе ~ 6 месяцев • Восстановление функции почек (в среднем в первые 6 недель) у больных ММ ассоциировано с достоверным увеличением их выживаемости • Функция почек – осн. показатель риска развития осл/смертности: 2 место среди причин смерти (п/ инф)
Множественная Миелома и острая почечная недостаточность • ОПН – у 18 -56% Sakhuja V. et al. Renal involvement in multiple mieloma, 2000 • Ранняя (в первые 2 мес п/начала лечения) летальность > 30% (Goldschmidt H. , et al. , NDT, 2000) • 9% больных первичных (ММ) пациентов нуждаются в ЗПТ (6 -8 случаев на млн. насел/год) Knudsen. L. , et a. 1994 • Пациенты с ОПН часто исключаются из протоколов высокодозной химиотерапии • Медиана выживаемости: 24 - 44 мес Greip P. , et al. , 2005 • Выживаемость больных ММ на диализе ~ 6 месяцев • Восстановление функции почек (в среднем в первые 6 недель) у больных ММ ассоциировано с достоверным увеличением их выживаемости • Функция почек – осн. показатель риска развития осл/смертности: 2 место среди причин смерти (п/ инф)
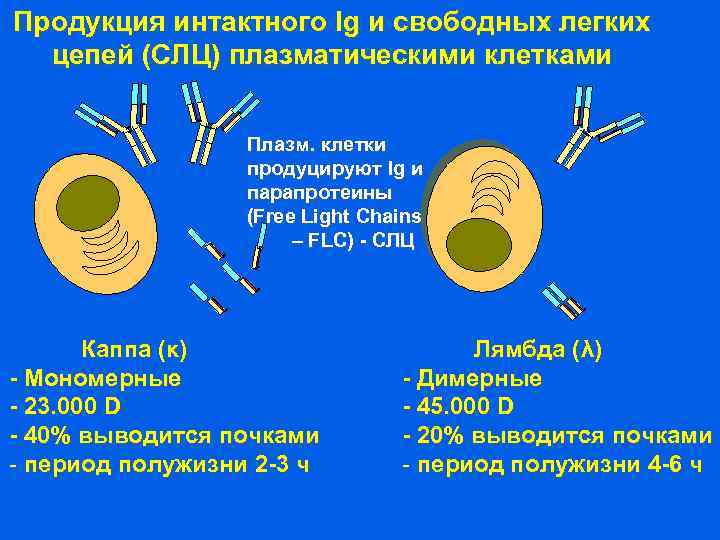 Продукция интактного Ig и свободных легких цепей (СЛЦ) плазматическими клетками Плазм. клетки продуцируют Ig и парапротеины (Free Light Chains – FLC) - СЛЦ Каппа (κ) - Мономерные - 23. 000 D - 40% выводится почками - период полужизни 2 -3 ч Лямбда (λ) - Димерные - 45. 000 D - 20% выводится почками - период полужизни 4 -6 ч
Продукция интактного Ig и свободных легких цепей (СЛЦ) плазматическими клетками Плазм. клетки продуцируют Ig и парапротеины (Free Light Chains – FLC) - СЛЦ Каппа (κ) - Мономерные - 23. 000 D - 40% выводится почками - период полужизни 2 -3 ч Лямбда (λ) - Димерные - 45. 000 D - 20% выводится почками - период полужизни 4 -6 ч
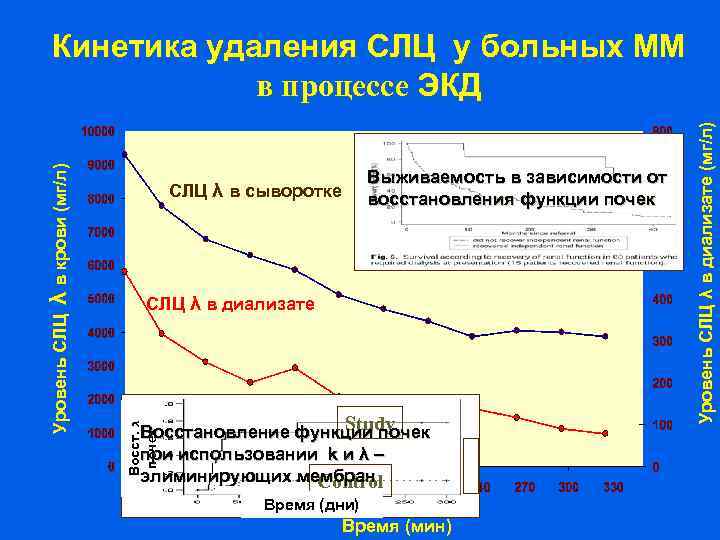 СЛЦ λ в диализате Study Восстановление функции почек при использовании k и λ – элиминирующих мембран Control Время (дни) Time (mins) Время (мин) Lambda in dialysate (mg/L) (мг/л) Уровень СЛЦ λ в диализате СЛЦ λ в сыворотке Выживаемость в зависимости от восстановления функции почек Восст. ג почек Serum free lambda крови (мг/л) Уровень СЛЦ λ в (mg/L) Кинетика удаления СЛЦ у больных ММ в процессе ЭКД
СЛЦ λ в диализате Study Восстановление функции почек при использовании k и λ – элиминирующих мембран Control Время (дни) Time (mins) Время (мин) Lambda in dialysate (mg/L) (мг/л) Уровень СЛЦ λ в диализате СЛЦ λ в сыворотке Выживаемость в зависимости от восстановления функции почек Восст. ג почек Serum free lambda крови (мг/л) Уровень СЛЦ λ в (mg/L) Кинетика удаления СЛЦ у больных ММ в процессе ЭКД
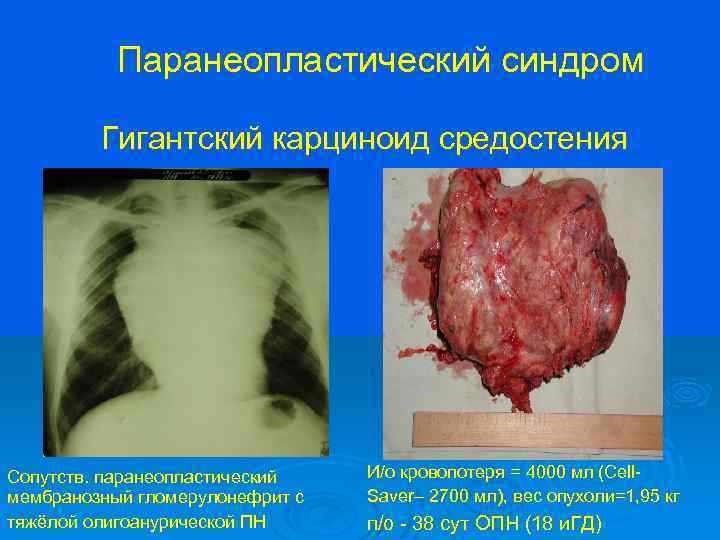 Паранеопластический синдром Гигантский карциноид средостения Сопутств. паранеопластический мембранозный гломерулонефрит с тяжёлой олигоанурической ПН И/о кровопотеря = 4000 мл (Cell. Saver– 2700 мл), вес опухоли=1, 95 кг п/о - 38 сут ОПН (18 и. ГД)
Паранеопластический синдром Гигантский карциноид средостения Сопутств. паранеопластический мембранозный гломерулонефрит с тяжёлой олигоанурической ПН И/о кровопотеря = 4000 мл (Cell. Saver– 2700 мл), вес опухоли=1, 95 кг п/о - 38 сут ОПН (18 и. ГД)
 Исходы ОПН в составе СПОН у онкологических больных Единственный независимый значимый прогностический фактор госпитальной летальности число поражённых органов. Летальность ГБ, нуждающихся в ЗПТ, коррелирует с числом поражённых органов: 36%→ 83% при недостаточности органов 1→ 3 • CVVHDF эффективна в ИТ ОПН у этих больных: выписаны 15(47%). • Онкологические параметры и общепринятые шкалы оценки тяжести состояния (APACHE II) не относятся к предиктивным факторам летальности у этих больных. • Berghmans T, Meert AP, Markiewicz E, Sculier JP/ Support Care Cancer, 2004
Исходы ОПН в составе СПОН у онкологических больных Единственный независимый значимый прогностический фактор госпитальной летальности число поражённых органов. Летальность ГБ, нуждающихся в ЗПТ, коррелирует с числом поражённых органов: 36%→ 83% при недостаточности органов 1→ 3 • CVVHDF эффективна в ИТ ОПН у этих больных: выписаны 15(47%). • Онкологические параметры и общепринятые шкалы оценки тяжести состояния (APACHE II) не относятся к предиктивным факторам летальности у этих больных. • Berghmans T, Meert AP, Markiewicz E, Sculier JP/ Support Care Cancer, 2004
 Острая печёночная недостаточность
Острая печёночная недостаточность
 Острая печёночная недостаточность Острое нарушение функции печени, с нарастающей желтухой, печёночной энцефалопатией, и/или гепаторенальным синдромом/мультиорганной дисфункцией. Jalan R et al. Blood purification, 2002 Летальность: 50 -66% Sen S. et al. Hepatology, 2004, Stauber R et al. J Hepatol 2006 В онкологии: Печень – первый орган на пути гематогенного распространения опухоли → частота её поражения достигает 70%
Острая печёночная недостаточность Острое нарушение функции печени, с нарастающей желтухой, печёночной энцефалопатией, и/или гепаторенальным синдромом/мультиорганной дисфункцией. Jalan R et al. Blood purification, 2002 Летальность: 50 -66% Sen S. et al. Hepatology, 2004, Stauber R et al. J Hepatol 2006 В онкологии: Печень – первый орган на пути гематогенного распространения опухоли → частота её поражения достигает 70%
 Печёночная недостаточность при хирургическом лечении больных первичным/метастатическим раком печени Ежегодно в России регистрируется 40. 000 случаев заболевания раком толстой кишки. У 20 -50% первичных больных + метастазы в печени. • 5 -летняя выживаемость больных первичным раком печени после хирургического лечения = 10, 3% - 77, 9%; при метастатическом поражении печени – 28%. • Летальность после резекций печени = 6, 1%, 18, 7% летальных исходов обусловлены печёночной недостаточностью. • Проф. Патютко Ю. И. , Сагайдак И. В. , Котельников А. Г. РОНЦ им. Н. Н. Блохина РАМН, 2006
Печёночная недостаточность при хирургическом лечении больных первичным/метастатическим раком печени Ежегодно в России регистрируется 40. 000 случаев заболевания раком толстой кишки. У 20 -50% первичных больных + метастазы в печени. • 5 -летняя выживаемость больных первичным раком печени после хирургического лечения = 10, 3% - 77, 9%; при метастатическом поражении печени – 28%. • Летальность после резекций печени = 6, 1%, 18, 7% летальных исходов обусловлены печёночной недостаточностью. • Проф. Патютко Ю. И. , Сагайдак И. В. , Котельников А. Г. РОНЦ им. Н. Н. Блохина РАМН, 2006
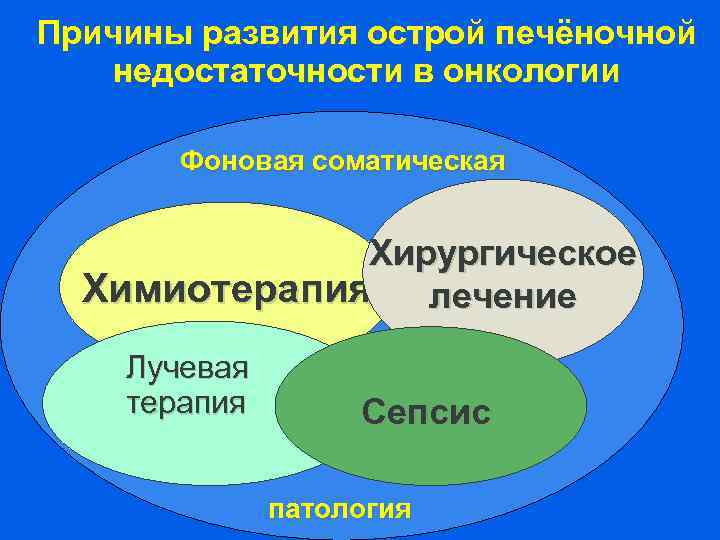 Причины развития острой печёночной недостаточности в онкологии Фоновая соматическая Хирургическое Химиотерапия лечение Лучевая терапия Сепсис патология
Причины развития острой печёночной недостаточности в онкологии Фоновая соматическая Хирургическое Химиотерапия лечение Лучевая терапия Сепсис патология
 Фульминантное течение печёночной недостаточности у онкологического больного с сопутствующим гепатитом С
Фульминантное течение печёночной недостаточности у онкологического больного с сопутствующим гепатитом С
 Всё большее число больных подвергается хирургическому лечению после длительной / многокомпонентной химиотерапии + Антибиотики Антиэметики Анальгетики Вирусные гепатиты Иммуносупрессия Полное парентеральное питание
Всё большее число больных подвергается хирургическому лечению после длительной / многокомпонентной химиотерапии + Антибиотики Антиэметики Анальгетики Вирусные гепатиты Иммуносупрессия Полное парентеральное питание
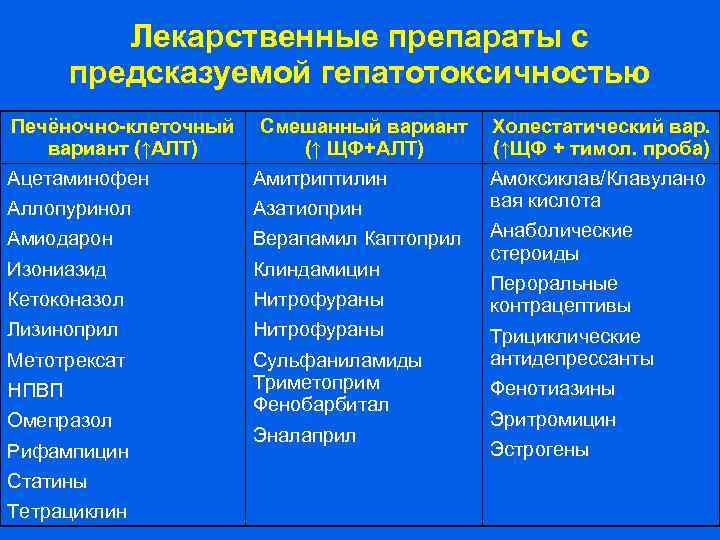 Лекарственные препараты с предсказуемой гепатотоксичностью Печёночно-клеточный Смешанный вариант (↑АЛТ) (↑ ЩФ+АЛТ) Ацетаминофен Амитриптилин Аллопуринол Азатиоприн Амиодарон Верапамил Каптоприл Изониазид Кетоконазол Клиндамицин Нитрофураны Лизиноприл Метотрексат Нитрофураны Сульфаниламиды Триметоприм Фенобарбитал Эналаприл НПВП Омепразол Рифампицин Статины Тетрациклин Холестатический вар. (↑ЩФ + тимол. проба) Амоксиклав/Клавулано вая кислота Анаболические стероиды Пероральные контрацептивы Трициклические антидепрессанты Фенотиазины Эритромицин Эстрогены
Лекарственные препараты с предсказуемой гепатотоксичностью Печёночно-клеточный Смешанный вариант (↑АЛТ) (↑ ЩФ+АЛТ) Ацетаминофен Амитриптилин Аллопуринол Азатиоприн Амиодарон Верапамил Каптоприл Изониазид Кетоконазол Клиндамицин Нитрофураны Лизиноприл Метотрексат Нитрофураны Сульфаниламиды Триметоприм Фенобарбитал Эналаприл НПВП Омепразол Рифампицин Статины Тетрациклин Холестатический вар. (↑ЩФ + тимол. проба) Амоксиклав/Клавулано вая кислота Анаболические стероиды Пероральные контрацептивы Трициклические антидепрессанты Фенотиазины Эритромицин Эстрогены
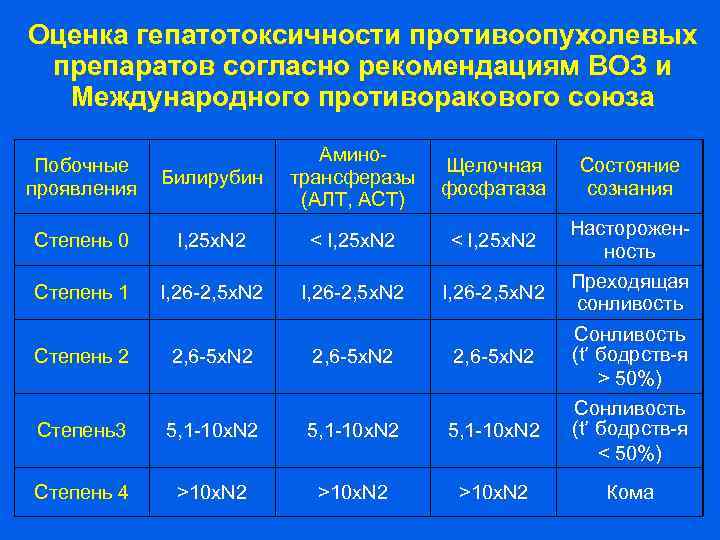 Оценка гепатотоксичности противоопухолевых препаратов согласно рекомендациям ВОЗ и Международного противоракового союза Билирубин Аминотрансферазы (АЛТ, АСТ) Щелочная фосфатаза Степень 0 l, 25 x. N 2 < l, 25 x. N 2 Степень 1 l, 26 -2, 5 x. N 2 Степень 2 2, 6 -5 x. N 2 Степень3 5, 1 -10 x. N 2 Степень 4 >10 x. N 2 Побочные проявления Состояние сознания Настороженность Преходящая сонливость Сонливость (t ׳ бодрств-я > 50%) Сонливость (t ׳ бодрств-я < 50%) Кома
Оценка гепатотоксичности противоопухолевых препаратов согласно рекомендациям ВОЗ и Международного противоракового союза Билирубин Аминотрансферазы (АЛТ, АСТ) Щелочная фосфатаза Степень 0 l, 25 x. N 2 < l, 25 x. N 2 Степень 1 l, 26 -2, 5 x. N 2 Степень 2 2, 6 -5 x. N 2 Степень3 5, 1 -10 x. N 2 Степень 4 >10 x. N 2 Побочные проявления Состояние сознания Настороженность Преходящая сонливость Сонливость (t ׳ бодрств-я > 50%) Сонливость (t ׳ бодрств-я < 50%) Кома
 Дозы цитостатиков у больных с печёночной недостаточностью ↓ дозы антрациклинов на 50%, прочих цитостатиков на 25% при ↑ уровня общего билирубина в 1, 26 -2, 5 раза, трансаминаз–в 2 -5 раз. 2. ↓ дозы антрациклинов на 75%, прочих цитостатиков – на 50% при ↑ уровня общего билирубина в 2, 6 -5 раз, трансаминаз – в 5, 1 -10 раз. 1. При сохраняющемся отклонении лабораторных показателей от нормального уровня противоопухолевая терапия прекращается
Дозы цитостатиков у больных с печёночной недостаточностью ↓ дозы антрациклинов на 50%, прочих цитостатиков на 25% при ↑ уровня общего билирубина в 1, 26 -2, 5 раза, трансаминаз–в 2 -5 раз. 2. ↓ дозы антрациклинов на 75%, прочих цитостатиков – на 50% при ↑ уровня общего билирубина в 2, 6 -5 раз, трансаминаз – в 5, 1 -10 раз. 1. При сохраняющемся отклонении лабораторных показателей от нормального уровня противоопухолевая терапия прекращается
 Некоторые варианты лекарственных поражений печени при химиотерапии Стеатогепатит • Поражение сосудов • • Синдром синусоидальной обструкции Пелиоз – морфологический вариант ЛПП, с образованием крупных, заполненных кровью, полостей Веноокклюзионная болезнь Канальцевый холестаз • Склерозирующий холангит •
Некоторые варианты лекарственных поражений печени при химиотерапии Стеатогепатит • Поражение сосудов • • Синдром синусоидальной обструкции Пелиоз – морфологический вариант ЛПП, с образованием крупных, заполненных кровью, полостей Веноокклюзионная болезнь Канальцевый холестаз • Склерозирующий холангит •
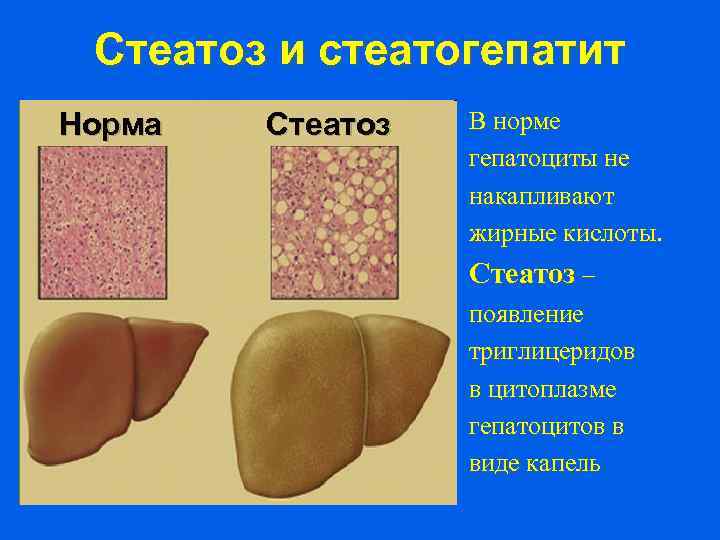 Стеатоз и стеатогепатит Норма Стеатоз В норме гепатоциты не накапливают жирные кислоты. Стеатоз – появление триглицеридов в цитоплазме гепатоцитов в виде капель
Стеатоз и стеатогепатит Норма Стеатоз В норме гепатоциты не накапливают жирные кислоты. Стеатоз – появление триглицеридов в цитоплазме гепатоцитов в виде капель
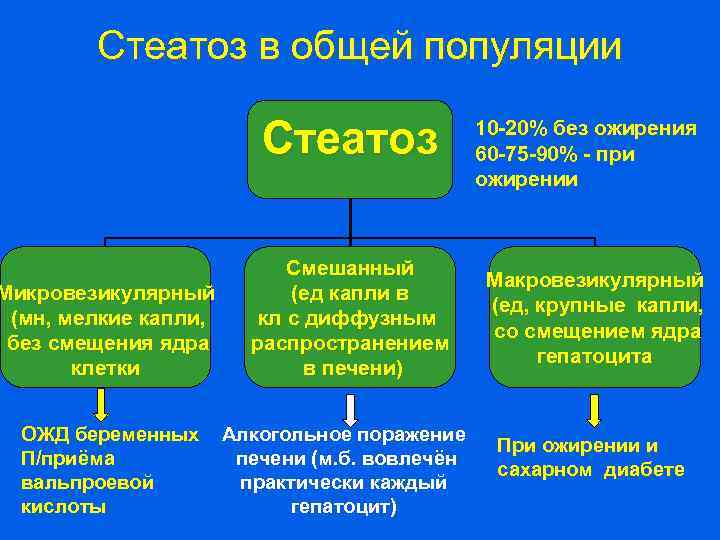 Стеатоз в общей популяции Стеатоз Микровезикулярный (мн, мелкие капли, без смещения ядра клетки ОЖД беременных П/приёма вальпроевой кислоты Смешанный (ед капли в кл с диффузным распространением в печени) Алкогольное поражение печени (м. б. вовлечён практически каждый гепатоцит) 10 -20% без ожирения 60 -75 -90% - при ожирении Макровезикулярный (ед, крупные капли, со смещением ядра гепатоцита При ожирении и сахарном диабете
Стеатоз в общей популяции Стеатоз Микровезикулярный (мн, мелкие капли, без смещения ядра клетки ОЖД беременных П/приёма вальпроевой кислоты Смешанный (ед капли в кл с диффузным распространением в печени) Алкогольное поражение печени (м. б. вовлечён практически каждый гепатоцит) 10 -20% без ожирения 60 -75 -90% - при ожирении Макровезикулярный (ед, крупные капли, со смещением ядра гепатоцита При ожирении и сахарном диабете
 Стеатогепатит, ассоциированный с химиотерапией Вариант токсического поражения печени. Невоспалительные изменения печеночной ткани • Увеличенные (за счёт жировых включений) гепатоциты в окружении нейтрофилов и лимфоцитов • Прогрессирующий синусоидальный фиброз • NAFLD – non-alcoholic fatty liver desease NASH - non-alcoholic steatohepatitis CASH – chemotherapy-associated steatohepatitis Fong, 2006 После в/а ХТ наибольшее накопление триглицеридов – в тех сегментах печени, которые получили максимум химиопрепарата Zeiss J, 1990
Стеатогепатит, ассоциированный с химиотерапией Вариант токсического поражения печени. Невоспалительные изменения печеночной ткани • Увеличенные (за счёт жировых включений) гепатоциты в окружении нейтрофилов и лимфоцитов • Прогрессирующий синусоидальный фиброз • NAFLD – non-alcoholic fatty liver desease NASH - non-alcoholic steatohepatitis CASH – chemotherapy-associated steatohepatitis Fong, 2006 После в/а ХТ наибольшее накопление триглицеридов – в тех сегментах печени, которые получили максимум химиопрепарата Zeiss J, 1990
 Патогенез CASH Two-hit theory: 1. 2. Накопление гепатоцитами триглицеридов Активация микросомальных ферментов системы Р-450 → активация ПОЛ → образование свободных радикалов → истощение клеточного запаса антиоксидантов → ↓ продукции митохондриального АТФ → снижение адекватной реакции гепатоцитов на гипоксию → снижение органной регенераторной способности Фиброз, цирроз, гепатоцеллюлярный рак
Патогенез CASH Two-hit theory: 1. 2. Накопление гепатоцитами триглицеридов Активация микросомальных ферментов системы Р-450 → активация ПОЛ → образование свободных радикалов → истощение клеточного запаса антиоксидантов → ↓ продукции митохондриального АТФ → снижение адекватной реакции гепатоцитов на гипоксию → снижение органной регенераторной способности Фиброз, цирроз, гепатоцеллюлярный рак
 Химиопрепараты, ответственные за развитие CASH 5 -Фторурацил - 4, 4 -6, 3% Лейковорин Оксалиплатин Иринотекан >20%, независимый фактор прогноза п/о летальности Вызванный цитостатиками стеатоз не является противопоказанием к резекции печени Kooby, 2003 НО! Особенное внимание после лечения иринотеканом необходимо уделять пациентам с ИМТ>25 кг/м 2 перед планируемой массивной резекцией печени
Химиопрепараты, ответственные за развитие CASH 5 -Фторурацил - 4, 4 -6, 3% Лейковорин Оксалиплатин Иринотекан >20%, независимый фактор прогноза п/о летальности Вызванный цитостатиками стеатоз не является противопоказанием к резекции печени Kooby, 2003 НО! Особенное внимание после лечения иринотеканом необходимо уделять пациентам с ИМТ>25 кг/м 2 перед планируемой массивной резекцией печени
 Синдром синусоидальной обструкции Обструкция мелких внутрипечёночных венул без признаков тромбоза или окклюзии вен более крупного калибра Летальность: 9 -98% Причина ССО – повреждение эндотелия венул и синусоидов В отличие от обычного тромбоза обусловлено обратимым (при устранении повреждающего фактора) появлением между эндотелием и подлежащим матриксом отёчной соед. ткани. При сохранении поврежд ф-ра множественная сосудистая окклюзия быстро приводит к фатальному застойному циррозу печени. Оксалиплатин! – у 79% больных (при др. схемах ХТ – 23%)
Синдром синусоидальной обструкции Обструкция мелких внутрипечёночных венул без признаков тромбоза или окклюзии вен более крупного калибра Летальность: 9 -98% Причина ССО – повреждение эндотелия венул и синусоидов В отличие от обычного тромбоза обусловлено обратимым (при устранении повреждающего фактора) появлением между эндотелием и подлежащим матриксом отёчной соед. ткани. При сохранении поврежд ф-ра множественная сосудистая окклюзия быстро приводит к фатальному застойному циррозу печени. Оксалиплатин! – у 79% больных (при др. схемах ХТ – 23%)
 Пелиоз Обструктивный синдром → к расширению просвета синусоидов, атрофии гепатоцитов, выходу эритроцитов в межклеточное пространство Пелиоз – образование в паренхиматозных органах заполненных кровью полостей. Микроскопически: мелкие кисты без эндотелиальной выстилки, с разрывами ретикулиновых волокон. Макроскопически: неравномерное синеватое обесцвечивание паренхимы с зонами отёчной ткани – «голубая печень» Bilchik A. , 2005
Пелиоз Обструктивный синдром → к расширению просвета синусоидов, атрофии гепатоцитов, выходу эритроцитов в межклеточное пространство Пелиоз – образование в паренхиматозных органах заполненных кровью полостей. Микроскопически: мелкие кисты без эндотелиальной выстилки, с разрывами ретикулиновых волокон. Макроскопически: неравномерное синеватое обесцвечивание паренхимы с зонами отёчной ткани – «голубая печень» Bilchik A. , 2005
 Как прервать каскад патологических реакций? Патогномоничная лекарственная терапия Экстракорпоральная гемокоррекция
Как прервать каскад патологических реакций? Патогномоничная лекарственная терапия Экстракорпоральная гемокоррекция
 Печёночная недостаточность Является результатом некроза гепатоцитов Наиболее грозный признак – развитие печёночной энцефалопатии как результат проникновения эндогенных нейротоксинов через ГЭБ Метаболиты, при ОПеч Н, различны по ММ и физико-химическим характеристикам: Значительная часть связывается с альбумином (неконъюгированный билирубин, желчные кислоты, гидрофобные аминокислоты и жирные кислоты) Другая часть – водорастворимые средне- и низкомолекулярные токсины (аммиак, мочевина, креатинин)
Печёночная недостаточность Является результатом некроза гепатоцитов Наиболее грозный признак – развитие печёночной энцефалопатии как результат проникновения эндогенных нейротоксинов через ГЭБ Метаболиты, при ОПеч Н, различны по ММ и физико-химическим характеристикам: Значительная часть связывается с альбумином (неконъюгированный билирубин, желчные кислоты, гидрофобные аминокислоты и жирные кислоты) Другая часть – водорастворимые средне- и низкомолекулярные токсины (аммиак, мочевина, креатинин)
 Плазмаферез и плазмофильтрация Плазмаферез – гравитационный вариант замены плазмы крови больного компонентами, препаратами крови и/или кровезаменителями. Плазмофильтрация — сепарационный вариант плазмообмена, по мембранной технологии. При ПА и ПФ элиминируются макромолекулы и связанные с белком токсины свободный миоглобин гемоглобиновый детрит микротромбы продукты цитолиза протеолиза криоглобулины парапротеины бактериальные эндотоксины связанные с белком и лекарства и эндотоксины
Плазмаферез и плазмофильтрация Плазмаферез – гравитационный вариант замены плазмы крови больного компонентами, препаратами крови и/или кровезаменителями. Плазмофильтрация — сепарационный вариант плазмообмена, по мембранной технологии. При ПА и ПФ элиминируются макромолекулы и связанные с белком токсины свободный миоглобин гемоглобиновый детрит микротромбы продукты цитолиза протеолиза криоглобулины парапротеины бактериальные эндотоксины связанные с белком и лекарства и эндотоксины
 Физиологические реакции на ПА и ПФ определяются: • • количеством удаляемого за один сеанс патологического субстрата; дренирующим эффектом операции; объёмом и кратностью сеансов; особенностями возмещения эксфузируемой плазмы по ходу операции и сразу после неё. Наибольший эффект – при небольшом коэффициенте распределения в организме удаляемых эндотоксинов и ограничении их локализации объёмом циркулирующей крови. Объём плазмоэксфузии (ПЭ) низкообъёмная ПЭ — до 20% ОЦП среднеобъёмная ПЭ — 20– 50% ОЦП высокообъёмная ПЭ — 50– 70% ОЦП массивный плазмообмен — более 150% ОЦП Термин “интенсивный плазмообмен” означает частоту ПА/ПФ с интервалом менее 48 часов.
Физиологические реакции на ПА и ПФ определяются: • • количеством удаляемого за один сеанс патологического субстрата; дренирующим эффектом операции; объёмом и кратностью сеансов; особенностями возмещения эксфузируемой плазмы по ходу операции и сразу после неё. Наибольший эффект – при небольшом коэффициенте распределения в организме удаляемых эндотоксинов и ограничении их локализации объёмом циркулирующей крови. Объём плазмоэксфузии (ПЭ) низкообъёмная ПЭ — до 20% ОЦП среднеобъёмная ПЭ — 20– 50% ОЦП высокообъёмная ПЭ — 50– 70% ОЦП массивный плазмообмен — более 150% ОЦП Термин “интенсивный плазмообмен” означает частоту ПА/ПФ с интервалом менее 48 часов.
 Гемосорбция метод ЭКД, основанный на сорбировании токсических веществ крови посредством экстракорпоральной перфузии её через сорбент
Гемосорбция метод ЭКД, основанный на сорбировании токсических веществ крови посредством экстракорпоральной перфузии её через сорбент
 Концепция экстракорпоральной терапии ОПеч. Н Токсины, связанные с альбумином Прямая адсорбция Очищенный альбумин пациента
Концепция экстракорпоральной терапии ОПеч. Н Токсины, связанные с альбумином Прямая адсорбция Очищенный альбумин пациента
 Прометеус in-line система сепарации и адсорбции фракционированной плазмы. • не требует донорского альбумина • сочетает процедуру диализа с адсорбцией •
Прометеус in-line система сепарации и адсорбции фракционированной плазмы. • не требует донорского альбумина • сочетает процедуру диализа с адсорбцией •
 Прометеус Кровь пациента проходит через уникальный фильтр Albu. Flow®, выделяющий из крови пациента плазму с фракциями альбумина и иммуноглобулинов.
Прометеус Кровь пациента проходит через уникальный фильтр Albu. Flow®, выделяющий из крови пациента плазму с фракциями альбумина и иммуноглобулинов.
 Прометеус Плазма вместе с альбумином и меньшими молекулами протеина проходит через две адсорбционных колонки, где связанные токсины (билирубин, желчные кислоты, аммиак) отделяются от альбумина.
Прометеус Плазма вместе с альбумином и меньшими молекулами протеина проходит через две адсорбционных колонки, где связанные токсины (билирубин, желчные кислоты, аммиак) отделяются от альбумина.
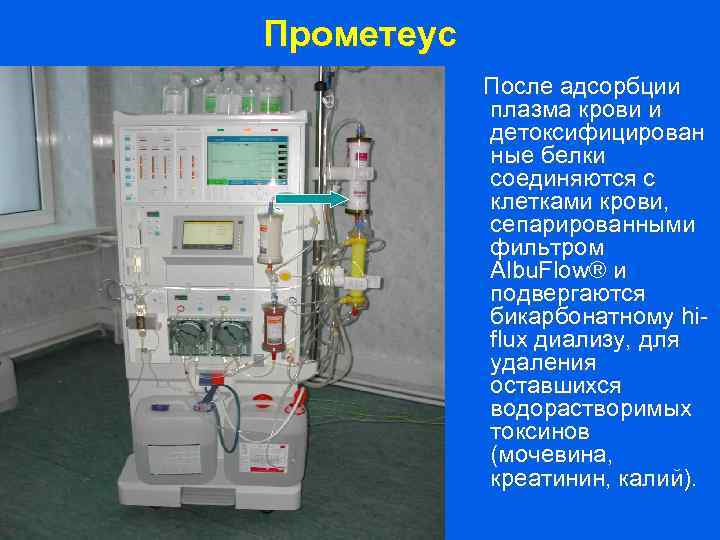 Прометеус После адсорбции плазма крови и детоксифицирован ные белки соединяются с клетками крови, сепарированными фильтром Albu. Flow® и подвергаются бикарбонатному hiflux диализу, для удаления оставшихся водорастворимых токсинов (мочевина, креатинин, калий).
Прометеус После адсорбции плазма крови и детоксифицирован ные белки соединяются с клетками крови, сепарированными фильтром Albu. Flow® и подвергаются бикарбонатному hiflux диализу, для удаления оставшихся водорастворимых токсинов (мочевина, креатинин, калий).
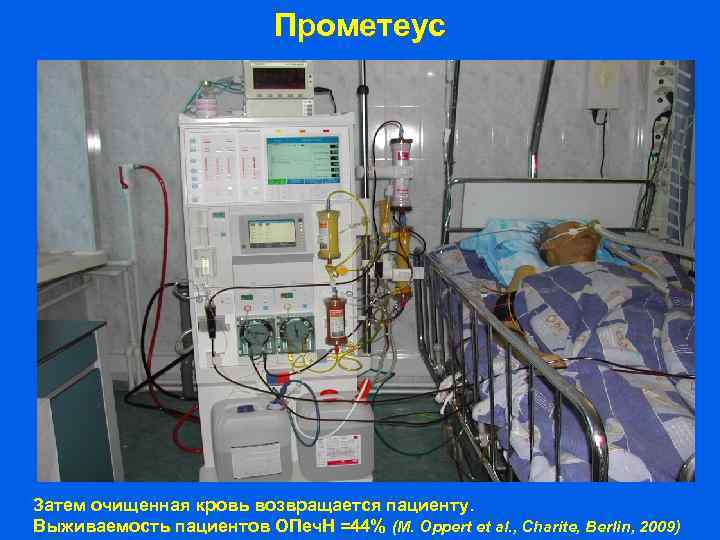 Прометеус Затем очищенная кровь возвращается пациенту. Выживаемость пациентов ОПеч. Н =44% (M. Oppert et al. , Charite, Berlin, 2009)
Прометеус Затем очищенная кровь возвращается пациенту. Выживаемость пациентов ОПеч. Н =44% (M. Oppert et al. , Charite, Berlin, 2009)
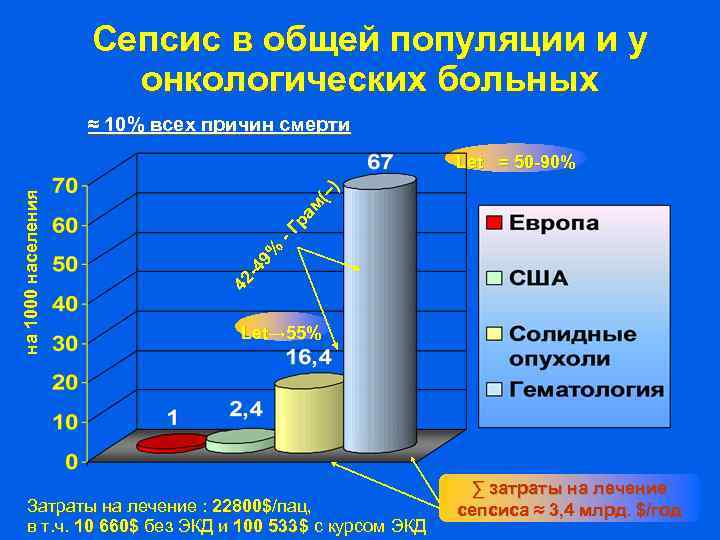 Сепсис в общей популяции и у онкологических больных ≈ 10% всех причин смерти -Г ра м (– ) 42 -4 9% на 1 0 0 0 на с е л е ни я Let = 50 -90% Let→ 55% Затраты на лечение : 22800$/пац, в т. ч. 10 660$ без ЭКД и 100 533$ с курсом ЭКД ∑ затраты на лечение сепсиса ≈ 3, 4 млрд. $/год
Сепсис в общей популяции и у онкологических больных ≈ 10% всех причин смерти -Г ра м (– ) 42 -4 9% на 1 0 0 0 на с е л е ни я Let = 50 -90% Let→ 55% Затраты на лечение : 22800$/пац, в т. ч. 10 660$ без ЭКД и 100 533$ с курсом ЭКД ∑ затраты на лечение сепсиса ≈ 3, 4 млрд. $/год
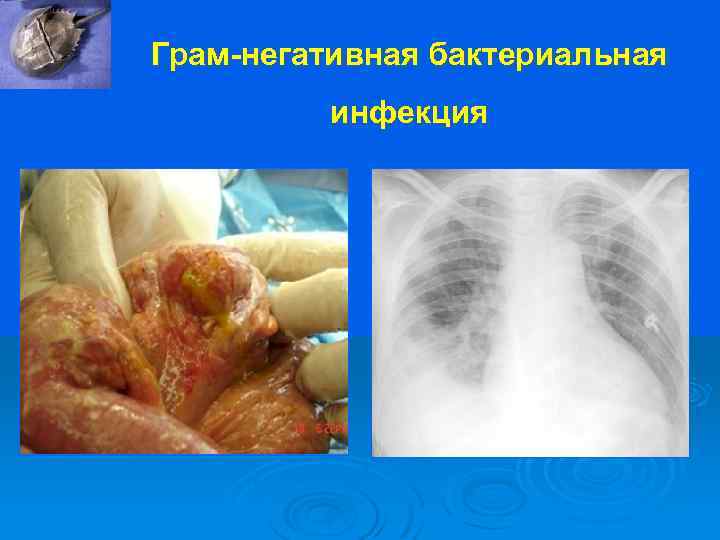 Грам-негативная бактериальная инфекция
Грам-негативная бактериальная инфекция
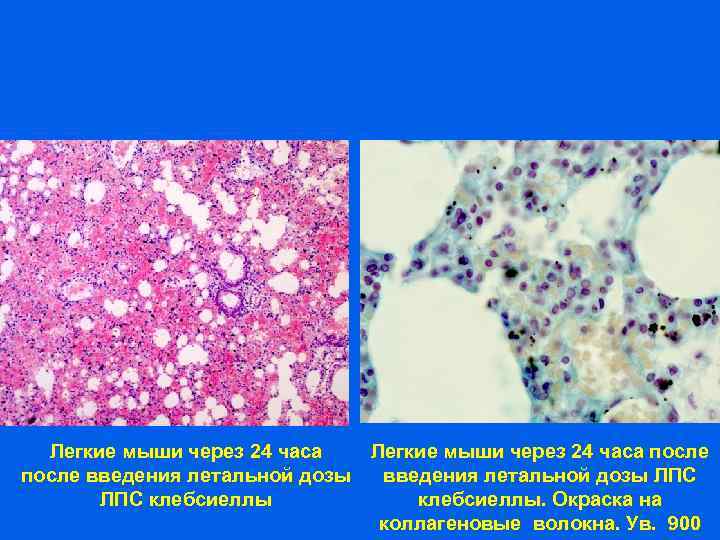 Легкие мыши через 24 часа после введения летальной дозы ЛПС клебсиеллы. Окраска на коллагеновые волокна. Ув. 900
Легкие мыши через 24 часа после введения летальной дозы ЛПС клебсиеллы. Окраска на коллагеновые волокна. Ув. 900
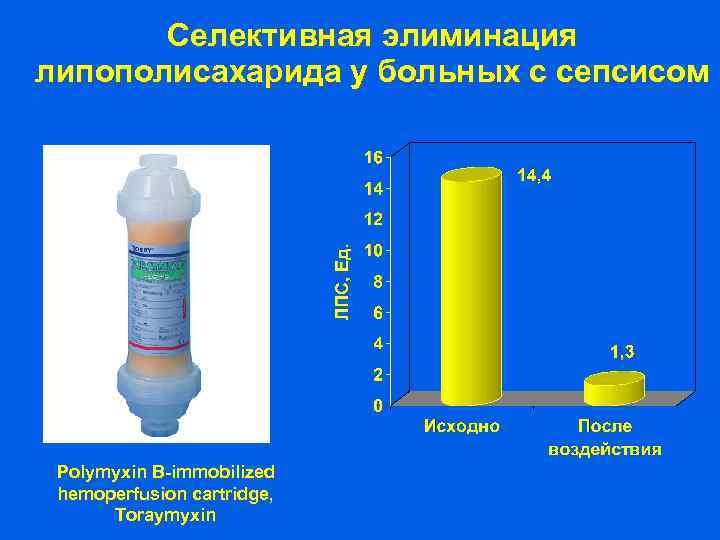 Селективная элиминация липополисахарида у больных с сепсисом Polymyxin B-immobilized hemoperfusion cartridge, Toraymyxin
Селективная элиминация липополисахарида у больных с сепсисом Polymyxin B-immobilized hemoperfusion cartridge, Toraymyxin
 Перспективы направления
Перспективы направления
 Гемосорбция на основе магнитоуправляемых наночастиц Идея: поток суспензии высокодисперсных наночастиц сорбента в магнитном поле обеспечивает максимально высокую степень очистки крови от низких и среднемолекулярных токсинов
Гемосорбция на основе магнитоуправляемых наночастиц Идея: поток суспензии высокодисперсных наночастиц сорбента в магнитном поле обеспечивает максимально высокую степень очистки крови от низких и среднемолекулярных токсинов
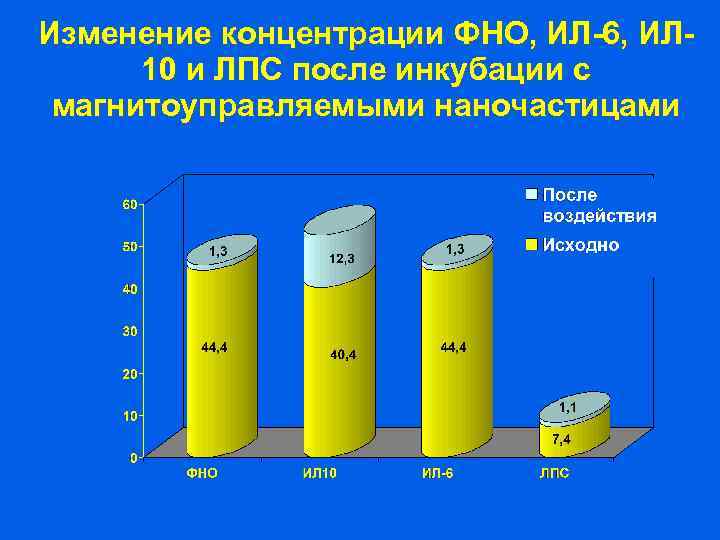 Изменение концентрации ФНО, ИЛ-6, ИЛ 10 и ЛПС после инкубации с магнитоуправляемыми наночастицами
Изменение концентрации ФНО, ИЛ-6, ИЛ 10 и ЛПС после инкубации с магнитоуправляемыми наночастицами
 ЭМД у больных с угрозой кровотечения Угроза послеоперационного кровотечения и критическая тромбоцитопения (менее 20 тыс. в 1 мм 3) не являются абсолютными противопоказаниями для проведения экстракорпоральной детоксикации • ЭКД может выполняться без применения антикоагулянтов с введением в “артериальный” сегмент экстракорпорального контура растворов кристаллоидов. •
ЭМД у больных с угрозой кровотечения Угроза послеоперационного кровотечения и критическая тромбоцитопения (менее 20 тыс. в 1 мм 3) не являются абсолютными противопоказаниями для проведения экстракорпоральной детоксикации • ЭКД может выполняться без применения антикоагулянтов с введением в “артериальный” сегмент экстракорпорального контура растворов кристаллоидов. •
 Осложнения ЭКЛ • • • Кровотечения Тромбозы (внутрисосудистые/на отрезке ЭК контура) Синдром нарушенной осмолярности Острый гемолиз Воздушная эмболия Синдром нового диализатора Эндотоксинемия Хронические, при многолетнем пребывании на программном ГД Травма форменных элементов, тромбоцитопения Эмболия частичками угля при ГС Абсорбция факторов свёртывания крови Кровопотеря вследствие остаточного объёма крови в колонке.
Осложнения ЭКЛ • • • Кровотечения Тромбозы (внутрисосудистые/на отрезке ЭК контура) Синдром нарушенной осмолярности Острый гемолиз Воздушная эмболия Синдром нового диализатора Эндотоксинемия Хронические, при многолетнем пребывании на программном ГД Травма форменных элементов, тромбоцитопения Эмболия частичками угля при ГС Абсорбция факторов свёртывания крови Кровопотеря вследствие остаточного объёма крови в колонке.
 Тромбоз перфузионного катетера
Тромбоз перфузионного катетера
 Трудности, сомнения, неудачи, перспективы… Риск осложнений = противопоказания: Тромбоцитопения, Ранние сроки п/о, Неуверенность в отсутствии источника кровотечения. Антикоагуляция? Критерии отбора больных (сепсис, ОПеч. Н, . . токсичность лек. препаратов), начала и окончания ЭКД, длительности лечения, . . Служба ранней диагностики /профилактики нарушений метаболизма Разработка новых технологий Выведение лек. препаратов (а/б, ХТ)
Трудности, сомнения, неудачи, перспективы… Риск осложнений = противопоказания: Тромбоцитопения, Ранние сроки п/о, Неуверенность в отсутствии источника кровотечения. Антикоагуляция? Критерии отбора больных (сепсис, ОПеч. Н, . . токсичность лек. препаратов), начала и окончания ЭКД, длительности лечения, . . Служба ранней диагностики /профилактики нарушений метаболизма Разработка новых технологий Выведение лек. препаратов (а/б, ХТ)
 ЭМД в интенсивной терапии онкологических больных при органных дисфункциях обоснованны и необходимы.
ЭМД в интенсивной терапии онкологических больных при органных дисфункциях обоснованны и необходимы.



