Молекулярная биотехнология 4.ppt
- Количество слайдов: 145

Экспрессия рекомбинантных генов в эукариотических клетках
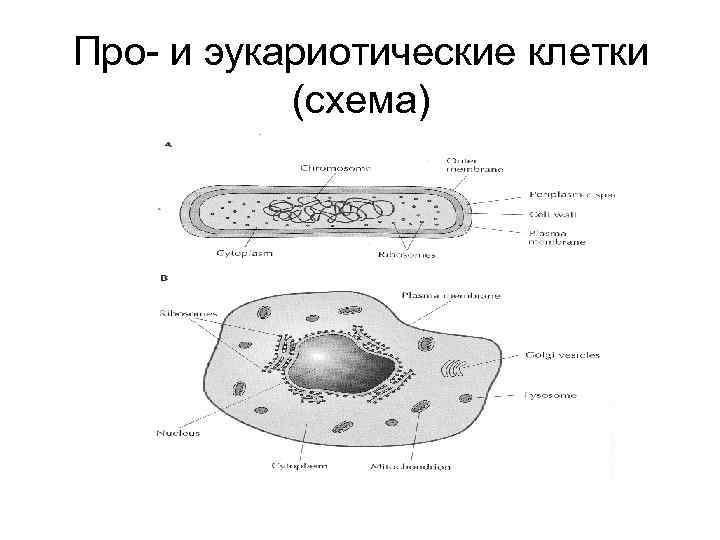
Про- и эукариотические клетки (схема)

Недостатки прокариотических систем • Невозможность экспрессии интронированных эукариотических генов из-за отсутствия сплайсинга у прокариот • Невозможность правильной пострансляционной модификации белков (протеолиз, фосфорилирование, гликозилирование, ацетилирование и др. ) • Нестабильность многих чужеродных белков в прокариотах

Эукариотические клетки, используемые как продуценты рекомбинантных белков • Дрожжи (пекарские дрожжи, метилотрофные дрожжи) • Культуры клеток насекомых • Культуры клеток млекопитающих и птиц

Преимущества эукариотических клеток • Обеспечивается правильное посттрансляционное процессирование рекомбинантных белков, особенно в клетках животных • Дрожжи сочетают достоинства эукариотических и прокариотических клеток

Недостатки эукариотических клеток • Использование эукариотических клеток, особенно клеток животных, менее технологично из-за более медленного размножения клеток и требует больших затрат Время удвоения: • Бактерии – 20 -30 мин • Дрожжи – 1, 5 -2, 5 ч. • Клетки животных – 8 -12 ч.

Пекарские дрожжи. Saccharomyces cerevisiae • • Размер клетки ~10 мкм Геном 1. 4 x 107 пн 16 хромосом Размножается почкованием и половым способом • Время удвоения – 1, 5 -2, 5 ч. • Образует колонии на агаре, легко культивируется в биореакторах

Векторы для дрожжевой системы • Вирусы дрожжей не описаны • Обнаружен один вид плазмиды – 2 мкм ДНК • На основе этой плазмиды получены векторы для дрожжей, в том числе челночные плазмиды

Челночный вектор • Способен размножаться и в бактерии и в эукариотической клетке • Содержит два участка ori – про- и эукариотический • Содержит селективные маркеры для прокариотических и для эукариотических клеток
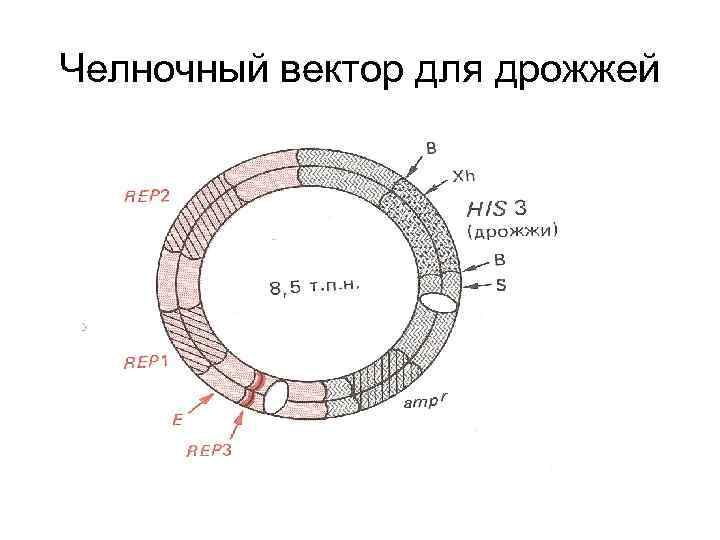
Челночный вектор для дрожжей
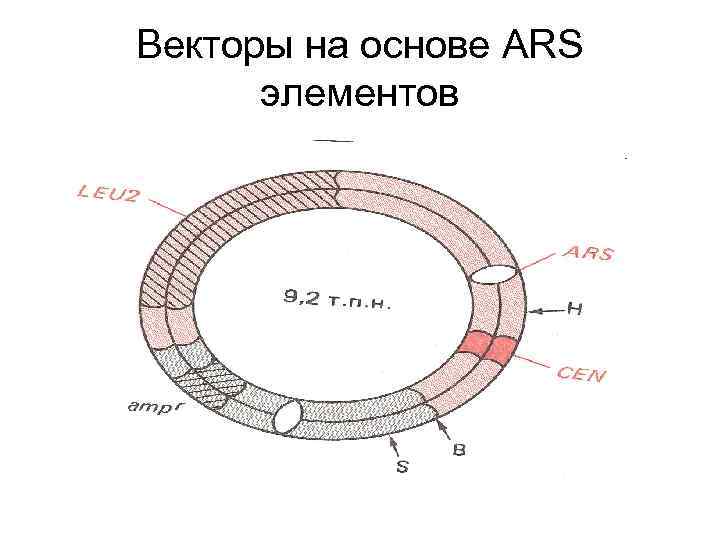
Векторы на основе ARS элементов

Трансфекция дрожжевых клеток • Клетки дрожжей имеют полисахаридную клеточную стенку, окружающую цитоплазматическую мембрану. Эта стенка не пропускает молекулы ДНК. • Клеточную стенку разрушают полисахаридрасщепляющим ферментом и получают сферопласты, которые обрабатывают Ca. Cl 2 и трансфицируют ДНК. Клеточная стенка восстанавливается при культивировании.

Неинтегративная и интегративная трансформация • Неинтегративная трансформация клетки достигается за счет размножения плазмиды в клеточном ядре. • Интегративная трансформация – результат интеграции части плазмиды с интересующим геном в хромосому.

Стабильная и нестабильная трансформация клеток • В отсутствие селективного давления автономные плазмиды легко утрачиваются (нестабильная трансформация) • Интегрированный ген обычно стабильно сохраняется в геноме, если не влияет негативно на жизнеспособность клетки (стабильная трансформация)
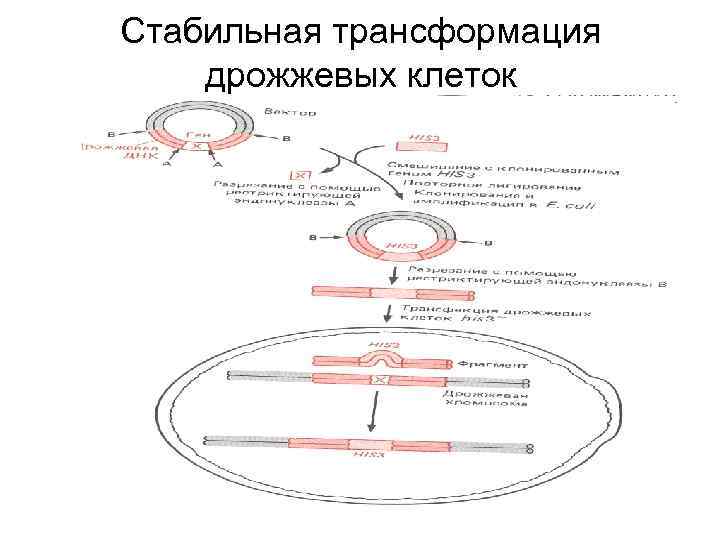
Стабильная трансформация дрожжевых клеток
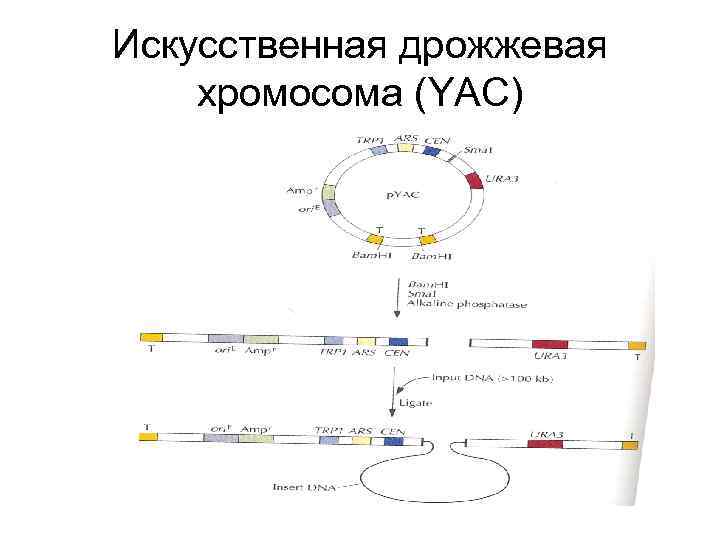
Искусственная дрожжевая хромосома (YAC)

Системы селекции для дрожжей • Использование мутантов дрожжей, дефектных по генам синтеза аминокислот (лейцин, гистидин, триптофан) и азотистых оснований. Маркерами являются гены LEU, HIS, TRP, URA и др. • Использование гена NEO устойчивости к антибиотику G 418 (генетицину)
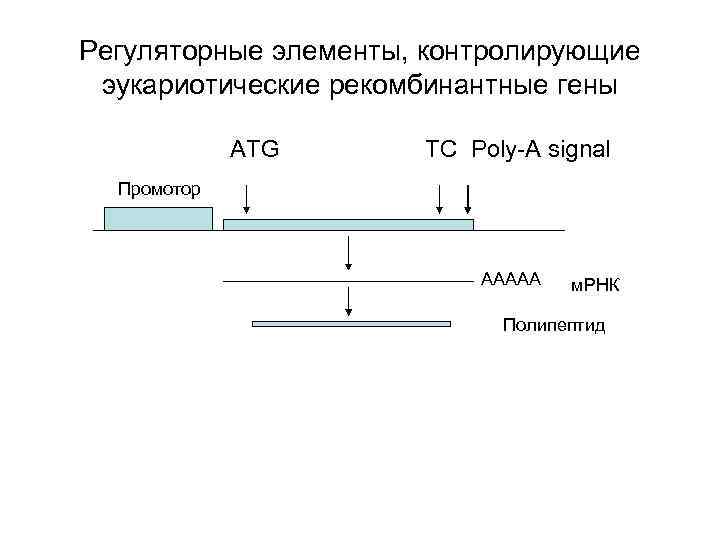
Регуляторные элементы, контролирующие эукариотические рекомбинантные гены ATG TC Poly-A signal Промотор AAAAA м. РНК Полипептид
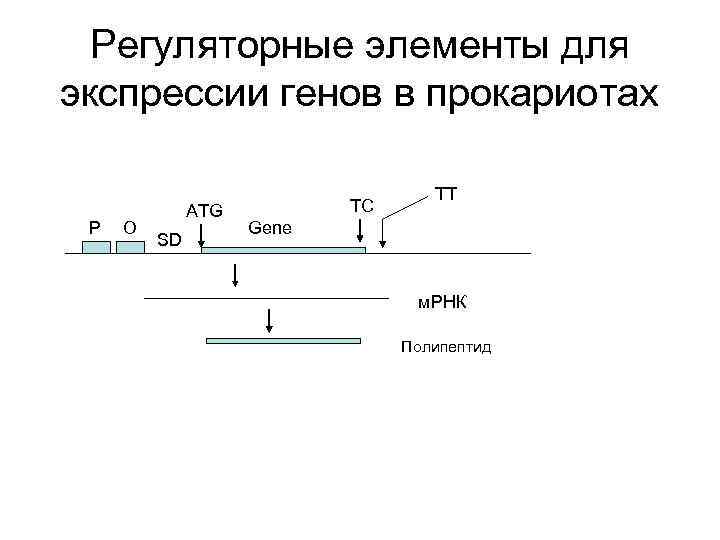
Регуляторные элементы для экспрессии генов в прокариотах P O ATG SD TC TT Gene м. РНК Полипептид

Дрожжевые промоторы • Промотор гена CYC 1 (кодирует цитохром С) • Промотор гена алкоголь-оксидазы (AOX 1)

Метилотрофные дрожжи • Метилотрофные дрожжи используют метиловый спирт в качестве источника углерода • Они накапливаются в большом количестве • Удобны для наработки рекомбинантных белков под контролем промотора гена алкоголь-оксидазы (АОХ 1)

Использование метилотрофных дрожжей Pichia pastoris для наработки белков
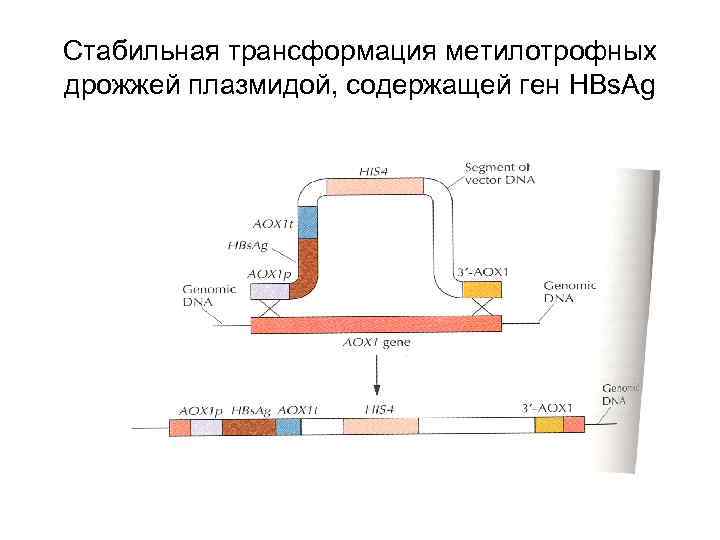
Стабильная трансформация метилотрофных дрожжей плазмидой, содержащей ген HBs. Ag

Рекомбинантные продукты, полученные в дрожжевых системах • • HBs. Ag (вакцина против гепатита В) Белки малярийного плазмодия Оболочечный антиген HIV Лекарственные белки человека (эпидермальный фактор роста, альфа 1 антитрипсин, факторы свёртываемости крови и др. )

Клетки животных в культуре • Первичные и вторичные культуры • Диплоидные штаммы клеток • Перевиваемые линии клеток

Векторы для клеток животных • Вирусы (поксвирусы, аденовирусы, полиома- и папилломавирусы, ретровирусы, бакуловирусы и др. ) • Прокариотические плазмиды
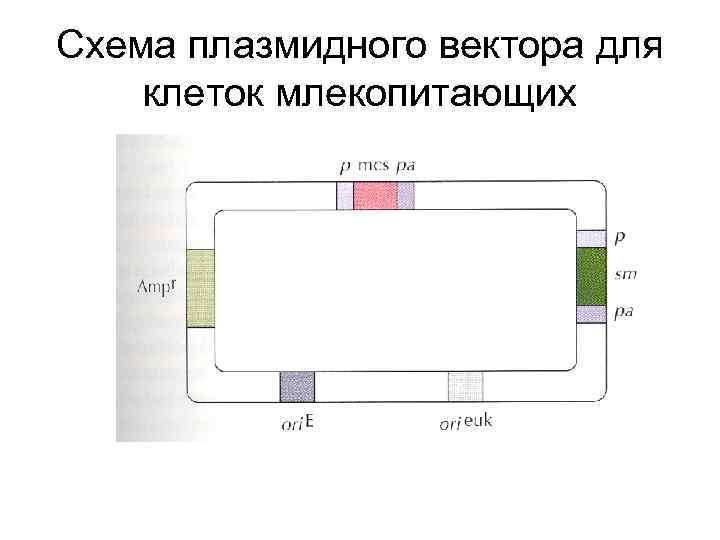
Схема плазмидного вектора для клеток млекопитающих

Введение плазмидных векторов в клетки • Кальций-фосфатный метод (Ca. Cl 2+ Na 3 PO 4 Ca 3(PO 4)2 • Полибрен, ДЕАЕ-декстран • Липосомы • Электропорация • Бомбардировка частичками золота

Селекция трансформированных клеток • Ген устойчивости к G 418 (генетицину) • Ген устойчивости к пуромицину • Устойчивость к аминоптерину или метотрексату • Устойчивость к микофеноловой кислоте • Окраска (lac. Z) или флуоресценция (флуоресцентные белки)

Транзиторная экспрессия генов в эукариотических клетках • В большинстве трансфицированных клеток происходит транзиторная (временная, проходящая) экспрессия трансфицированного гена, достигающая максимума через 2 -3 дня и спадающая к 6 -7 дню после трансфекции. • Небольшая часть трансфицированных клеток становится стабильно трансформированной.

Стабильная трансформация клеток животных рекомбинантными плазмидами • Попав в клеточное ядро, рекомбинантные плазмиды способны встраиваться в геном клетки, что ведет к стабильной трансформации • Встройка обычно происходит по принципу случайной рекомбинации • Существуют способы увеличения числа копий встроенного гена
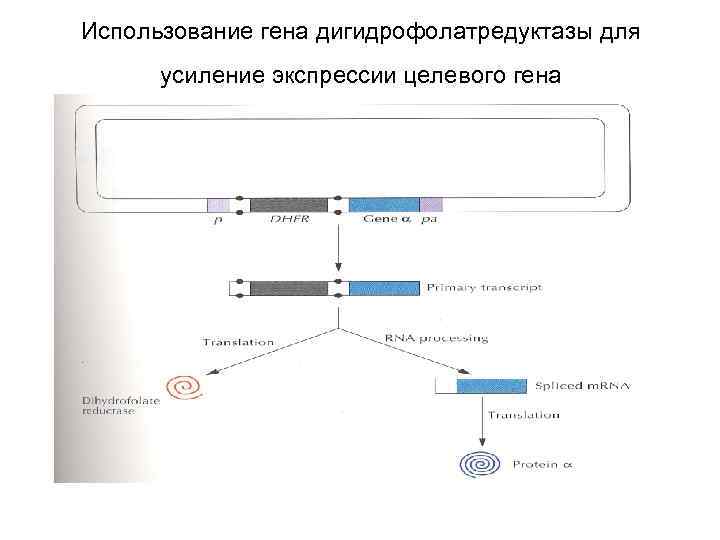
Использование гена дигидрофолатредуктазы для усиление экспрессии целевого гена

Увеличения числа копий введенного гена • Выращивание клеток в присутствии аминоптерина ведет к амплификации участка генома, содержащего ген дигидрофолатредуктазы (ДГФР) и прилежащие гены • При этом резко увеличивается число копий гена ДГФР и расположенных рядом с ним генов. Количество продукта значительно увеличивается.

Эритропоэтин • Важное лекарство – эритропоэтин – было получено в клетках СНО после амплификации гена эритропоэтина, встроенного рядом с геном ДГФР
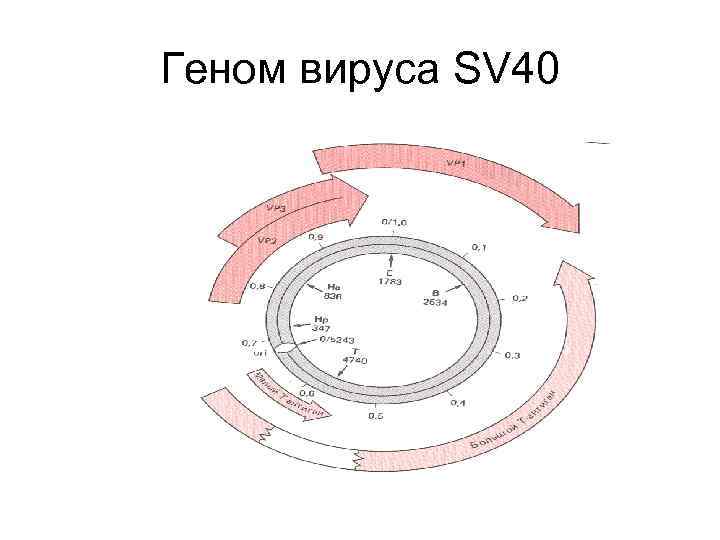
Геном вируса SV 40

Размножение плазмид в клетках животных • Обезьяньи СOS клетки Я. Глузмана • Эти клетки продуцируют Т антиген вируса SV 40 • T антиген, связываясь с ori SV 40, вызывает репликацию вирусной ДНК клеточной репликационной машиной • Если ori SV 40 включен в плазмиду, она будет реплицироваться в COS клетках

Бакуловирусная система • Вирус множественного ядерного полиэдроза – ДНК-содержащий вирус с кольцевой дц. ДНК ~120 тпн, поражает насекомых свыше 30 видов, вызывает образование полиэдров в ядрах клеток • Полиэдры построены из вирусного белка полиэдрина. • Ген полиэдрина имеет мощный промотор
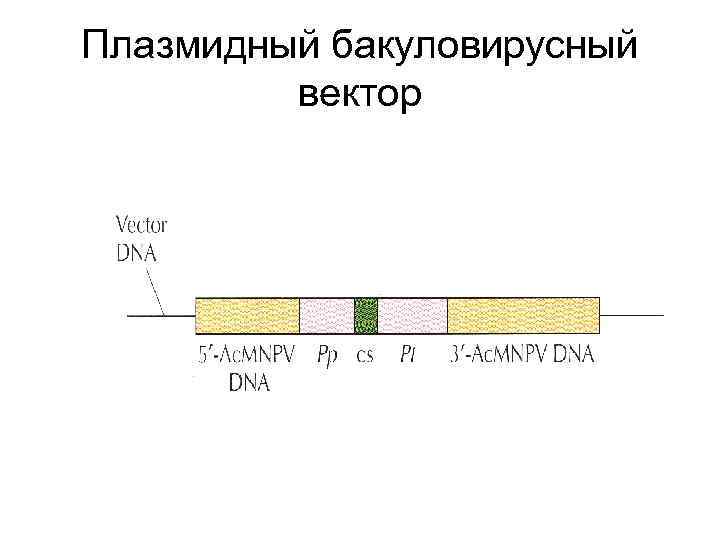
Плазмидный бакуловирусный вектор

Получение рекомбинантного бакуловируса • Клетки заражают «диким» бакуловирусом • Трансфицируют зараженные клетки плазмидой, содержащей участок вирусной ДНК и ген интереса • В результате гомологичной рекомбинации ген интереса встраивается в вирусную ДНК • Затем отбирают и клонируют рекомбинантные вирионы методом бляшек
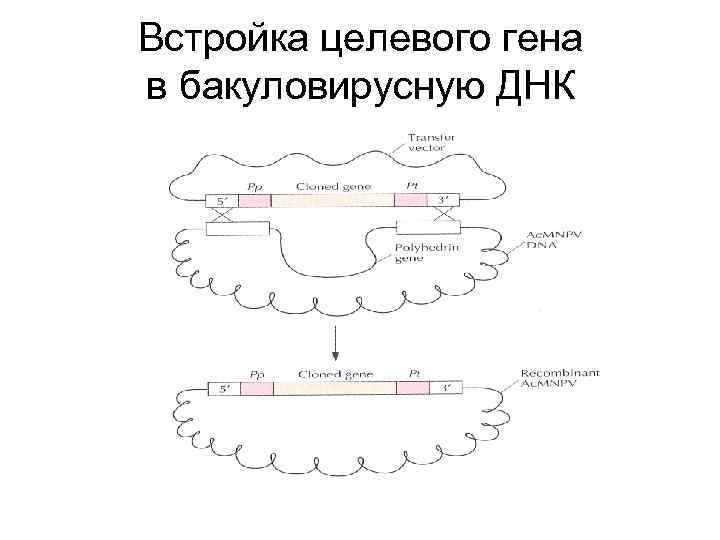
Встройка целевого гена в бакуловирусную ДНК

Получение рекомбинантного белка в бакуловирусной системе • Культуру клеток насекомых заражают рекомбинантным бакуловирусом • Целевой белок образуется в заражённых клетках и может быть выделен и очищен из культуральной жидкости или клеточного экстракта

Рекомбинантные белки, полученные в бакуловирусной системе • В системе получены сотни рекомбинантных белков различного назначения • Недавно была разработана вакцина против папилломавирусных инфекций, вызывающих рак шейки матки (антигены для этой вакцины нарабатываются в бакуловирусной системе)

Трансгенные животные

Биологические системы, используемые молекулярной биотехнологией • • Вирусы Прокариоты Дрожжи Культура клеток животных и человека (клетки насекомых, птиц, млекопитающих), растений • Животные • Растения

Трансгенные животные • Трансгенные животные - это животные, в геном которых искусственно встроен чужеродный генетический материал • Чужеродный ген содержится во всех клетках трансгенного организма

ТРАНСГЕНЫ И ТРАНСГЕНЕЗ • ТРАНСГЕНЫ: ВСТРОЕННЫЙ ГЕНЕТИЧЕСКИЙ МАТЕРИАЛ ОБОЗНАЧАЕТСЯ ТЕРМИНОМ “ТРАНСГЕН” • ТРАНСГЕНЕЗ: ПРОЦЕСС ПОЛУЧЕНИЯ ТРАНСГЕННЫХ ОРГАНИЗМОВ ОБОЗНАЧАЕТСЯ ТЕРМИНОМ “ТРАНСГЕНЕЗ”

Подготовка генной конструкции для трансгенеза • Экспрессирующие векторы (плазмиды) – такие же, как для экспрессии генов в клетках животных. Они должны содержать регуляторные элементы (промоторы, энхенсеры и др. ), соответствующие поставленной задаче • Специальные конструкции для введения гена в заданную область генома
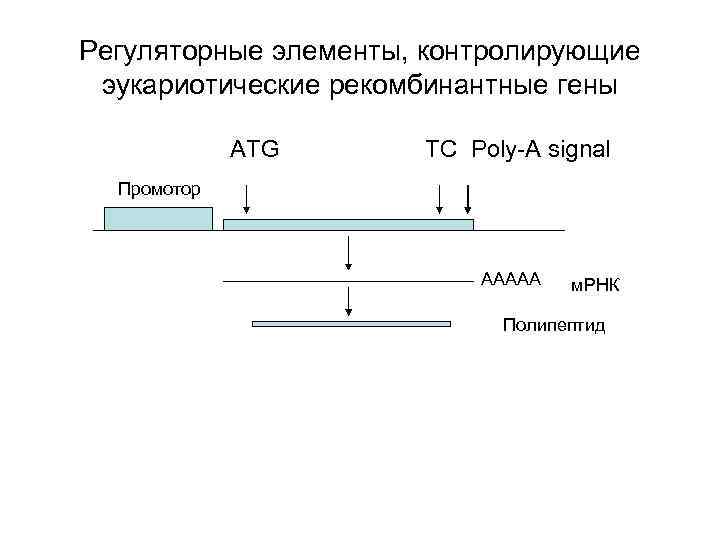
Регуляторные элементы, контролирующие эукариотические рекомбинантные гены ATG TC Poly-A signal Промотор AAAAA м. РНК Полипептид

Стабильная трансформация клеток животных трансгеном • В качестве трансгенов используют линейную ДНК, освобожденную от плазмидных последовательностей • Попав в клеточное ядро, трансгены способны встроиться в геном клетки, что ведет к стабильной трансформации трансфицированной клетки • Встройка обычно происходит по принципу случайной (негомологичной) рекомбинации

ВИДЫ ЖИВОТНЫХ, ИСПОЛЬЗУЕМЫЕ ДЛЯ ТРАНСГЕНЕЗА • • • ДРОЗОФИЛЫ ЗЕМНОВОДНЫЕ МЫШИ КРОЛИКИ КОЗЫ ОВЦЫ СВИНЬИ КОРОВЫ КУРЫ РЫБЫ

ОБЩАЯ СХЕМА ПОЛУЧЕНИЯ ТРАНСГЕННЫХ ЖИВОТНЫХ • • • ПОЛУЧЕНИЕ ОПЛОДОТВОРЕННЫХ ЯЙЦЕКЛЕТОК ВВЕДЕНИЕ КЛОНИРОВАННОГО ГЕНА В ЯДРО ОПЛОДОТВОРЕННОЙ ЯЙЦЕКЛЕТКИ ИМПЛАНТАЦИЯ ТАКИХ ЯЙЦЕКЛЕТОК В МАТКУ ПОДГОТОВЛЕННОЙ САМКИ ВЫЯВЛЕНИЕ ЖИВОТНЫХ, СОДЕРЖАЩИХ ТРАНСГЕН, СРЕДИ РОДИВШЕГОСЯ ПОТОМСТВА СКРЕЩИВАНИЕ ОСОБЕЙ, СОДЕРЖАЩИХ ТРАНСГЕН, ДЛЯ ВЫВЕДЕНИЯ ЛИНИИ ТРАНСГЕННЫХ ЖИВОТНЫХ

Введение трансгена • Введение трансгена с помощью ретровируса • Микроинъекции трансгена в яйцеклетку, микроманипуляторы

ТРАНСГЕННЫЕ МЫШИ • • ПОЛУЧЕНИЕ ОПЛОДОТВОРЕННЫХ ЯЙЦЕКЛЕТОК ОТ СУПЕРОВУЛИРОВАН-НЫХ САМОК (ДО 35 ЯЙЦЕКЛЕТОК ВМЕСТО ОБЫЧНЫХ 5 -10) МИКРОИНЪЕКЦИЯ ТРАНСГЕНА В МУЖСКОЙ ПРОНУКЛЕУС ИМПЛАНТАЦИЯ ИНОКУЛИРОВАННЫХ ЯЙЦЕКЛЕТОК В МАТКУ ПОДГОТОВЛЕННЫХ САМОК ПОЛУЧЕНИЕ И АНАЛИЗ ПОТОМСТВА НА НАЛИЧИЕ ТРАНСГЕНА (БЛОТ-ГИБРИДИЗАЦИЯ И ПЦР)
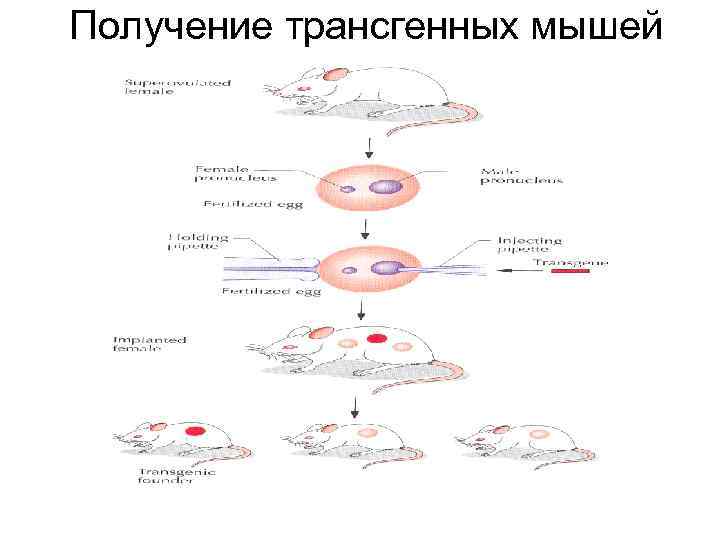
Получение трансгенных мышей

ЭМБРИОНАЛЬНЫЕ СТВОЛОВЫЕ (ЭС) КЛЕТКИ • ЭС КЛЕТКИ – НЕДИФФЕРЕНЦИРОВАННЫЕ КЛЕТКИ, ДАЮЩИЕ НАЧАЛО ВСЕМ ТКАНЯМ ОРГАНИЗМА • ИСПОЛЬЗОВАНИЕ ДЛЯ ПОЛУЧЕНИЯ ТРАНСГЕННЫХ МЫШЕЙ • ВВЕДЕНИЕ ТРАНСГЕНА В ЗАДАННОЕ МЕСТО ГЕНОМА

ПОЛУЧЕНИЕ ЭС КЛЕТОК • • ЭС КЛЕТКИ ПОЛУЧАЮТ ИЗ ВНУТРЕННЕЙ КЛЕТОЧНОЙ МАССЫ БЛАСТОЦИСТА КУЛЬТИВИРОВАНИЕ ЭТИХ КЛЕТОК ПОЗВОЛЯЕТ ПОЛУЧИТЬ ПЕРЕВИВАЕМЫЕ КЛЕТОЧНЫЕ ЛИНИИ, ПРИГОДНЫЕ ДЛЯ ПОЛУЧЕНИЯ ТРАНСГЕННЫХ ЖИВОТНЫХ
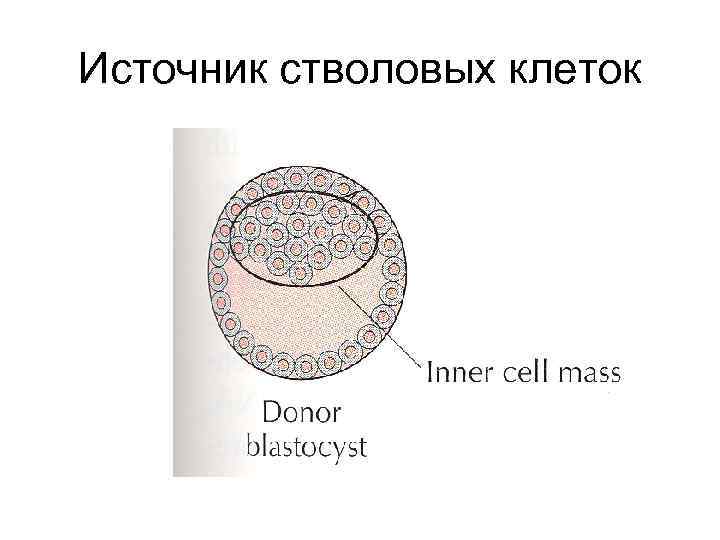
Источник стволовых клеток

ИСПОЛЬЗОВАНИЕ ЭС КЛЕТОК ДЛЯ ТРАНСГЕНЕЗА • ПОДГОТОВКА ЭС КЛЕТОК • ТРАНСФЕКЦИЯ ЭС КЛЕТОК ТРАНСГЕНОМ, ОТБОР ТРАНСФОРМИРОВАННЫХ КЛЕТОК • ВВЕДЕНИЕ ТРАНСФОРМИРОВАННЫХ ТРАНСГЕНОМ ЭС КЛЕТОК В БЛАСТОЦИСТЫ • ИМПЛАНТАЦИЯ БЛАСТОЦИСТОВ ПОДГОТОВЛЕННЫМ САМКАМ • ПОЛУЧЕНИЕ ПОТОМСТВА И ЕГО АНАЛИЗ НА НАЛИЧИЕ ТРАНСГЕНА

Введение трансгенов в ЭС клетки • Кальций-фосфатный метод Ca. Cl 2+ Na 3 PO 4 Ca 3(PO 4)2 • Полибрен, ДЕАЕ-декстран • Липосомы • Электропорация
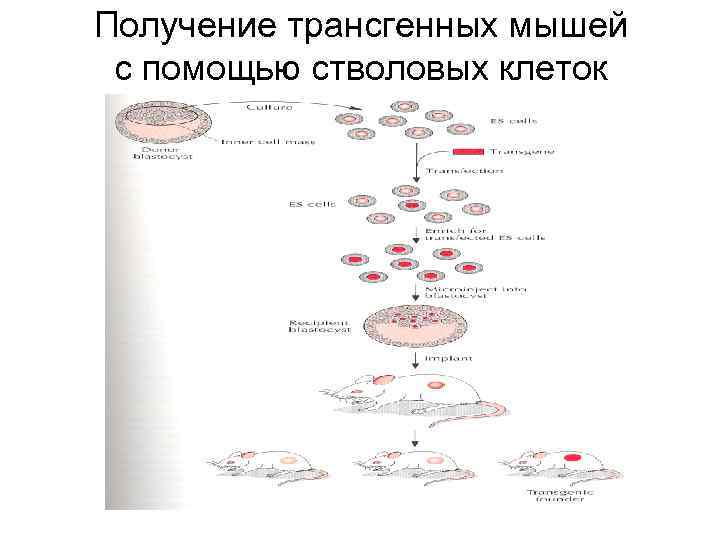
Получение трансгенных мышей с помощью стволовых клеток

ВВЕДЕНИЕ ТРАНСГЕНА В ЗАДАННОЕ МЕСТО ГЕНОМА • ОБЫЧНО ТРАНСГЕН НЕ ИМЕЕТ ОПРЕДЕЛЕННОГО АДРЕСА ДЛЯ ВСТРОЙКИ • ДЛЯ ВВЕДЕНИЯ ТРАНСГЕНА В ЗАДАННЫЙ УЧАСТОК ГЕНОМА ИСПОЛЬЗУЮТ ПРИНЦИП ГОМОЛОГИЧНОЙ РЕКОМБИНАЦИИ

ГЕН ТИМИДИНКИНАЗЫ (tk) ВИРУСА ПРОСТОГО ГЕРПЕСА • TK ГЕНЫ ФОСФОРИЛИРУЮТ ТИМИДИН, ПРЕВРАЩАЯ ЕГО В ТМР (Td. R-PO 4) • TK ГЕН ВПГ ОТЛИЧАЕТСЯ НИЗКОЙ СПЕЦИФИЧНОСТЬЮ И СПОСОБЕН ФОСФОРИЛИРОВАТЬ ЦИТИДИН И «НЕПРАВИЛЬНЫЕ» НУКЛЕОЗИДЫ (НАПРИМЕР, ГАНЦИКЛОВИР). • ФОСФОРИЛИРОВАННЫЙ ГАНЦИКЛОВИР УБИВАЕТ КЛЕТКУ
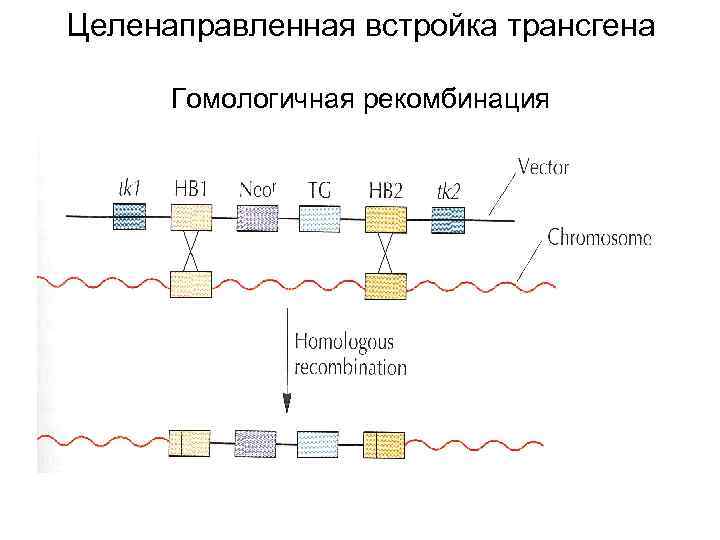
Целенаправленная встройка трансгена Гомологичная рекомбинация
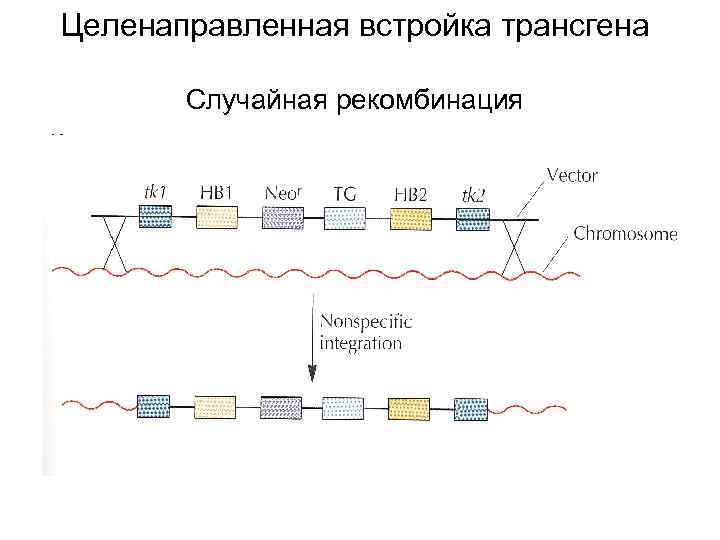
Целенаправленная встройка трансгена Случайная рекомбинация

Позитивная и негативная селекция Ген Ингибитор Рост клеток (позитивная селекция) Neo G 418 Neo + G 418 + (негативная селекция) tk HSV ганцикловир + tk HSV+ ганцикловир -

ИСПОЛЬЗОВАНИЕ ТРАНСГЕННЫХ МЫШЕЙ • • ИЗУЧЕНИЕ ФУНКЦИИ ГЕНОВ ПОИСК ТКАНЕСПЕЦИФИЧЕСКИХ ПРОМОТОРОВ

НОКАУТ ГЕНОВ У МЫШЕЙ • Нокаут гена – это его инактивация во всех клетках организма • Это достигается встройкой маркерного гена внутрь нокаутируемого гена

ТКАНЕСПЕЦИФИЧЕСКАЯ ЭКСПРЕССИЯ ГЕНОВ У ТРАНСГЕННЫХ МЫШЕЙ • Выявление промоторов, способных экспрессироваться в строго определенных тканях (в поджелудочной железе, в мозгу, в молочной железе и т. д. ) • Поставив онкоген под соответствующий промотор, можно вызвать опухоли у трансгенных мышей в определенной ткани или органе

ИСПОЛЬЗОВАНИЕ ТРАНСГЕННЫХ МЫШЕЙ • ИЗУЧЕНИЕ ФУНКЦИИ ГЕНОВ • ПОИСК ТКАНЕСПЕЦИФИЧЕСКИХ ПРОМОТОРОВ • СОЗДАНИЕ МОДЕЛЕЙ БОЛЕЗНЕЙ ЧЕЛОВЕКА: – БОЛЕЗНЬ АЛЬЦГЕЙМЕРА (ГЕН ПРЕДШЕСТВЕННИКА БЕТААМИЛОИДНОГО БЕЛКА) – МЫШИ, ЧУВСТВИТЕЛЬНЫЕ К ВИРУСУ ПОЛИОМИЕЛИТА

Болезнь Альцгеймера • Накопление сенильных бляшек в синапсах нейронов • Бляшки содержат амилоид бета (Аβ, 4 к. Д) • Ген предшественника Аβ кодирует белокпредшественник Аβ (АРР) • Мутации в гене АРР ведут к накоплению Аβ • Мыши, трансгенные по мутантному гену АРР, проявляют симптомы болезни и характерные патологические изменения

МЫШИ, ЧУВСТВИТЕЛЬНЫЕ К ВИРУСУ ПОЛИОМИЕЛИТА • Рецептор полиовируса отсутствует в клетках мышей, поэтому они нечувствительны к этому вирусу • Мыши, трансгенные по гену рецептора полиовируса, чувствительны к нему и могут использоваться для контроля полиомиелитной вакцины вместо обезьян

ИСПОЛЬЗОВАНИЕ ТРАНСГЕННЫХ МЫШЕЙ • ИЗУЧЕНИЕ ФУНКЦИИ ГЕНОВ • ПОИСК ТКАНЕСПЕЦИФИЧЕСКИХ ПРОМОТОРОВ • СОЗДАНИЕ МОДЕЛЕЙ БОЛЕЗНЕЙ ЧЕЛОВЕКА • МОДЕЛЬНЫЕ ЭКСПЕРИМЕНТЫ ПО ПРОДУКЦИИ БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ (БАВ)

ПРОДУКЦИЯ БАВ В МОЛОЧНОЙ ЖЕЛЕЗЕ ТРАНСГЕННЫХ ЖИВОТНЫХ • МОЛОЧНАЯ ЖЕЛЕЗА - ФАБРИКА ПО • • • СИНТЕЗУ БЕЛКОВ (ДО 600 КГ/КОРОВА/ПЕРИОД ЛАКТАЦИИ). ГЛАВНЫЕ БЕЛКИ: АЛЬФА-S 1 -КАЗЕИН АЛЬФА-S 2 -КАЗЕИН, БЕТА-КАЗЕИН КАППА-КАЗЕИН ЛАКТАЛЬБУМИН

ПРОМОТОРЫ, СПЕЦИФИЧНЫЕ ДЛЯ МОЛОЧНОЙ ЖЕЛЕЗЫ • ГЕНЫ КАЗЕИНОВ И ЛАКТАЛЬБУМИНА ИМЕЮТ ПРОМОТОРЫ, СПЕЦИФИЧНЫЕ ДЛЯ МОЛОЧНОЙ ЖЕЛЕЗЫ • ГЕН, КОНТРОЛИРУЕМЫЙ ТАКИМ ПРОМОТОРОМ, ЭКСПРЕССИРУЕТСЯ ИЗБИРАТЕЛЬНО В МОЛОЧНОЙ ЖЕЛЕЗЕ • ЕГО БЕЛКОВЫЙ ПРОДУКТ ВЫДЕЛЯЕТСЯ В МОЛОКО, ОТКУДА ОН МОЖЕТ БЫТЬ ПОЛУЧЕН В ЧИСТОМ ВИДЕ

• • • ТРАНСГЕННЫЕ СЕЛЬСКОХОЗЯЙСТВЕННЫЕ ЖИВОТНЫЕ КОЗЫ ОВЦЫ СВИНЬИ КОРОВЫ КУРЫ

НЕКОТОРЫЕ БИОЛОГИЧЕСКИ АКТИВНЫЕ БЕЛКИ, ПОЛУЧАЕМЫЕ С ПОМОЩЬЮ ТРАНСГЕННЫХ ЖИВОТНЫХ БЕЛОК • • • ЖИВОТНОЕ ТКАНЕВОЙ АКТИВАТОР ПЛАЗМИНОГЕНА - КОЗА УРОКИНАЗА КОЗА ФАКТОР IX СВЕРТЫВАНИЯ КРОВИ ОВЦА ЛАКТОФЕРРИН КОЗА КОРОВ А • ХИМОЗИН ОВЦА

ИЗМЕНЕНИЕ БИОЛОГИЧЕСКИХ СВОЙСТВ ТРАНСГЕННЫХ ЖИВОТНЫХ • УСТОЙЧИВОСТЬ К ИНФЕКЦИЯМ, • УСКОРЕНИЕ РОСТА (ГЕН ГОРМОНА РОСТА) • ДРУГИЕ СВОЙСТВА

НАУЧНОЕ И БИОТЕХНОЛОГИЧЕСКОЕ ЗНАЧЕНИЕ ТРАНСГЕННЫХ ЖИВОТНЫХ • • ОПРЕДЕЛЕНИЕ ФУНКЦИИ ТРАНСГЕНА СОЗДАНИЕ МОДЕЛЕЙ НЕКОТОРЫХ БОЛЕЗНЕЙ ЧЕЛОВЕКА ПОЛУЧЕНИЕ БИОЛОГИЧЕСКИ АКТИВНЫХ БЕЛКОВ УЛУЧШЕНИЕ СВОЙСТВ СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ

ПЕРСПЕКТИВЫ • СОЗДАНИЕ НОВЫХ ПОРОД СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ С РАЗЛИЧНЫМИ ПОЛЕЗНЫМИ СВОЙСТВАМИ • СУЩЕСТВЕННОЕ РАСШИРЕНИЕ АССОРТИМЕНТА БАВ, ПОЛУЧАЕМЫХ В ТРАНСГЕННЫХ ЖИВОТНЫХ

Трансгенные растения

Трансгенные растения • это растения, в каждой клетке которых присутствует чужеродный ген (трансген), подготовленный методом генетической инженерии (рекомбинантной ДНК) • получение трансгенных растений трансгенез

Для чего нужны трансгенные растения? • Устойчивость к вредителям (насекомым, вирусам, бактериям, грибкам) • Устойчивость к гербицидам и пестицидам • Устойчивость к стрессам • Изменение качества пищи, окраски цветов • Растения как биореакторы

Тотипотентность растительных клеток • Многие типы растительных клеток способны дать начало полноценному растению, т. е. являются тотипотентными • Такие тотипотентные клетки используются для введения в них чужеродных генов при получении трансгенных растений

Стабильная трансформация клеток растений трансгеном • Трансгены вводят в растительные клетки, из которых затем можно получить растения. • Попав в клеточное ядро, трансгены способны встроиться в геном растительной клетки, что ведет к ее стабильной трансформации. • Трансген окажется в каждой клетке растения, полученного из трансформированной клетки. • Встройка обычно происходит по принципу случайной (негомологичной) рекомбинации.

ОБЩАЯ СХЕМА ПОЛУЧЕНИЯ ТРАНСГЕННЫХ РАСТЕНИЙ • • • ВВЕДЕНИЕ КЛОНИРОВАННОГО ГЕНА В ТОТИПОТЕНТНЫЕ РАСТИТЕЛЬНЫЕ КЛЕТКИ СЕЛЕКЦИЯ ТРАНСФОРМИРОВАННЫХ КЛЕТОК ВЫРАЩИВАНИЕ РАСТЕНИЙ ИЗ ТРАНСФОРМИРОВАННЫХ КЛЕТОК ВЫЯВЛЕНИЕ РАСТЕНИЙ, СОДЕРЖАЩИХ ТРАНСГЕН СКРЕЩИВАНИЕ ОСОБЕЙ, СОДЕРЖАЩИХ ТРАНСГЕН, ДЛЯ ВЫВЕДЕНИЯ СТАБИЛЬНОЙ ЛИНИИ ТРАНСГЕННЫХ РАСТЕНИЙ

Подготовка генной конструкции для трансгенеза • Конструкция должна содержать нужный ген, поставленный под контроль соответствующих регуляторных элементов (промоторы, энхансеры, сигналы полиаденилирования и др. ) и быть пригодной для введения в растительную клетку
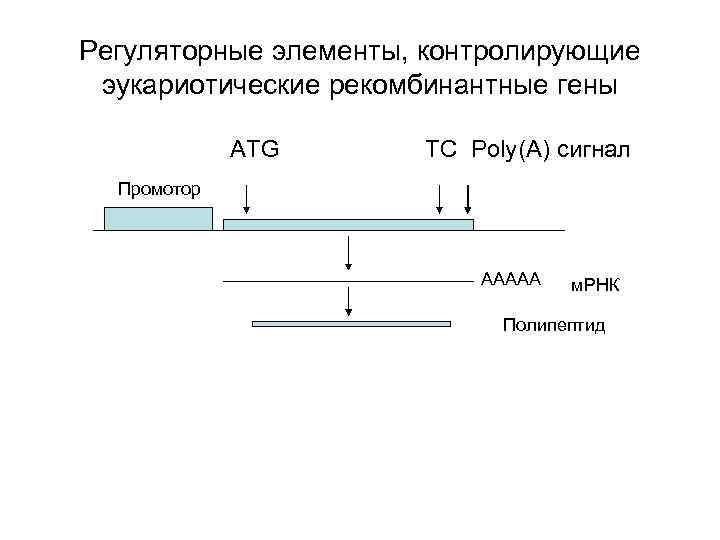
Регуляторные элементы, контролирующие эукариотические рекомбинантные гены ATG TC Poly(A) сигнал Промотор AAAAA м. РНК Полипептид

Векторы для растительных клеток • Растения не имеют собственных плазмид • В качестве векторов, в принципе, могут использоваться вирусы растений (например, ДНК-содержащий вирус мозаики цветной капусты) • Существует специальная система (Tiплазмиды) для трансформации растений

Введение трансгена • Введение трансгена в растительные клетки с помощью Ti-плазмид • Введение трансгенов в протопласты растительных клеток

Agrobacterium tumefaciens • Почвенная грамотрицательная бактерия Agrobacterium tumefaciens способна вызывать опухоли (корончатые галлы) у многих растений • За развитие опухолей отвечают Тiплазмиды (150 -250 тпн), содержащиеся в этих бактериях

Ti (tumor inducing) плазмиды (р. Ti) Типичная Ti-плазмида содержит: • Область вирулентности (6 -8 генов), необходимую для проникновения плазмиды из бактерии в растение • Область Т-ДНК, содержащую гены синтеза растительных гормонов - ауксина и цитокинина, а также опинов – производных аргинина (нопалина, октопина) • Оri (точка начала репликации в агробактерии)
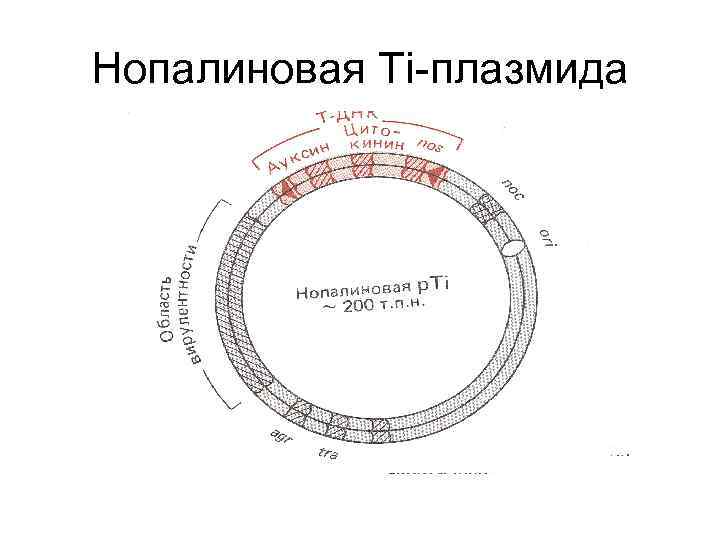
Нопалиновая Тi-плазмида

Два типа регуляторных элементов в p. Ti • Промоторы генов, локализованных в ТДНК, - эукариотические промоторы, распознаваемые РНК-полимеразой II. Эти гены имеют эукариотические сигналы полиаденилирования • Остальные гены p. Ti имеют прокариотические промоторы и сигналы терминации транскрипции
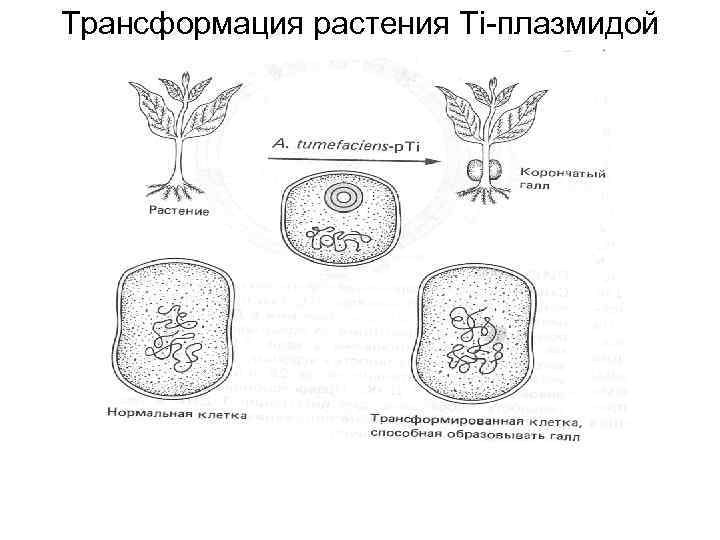
Трансформация растения Ti-плазмидой

Т-плазмиды • Плазмиды Е. coli, содержащие Т-ДНК из Тi-плазмиды, обозначаются как Тплазмиды

Челночные Т-плазмиды для E. coli Содержат: • Т-ДНК, содержащую правую и левую пограничные последовательности из Tiплазмиды (~25 пн) • Ori для репликации в E. coli и агробактерии • Необходимые маркерные гены
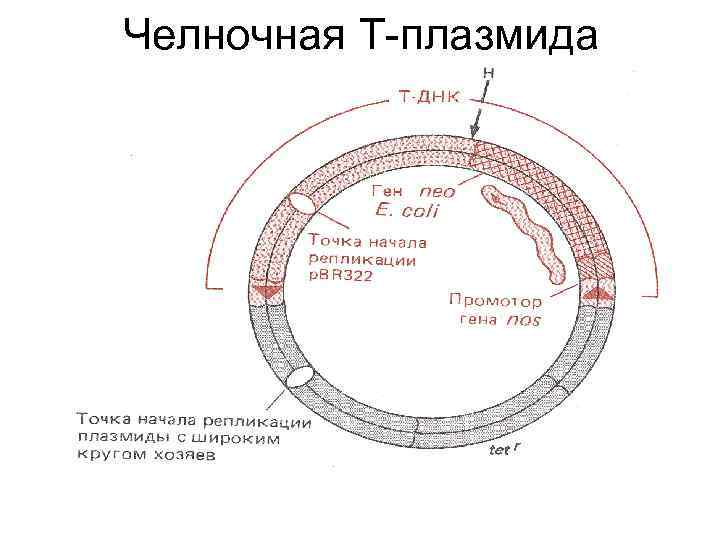
Челночная Т-плазмида

Использование Т-плазмиды могут использоваться: • Для трансформации растительных клеток вместе с Тi-плазмидой (бинарный вектор) • Для переноса встроенного в область ТДНК гена в р. Тi • Для внесения чужеродного гена в протопласты растительных клеток
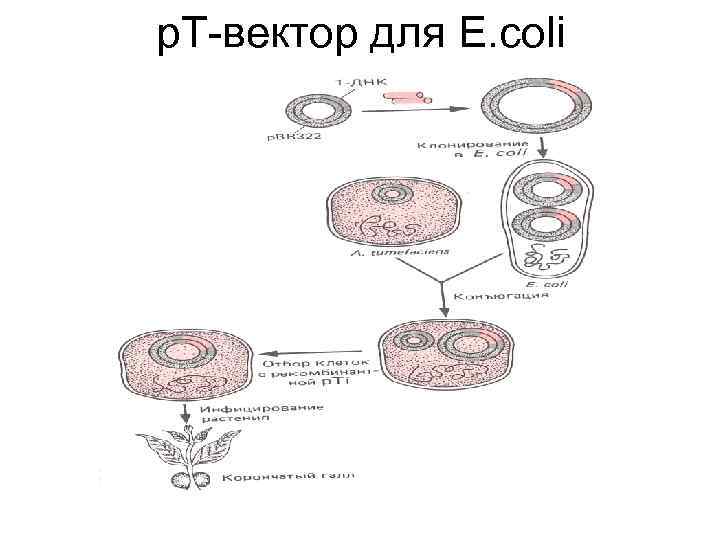
p. T-вектор для E. coli

Введение трансгенов в протопласты растительных клеток • Протопласты растительных клеток получают путем обработки целлюлазой – ферментом, разрушающим целлюлозную стенку клеток • Электропорация • Микроинъекции • Бомбардировка частичками золота

Селективные маркерные гены Для селекции трансформированных растительных клеток используют свыше 10 различных генов. Это гены устойчивости к антибиотикам G 418, гигромицину, блеомицину, бластицидину и др.

Репортерные гены • • Описано около 15 различных репортерных генов, используемых в растениях Ген бета-галактозидазы (Lac. Z) Гены люциферазы (из светлячка, из бактерий) Гены опинсинтетаз Ген хлорамфениколацетилтрансферазы

Разница между селективным и репортерным геном • Селективный ген позволяет выращивать трансформированные клетки и подавлять рост нетрансформированных клеток • Репортерный ген позволяет оценить активность промотора или отличить трансформированные клетки от нетрансформированных без подавления роста последних • Ген может быть только селективным или только репортерным (Lac. Z) или совмещать оба варианта использования

Удаление маркерного гена • Если трансгенное растение предназначено для сельскохозяйственного использования, маркерный ген удаляется генетическими методами (отбор и скрещивание)

Промоторы для экспрессии чужеродных генов в растениях 1. 35 S промотор вируса мозаики цветной капусты 2. Промоторы генов опинов (нопалина, октопина) из р. Тi 3. Другие промоторы растительных генов

Проблема экспрессии чужеродных генов в трансгенных растениях • Добавление энхансеров к 35 S промотору • Введение чужеродного гена в ДНК хлоропластов (в клетке около 10000 хлоропластных геномов) • Модификация кодонов гена (замена кодонов на наиболее используемые) методом точечных мутаций
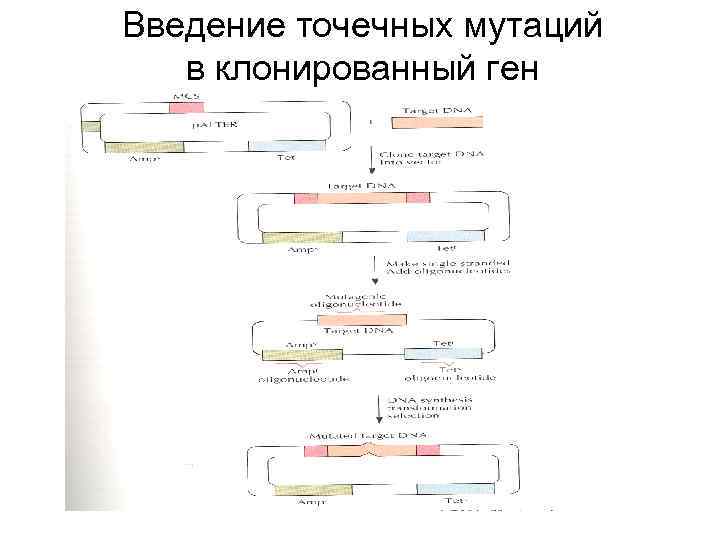
Введение точечных мутаций в клонированный ген
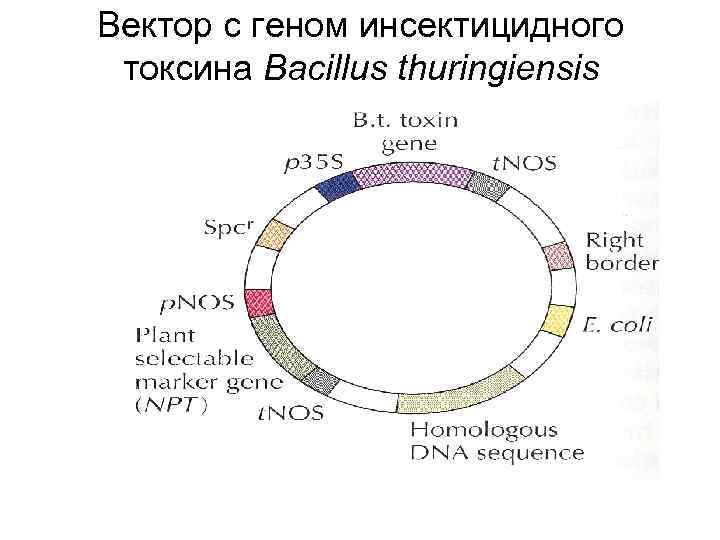
Вектор с геном инсектицидного токсина Bасillus thuringiensis
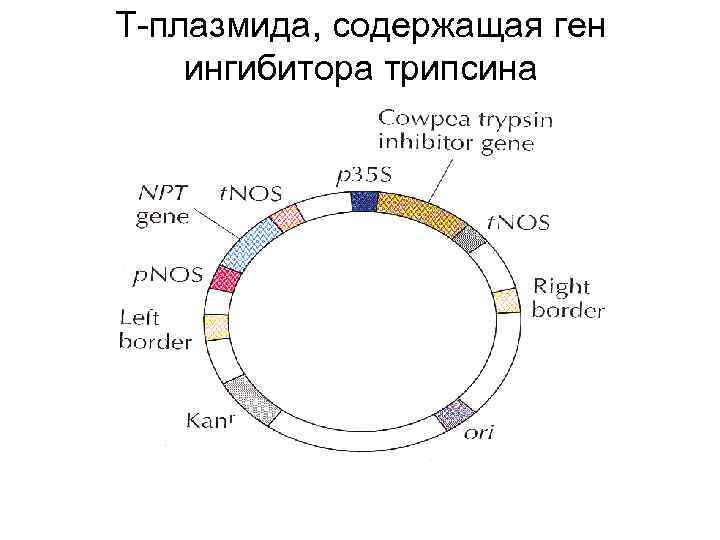
Т-плазмида, содержащая ген ингибитора трипсина

Создание устойчивости к вирусам • Экспрессия гена капсидного вирусного белка в трансгенных растениях подавляет вирусную инфекцию • Антисмысловые РНК подавляют вирусные гены
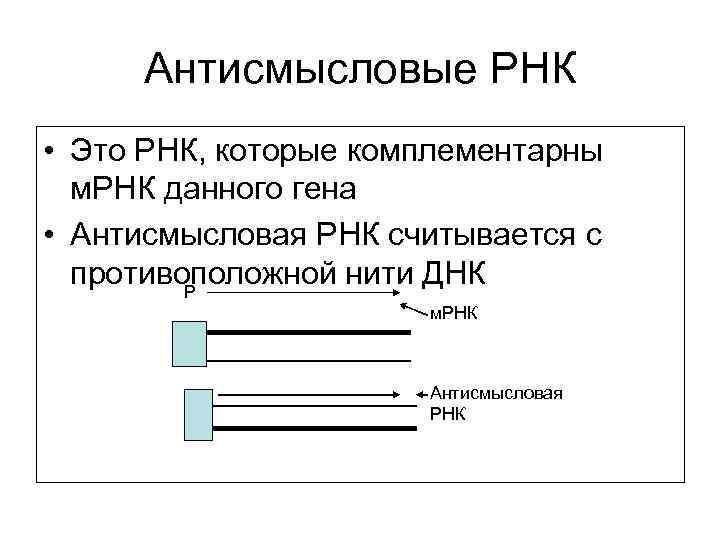
Антисмысловые РНК • Это РНК, которые комплементарны м. РНК данного гена • Антисмысловая РНК считывается с противоположной нити ДНК P м. РНК Антисмысловая РНК

Создание устойчивости к грибкам и бактериям • Гены белков патогенеза (PR) активируются в ответ на бактериальную или грибковую инфекцию • Экспрессия таких белков в трансгенных растениях повышает их устойчивость к инфекции • Пример PR белков – хитиназа, разрушающая оболочку грибковых клеток • Для защиты от бактериальной инфекции используют ген лизоцима фага Т 4

Устойчивость к различным стрессам • Окислительный стресс (ген супероксиддисмутазы) • Солевой стресс (гены синтеза бетаина) • Перезревание и размягчение плодов (подавление гена полигалактуроназы с помощью антисмысловой РНК): томаты FLAVR SAVR (flavor savеr) – 1 -й лицензированный трансгенный продукт (1994)

Создание устойчивости к гербицидам Для повышения устойчивости к гербицидам: • Повышают продукцию белка, повреждаемого гербицидом • Уменьшают способность соответствующего белка связываться с гербицидом • Повышают способность растения разрушать гербицид

Другие возможности трансгенных растений • Изменение пигментации цветов (трансгенные розы, тюльпаны, гвоздики, хризантемы) • Увеличение содержания лизина (в сое) • Улучшение качества растительного масла • Модификация вида и вкуса плодов изменение цвета, повышение сладости (белок монеллин слаще сахара в 10000 раз)

Растения как биореакторы • Растения можно использовать для накопления различных дефицитных белков (антител, вирусных белков для создания вакцин, биологически активных веществ животного и человеческого происхождения)

ТРАНСГЕННЫЕ СЕЛЬСКОХОЗЯЙСТВЕННЫЕ РАСТЕНИЯ • Создано свыше 50 трансгенных сельскохозяйственных растений, часть из них лицензировано • Среди них наиболее практичные и широко используемые виды: соя, рис, картофель, томаты, кукуруза и др.

ПЕРСПЕКТИВЫ • СОЗДАНИЕ НОВЫХ ВАРИАНТОВ СЕЛЬСКОХОЗЯЙСТВЕННЫХ РАСТЕНИЙ С РАЗЛИЧНЫМИ ПОЛЕЗНЫМИ СВОЙСТВАМИ • СУЩЕСТВЕННОЕ РАСШИРЕНИЕ АССОРТИМЕНТА БАВ, ПОЛУЧАЕМЫХ В ТРАНСГЕННЫХ РАСТЕНИЯХ КАК БИОРЕАКТОРАХ
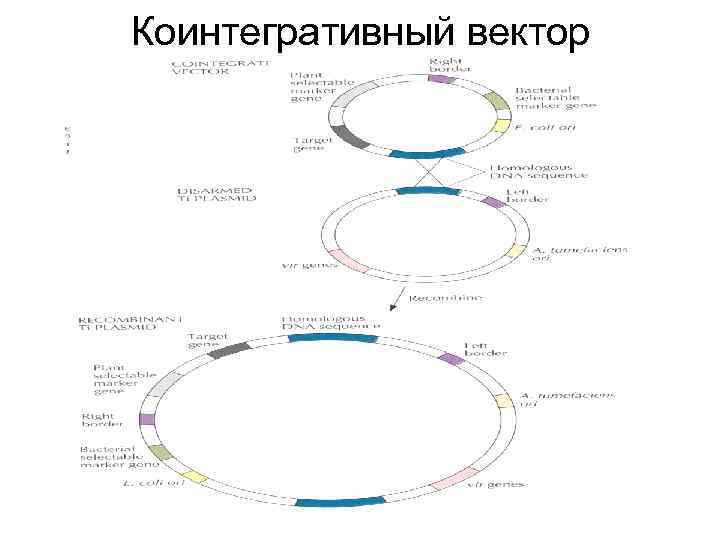
Коинтегративный вектор

Клеточная инженерия и клеточная биотехнология

ВОЗНИКНОВЕНИЕ КЛЕТОЧНОЙ ИНЖЕНЕРИИ И КЛЕТОЧНОЙ БИОТЕХНОЛОГИИ • КУЛЬТУРЫ КЛЕТОК В БИОТЕХНОЛОГИИ ИСПОЛЬЗУЮТСЯ С 1950 -х гг. • В 1960 -е гг. БЫЛА СОЗДАНА ТЕХНОЛОГИЯ ПОЛУЧЕНИЯ ГИБРИДНЫХ КЛЕТОК, ОБЪЕДИНЯЮЩИХ ГЕНОМЫ ДВУХ ТИПОВ КЛЕТОК • ТЕХНОЛОГИЯ ПЕРЕСАДКИ КЛЕТОЧНОГО ЯДРА • СТВОЛОВЫЕ КЛЕТКИ

Клеточная биотехнология Использование клеточных культур для биотехнологических целей 1. Получение полезных продуктов с помощью клеточных культур (вакцины, антитела, БАВ) 2. Использование стволовых клеток в биотехнологии

КЛЕТОЧНАЯ ИНЖЕНЕРИЯ - СОЗДАНИЕ ГЕНЕТИЧЕСКИ ИЗМЕНЁННЫХ КЛЕТОК НА ОСНОВЕ ИХ СЛИЯНИЯ ИЛИ ПЕРЕСАДКИ ЯДЕР

Антитела • Особые белки (иммуноглобулины), возникающие в организме в ответ на введение антигена и способные специфически соединяться с этим антигеном in vitro и in vivo
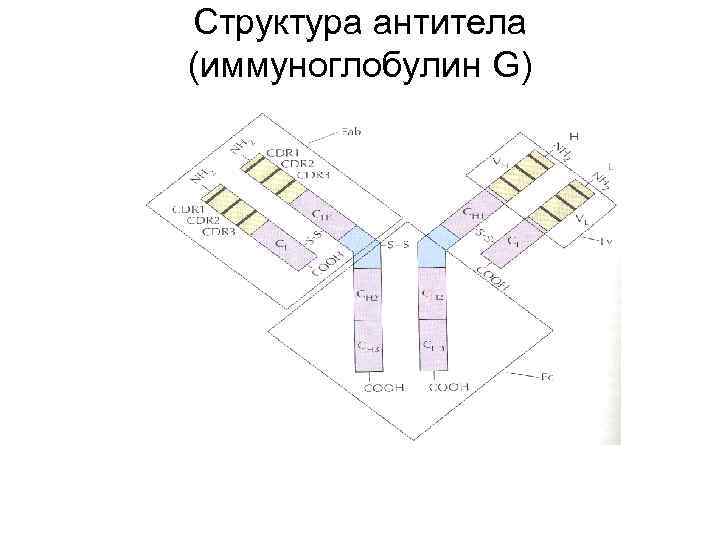
Структура антитела (иммуноглобулин G)

Теории образования антител • Индукционная теория П. Эрлиха • Клональная теория Ф. М. Бернета

Индукционная теория (Пауль Эрлих) • Если организм не встречался с данным антигеном, то антител к нему нет • В ответ на введение антигена клетки начинают производить антитела нужной специфичности • Антиген влияет на специфичность возникающих антител

Клональная теория (Фрэнк Макферлан Бернет) • В эмбриональном периоде развития организма закладываются сотни тысяч клонов В-лимфоцитов, спонтанно образующих антитела разной специфичности • Антиген лишь специфически вызывает размножение клеток тех клонов, которые вырабатывали антитела, способные с ним связываться

Поликлональные антитела • Антиген обычно имеет несколько антигенных детерминант (эпитопов) • Каждый эпитоп вызывает размножение определенного клона В-лимфоцитов и, следовательно, образование антител против этого эпитопа • Таким образом, иммунная сыворотка против данного антигена обычно является поликлональной

Недостатки поликлональных антител • Препарат поликлональных антител включает антитела разной специфичности, в том числе против неспецифических примесей • Препараты поликлональных антител недостаточно стандартны

Моноклональные антитела КЕЛЕР И МИЛЬШТЕЙН (1975) разработали технологию получения МОНОКЛОНАЛЬНЫХ АНТИТЕЛ

Моноклональные антитела - это антитела, которые направлены против одного эпитопа данного антигена и вырабатываются одним клоном В-лимфоцитов

Mетоды выявления антител и антигенов • Существует много различных методов выявления антител и антигенов (реакция преципитации и ее варианты, реакция связывания комплемента и др. ) • Наиболее широко используемый метод - Иммуно. Ферментный Анализ (ИФА), или Enzyme Linked Immuno. Sorbent Assay (ELISA)
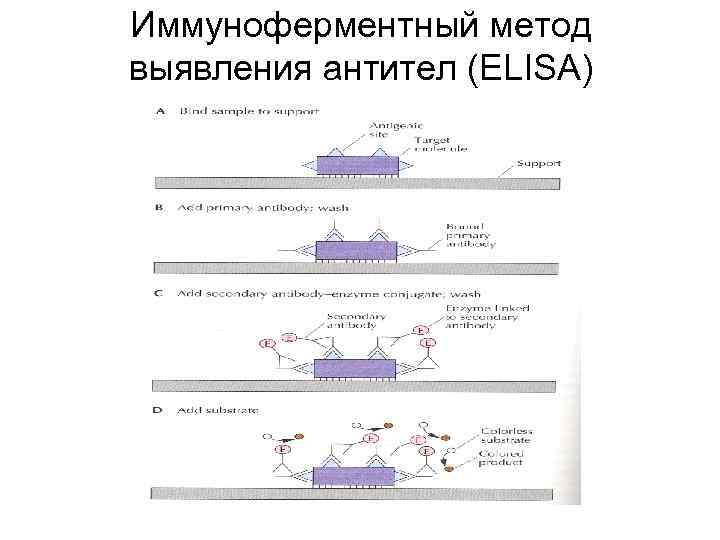
Иммуноферментный метод выявления антител (ELISA)

Получение мышиных моноклональных антител (МКА) • Иммунизация животных антигеном • Получение селезёночных В-лимфоцитов • Слияние В-лимфоцитов с миеломными клетками • Отбор гибридных клеток «В-лимфоцит. Миелома» на среде НАТ (ГАТ) • Отбор клонов гибридных клеток, продуцирующих нужные антитела • Накопление клеток и получение антител
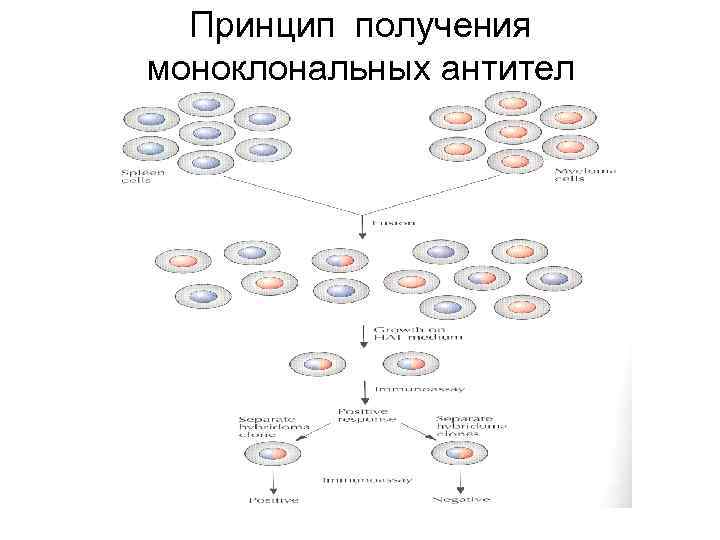
Принцип получения моноклональных антител

Миеломные клетки • Миеломы – опухоли из В-лимфоцитов • Перевиваемые миеломные клетки выращивают в присутствии 8 -азогуанина и получают клетки, дефектные по гену фермента Гипоксантин. Гуанин. Фосфо. Рибозил. Трансферазы (ГГФРТ, HGPRT) • Такие клетки не растут на среде НАТ

Среда НАТ • Это питательная среда, содержащая Гипоксантин+Аминоптерин (ингибитор дигидрофолатредуктазы, DHFR) +Тимидин • HGPRT- и TK- клетки не растут на среде НАТ, так как не способны образовывать пуриновые нуклеотиды (HGPRT-) или тимидинмонофосфат (TK-)
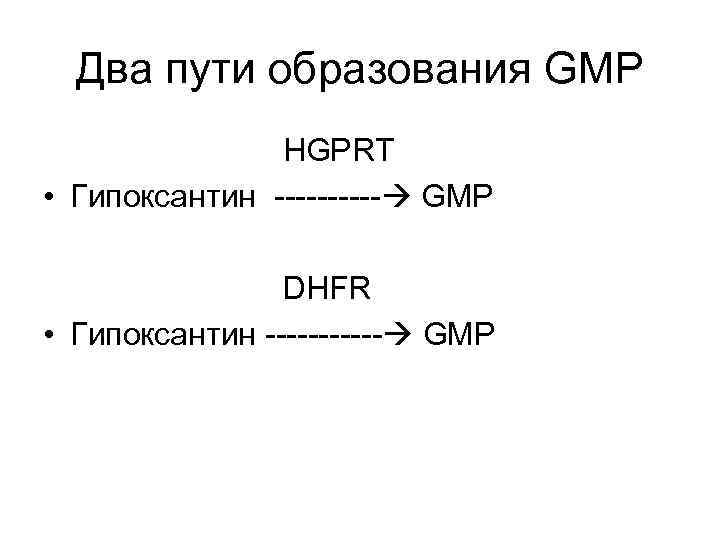
Два пути образования GMP HGPRT • Гипоксантин ----- GMP DHFR • Гипоксантин ------ GMP

Варианты клеток, образующихся при слиянии В-лимфоцитов (Л) и миеломных клеток (М) • • • Л(HPRT+) - не размножаются в культуре ЛЛ (HGPRT+) -”M (HGPRT-) – не размножаются на среде НАТ ММ (HGPRT-) – -“– LM (HPRT+) – размножаются на среде НАТ

Гибридомы • Это опухоли, возникающие у мышей, привитых гибридными клетками «лимфоцит-миелома» • При внутрибрюшинном введении гибридомных клеток возникают асцитные опухоли • Асцит содержит антитела, продуцируемые гибридными клетками

Накопление МКА • В культуре клеток • В асците мышей с внутрибрюшинным ростом гибридомы • МКА очищают из культуральной среды или из асцита методом аффинной хроматографии (колонки с протеин Аили протеин G-сефарозой)

Главные преимущества МКА • Высокая специфичность • Стандартность приготовления

Применение МКА • Высокоспецифическое обнаружение антигенов в научных и диагностических исследованиях • Очистка антигенов методом аффинной хроматографии • Терапевтическое использование, иммунотоксины

Иммунотоксины Это комплекс из специфического МКА и токсина, который связывается с клетками, имеющими на поверхности антиген, против которого направлено данное антитело
Молекулярная биотехнология 4.ppt