Презентация Инстр методов + ИВ V2.ppt
- Количество слайдов: 40

Экология Инструментальные методы анализа 1

Экологические объекты Воздух Почва Вода 2
Методы анализа Физико-химические Классические (весовой, титрование) Оптические Электрохимические Хроматографические 3

Фотометрия Теоретическая основа метода Закон Бугера – Ламберта – Бера А=ε×l×C А - оптическая плотность; А = lg(I 0/I); I 0 – интенсивность падающего света; I – интенсивность прошедшего света; ε - молярный коэффициент поглощения: l - толщина слоя раствора, см; С - концентрация раствора, моль/л. 4

Классификация электрохимических методов анализа Полярография (Вольтамперометрия) (измерение зависимости «величина тока - напряжение» ) Амперометрия (измерение величины тока при постоянном потенциале) Кондуктометрия (измерение величины сопротивления) Потенциометрия (измерение величины потенциала) Кулонометрия (количественный электролиз) 5

Потенциометрия (ионометрия) H+, NH 4+, Na+, K+, Ca 2+, Mg 2+ , Ba 2+, Ag+, Cu 2+, Pb 2+, Cd 2+, Hg 2+, Br-, I-, Cl-, F-, NO 3 -, NO 2 -, SO 42 -, CO 32 -, Cl. O 4 -, CNS- Прямая Потенциометрическое титрование Теоретическая основа метода уравнение Нернста 6
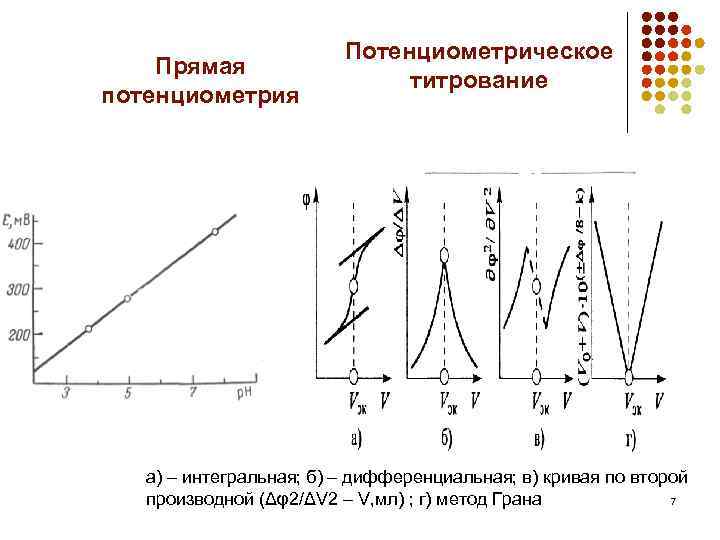
Прямая потенциометрия Потенциометрическое титрование а) – интегральная; б) – дифференциальная; в) кривая по второй производной (Δφ2/ΔV 2 – V, мл) ; г) метод Грана 7
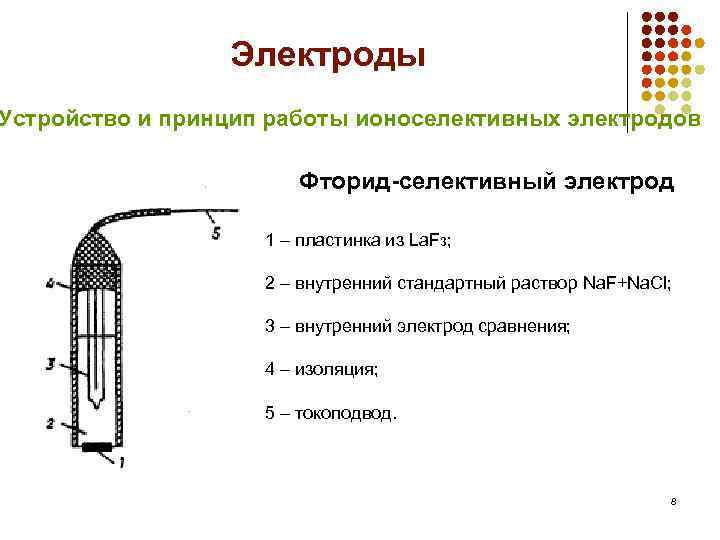
Электроды Устройство и принцип работы ионоселективных электродов Фторид-селективный электрод 1 – пластинка из La. F 3; 2 – внутренний стандартный раствор Na. F+Na. Cl; 3 – внутренний электрод сравнения; 4 – изоляция; 5 – токоподвод. 8

Полярография Инверсионная вольтамперометрия 1922 г. Ярослав Гейровский (Нобелевская премия 1959 г. ) Области применения Микроэлектроника Фармакология Экологический мониторинг объектов окружающей среды Экологическая безопасность продуктов питания 9

Уравнение Ильковича I=KC I- сила тока К – коэффициент пропорциональности С- концентрация 10
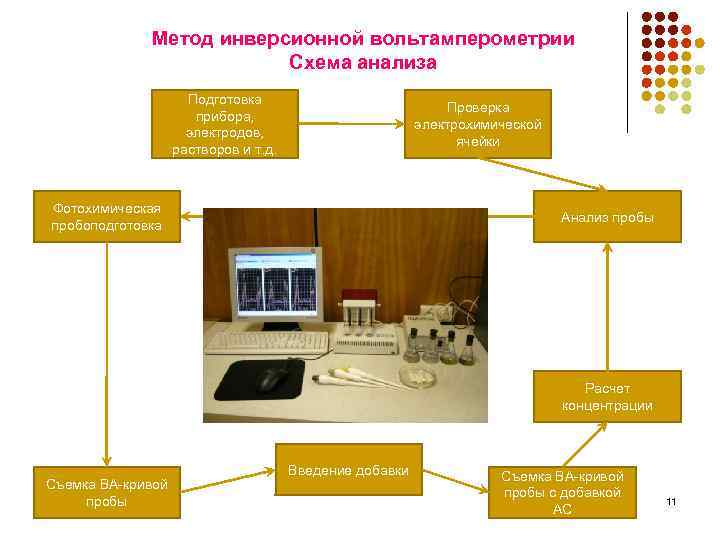
Метод инверсионной вольтамперометрии Схема анализа Подготовка прибора, электродов, растворов и т. д. Проверка электрохимической ячейки Фотохимическая пробоподготовка Анализ пробы Расчет концентрации Съемка ВА-кривой пробы Введение добавки Съемка ВА-кривой пробы с добавкой АС 11 11

Схема анализа 12
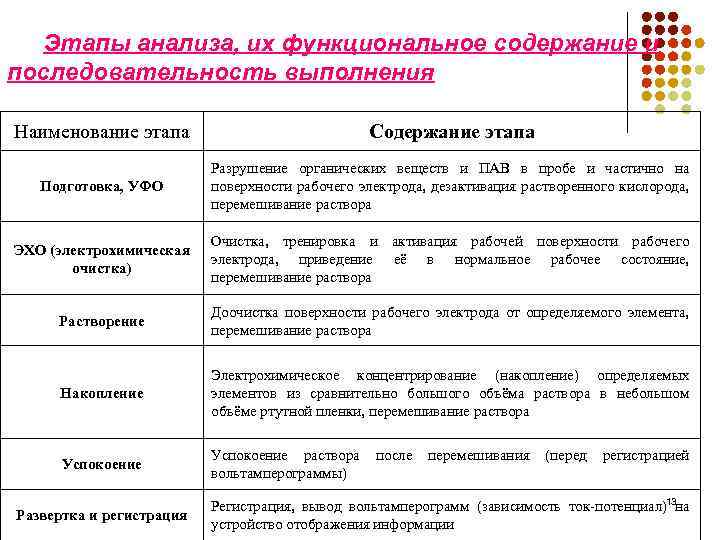
Этапы анализа, их функциональное содержание и последовательность выполнения Наименование этапа Содержание этапа Подготовка, УФО Разрушение органических веществ и ПАВ в пробе и частично на поверхности рабочего электрода, дезактивация растворенного кислорода, перемешивание раствора ЭХО (электрохимическая очистка) Очистка, тренировка и активация рабочей поверхности рабочего электрода, приведение её в нормальное рабочее состояние, перемешивание раствора Растворение Доочистка поверхности рабочего электрода от определяемого элемента, перемешивание раствора Накопление Электрохимическое концентрирование (накопление) определяемых элементов из сравнительно большого объёма раствора в небольшом объёме ртутной пленки, перемешивание раствора Успокоение раствора вольтамперограммы) Развертка и регистрация после перемешивания (перед регистрацией Регистрация, вывод вольтамперограмм (зависимость ток-потенциал)13 на устройство отображения информации
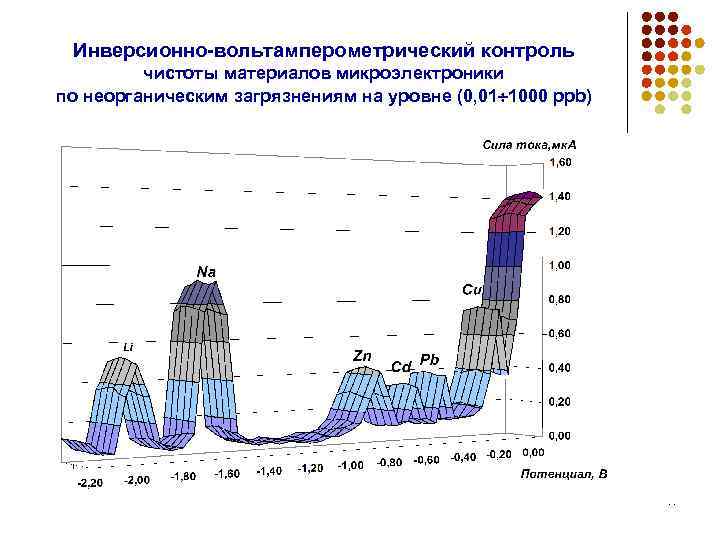
Инверсионно-вольтамперометрический контроль чистоты материалов микроэлектроники по неорганическим загрязнениям на уровне (0, 01 1000 ppb) 14
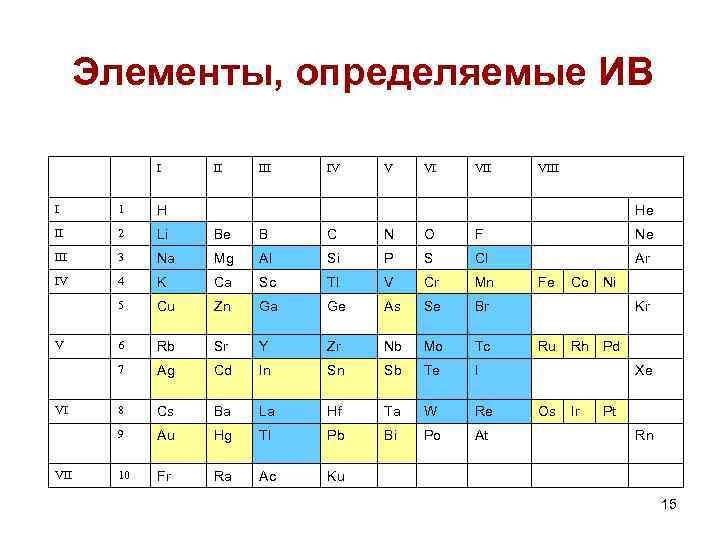
Элементы, определяемые ИВ I II IV V VI VIII I 1 H II 2 Li Be B C N O F Ne III 3 Na Mg Al Si P S Cl Ar IV 4 K Ca Sc Tl V Cr Mn 5 Cu Zn Gа Ge As Se Br 6 Rb Sr Y Zr Nb Mo Tc 7 Ag Cd In Sn Sb Te I 8 Cs Ba La Hf Ta W Re 9 Au Hg Tl Pb Bi Po At 10 Fr Ra Ac Ku V VI VII He Fe Co Ni Kr Ru Rh Pd Xe Os Ir Pt Rn 15
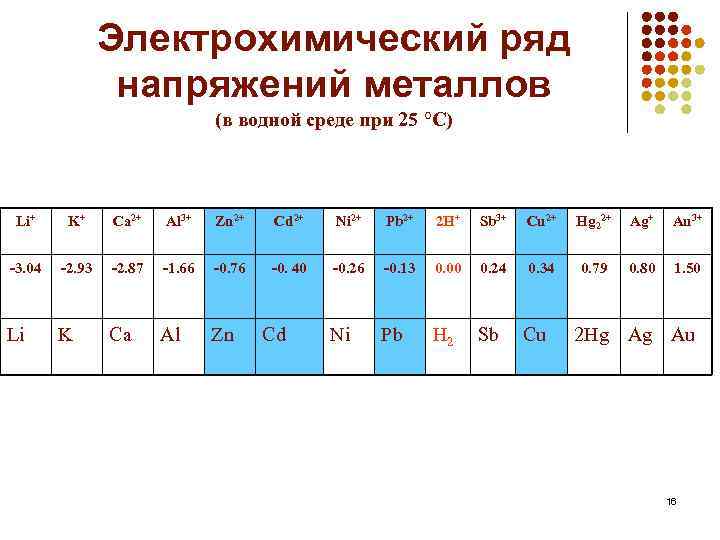
Электрохимический ряд напряжений металлов (в водной среде при 25 °С) Li+ K+ Ca 2+ Al 3+ Zn 2+ Cd 2+ Ni 2+ Pb 2+ 2 H+ Sb 3+ Cu 2+ Hg 22+ Ag+ Au 3+ -3. 04 -2. 93 -2. 87 -1. 66 -0. 76 -0. 40 -0. 26 -0. 13 0. 00 0. 24 0. 34 0. 79 0. 80 1. 50 Li K Ca Al Zn Ni Pb H 2 Sb Cd Cu 2 Hg Ag Au 16

Электроды для ИВ (анализ на тяжелые металлы) Ртутно-пленочный (поляризующийся) рабочая область потенциалов +0, 4. . . -1, 6 В l Хлорсеребряный (неполяризующийся) l Аналитический сигнал в ИВ ток растворения продукта электролиза с электрода, имеющий форму пика, характеризуется высотой, потенциалом пика. Высота прямо пропорциональна концентрации, потенциал определяет природу элемента. 17
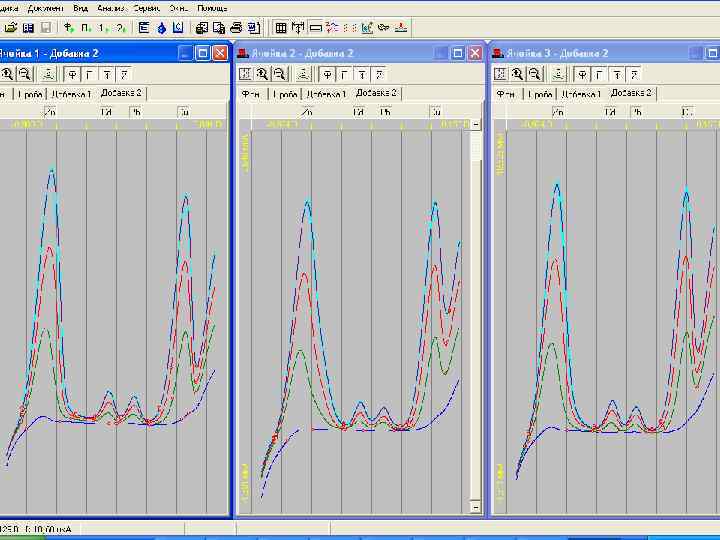
18
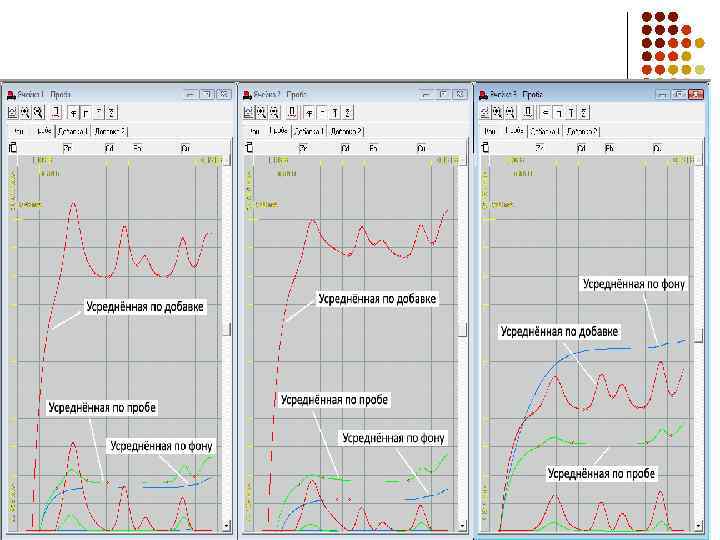
Результаты ИВ определений экотоксикантов 19 19

Стадии метода l 1) концентрирование вещества (элемента) из раствора на поверхности электрода при постоянном потенциале; l 2) электрохимическое растворение концентрата и фиксирование изменения анодного тока при линейном изменении потенциала. 20

Пример l 1) Электролиз при потенциале -1, 2 В с образованием амальгамы Cd 2+ +2 e+Hg→Cd(Hg) l 2) Анодное растворение концентрата при линейном изменение потенциала. Cd(Hg)→Cd 2++2 e+Hg 21
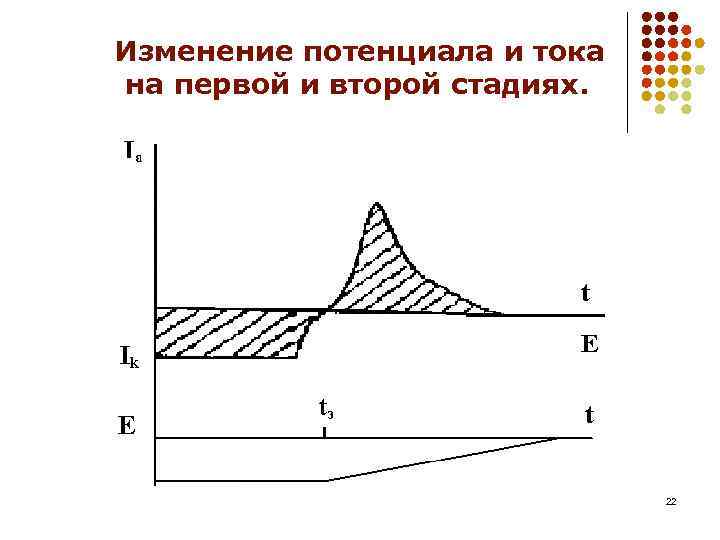
Изменение потенциала и тока на первой и второй стадиях. 22

Факторы, искажающие аналитический сигнал. Их устранение. l Растворенный кислород l Наложение пиков l ПАВ 23

Наложение пиков l выбора потенциала электролиза l подбор фона, содержащего лиганд, для маскировки одного из ионов. 24
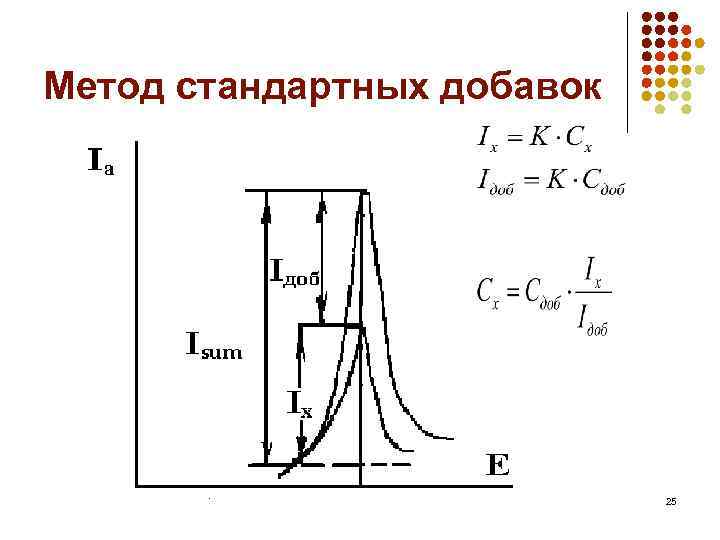
Метод стандартных добавок 25
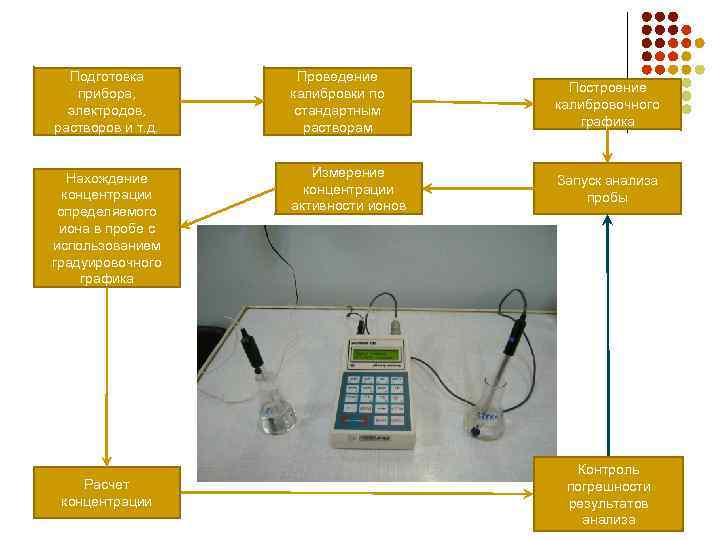
Ионометрия. Схема анализа Подготовка прибора, электродов, растворов и т. д. Проведение калибровки по стандартным растворам Построение калибровочного графика Нахождение концентрации определяемого иона в пробе с использованием градуировочного графика Измерение концентрации активности ионов Запуск анализа пробы Расчет концентрации Контроль погрешности результатов анализа 26 26
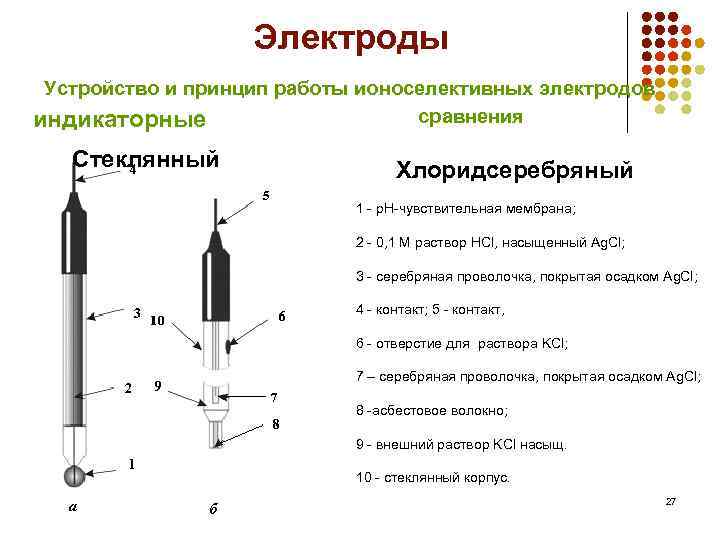
Электроды Устройство и принцип работы ионоселективных электродов сравнения индикаторные Стеклянный Хлоридсеребряный 1 - р. Н-чувствительная мембрана; 2 - 0, 1 М раствор HCl, насыщенный Ag. Cl; 3 - серебряная проволочка, покрытая осадком Ag. Cl; 4 - контакт; 5 - контакт, 6 - отверстие для раствора KCl; 7 – серебряная проволочка, покрытая осадком Ag. Cl; 8 -асбестовое волокно; 9 - внешний раствор KCl насыщ. 10 - стеклянный корпус. 27
28

КАДМИЙ n Разница между содержанием этого вещества в организме современных подростков и критической величиной, когда придется считаться с нарушениями функции почек, болезнями легких и костей, оказывается очень малой. Особенно у курильщиков. C каждой затяжкой дымом вместе с такими вредными веществами, как никотин и окись углерода, в организм поступает и кадмий. В одной сигарете содержится от 1, 2 до 2, 5 мкг этого яда. Одна сигарета содержит около 1 гр. табака. Следовательно, при выкуривании всех сигарет, папирос и трубок в мире в окружающую среду выделяется от 5, 7 до 11, 4 т. кадмия, попадая не только в легкие курильщиков, но и в легкие некурящих людей. 29

Кадмий n n n Кадмий относится к наиболее токсичным элементам. Он накапливается в организме и очень медленно выводится из него. Приводит к гипертонии, разрушению нервной системы. Источником поступления кадмия являются кадмиевые покрытия, аккумуляторы.

ЦИНК l l l l Избыток цинка в организме проявляется следующими симптомами: - замедление роста у детей, - позднее половое созревание, - импотенция у мужчин и стерильность у женщин, - плохое заживление ран, - раздражительность и потеря памяти, - появление угрей, - очаговое выпадение волос, - потеря аппетита, вкусовых ощущений и обоняния, - ломкость ногтей, - частые инфекции, - нарушение усвоения витаминов А, С и Е, - повышение уровня холестерина. 31

Цинк l l Цинк относится к элементам с сравнительно низкой токсичностью. Избыток приводит к кишечным заболеваниям. Источниками поступления цинка в воду являются отходы металлургической промышленности, продукты коррозии сплавов и цинковых покрытий. ПДК составляет 5 мг/л

СВИНЕЦ l Одним из самых распространенных и опасных токсикантов является свинец. В земной коре он содержится в незначительных количествах. Вместе с тем мировое производство свинца составляет более 3, 5× 106 т в год, и только в атмосферу поступает в переработанном и мелкодисперсном состоянии 4, 5× 105 т свинца в год. Среднее содержание свинца в продуктах питания 0, 2 мг/кг [1]. 33

Свинец l l Свинец относится к наиболее токсичным элементам. Избыток приводит к анемии, почечной недостаточности. Способен замещать кальций в костях, уменьшая их прочность. Источниками являются свинцовые трубы, краски, аккумуляторы. ПДК составляет 0, 03 мг/л.

Медь Cu. l l В избыточных количествах медь оказывает токсическое действие. При попадании в организм с пищей, содержащей более 50 мкг/кг, наблюдаются характерные признаки отравления -металлический вкус во рту, неукротимая рвота, боли в животе. При поступлении в меньших количествах медь накапливается в печени, что вызывает физиологические расстройства в организме - тошноту, рвоту, желудочную боль. Некоторые соединения меди играют роль катализаторов окислительных процессов в пищевых продуктах. Кроме того, ряд соединений меди разрушают витамины С и А, ухудшают органолептические показатели, способствуют образованию токсичных продуктов окисления липидов. Вследствие отмеченных свойств допустимые нормы содержания меди в продуктах устанавливают часто ниже норм, определенных по токсикологическим показателям. 35

Медь l l Степень токсичности меди определяется между низкой и средней. Избыток приводит к болезни Вильсона, нарушению функций печени. Источниками является продукты коррозии медьсодержащих сплавов. ПДК составляет 1 мг/л.

Железо l l Степень токсичности железа низкая. Высокое содержание приводит к разрушению нервной системы, повреждению печени. Источниками являются ржавые трубы и металлолом. ПДК составляет 0, 3 мг/л.

Нитраты и нитриты n В воде поверхностных источников, реже в подземных, присутствуют соединения азота в виде нитратов и нитритов. В настоящее время происходит постоянный рост их концентрации, связанный прежде всего с широким использованием нитратных удобрений, избыток которых с грунтовыми водами поступает в реки и озера. Установленные нормы на содержание нитратов составляют NO 3– < 45 мг/л, нитритов – NO 2– < 3 мг/л. 38

Кислотность и щелочность воды. l Данная характеристика воды также известна многим людям благодаря рекламе, поскольку именно эта характеристика измеряется величиной р. Н, то есть мерой активной кислотности, которая обусловливается наличием в воде активных ионов водорода. Вода хозяйственно-питьевого назначения должна иметь величину р. Н = 6, 5 -7, 5. В большинстве случаев характеристики воды природных источников с этой точки зрения не выходят за пределы нормы. 39
СПАСИБО ЗА ВНИМАНИЕ !!! 40
Презентация Инстр методов + ИВ V2.ppt