ЕГЭ часть ВС-13.ppt
- Количество слайдов: 128

ЕГЭ по химии 2013 г. Катраков Игорь Борисович, канд. хим. наук, доцент, зам. декана ХФ Алт. ГУ по учебной работе
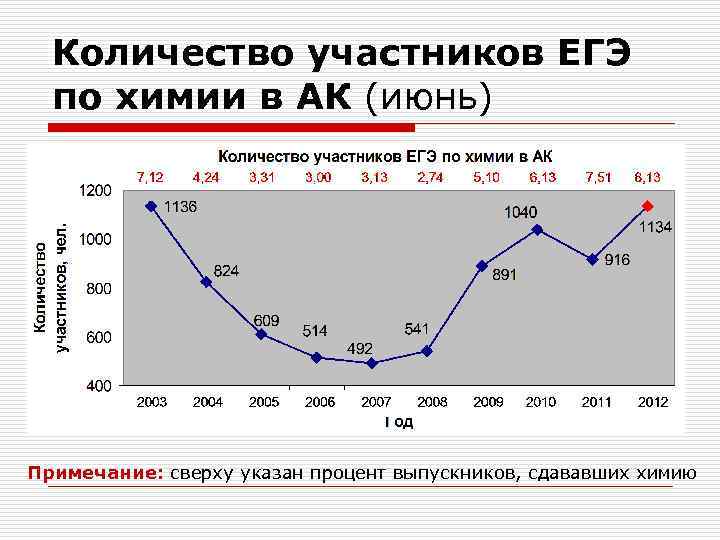
Количество участников ЕГЭ по химии в АК (июнь) Примечание: сверху указан процент выпускников, сдававших химию
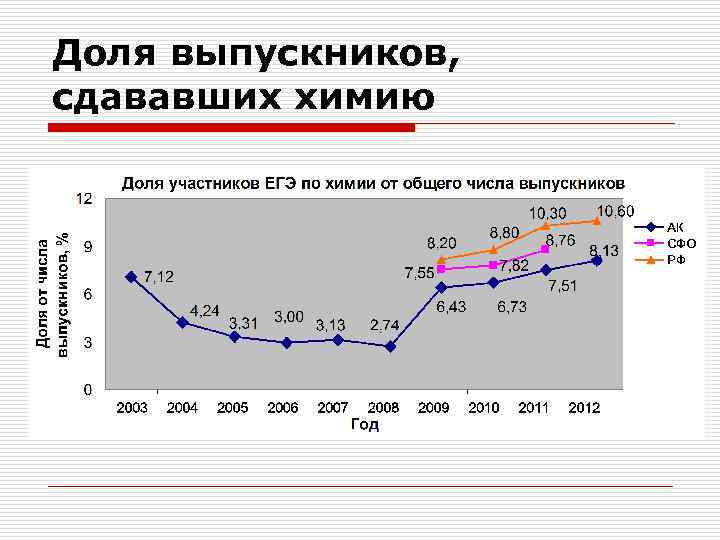
Доля выпускников, сдававших химию
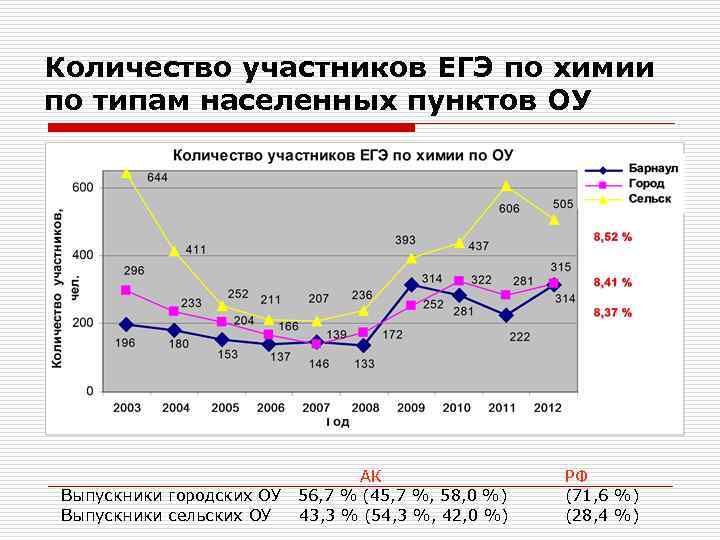
Количество участников ЕГЭ по химии по типам населенных пунктов ОУ Выпускники городских ОУ Выпускники сельских ОУ АК 56, 7 % (45, 7 %, 58, 0 %) 43, 3 % (54, 3 %, 42, 0 %) РФ (71, 6 %) (28, 4 %)
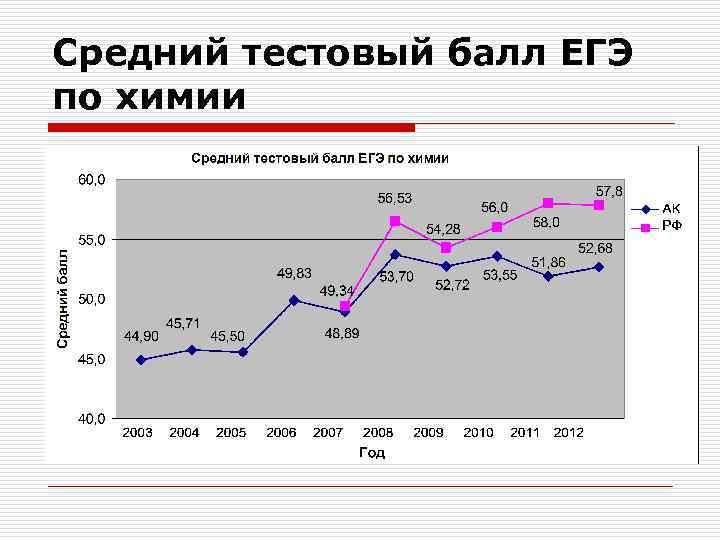
Средний тестовый балл ЕГЭ по химии
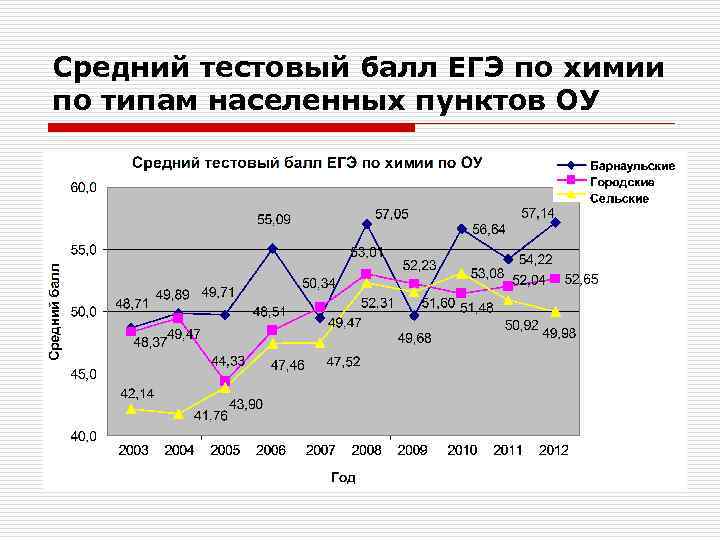
Средний тестовый балл ЕГЭ по химии по типам населенных пунктов ОУ
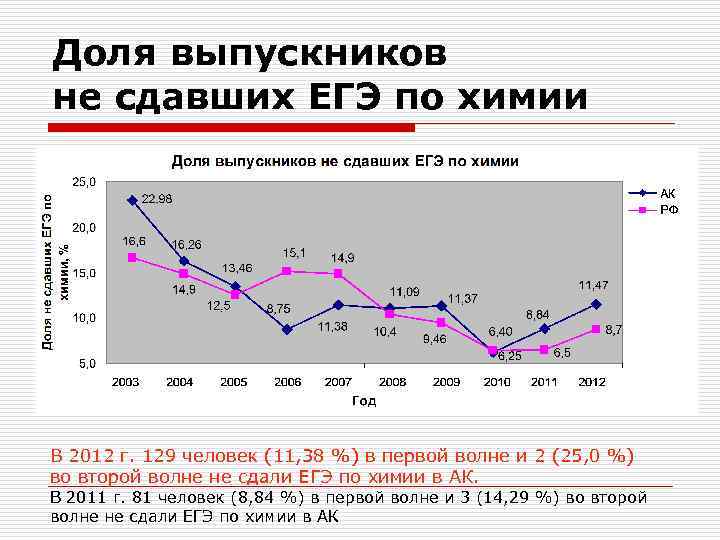
Доля выпускников не сдавших ЕГЭ по химии В 2012 г. 129 человек (11, 38 %) в первой волне и 2 (25, 0 %) во второй волне не сдали ЕГЭ по химии в АК. В 2011 г. 81 человек (8, 84 %) в первой волне и 3 (14, 29 %) во второй волне не сдали ЕГЭ по химии в АК
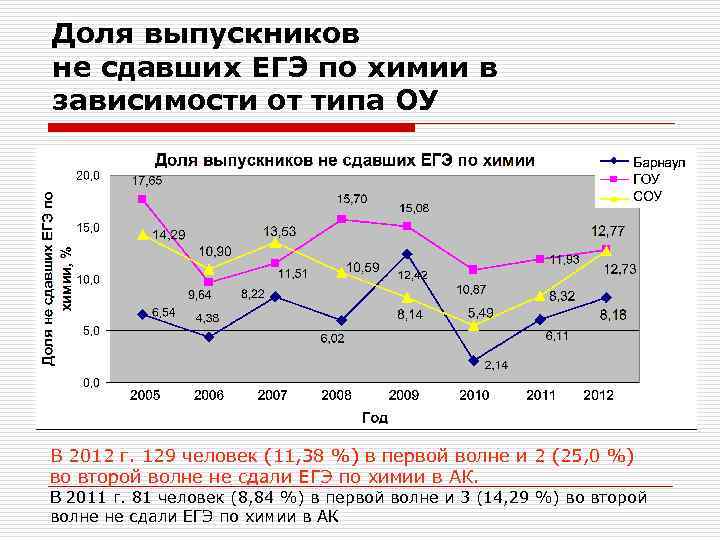
Доля выпускников не сдавших ЕГЭ по химии в зависимости от типа ОУ В 2012 г. 129 человек (11, 38 %) в первой волне и 2 (25, 0 %) во второй волне не сдали ЕГЭ по химии в АК. В 2011 г. 81 человек (8, 84 %) в первой волне и 3 (14, 29 %) во второй волне не сдали ЕГЭ по химии в АК
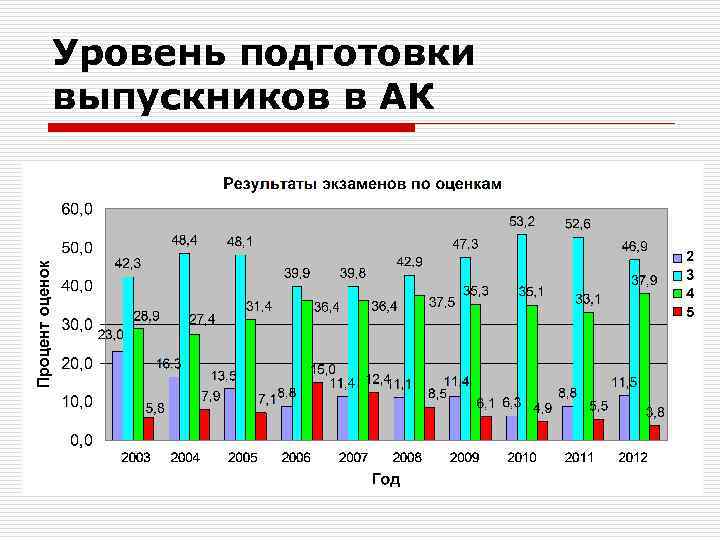
Уровень подготовки выпускников в АК
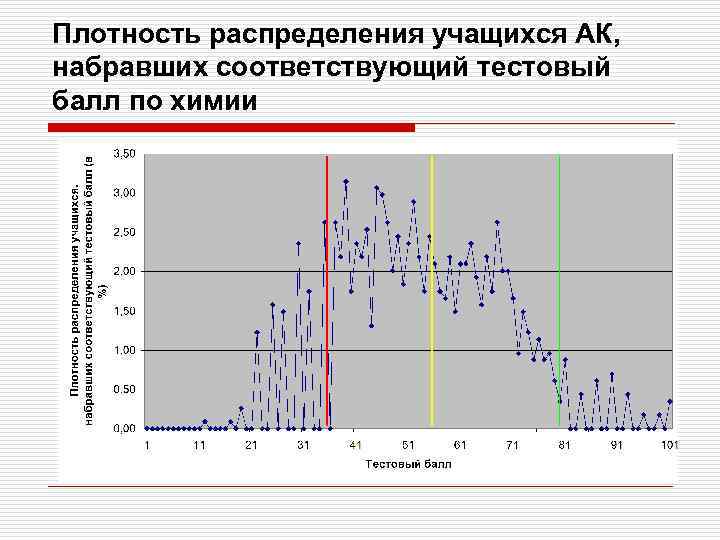
Плотность распределения учащихся АК, набравших соответствующий тестовый балл по химии
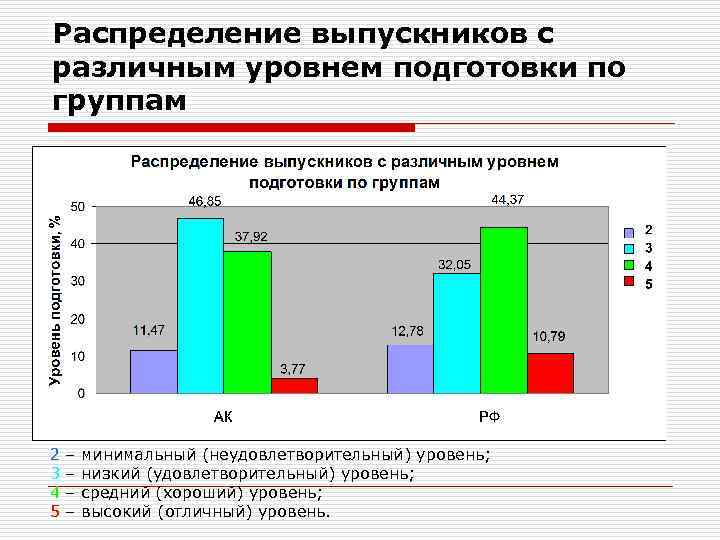
Распределение выпускников с различным уровнем подготовки по группам 2 3 4 5 – – минимальный (неудовлетворительный) уровень; низкий (удовлетворительный) уровень; средний (хороший) уровень; высокий (отличный) уровень.

Требования к подготовке выпускников По итогам обучения выпускники должны уметь: o характеризовать общие свойства химических элементов и их соединений на основе положения в периодической системе Д. И. Менделеева; состав, свойства и применение веществ; факторы, влияющие на изменение скорости химической реакции и состояние химического равновесия; o объяснять закономерности в изменении свойств веществ, сущность химических реакций; o составлять формулы веществ, схемы строения атомов, уравнения химических реакций различных типов; o называть и определять вещества, их свойства, признаки классификации веществ, типы реакций и др. ; o проводить вычисления по химическим формулам и уравнениям; o использовать приобретенные знания для объяснения химических явлений, происходящих в природе, быту и на производстве; для распознавания важнейших веществ, безопасной работы с веществами и т. д.

Структура экзаменационной работы o o o Часть 1 содержит 28 заданий закрытого типа (с выбором одного правильного ответа из четырех предложенных) – базовый уровень сложности. Их обозначают в работе под литером А: А 1, А 2 и т. д. Часть 2 содержит 10 заданий открытого типа (с кратким ответом) – повышенный уровень сложности. Их обозначают в работе под литером В: В 1, В 2 и т. д. Часть 3 содержит 5 заданий открытого типа (с развернутым ответом) – высокий уровень сложности. Их обозначают в работе под литером С: С 1, С 2 и т. д.
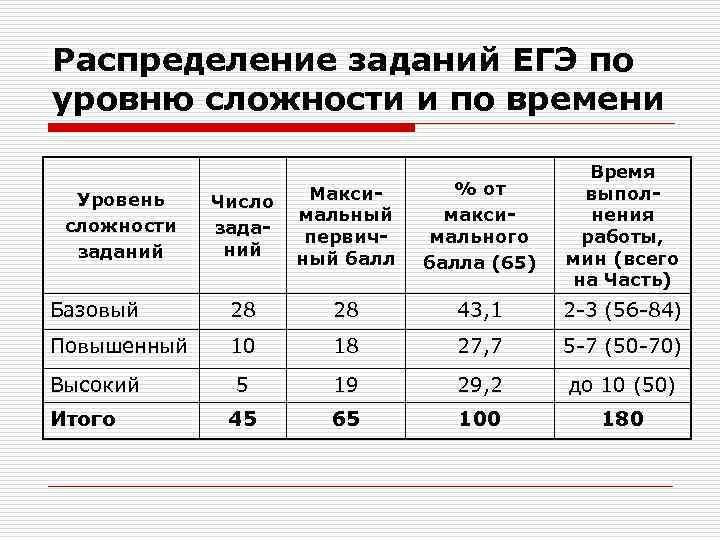
Распределение заданий ЕГЭ по уровню сложности и по времени Число заданий Максимальный первичный балл % от максимального балла (65) Время выполнения работы, мин (всего на Часть) Базовый 28 28 43, 1 2 -3 (56 -84) Повышенный 10 18 27, 7 5 -7 (50 -70) 5 19 29, 2 до 10 (50) 45 65 100 180 Уровень сложности заданий Высокий Итого

Дополнительные материалы и оборудование В аудитории во время экзамена у каждого экзаменующегося должны быть следующие материалы и оборудование: 1. периодическая система химических элементов Д. И. Менделеева*; 2. таблица растворимости солей, кислот и оснований в воде*; 3. электрохимический ряд напряжения металлов; 4. непрограммируемый калькулятор. * Ч-б таблицы по учебнику Кузьменко Н. Е. , Еремин В. В. , Попков В. А. «Начала химии»

Система оценивания работ Части 1 (А) Ответы на задания Части 1 (А) автоматически обрабатываются после сканирования бланков ответов № 1. o Верное выполнение каждого задания Части 1 оценивается в 1 балл. o Задание считается выполненным верно, если учащийся указал код правильного ответа. o Задание считается выполненным неверно: 1. выбран другой ответ; 2. выбрано два ответа, среди которых может быть и правильный; 3. ответ на вопрос отсутствует.

Особенности подготовки к ЕГЭ по химии Вопросы Части 2 ЕГЭ по химии

Система оценивания работ Части 2 (В) o o o Задание Части 2 считается выполненным верно, если правильно указана последовательность цифр (число). За полный правильный ответ на задания В 1–В 8 ставится 2 балла, допущена одна ошибка – 1 балл, за неверный ответ (более одной ошибки) или его отсутствии) – 0 баллов. За правильный ответ на задания В 9 и В 10 ставится 1 балл, за неверный ответ или его отсутствии) – 0 баллов.
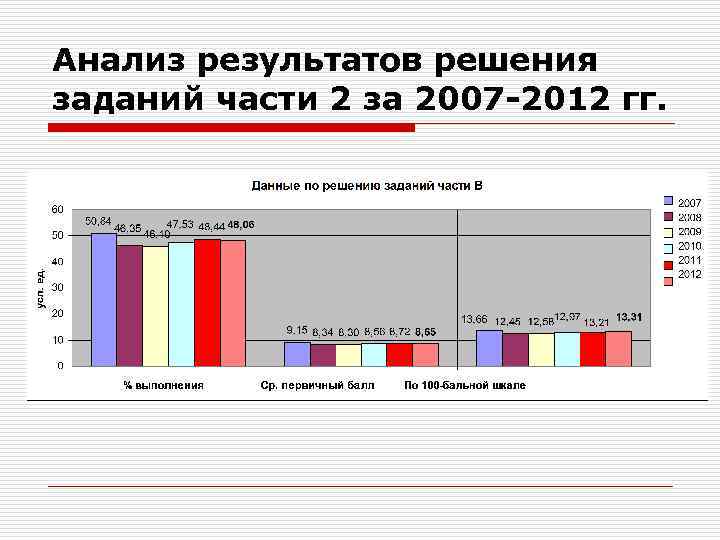
Анализ результатов решения заданий части 2 за 2007 -2012 гг.
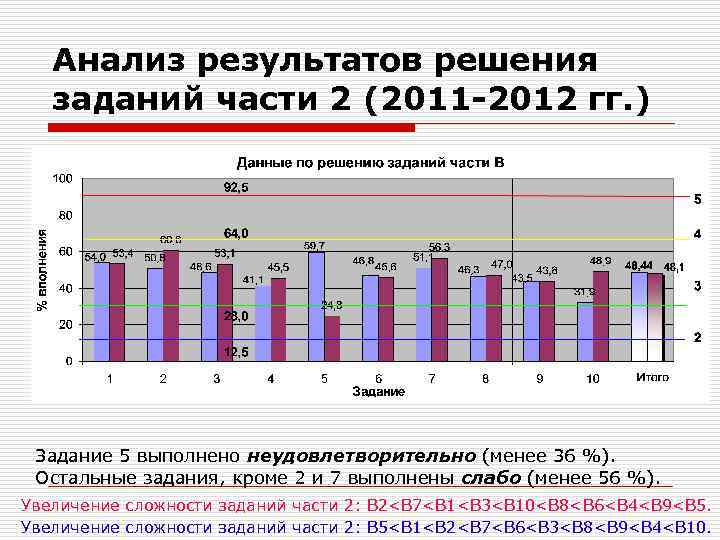
Анализ результатов решения заданий части 2 (2011 -2012 гг. ) Задание 5 выполнено неудовлетворительно (менее 36 %). Остальные задания, кроме 2 и 7 выполнены слабо (менее 56 %). Увеличение сложности заданий части 2: В 2<В 7<В 1<В 3<В 10<В 8<В 6<В 4<В 9<В 5. Увеличение сложности заданий части 2: В 5<В 1<В 2<В 7<В 6<В 3<В 8<В 9<В 4<В 10.
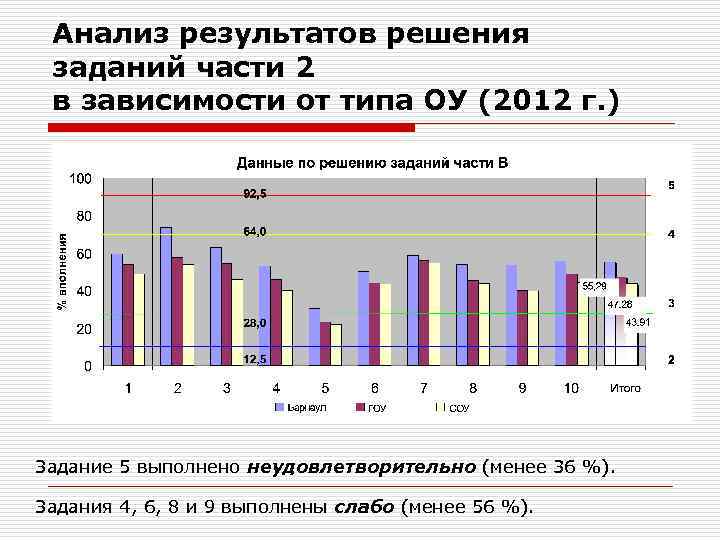
Анализ результатов решения заданий части 2 в зависимости от типа ОУ (2012 г. ) Задание 5 выполнено неудовлетворительно (менее 36 %). Задания 4, 6, 8 и 9 выполнены слабо (менее 56 %).
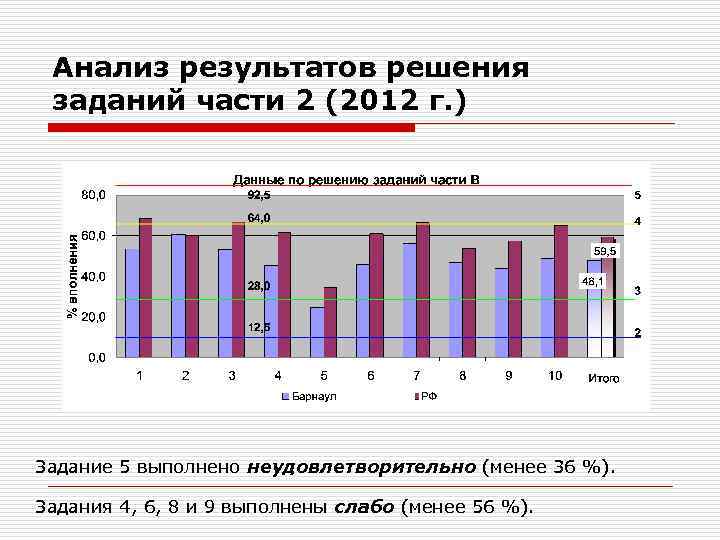
Анализ результатов решения заданий части 2 (2012 г. ) Задание 5 выполнено неудовлетворительно (менее 36 %). Задания 4, 6, 8 и 9 выполнены слабо (менее 56 %).

Часть 2

В 1 Классификация неорганических веществ. Классификация и номенклатура органических соединений Тривиальная номенклатура неорганических веществ: Бертолетова соль – KCl. O 3 Генераторный газ – N 2 + CO Гипс (алебастр) – Ca. SO 4. 2 H 2 O Жидкое стекло (конторский клей) – Na 2 Si. O 3 Известь негашеная (кипелка) – Ca. O Известь гашеная (пушенка, известковое молоко) – Ca(OH)2 Каменная (поваренная) соль – Na. Cl Купорос медный (синий) – Cu. SO 4. 5 H 2 O Мел (мрамор, известняк) – Ca. СO 3 Нашатырный спирт – NH 4 OH Нашатырь – NH 4 Cl Плавиковая кислота – HF Поташ – K 2 CO 3 Селитра аммиачная – NH 4 NO 3 Синтез-газ (водяной газ) – H 2 + CO Сода пищевая – Na. HCO 3 Сода каустическая – Na. OH Сухой лед – CO 2 (твердый) Угарный газ – CO Углекислый газ – CO 2
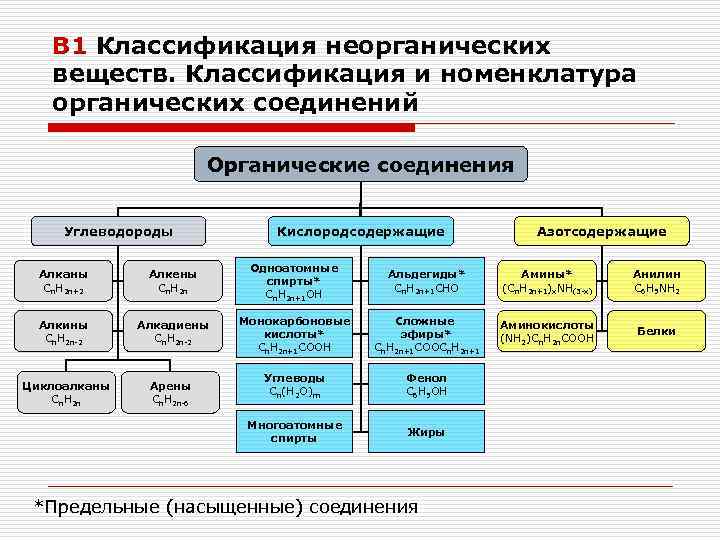
В 1 Классификация неорганических веществ. Классификация и номенклатура органических соединений Органические соединения Углеводороды Кислородсодержащие Азотсодержащие Алканы Cn. H 2 n+2 Алкены Cn. H 2 n Одноатомные спирты* Cn. H 2 n+1 OH Альдегиды* Cn. H 2 n+1 CHО Амины* (Cn. H 2 n+1)x. NH(3 -x) Анилин C 6 H 5 NH 2 Алкины Cn. H 2 n-2 Алкадиены Cn. H 2 n-2 Монокарбоновые кислоты* Cn. H 2 n+1 COOH Сложные эфиры* Cn. H 2 n+1 COOCn. H 2 n+1 Аминокислоты (NH 2)Cn. H 2 n. COOH Белки Циклоалканы Cn. H 2 n Арены Cn. H 2 n-6 Углеводы Cn(H 2 O)m Фенол C 6 H 5 OH Многоатомные спирты Жиры *Предельные (насыщенные) соединения

В 1 Классификация неорганических веществ. Классификация и номенклатура органических соединений Тривиальная номенклатура органических веществ: Аланин (2 -аминопропановая кислота) – СH 3 СH(NH 2)COOH Аллилхлорид (2 -хлорпропен-1) – СН 2=СH–СН 2–Cl Амиловый спирт (пентанол– 1) – СH 3 СH 2 СH 2 CH 2 OH Ацетилен (этин) – СН≡СН Ацетон (пропанон, диметилкетон) – CH 3 C(O)CH 3 Валериановая кислота (пентановая кислота) – СH 3 СH 2 СH 2 COOH Винилхлорид (хлорэтен) – СН 2=СHCl Винный спирт (этанол) – СH 3 CH 2 OH Глицерин (пропантриол-1, 2, 3) – НОCH 2 CН(OН)CH 2 ОН Глицин (аминоуксусная кислота) – NH 2 СH 2 COOH Дивинил (бутадиен-1, 3) – СН 2=СH–СН=СH 2 Древесный спирт (метанол) – СH 3 OH Изопрен (2 -метилбутадиен-1, 3) – СН 2=С(СН 3)–СН=СH 2 Капроновая кислота (гексановая кислота) – СH 3 СH 2 СH 2 COOH Карболовая кислота (фенол) – С 6 Н 5 ОН Кумол (изопропилбензол) – С 6 Н 5 СН(СН 3)2 Масляная кислота (бутановая кислота) – СH 3 СH 2 COOH Муравьиная кислота (матановая кислота) – HCOOH Пальмитиновая кислота (гексадекановая кислота) – СH 3(СH 2)14 COOH Пропионовая кислота (пропановая кислота) – СH 3 СH 2 COOH Стеариновая кислота (октадекановая кислота) – СH 3(СH 2)16 COOH Стирол (винилбензол) – С 6 H 5–СН=СH 2 Уксусная кислота (этановая кислота) – СH 3 COOH
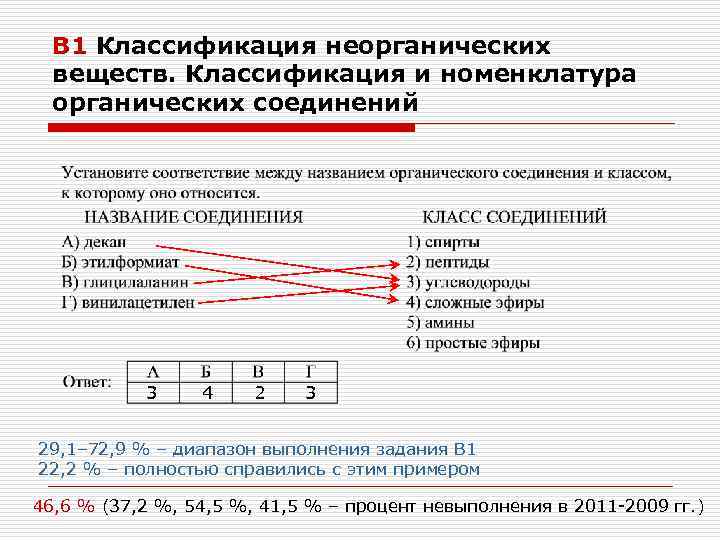
В 1 Классификация неорганических веществ. Классификация и номенклатура органических соединений 3 4 2 3 29, 1– 72, 9 % – диапазон выполнения задания В 1 22, 2 % – полностью справились с этим примером 46, 6 % (37, 2 %, 54, 5 %, 41, 5 % – процент невыполнения в 2011 -2009 гг. )

В 1 Классификация неорганических веществ. Классификация и номенклатура органических соединений 3 4 6 2

В 1 Классификация неорганических веществ. Классификация и номенклатура органических соединений 3 1 2 5

В 1 Классификация неорганических веществ. Классификация и номенклатура органических соединений 6 3 1 4

Часть 2 В 2 Электроотрицательность. Степень окисления и валентность химических элементов. Реакции окислительно-восстановительные. Коррозия металлов и способы защиты от нее.

В 2 Электроотрицательность. Степень окисления и валентность химических элементов. Реакции окислительно-восстановительные. Коррозия металлов и способы защиты от нее +7 – 2 – 1 +5 0 – 1 +5 – 2 +7 – 1 +1 – 1 2 0 +5 6 2 5 39, 5 (39, 6 %, 41, 6 %, 34, 2 %) 50, 1– 72, 7 % 49, 8 %

В 2 Электроотрицательность. Степень окисления и валентность химических элементов. Реакции окислительно-восстановительные. Коррозия металлов и способы защиты от нее +1 0 – 2 0 0 0 +1 +1 – 1 +1 0 0 – 3 +1 2 4 2 1

Часть 2 В 3 Электролиз расплавов и растворов (солей, щелочей, кислот). Li K Ba Ca Na Mg Al Mn Zn Cr Fe Co Ni Sn Pb H 2 Cu Hg Ag Pt Au

Часть 2 В 3 Электролиз расплавов и растворов (солей, щелочей, кислот).

В 3 Электролиз расплавов и растворов (солей, щелочей, кислот) 3 3 5 3 38, 5– 64, 3 % 31, 1 % 46, 9 % (46, 7 %, 50, 7 %, 46, 8 %)

В 3 Электролиз расплавов и растворов (солей, щелочей, кислот) 2 1 1 2

В 3 Электролиз расплавов и растворов (солей, щелочей, кислот) 3 2 1 1

Часть 2 В 4 Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная. o o Сильные основания (щелочи): Li. OH, Na. OH, KOH, Rb. OH, Cs. OH, Ca(OH)2, Sr(OH)2, Ba(OH)2. Сильные кислоты: HCl, HBr, HI, HNO 3, H 2 SO 4, H 2 Cr. O 4, HMn. O 4, HCl. O 4

Часть 2 В 4 Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная. 1. 2. Гидролиз солей осуществляется по слабому компоненту (например, по катиону: NH 4+, Cu 2+, Cr 3+, Al 3+, Fe 3+ и др. или аниону: CO 32–, Si. O 32–, Cl. O–, CN–, CH 3 COO– и др. ); Среда водных растворов определяется по сильному компоненту (у кого больше Кдис) например, по катиону: Li+, Na+, K+, Rb+, Ca 2+, Sr 2+, Ba 2+ – щелочная среда; или аниону: l–, Br–, Cl–, NO 3–, Cl. O 4–, SO 42– – кислая среда.

В 4 Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная 1 3 1 2 25, 1– 64, 7 % 18, 5 % 55, 6 % (50, 1 %, 49, 0 %, 47, 8 %)

В 4 Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная 1 3 2 4 50, 1 % (49, 0 %, 47, 8 %, 80, 0 %)

В 4 Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная 2 3 1 1

Часть 2 В 5 Характерные химические свойства неорганических веществ: простых веществ-металлов: щелочных, щелочноземельных, алюминия, переходных металлов (меди, цинка, хрома, железа); простых веществ-неметаллов: водорода, галогенов, кислорода, серы, азота, фосфора, углерода, кремния; оксидов: оснóвных, амфотерных, кислотных; оснований и амфотерных гидроксидов; кислот; солей: средних, кислых и основных); комплексных (на примере соединений алюминия и цинка).

Часть 2 В 5 Характерные химические свойства неорганических веществ: Порядок рассмотрения вопроса по формуле вещества и реагентам : 1. Классифицировать неорганическое вещество в определенной степени окисления основного элемента; 2. Отметить его характерные свойства; 3. Отметить его специфические свойства (ОВР). 4. Пересекающие свойства удовлетворяют требованиям задания – реакция возможна.

В 5 Характерные химические свойства неорганических веществ неметалл, вос-ль с более Э. О. неметаллами, ок-ль с менее Э. О. элементами, спецефич. ОВР со щелочами и кислотами-окислителями амф. оксид неметалл, вос-ль с более Э. О. неметаллами и оксидами металлов, водой, ок-ль с менее Э. О. элементами (металлами, водородом), спецефич. силь. ок-ль, к-та ОВР с кислотами-окислителями осн. оксид в низшей ст. ок. , вос-ль с сильными ок-лями, ок-ль с восстановителями сл. ок-ль кисл. оксид в высшей ст. ок. , ок-ль с восстановителями силь. ок-ль к-та, вос-ль 2 4 2 1 75, 2 % (27, 3 %, 64, 3 %, 88, 6 %) щелочь вос-ль осн. оксид силь. ок-ль вос-ль кисл. оксид, сл. ок-ль инерт. мет. ок-ль осн. оксид сильн. вос-ль 10, 8– 34, 2 % 5, 0 %

В 5 Характерные химические свойства неорганических веществ соль сильн. осн-я и сильн. к-ты, р-ции ионного обмена неметалл, сильн. ок-ль, спецефич. ОВР со щелочами осн. оксид щелочь сильн. ок-ль сл. ок-ль сильн. ок-ль, к-та сл. ок-ль и вос-ль осн. оксид амф. оксид ср. вос-ль кисл. оксид вос-ль, сл. ок-ль сл. к-та амф. оксид, сл. ок-ль раств. соль сл. к-ты 5 3 4 2 сильн. ок-ль и к-та амф. оксид раств. соль. сл. осн-я

Часть 2

В 6 Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов, диенов, алкинов, ароматических углеводородов (бензола и толуола). Ионный (правило В. В. Марковникова) и радикальный механизмы реакций в органической химии 1. o o o 2. o o o Характерные химические реакции алканов: замещения (радикальный механизм – образование новой σ-связи); дегидрирование; окисления (горение). Характерные химические реакции циклоалканов: присоединения (циклопропан и циклобутан); замещения (циклопентан, циклогексан); окисления (горение).

В 6 Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов, диенов, алкинов, ароматических углеводородов (бензола и толуола). Ионный (правило В. В. Марковникова) и радикальный механизмы реакций в органической химии 3. o o 4. o o Характерные химические реакции алкенов, диенов и алкинов: присоединения (ионный механизм – разрыв π-связи); полимеризация; восстановления; окисления (горение). Характерные химические реакции аренов (бензола и толуола): замещения (электрофильное по кольцу; радикальное в боковой цепи толуола); окисления (горение); окисления боковой цепи толуола; восстановления.

В 6 Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов, диенов, алкинов, ароматических углеводородов (бензола и толуола). Ионный (правило В. В. Марковникова) и радикальный механизмы реакций в органической химии 2 3 6 36, 9– 57, 6 % 15, 5 % 54, 4 % (32, 1 %, 51, 8 %, 63, 3 %)

В 6 Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов, диенов, алкинов, ароматических углеводородов (бензола и толуола). Ионный (правило В. В. Марковникова) и радикальный механизмы реакций в органической химии 2 5 6

В 7 Характерные химические свойства предельных одноатомных и многоатомных спиртов, фенола, альдегидов, предельных карбоновых кислот, сложных эфиров 1. o o o 2. o 3. o o Характерные химические реакции предельных одноатомных спиртов: замещения; этерификации; слабые кислотные свойства; дегидратация; окисления и восстановления. Характерные химические реакции многоатомных спиртов: кислотные свойства (комплекс с Cu(OH)2 – качественная реакция). Характерные химические реакции фенола: кислотные свойства; замещения в кольце (в т. ч. с Br 2 (aq) – качественная реакция); комплексные соединения с Fe. Cl 3 – качественная реакция; окисления.

В 7 Характерные химические свойства предельных одноатомных и многоатомных спиртов, фенола, альдегидов, предельных карбоновых кислот, сложных эфиров 4. o o o 5. o o 6. o Характерные химические реакции альдегидов: присоединения (присоединение-отщепление); окисления (с Ag 2 O (NH 3), Cu(OH)2 – качественные реакции); восстановления. Характерные химические реакции предельных карбоновых кислот: кислотные свойства; этерификации; окисления (горение); восстановления. Характерные химические реакции сложных эфиров: гидролиз.

В 7 Характерные химические свойства предельных одноатомных и многоатомных спиртов, фенола, альдегидов, предельных карбоновых кислот, сложных эфиров 1 3 5 33, 7– 82, 3 % 22, 6 % 43, 7 % (26, 6 %, 54, 6 %, 37, 7 %)

В 7 Характерные химические свойства предельных одноатомных и многоатомных спиртов, фенола, альдегидов, предельных карбоновых кислот, сложных эфиров 2 4 5

В 8 Характерные химические свойства азотсодержащих органических соединений: аминов и аминокислот. Биологически важные вещества: жиры, углеводы (моносахариды, дисахариды, полисахариды), белки 1. o o o 2. o o o 3. o o Характерные химические реакции аминов: оснóвные свойства; горение (азот, углекислый газ и вода); с Br 2 (aq) - качественная реакция на анилин. Характерные химические реакции аминокислот: амфотерные свойства; этерификация; пептизация. Характерные химические реакции белков: денатурация; цветные реакции (биуретовая, ксантопротеиновая, реакция на серу).

В 8 Характерные химические свойства азотсодержащих органических соединений: аминов и аминокислот. Биологически важные вещества: жиры, углеводы (моносахариды, дисахариды, полисахариды), белки 4. o o 5. o o o Характерные химические реакции жиров: омыление (гидролиз); гидрогенизация (восстановление) непредельных жиров. Характерные химические реакции углеводов (моносахариды, дисахариды, полисахариды): образование комплексных соединений с Cu(OH)2; замещения; окисление (моносахариды, дисахариды); восстановление (моносахариды, дисахариды); гидролиз (дисахариды, полисахариды).

В 8 Характерные химические свойства азотсодержащих органических соединений: аминов и аминокислот. Биологически важные вещества: жиры, углеводы (моносахариды, дисахариды, полисахариды), белки 4 5 6 37, 3– 63, 2 % 14, 1 % 53, 0 % (32, 3 %, 49, 5 %, 34, 9 %)

В 8 Характерные химические свойства азотсодержащих органических соединений: аминов и аминокислот. Биологически важные вещества: жиры, углеводы (моносахариды, дисахариды, полисахариды), белки 2 3 5

Часть 2

В 9 Вычисление массы растворенного вещества, содержащегося в определенной массе раствора с известной массовой долей Из раствора хлорида бария массой 50 г с массовой долей соли 3 % выпарили 6 г воды и добавили 1, 5 г соли. Массовая доля соли в 6, 6 полученном растворе равна _______ %. (Запишите число с точностью до десятых. ) m(Ba. Cl 2) = m(р-ра). ω = 50 г. 0, 03 = 1, 5 г m(в-ва) = 1, 5 г + 1, 5 г = 3, 0 г m(р-ра 2) = m(р-ра 1) – m(воды) + m(соли) = 50, 0 г – 6, 0 + 1, 5 г = 45, 5 г m(в-ва) 6, 6 % · 100 % = (3, 0 г / 45, 5 г) · 100 % = 6, 5934… % ω (Ba. Cl 2) = m(р-ра) 32, 4– 60, 1 % 37, 3 % 56, 2 % (56, 6 %, 60, 2 %, 82, 3 %)

В 9 Вычисление массы растворенного вещества, содержащегося в определенной массе раствора с известной массовой долей Из раствора хлорида бария массой 50 г с массовой долей соли 3 % выпарили 6 г воды и добавили 1, 5 г соли. Массовая доля соли в 6, 6 полученном растворе равна _______ %. (Запишите число с точностью до десятых. ) m(1 р-ра). ω1 + m(2 р-ра). ω2 = (m(1 р-ра) + m(2 р-ра)). ω3 . 0, 03 – 6. 0 50 m 1. ω1 – m 2. ω2 + 1, 5. 1, 0 = (m 1 – 6 + + m 3 ). ω4 + m 3. ω3 (50 – m 2 1, 5). ω4 ω (Ba. Cl 2) = 0, 065934…. 100 % = 6, 6 %

В 10 Расчеты массы вещества или объема газов по известному количеству вещества, массе или объёму одного из участвующих в реакции веществ Цинк массой 14, 5 г растворили в избытке водного раствора гидроксида натрия. Рассчитайте объём (н. у. ) газа, выделившегося в результате этой реакции. 5 Ответ: _______ л. (Запишите число с точностью до целых. ) Zn + 2 Na. OH + 2 H 2 O = Na 2[Zn(OH)4] + H 2↑ 1 моль 0, 223 моль 1 моль – по теории 0, 223 моль – на практике n = m/M = 14, 5 г / 65 г/моль = 0, 223 моль 5 л V = n · Vm = 0, 223 моль · 22, 4 л/моль = 4, 9952 л 40, 9– 65, 0 % 45, 0 % 51, 1 % (68, 1 %, 52, 2 %, 63, 5 %)

В 10 Расчеты массы вещества или объема газов по известному количеству вещества, массе или объёму одного из участвующих в реакции веществ Сульфид железа (II) массой 66, 8 г обработали избытком водного раствора хлороводородной кислоты. Рассчитайте объем (н. у. ) газа, выделившегося в результате этой реакции. 17 Ответ: _______ л. (Запишите число с точностью до десятых. ) Fe. S + 2 HCl = Fe. Cl 2 + H 2 S↑ 1 моль – по теории 0, 759 моль – на практике n = m/M = 66, 8 г / 88, 0 г/моль = 0, 759 моль 17 л V = n · Vm = 0, 759 моль · 22, 4 л/моль = 17, 0018 л

Особенности подготовки к ЕГЭ по химии Вопросы Части 3 ЕГЭ по химии

Система оценивания работ Ответы к заданиям Части 3 (С) записываются в бланке ответов № 2 и проверяются экспертной комиссией, в состав которой входят методисты, опытные учителя и преподаватели вузов. o Задания Части 3 имеют различную степень сложности и предусматривают проверку от 3 до 5 элементов содержания. o Наличие в ответе каждого элемента оценивается в 1 балл, поэтому максимальная оценка верно выполненного задания составляет от 3 до 5 баллов (в зависимости от степени сложности). o Задания с развернутым ответом могут быть выполнены учащимися разными способами.
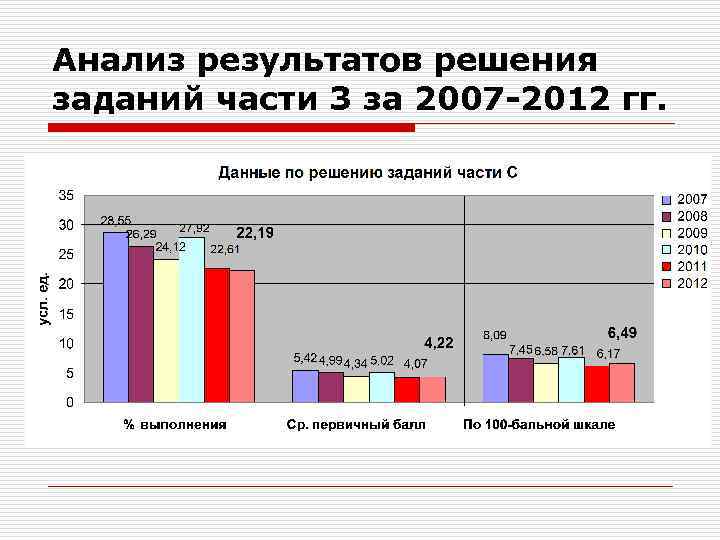
Анализ результатов решения заданий части 3 за 2007 -2012 гг.
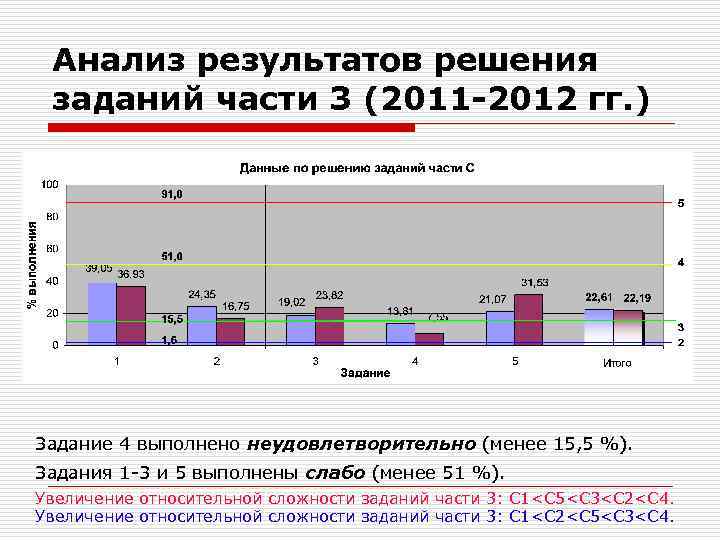
Анализ результатов решения заданий части 3 (2011 -2012 гг. ) Задание 4 выполнено неудовлетворительно (менее 15, 5 %). Задания 1 -3 и 5 выполнены слабо (менее 51 %). Увеличение относительной сложности заданий части 3: С 1<C 5<C 3<C 2<C 4. Увеличение относительной сложности заданий части 3: С 1<C 2<C 5<C 3<C 4.
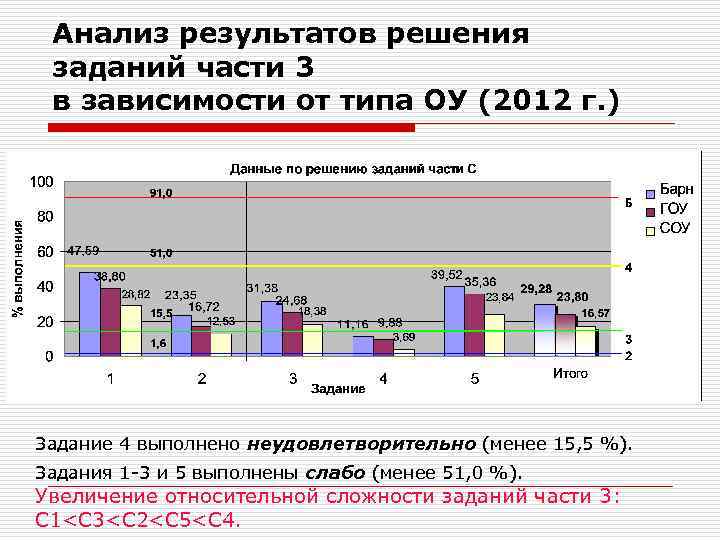
Анализ результатов решения заданий части 3 в зависимости от типа ОУ (2012 г. ) Задание 4 выполнено неудовлетворительно (менее 15, 5 %). Задания 1 -3 и 5 выполнены слабо (менее 51, 0 %). Увеличение относительной сложности заданий части 3: С 1<C 3<C 2<C 5<C 4.
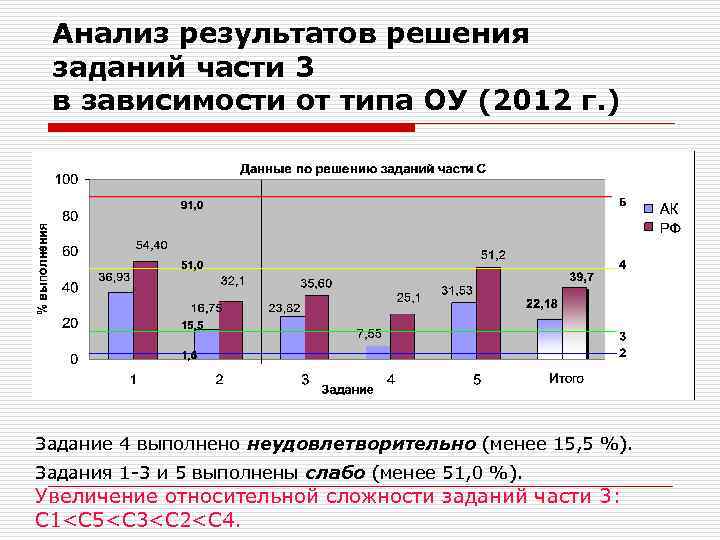
Анализ результатов решения заданий части 3 в зависимости от типа ОУ (2012 г. ) Задание 4 выполнено неудовлетворительно (менее 15, 5 %). Задания 1 -3 и 5 выполнены слабо (менее 51, 0 %). Увеличение относительной сложности заданий части 3: С 1<C 5<C 3<C 2<C 4.
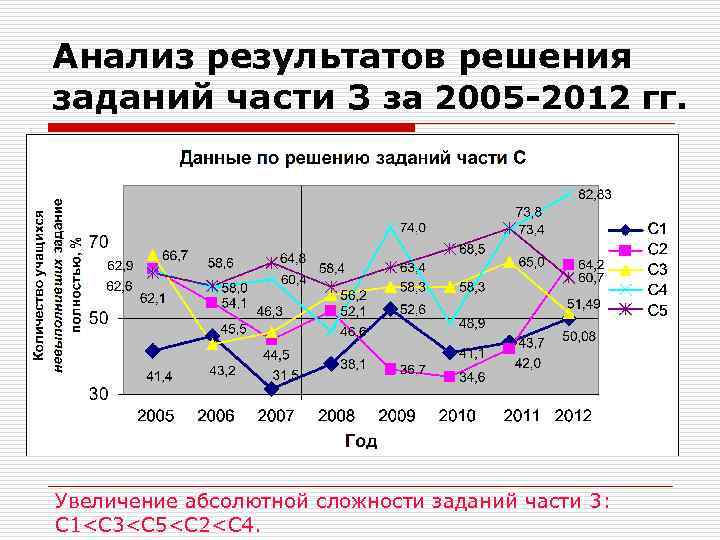
Анализ результатов решения заданий части 3 за 2005 -2012 гг. Увеличение абсолютной сложности заданий части 3: С 1<C 3<C 5<C 2<C 4.

Часть 3

С 1 Реакции окислительновосстановительные. Коррозия металлов и способы защиты от нее 1. Уравнения ОВР даны как в явном (полном), так и неявном (не полном) виде. 2. Обычно три компонента вступают в реакции ОВР: восстановитель, окислитель и среда. 3. Если есть среда, то обязательно будет вода. 4. Часто нужно знать существование ионов в различных средах (Mn, Cr). 5. Наиболее встречающиеся реакции с элементами: S, Mn, Hal, N, Cr, P, С (в орг. соединениях)

Типичные восстановители o o o Нейтральные атомы и молекулы: Al, Zn, Cr, Fe, H, С, Li. Al. H 4, H 2, NH 3, и др. Отрицательно заряженные ионы неметаллов: S 2–, I–, Br–, Cl– и др. Положительно заряженные ионы металлов в низшей степени окисления: Cr 2+, Fe 2+, Cu+ и др. Сложные ионы и молекулы, содержащие атомы в состоянии промежуточной степени окисления: SO 32–, NO 2–, Cr. O 2–, CO, SO 2, NO, P 4 O 6, C 2 H 5 OH, CH 3 CHO, HCOOH, H 2 C 2 O 4, C 6 H 12 O 6 и др. Электрический ток на катоде.

Типичные окислители o o o Нейтральные молекулы: F 2, Cl 2, Br 2, O 3, S, H 2 O 2 и др. Положительно заряженные ионы металлов и водорода: Cr 3+, Fe 3+, Cu 2+, Ag+, H+ и др. Сложные молекулы и ионы, содержащие атомы металла в состоянии высшей степени окисления: KMn. O 4, Na 2 Cr 2 O 7, Na 2 Cr. O 4, Cu. O, Ag 2 O, Mn. O 2, Cr. O 3, Pb. O 2, Pb 4+, Sn 4+ и др. Сложные ионы и молекулы, содержащие атомы неметалла в состоянии положительной степени окисления: NO 3–, HNO 3, H 2 SO 4(конц. ), SO 3, KCl. O, Ca(Cl. O)Cl и др. Электрический ток на аноде.

Среда o o o Кислая: H 2 SO 4, реже HCl и HNO 3 Щелочная: Na. OH или KOH Нейтральная: H 2 O

Полуреакции Mn и Cr кислая среда: Mn. O 4– + 8 H+ + 5ē → Mn 2+ + 4 H 2 O Mn+7 + 5ē → Mn+2 щелочная среда: Mn. O 4– + ē → Mn. O 42– Mn+7 + ē → Mn+6 нейтральная среда: Mn. O 4– + 2 H 2 O + 3ē → Mn. O 2 + 4 OH– Mn+7 + 3ē → Mn+4 кислая среда: Cr 2 O 72– + 14 H+ + 6ē → 2 Cr 3+ + 7 H 2 O 2 Cr+6 + 6ē → 2 Cr+3 щелочная среда: Cr 3+ + 8 OH– – 3ē → Cr. O 42+ + 4 H 2 O Cr+3 – 3ē → Cr+6

Наиболее известные полуреакции восстановления окислителей O 2 + 4ē → 2 O− 2; O 3 + 6ē → 3 O− 2; F 2 + 2ē → 2 F−; Cl 2 + 2ē → 2 Cl−; S+6 + 2ē → S+4 (H 2 SO 4 → SO 2); N+5 + ē → N+4 (концентрированная HNO 3 → NO 2); N+5 + 3ē → N+2 (разбавленная HNO 3 → NO; реакции со слабыми восстановителями); N+5 + 8ē → N− 3 (разбавленная HNO 3 → NH 4 NO 3; реакции с сильными восстановителями); 2 O− 1 + 2ē → 2 O− 2 (H 2 O 2)

С 1 Реакции окислительновосстановительные. Коррозия металлов и способы защиты от нее Используя метод электронного баланса, составьте уравнение реакции: Ca 3 P 2 +. . . + H 2 O → Ca 3(PO 4)2 + Mn. O 2 +. . Определите окислитель и восстановитель. 22, 8– 52, 6 % – диапазон выполнения задания С 1 16, 9 % – полностью справились с этим примером

C 1 – 3 +5 +4 Ca 3 P 2 +. . . + H 2 O → Ca 3(PO 4)2 + Mn. O 2 +. . 1) Составляем электронный баланс: – 3 +5 3 окисление 2 P – 16ē → 2 P Mn+7 + 3ē → Mn+4 16 восстановление 2) Расставляем коэффициенты в уравнении реакции: 3 Ca 3 P 2 + 16 KMn. O 4 + 8 H 2 O → 3 Ca 3(PO 4)2 + 16 Mn. O 2 + 16 KOH вос-тель ок-тель 3) Определяем окислитель и восстановитель 63, 1 % (61, 0 %, 55, 8 %, 66, 2 % – процент невыполнения в 2011 -2009 гг. )

С 1 Используя метод электронного баланса, составьте уравнение реакции: HCHO + KMn. O 4 +. . . → CO 2 + K 2 SO 4 +. . . . Определите окислитель и восстановитель. 29, 1– 65, 1 % – диапазон выполнения 30, 0 % – полностью справились с заданием

C 1 0 +7 +4 HCHO + KMn. O 4 +. . . → CO 2 + K 2 SO 4 +. . . 1) Составляем электронный баланс: 5 окисление C 0 – 4ē → C+4 4 восстановление Mn+7 + 5ē → Mn+2 2) Расставляем коэффициенты в уравнении реакции: 5 HCOH + 4 KMn. O 4 + 6 H 2 SO 4 = 5 CO 2 + 2 K 2 SO 4 + 4 Mn. SO 4 + 11 H 2 O вос-тель ок-тель 3) Определяем окислитель и восстановитель

С 1 Используя метод электронного баланса, составьте уравнение реакции: Ca(HS)2 + HNO 3 (конц. ) → . . . + Ca. SO 4 + NO 2 +. . Определите окислитель и восстановитель. 26, 3– 57, 7 % – диапазон выполнения задания С 1 4, 9 % – полностью справились с этим заданием

C 1 -2 +5 +6 +4 Ca(HS)2 + HNO 3 (конц. ) → . . . + Ca. SO 4 + NO 2 +. . 1) Составляем электронный баланс: -2 +6 1 окисление 2 S – 16ē → 2 S N+5 + ē → N+4 16 восстановление 2) Расставляем коэффициенты в уравнении реакции: Ca(HS)2 + 16 HNO 3 (конц. ) → H 2 SO 4 + Ca. SO 4 + 16 NO 2 + 8 H 2 O вос-тель ок-тель 3) Определяем окислитель и восстановитель

С 2 Реакции, подтверждающие взаимосвязь различных классов неорганических веществ 1. Изобразите генетическую связь неорганических веществ. 2. Отметьте характерные свойства вещества: кислотноосновные и окислительно-восстановительные, специфические. 3. Обратите внимание на концентрации веществ (если указывается): твердое, раствор, концентрированное вещество. 4. Если реакции ионного обмена, то продукт реакции проверьте по таблице растворимости на предмет существования (некоторые вещества гидролизуются). 5. Как правило, две реакции являются ОВР. 6. Необходимо записать четыре уравнения реакций (не схемы).

С 2 Реакции, подтверждающие взаимосвязь различных классов неорганических веществ Твёрдый хлорид лития нагрели с концентрированной серной кислотой. Выделившийся при этом газ растворили в воде. При взаимодействии полученного раствора с перманганатом калия образовалось простое газообразное вещество жёлто-зелёного цвета. При горении железной проволоки в этом веществе получили соль. Соль растворили в воде и смешали с раствором карбоната натрия. Напишите уравнения четырёх описанных реакций. 11, 3– 24, 2 % – диапазон выполнения задания С 2 2, 7 % – полностью справились с этим примером

C 2 Li. Cl(тв), H 2 SO 4 (конц. ), KMn. O 4, Fe, Na 2 CO 3 (р-р) соль ок-ль, к-та ок-ль мет. , в-ль соль сл. к-ты Записываем возможные уравнения реакций: 1) Li. Cl + H 2 SO 4 = HCl↑ + Li. HSO 4 2) 2 KMn. O 4 + 16 HCl = 2 Mn. Cl 2 + 5 Cl 2↑ + 2 KCl + 8 H 2 O 3) 2 Fe + 3 Cl 2 = 2 Fe. Cl 3 4) 2 Fe. Cl 3 + 3 Na 2 CO 3 + 3 H 2 O = 2 Fe(OH)3↓ + 6 Na. Cl + 3 CO 2↑ 83, 25 % (75, 7 %, 68, 9 %, 72, 6 %)

С 2 Реакции, подтверждающие взаимосвязь различных классов неорганических веществ Смесь оксида азота (IV) и кислорода пропустили через раствор гидроксида калия. Полученную при этом соль высушили и прокалили. Остаток, полученный после прокаливания соли, растворили в воде и смешали с раствором иодида калия и серной кислотой. Образовавшееся в ходе этой реакции простое вещество прореагировало с алюминием. Напишите уравнения четырёх описанных реакций.
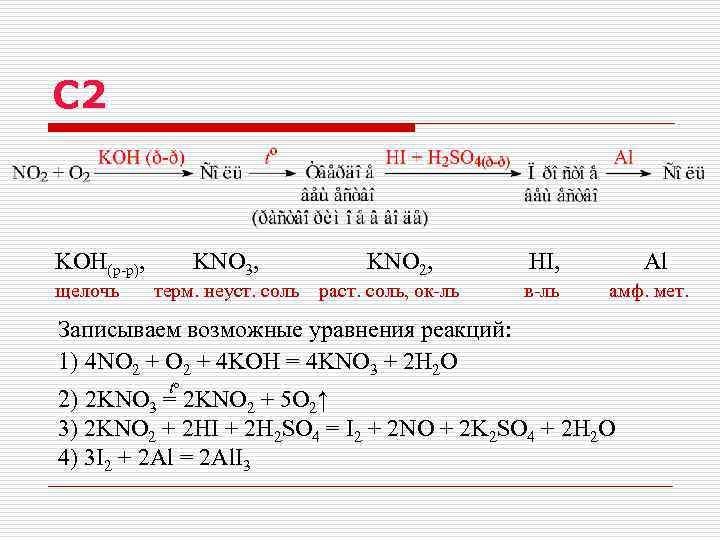
C 2 KOH(р-р), KNO 3, KNO 2, HI, Al щелочь терм. неуст. соль раст. соль, ок-ль в-ль амф. мет. Записываем возможные уравнения реакций: 1) 4 NO 2 + 4 KOH = 4 KNO 3 + 2 H 2 O to 2) 2 KNO 3 = 2 KNO 2 + 5 O 2↑ 3) 2 KNO 2 + 2 HI + 2 H 2 SO 4 = I 2 + 2 NO + 2 K 2 SO 4 + 2 H 2 O 4) 3 I 2 + 2 Al = 2 Al. I 3

С 3 Реакции, подтверждающие взаимосвязь органических соединений 1. Участвуют все классы органических соединений. 2. Цепочки представлены в неявном виде (по продукту или по условиям реакции). 3. Особое внимание необходимо обратить на условия протекания реакций (альтернативные реакции). 4. Все реакции необходимо уравнивать (в т. ч. ОВР). Никаких схем реакций быть не должно! 5. В случае затруднения выполнения цепи в прямом направлении, решайте с конца цепи или фрагментарно. Пытайтесь что-либо выполнить.

Альтернативные реакции
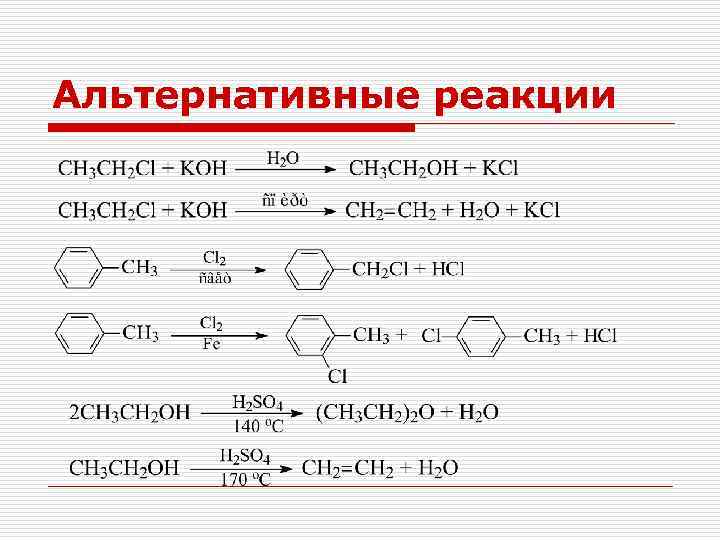
Альтернативные реакции

С 3 Реакции, подтверждающие взаимосвязь органических соединений Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: При написании уравнений реакций используйте структурные формулы органических веществ. 16, 0– 34, 6 % – диапазон выполнения задания С 3 3, 5 % - полностью справились с этим заданием

C 3 Записываем уравнения реакций: 1) Br. CH 2 CH 2 Br + Zn → Zn. Br 2 + t° 2) + HBr → CH 3 CH 2 Br 3) CH 3 CH 2 Br + KOH(спирт. р-р) → CH 3–CH=CH 2 + H 2 O +KBr 4) 3 CH 3–CH=CH 2 + 2 KMn. O 4 + 4 H 2 O → 3 CH 3–CH(OH)–CH 2 OH + 2 KOH + + 2 Mn. O 2 5) CH 3–CH(OH)–CH 2 OH + 2 HBr → CH 3–CH(Br)–CH 2 Br + 2 H 2 O 76, 2 % (81, 0 %, 81, 4 %)

С 3 Реакции, подтверждающие взаимосвязь органических соединений Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: При написании уравнений реакций используйте структурные формулы органических веществ.

C 3 Записываем уравнения реакций: hv 1) CH 3–CH 3 + Br 2 → CH 3–CH 2 Br + HBr H O, t° 2 2) CH 3–CH 2 Br + KOH –––→ CH 3–CH 2 OH + KBr 3) 3 CH 3–CH 2 OH + K 2 Cr 2 O 7 + 4 H 2 SO 4 → → 3 CH 3–CHO + Cr 2(SO 4)3 + K 2 SO 4 + 7 H 2 O kat, t° 4) CH 3–CHO + H 2 –––→ CH 3–CH 2 OH kat, t° 5) 2 CH 3–CH 2 OH –––→ CH 2=CH–CH=CH 2 + 2 H 2 O

С 4 Расчетные задачи на растворы 1. 2. 3. 4. 5. 6. 7. 8. Записываем уравнение(ия) реакции(ий). Выбираем алгоритм решения задачи: на избыток (или примесь), выход продукта реакции от теоретически возможного и определяем массовую долю (массу) химического соединения в смеси. Всего 4 этапа решения задачи. В расчетах ссылаться на уравнения реакций и использовать соответствующие математические формулы. Не забывайте проверять единицы измерения. Если количество вещества менее 1 моль, то необходимо брать три цифры после запятой. Массовые доли и процент пишите, отделяя скобками, или через союз или. Не забудьте записать ответ.

С 4 Расчетные задачи на растворы Смесь порошков железа и алюминия реагирует с 810 мл 10 %-ного раствора серной кислоты (ρ = 1, 07 г/мл). При взаимодействии такой же массы смеси с избытком раствора гидроксида натрия выделилось 14, 78 л водорода (н. у. ). Определите массовую долю железа в смеси. 3, 0– 12, 9 % – диапазон выполнения задания С 4 1, 9 % - полностью справились с этим заданием

С 4 Смесь порошков железа и алюминия реагирует с 810 мл 10 %-ного раствора серной кислоты (ρ = 1, 07 г/мл). При взаимодействии такой же массы смеси с избытком раствора гидроксида натрия выделилось 14, 78 л водорода (н. у. ). Определите массовую долю железа в смеси. 1) Записываем уравнения реакций металлов Fe + H 2 SO 4 = Fe. SO 4 + H 2 2 Al + 3 H 2 SO 4 = Al 2(SO 4)3 + 3 H 2 2 Al + 2 Na. OH + 6 H 2 O = 2 Na[Al(OH)4] + 3 H 2

C 4 Смесь порошков железа и алюминия реагирует с 810 мл 10 %-ного раствора серной кислоты (ρ = 1, 07 г/мл). При взаимодействии такой же массы смеси с избытком раствора гидроксида натрия выделилось 14, 78 л водорода (н. у. ). Определите массовую долю железа в смеси. 2) Рассчитываем количества веществ реагентов: n = m/M n = V/Vm n(H 2 SO 4) = (810 г · 1, 07 г/мл · 0, 1) / 98 г/моль = 0, 88 моль n(H 2) = 14, 78 л / 22, 4 л/моль = 0, 66 моль n(Al) = 2/3 n(H 2) = 0, 44 моль 2 Al + 2 Na. OH + 6 H 2 O = 2 Na[Al(OH)4] + 3 H 2 2 моль 0, 44 3 моль 0, 66

C 4 Смесь порошков железа и алюминия реагирует с 810 мл 10 %-ного раствора серной кислоты (ρ = 1, 07 г/мл). При взаимодействии такой же массы смеси с избытком раствора гидроксида натрия выделилось 14, 78 л водорода (н. у. ). Определите массовую долю железа в смеси. 2) Рассчитываем количества веществ реагентов: n(H 2 SO 4, израсходованной на реакцию с Al) = 1, 5 n(Al) = 0, 66 моль n(H 2 SO 4, израсходованной на реакцию с Fe) = = 0, 88 моль – 0, 66 моль = 0, 22 моль n(Fe) = n(H 2 SO 4) = 0, 22 моль 2 Al + 3 H 2 SO 4 = Al 2(SO 4)3 + 3 H 2 0, 44 0, 66 Fe + H 2 SO 4 = Fe. SO 4 + H 2 0, 22

C 4 Смесь порошков железа и алюминия реагирует с 810 мл 10 %-ного раствора серной кислоты (ρ = 1, 07 г/мл). При взаимодействии такой же массы смеси с избытком раствора гидроксида натрия выделилось 14, 78 л водорода (н. у. ). Определите массовую долю железа в смеси. 3) Вычисляем массы металлов и их смеси: m(Al) = 0, 440 моль · 27 г/моль = 11, 88 г m(Fe) = 0, 22 моль · 56 г/моль = 12, 32 г m(смеси) = 1, 88 г + 12, 32 г = 24, 2 г

C 4 Смесь порошков железа и алюминия реагирует с 810 мл 10 %-ного раствора серной кислоты (ρ = 1, 07 г/мл). При взаимодействии такой же массы смеси с избытком раствора гидроксида натрия выделилось 14, 78 л водорода (н. у. ). Определите массовую долю железа в смеси. 4) Рассчитываем массовую долю железа в смеси: ω(Fe) = 12, 32 г / 24, 2 г = 0, 509 или 50, 9 % Примечание. Не забудьте записать ответ. 92, 5 % (86, 2 %, 74, 7 %, 84, 3 %)

C 4 Примечание. В случае, когда в ответе содержится ошибка в вычислениях в одном из трёх элементов (втором, третьем или четвёртом), которая привела к неверному ответу, оценка за выполнение задания снижается только на 1 балл.

С 4 Расчетные задачи на растворы Определите массовую долю веществ в растворе, полученном в результате последовательного растворения в 150 мл воды 5, 75 г натрия и 8, 1 г оксида цинка.

С 4 Определите массовую долю веществ в растворе, полученном в результате последовательного растворения в 150 мл воды 5, 75 г натрия и 8, 1 г оксида цинка. 1) Записываем уравнения реакций металлов 2 Na + 2 H 2 O = 2 Na. OH + H 2 2 моль 1 моль – по теории Zn. O + 2 Na. OH + H 2 O = Na 2[Zn(OH)4] 1 моль 2 моль 1 моль – по теории

C 4 2 Na + 2 H 2 O = 2 Na. OH + H 2 2 моль 0, 25 моль 2 моль 1 моль 0, 25 моль 0, 125 моль – по теории – на практике Zn. O + 2 Na. OH + H 2 O = Na 2[Zn(OH)4] 1 моль 2 моль 0, 1 моль 0, 20 моль 1 моль 0, 1 моль 2) Рассчитываем количества веществ реагентов: n = m/M n(Na) = 5, 75 г / 23 г/моль = 0, 25 моль n(Zn. O) = 8, 1 г / 81 г/моль = 0, 10 моль n(Na. OH) = n(Na) = 0, 25 моль – избыток – по теории – на практике

C 4 2 Na + 2 H 2 O = 2 Na. OH + H 2 2 моль 0, 25 моль 2 моль 1 моль 0, 25 моль 0, 125 моль – по теории – на практике Zn. O + 2 Na. OH + H 2 O = Na 2[Zn(OH)4] 1 моль 2 моль 1 моль – по теории 0, 1 моль 0, 20 моль 0, 1 моль – на практике 3) Вычисляем массы продуктов реакций: n(H 2) = 0, 5 n(Na) = 0, 25 моль / 2 = 0, 125 моль m(H 2) = n · M = 0, 125 моль · 2 г/моль = 0, 25 г n(Na. OH прореагировало) = 2 n(Zn. O) = 0, 20 моль n(Na. OH осталось в растворе) = 0, 25 – 0, 20 = 0, 05 моль m(Na. OH) = 0, 05 моль · 40 г/моль = 2 г n(Na 2[Zn(OH)4]) = n(Zn. O) = 0, 10 моль m(Na 2[Zn(OH)4) = 0, 10 моль · 179 г/моль = 17, 9 г

C 4 Определите массовую долю веществ в растворе, полученном в результате последовательного растворения в 150 мл воды 5, 75 г натрия и 8, 1 г оксида цинка. 4) Рассчитываем массовые доли веществ в растворе: ω(Na. OH) = mв-ва / mр-ра = 2 г / (150 + 5, 75 + 8, 1 – 0, 25) г = = 2 / 163, 6 г = 0, 0122249… = 0, 0122 или 1, 22 % ω(Na 2[Zn(OH)4]) = mв-ва / mр-ра = 17, 9 г / 163, 6 г = 0, 109413… = 0, 1094 или 10, 94 % Примечание. Не забудьте записать ответ.

С 5 Нахождение молекулярной формулы веществ 1. 2. 3. 4. Необходимо знать брутто-формулы классов органических соединений. Необходимо уметь записывать химические реакции органических веществ с использованием брутто-формул. При горении органических веществ, содержащих углерод, водород и кислород выделяется углекислый газ и вода. При горении органических веществ (СН), содержащих азот выделяется N 2, а галогены – галогеноводород.

С 5 Нахождение молекулярной формулы веществ Решение задачи будет включать три последовательные операции: 1. составление схемы химической реакции и определение стехиометрических соотношений реагирующих веществ; 2. расчет молярной массы искомого соединения; 3. вычисления на их основе, приводящие к установлению молекулярной формулы вещества.

С 5 Нахождение молекулярной формулы веществ В результате реакции предельного одноатомного спирта с 9, 75 г металлического калия получено 28 г алкоголята. Определите молекулярную формулу исходного спирта. 26, 4– 38, 1 % – диапазон выполнения задания С 5 22, 6 % - полностью справились с этим заданием

С 5 В результате реакции предельного одноатомного спирта с 9, 75 г металлического калия получено 28 г алкоголята. Определите молекулярную формулу исходного спирта. 1) Записываем общее уравнение реакции и рассчитываем количества калия: 2 Сn. H 2 n+1 OH + 2 K = 2 Сn. H 2 n+1 OK + H 2↑ 2 моль 0, 25 моль n(K) = m / M = 9, 75 г / 39 г/моль = 0, 25 моль

С 5 В результате реакции предельного одноатомного спирта с 9, 75 г металлического калия получено 28 г алкоголята. Определите молекулярную формулу исходного спирта. 2) Рассчитываем молярную массу спирта: n(K) = n(Сn. H 2 n+1 OK) = 0, 25 моль (согласно закона сохранения массы вещества) M(Сn. H 2 n+1 OK) = m / n = 28 г / 0, 25 моль = 112 г/моль M(Сn. H 2 n+1 OH) = 112 – 39 + 1 = 74 г/моль

С 5 В результате реакции предельного одноатомного спирта с 9, 75 г металлического калия получено 28 г алкоголята. Определите молекулярную формулу исходного спирта. 3) Устанавливаем молекулярную формулу спирта: M(Сn. H 2 n+1 OH) = 12 n + 1 + 16 + 1 = 74 г/моль 14 n + 18 = 74 14 n = 56 n = 4 Молекулярная формула спирта – C 4 Н 9 OH Примечание. Не забудьте записать ответ. 68, 5 % (78, 9 %, 75, 5 %, 66, 4 %)

С 5 Нахождение молекулярной формулы веществ В результате окисления 11, 5 г предельного одноатомного спирта оксидом меди (II) получены продукты реакции общей массой 31, 5 г. Определите молекулярную формулу исходного спирта.

С 5 В результате окисления 11, 5 г предельного одноатомного спирта оксидом меди (II) получены продукты реакции общей массой 31, 5 г. Определите молекулярную формулу исходного спирта. 1) Записываем общее уравнение реакции и рассчитываем количество вещества оксида меди (II): Сn. H 2 n+1 OH + Cu. O = Сn. H 2 n. O + Cu + H 2 O 1 моль 0, 25 моль m(Cu. O) = 31, 5 г – 11, 5 г = 20 г (согласно закона сохранения массы вещества) n(Cu. O) = m / M = 20 г / 80 г/моль = 0, 25 моль

С 5 Сn. H 2 n+1 OH + Cu. O = Сn. H 2 n. O + Cu + H 2 O 0, 25 моль 2) Рассчитываем молярную массу спирта: n(Сn. H 2 n+1 OH) = n(Cu. O) = 0, 25 моль M(Сn. H 2 n+1 OH) = m / n = 11, 5 г / 0, 25 моль = 46 г/моль M(Сn. H 2 n+1 OH) = 112 – 39 + 1 = 74 г/моль

С 5 В результате окисления 11, 5 г предельного одноатомного спирта оксидом меди (II) получены продукты реакции общей массой 31, 5 г. Определите молекулярную формулу исходного спирта. 3) Устанавливаем молекулярную формулу спирта: M(Сn. H 2 n+1 OH) = 12 n + 1 + 16 + 1 = 46 г/моль 14 n + 18 = 46 14 n = 28 n = 2 Молекулярная формула спирта – C 2 Н 5 OH Примечание. Не забудьте записать ответ.

Литература 1. 2. 3. 4. 5. 6. 7. Кузьменко Н. Е. , Еремин В. В. , Попков В. А. Начала химии. В 2 Т. – М. : Экзамен, 2010. Дроздов А. А. , Еремин В. В. Пособие для подготовки к ЕГЭ по химии. – М. : БИНОМ. Лаборатория знаний, 2012. – 191 с. ЕГЭ-2013: Химия: самое полное издание типовых вариантов заданий / А. А. Каверина, Д. Ю. Добротин, М. Г. Снастина. – М. : Астрель, 2013. – 186 с. Химия. Подготовка к ЕГЭ-2012: учебно-методическое пособие / под ред. В. Н. Доронькина – Ростов н/Д: Легион. М, 2012. – 329 с. Егоров А. С. , Аминова Г. Х. Химия: экспресс-репетитор для подготовки к ЕГЭ. – Ростов н/Д: Феникс, 2011. – 279 с. Мешкова О. В. ЕГЭ. Химия: универсальный справочник. – М. : Эксмо, 2010. – 368 с. ЕГЭ 2009. Химия. Репетитор / П. А. Оржековский, Н. Н. Богданова, В. В. Загорский и др. – М. : Эксмо, 2009. – 112 с.

Официальные сайты ЕГЭ Официальный информационный портал ЕГЭ http: //www 1. ege. edu. ru Официальный сайт Федерального института педагогических измерений (ФИПИ) http: //www. fipi. ru Сайт информационной поддержки ЕГЭ в Алтайском крае http: //ege. uni-altai. ru/
http: //www. ege. edu. ru/ru/main/consult/ video_item/? vid_39=40

http: //www 1. ege. edu. ru/onlinetesting/chem
http: //www. edu. ru/moodle/
http: //www. fipi. ru/view/sections/ 155/docs/

Химический факультет Алт. ГУ Декан: Базарнова Наталья Григорьевна, д. х. н. , профессор Деканат: ауд. 102 К (пр-т, Красноармейский, 90) Телефон: 8(3852) 66 -66 -82 Сайт: www. chem. asu. ru E-mail: dekanat@chem. asu. ru

Спасибо за внимание! Желаю успехов!
ЕГЭ часть ВС-13.ppt