8c3064aad965e32d5841bd2b9ebe3316.ppt
- Количество слайдов: 27
 Ефекти на разтворителя, отчитани в квантово-химичните изчисления. Солватационни модели.
Ефекти на разтворителя, отчитани в квантово-химичните изчисления. Солватационни модели.
 При обичайните методи за изследване на електронната структура уравнението на Шрьодингер се решава за изолирана молекула или за молекули, отдалечени на безкрайно разстояние една от друга. Физически това съответства на ситуация в газова фаза при ниско налягане (вакуум). Експериментално обаче множеството химични реакции се провеждат в разтвор. Някои характеристики на молекулите (геометрия, вибрационни честоти, електронен спектър) зависят от вида на разтворителя поради взаимодействието между разтвореното вещество и разтворителя. Наличието на разтворител, в частност на полярен разтворител, може да промени разпределението на зарядите в молекулата. Това води до промяна на енергията и електронната плътност и свързаните с тях свойства.
При обичайните методи за изследване на електронната структура уравнението на Шрьодингер се решава за изолирана молекула или за молекули, отдалечени на безкрайно разстояние една от друга. Физически това съответства на ситуация в газова фаза при ниско налягане (вакуум). Експериментално обаче множеството химични реакции се провеждат в разтвор. Някои характеристики на молекулите (геометрия, вибрационни честоти, електронен спектър) зависят от вида на разтворителя поради взаимодействието между разтвореното вещество и разтворителя. Наличието на разтворител, в частност на полярен разтворител, може да промени разпределението на зарядите в молекулата. Това води до промяна на енергията и електронната плътност и свързаните с тях свойства.
 Ефектът на разтворителя може да бъде разделен на 2 важни части: -ефекти на специфична солватация (“short-range” effects), например водородно свързване или предпочетена ориентация на молекулите на разтворителя близо до молекулата на разтвореното вещество; -„макроскопски” ефекти (“long-range” effects), включващи поляризация на разтворителя. Тази long-range част е отговорна за генерирането на (макроскопска) диелектрична константа различна от 1. -Ефектът на специфичната солватация е концентриран главно върху първата солватационна сфера, а „макроскопския” (long-range) ефект изисква разглеждане на голям брой молекули.
Ефектът на разтворителя може да бъде разделен на 2 важни части: -ефекти на специфична солватация (“short-range” effects), например водородно свързване или предпочетена ориентация на молекулите на разтворителя близо до молекулата на разтвореното вещество; -„макроскопски” ефекти (“long-range” effects), включващи поляризация на разтворителя. Тази long-range част е отговорна за генерирането на (макроскопска) диелектрична константа различна от 1. -Ефектът на специфичната солватация е концентриран главно върху първата солватационна сфера, а „макроскопския” (long-range) ефект изисква разглеждане на голям брой молекули.
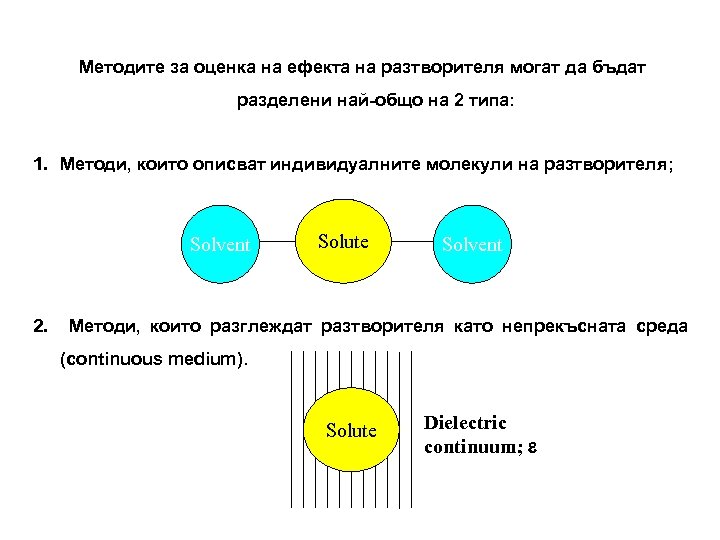 Методите за оценка на ефекта на разтворителя могат да бъдат разделени най-общо на 2 типа: 1. Методи, които описват индивидуалните молекули на разтворителя; Solvent 2. Solute Solvent Методи, които разглеждат разтворителя като непрекъсната среда (continuous medium). Solute Dielectric continuum; e
Методите за оценка на ефекта на разтворителя могат да бъдат разделени най-общо на 2 типа: 1. Методи, които описват индивидуалните молекули на разтворителя; Solvent 2. Solute Solvent Методи, които разглеждат разтворителя като непрекъсната среда (continuous medium). Solute Dielectric continuum; e
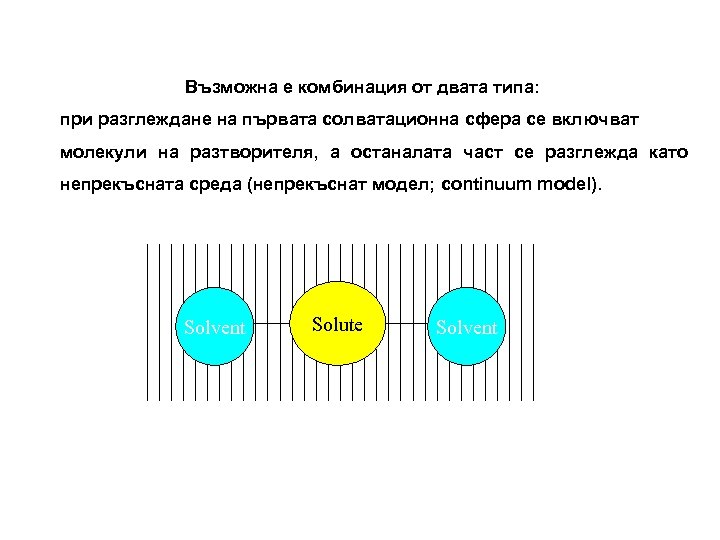 Възможна е комбинация от двата типа: при разглеждане на първата солватационна сфера се включват молекули на разтворителя, а останалата част се разглежда като непрекъсната среда (непрекъснат модел; continuum mоdel). Solvent Solute Solvent
Възможна е комбинация от двата типа: при разглеждане на първата солватационна сфера се включват молекули на разтворителя, а останалата част се разглежда като непрекъсната среда (непрекъснат модел; continuum mоdel). Solvent Solute Solvent
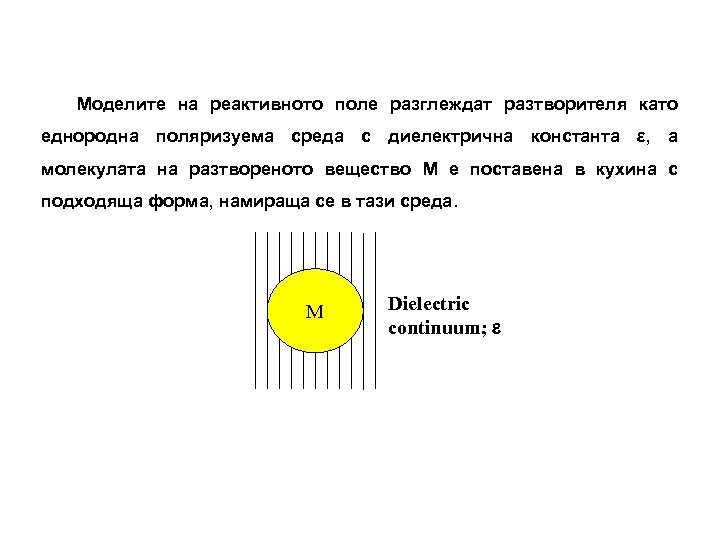 Моделите на реактивното поле разглеждат разтворителя като еднородна поляризуема среда с диелектрична константа ε, а молекулата на разтвореното вещество М е поставена в кухина с подходяща форма, намираща се в тази среда. М Dielectric continuum; e
Моделите на реактивното поле разглеждат разтворителя като еднородна поляризуема среда с диелектрична константа ε, а молекулата на разтвореното вещество М е поставена в кухина с подходяща форма, намираща се в тази среда. М Dielectric continuum; e
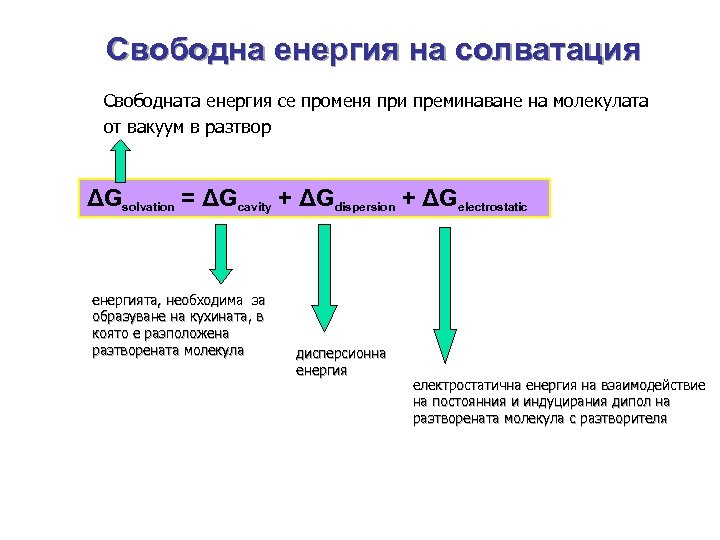 Свободна енергия на солватация Свободната енергия се променя при преминаване на молекулата от вакуум в разтвор ΔGsоlvation = ΔGcavity + ΔGdispersion + ΔGelectrostatic енергията, необходима за образуване на кухината, в която е разположена разтворената молекула дисперсионна енергия електростатична енергия на взаимодействие на постоянния и индуцирания дипол на разтворената молекула с разтворителя
Свободна енергия на солватация Свободната енергия се променя при преминаване на молекулата от вакуум в разтвор ΔGsоlvation = ΔGcavity + ΔGdispersion + ΔGelectrostatic енергията, необходима за образуване на кухината, в която е разположена разтворената молекула дисперсионна енергия електростатична енергия на взаимодействие на постоянния и индуцирания дипол на разтворената молекула с разтворителя
 Моделите на реактивното поле се различават по 5 аспекта: 1. Как се дефинират размера и формата на кухината; 2. Как се изчисляват дисперсионните приноси; 3. Как се представя разпределението на заряда на молекулата; 4. Как се описва молекулата М на разтвореното вещество: - класически (силово поле) - изразява се количествено (с полуемпирични или ab initio методи) 5. Как се описва диелектричната среда.
Моделите на реактивното поле се различават по 5 аспекта: 1. Как се дефинират размера и формата на кухината; 2. Как се изчисляват дисперсионните приноси; 3. Как се представя разпределението на заряда на молекулата; 4. Как се описва молекулата М на разтвореното вещество: - класически (силово поле) - изразява се количествено (с полуемпирични или ab initio методи) 5. Как се описва диелектричната среда.
 The Born Model n n Born, 1920: електростатичната компонента на свободната енергия на солватация за заряд поставен в сферична кухина, намираща се в разтворителя. Солватационната енергия е равна на работата за преминаване на йон от вакуум в среда. e q a n n Използват се йонни радиуси, определени по кристалографски път. Подходящ само за описание на йони.
The Born Model n n Born, 1920: електростатичната компонента на свободната енергия на солватация за заряд поставен в сферична кухина, намираща се в разтворителя. Солватационната енергия е равна на работата за преминаване на йон от вакуум в среда. e q a n n Използват се йонни радиуси, определени по кристалографски път. Подходящ само за описание на йони.
 Обобщено уравнение на Борн Generalized Born (GB) Equation n Разглежда система от N частици с радиус ai и заряди qi в среда с диелектрична проницаемост e.
Обобщено уравнение на Борн Generalized Born (GB) Equation n Разглежда система от N частици с радиус ai и заряди qi в среда с диелектрична проницаемост e.
 Приложение на обобщеното уравнение на Борн когато i = j този израз преминава в уравнението на Born; for two charges close together the expression returns the Onsager result (ie. a dipole where rij ai, aj); for two charges very far apart (rij ai, aj)) it is close to sum of Coulomb and Born expressions. Предимство: изразът може да се диференцира аналитично; затова е възможна бърза оптимизация!
Приложение на обобщеното уравнение на Борн когато i = j този израз преминава в уравнението на Born; for two charges close together the expression returns the Onsager result (ie. a dipole where rij ai, aj); for two charges very far apart (rij ai, aj)) it is close to sum of Coulomb and Born expressions. Предимство: изразът може да се диференцира аналитично; затова е възможна бърза оптимизация!
 Модел на Onsager n Onsager, 1936: разглежда поляризуем дипол с поляризуемост a в центъра на сфера. n Разтворената молекула индуцира реактивно поле в околната среда. Тя от своя страна индуцира електрично поле в кухината, което взаимодейства с дипола. a e
Модел на Onsager n Onsager, 1936: разглежда поляризуем дипол с поляризуемост a в центъра на сфера. n Разтворената молекула индуцира реактивно поле в околната среда. Тя от своя страна индуцира електрично поле в кухината, което взаимодейства с дипола. a e
 класически Onsager n n Ако структурата е заредена, трябва да се добави съответен член от модела на Born. Други модели: точков дипол в центъра на сфера (Bell), квадрупол в центъра на сфера (Abraham), мултиполно разширение за да се представи разтворената молекула, елипсоидална кухина.
класически Onsager n n Ако структурата е заредена, трябва да се добави съответен член от модела на Born. Други модели: точков дипол в центъра на сфера (Bell), квадрупол в центъра на сфера (Abraham), мултиполно разширение за да се представи разтворената молекула, елипсоидална кухина.
 квантов Onsager самосъгласовано реактивно поле (Self-Consistent Reaction Field) n Реактивното поле е пертурбация от първи порядък на Хамилтониана. Корекционен фактор за извършената работа при създаване на зарядовото разпределение на разтворената молекула в кухината от средата.
квантов Onsager самосъгласовано реактивно поле (Self-Consistent Reaction Field) n Реактивното поле е пертурбация от първи порядък на Хамилтониана. Корекционен фактор за извършената работа при създаване на зарядовото разпределение на разтворената молекула в кухината от средата.
 Модел на Onsager n n Могат да се използват сферични и елипсовидни кухини предимство: могат да се получат аналитични изрази за първите и вторите производни недостатък: рядко това е истина! Как се определя радиуса? n За сферична молекула може да се намери от молекулния обем, Vm : n n n Определя се от най-голямото междуатомно разстояние Използват се радиусите от контура на електронните плътности Често получените по горните процедури радиуси се завишават за да се отчете факта, че молекулите на разтворителя не могат да се приближат толкова близо до разтворената молекула.
Модел на Onsager n n Могат да се използват сферични и елипсовидни кухини предимство: могат да се получат аналитични изрази за първите и вторите производни недостатък: рядко това е истина! Как се определя радиуса? n За сферична молекула може да се намери от молекулния обем, Vm : n n n Определя се от най-голямото междуатомно разстояние Използват се радиусите от контура на електронните плътности Често получените по горните процедури радиуси се завишават за да се отчете факта, че молекулите на разтворителя не могат да се приближат толкова близо до разтворената молекула.
 The Polarizable Continuum Method (PCM) n n n van der Waals радиуси на атомите се използват за да се определи повърхнината от кухините. Повърхнината се разделя на голям бой малки повърхнинни елементи с област DS. ако Ei е градиента на електричното поле в точка i на молекулата то тогава първоначалния заряд qi се присвоява на всеки елемент като: Намира се потенциала, дължащ се на точковите заряди, fs(r), получава се нов градиент на електричното поле. Зарядите се модифицират докато се достигне конвергенция. Хамилтониана, описващ разтворената молекула се модифицира: След всяка SCF процедура се изчисляват нови qi и fs(r).
The Polarizable Continuum Method (PCM) n n n van der Waals радиуси на атомите се използват за да се определи повърхнината от кухините. Повърхнината се разделя на голям бой малки повърхнинни елементи с област DS. ако Ei е градиента на електричното поле в точка i на молекулата то тогава първоначалния заряд qi се присвоява на всеки елемент като: Намира се потенциала, дължащ се на точковите заряди, fs(r), получава се нов градиент на електричното поле. Зарядите се модифицират докато се достигне конвергенция. Хамилтониана, описващ разтворената молекула се модифицира: След всяка SCF процедура се изчисляват нови qi и fs(r).
 The PCM Approach Извършената работа при създаването на зарядовото разпределение вътре в кухината на диелектричната среда.
The PCM Approach Извършената работа при създаването на зарядовото разпределение вътре в кухината на диелектричната среда.
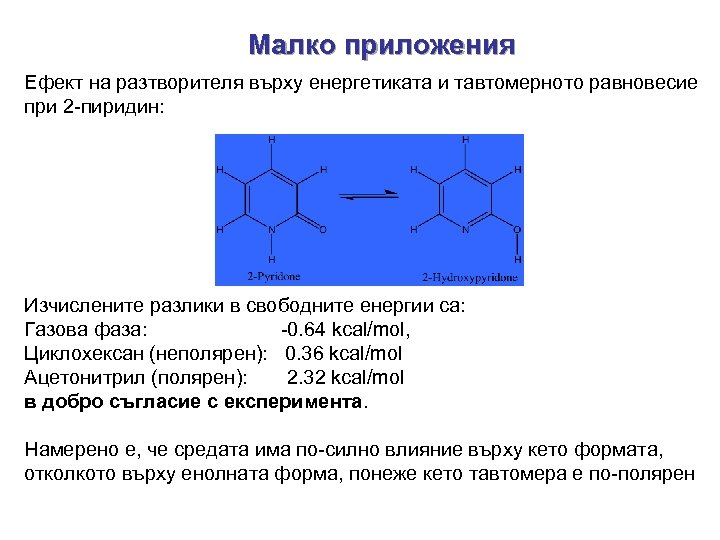 Малко приложения Ефект на разтворителя върху енергетиката и тавтомерното равновесие при 2 -пиридин: Изчислените разлики в свободните енергии са: Газова фаза: -0. 64 kcal/mol, Циклохексан (неполярен): 0. 36 kcal/mol Ацетонитрил (полярен): 2. 32 kcal/mol в добро съгласие с експеримента. Намерено е, че средата има по-силно влияние върху кето формата, отколкото върху енолната форма, понеже кето тавтомера е по-полярен
Малко приложения Ефект на разтворителя върху енергетиката и тавтомерното равновесие при 2 -пиридин: Изчислените разлики в свободните енергии са: Газова фаза: -0. 64 kcal/mol, Циклохексан (неполярен): 0. 36 kcal/mol Ацетонитрил (полярен): 2. 32 kcal/mol в добро съгласие с експеримента. Намерено е, че средата има по-силно влияние върху кето формата, отколкото върху енолната форма, понеже кето тавтомера е по-полярен
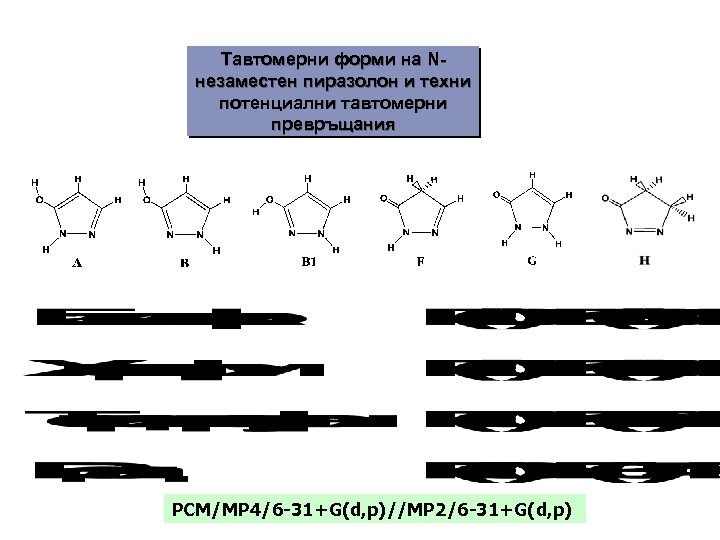 Тавтомерни форми на Nнезаместен пиразолон и техни потенциални тавтомерни превръщания PCM/MP 4/6 -31+G(d, p)//MP 2/6 -31+G(d, p)
Тавтомерни форми на Nнезаместен пиразолон и техни потенциални тавтомерни превръщания PCM/MP 4/6 -31+G(d, p)//MP 2/6 -31+G(d, p)
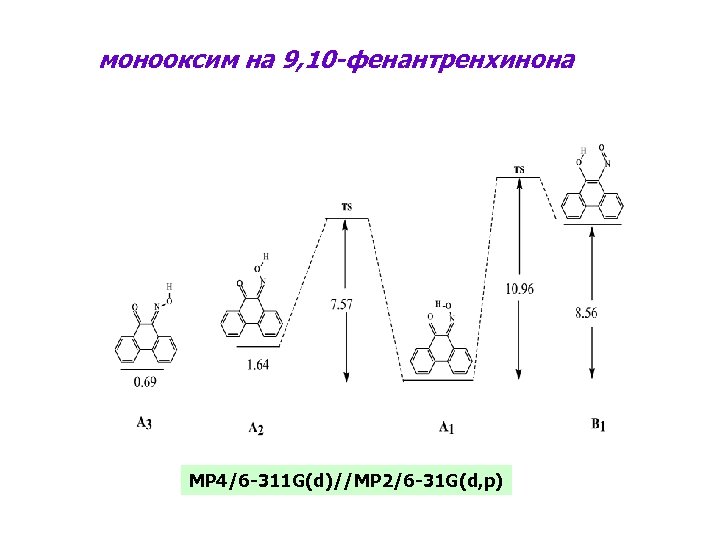 монооксим на 9, 10 -фенантренхинона MP 4/6 -311 G(d)//MP 2/6 -31 G(d, p)
монооксим на 9, 10 -фенантренхинона MP 4/6 -311 G(d)//MP 2/6 -31 G(d, p)
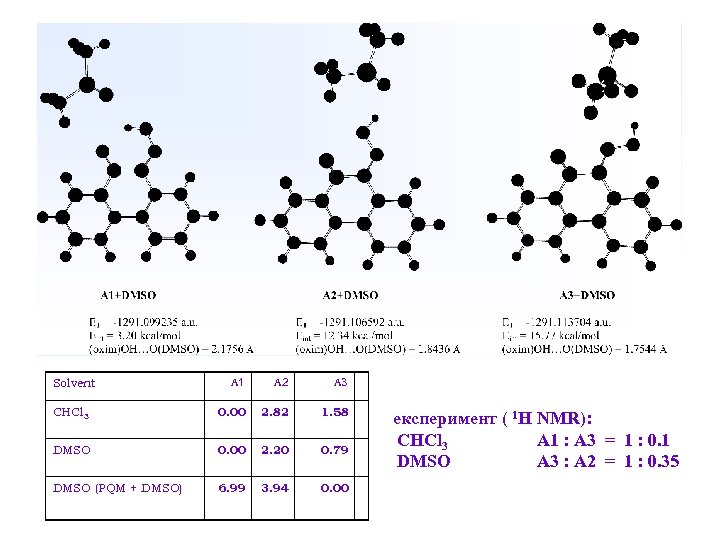 A 1 A 2 A 3 CHCl 3 0. 00 2. 82 1. 58 DMSO 0. 00 2. 20 0. 79 DMSO (PQM + DMSO) 6. 99 3. 94 0. 00 Solvent експеримент ( 1 H NMR): CHCl 3 A 1 : A 3 = 1 : 0. 1 DMSO A 3 : A 2 = 1 : 0. 35
A 1 A 2 A 3 CHCl 3 0. 00 2. 82 1. 58 DMSO 0. 00 2. 20 0. 79 DMSO (PQM + DMSO) 6. 99 3. 94 0. 00 Solvent експеримент ( 1 H NMR): CHCl 3 A 1 : A 3 = 1 : 0. 1 DMSO A 3 : A 2 = 1 : 0. 35
 Разгледаните до сега модели n n n Разглеждат разтворителя като поляризуема среда вместо точно отчитане на молекулите на разтворителя Зарядовото рапределение на разтворената молекула поляризира разтворителя пораждайки реакционно поле Реакционното поле на разтворителя променя разтворената молекула Взаимодействията трябва да се изчисляват самосъгласовано Тези методи са известни като методи на самосъгласованото реактивно поле – SCRF Не могат да отчитат специфични взаимодействия, такива като водородни връзки
Разгледаните до сега модели n n n Разглеждат разтворителя като поляризуема среда вместо точно отчитане на молекулите на разтворителя Зарядовото рапределение на разтворената молекула поляризира разтворителя пораждайки реакционно поле Реакционното поле на разтворителя променя разтворената молекула Взаимодействията трябва да се изчисляват самосъгласовано Тези методи са известни като методи на самосъгласованото реактивно поле – SCRF Не могат да отчитат специфични взаимодействия, такива като водородни връзки
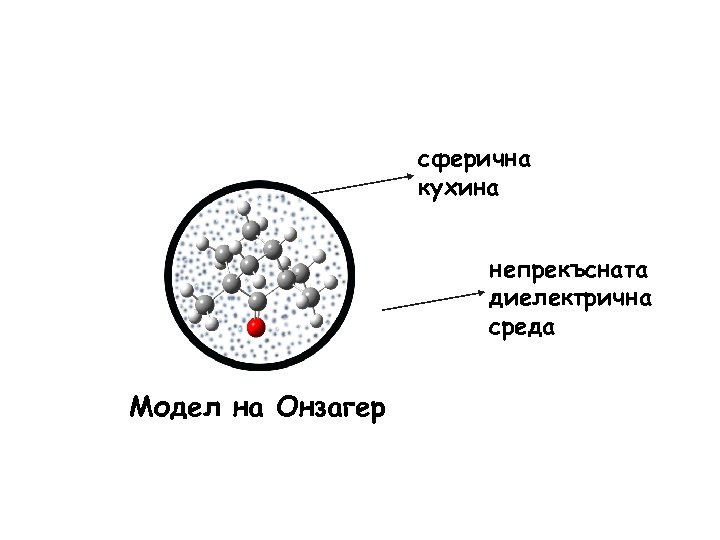 сферична кухина непрекъсната диелектрична среда Модел на Онзагер
сферична кухина непрекъсната диелектрична среда Модел на Онзагер
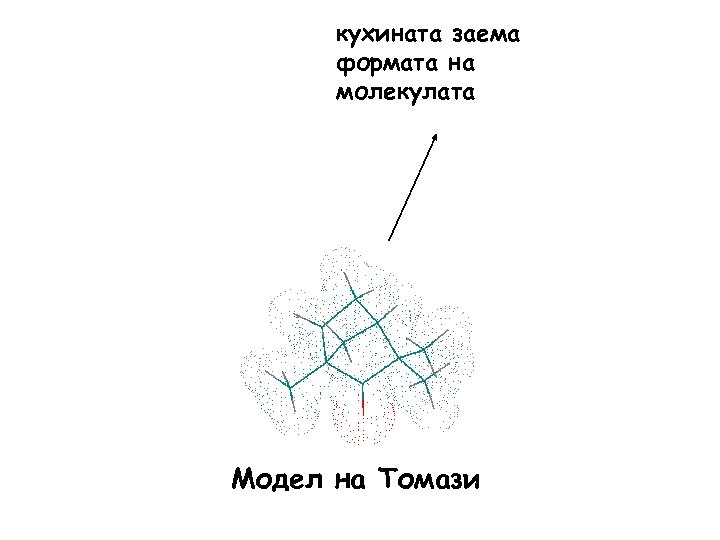 кухината заема формата на молекулата Модел на Томази
кухината заема формата на молекулата Модел на Томази
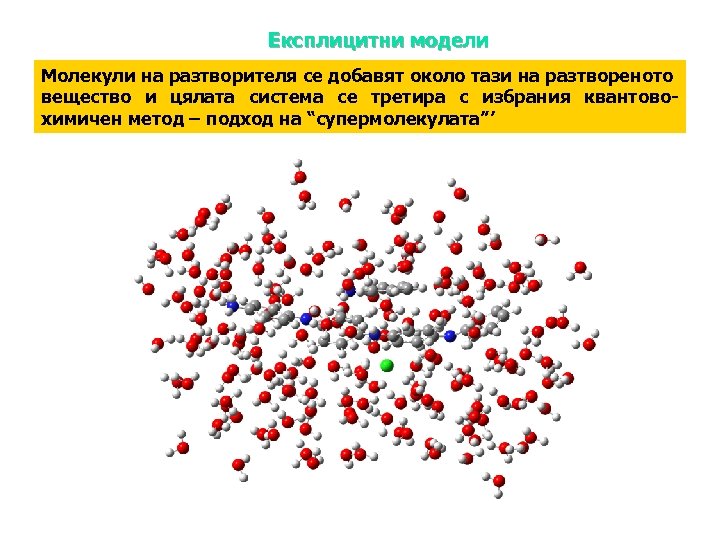 Експлицитни модели Молекули на разтворителя се добавят около тази на разтвореното вещество и цялата система се третира с избрания квантовохимичен метод – подход на “супермолекулата”’
Експлицитни модели Молекули на разтворителя се добавят около тази на разтвореното вещество и цялата система се третира с избрания квантовохимичен метод – подход на “супермолекулата”’
 Модел на супермолекулата Не изисква специални входни данни; изходните данни са стандартни. Предимства: • възможност за отчитане на специфични взаимодействия с молекулите на разтворителя, например водородни връзки; • получават се и МО на разтворителя; • по-точна структура. Недостатъци: • по-трудно се разграничават приносите на разтворителя и на разтвореното вещество; • изисква огромни компютърни ресурси; • обикновено се работи с методи от ниско ниво.
Модел на супермолекулата Не изисква специални входни данни; изходните данни са стандартни. Предимства: • възможност за отчитане на специфични взаимодействия с молекулите на разтворителя, например водородни връзки; • получават се и МО на разтворителя; • по-точна структура. Недостатъци: • по-трудно се разграничават приносите на разтворителя и на разтвореното вещество; • изисква огромни компютърни ресурси; • обикновено се работи с методи от ниско ниво.
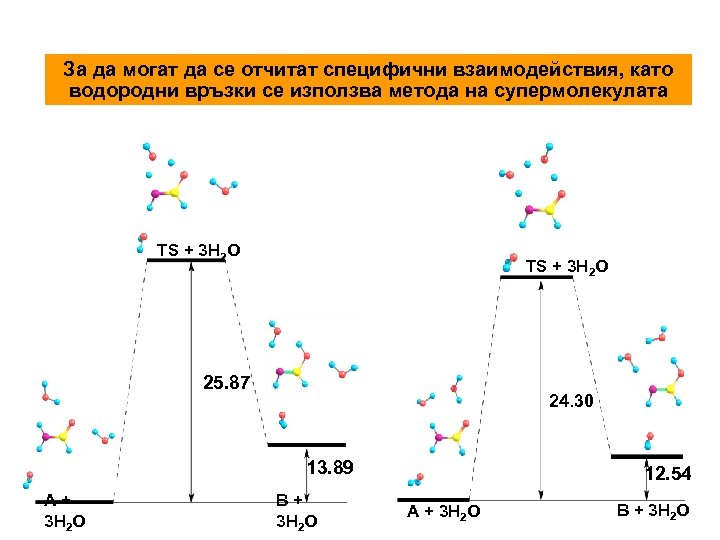 За да могат да се отчитат специфични взаимодействия, като водородни връзки се използва метода на супермолекулата TS + 3 H 2 O 25. 87 24. 30 13. 89 А+ 3 H 2 O В+ 3 H 2 O 12. 54 А + 3 H 2 O В + 3 H 2 O
За да могат да се отчитат специфични взаимодействия, като водородни връзки се използва метода на супермолекулата TS + 3 H 2 O 25. 87 24. 30 13. 89 А+ 3 H 2 O В+ 3 H 2 O 12. 54 А + 3 H 2 O В + 3 H 2 O


