 Д/з - § 21; конспект - установить окислитель и восстановитель в реакциях конспекта; - выписать качественные реакции в конец тетради – кислород и озон.
Д/з - § 21; конспект - установить окислитель и восстановитель в реакциях конспекта; - выписать качественные реакции в конец тетради – кислород и озон.
 КИСЛОРОД 1. Получение в промышленности: 1. фракционная перегонка (разделение) жидкого воздуха; 2. Электролиз воды.
КИСЛОРОД 1. Получение в промышленности: 1. фракционная перегонка (разделение) жидкого воздуха; 2. Электролиз воды.
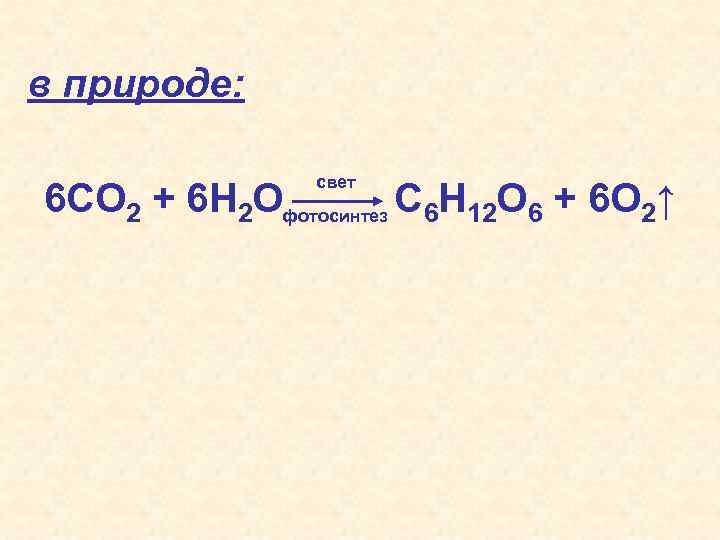 в природе: свет 6 СO 2 + 6 H 2 Oфотосинтез C 6 H 12 O 6 + 6 O 2↑
в природе: свет 6 СO 2 + 6 H 2 Oфотосинтез C 6 H 12 O 6 + 6 O 2↑
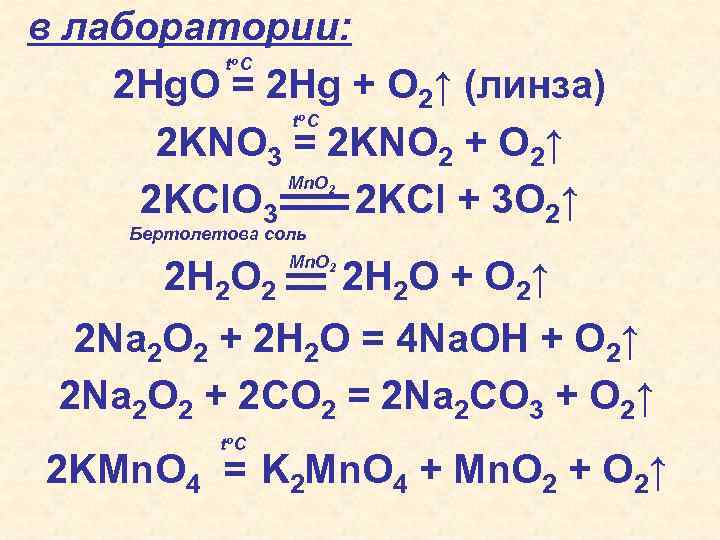 в лаборатории: t C 2 Hg. O = 2 Hg + O 2↑ (линза) t C 2 KNO 3 = 2 KNO 2 + O 2↑ Mn. O 2 KCl. O 3 2 KCl + 3 O 2↑ o o 2 Бертолетова соль 2 H 2 O 2 Mn. O 2 2 H 2 O + O 2↑ 2 Na 2 O 2 + 2 H 2 O = 4 Na. OH + O 2↑ 2 Na 2 O 2 + 2 CO 2 = 2 Na 2 CO 3 + O 2↑ to C 2 KMn. O 4 = K 2 Mn. O 4 + Mn. O 2 + O 2↑
в лаборатории: t C 2 Hg. O = 2 Hg + O 2↑ (линза) t C 2 KNO 3 = 2 KNO 2 + O 2↑ Mn. O 2 KCl. O 3 2 KCl + 3 O 2↑ o o 2 Бертолетова соль 2 H 2 O 2 Mn. O 2 2 H 2 O + O 2↑ 2 Na 2 O 2 + 2 H 2 O = 4 Na. OH + O 2↑ 2 Na 2 O 2 + 2 CO 2 = 2 Na 2 CO 3 + O 2↑ to C 2 KMn. O 4 = K 2 Mn. O 4 + Mn. O 2 + O 2↑
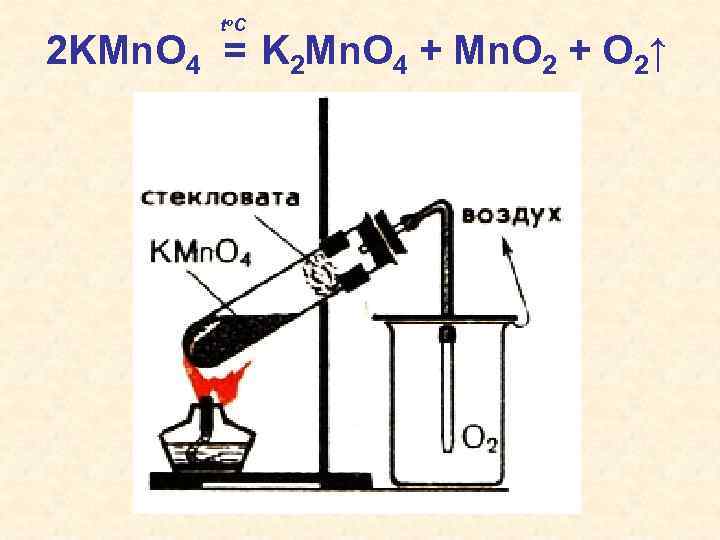 to C 2 KMn. O 4 = K 2 Mn. O 4 + Mn. O 2 + O 2↑
to C 2 KMn. O 4 = K 2 Mn. O 4 + Mn. O 2 + O 2↑
 2. Физические свойства У кислорода есть три аллотропные модификации (видоизменения): О – атомарный кислород; О 2 – кислород; О 3 – озон.
2. Физические свойства У кислорода есть три аллотропные модификации (видоизменения): О – атомарный кислород; О 2 – кислород; О 3 – озон.
 O 2 г; ц; з; в; в жидком и тв. состоянии – голубого цвета; малорастворим в воде – при 20 о. С в 1 V воды – 0, 031 V(O 2). Но увеличивается с понижением температуры: 0 о. С в 1 V воды – 0, 05 V(O 2). Тяжелее воздуха
O 2 г; ц; з; в; в жидком и тв. состоянии – голубого цвета; малорастворим в воде – при 20 о. С в 1 V воды – 0, 031 V(O 2). Но увеличивается с понижением температуры: 0 о. С в 1 V воды – 0, 05 V(O 2). Тяжелее воздуха
 O 2 Собирают: - методом вытеснения воды; - методом вытеснения воздуха;
O 2 Собирают: - методом вытеснения воды; - методом вытеснения воздуха;
 O 2 Качественная реакция: - вспыхивает тлеющая лучинка; хранение см. стр. 128 (рис. 69)
O 2 Качественная реакция: - вспыхивает тлеющая лучинка; хранение см. стр. 128 (рис. 69)
 O 3 г; ц – голубой; з - специфический; в жидком и тв. состоянии – тёмно-синего (почти чёрный) цвета; Тяжелее воздуха Яд в больших количествах! «Чистым озоном нельзя дышать»
O 3 г; ц – голубой; з - специфический; в жидком и тв. состоянии – тёмно-синего (почти чёрный) цвета; Тяжелее воздуха Яд в больших количествах! «Чистым озоном нельзя дышать»
 O 3 Качественная реакция: - вспыхивает тлеющая лучинка; - посинение иодокрахмальной бумаги 2 KI + H 2 O + O 3 = I 2↓ + 2 KOH + O 2↑ + крахмал
O 3 Качественная реакция: - вспыхивает тлеющая лучинка; - посинение иодокрахмальной бумаги 2 KI + H 2 O + O 3 = I 2↓ + 2 KOH + O 2↑ + крахмал
 O 3 Получение: - «Гроза» , мощные электрические разряды, УФлампа; 3 O 2↑ 2 O 3↑ - Разложение сильных окислителей: t C K 2 S 2 O 8 + HNO 3 → O 3↑ + …. o персульфат калия
O 3 Получение: - «Гроза» , мощные электрические разряды, УФлампа; 3 O 2↑ 2 O 3↑ - Разложение сильных окислителей: t C K 2 S 2 O 8 + HNO 3 → O 3↑ + …. o персульфат калия
 3. Химические свойства При нагревании O 2 энергично реагирует со многими веществами, является окислителем. Реакции с кислородом, сопровождающиеся выделением тепла (+Q) и света, называются горением.
3. Химические свойства При нагревании O 2 энергично реагирует со многими веществами, является окислителем. Реакции с кислородом, сопровождающиеся выделением тепла (+Q) и света, называются горением.
 При реакции с щ/Ме (кроме лития) – образуются пероксиды: 2 Na + O 2 = Na 2 O 2
При реакции с щ/Ме (кроме лития) – образуются пероксиды: 2 Na + O 2 = Na 2 O 2
 C остальными металлами оксиды: 4 Li + O 2 = 2 Li 2 O 3 Fe + 2 O 2 = Fe 3 O 4 железная окалина
C остальными металлами оксиды: 4 Li + O 2 = 2 Li 2 O 3 Fe + 2 O 2 = Fe 3 O 4 железная окалина
 C неметаллами - оксиды: +4 S + O 2 = SO 2 +5 4 P + 5 O 2 = 2 P 2 O 5 +2 N 2 + O 2 = 2 NO – Q, к. Дж
C неметаллами - оксиды: +4 S + O 2 = SO 2 +5 4 P + 5 O 2 = 2 P 2 O 5 +2 N 2 + O 2 = 2 NO – Q, к. Дж
 Cо сложными веществами – несколько оксидов: СH 4 + 2 O 2 = CO 2 + 2 H 2 O 2 H 2 S + 3 O 2 = 2 SO 2 + 2 H 2 O Исключения: соединения с азотом – они сгорают до N 2 4 NH 3 + 3 O 2 = 2 N 2↑ + 6 H 2 O аммиак
Cо сложными веществами – несколько оксидов: СH 4 + 2 O 2 = CO 2 + 2 H 2 O 2 H 2 S + 3 O 2 = 2 SO 2 + 2 H 2 O Исключения: соединения с азотом – они сгорают до N 2 4 NH 3 + 3 O 2 = 2 N 2↑ + 6 H 2 O аммиак
 Т. о. в ходе химических реакций кислород проявляет с. о. : -2 -1 0 Оксиды Пероксиды O Основания O 2 Кислоты O 3 Соли HOF +1 +2 O 2 F
Т. о. в ходе химических реакций кислород проявляет с. о. : -2 -1 0 Оксиды Пероксиды O Основания O 2 Кислоты O 3 Соли HOF +1 +2 O 2 F