 Дыхание растений
Дыхание растений
 Понятие о дыхании Дыхание – это процесс распада сложных органических соединений до СО 2 и воды при участии кислорода воздуха, сопровождаемый выделением энергии. С 6 Н 12 О 6+6 О 2→ 6 СО 2 + 6 Н 2 О + 2824 к. Дж
Понятие о дыхании Дыхание – это процесс распада сложных органических соединений до СО 2 и воды при участии кислорода воздуха, сопровождаемый выделением энергии. С 6 Н 12 О 6+6 О 2→ 6 СО 2 + 6 Н 2 О + 2824 к. Дж
 Клеточное (тканевое) дыхание — совокупность биохимических реакций, протекающих в клетках живых организмов, в ходе которых происходит окисление углеводов, липидов и аминокислот до углекислого газа и воды. Высвобожденная энергия запасается в химических связях и может быть использована по мере необходимости.
Клеточное (тканевое) дыхание — совокупность биохимических реакций, протекающих в клетках живых организмов, в ходе которых происходит окисление углеводов, липидов и аминокислот до углекислого газа и воды. Высвобожденная энергия запасается в химических связях и может быть использована по мере необходимости.
 Значение дыхания 1. 2. 3. 4. Энергетическое. Конструкционное. Образование метаболической воды. Разрушение токсических веществ.
Значение дыхания 1. 2. 3. 4. Энергетическое. Конструкционное. Образование метаболической воды. Разрушение токсических веществ.
 История развития представлений о дыхании Дыхание было обнаружено вместе с фотосинтезом (1771 1779 гг. ). Д. Пристли В опытах Шееле растения не исправляли «испорченный» воздух, но и сами поглощали «огневой воздух» (кислород) и выделяли «связанный воздух» (углекислоту). К. Шелле
История развития представлений о дыхании Дыхание было обнаружено вместе с фотосинтезом (1771 1779 гг. ). Д. Пристли В опытах Шееле растения не исправляли «испорченный» воздух, но и сами поглощали «огневой воздух» (кислород) и выделяли «связанный воздух» (углекислоту). К. Шелле
 Ингенгуз и Сенебье – растения могут выделять и поглощать кислород. «Когда солнце разбудит своими лучами заснувшие растения, оно сделает их способными исправлять воздух для животных; во мраке ночи эта деятельность совсем прекращается; днем совершается с тем большим оживлением, чем светлее день и чем выгоднее расположено растение в отношении солнечных лучей. Затененные растения не исправляют воздух, а, наоборот, выделяют вредный для дыхания животных воздух. К концу дня выработка очищенного воздуха ослабевает и при заходе солнца совершенно прекращается» .
Ингенгуз и Сенебье – растения могут выделять и поглощать кислород. «Когда солнце разбудит своими лучами заснувшие растения, оно сделает их способными исправлять воздух для животных; во мраке ночи эта деятельность совсем прекращается; днем совершается с тем большим оживлением, чем светлее день и чем выгоднее расположено растение в отношении солнечных лучей. Затененные растения не исправляют воздух, а, наоборот, выделяют вредный для дыхания животных воздух. К концу дня выработка очищенного воздуха ослабевает и при заходе солнца совершенно прекращается» .
 Первые точные исследования процесса дыхания у растений принадлежат Соссюру (1804): Свежие листья помещал на ночь в сосуд, наполненный воздухом. При этом кислород воздуха поглощался и выделялся углекислый газ. Универсальность дыхания дыхание наблюдается и в клетках стеблей древесных растений, цветков, корней, плодов. Обнаружил, что при дыхании потеря в весе растения равна весу выделенного углерода. Молодые, растущие части растения дышат интенсивнее и потребляют кислорода больше, чем части растения, прекратившие рост.
Первые точные исследования процесса дыхания у растений принадлежат Соссюру (1804): Свежие листья помещал на ночь в сосуд, наполненный воздухом. При этом кислород воздуха поглощался и выделялся углекислый газ. Универсальность дыхания дыхание наблюдается и в клетках стеблей древесных растений, цветков, корней, плодов. Обнаружил, что при дыхании потеря в весе растения равна весу выделенного углерода. Молодые, растущие части растения дышат интенсивнее и потребляют кислорода больше, чем части растения, прекратившие рост.
 Лавуазье Дыхание организмов отождествлялось с медленным горением, причем его сущностью считалось прямое окисление углеводов и жиров организма кислородом вдыхаемого воздуха.
Лавуазье Дыхание организмов отождествлялось с медленным горением, причем его сущностью считалось прямое окисление углеводов и жиров организма кислородом вдыхаемого воздуха.
 Луи Пастер (1822– 1895), в 1872 г. обратил внимание ботаников на сходство дыхания со спиртовым брожением. Пастер предположил, что некоторые начальные этапы дыхательного процесса у высших растений и животных сходны с процессом анаэробного дыхания у микроорганизмов. Пфеффер (1878) разбил дыхание на два этапа: 1) С 6 Н 12 О 6 = 2 С 2 Н 5 ОН + 2 СО 2, 2) 2 С 2 Н 5 ОН + 6 О 2 = 4 СО 2 + 6 Н 2 О. Первая стадия соответствовала бескислородному дыханию и представляла собой распад сахара на спирт и углекислоту. Вторая стадия, требующая кислорода, состояла в окислении спирта до углекислоты и воды.
Луи Пастер (1822– 1895), в 1872 г. обратил внимание ботаников на сходство дыхания со спиртовым брожением. Пастер предположил, что некоторые начальные этапы дыхательного процесса у высших растений и животных сходны с процессом анаэробного дыхания у микроорганизмов. Пфеффер (1878) разбил дыхание на два этапа: 1) С 6 Н 12 О 6 = 2 С 2 Н 5 ОН + 2 СО 2, 2) 2 С 2 Н 5 ОН + 6 О 2 = 4 СО 2 + 6 Н 2 О. Первая стадия соответствовала бескислородному дыханию и представляла собой распад сахара на спирт и углекислоту. Вторая стадия, требующая кислорода, состояла в окислении спирта до углекислоты и воды.
 Костычев Сергей Павлович (1877 — 1931) Изучал процесс химизма дыхания и брожения, вскрыл сущность генетической связи между ними. Показал, что спиртовое брожение не является первой фазой дыхания.
Костычев Сергей Павлович (1877 — 1931) Изучал процесс химизма дыхания и брожения, вскрыл сущность генетической связи между ними. Показал, что спиртовое брожение не является первой фазой дыхания.
 Бах Алексей Николаевич (1857 1946) сформулировал перекисную теорию медленного окисления; показал, что в основе дыхания лежит ряд ферментных окислительных и окислительно восстановительных реакций, последовательно сменяющих друга в длинной цепи химических превращений.
Бах Алексей Николаевич (1857 1946) сформулировал перекисную теорию медленного окисления; показал, что в основе дыхания лежит ряд ферментных окислительных и окислительно восстановительных реакций, последовательно сменяющих друга в длинной цепи химических превращений.
 Палладин Владимир Иванович (1859– 1922) Дыхание – окислительно восстановительный процесс, состоящий из двух этапов: анаэробного и аэробного. На первом, анаэробном, этапе происходит окисление органических субстратов за счет отнятия водорода с участием воды. На втором, аэробном, этапе «дыхательный хромоген» окисляется оксидазами и пероксидазами, активирующими кислород. Все положения теории В. И. Палладина в дальнейшем были полностью подтверждены и на растительных, и на животных объектах.
Палладин Владимир Иванович (1859– 1922) Дыхание – окислительно восстановительный процесс, состоящий из двух этапов: анаэробного и аэробного. На первом, анаэробном, этапе происходит окисление органических субстратов за счет отнятия водорода с участием воды. На втором, аэробном, этапе «дыхательный хромоген» окисляется оксидазами и пероксидазами, активирующими кислород. Все положения теории В. И. Палладина в дальнейшем были полностью подтверждены и на растительных, и на животных объектах.
 1 этап - анаэробный С 6 Н 12 О 6 + 6 Н 2 О + 12 R→ 6 СО 2 + 12 RН 2 Ферменты дегидразы 2 этап - аэробный 12 RН 2 + 6 О 2 → 12 R + 12 Н 2 О Ферменты – оксидазы и пероксидазы Общее уравнение: С 6 Н 12 О 6 + 6 О 2 → 6 СО 2 + 6 Н 2 О R – дыхательный пигмент (окрашенный) RН 2 – дыхательный хромоген (бесцветный)
1 этап - анаэробный С 6 Н 12 О 6 + 6 Н 2 О + 12 R→ 6 СО 2 + 12 RН 2 Ферменты дегидразы 2 этап - аэробный 12 RН 2 + 6 О 2 → 12 R + 12 Н 2 О Ферменты – оксидазы и пероксидазы Общее уравнение: С 6 Н 12 О 6 + 6 О 2 → 6 СО 2 + 6 Н 2 О R – дыхательный пигмент (окрашенный) RН 2 – дыхательный хромоген (бесцветный)
 Ферменты дыхания Способы окисления: непосредственная отдача электронов (Fe 2+ — Fe 3+); отнятие водорода; присоединение кислорода; образование промежуточного гидратированного соединения с последующей отдачей двух электронов и протонов.
Ферменты дыхания Способы окисления: непосредственная отдача электронов (Fe 2+ — Fe 3+); отнятие водорода; присоединение кислорода; образование промежуточного гидратированного соединения с последующей отдачей двух электронов и протонов.
 Классификация оксидоредуктаз: • анаэробные дегидрогеназы, ОВП которых близок таковому органических веществ, способны передавать электроны только промежуточным акцепторам; • аэробные дегидрогеназы, обладающие более высоким ОВП, могут передавать электроны не только органическим акцепторам, но и кислороду; • оксидазы, ОВП которых незначительно отличается от потенциала кислорода, передают электроны только кислороду.
Классификация оксидоредуктаз: • анаэробные дегидрогеназы, ОВП которых близок таковому органических веществ, способны передавать электроны только промежуточным акцепторам; • аэробные дегидрогеназы, обладающие более высоким ОВП, могут передавать электроны не только органическим акцепторам, но и кислороду; • оксидазы, ОВП которых незначительно отличается от потенциала кислорода, передают электроны только кислороду.
 Анаэробные дегидрогеназы Двухкомпонентные ферменты, состоящие из белковой части и кофермента, которым может быть НАД+ или НАДФ+
Анаэробные дегидрогеназы Двухкомпонентные ферменты, состоящие из белковой части и кофермента, которым может быть НАД+ или НАДФ+
 Аэробные дегидрогеназы Двухкомпонентные ферменты, состоящие из белка и прочно связанной с ними простетической группы — рибофлавина (витамина Вз). Различают два активных компонента простетической группы: флавинмононуклеотид (ФМН) и флавинадениндинуклеотид (ФАД). • ФМН содержит гетероциклическое азотистое основание — диметилизоаллоксазин, спирт рибит и фосфат: • В ФАД содержит ФМН и аденозинмонофосфат.
Аэробные дегидрогеназы Двухкомпонентные ферменты, состоящие из белка и прочно связанной с ними простетической группы — рибофлавина (витамина Вз). Различают два активных компонента простетической группы: флавинмононуклеотид (ФМН) и флавинадениндинуклеотид (ФАД). • ФМН содержит гетероциклическое азотистое основание — диметилизоаллоксазин, спирт рибит и фосфат: • В ФАД содержит ФМН и аденозинмонофосфат.
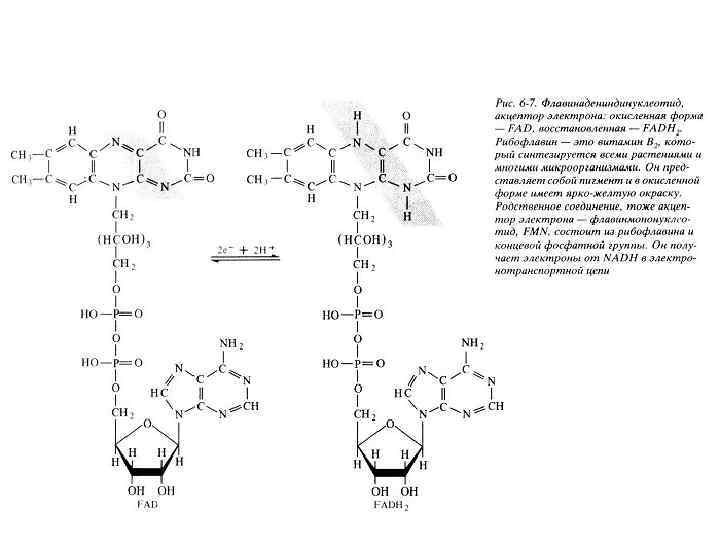
 Оксидазы Передают электроны от окисляемого субстрата только на кислород. При этом образуется или вода, или пероксид водорода, или супероксидный анион кислорода. В первом случае на кислород переносятся четыре электрона, во втором два, в третьем один. К оксидазам I группы относят цитохромоксидазу, полифенолоксидазу, II флавопротеиновые оксидазы (оксидазы аминокислот), III ферменты типа ксантиноксидазы.
Оксидазы Передают электроны от окисляемого субстрата только на кислород. При этом образуется или вода, или пероксид водорода, или супероксидный анион кислорода. В первом случае на кислород переносятся четыре электрона, во втором два, в третьем один. К оксидазам I группы относят цитохромоксидазу, полифенолоксидазу, II флавопротеиновые оксидазы (оксидазы аминокислот), III ферменты типа ксантиноксидазы.
 К цитохромной системе относятся: железосодержащие ферменты; переносчики — цитохромы; цитохромоксидаза. Все компоненты цитохромной системы содержат железо порфириновую простетическую группу:
К цитохромной системе относятся: железосодержащие ферменты; переносчики — цитохромы; цитохромоксидаза. Все компоненты цитохромной системы содержат железо порфириновую простетическую группу:

 Строение митохондрий
Строение митохондрий
 Характеристика структуры митохондрий Количество митохондрий в клетке зависит от размера и типа клетки. Локализуются рядом с местом снабжения субстратами, или где необходима энергия АТФ, клеточными мембранами. Митохондрии являются двумембранными органоидами, содержат два компартмента: межмембранное пространство и матрикс. Наружная мембрана митохондрий гладкая и содержит белки, которые образуют неспецифические поры. Внутренняя мембрана образует очень большое количество впячиваний крист. В мембране крист локализованы все ферменты ЭТЦ и окислительного фосфорилирования. На кристах имеются АТФ азы. Внутренняя мембрана митохондрий не проницаема для большинства веществ. В матриксе митохондрий находятся плотно упакованные молекулы белка и небольшое количество ДНК.
Характеристика структуры митохондрий Количество митохондрий в клетке зависит от размера и типа клетки. Локализуются рядом с местом снабжения субстратами, или где необходима энергия АТФ, клеточными мембранами. Митохондрии являются двумембранными органоидами, содержат два компартмента: межмембранное пространство и матрикс. Наружная мембрана митохондрий гладкая и содержит белки, которые образуют неспецифические поры. Внутренняя мембрана образует очень большое количество впячиваний крист. В мембране крист локализованы все ферменты ЭТЦ и окислительного фосфорилирования. На кристах имеются АТФ азы. Внутренняя мембрана митохондрий не проницаема для большинства веществ. В матриксе митохондрий находятся плотно упакованные молекулы белка и небольшое количество ДНК.
 Функции Метаболическая: • расщепление жирных кислот путем β окисления и частично цикл мочевины; • поставляют клетке продукты промежуточного метаболизма; Окислительное фосфорилирование; Поддержание концентрации Са 2+ в цитоплазме на постоянном низком уровне.
Функции Метаболическая: • расщепление жирных кислот путем β окисления и частично цикл мочевины; • поставляют клетке продукты промежуточного метаболизма; Окислительное фосфорилирование; Поддержание концентрации Са 2+ в цитоплазме на постоянном низком уровне.
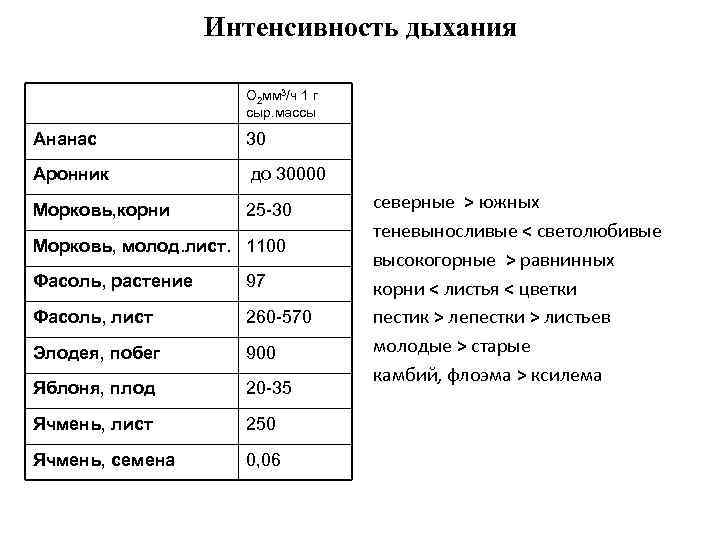 Интенсивность дыхания О 2 мм 3/ч 1 г сыр. массы Ананас 30 Аронник до 30000 Морковь, корни 25 -30 Морковь, молод. лист. 1100 Фасоль, растение 97 Фасоль, лист 260 -570 Элодея, побег 900 Яблоня, плод 20 -35 Ячмень, лист 250 Ячмень, семена 0, 06 северные > южных теневыносливые < светолюбивые высокогорные > равнинных корни < листья < цветки пестик > лепестки > листьев молодые > старые камбий, флоэма > ксилема
Интенсивность дыхания О 2 мм 3/ч 1 г сыр. массы Ананас 30 Аронник до 30000 Морковь, корни 25 -30 Морковь, молод. лист. 1100 Фасоль, растение 97 Фасоль, лист 260 -570 Элодея, побег 900 Яблоня, плод 20 -35 Ячмень, лист 250 Ячмень, семена 0, 06 северные > южных теневыносливые < светолюбивые высокогорные > равнинных корни < листья < цветки пестик > лепестки > листьев молодые > старые камбий, флоэма > ксилема
 Дыхательный коэффициент ДК = V(СО 2 )/ V(О 2) отношение объёма выделяемого из организма углекислого газа к объёму поглощаемого за то же время кислорода Факторы влияющие на ДК: 1. Степень окисления С в субстрате 2. Концентрация кислорода 3. Особенности тканей 4. Целостность мембран
Дыхательный коэффициент ДК = V(СО 2 )/ V(О 2) отношение объёма выделяемого из организма углекислого газа к объёму поглощаемого за то же время кислорода Факторы влияющие на ДК: 1. Степень окисления С в субстрате 2. Концентрация кислорода 3. Особенности тканей 4. Целостность мембран
 Пути дыхательного обмена
Пути дыхательного обмена
 Существуют две основные системы и два основных пути окисления углеводов: 1) гликолиз + цикл Кребса (гликолитический); 2) пентозофосфатный (апотомический). Относительная роль этих путей дыхания может меняться в зависимости от типа растений, возраста, фазы развития, а также в зависимости от факторов среды.
Существуют две основные системы и два основных пути окисления углеводов: 1) гликолиз + цикл Кребса (гликолитический); 2) пентозофосфатный (апотомический). Относительная роль этих путей дыхания может меняться в зависимости от типа растений, возраста, фазы развития, а также в зависимости от факторов среды.
 Гликолитический путь Первая фаза — анаэробная (гликолиз), вторая фаза — аэробная. Эти фазы локализованы в различных компартментах клетки. Анаэробная фаза гликолиз — в цитоплазме, аэробная фаза — в мито хондриях.
Гликолитический путь Первая фаза — анаэробная (гликолиз), вторая фаза — аэробная. Эти фазы локализованы в различных компартментах клетки. Анаэробная фаза гликолиз — в цитоплазме, аэробная фаза — в мито хондриях.
 Анаэробная стадия дыхания Гликолиз (фосфотриозный путь, или шунт Эмбдена — Мейергофа) Глико лиз — ферментативный процесс последовательного расщепления глюкозы в клетках, сопровождающийся синтезом АТФ. Гликолиз осуществляется во всех живых клетках организмов. Полное уравнение: С 6. 12 О 6 + 2 НАД+ + 2 АДФ + 2 Фн = Н 2 НАД*Н + 2 ПВК + 2 АТФ + 2 Н 2 О + 2 Н+. При отсутствии или недостатке в клетке кислорода ПВК подвергается восстановлению до молочной кислоты: Глюкоза + 2 АДФ + 2 Фн = 2 лактат + 2 АТФ + 2 Н 2 О
Анаэробная стадия дыхания Гликолиз (фосфотриозный путь, или шунт Эмбдена — Мейергофа) Глико лиз — ферментативный процесс последовательного расщепления глюкозы в клетках, сопровождающийся синтезом АТФ. Гликолиз осуществляется во всех живых клетках организмов. Полное уравнение: С 6. 12 О 6 + 2 НАД+ + 2 АДФ + 2 Фн = Н 2 НАД*Н + 2 ПВК + 2 АТФ + 2 Н 2 О + 2 Н+. При отсутствии или недостатке в клетке кислорода ПВК подвергается восстановлению до молочной кислоты: Глюкоза + 2 АДФ + 2 Фн = 2 лактат + 2 АТФ + 2 Н 2 О
 Процесс гликолиза условно можно разделить на два этапа: 1 этап протекает с расходом энергии 2 АТФ, заключается в расщеплении глюкозы на 2 молекулы 3 ФГА. 2 этап происходит НАД зависимое окисление 3 ФГА, сопровождающееся синтезом АТФ.
Процесс гликолиза условно можно разделить на два этапа: 1 этап протекает с расходом энергии 2 АТФ, заключается в расщеплении глюкозы на 2 молекулы 3 ФГА. 2 этап происходит НАД зависимое окисление 3 ФГА, сопровождающееся синтезом АТФ.


 Характеристика гликолиза • большинство реакций обратимо, за исключением трех (реакций 1, 3, 10); • все метаболиты находятся в фосфорилированной форме; • источником фосфатной группы в реакциях фосфорилирования являются АТР или неорганический фосфат; • регенерация NAD происходит при аэробном гликолизе посредством дыхательной цепи; при анаэробном независимо от дыхательной цепи; • образование АТР при гликолизе может идти двумя путями: субстратным фосфорилированием, когда для фосфорилирования ADP используется энергия макроэргической связи субстрата (реакции 7, 9), путем окислительного фосфорилирования ADP, сопряженного с дыхательной цепью (реакция 6);
Характеристика гликолиза • большинство реакций обратимо, за исключением трех (реакций 1, 3, 10); • все метаболиты находятся в фосфорилированной форме; • источником фосфатной группы в реакциях фосфорилирования являются АТР или неорганический фосфат; • регенерация NAD происходит при аэробном гликолизе посредством дыхательной цепи; при анаэробном независимо от дыхательной цепи; • образование АТР при гликолизе может идти двумя путями: субстратным фосфорилированием, когда для фосфорилирования ADP используется энергия макроэргической связи субстрата (реакции 7, 9), путем окислительного фосфорилирования ADP, сопряженного с дыхательной цепью (реакция 6);
 Регуляция гликолиза Регуляция осуществляется через несколько ключевых этапов. Реакции, катализируемые гексокиназой (1), пируваткиназой (10) и фосфофруктокиназой (3) являются практически необратимыми. Регуляция гексокиназы Гексокиназа ингибируется продуктом реакции — глюкозо 6 фосфатом, который аллостерически связывается с ферментом.
Регуляция гликолиза Регуляция осуществляется через несколько ключевых этапов. Реакции, катализируемые гексокиназой (1), пируваткиназой (10) и фосфофруктокиназой (3) являются практически необратимыми. Регуляция гексокиназы Гексокиназа ингибируется продуктом реакции — глюкозо 6 фосфатом, который аллостерически связывается с ферментом.
 Регуляция фосфофруктокиназы Интенсивность протекания фосфофруктокиназной реакции сказывается на всей пропускной способности гликолиза. Аллостерический ингибитор ФФК – АТФ; активатор фруктозо 2, 6 бифосфат. Пируваткиназа Активатор фруктозо 1, 6 дифосфат, ингибиторы АТФ, аланин, ацетил. Ко. А. Енолаза Активируется Mg 2+ или Мn 2+, ингибируется фторидом.
Регуляция фосфофруктокиназы Интенсивность протекания фосфофруктокиназной реакции сказывается на всей пропускной способности гликолиза. Аллостерический ингибитор ФФК – АТФ; активатор фруктозо 2, 6 бифосфат. Пируваткиназа Активатор фруктозо 1, 6 дифосфат, ингибиторы АТФ, аланин, ацетил. Ко. А. Енолаза Активируется Mg 2+ или Мn 2+, ингибируется фторидом.
 Значение окисление гексоз для генерации АТФ, восстанови телей, пирувата; синтез гексоз из низкомолекулярных со единений в процессе энергозависимого глюконеогенеза.
Значение окисление гексоз для генерации АТФ, восстанови телей, пирувата; синтез гексоз из низкомолекулярных со единений в процессе энергозависимого глюконеогенеза.
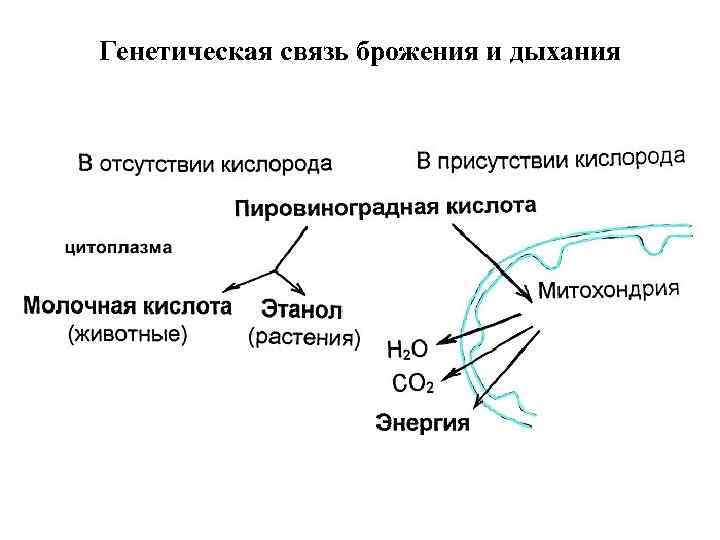 Генетическая связь брожения и дыхания
Генетическая связь брожения и дыхания
 Аэробная стадия дыхания Основные стадии: 1) окислительное декарбоксилирование пировиноградной кислоты; 2) цикл трикарбоновых кислот (цикл Кребса); 3) электронтранспортная цепь (ЭТЦ).
Аэробная стадия дыхания Основные стадии: 1) окислительное декарбоксилирование пировиноградной кислоты; 2) цикл трикарбоновых кислот (цикл Кребса); 3) электронтранспортная цепь (ЭТЦ).
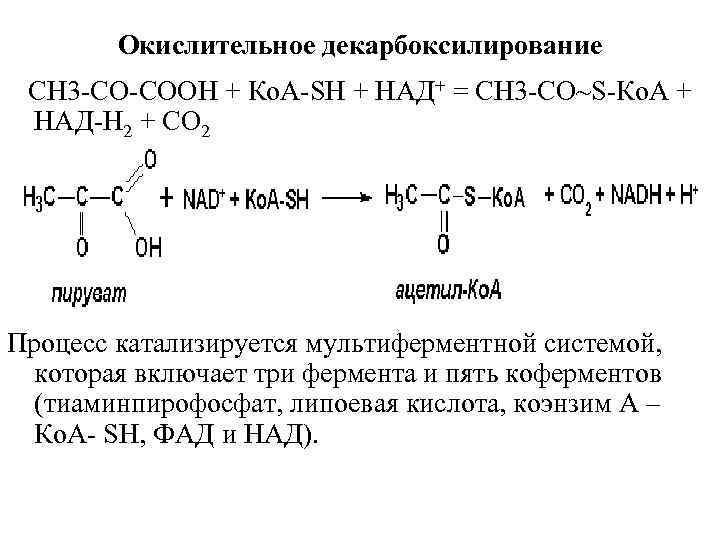 Окислительное декарбоксилирование CH 3 CO COOH + Ко. A SH + НАД+ = CH 3 CO~S Ко. A + НАД H 2 + CO 2 Процесс катализируется мультиферментной системой, которая включает три фермента и пять коферментов (тиаминпирофосфат, липоевая кислота, коэнзим А – Ко. А SH, ФАД и НАД).
Окислительное декарбоксилирование CH 3 CO COOH + Ко. A SH + НАД+ = CH 3 CO~S Ко. A + НАД H 2 + CO 2 Процесс катализируется мультиферментной системой, которая включает три фермента и пять коферментов (тиаминпирофосфат, липоевая кислота, коэнзим А – Ко. А SH, ФАД и НАД).
 Ко. А
Ко. А
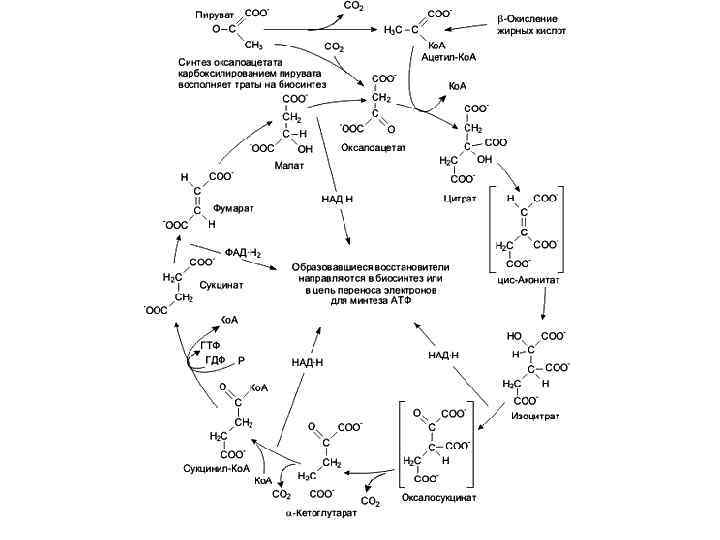
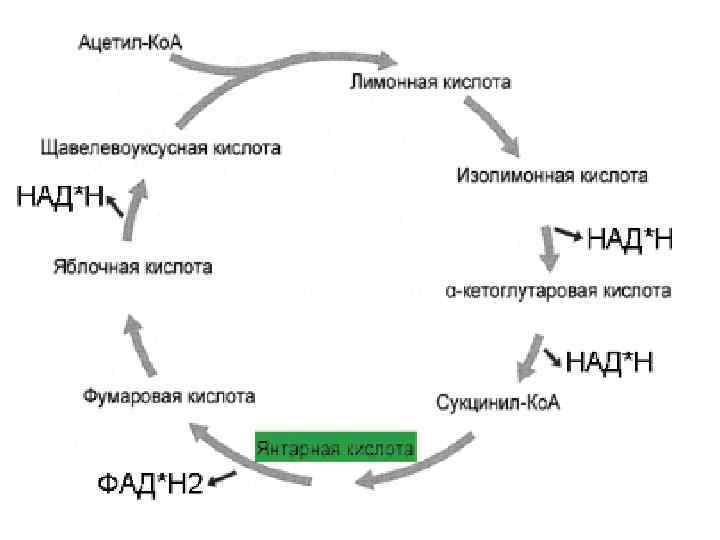
 Общее уравнение одного оборота цикла Кребса: Ацетил Ко. А → 2 CO 2 + Ко. А + 8 е
Общее уравнение одного оборота цикла Кребса: Ацетил Ко. А → 2 CO 2 + Ко. А + 8 е
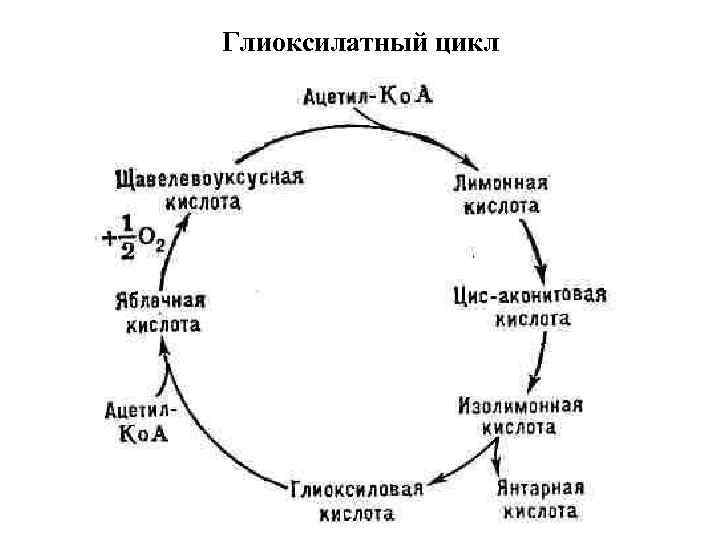 Глиоксилатный цикл
Глиоксилатный цикл

 • Осуществляется в прорастающих семенах масличных растений, а также у некоторых микроорганизмов (бактерий и плесневых грибов). • Впервые описан в 1957 г. у бактерий и плесневых грибов Г. Л. Корнбергом и Г. А. Кребсом. • Г. ц. локализован в глиоксисомах. • При прорастании семян масличных растений через Г. ц. осуществляется превращение жиров в углеводы. • Наличие Г. ц. в животных тканях остаётся спорным.
• Осуществляется в прорастающих семенах масличных растений, а также у некоторых микроорганизмов (бактерий и плесневых грибов). • Впервые описан в 1957 г. у бактерий и плесневых грибов Г. Л. Корнбергом и Г. А. Кребсом. • Г. ц. локализован в глиоксисомах. • При прорастании семян масличных растений через Г. ц. осуществляется превращение жиров в углеводы. • Наличие Г. ц. в животных тканях остаётся спорным.
 Пентозофосфатный путь (пентозный путь, фосфоглюконатный путь, гексозомонофосфатный шунт) • совокупность обратимых ферментативных реакций, в результате которых происходит окисление глюкозы до CO 2 с образованием восстановленного НАДФН и H + , а также синтез фосфорилированных сахаров, содержащих от 3 до 7 атомов С. 6 Глюкозо 6 фосфат + 12 НАДФ = 5 Глюкозо 6 фосфат+ 6 CO 2 + 12 НАДФН +12 H+ + Н 2 РО 4 Локализован в цитоплазме.
Пентозофосфатный путь (пентозный путь, фосфоглюконатный путь, гексозомонофосфатный шунт) • совокупность обратимых ферментативных реакций, в результате которых происходит окисление глюкозы до CO 2 с образованием восстановленного НАДФН и H + , а также синтез фосфорилированных сахаров, содержащих от 3 до 7 атомов С. 6 Глюкозо 6 фосфат + 12 НАДФ = 5 Глюкозо 6 фосфат+ 6 CO 2 + 12 НАДФН +12 H+ + Н 2 РО 4 Локализован в цитоплазме.
 Значение пентозофосфатного пути • Энергетическое: при окислении одной молекулы глюкозы выделяется 37 молекул АТФ. • Образуется восстановленный НАДФ, который может быть использован на различные синтетические процессы, в том числе и в темновых реакциях фотосинтеза. • Образование пентоз. Пентозы входят в состав нуклеиновых кислот. • Может в отсутствие света осуществляться и в хлоропластах. На протяжении онтогенеза растений и в зависимости от условий происходит смена дыхательных путей.
Значение пентозофосфатного пути • Энергетическое: при окислении одной молекулы глюкозы выделяется 37 молекул АТФ. • Образуется восстановленный НАДФ, который может быть использован на различные синтетические процессы, в том числе и в темновых реакциях фотосинтеза. • Образование пентоз. Пентозы входят в состав нуклеиновых кислот. • Может в отсутствие света осуществляться и в хлоропластах. На протяжении онтогенеза растений и в зависимости от условий происходит смена дыхательных путей.
 Брожение
Брожение
 Виды брожения • Спиртовое брожение: ПВК → 2 этанол + 2 CO 2 • Лимоннокислое брожение: ПВК → лимонная кислота + 2 H 2 O • Молочнокислое брожение: ПВК + НАД∙НH+ → молочная кислота + НАД+ • Маслянокислое брожение: ПВК →масляная кислота + 2 CO 2+2 H 2 O
Виды брожения • Спиртовое брожение: ПВК → 2 этанол + 2 CO 2 • Лимоннокислое брожение: ПВК → лимонная кислота + 2 H 2 O • Молочнокислое брожение: ПВК + НАД∙НH+ → молочная кислота + НАД+ • Маслянокислое брожение: ПВК →масляная кислота + 2 CO 2+2 H 2 O
 ЭТЦ Дыхательная электронтранспортная цепь— система структурно и функционально связанных трансмембранных белков и переносчиков электронов. ЭТЦ позволяет запасти энергию, выделяющуюся в ходе окисления НАД∙Н и ФАДН 2 молекулярным кислородом или иными веществами в форме трансмембранного протонного потенциала за счёт последовательного переноса электрона по цепи, сопряжённого с перекачкой протонов через мембрану. Переносчики расположены по своему окислительно восстановительному потенциалу, транспорт электрона на всём протяжении цепи протекает самопроизвольно.
ЭТЦ Дыхательная электронтранспортная цепь— система структурно и функционально связанных трансмембранных белков и переносчиков электронов. ЭТЦ позволяет запасти энергию, выделяющуюся в ходе окисления НАД∙Н и ФАДН 2 молекулярным кислородом или иными веществами в форме трансмембранного протонного потенциала за счёт последовательного переноса электрона по цепи, сопряжённого с перекачкой протонов через мембрану. Переносчики расположены по своему окислительно восстановительному потенциалу, транспорт электрона на всём протяжении цепи протекает самопроизвольно.
 Компоненты дыхательной цепи • Комплекс I (НАДН дегидрогеназа) окисляет НАД∙Н, отбирая у него два электрона и перенося их на растворимый в липидах убихинон, который внутри мембраны диффундирует к комплексу III. Вместе с этим, комплекс I перекачивает 4 протона из матрикса в межмембранное пространство митохондрии. • Комплекс II (Сукцинат дегидрогеназа) не перекачивает протоны, но обеспечивает вход в цепь дополнительных электронов за счёт окисления сукцината.
Компоненты дыхательной цепи • Комплекс I (НАДН дегидрогеназа) окисляет НАД∙Н, отбирая у него два электрона и перенося их на растворимый в липидах убихинон, который внутри мембраны диффундирует к комплексу III. Вместе с этим, комплекс I перекачивает 4 протона из матрикса в межмембранное пространство митохондрии. • Комплекс II (Сукцинат дегидрогеназа) не перекачивает протоны, но обеспечивает вход в цепь дополнительных электронов за счёт окисления сукцината.
 • Комплекс III (Цитохром bc 1 комплекс) переносит электроны с убихинола на два водорастворимых цитохрома с, расположенных на внутренней мембране митохондрии. Убихинол передаёт 2 электрона, а цитохромы за один цикл переносят по одному электрону. При этом туда также переходят 2 протона убихинола и 2 перекачиваются комплексом. • Комплекс IV (Цитохром c оксидаза) катализирует перенос 4 электронов с 4 молекул цитохрома на O 2 и перекачивает при этом 4 протона в межмембранное пространство. Комплекс состоит из цитохромов a и a 3, которые, помимо гема, содержат ионы меди.
• Комплекс III (Цитохром bc 1 комплекс) переносит электроны с убихинола на два водорастворимых цитохрома с, расположенных на внутренней мембране митохондрии. Убихинол передаёт 2 электрона, а цитохромы за один цикл переносят по одному электрону. При этом туда также переходят 2 протона убихинола и 2 перекачиваются комплексом. • Комплекс IV (Цитохром c оксидаза) катализирует перенос 4 электронов с 4 молекул цитохрома на O 2 и перекачивает при этом 4 протона в межмембранное пространство. Комплекс состоит из цитохромов a и a 3, которые, помимо гема, содержат ионы меди.


 Ингибиторы ЭТЦ • Ингибиторы окислительной цепи – блокируют перенос электронов на определенном участке дыхательной цепи (цианид, антимицин, азид). • Разобщители – подавляют фосфорилирование АДФ, не влияя на перенос электронов, и стимулируют рассеивание энергии в виде тепла (2, 4 динитрофенол). • Ингибиторы переноса энергии препятствуют превращению энергии окисления в АТФ, ингибируя перенос энергии (олигомицин, рутамицин).
Ингибиторы ЭТЦ • Ингибиторы окислительной цепи – блокируют перенос электронов на определенном участке дыхательной цепи (цианид, антимицин, азид). • Разобщители – подавляют фосфорилирование АДФ, не влияя на перенос электронов, и стимулируют рассеивание энергии в виде тепла (2, 4 динитрофенол). • Ингибиторы переноса энергии препятствуют превращению энергии окисления в АТФ, ингибируя перенос энергии (олигомицин, рутамицин).
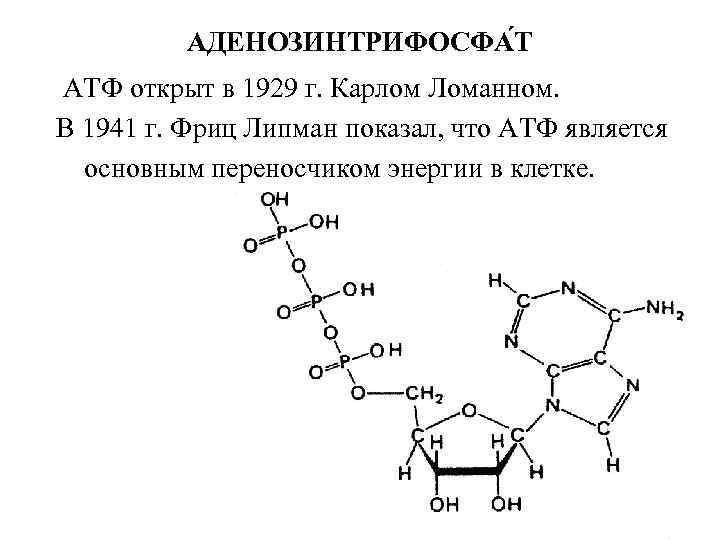 АДЕНОЗИНТРИФОСФА Т АТФ открыт в 1929 г. Карлом Ломанном. В 1941 г. Фриц Липман показал, что АТФ является основным переносчиком энергии в клетке.
АДЕНОЗИНТРИФОСФА Т АТФ открыт в 1929 г. Карлом Ломанном. В 1941 г. Фриц Липман показал, что АТФ является основным переносчиком энергии в клетке.
 Роль в организме • • Обеспечение энергией биохимических реакций. Исходный продукт при синтезе нуклеиновых кислот. Аллостерический эффектор ряда ферментов. Непосредственный предшественник синтеза ц. АМФ — вторичного посредника передачи в клетку гормонального сигнала.
Роль в организме • • Обеспечение энергией биохимических реакций. Исходный продукт при синтезе нуклеиновых кислот. Аллостерический эффектор ряда ферментов. Непосредственный предшественник синтеза ц. АМФ — вторичного посредника передачи в клетку гормонального сигнала.
 Пути синтеза АТФ • Субстратное фосфорилирование Перенос неорганического фосфата на АДФ. • Окислительное фосфорилирование Синтез молекул АТФ из АДФ и фосфата за счёт энергии окисления молекул органических веществ. Открыт в 1930 г. Энгельгардтом В. А. В 1939 Белицер В. А. и Цыбакова Е. Т. показали, что ОФ сопряжено с переносом электронов по цепи дыхательных ферментов, встроенных во внутреннюю мембрану митохондрий. Эффективность ОФ оценивают с помощью отношения количества фосфата, связанного при фосфорилировании АДФ, отнесённого к поглощённому О 2.
Пути синтеза АТФ • Субстратное фосфорилирование Перенос неорганического фосфата на АДФ. • Окислительное фосфорилирование Синтез молекул АТФ из АДФ и фосфата за счёт энергии окисления молекул органических веществ. Открыт в 1930 г. Энгельгардтом В. А. В 1939 Белицер В. А. и Цыбакова Е. Т. показали, что ОФ сопряжено с переносом электронов по цепи дыхательных ферментов, встроенных во внутреннюю мембрану митохондрий. Эффективность ОФ оценивают с помощью отношения количества фосфата, связанного при фосфорилировании АДФ, отнесённого к поглощённому О 2.
 Гипотеза П. Митчелла требует соблюдения ряда условий: • Внутренняя мембрана митохондрий должна быть непроницаема для протонов, направляющихся снаружи внутрь. • В результате активности дыхательной цепи ионы водорода поступают в нее из матрикса, а освобождаются в межмембранное пространство. • В результате они накапливаются между мембранами, вследствие чего между возникает градиент р. Н. • Поддержание такого градиента требует затраты энергии. Эту энергию поставляет перенос электронов по ЭТЦ.
Гипотеза П. Митчелла требует соблюдения ряда условий: • Внутренняя мембрана митохондрий должна быть непроницаема для протонов, направляющихся снаружи внутрь. • В результате активности дыхательной цепи ионы водорода поступают в нее из матрикса, а освобождаются в межмембранное пространство. • В результате они накапливаются между мембранами, вследствие чего между возникает градиент р. Н. • Поддержание такого градиента требует затраты энергии. Эту энергию поставляет перенос электронов по ЭТЦ.
 Структура и номенклатура АТФ синтазный комплекс напоминает плодовое тело гриба, у которого компонент F 1 — это шляпка, ножка — это γ субъединица компонента F 1, а «корни» гриба — компонент FO, углубленный в мембрану. • Субъединицы фермента : α, β, γ, δ, ε; a, b, c, d, e, f, g, h, F 6, A 6 L OSCP — белок, чувствительный к олигомицину
Структура и номенклатура АТФ синтазный комплекс напоминает плодовое тело гриба, у которого компонент F 1 — это шляпка, ножка — это γ субъединица компонента F 1, а «корни» гриба — компонент FO, углубленный в мембрану. • Субъединицы фермента : α, β, γ, δ, ε; a, b, c, d, e, f, g, h, F 6, A 6 L OSCP — белок, чувствительный к олигомицину

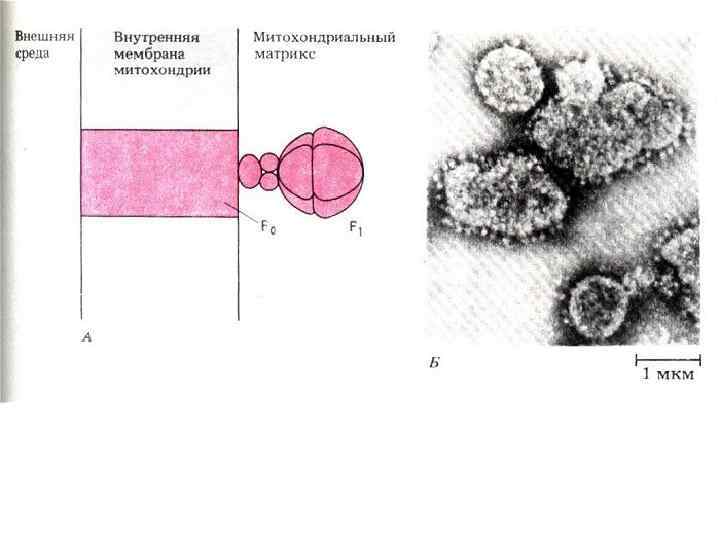

 Принципы функционирования АТФ-синтетазы • Энергия должна быть в форме ΔµH+. • Энергия требуется для переноса связанного АТФ из активного центра фактора F 1 в воду или переноса АДФ и фосфата из воды в активный центр. • АДФ и фосфор, связанные с фактором F 1 могут образовывать АТФ без притока энергии извне. • В переносе протонов через АТФ синтетазный комплекс участвует фактор F 0. • АТФ синтетаза может работать и как АТФ аза, используя АТФ для поддержания ΔµH+
Принципы функционирования АТФ-синтетазы • Энергия должна быть в форме ΔµH+. • Энергия требуется для переноса связанного АТФ из активного центра фактора F 1 в воду или переноса АДФ и фосфата из воды в активный центр. • АДФ и фосфор, связанные с фактором F 1 могут образовывать АТФ без притока энергии извне. • В переносе протонов через АТФ синтетазный комплекс участвует фактор F 0. • АТФ синтетаза может работать и как АТФ аза, используя АТФ для поддержания ΔµH+


