тема6.ppt
- Количество слайдов: 74
 Дыхание микроорганизмов. Дезинфекция, стерилизация Тема 6
Дыхание микроорганизмов. Дезинфекция, стерилизация Тема 6
 Классификация микроорганизмов по типу дыхания № 1
Классификация микроорганизмов по типу дыхания № 1
 Путем дыхания микроорганизмы добывают энергию. Дыхание- биологический процесс переноса электронов через дыхательную цепь от доноров к акцепторам с образованием АТФ. В зависимости от того, что является конечным акцептором электронов, выделяют аэробное и анаэробное дыхание. При аэробном дыхании конечным акцептором электронов является молекулярный кислород (О 2), при анаэробном- связанный кислород ( -NO 3 , =SO 4, =SO 3).
Путем дыхания микроорганизмы добывают энергию. Дыхание- биологический процесс переноса электронов через дыхательную цепь от доноров к акцепторам с образованием АТФ. В зависимости от того, что является конечным акцептором электронов, выделяют аэробное и анаэробное дыхание. При аэробном дыхании конечным акцептором электронов является молекулярный кислород (О 2), при анаэробном- связанный кислород ( -NO 3 , =SO 4, =SO 3).
 По типу дыхания выделяют четыре группы микроорганизмов. 1. Облигатные (строгие) аэробы. Им необходим молекулярный (атмосферный) кислород для дыхания. 2. Микроаэрофилы нуждаются в уменьшенной концентрации (низком парциальном давлении) свободного кислорода. Для создания этих условий в газовую смесь для культивирования обычно добавляют CO 2, например до 10 - процентной концентрации. 3. Факультативные анаэробы могут потреблять глюкозу и размножаться в аэробных и анаэробных условиях. Среди них имеются микроорганизмы, толерантные к относительно высоким (близких к атмосферным) концентрациям молекулярного кислорода - т. е. аэротолерантные, а также микроорганизмы , которые способны в определенных условиях переключаться с анаэробного на аэробное дыхание. 4. Строгие анаэробы размножаются только в анаэробных условиях т. е. при очень низких концентрациях молекулярного кислорода, который в больших концентрациях для них губителен. Биохимически анаэробное дыхание протекает по типу бродильных процессов, молекулярный кислород при этом не используется.
По типу дыхания выделяют четыре группы микроорганизмов. 1. Облигатные (строгие) аэробы. Им необходим молекулярный (атмосферный) кислород для дыхания. 2. Микроаэрофилы нуждаются в уменьшенной концентрации (низком парциальном давлении) свободного кислорода. Для создания этих условий в газовую смесь для культивирования обычно добавляют CO 2, например до 10 - процентной концентрации. 3. Факультативные анаэробы могут потреблять глюкозу и размножаться в аэробных и анаэробных условиях. Среди них имеются микроорганизмы, толерантные к относительно высоким (близких к атмосферным) концентрациям молекулярного кислорода - т. е. аэротолерантные, а также микроорганизмы , которые способны в определенных условиях переключаться с анаэробного на аэробное дыхание. 4. Строгие анаэробы размножаются только в анаэробных условиях т. е. при очень низких концентрациях молекулярного кислорода, который в больших концентрациях для них губителен. Биохимически анаэробное дыхание протекает по типу бродильных процессов, молекулярный кислород при этом не используется.
 В процессе аэробного дыхания образуются токсические продукты окисления (H 2 O 2 - перекись водорода, -О 2 - свободные кислородные радикалы), от которых защищают специфические ферменты, прежде всего каталаза, пероксидаза, пероксиддисмутаза. У анаэробов эти ферменты отсутствуют, также как и система регуляции окислительно- восстановительного потенциала (r. H 2).
В процессе аэробного дыхания образуются токсические продукты окисления (H 2 O 2 - перекись водорода, -О 2 - свободные кислородные радикалы), от которых защищают специфические ферменты, прежде всего каталаза, пероксидаза, пероксиддисмутаза. У анаэробов эти ферменты отсутствуют, также как и система регуляции окислительно- восстановительного потенциала (r. H 2).
 Классификация микроорганизмов по отношению к кислороду
Классификация микроорганизмов по отношению к кислороду
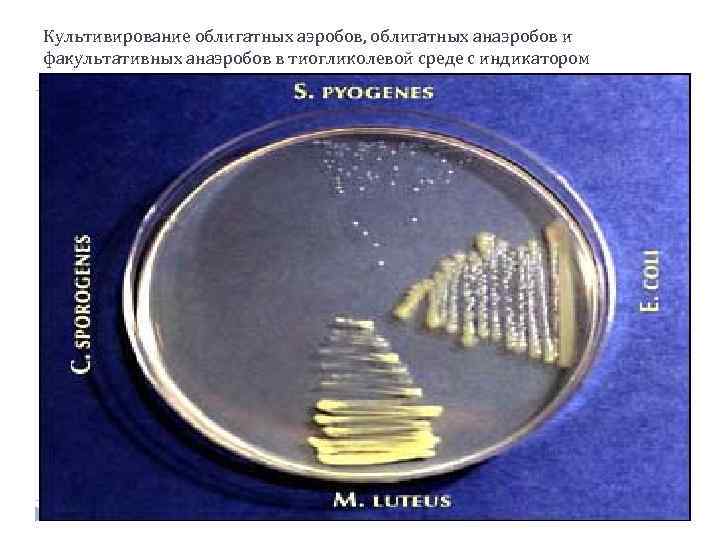 Культивирование облигатных аэробов, облигатных анаэробов и факультативных анаэробов в тиогликолевой среде с индикатором
Культивирование облигатных аэробов, облигатных анаэробов и факультативных анаэробов в тиогликолевой среде с индикатором
 Культивирование облигатных аэробов, облигатных анаэробов и факультативных анаэробов в аэробных условиях
Культивирование облигатных аэробов, облигатных анаэробов и факультативных анаэробов в аэробных условиях
 Культивирование облигатных аэробов, облигатных анаэробов и факультативных анаэробов в микроаэрофильных условиях
Культивирование облигатных аэробов, облигатных анаэробов и факультативных анаэробов в микроаэрофильных условиях
 Культивирование облигатных аэробов, облигатных анаэробов и факультативных анаэробов в анаэробных условиях
Культивирование облигатных аэробов, облигатных анаэробов и факультативных анаэробов в анаэробных условиях
 Дыхательные цепи № 2 Страница 46 пособия «Общая микробиология и иммунология»
Дыхательные цепи № 2 Страница 46 пособия «Общая микробиология и иммунология»
 Особенности питательных сред для анаэробов № 3
Особенности питательных сред для анаэробов № 3
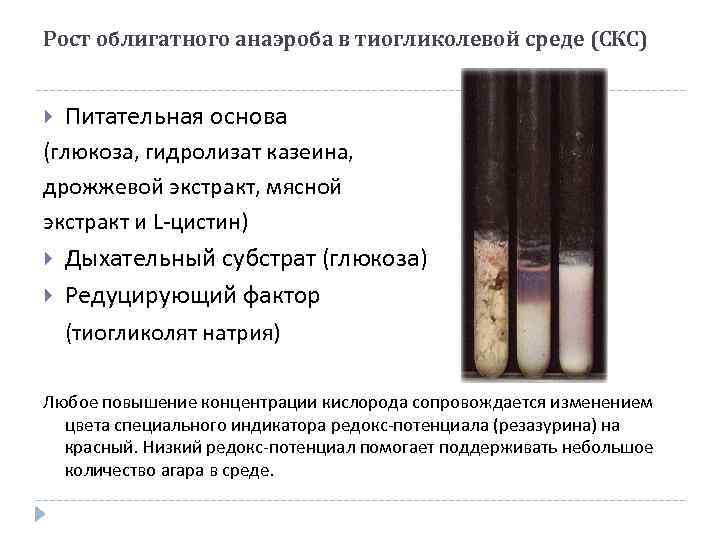 Рост облигатного анаэроба в тиогликолевой среде (СКС) Питательная основа (глюкоза, гидролизат казеина, дрожжевой экстракт, мясной экстракт и L-цистин) Дыхательный субстрат (глюкоза) Редуцирующий фактор (тиогликолят натрия) Любое повышение концентрации кислорода сопровождается изменением цвета специального индикатора редокс-потенциала (резазурина) на красный. Низкий редокс-потенциал помогает поддерживать небольшое количество агара в среде.
Рост облигатного анаэроба в тиогликолевой среде (СКС) Питательная основа (глюкоза, гидролизат казеина, дрожжевой экстракт, мясной экстракт и L-цистин) Дыхательный субстрат (глюкоза) Редуцирующий фактор (тиогликолят натрия) Любое повышение концентрации кислорода сопровождается изменением цвета специального индикатора редокс-потенциала (резазурина) на красный. Низкий редокс-потенциал помогает поддерживать небольшое количество агара в среде.
 Характер роста различных видов клостридий в пробирках с лакмусовым молоком. C. perfringens (слева) створаживает молоко с образованием пронизанного пузырьками газа сгустка казеина. C. tetani (справа) пептонизирует молоко. С. sporogenes (в центре) сначала створаживает молоко, а затем сгустки казеина быстро перевариваются под действием протеолитических ферментов возбудителя. Питательная основа (обезжиренное молоко) Дыхательный субстрат (глюкоза) Редуцирующий фактор (казеин)
Характер роста различных видов клостридий в пробирках с лакмусовым молоком. C. perfringens (слева) створаживает молоко с образованием пронизанного пузырьками газа сгустка казеина. C. tetani (справа) пептонизирует молоко. С. sporogenes (в центре) сначала створаживает молоко, а затем сгустки казеина быстро перевариваются под действием протеолитических ферментов возбудителя. Питательная основа (обезжиренное молоко) Дыхательный субстрат (глюкоза) Редуцирующий фактор (казеин)
 Рост различных видов клостридий в пробирках с сахарным агаром. C. perfringens (слева) разлагает глюкозу с большим количеством газа, что приводит к разрыву столбика сахарного агара в нескольких местах. C. sporogenes (справа) также разлагает глюкозу с образованием газа, однако количество газообразных продуктов относительно невелико. C. tetani (в центре) не ферментирует сахара, поэтому столбик сахарного агара не изменен. Питательная основа Дыхательный субстрат (глюкоза) Редуцирующий фактор (циклосерин)
Рост различных видов клостридий в пробирках с сахарным агаром. C. perfringens (слева) разлагает глюкозу с большим количеством газа, что приводит к разрыву столбика сахарного агара в нескольких местах. C. sporogenes (справа) также разлагает глюкозу с образованием газа, однако количество газообразных продуктов относительно невелико. C. tetani (в центре) не ферментирует сахара, поэтому столбик сахарного агара не изменен. Питательная основа Дыхательный субстрат (глюкоза) Редуцирующий фактор (циклосерин)
 Среда Вильсон-Блер Питательная основа (МПА) Дыхательный субстрат (глюкоза) Редуцирующий фактор (сульфит натрия) используется для выделения анаэробных бактерий. Готовится из питательного агара, к которому добавляют 1% глюкозы, хлорид железа и сульфит натрия. Анаэробные клостридии (Clostridium perfringens) образуют на среде колонии черного цвета за счет образования соединений железа с серой.
Среда Вильсон-Блер Питательная основа (МПА) Дыхательный субстрат (глюкоза) Редуцирующий фактор (сульфит натрия) используется для выделения анаэробных бактерий. Готовится из питательного агара, к которому добавляют 1% глюкозы, хлорид железа и сульфит натрия. Анаэробные клостридии (Clostridium perfringens) образуют на среде колонии черного цвета за счет образования соединений железа с серой.
 СРЕДА КИТТА-ТАРОЦЦИ Питательная основа (МПА) Дыхательный субстрат (глюкоза) Редуцирующий фактор (печень/мясо) обеспечивает рост многих спорообразующих и строгих аспорогенных анаэробов. Ее используют для культивирования и хранения клостридий. Состоит из питательного бульона, 2% глюкозы и кусочков печени или мясного фарша для адсорбции кислорода. Перед посевом среду прогревают на кипящей водяной бане в течение 10 -15 минут для удаления воздуха. После посева среду заливают небольшим слоем вазелинового масла. Выросшие анаэробы вызывают помутнение питательной среды.
СРЕДА КИТТА-ТАРОЦЦИ Питательная основа (МПА) Дыхательный субстрат (глюкоза) Редуцирующий фактор (печень/мясо) обеспечивает рост многих спорообразующих и строгих аспорогенных анаэробов. Ее используют для культивирования и хранения клостридий. Состоит из питательного бульона, 2% глюкозы и кусочков печени или мясного фарша для адсорбции кислорода. Перед посевом среду прогревают на кипящей водяной бане в течение 10 -15 минут для удаления воздуха. После посева среду заливают небольшим слоем вазелинового масла. Выросшие анаэробы вызывают помутнение питательной среды.
 Создание условий для культивирования микроорганизмов № 4
Создание условий для культивирования микроорганизмов № 4
 Основные методы создания анаэробных условий для культивирования микроорганизмов. 1. Физический- откачивание воздуха, введение специальной газовой бескислородной смеси (чаще- N 2 - 85%, CO 2 - 10%, H 2 - 5%) или специальные приемы посева. 2. Химический- применяют химические поглотители кислорода. 3. Биологический- совместное культивирование строгих аэробов и анаэробов (аэробы поглощают кислород и создают условия для размножения анаэробов). 4. Смешанный- используют несколько разных подходов. Необходимо отметить, что создание оптимальных условий для строгих анаэробов- очень сложная задача. Очень непросто обеспечить постоянное поддержание бескислородных условий культивирования, необходимы специальные среды без содержания растворенного кислорода, поддержание необходимого окислительно- восстановительного потенциала питательных сред, взятие и доставка, посев материала в анаэробных условиях.
Основные методы создания анаэробных условий для культивирования микроорганизмов. 1. Физический- откачивание воздуха, введение специальной газовой бескислородной смеси (чаще- N 2 - 85%, CO 2 - 10%, H 2 - 5%) или специальные приемы посева. 2. Химический- применяют химические поглотители кислорода. 3. Биологический- совместное культивирование строгих аэробов и анаэробов (аэробы поглощают кислород и создают условия для размножения анаэробов). 4. Смешанный- используют несколько разных подходов. Необходимо отметить, что создание оптимальных условий для строгих анаэробов- очень сложная задача. Очень непросто обеспечить постоянное поддержание бескислородных условий культивирования, необходимы специальные среды без содержания растворенного кислорода, поддержание необходимого окислительно- восстановительного потенциала питательных сред, взятие и доставка, посев материала в анаэробных условиях.
 Физические методы • Регенерация питательных сред – кипячение на водяной бане в течение 15 -20 мин с последующим быстрым охлаждением под струей холодной воды. 2. Посев патологического материала в высокий столбик полужидкой или плотной питательной среды (10 -12 мл среды в пробирке). 3. Заливка сред вазелиновым маслом 4. Эвакуационно-заместительный метод – удаление воздуха из герметически закрытых сосудов (анаэростатов, эксикаторов, боксов и др. ) с помощью вакуумного насоса с последующим замещением бескислородной газовой смесью (азот, двуокись углерода, водород) из баллона.
Физические методы • Регенерация питательных сред – кипячение на водяной бане в течение 15 -20 мин с последующим быстрым охлаждением под струей холодной воды. 2. Посев патологического материала в высокий столбик полужидкой или плотной питательной среды (10 -12 мл среды в пробирке). 3. Заливка сред вазелиновым маслом 4. Эвакуационно-заместительный метод – удаление воздуха из герметически закрытых сосудов (анаэростатов, эксикаторов, боксов и др. ) с помощью вакуумного насоса с последующим замещением бескислородной газовой смесью (азот, двуокись углерода, водород) из баллона.
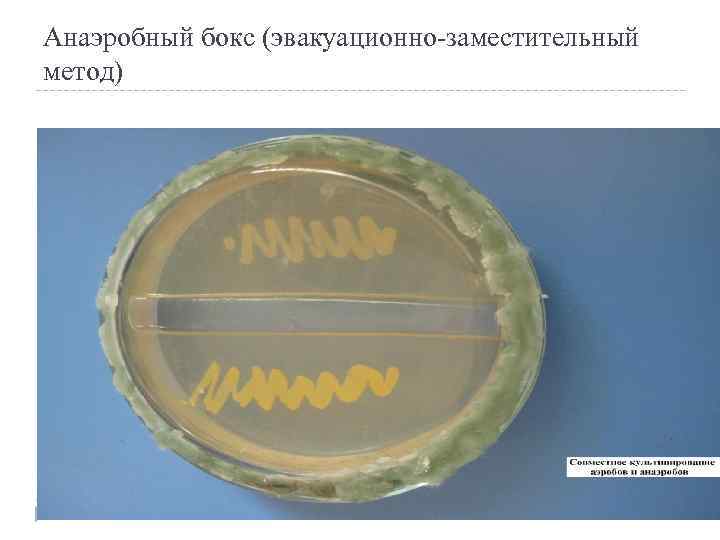 Анаэробный бокс (эвакуационно-заместительный метод)
Анаэробный бокс (эвакуационно-заместительный метод)
 Метод Фортнера Посевы проводят на чашку Петри с толстым слоем среды, разделённым пополам узкой канавкой, вырезанной в агаре. На одну половину засевают культуру аэробных бактерий, на другую — анаэробных. Края чашки заливают парафином и инкубируют в термостате. Первоначально наблюдают рост аэробов, а затем (после поглощения кислорода) — рост анаэробов.
Метод Фортнера Посевы проводят на чашку Петри с толстым слоем среды, разделённым пополам узкой канавкой, вырезанной в агаре. На одну половину засевают культуру аэробных бактерий, на другую — анаэробных. Края чашки заливают парафином и инкубируют в термостате. Первоначально наблюдают рост аэробов, а затем (после поглощения кислорода) — рост анаэробов.
 СОВМЕСТНОЕ КУЛЬТИВИРОВАНИЕ АЭРОБОВ И АНАЭРОБОВ (МЕТОД ФОРТНЕРА) В чашке с сахарным агаром вырезается «траншея» ( «ров» ) для невозможности миграции, смешивания разных культур бактерий. С одной стороны выполняется посев культуры аэробных бактерий, с другой – умеренно строгих анаэробов. Чашка закрывается, ее края запаиваются парафином (с целью не допустить попадания воздуха, кислорода внутрь чашки). Сначала вырастают в присутствии кислорода аэробы, а затем – анаэробы.
СОВМЕСТНОЕ КУЛЬТИВИРОВАНИЕ АЭРОБОВ И АНАЭРОБОВ (МЕТОД ФОРТНЕРА) В чашке с сахарным агаром вырезается «траншея» ( «ров» ) для невозможности миграции, смешивания разных культур бактерий. С одной стороны выполняется посев культуры аэробных бактерий, с другой – умеренно строгих анаэробов. Чашка закрывается, ее края запаиваются парафином (с целью не допустить попадания воздуха, кислорода внутрь чашки). Сначала вырастают в присутствии кислорода аэробы, а затем – анаэробы.
 Химические методы • Для поглощения кислорода из 220 мл воздуха применяют смесь, состоящую из 1 мл 20 % водного раствора пирогаллола и 1 мл насыщенного раствора карбоната натрия (Na 2 CO 3). • Для связывания кислорода в 1 л объема берут 100 мл свежеприготовленного 20 % раствора гидросульфита натрия (Na 2 S 2 O 4) и 16 мл 50 % раствора КОН. • Для связывания кислорода в питательной среде используют веществаредуценты: тиогликолят натрия (0, 01 -0, 02 %), цистеин (0, 03 -0, 05 %), глюкоза (0, 1 -1 %) и др. • Применение газогенерирующих систем, вырабатывающих водород и двуокись углерода и связывающих кислород в замкнутом воздушном пространстве в присутствии палладиевого катализатора.
Химические методы • Для поглощения кислорода из 220 мл воздуха применяют смесь, состоящую из 1 мл 20 % водного раствора пирогаллола и 1 мл насыщенного раствора карбоната натрия (Na 2 CO 3). • Для связывания кислорода в 1 л объема берут 100 мл свежеприготовленного 20 % раствора гидросульфита натрия (Na 2 S 2 O 4) и 16 мл 50 % раствора КОН. • Для связывания кислорода в питательной среде используют веществаредуценты: тиогликолят натрия (0, 01 -0, 02 %), цистеин (0, 03 -0, 05 %), глюкоза (0, 1 -1 %) и др. • Применение газогенерирующих систем, вырабатывающих водород и двуокись углерода и связывающих кислород в замкнутом воздушном пространстве в присутствии палладиевого катализатора.
 Анаэростаты с газогенерирующими пакетами
Анаэростаты с газогенерирующими пакетами
 Методы выделения чистой культуры анаэробов № 5
Методы выделения чистой культуры анаэробов № 5
 1. Метод Цейсслера – рассев патологического материала штрихами по поверхности плотной питательной среды для получения изолированных колоний. 2. Метод Вейнберга. Патологический материал с помощью запаянного капилляра переносят в пробирку с расплавленной и охлажденной до 45 -50 С плотной питательной средой, разлитой «высоким столбиком» и тщательно перемешивают содержимое. С помощью нового капилляра переносят исследуемый материал из первой пробирки во вторую, после чего таким же образом засевают третью пробирку с питательной средой. Засеянные пробирки охлаждают под струей холодной воды и помещают в термостат на 48 -72 ч. Выросшие в глубине агара изолированные колонии проверяют на аэротолерантность и пересевают на питательную среду для накопления «чистой» культуры 3. Метод Вейон-Виньяля. Готовят разведения исследуемого материала по методу Вейнберга. Из каждой пробирки разведенный материал насасывают в пастеровские пипетки, быстро охлаждают под струей воды и помещают в термостат на 48 -72 ч. Выросшие в глубине агара изолированные колонии проверяют на аэротолерантность и пересевают на питательную среду для накопления «чистой» культуры. 4. Метод «перевернутых чашек» . Готовят разведения исследуемого материала по методу Вейнберга. Каждую пробирку с соответствующим разведением материала выливают в крышку чашки Петри и стерильно закрывают ее донышком чашки, избегая образования пузырей воздуха. После застывания агара чашку накрывают крышкой и помещают посев в термостат на 48 -72 ч.
1. Метод Цейсслера – рассев патологического материала штрихами по поверхности плотной питательной среды для получения изолированных колоний. 2. Метод Вейнберга. Патологический материал с помощью запаянного капилляра переносят в пробирку с расплавленной и охлажденной до 45 -50 С плотной питательной средой, разлитой «высоким столбиком» и тщательно перемешивают содержимое. С помощью нового капилляра переносят исследуемый материал из первой пробирки во вторую, после чего таким же образом засевают третью пробирку с питательной средой. Засеянные пробирки охлаждают под струей холодной воды и помещают в термостат на 48 -72 ч. Выросшие в глубине агара изолированные колонии проверяют на аэротолерантность и пересевают на питательную среду для накопления «чистой» культуры 3. Метод Вейон-Виньяля. Готовят разведения исследуемого материала по методу Вейнберга. Из каждой пробирки разведенный материал насасывают в пастеровские пипетки, быстро охлаждают под струей воды и помещают в термостат на 48 -72 ч. Выросшие в глубине агара изолированные колонии проверяют на аэротолерантность и пересевают на питательную среду для накопления «чистой» культуры. 4. Метод «перевернутых чашек» . Готовят разведения исследуемого материала по методу Вейнберга. Каждую пробирку с соответствующим разведением материала выливают в крышку чашки Петри и стерильно закрывают ее донышком чашки, избегая образования пузырей воздуха. После застывания агара чашку накрывают крышкой и помещают посев в термостат на 48 -72 ч.
 Метод Цейсслера используют для выделения чистых культур спорообразующих анаэробов. Для этого проводят посев на среду Китта-Тароцци, прогревают 15 мин при 80 °С (для уничтожения вегетативных форм), заливают вазелиновым маслом и инкубируют 24 ч. Затем проводят посев на сахарно-кровяной агар для получения чистых культур. После 24 -часового культивирования подозрительные колонии изучают и отсевают на среду Китта-Тароци (с последующим контролем чистоты выделенной культуры).
Метод Цейсслера используют для выделения чистых культур спорообразующих анаэробов. Для этого проводят посев на среду Китта-Тароцци, прогревают 15 мин при 80 °С (для уничтожения вегетативных форм), заливают вазелиновым маслом и инкубируют 24 ч. Затем проводят посев на сахарно-кровяной агар для получения чистых культур. После 24 -часового культивирования подозрительные колонии изучают и отсевают на среду Китта-Тароци (с последующим контролем чистоты выделенной культуры).
 Метод Вейнберга используют для получения чистых культур строгих анаэробов. Культуры, выращенные на среде Китта-Тароцци, вносят в сахарный бульон. Затем пастеровской пипеткой с запаянным концом материал переносят в узкие пробирки (трубки Виньяля) с сахарным МПА, погружая пипетку до дна пробирки. Засеянные пробирки быстро охлаждают холодной водой, что позволяет зафиксировать отдельные бактериальные клетки в толще затвердевшего агара. Пробирки инкубируют, и изучают выросшие колонии. При обнаружении подозрительной колонии на сё месте делают распил, колонию быстро отбирают и засевают на среду Китта-Тароцци (с последующим контролем чистоты выделенной культуры).
Метод Вейнберга используют для получения чистых культур строгих анаэробов. Культуры, выращенные на среде Китта-Тароцци, вносят в сахарный бульон. Затем пастеровской пипеткой с запаянным концом материал переносят в узкие пробирки (трубки Виньяля) с сахарным МПА, погружая пипетку до дна пробирки. Засеянные пробирки быстро охлаждают холодной водой, что позволяет зафиксировать отдельные бактериальные клетки в толще затвердевшего агара. Пробирки инкубируют, и изучают выросшие колонии. При обнаружении подозрительной колонии на сё месте делают распил, колонию быстро отбирают и засевают на среду Китта-Тароцци (с последующим контролем чистоты выделенной культуры).
 Метод «перевернутых чашек» . «Наложение» стерильного донышка чашки Петри на разведенный по методу Вейнберга патологический материал в крышке путем вытеснения воздуха.
Метод «перевернутых чашек» . «Наложение» стерильного донышка чашки Петри на разведенный по методу Вейнберга патологический материал в крышке путем вытеснения воздуха.
 Для создания анаэробных условий тоже используется метод Хеннеля (часовых стеклышек).
Для создания анаэробных условий тоже используется метод Хеннеля (часовых стеклышек).
 Влияние физических факторов на микроорганизмы № 6
Влияние физических факторов на микроорганизмы № 6
 Факторы внешней среды, действующие на м/м абиотические Температура Вода Свет Давление Радиация ……………. . Воздействие других живых организмов или продуктов их жизнедеятельности
Факторы внешней среды, действующие на м/м абиотические Температура Вода Свет Давление Радиация ……………. . Воздействие других живых организмов или продуктов их жизнедеятельности
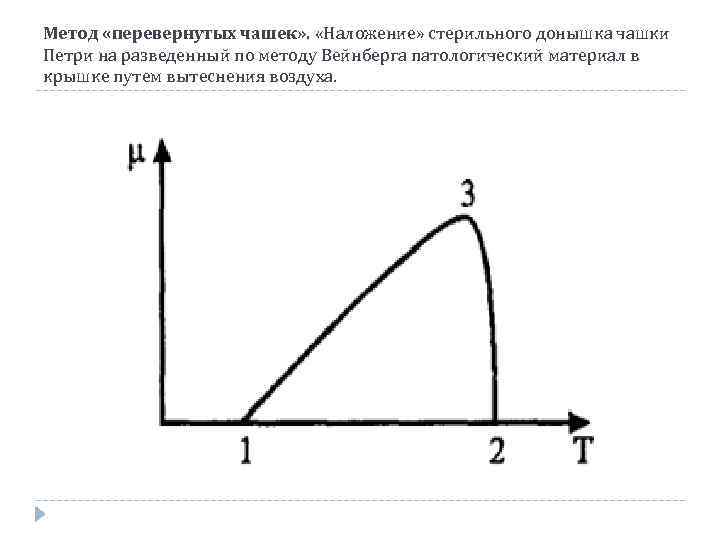
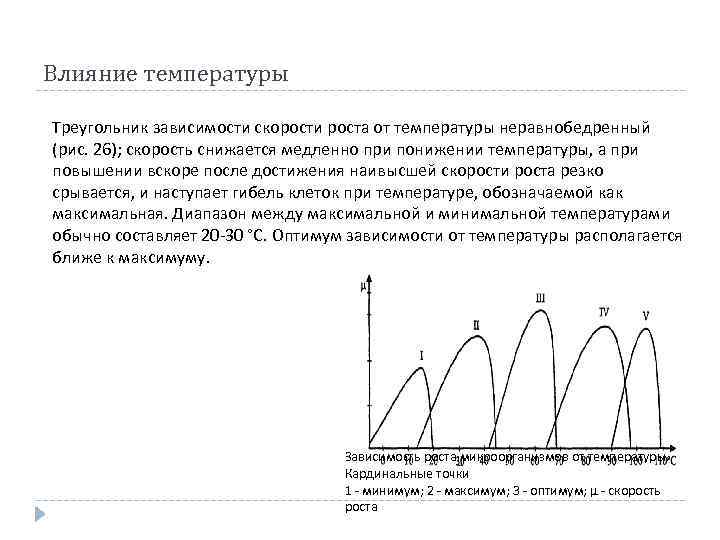 Влияние температуры Треугольник зависимости скорости роста от температуры неравнобедренный (рис. 26); скорость снижается медленно при понижении температуры, а при повышении вскоре после достижения наивысшей скорости роста резко срывается, и наступает гибель клеток при температуре, обозначаемой как максимальная. Диапазон между максимальной и минимальной температурами обычно составляет 20 -30 °С. Оптимум зависимости от температуры располагается ближе к максимуму. Зависимость роста микроорганизмов от температуры. Кардинальные точки 1 - минимум; 2 - максимум; 3 - оптимум; μ - скорость роста
Влияние температуры Треугольник зависимости скорости роста от температуры неравнобедренный (рис. 26); скорость снижается медленно при понижении температуры, а при повышении вскоре после достижения наивысшей скорости роста резко срывается, и наступает гибель клеток при температуре, обозначаемой как максимальная. Диапазон между максимальной и минимальной температурами обычно составляет 20 -30 °С. Оптимум зависимости от температуры располагается ближе к максимуму. Зависимость роста микроорганизмов от температуры. Кардинальные точки 1 - минимум; 2 - максимум; 3 - оптимум; μ - скорость роста
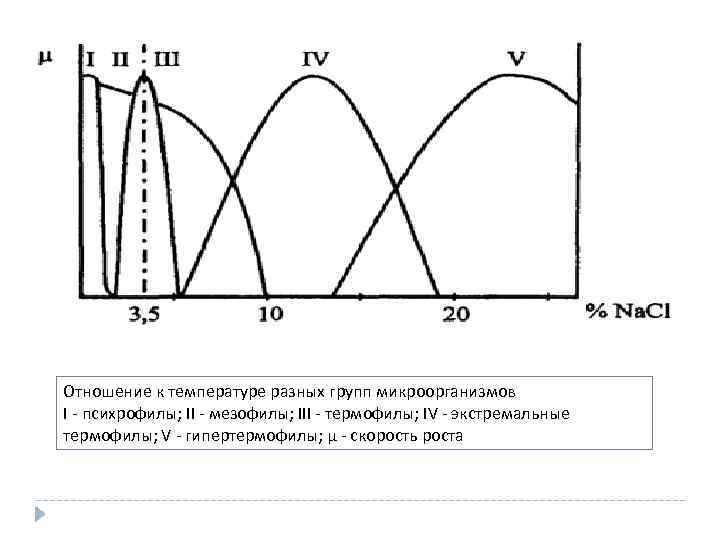 Отношение к температуре разных групп микроорганизмов I - психрофилы; II - мезофилы; III - термофилы; IV - экстремальные термофилы; V - гипертермофилы; μ - скорость роста
Отношение к температуре разных групп микроорганизмов I - психрофилы; II - мезофилы; III - термофилы; IV - экстремальные термофилы; V - гипертермофилы; μ - скорость роста
 Психрофилы - рост в диапазоне от 0 до 20 °С с оптимумом ниже 20 °С, причем здесь имеются разные категории, вплоть до организмов, развивающихся при температуре около О °С, в том числе при отрицательной во льдах, например, на нижней стороне плавучих льдов. Расти при низкой температуре могут также организмы, получившие название психроактивных (часто употребляется неудачный термин "психротрофные-). По сути дела, это эвритермные организмы, обладающие достаточной активностью при низкой температуре. Экофизиологическое различие между психрофилами и психроактивными организмами достаточно велико. Психрофилы существуют в постоянно холодных условиях, как, например, в глубинах океана или глубоких водоемах, где колебания температуры очень незначительны. Психроактивные организмы приспособлены к сезонным изменениям климата, в теплый период они накапливают биомассу, но продолжают расти и в то время, когда активность других подавлена. Несмотря на важность психрофильных организмов в условиях нашей страны, они изучены крайне недостаточно, так как замедленный рост делает их неудобными лабораторными объектами. Приспособление к понижению температуры связывают с изменением состава мембран и со способностью к образованию криопротекторов. Важно отметить, что при пониженных температурах снижается не только скорость роста, но и скорость отмирания, и, соответственно, увеличивается выживание. Другой механизм связан с повышенным синтезом ключевых ферментов, имеющих более высокий температурный оптимум, но только благодаря накоплению сохраняющих достаточную для функционирования клетки активность. Среди психрофилов много протистов и многоклеточных.
Психрофилы - рост в диапазоне от 0 до 20 °С с оптимумом ниже 20 °С, причем здесь имеются разные категории, вплоть до организмов, развивающихся при температуре около О °С, в том числе при отрицательной во льдах, например, на нижней стороне плавучих льдов. Расти при низкой температуре могут также организмы, получившие название психроактивных (часто употребляется неудачный термин "психротрофные-). По сути дела, это эвритермные организмы, обладающие достаточной активностью при низкой температуре. Экофизиологическое различие между психрофилами и психроактивными организмами достаточно велико. Психрофилы существуют в постоянно холодных условиях, как, например, в глубинах океана или глубоких водоемах, где колебания температуры очень незначительны. Психроактивные организмы приспособлены к сезонным изменениям климата, в теплый период они накапливают биомассу, но продолжают расти и в то время, когда активность других подавлена. Несмотря на важность психрофильных организмов в условиях нашей страны, они изучены крайне недостаточно, так как замедленный рост делает их неудобными лабораторными объектами. Приспособление к понижению температуры связывают с изменением состава мембран и со способностью к образованию криопротекторов. Важно отметить, что при пониженных температурах снижается не только скорость роста, но и скорость отмирания, и, соответственно, увеличивается выживание. Другой механизм связан с повышенным синтезом ключевых ферментов, имеющих более высокий температурный оптимум, но только благодаря накоплению сохраняющих достаточную для функционирования клетки активность. Среди психрофилов много протистов и многоклеточных.
 Мезофилы имеют оптимум, близкий к температуре тела теплокровных животных, однако многие лучше растут при 20 -25 °С. Максимальная температура для свободноживущих мезофилов, около 45 °С, близка к максимальному нагреву почвы солнцем. Это наиболее изученная группа организмов, самая удобная для исследования в лабораторных условиях. Как уже упоминалось, среди этой группы выделяются стенотермные и эвритермные организмы. К мезофилам относятся наиболее массовые группы протео-бактерий, цианобактерий, грамположительных организмов. Термофилы представлены организмами, растущими при температуре выше 50 °С, но сейчас их разделили на несколько групп со специальными названиями. Собственно термофилы имеют максимум при температуре ниже 70 °С и минимум - выше 40 °С. Это обитатели термальных источников разогревающихся куч органического вещества в компостах или куч угля. Целый ряд важных функциональных групп, например цианобактерий, имеет своим пределом температуру 70 °С. Причины, по которым для многих функциональных групп эта температура, близкая к температуре, убивающей вегетативные клетки мезофилов, оказывается максимальной, легко представить. Особо следует заметить отсутствие термофильных эукариот, для которых температура 60°С оказывается предельной. Многоклеточные обычно отсутствуют при температуре выше 50 °С.
Мезофилы имеют оптимум, близкий к температуре тела теплокровных животных, однако многие лучше растут при 20 -25 °С. Максимальная температура для свободноживущих мезофилов, около 45 °С, близка к максимальному нагреву почвы солнцем. Это наиболее изученная группа организмов, самая удобная для исследования в лабораторных условиях. Как уже упоминалось, среди этой группы выделяются стенотермные и эвритермные организмы. К мезофилам относятся наиболее массовые группы протео-бактерий, цианобактерий, грамположительных организмов. Термофилы представлены организмами, растущими при температуре выше 50 °С, но сейчас их разделили на несколько групп со специальными названиями. Собственно термофилы имеют максимум при температуре ниже 70 °С и минимум - выше 40 °С. Это обитатели термальных источников разогревающихся куч органического вещества в компостах или куч угля. Целый ряд важных функциональных групп, например цианобактерий, имеет своим пределом температуру 70 °С. Причины, по которым для многих функциональных групп эта температура, близкая к температуре, убивающей вегетативные клетки мезофилов, оказывается максимальной, легко представить. Особо следует заметить отсутствие термофильных эукариот, для которых температура 60°С оказывается предельной. Многоклеточные обычно отсутствуют при температуре выше 50 °С.
 Соль По отношению к солености микроорганизмы разделяются на несколько групп. Соленость действует на клетки как осмотический фактор. Для своего существования клетки должны поддерживать тургор: мембрана должна плотно прилегать к клеточной стенке, как пластиковый мешок с жидкостью к сетке. При нарушении этого состояния происходит плазмолиз. Организмы разделяются на физиологические группы в соответствии с осмотическими условиями среды. Считается, что обитатели пресных вод чувствительны к 3, 5%-ной концентрации Na. Cl, как в морской воде, и в описание организмов обычно входит такой тест. Обитатели ультрапресных вод развиваются в среде с содержанием солей ниже 100 мг/л. Морские организмы развиваются при солености, равной 2 -4%, причем под соленостью здесь понимается именно содержание Na. Cl. Обозначение морских организмов как галофилов не совсем удачно, так как они не приспособлены к значительному повышению солености. Галофилы развиваются при солености, существенно превышающей соленость морской воды. К умеренным галофилам относятся организмы, имеющие верхний предел солености до 15%.
Соль По отношению к солености микроорганизмы разделяются на несколько групп. Соленость действует на клетки как осмотический фактор. Для своего существования клетки должны поддерживать тургор: мембрана должна плотно прилегать к клеточной стенке, как пластиковый мешок с жидкостью к сетке. При нарушении этого состояния происходит плазмолиз. Организмы разделяются на физиологические группы в соответствии с осмотическими условиями среды. Считается, что обитатели пресных вод чувствительны к 3, 5%-ной концентрации Na. Cl, как в морской воде, и в описание организмов обычно входит такой тест. Обитатели ультрапресных вод развиваются в среде с содержанием солей ниже 100 мг/л. Морские организмы развиваются при солености, равной 2 -4%, причем под соленостью здесь понимается именно содержание Na. Cl. Обозначение морских организмов как галофилов не совсем удачно, так как они не приспособлены к значительному повышению солености. Галофилы развиваются при солености, существенно превышающей соленость морской воды. К умеренным галофилам относятся организмы, имеющие верхний предел солености до 15%.
 В общем плане реакция организмов на неблагоприятные внешние воздействия подчиняется правилу доза-эффект: чем выше доза, тем сильнее эффект. Для дозы применяется понятие L 1/2, или половина летальной дозы, которая соответствует дозе, обуславливающей половину эффекта. Отмирание организмов происходит по экспоненциальному закону, предполагающему гибель постоянной части определенной популяции: -dx / dt = k. X где k - константа, зависящая от качества агента и его интенсивности и, естественно, от свойств популяции, например, вегетативных клеток или спор.
В общем плане реакция организмов на неблагоприятные внешние воздействия подчиняется правилу доза-эффект: чем выше доза, тем сильнее эффект. Для дозы применяется понятие L 1/2, или половина летальной дозы, которая соответствует дозе, обуславливающей половину эффекта. Отмирание организмов происходит по экспоненциальному закону, предполагающему гибель постоянной части определенной популяции: -dx / dt = k. X где k - константа, зависящая от качества агента и его интенсивности и, естественно, от свойств популяции, например, вегетативных клеток или спор.
 Возникновение устойчивости к тяжелым металлам, антибиотикам, дезинфектантам, которые широко применяются на практике, включает генетические изменения, часто обусловленные плазми-дами и составляющие специальный раздел молекулярной генетики. В природных условиях приходится рассматривать способы подавления микробной деятельности путем стерилизации, дезинфекции, избирательного ингибирования групп организмов или их функций антибиотиками. Под стерилизацией подразумевается полная гибель организмов и отсутствие жизнеспособных клеток. Под дезинфекцией - сильное снижение численности, как правило, под воздействием химических агентов. Различают бактерио-статическое, бактериоцидное, бактериолитическое действие, которое соответственно останавливает рост бактерий, убивает клетки, разрушает их. Механическая стерилизация фильтрованием пригодна лишь для чистых жидкостей и газов. В большинстве случаев достаточно пользоваться фильтрами с порами размером 0, 45 мкм, но для мелких форм приходится применять фильтр с размером пор 0, 2 мкм, который требует значительно больших усилий при фильтровании. Особые предосторожности следует принимать, работая с "ультрамикробами", для которых эти размеры критичны. Фильтрование удобно для отделения эукариот, которые обычно имеют размеры около 10 мкм, и этим способом можно разделить микроорганизмы на размерные группы. В природе фильтрование происходит при движении воды через пористые среды, например, через песок, как это применяется при подготовке питьевой воды. Движение воды через пористые среды служит важным фактором в гидрогеологии. Механическое разрушение части клеток вызывается резким перепадом гидростатического давления, которое достигается разными способами, в том числе кавитацией при обработке ультразвуком.
Возникновение устойчивости к тяжелым металлам, антибиотикам, дезинфектантам, которые широко применяются на практике, включает генетические изменения, часто обусловленные плазми-дами и составляющие специальный раздел молекулярной генетики. В природных условиях приходится рассматривать способы подавления микробной деятельности путем стерилизации, дезинфекции, избирательного ингибирования групп организмов или их функций антибиотиками. Под стерилизацией подразумевается полная гибель организмов и отсутствие жизнеспособных клеток. Под дезинфекцией - сильное снижение численности, как правило, под воздействием химических агентов. Различают бактерио-статическое, бактериоцидное, бактериолитическое действие, которое соответственно останавливает рост бактерий, убивает клетки, разрушает их. Механическая стерилизация фильтрованием пригодна лишь для чистых жидкостей и газов. В большинстве случаев достаточно пользоваться фильтрами с порами размером 0, 45 мкм, но для мелких форм приходится применять фильтр с размером пор 0, 2 мкм, который требует значительно больших усилий при фильтровании. Особые предосторожности следует принимать, работая с "ультрамикробами", для которых эти размеры критичны. Фильтрование удобно для отделения эукариот, которые обычно имеют размеры около 10 мкм, и этим способом можно разделить микроорганизмы на размерные группы. В природе фильтрование происходит при движении воды через пористые среды, например, через песок, как это применяется при подготовке питьевой воды. Движение воды через пористые среды служит важным фактором в гидрогеологии. Механическое разрушение части клеток вызывается резким перепадом гидростатического давления, которое достигается разными способами, в том числе кавитацией при обработке ультразвуком.
 Термическая стерилизация служит наиболее распространенным способом стерилизации. Обычно применяется нагревание выше 120 °С, приводящее к денатурации белков или разрушению других компонентов среды, например, к карамелизации Сахаров. При работе с гипертермофилами и некоторыми споровыми организмами полная стерилизация при этих условиях может быть не достигнута. Тем не менее это универсальный метод стерилизации, от которого приходится отказываться только в некоторых специальных ситуациях. К физическим методам стерилизации относится и облучение ультрафиолетом в области поглощения нуклеиновых кислот 250 -280 нм, достигаемой кварцевыми "бактерицидными" лампами. От этого воздействия бактерии защищает даже небольшая тень, в которой их достигают лишь фотохимически образуемые окислители. Для защиты от радиации у бактерий выработаны антиокислительные механизмы, например, каротиноиды, а также система генетической репарации поврежденных участков ДНК. Такими механизмами особенно славится Deinococcus radiodurans, а также ряд термофильных эу- и архебактерий. Химическая дезинфекция связана с применением сильных окисляющих агентов, таких как: хлор, озон, 3%-ная перекись. водорода. С SH-группами реагируют соединения, содержащие ртуть. Йод служит окислителем, а также образует соединение с тирозином и в виде слабого раствора в KI (раствор Люголя) подавляет развитие бактерий. 70%-ный спирт денатурирует белки и растворяет некоторые липиды. Фенолы денатурируют белки. Газообразная окись этилена служит алкилирующим агентом и применяется для стерилизации пластмасс. Применение химических агентов требует внимательного анализа условий, необходимо учитывать взаимодействие химического агента с компонентами среды, например бессмысленно применять окислительные агенты для богатых органическими веществами или восстановителями жидкостей, или же сулему в сероводородной среде.
Термическая стерилизация служит наиболее распространенным способом стерилизации. Обычно применяется нагревание выше 120 °С, приводящее к денатурации белков или разрушению других компонентов среды, например, к карамелизации Сахаров. При работе с гипертермофилами и некоторыми споровыми организмами полная стерилизация при этих условиях может быть не достигнута. Тем не менее это универсальный метод стерилизации, от которого приходится отказываться только в некоторых специальных ситуациях. К физическим методам стерилизации относится и облучение ультрафиолетом в области поглощения нуклеиновых кислот 250 -280 нм, достигаемой кварцевыми "бактерицидными" лампами. От этого воздействия бактерии защищает даже небольшая тень, в которой их достигают лишь фотохимически образуемые окислители. Для защиты от радиации у бактерий выработаны антиокислительные механизмы, например, каротиноиды, а также система генетической репарации поврежденных участков ДНК. Такими механизмами особенно славится Deinococcus radiodurans, а также ряд термофильных эу- и архебактерий. Химическая дезинфекция связана с применением сильных окисляющих агентов, таких как: хлор, озон, 3%-ная перекись. водорода. С SH-группами реагируют соединения, содержащие ртуть. Йод служит окислителем, а также образует соединение с тирозином и в виде слабого раствора в KI (раствор Люголя) подавляет развитие бактерий. 70%-ный спирт денатурирует белки и растворяет некоторые липиды. Фенолы денатурируют белки. Газообразная окись этилена служит алкилирующим агентом и применяется для стерилизации пластмасс. Применение химических агентов требует внимательного анализа условий, необходимо учитывать взаимодействие химического агента с компонентами среды, например бессмысленно применять окислительные агенты для богатых органическими веществами или восстановителями жидкостей, или же сулему в сероводородной среде.
 Действие ионизирующих излучений на живые объекты Биологическое действие ионизирующих излучений - изменения, вызываемые в жизнедеятельности и структуре живых организмов при воздействии коротковолновых электромагнитных волн (рентгеновского излучения и гамма-излучения) или потоков заряженных частиц (альфачастиц, бета - излучения, протонов) и нейтронов. Исследования влияния ионизирующих излучений на биологические объекты были начаты сразу после открытия рентгеновского излучения (1895) и радиоактивности (1896). В 1896 физиолог И. Р. Тарханов показал, что рентгеновское излучение, проходя через живые организмы, нарушает их жизнедеятельность. Особенно интенсивно стали развиваться исследования биологического действия ионизирующих излучений с началом применения атомного оружия (1945), а затем и мирного использования атомной энергии.
Действие ионизирующих излучений на живые объекты Биологическое действие ионизирующих излучений - изменения, вызываемые в жизнедеятельности и структуре живых организмов при воздействии коротковолновых электромагнитных волн (рентгеновского излучения и гамма-излучения) или потоков заряженных частиц (альфачастиц, бета - излучения, протонов) и нейтронов. Исследования влияния ионизирующих излучений на биологические объекты были начаты сразу после открытия рентгеновского излучения (1895) и радиоактивности (1896). В 1896 физиолог И. Р. Тарханов показал, что рентгеновское излучение, проходя через живые организмы, нарушает их жизнедеятельность. Особенно интенсивно стали развиваться исследования биологического действия ионизирующих излучений с началом применения атомного оружия (1945), а затем и мирного использования атомной энергии.
 При ионизации молекул воды в живом организме, состоящем до 90% из воды, в присутствии кислорода возникают активные радикалы (ОН- и др. ), гидратированные электроны, а также молекулы перекиси водорода, включающиеся затем в цепь химических реакций в клетке, что обеспечивает косвенное действие излучения. При облучении в дозе 1000 Р (что соответствует поглощенной дозе порядка 10 Гр) в клетке средней величины (10 -9 г) возникает около 1 млн. таких радикалов, каждый из которых в присутствии кислорода воздуха может дать начало цепным реакциям окисления, во много раз увеличивающим количество измененных молекул в клетке и вызывающим дальнейшее изменение надмолекулярных (субмикроскопических) структур. Выяснение большой роли свободного кислорода в цепных реакциях, ведущих к лучевому поражению, т. н. кислородного эффекта, способствовало разработке ряда эффективных радиозащитных веществ, вызывающих искусственную гипоксию в тканях организма. Последующие биохимические процессы лучевого повреждения развиваются медленнее. Образовавшиеся активные радикалы нарушают нормальные ферментативные процессы в клетке, что ведёт к уменьшению макроэргических (богатых энергией) соединений. Особенно чувствителен к облучению синтез дезоксирибонуклеиновых кислот (ДНК) в интенсивно делящихся клетках. Таким образом, в результате цепных реакций, возникающих при поглощении энергии излучения, изменяются многие компоненты клетки, в том числе макромолекулы (ДНК, ферменты и др. ) и сравнительно малые молекулы (аденозинтрифосфорная кислота, коферменты и др. ). Это приводит к нарушению ферментативных реакций, физиологических процессов и клеточных структур.
При ионизации молекул воды в живом организме, состоящем до 90% из воды, в присутствии кислорода возникают активные радикалы (ОН- и др. ), гидратированные электроны, а также молекулы перекиси водорода, включающиеся затем в цепь химических реакций в клетке, что обеспечивает косвенное действие излучения. При облучении в дозе 1000 Р (что соответствует поглощенной дозе порядка 10 Гр) в клетке средней величины (10 -9 г) возникает около 1 млн. таких радикалов, каждый из которых в присутствии кислорода воздуха может дать начало цепным реакциям окисления, во много раз увеличивающим количество измененных молекул в клетке и вызывающим дальнейшее изменение надмолекулярных (субмикроскопических) структур. Выяснение большой роли свободного кислорода в цепных реакциях, ведущих к лучевому поражению, т. н. кислородного эффекта, способствовало разработке ряда эффективных радиозащитных веществ, вызывающих искусственную гипоксию в тканях организма. Последующие биохимические процессы лучевого повреждения развиваются медленнее. Образовавшиеся активные радикалы нарушают нормальные ферментативные процессы в клетке, что ведёт к уменьшению макроэргических (богатых энергией) соединений. Особенно чувствителен к облучению синтез дезоксирибонуклеиновых кислот (ДНК) в интенсивно делящихся клетках. Таким образом, в результате цепных реакций, возникающих при поглощении энергии излучения, изменяются многие компоненты клетки, в том числе макромолекулы (ДНК, ферменты и др. ) и сравнительно малые молекулы (аденозинтрифосфорная кислота, коферменты и др. ). Это приводит к нарушению ферментативных реакций, физиологических процессов и клеточных структур.
 Микроорганизмы, по чувствительности к радиационному действию, обычно располагают в таком порядке: - наиболее чувствительны бактерии, затем плесени, дрожжи, споры бактерий, вирусы. Однако это разделение не абсолютно, так как среди бактерий есть виды более радиоустойчивые, чем вирусы. Радиочувствительность микроорганизмов модифицируют различные факторы, как внутренние: генетическая природа самой клетки, жизненная фаза клетки и другие, так и внешние: температура, концентрация кислорода и других газов, состав и свойства среды в которой производится облучение, а также тип радиационного воздействия и его мощность и другие факторы. Радиочувствительность микроорганизмов значительно ниже, чем у растений и животных на 1 -2 порядка, в ряде случаев бактерицидный эффект для некоторых видов может быть достигнут только при значительных дозах: 1 -2 Мрад. Уже на первых этапах исследования радиационной чувствительности микроорганизмов было показано, что при дозе 5000 Р значительно снижается выживаемость кишечной палочки, а при дозе 20 к. Р погибает 95 % бактерий. Культура микроорганизмов каждого вида содержит смесь клеток, различных по чувствительности к радиации. Например для культуры кишечной палочки 66% LD 50 соответствовала доза 1, 2 крад, а для 34 % бактерий – 3, 5 крад. При облучении бактерий кишечной группы гамма лучами, их инактивация происходит в пределах от 24 до 168 крад, а гибель всех клеток при дозах около 300 крад.
Микроорганизмы, по чувствительности к радиационному действию, обычно располагают в таком порядке: - наиболее чувствительны бактерии, затем плесени, дрожжи, споры бактерий, вирусы. Однако это разделение не абсолютно, так как среди бактерий есть виды более радиоустойчивые, чем вирусы. Радиочувствительность микроорганизмов модифицируют различные факторы, как внутренние: генетическая природа самой клетки, жизненная фаза клетки и другие, так и внешние: температура, концентрация кислорода и других газов, состав и свойства среды в которой производится облучение, а также тип радиационного воздействия и его мощность и другие факторы. Радиочувствительность микроорганизмов значительно ниже, чем у растений и животных на 1 -2 порядка, в ряде случаев бактерицидный эффект для некоторых видов может быть достигнут только при значительных дозах: 1 -2 Мрад. Уже на первых этапах исследования радиационной чувствительности микроорганизмов было показано, что при дозе 5000 Р значительно снижается выживаемость кишечной палочки, а при дозе 20 к. Р погибает 95 % бактерий. Культура микроорганизмов каждого вида содержит смесь клеток, различных по чувствительности к радиации. Например для культуры кишечной палочки 66% LD 50 соответствовала доза 1, 2 крад, а для 34 % бактерий – 3, 5 крад. При облучении бактерий кишечной группы гамма лучами, их инактивация происходит в пределах от 24 до 168 крад, а гибель всех клеток при дозах около 300 крад.
 Для получения одинакового биологического эффекта у различных видов микроорганизмов требуются различные дозы излучения. Эти различия зависят от ряда биологических особенностей облучаемых бактерий, условий облучения, влияния внешней среды и других факторов. Особое значение придается неодинаковой чувствительности нуклеинового обмена и ДНК различных организмов к радиационному облучению. Чувствительность бактерий к радиации значительно изменяется внутри одного и того же вида и, даже, популяции бактериальных клеток. Популяция клеток состоит из бактерий, располагающихся по устойчивости к радиации в вариационный ряд, так же, как и по другим биологическим признакам. Поэтому в популяции всегда присутствуют особо радиорезистентные клетки, для того, чтобы их убить, нужно облучать более мощными дозами, чем те, при которых погибает основная масса клеток более радиочувствительных. Грамположительные бактерии менее чувствительны к облучению, чем грамотрицательные. Споры бактерий обладают очень низкой радиочувствительностью, но и среди неспорообразующих микроорганизмов известны организмы радиоустойчивость которых может превышать устойчивость спор. Чаще всего они принадлежат к кокам или сарцинам. Известны микрококки, у которых полулетальная доза равна 400 крад (4 к. Гр). При лучевой стерилизации мяса, рыбы и других продуктов наиболее часто после облучения в дозах от 600 до 1500 крад обнаруживали кокков. Примером высокой радиоустойчивости могут быть также бактерии, выделяемые из вод атомных реакторов.
Для получения одинакового биологического эффекта у различных видов микроорганизмов требуются различные дозы излучения. Эти различия зависят от ряда биологических особенностей облучаемых бактерий, условий облучения, влияния внешней среды и других факторов. Особое значение придается неодинаковой чувствительности нуклеинового обмена и ДНК различных организмов к радиационному облучению. Чувствительность бактерий к радиации значительно изменяется внутри одного и того же вида и, даже, популяции бактериальных клеток. Популяция клеток состоит из бактерий, располагающихся по устойчивости к радиации в вариационный ряд, так же, как и по другим биологическим признакам. Поэтому в популяции всегда присутствуют особо радиорезистентные клетки, для того, чтобы их убить, нужно облучать более мощными дозами, чем те, при которых погибает основная масса клеток более радиочувствительных. Грамположительные бактерии менее чувствительны к облучению, чем грамотрицательные. Споры бактерий обладают очень низкой радиочувствительностью, но и среди неспорообразующих микроорганизмов известны организмы радиоустойчивость которых может превышать устойчивость спор. Чаще всего они принадлежат к кокам или сарцинам. Известны микрококки, у которых полулетальная доза равна 400 крад (4 к. Гр). При лучевой стерилизации мяса, рыбы и других продуктов наиболее часто после облучения в дозах от 600 до 1500 крад обнаруживали кокков. Примером высокой радиоустойчивости могут быть также бактерии, выделяемые из вод атомных реакторов.
 Действие химических факторов на микроорганизмы № 7
Действие химических факторов на микроорганизмы № 7
 Кислотность и щелочность В отличие от температуры, действию химических факторов микроорганизмы могут хотя бы частично противостоять за счет мембранного барьера проницаемости. Внутренний р. Н клетки поддерживается близнейтральным, р. Н 6 -8, и это связано прежде всего с протонной энергетикой, которая заставляет клетку поддерживать внутриклеточное значение р. Н < 9 с помощью ионного обмена. Однако некоторые группы организмов способны развиваться при экстремальных значениях среды р. Н. По отношению к р. Н выделяются следующие физиологические группы: Нейтрофилы, развивающиеся при нейтральном р. Н в диапазоне р. Н > 5 и р. Н < 9, но главным образом в области р. Н 6 -8; к ним относится большинство организмов. Подкисление среды, например, за счет образования органических кислот ведет к остановке роста нейтрофилов, что и используется при сквашивании и сохранении растительных продуктов. Ацидофилы живут при р. Н < 6 до предельной кислотности р. Н < 2. Алкалофилы развиваются при р. Н > 8, 5 с предельным значением р. Н ≈ 11.
Кислотность и щелочность В отличие от температуры, действию химических факторов микроорганизмы могут хотя бы частично противостоять за счет мембранного барьера проницаемости. Внутренний р. Н клетки поддерживается близнейтральным, р. Н 6 -8, и это связано прежде всего с протонной энергетикой, которая заставляет клетку поддерживать внутриклеточное значение р. Н < 9 с помощью ионного обмена. Однако некоторые группы организмов способны развиваться при экстремальных значениях среды р. Н. По отношению к р. Н выделяются следующие физиологические группы: Нейтрофилы, развивающиеся при нейтральном р. Н в диапазоне р. Н > 5 и р. Н < 9, но главным образом в области р. Н 6 -8; к ним относится большинство организмов. Подкисление среды, например, за счет образования органических кислот ведет к остановке роста нейтрофилов, что и используется при сквашивании и сохранении растительных продуктов. Ацидофилы живут при р. Н < 6 до предельной кислотности р. Н < 2. Алкалофилы развиваются при р. Н > 8, 5 с предельным значением р. Н ≈ 11.
 Окислительно-востановительные условия Распределение физиологических групп организмов в зависимости от р. Н среды согласуется с гидрохимическими характеристиками природных вод, описываемых в координатах Eh - р. Н. Границами поля служит устойчивость воды, определяемая выделением из нее кислорода при высоком Eh и водорода при низком Eh. Окислительно-восстановительные условия характеризуются значением Eh, связанным с доминирующей в данных условиях окислительно-восстановительной парой. Поскольку микроорганизмы получают энергию от окислительновосстановительных реакций, возможность их развития зависит от Eh среды. В координатах Eh - р. Н для веществ вычислены термодинамические поля устойчивости. Хемотрофный организм может развиваться в области термодинамической устойчивости продукта реакции катаболизма и метастабильности субстрата. Отсюда следует приуроченность организмов к соответствующим полям в координатах Eh-p. H.
Окислительно-востановительные условия Распределение физиологических групп организмов в зависимости от р. Н среды согласуется с гидрохимическими характеристиками природных вод, описываемых в координатах Eh - р. Н. Границами поля служит устойчивость воды, определяемая выделением из нее кислорода при высоком Eh и водорода при низком Eh. Окислительно-восстановительные условия характеризуются значением Eh, связанным с доминирующей в данных условиях окислительно-восстановительной парой. Поскольку микроорганизмы получают энергию от окислительновосстановительных реакций, возможность их развития зависит от Eh среды. В координатах Eh - р. Н для веществ вычислены термодинамические поля устойчивости. Хемотрофный организм может развиваться в области термодинамической устойчивости продукта реакции катаболизма и метастабильности субстрата. Отсюда следует приуроченность организмов к соответствующим полям в координатах Eh-p. H.
 Ингибирование антибиотиками и химиотерапевтическими агентами обусловлено тем, что они имеют в клетках определенную мишень, например пенициллины - синтез клеточной стенки; хлорамфеникол, стрептомицин, тетрациклин, эритромицин действуют на синтез белка на бактериальных рибосомах, а циклогексимид - на эукариотных; синтез ДНК ингибирует налидиксовая кислота. В настоящее время получены очень детальные сведения о действии таких агентов, что позволяет использовать их как для ингибиторного анализа функций клеток, так и избирательного подавления групп организмов. В природе антибиотики служат естественным средством межвидовой борьбы у бактерий; обычным методом их распознавания служит появление зоны ингибирования роста тест-организма вокруг колонии на чашке. Такое же подавление может быть вызвано конкуренцией за субстрат, образованием токсичного продукта обмена, как, например, кислоты, действием хищников, фагов. Чтобы различить эти явления, пользуются фильтратом культуральной жидкости. Очевидно, что антибиотики представляют очень специфические по воздействию агенты, которые не должны действовать на организм-продуцент
Ингибирование антибиотиками и химиотерапевтическими агентами обусловлено тем, что они имеют в клетках определенную мишень, например пенициллины - синтез клеточной стенки; хлорамфеникол, стрептомицин, тетрациклин, эритромицин действуют на синтез белка на бактериальных рибосомах, а циклогексимид - на эукариотных; синтез ДНК ингибирует налидиксовая кислота. В настоящее время получены очень детальные сведения о действии таких агентов, что позволяет использовать их как для ингибиторного анализа функций клеток, так и избирательного подавления групп организмов. В природе антибиотики служат естественным средством межвидовой борьбы у бактерий; обычным методом их распознавания служит появление зоны ингибирования роста тест-организма вокруг колонии на чашке. Такое же подавление может быть вызвано конкуренцией за субстрат, образованием токсичного продукта обмена, как, например, кислоты, действием хищников, фагов. Чтобы различить эти явления, пользуются фильтратом культуральной жидкости. Очевидно, что антибиотики представляют очень специфические по воздействию агенты, которые не должны действовать на организм-продуцент
 Стерилизация и дезинфекция № 8
Стерилизация и дезинфекция № 8
 Методы обеззараживания биологических объектов. Стерилизация Дезинфекция Антисептика – комплекс лечебно-профилактических мероприятий, направленных на уничтожение или угнетение роста микробов в ране, на поверхности кожи или слизистых оболочек. Асептика – система профилактических мероприятий, направленных против проникновения микробов в рану, ткани, органы больного.
Методы обеззараживания биологических объектов. Стерилизация Дезинфекция Антисептика – комплекс лечебно-профилактических мероприятий, направленных на уничтожение или угнетение роста микробов в ране, на поверхности кожи или слизистых оболочек. Асептика – система профилактических мероприятий, направленных против проникновения микробов в рану, ткани, органы больного.
 Стерилизация (от лат. sterilis — бесплодный) 1) полное освобождение различных веществ, предметов, пищевых продуктов от живых микроорганизмов. Наиболее распространённые методы С. — действие высоких температур, а для жидкостей — фильтрация, в результате которой клетки микроорганизмов задерживаются на фильтрах. Вегетативные клетки большинства бактерий, дрожжей и микроскопических грибов погибают при 50— 70 °С в течение 30 мин, тогда как споры ряда бактерий выдерживают продолжительное кипячение. Этим объясняется применение высоких температур при С. Простейший способ С. — обжигание металлических и стеклянных предметов в пламени горелки. С. сухим жаром производится в сушильных шкафах при 160— 165 °С в течение 2 ч. Таким методом стерилизуют лабораторную посуду, металлические предметы, некоторые порошкообразные, не портящиеся при нагревании вещества и т. п. С. водяным паром под давлением производят в автоклавах. Питательные среды для микроорганизмов стерилизуют при 4 am и 121 °С 20— 30 мин или при 0, 5 am и 112 °С — 20 мин. Хирургические инструменты, перевязочные и шовные материалы, различные консервы в пищевой промышленности стерилизуют обычно при 1 am 30 мин. Некоторые жидкости и растворы нельзя стерилизовать при высоких температурах, так как при этом происходит их испарение или инактивация витаминов и других биологически активных соединений, разложение лекарственных веществ, карамелизация сахаров, денатурация белков и т. п. В этих случаях осуществляют "холодную" С. , при которой жидкости фильтруют через мелкопористые бактериальные фильтры. С. твёрдых предметов, портящихся при нагревании (некоторые пластмассы, электронная аппаратура и др. ), может быть осуществлена обработкой газами (например, окисью этилена в смеси с СО 2 или бромистым метилом), спиртом, растворами сулемы и др. химических веществ. В этих же случаях может быть применена т. н. лучевая С. (обычно используют ионизирующее излучение в дозах 3— 10 млн. рад). Значительное уменьшение количества микроорганизмов, содержащихся в воздухе помещений (операционных, цехов фасовки антибиотиков и т. п. ), достигается с помощью ультрафиолетового излучения, обладающего бактерицидным действием. С. широко применяется в микробиологических и др. научных исследованиях, медицине и пищевой промышленности. С. подвергаются также космические корабли, чтобы исключить возможность загрязнения других планет земными микроорганизмами. Стерильность объектов доказывается полным отсутствием в них живых микроорганизмов. Для этого производят посевы в жидкие или на плотные богатые питательными веществами среды, чтобы обеспечить прорастание поврежденных, но не убитых клеток.
Стерилизация (от лат. sterilis — бесплодный) 1) полное освобождение различных веществ, предметов, пищевых продуктов от живых микроорганизмов. Наиболее распространённые методы С. — действие высоких температур, а для жидкостей — фильтрация, в результате которой клетки микроорганизмов задерживаются на фильтрах. Вегетативные клетки большинства бактерий, дрожжей и микроскопических грибов погибают при 50— 70 °С в течение 30 мин, тогда как споры ряда бактерий выдерживают продолжительное кипячение. Этим объясняется применение высоких температур при С. Простейший способ С. — обжигание металлических и стеклянных предметов в пламени горелки. С. сухим жаром производится в сушильных шкафах при 160— 165 °С в течение 2 ч. Таким методом стерилизуют лабораторную посуду, металлические предметы, некоторые порошкообразные, не портящиеся при нагревании вещества и т. п. С. водяным паром под давлением производят в автоклавах. Питательные среды для микроорганизмов стерилизуют при 4 am и 121 °С 20— 30 мин или при 0, 5 am и 112 °С — 20 мин. Хирургические инструменты, перевязочные и шовные материалы, различные консервы в пищевой промышленности стерилизуют обычно при 1 am 30 мин. Некоторые жидкости и растворы нельзя стерилизовать при высоких температурах, так как при этом происходит их испарение или инактивация витаминов и других биологически активных соединений, разложение лекарственных веществ, карамелизация сахаров, денатурация белков и т. п. В этих случаях осуществляют "холодную" С. , при которой жидкости фильтруют через мелкопористые бактериальные фильтры. С. твёрдых предметов, портящихся при нагревании (некоторые пластмассы, электронная аппаратура и др. ), может быть осуществлена обработкой газами (например, окисью этилена в смеси с СО 2 или бромистым метилом), спиртом, растворами сулемы и др. химических веществ. В этих же случаях может быть применена т. н. лучевая С. (обычно используют ионизирующее излучение в дозах 3— 10 млн. рад). Значительное уменьшение количества микроорганизмов, содержащихся в воздухе помещений (операционных, цехов фасовки антибиотиков и т. п. ), достигается с помощью ультрафиолетового излучения, обладающего бактерицидным действием. С. широко применяется в микробиологических и др. научных исследованиях, медицине и пищевой промышленности. С. подвергаются также космические корабли, чтобы исключить возможность загрязнения других планет земными микроорганизмами. Стерильность объектов доказывается полным отсутствием в них живых микроорганизмов. Для этого производят посевы в жидкие или на плотные богатые питательными веществами среды, чтобы обеспечить прорастание поврежденных, но не убитых клеток.
 Дезинфекция — комплекс мероприятий, направленных на уничтожение во внешней среде патогенных микроорганизмов. В широком смысле дезинфекция включает также уничтожение членистоногих — переносчиков инфекций (Дезинсекция) и грызунов — носителей и переносчиков инфекций (Дератизация). Дезинфекция входит в комплекс противоэпидемических и санитарно-профилактических мероприятий. Дезинфекцию подразделяют на текущую, заключительную и профилактическую. Текущую дезинфекцию проводят до госпитализации инфекционного больного, в случае оставления его на дому, а также в инфекционных, противотуберкулезных и поликлинических учреждениях. При этом систематически обеззараживают выделения больного, посуду, белье и другие предметы, бывшие в пользовании больного, производят ежедневно влажную уборку помещений с применением дезинфицирующих средств. Текущая дезинфекция сопровождается строгим соблюдением правил личной гигиены больным и ухаживающим персоналом. Наиболее простыми и доступными способами текущей дезинфекции являются кипячение, влажная уборка помещений с применением дезинфицирующих растворов, использование химических дезинфицирующих средств для обеззараживания выделений больного, замачивания белья и т. д.
Дезинфекция — комплекс мероприятий, направленных на уничтожение во внешней среде патогенных микроорганизмов. В широком смысле дезинфекция включает также уничтожение членистоногих — переносчиков инфекций (Дезинсекция) и грызунов — носителей и переносчиков инфекций (Дератизация). Дезинфекция входит в комплекс противоэпидемических и санитарно-профилактических мероприятий. Дезинфекцию подразделяют на текущую, заключительную и профилактическую. Текущую дезинфекцию проводят до госпитализации инфекционного больного, в случае оставления его на дому, а также в инфекционных, противотуберкулезных и поликлинических учреждениях. При этом систематически обеззараживают выделения больного, посуду, белье и другие предметы, бывшие в пользовании больного, производят ежедневно влажную уборку помещений с применением дезинфицирующих средств. Текущая дезинфекция сопровождается строгим соблюдением правил личной гигиены больным и ухаживающим персоналом. Наиболее простыми и доступными способами текущей дезинфекции являются кипячение, влажная уборка помещений с применением дезинфицирующих растворов, использование химических дезинфицирующих средств для обеззараживания выделений больного, замачивания белья и т. д.
 Заключительную дезинфекцию проводят после удаления больного из очага (в случае госпитализации, выздоровления или смерти). Цель заключительной дезинфекции — полное освобождение очага инфекции от возбудителей заболеваний. Заключительная дезинфекция имеет особенно большое эпидемиологическое значение в связи с тем, что многие возбудители инфекций способны длительное время оставаться жизнеспособными на объектах внешней среды. Эффективность заключительной дезинфекции определяется сроками и полнотой ее проведения после удаления больного из очага. Профилактическую дезинфекцию проводят с целью предупредить распространение инфекционных заболеваний преимущественно в местах скопления людей (в детских коллективах, учреждениях общественного питания, медицинских учреждениях). Наиболее распространенными методами профилактической дезинфекции являются: кипячение, своевременная уборка с вывозом мусора и других отходов, хлорирование воды и т. п. К профилактическим мероприятиям относится также борьба с насекомыми и грызунами.
Заключительную дезинфекцию проводят после удаления больного из очага (в случае госпитализации, выздоровления или смерти). Цель заключительной дезинфекции — полное освобождение очага инфекции от возбудителей заболеваний. Заключительная дезинфекция имеет особенно большое эпидемиологическое значение в связи с тем, что многие возбудители инфекций способны длительное время оставаться жизнеспособными на объектах внешней среды. Эффективность заключительной дезинфекции определяется сроками и полнотой ее проведения после удаления больного из очага. Профилактическую дезинфекцию проводят с целью предупредить распространение инфекционных заболеваний преимущественно в местах скопления людей (в детских коллективах, учреждениях общественного питания, медицинских учреждениях). Наиболее распространенными методами профилактической дезинфекции являются: кипячение, своевременная уборка с вывозом мусора и других отходов, хлорирование воды и т. п. К профилактическим мероприятиям относится также борьба с насекомыми и грызунами.
 Цикл обработки изделий медицинского назначения № 9 Страница 54 пособия «Общая микробиология и иммунология»
Цикл обработки изделий медицинского назначения № 9 Страница 54 пособия «Общая микробиология и иммунология»
 Этапы стерилизации: дезинфекция; предстерилизационная очистка (ПСО); стерилизация. Методы стерилизации: термические (паровой, воздушный, глассперленовый); химические (газовый, растворы химических соединений); радиационный; плазменный и озоновый (группа хим. средств) В условиях клиники наиболее распространенными методами стерилизации инструментов и медицинских изделий являются: паровой (автоклавирование), воздушный (сухожаровой шкаф), химический ( газовый, р-рами хим. соединений).
Этапы стерилизации: дезинфекция; предстерилизационная очистка (ПСО); стерилизация. Методы стерилизации: термические (паровой, воздушный, глассперленовый); химические (газовый, растворы химических соединений); радиационный; плазменный и озоновый (группа хим. средств) В условиях клиники наиболее распространенными методами стерилизации инструментов и медицинских изделий являются: паровой (автоклавирование), воздушный (сухожаровой шкаф), химический ( газовый, р-рами хим. соединений).
 Предстерилизационная очистка Предстерилизационной очистке должны подвергаться все изделия перед их стерилизацией с целью удаления белковых, жировых и механических загрязнений, а также лекарственных препаратов. 2. 2. Разъемные изделия должны подвергаться предстерилизационной очистке в разобранном виде.
Предстерилизационная очистка Предстерилизационной очистке должны подвергаться все изделия перед их стерилизацией с целью удаления белковых, жировых и механических загрязнений, а также лекарственных препаратов. 2. 2. Разъемные изделия должны подвергаться предстерилизационной очистке в разобранном виде.
 Стерилизация Стерилизации должны подвергаться все изделия, соприкасающиеся с раневой поверхностью, контактирующие с кровью или инъекционными препаратами, и отдельные виды медицинских инструментов, которые в процессе эксплуатации соприкасаются со слизистой оболочкой и могут вызвать ее повреждения.
Стерилизация Стерилизации должны подвергаться все изделия, соприкасающиеся с раневой поверхностью, контактирующие с кровью или инъекционными препаратами, и отдельные виды медицинских инструментов, которые в процессе эксплуатации соприкасаются со слизистой оболочкой и могут вызвать ее повреждения.
 Дезинфекция Дезинфекции должны подвергаться все изделия, не имеющие контакта с раневой поверхностью, кровью или инъекционными препаратами. Изделия, используемые при проведении гнойных операций или оперативных манипуляций у инфекционного больного, подвергают дезинфекции перед предстерилизационной очисткой и стерилизацией. Кроме того, дезинфекции подлежат изделия медицинского назначения после операций, инъекций и т. п. лицам, перенесшим гепатит В или гепатит с неуточненным диагнозом (вирусный гепатит), а также являющимся носителем НВ-антигена.
Дезинфекция Дезинфекции должны подвергаться все изделия, не имеющие контакта с раневой поверхностью, кровью или инъекционными препаратами. Изделия, используемые при проведении гнойных операций или оперативных манипуляций у инфекционного больного, подвергают дезинфекции перед предстерилизационной очисткой и стерилизацией. Кроме того, дезинфекции подлежат изделия медицинского назначения после операций, инъекций и т. п. лицам, перенесшим гепатит В или гепатит с неуточненным диагнозом (вирусный гепатит), а также являющимся носителем НВ-антигена.
 Способы дезинфекции и стерилизации № 10
Способы дезинфекции и стерилизации № 10
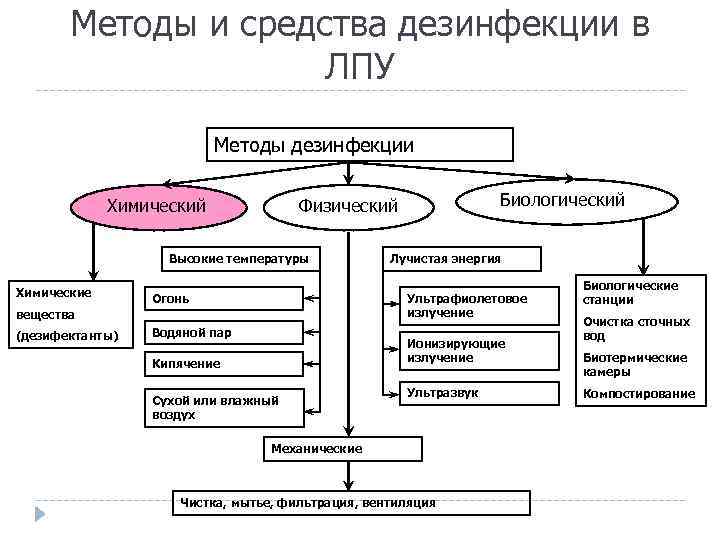 Методы и средства дезинфекции в ЛПУ Методы дезинфекции Химический Высокие температуры Химические Огонь Лучистая энергия Ультрафиолетовое излучение вещества (дезифектанты) Биологический Физический Водяной пар Ионизирующие излучение Кипячение Сухой или влажный воздух Ультразвук Механические Чистка, мытье, фильтрация, вентиляция Биологические станции Очистка сточных вод Биотермические камеры Компостирование
Методы и средства дезинфекции в ЛПУ Методы дезинфекции Химический Высокие температуры Химические Огонь Лучистая энергия Ультрафиолетовое излучение вещества (дезифектанты) Биологический Физический Водяной пар Ионизирующие излучение Кипячение Сухой или влажный воздух Ультразвук Механические Чистка, мытье, фильтрация, вентиляция Биологические станции Очистка сточных вод Биотермические камеры Компостирование
 Типы дезинфицирующих средств (по химическому составу) Хлоросодержащие препараты Препараты на основе фенола Кислородсодержащие препараты Спиртсодержащие препараты Альдегидсодержащие препараты Препараты на основе ЧАС (ПАВ) Препараты, содержащие гуанидин
Типы дезинфицирующих средств (по химическому составу) Хлоросодержащие препараты Препараты на основе фенола Кислородсодержащие препараты Спиртсодержащие препараты Альдегидсодержащие препараты Препараты на основе ЧАС (ПАВ) Препараты, содержащие гуанидин
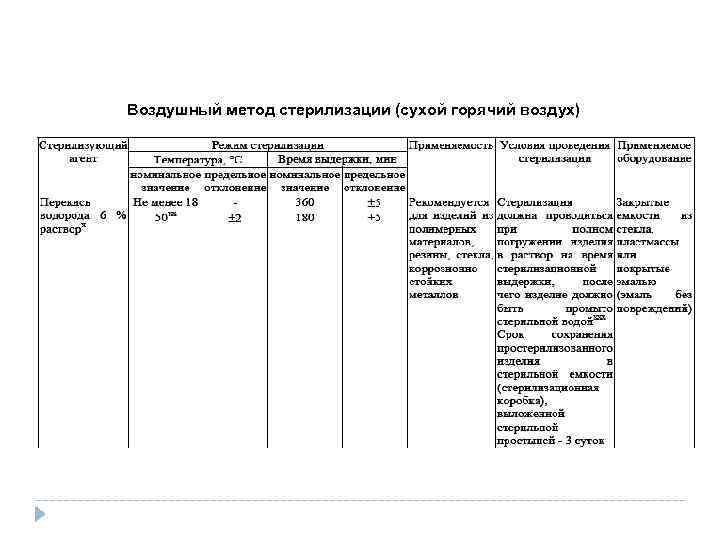 Воздушный метод стерилизации (сухой горячий воздух)
Воздушный метод стерилизации (сухой горячий воздух)
 Химический метод стерилизации (растворы химических препаратов)
Химический метод стерилизации (растворы химических препаратов)
 • . Методы стерилизации: • стерилизация паром под давлением, • текущим паром, • сухим жаром, • ионизирующее и ультрафиолетовое облучение, • холодная стерилизация.
• . Методы стерилизации: • стерилизация паром под давлением, • текущим паром, • сухим жаром, • ионизирующее и ультрафиолетовое облучение, • холодная стерилизация.
 Стерилизация кипячением в течение 30 мин убивает вегетативные формы микробов. Споры многих бактерий при этом сохраняются, выдерживая кипячение в течение нескольких часов. Для уничтожения вирусов — возбудителей болезни Боткина необходимо кипячение в течение 45— 60 мин. Кипячению в специальных стерилизаторах подвергают шприцы, хирургические инструменты, иглы, резиновые трубки. Для повышения точки кипения и устранения жесткости воды добавляют 2% гидрокарбоната натрия. Стерилизация насыщенным паром под давлением (автоклавирование) является наиболее надежным и быстрым методом стерилизации. Обеспложивание достигается воздействием пара, температура которого под давлением выше, чем температура кипящей воды: при давлении 0, 5 атм 112°С, при 1 атм. 121 °С , при 1, 5 атм 127°С и при 2 атм 134°С. автоклав
Стерилизация кипячением в течение 30 мин убивает вегетативные формы микробов. Споры многих бактерий при этом сохраняются, выдерживая кипячение в течение нескольких часов. Для уничтожения вирусов — возбудителей болезни Боткина необходимо кипячение в течение 45— 60 мин. Кипячению в специальных стерилизаторах подвергают шприцы, хирургические инструменты, иглы, резиновые трубки. Для повышения точки кипения и устранения жесткости воды добавляют 2% гидрокарбоната натрия. Стерилизация насыщенным паром под давлением (автоклавирование) является наиболее надежным и быстрым методом стерилизации. Обеспложивание достигается воздействием пара, температура которого под давлением выше, чем температура кипящей воды: при давлении 0, 5 атм 112°С, при 1 атм. 121 °С , при 1, 5 атм 127°С и при 2 атм 134°С. автоклав
 При давлении 2 атм обеззараживают инфицированный материал и отработанные культуры микробов. Стерилизация в автоклаве таких веществ, как вазелин, масло, песок, малоэффективна вследствие того, что в них пар проникает плохо или совсем не проникает. Некоторые питательные среды (например, содержащие сахара) нельзя стерилизовать паром под давлением, так как они карамелизуются, поэтому их подвергают дробной стерилизации текучим паром. Стерилизация текучим паром проводится в аппарате Коха или в автоклаве при не завинченной крышке и открытом выпускном кране. На дно аппарата Коха наливают воду и нагревают до 100°С. Образующийся пар движется вверх через заложенный материал и стерилизует его. Так как однократное действие паров воды не убивает споры, применяют дробную стерилизацию — 3 дня подряд по 30 мин. Споры, не погибшие при первом прогревании, прорастают до следующего дня в вегетативные формы и погибают при втором и третьем прогревания. Для веществ, разрушающихся при 100°С (например, жидкости содержащие белок), применяют другой вид дробной стерилизации — тиндализацию. Стерилизуемое вещество прогревают на водяной бане по 1 ч при 56— 60°С в течение 5— 6 дней. Для освобождения от вегетативных форм микробов прибегают к пастеризации — однократному прогреванию при 70°С в течение 30 мин с последующим быстрым охлаждением и хранением на холоду, чтобы не проросли споры. Этот метод применяют для обеззараживания и сохранения молока.
При давлении 2 атм обеззараживают инфицированный материал и отработанные культуры микробов. Стерилизация в автоклаве таких веществ, как вазелин, масло, песок, малоэффективна вследствие того, что в них пар проникает плохо или совсем не проникает. Некоторые питательные среды (например, содержащие сахара) нельзя стерилизовать паром под давлением, так как они карамелизуются, поэтому их подвергают дробной стерилизации текучим паром. Стерилизация текучим паром проводится в аппарате Коха или в автоклаве при не завинченной крышке и открытом выпускном кране. На дно аппарата Коха наливают воду и нагревают до 100°С. Образующийся пар движется вверх через заложенный материал и стерилизует его. Так как однократное действие паров воды не убивает споры, применяют дробную стерилизацию — 3 дня подряд по 30 мин. Споры, не погибшие при первом прогревании, прорастают до следующего дня в вегетативные формы и погибают при втором и третьем прогревания. Для веществ, разрушающихся при 100°С (например, жидкости содержащие белок), применяют другой вид дробной стерилизации — тиндализацию. Стерилизуемое вещество прогревают на водяной бане по 1 ч при 56— 60°С в течение 5— 6 дней. Для освобождения от вегетативных форм микробов прибегают к пастеризации — однократному прогреванию при 70°С в течение 30 мин с последующим быстрым охлаждением и хранением на холоду, чтобы не проросли споры. Этот метод применяют для обеззараживания и сохранения молока.
 Сухожаровой шкаф
Сухожаровой шкаф
 Химическая стерилизация применяется в том случае, если объекты нельзя автоклавировать. Обычно это питательные среды, содержащие термолабильные вещества. Химическое вещество должно быть не только токсичным, но и летучим для быстрого исчезновения из простерилизованного объекта. Наилучшим является окись этилена — жидкость кипящая при 10, 7°С. Окись этилена в жидком виде добавляют в раствор при температуре от 0 до 4°С в конечной концентрации 0, 5— 1%. При температуре выше точки кипения окись этилена используют как стерилизующий газ, для стерилизации сложной медицинской аппаратуры. Окись этилена губительно действует на вегетативные и споровые формы бактерий. Ее используют в промышленности для стерилизации пластмассовых чашек Петри и других предметов, которые плавятся при температуре выше 100°С. Применение окиси этилена ограничено, так как вещество токсично, нестойко, взрывоопасно.
Химическая стерилизация применяется в том случае, если объекты нельзя автоклавировать. Обычно это питательные среды, содержащие термолабильные вещества. Химическое вещество должно быть не только токсичным, но и летучим для быстрого исчезновения из простерилизованного объекта. Наилучшим является окись этилена — жидкость кипящая при 10, 7°С. Окись этилена в жидком виде добавляют в раствор при температуре от 0 до 4°С в конечной концентрации 0, 5— 1%. При температуре выше точки кипения окись этилена используют как стерилизующий газ, для стерилизации сложной медицинской аппаратуры. Окись этилена губительно действует на вегетативные и споровые формы бактерий. Ее используют в промышленности для стерилизации пластмассовых чашек Петри и других предметов, которые плавятся при температуре выше 100°С. Применение окиси этилена ограничено, так как вещество токсично, нестойко, взрывоопасно.
 Контроль качества дезинфекции № 11
Контроль качества дезинфекции № 11
 Смыв c помощью контактных пластин
Смыв c помощью контактных пластин
 Контроль стерилизации и контроль стерильности № 12 Страница 51 -52 пособия «Общая микробиология и иммунология»
Контроль стерилизации и контроль стерильности № 12 Страница 51 -52 пособия «Общая микробиология и иммунология»
 Контроли стерилизации. Химические индикаторы. После окончания процесса, отчётливые изменения цвета индикаторов показывают, были ли достигнуты требуемые условия процесса в месте нахождения индикатора В основе биологического метода контроля процесса стерилизации лежит гибель определенного числа тестовых, устойчивых к воздействию стерилизующего реагента микроор микропроцессорный контроль температуры и давления; 4 предустановленные программы: 3 — для стерилизации, 1 — для сушки; диапазон температур, °C — 100 — 134; принтер для документирования процесса стерилизации (опция);
Контроли стерилизации. Химические индикаторы. После окончания процесса, отчётливые изменения цвета индикаторов показывают, были ли достигнуты требуемые условия процесса в месте нахождения индикатора В основе биологического метода контроля процесса стерилизации лежит гибель определенного числа тестовых, устойчивых к воздействию стерилизующего реагента микроор микропроцессорный контроль температуры и давления; 4 предустановленные программы: 3 — для стерилизации, 1 — для сушки; диапазон температур, °C — 100 — 134; принтер для документирования процесса стерилизации (опция);
 Контроль стерильности Тиогликолевая среда 32 °С бульон Сабуро 20 - 22 °С 14 суток при контроле изделий, простерилизованных растворами химических средств и газовым методом, в течение 7 суток - простерилизованных физическими методами
Контроль стерильности Тиогликолевая среда 32 °С бульон Сабуро 20 - 22 °С 14 суток при контроле изделий, простерилизованных растворами химических средств и газовым методом, в течение 7 суток - простерилизованных физическими методами


