ДЫХАНИЕ.ppt
- Количество слайдов: 34
 ДЫХАНИЕ Дыхание – окислительный распад сложных органических веществ до простейших конечных продуктов – CO 2 и H 2 O, катализирующийся ферментами и сопровождающийся выделением энергии. Значительная часть энергии фиксируется в макроэргических фосфатных связях АТФ и используется на различные жизненные процессы растений. В связи с этим процесс дыхания называют окислительным фосфорилированием.
ДЫХАНИЕ Дыхание – окислительный распад сложных органических веществ до простейших конечных продуктов – CO 2 и H 2 O, катализирующийся ферментами и сопровождающийся выделением энергии. Значительная часть энергии фиксируется в макроэргических фосфатных связях АТФ и используется на различные жизненные процессы растений. В связи с этим процесс дыхания называют окислительным фосфорилированием.
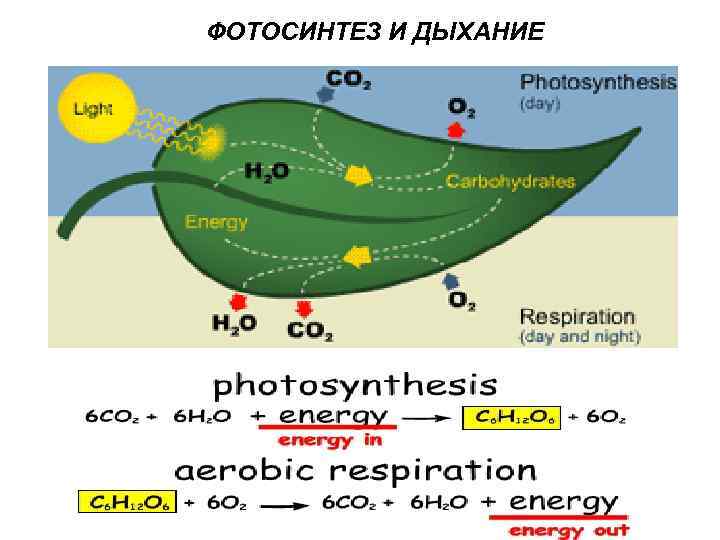 ФОТОСИНТЕЗ И ДЫХАНИЕ
ФОТОСИНТЕЗ И ДЫХАНИЕ
 C 6 H 12 O 6 + 6 O 2 = 6 CO 2 + 6 H 2 O + 38 ATФ ГОРЕНИЕ ДЫХАНИЕ Энергия выделяется в виде тепла молекул АТФ Скорость реакции более высокая медленная Катализатор реакции Катализаторы реакции O 2 ферменты Температура высокая Оптимальная температура 40 °С, max 50°С ! В живых системах не происходит прямого соединения веществ с кислородом !
C 6 H 12 O 6 + 6 O 2 = 6 CO 2 + 6 H 2 O + 38 ATФ ГОРЕНИЕ ДЫХАНИЕ Энергия выделяется в виде тепла молекул АТФ Скорость реакции более высокая медленная Катализатор реакции Катализаторы реакции O 2 ферменты Температура высокая Оптимальная температура 40 °С, max 50°С ! В живых системах не происходит прямого соединения веществ с кислородом !
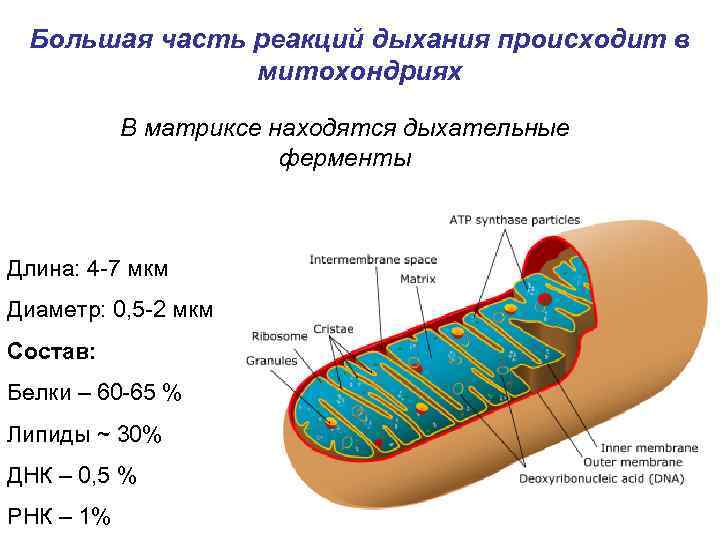 Большая часть реакций дыхания происходит в митохондриях В матриксе находятся дыхательные ферменты Длина: 4 -7 мкм Диаметр: 0, 5 -2 мкм Состав: Белки – 60 -65 % Липиды ~ 30% ДНК – 0, 5 % РНК – 1%
Большая часть реакций дыхания происходит в митохондриях В матриксе находятся дыхательные ферменты Длина: 4 -7 мкм Диаметр: 0, 5 -2 мкм Состав: Белки – 60 -65 % Липиды ~ 30% ДНК – 0, 5 % РНК – 1%
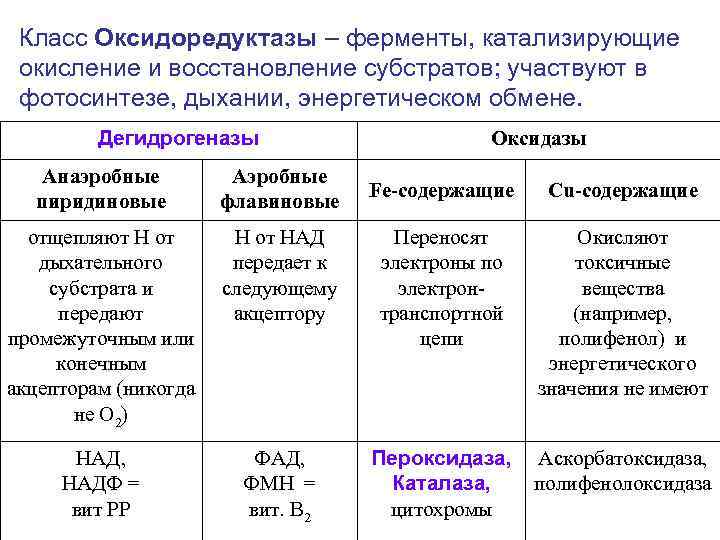 Класс Оксидоредуктазы – ферменты, катализирующие окисление и восстановление субстратов; участвуют в фотосинтезе, дыхании, энергетическом обмене. Дегидрогеназы Оксидазы Анаэробные Аэробные Fe-содержащие Cu-содержащие пиридиновые флавиновые отщепляют H от Н от НАД Переносят Окисляют дыхательного передает к электроны по токсичные субстрата и следующему электрон- вещества передают акцептору транспортной (например, промежуточным или цепи полифенол) и конечным энергетического акцепторам (никогда значения не имеют не О 2) НАД, ФАД, Пероксидаза, Аскорбатоксидаза, НАДФ = ФМН = Каталаза, полифенолоксидаза вит PP вит. В 2 цитохромы
Класс Оксидоредуктазы – ферменты, катализирующие окисление и восстановление субстратов; участвуют в фотосинтезе, дыхании, энергетическом обмене. Дегидрогеназы Оксидазы Анаэробные Аэробные Fe-содержащие Cu-содержащие пиридиновые флавиновые отщепляют H от Н от НАД Переносят Окисляют дыхательного передает к электроны по токсичные субстрата и следующему электрон- вещества передают акцептору транспортной (например, промежуточным или цепи полифенол) и конечным энергетического акцепторам (никогда значения не имеют не О 2) НАД, ФАД, Пероксидаза, Аскорбатоксидаза, НАДФ = ФМН = Каталаза, полифенолоксидаза вит PP вит. В 2 цитохромы
 ЭТАПЫ ДЫХАНИЯ 1 ЭТАП: в процессе распада органических веществ происходит синтез АТФ (субстратное фосфорилирование) и восстановление коферментов: НАД, ФАД, НАДФ. Распад дыхательного субстрата происходит в анаэробных условиях, циклы Кребса, пентозофосфатный и глиоксилатный осуществляются только в аэробных условиях. 2 ЭТАП: восстановленные коферменты могут → окисляться с помощью атмосферного кислорода с образованием воды и одновременным синтезом АТФ или → служить донорами Н для восстановительных процессов, протекающих в клетке.
ЭТАПЫ ДЫХАНИЯ 1 ЭТАП: в процессе распада органических веществ происходит синтез АТФ (субстратное фосфорилирование) и восстановление коферментов: НАД, ФАД, НАДФ. Распад дыхательного субстрата происходит в анаэробных условиях, циклы Кребса, пентозофосфатный и глиоксилатный осуществляются только в аэробных условиях. 2 ЭТАП: восстановленные коферменты могут → окисляться с помощью атмосферного кислорода с образованием воды и одновременным синтезом АТФ или → служить донорами Н для восстановительных процессов, протекающих в клетке.
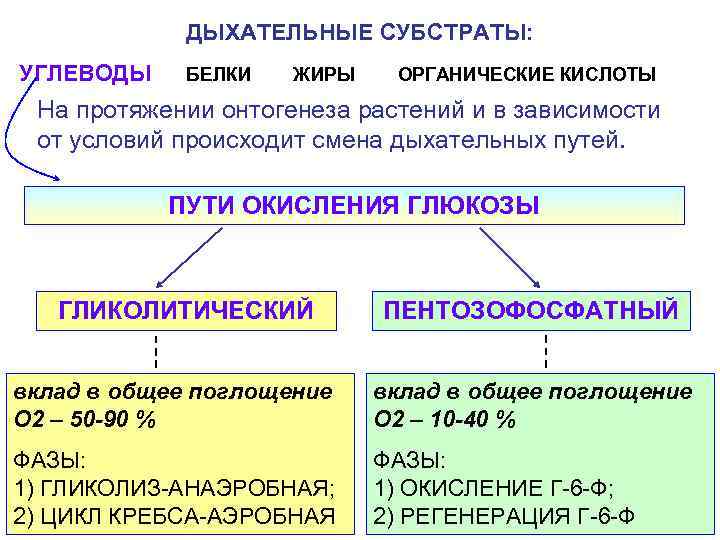 ДЫХАТЕЛЬНЫЕ СУБСТРАТЫ: УГЛЕВОДЫ БЕЛКИ ЖИРЫ ОРГАНИЧЕСКИЕ КИСЛОТЫ На протяжении онтогенеза растений и в зависимости от условий происходит смена дыхательных путей. ПУТИ ОКИСЛЕНИЯ ГЛЮКОЗЫ ГЛИКОЛИТИЧЕСКИЙ ПЕНТОЗОФОСФАТНЫЙ вклад в общее поглощение O 2 – 50 -90 % O 2 – 10 -40 % ФАЗЫ: ФАЗЫ: 1) ГЛИКОЛИЗ-АНАЭРОБНАЯ; 1) ОКИСЛЕНИЕ Г-6 -Ф; 2) ЦИКЛ КРЕБСА-АЭРОБНАЯ 2) РЕГЕНЕРАЦИЯ Г-6 -Ф
ДЫХАТЕЛЬНЫЕ СУБСТРАТЫ: УГЛЕВОДЫ БЕЛКИ ЖИРЫ ОРГАНИЧЕСКИЕ КИСЛОТЫ На протяжении онтогенеза растений и в зависимости от условий происходит смена дыхательных путей. ПУТИ ОКИСЛЕНИЯ ГЛЮКОЗЫ ГЛИКОЛИТИЧЕСКИЙ ПЕНТОЗОФОСФАТНЫЙ вклад в общее поглощение O 2 – 50 -90 % O 2 – 10 -40 % ФАЗЫ: ФАЗЫ: 1) ГЛИКОЛИЗ-АНАЭРОБНАЯ; 1) ОКИСЛЕНИЕ Г-6 -Ф; 2) ЦИКЛ КРЕБСА-АЭРОБНАЯ 2) РЕГЕНЕРАЦИЯ Г-6 -Ф
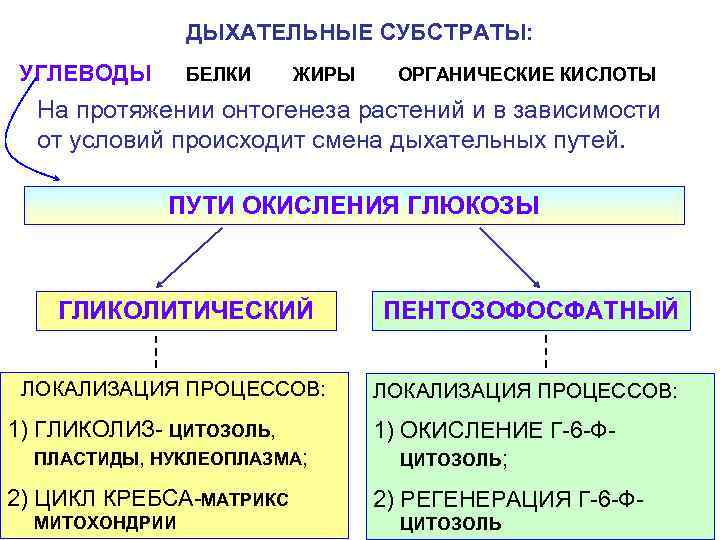 ДЫХАТЕЛЬНЫЕ СУБСТРАТЫ: УГЛЕВОДЫ БЕЛКИ ЖИРЫ ОРГАНИЧЕСКИЕ КИСЛОТЫ На протяжении онтогенеза растений и в зависимости от условий происходит смена дыхательных путей. ПУТИ ОКИСЛЕНИЯ ГЛЮКОЗЫ ГЛИКОЛИТИЧЕСКИЙ ПЕНТОЗОФОСФАТНЫЙ ЛОКАЛИЗАЦИЯ ПРОЦЕССОВ: 1) ГЛИКОЛИЗ- ЦИТОЗОЛЬ, 1) ОКИСЛЕНИЕ Г-6 -Ф- ПЛАСТИДЫ, НУКЛЕОПЛАЗМА; ЦИТОЗОЛЬ; 2) ЦИКЛ КРЕБСА-МАТРИКС 2) РЕГЕНЕРАЦИЯ Г-6 -Ф- МИТОХОНДРИИ ЦИТОЗОЛЬ
ДЫХАТЕЛЬНЫЕ СУБСТРАТЫ: УГЛЕВОДЫ БЕЛКИ ЖИРЫ ОРГАНИЧЕСКИЕ КИСЛОТЫ На протяжении онтогенеза растений и в зависимости от условий происходит смена дыхательных путей. ПУТИ ОКИСЛЕНИЯ ГЛЮКОЗЫ ГЛИКОЛИТИЧЕСКИЙ ПЕНТОЗОФОСФАТНЫЙ ЛОКАЛИЗАЦИЯ ПРОЦЕССОВ: 1) ГЛИКОЛИЗ- ЦИТОЗОЛЬ, 1) ОКИСЛЕНИЕ Г-6 -Ф- ПЛАСТИДЫ, НУКЛЕОПЛАЗМА; ЦИТОЗОЛЬ; 2) ЦИКЛ КРЕБСА-МАТРИКС 2) РЕГЕНЕРАЦИЯ Г-6 -Ф- МИТОХОНДРИИ ЦИТОЗОЛЬ
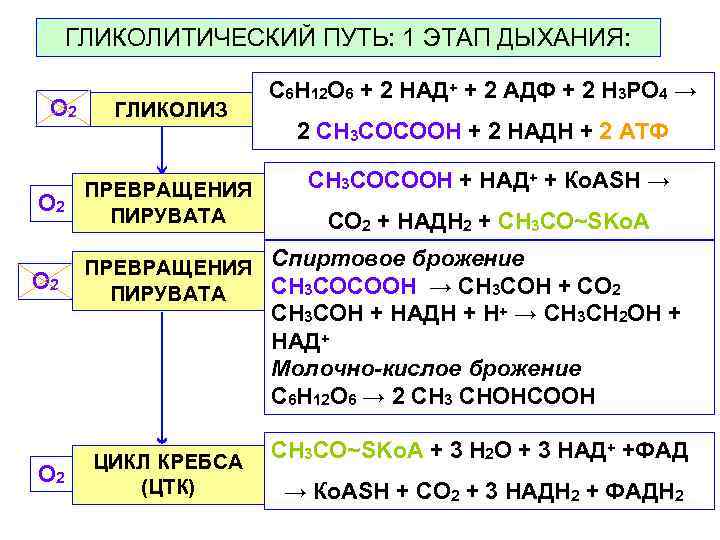 ГЛИКОЛИТИЧЕСКИЙ ПУТЬ: 1 ЭТАП ДЫХАНИЯ: C 6 H 12 O 6 + 2 НАД+ + 2 АДФ + 2 H 3 PO 4 → O 2 ГЛИКОЛИЗ 2 CH 3 COCOOH + 2 HAДH + 2 АТФ ПРЕВРАЩЕНИЯ CH 3 COCOOH + НАД+ + Кo. ASH → O 2 ПИРУВАТА CO 2 + HAДH 2 + CH 3 CO~SKo. A ПРЕВРАЩЕНИЯ Спиртовое брожение O 2 ПИРУВАТА CH 3 COCOOH → CH 3 COH + CO 2 CH 3 COH + HAДН + Н+ → CH 3 CН 2 OH + НАД+ Молочно-кислое брожение C 6 H 12 O 6 → 2 CH 3 СНОНСООH ЦИКЛ КРЕБСА CH 3 CO~SKo. A + 3 H 2 O + 3 НАД+ +ФАД O 2 (ЦТК) → Кo. ASH + CO 2 + 3 HAДH 2 + ФАДH 2
ГЛИКОЛИТИЧЕСКИЙ ПУТЬ: 1 ЭТАП ДЫХАНИЯ: C 6 H 12 O 6 + 2 НАД+ + 2 АДФ + 2 H 3 PO 4 → O 2 ГЛИКОЛИЗ 2 CH 3 COCOOH + 2 HAДH + 2 АТФ ПРЕВРАЩЕНИЯ CH 3 COCOOH + НАД+ + Кo. ASH → O 2 ПИРУВАТА CO 2 + HAДH 2 + CH 3 CO~SKo. A ПРЕВРАЩЕНИЯ Спиртовое брожение O 2 ПИРУВАТА CH 3 COCOOH → CH 3 COH + CO 2 CH 3 COH + HAДН + Н+ → CH 3 CН 2 OH + НАД+ Молочно-кислое брожение C 6 H 12 O 6 → 2 CH 3 СНОНСООH ЦИКЛ КРЕБСА CH 3 CO~SKo. A + 3 H 2 O + 3 НАД+ +ФАД O 2 (ЦТК) → Кo. ASH + CO 2 + 3 HAДH 2 + ФАДH 2
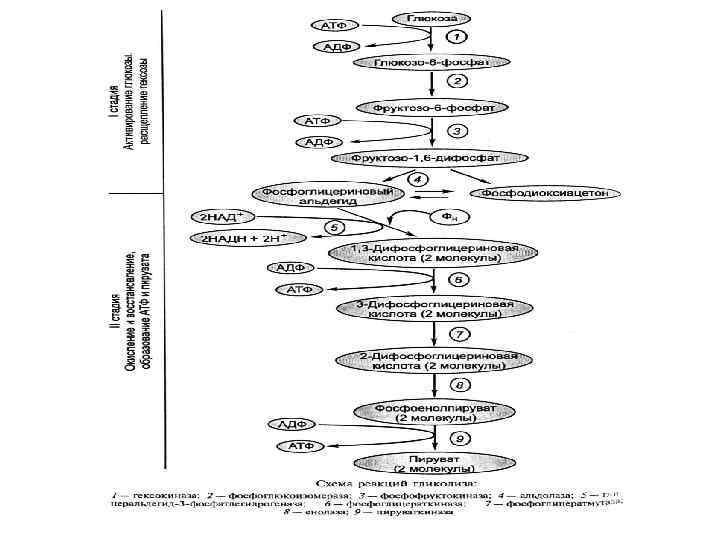
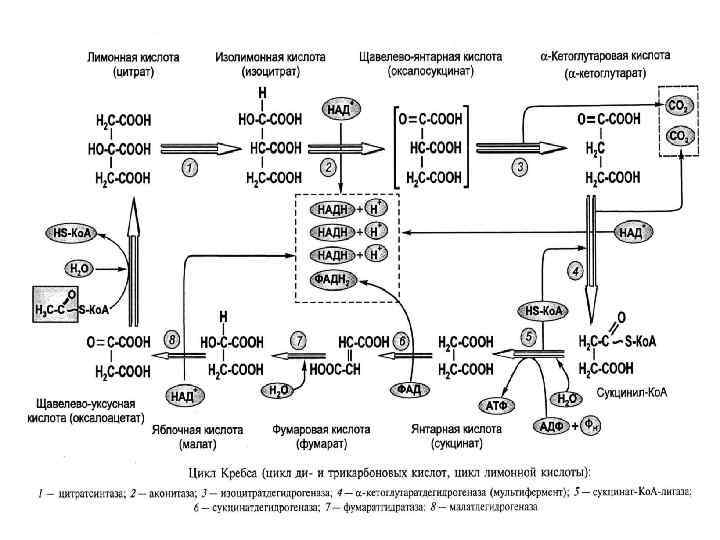
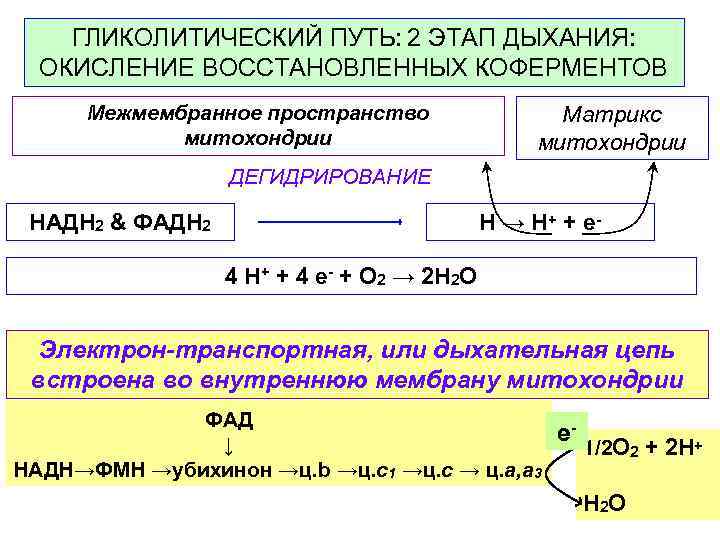 ГЛИКОЛИТИЧЕСКИЙ ПУТЬ: 2 ЭТАП ДЫХАНИЯ: ОКИСЛЕНИЕ ВОССТАНОВЛЕННЫХ КОФЕРМЕНТОВ Межмембранное пространство Матрикс митохондрии ДЕГИДРИРОВАНИЕ HAДH 2 & ФАДH 2 Н → Н+ + е - 4 Н+ + 4 e- + O 2 → 2 Н 2 O Электрон-транспортная, или дыхательная цепь встроена во внутреннюю мембрану митохондрии ФАД ↓ e- 1/2 О 2 + 2 Н+ НАДН→ФМН →убихинон →ц. b →ц. с1 →ц. с → ц. а, а 3 Н 2 О
ГЛИКОЛИТИЧЕСКИЙ ПУТЬ: 2 ЭТАП ДЫХАНИЯ: ОКИСЛЕНИЕ ВОССТАНОВЛЕННЫХ КОФЕРМЕНТОВ Межмембранное пространство Матрикс митохондрии ДЕГИДРИРОВАНИЕ HAДH 2 & ФАДH 2 Н → Н+ + е - 4 Н+ + 4 e- + O 2 → 2 Н 2 O Электрон-транспортная, или дыхательная цепь встроена во внутреннюю мембрану митохондрии ФАД ↓ e- 1/2 О 2 + 2 Н+ НАДН→ФМН →убихинон →ц. b →ц. с1 →ц. с → ц. а, а 3 Н 2 О
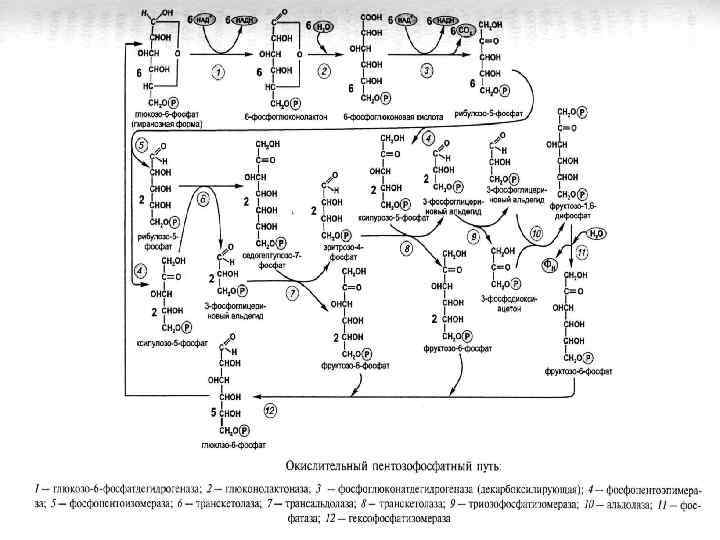
 ПЕНТОЗОФОСФАТНЫЙ ПУТЬ: 1 ФАЗА: ОКИСЛЕНИЕ ГЛЮКОЗО-6 -ФОСФАТА ЗАКАНЧИВАЕТСЯ ОБРАЗОВАНИЕМ РИБУЛОЗО-5 -ФОСФАТА ПЕНТОЗОФОСФАТНЫЙ ПУТЬ: 2 ФАЗА: РЕГЕНЕРАЦИЯ ГЛЮКОЗО-6 -ФОСФАТА СУММАРНОЕ УРАВНЕНИЕ: 6 Г-6 -Ф + 12 НАДФ + 7 H 2 O → 5 Г-6 -Ф + 6 CO 2 + 12 НАДФН + 12 Н+ + Н 3 PO 4
ПЕНТОЗОФОСФАТНЫЙ ПУТЬ: 1 ФАЗА: ОКИСЛЕНИЕ ГЛЮКОЗО-6 -ФОСФАТА ЗАКАНЧИВАЕТСЯ ОБРАЗОВАНИЕМ РИБУЛОЗО-5 -ФОСФАТА ПЕНТОЗОФОСФАТНЫЙ ПУТЬ: 2 ФАЗА: РЕГЕНЕРАЦИЯ ГЛЮКОЗО-6 -ФОСФАТА СУММАРНОЕ УРАВНЕНИЕ: 6 Г-6 -Ф + 12 НАДФ + 7 H 2 O → 5 Г-6 -Ф + 6 CO 2 + 12 НАДФН + 12 Н+ + Н 3 PO 4
 ДЫХАНИЕ ФОТОСИНТЕЗ С 3 -путь = окислительный цикл Кальвина = пентозофосфатный восстановительный цикл пентозофосфатный цикл (ВПФ-цикл) УЧАСТВУЮТ ОДНИ И ТЕ ЖЕ ФОСФОРНЫЕ ЭФИРЫ САХАРОВ ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ ОДНОГО ЦИКЛА МОГУТ ИСПОЛЬЗОВАТЬСЯ В СЛУЧАЕ НЕОБХОДИМОСТИ В РЕАКЦИЯХ ДРУГОГО ЦИКЛ НЕОБЯЗАТЕЛЬНО ДОЛЖЕН ИДТИ ДО КОНЦА, ВОЗМОЖНЫ ПЕРЕХОДЫ ИЗ ОДНОГО В ДРУГОЙ
ДЫХАНИЕ ФОТОСИНТЕЗ С 3 -путь = окислительный цикл Кальвина = пентозофосфатный восстановительный цикл пентозофосфатный цикл (ВПФ-цикл) УЧАСТВУЮТ ОДНИ И ТЕ ЖЕ ФОСФОРНЫЕ ЭФИРЫ САХАРОВ ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ ОДНОГО ЦИКЛА МОГУТ ИСПОЛЬЗОВАТЬСЯ В СЛУЧАЕ НЕОБХОДИМОСТИ В РЕАКЦИЯХ ДРУГОГО ЦИКЛ НЕОБЯЗАТЕЛЬНО ДОЛЖЕН ИДТИ ДО КОНЦА, ВОЗМОЖНЫ ПЕРЕХОДЫ ИЗ ОДНОГО В ДРУГОЙ
 ФИЗИОЛОГИЧЕСКОЕ ЗНАЧЕНИЕ ПЕНТОЗОФОСФАТНОГО ЦИКЛА ДЫХАНИЯ 1) Снабжает клетки НАДФН – донором H+ для синтеза жирных кислот, восстановительного аминирования и др. 2) Промежуточные вещества цикла – пентозы – используются для синтеза АТФ, АДФ, АМФ, нуклеиновых кислот, пиридиновых ферментов, веществ клеточной стенки и др. 3) Эритрозо-4 -фосфат участвует в образовании шикимата, необходимого для синтеза гормонов. 4) ФГА может включиться в гликолиз, превратиться в пируват и далее участвовать в цикле Кребса.
ФИЗИОЛОГИЧЕСКОЕ ЗНАЧЕНИЕ ПЕНТОЗОФОСФАТНОГО ЦИКЛА ДЫХАНИЯ 1) Снабжает клетки НАДФН – донором H+ для синтеза жирных кислот, восстановительного аминирования и др. 2) Промежуточные вещества цикла – пентозы – используются для синтеза АТФ, АДФ, АМФ, нуклеиновых кислот, пиридиновых ферментов, веществ клеточной стенки и др. 3) Эритрозо-4 -фосфат участвует в образовании шикимата, необходимого для синтеза гормонов. 4) ФГА может включиться в гликолиз, превратиться в пируват и далее участвовать в цикле Кребса.
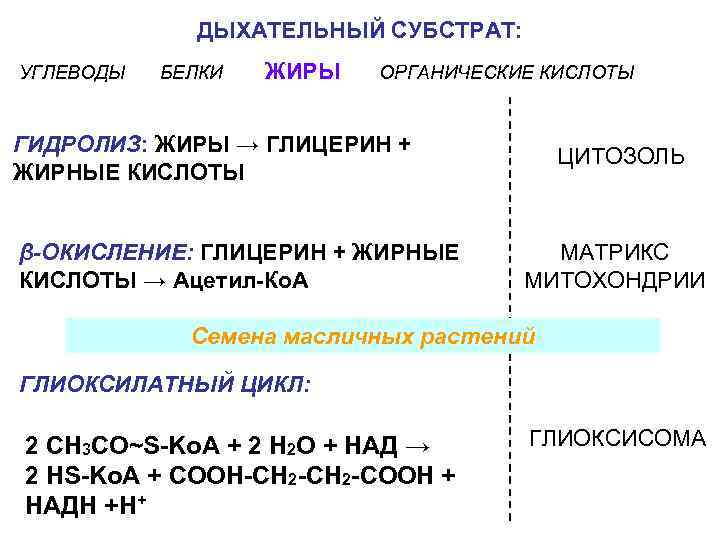 ДЫХАТЕЛЬНЫЙ СУБСТРАТ: УГЛЕВОДЫ БЕЛКИ ЖИРЫ ОРГАНИЧЕСКИЕ КИСЛОТЫ ГИДРОЛИЗ: ЖИРЫ → ГЛИЦЕРИН + ЦИТОЗОЛЬ ЖИРНЫЕ КИСЛОТЫ β-ОКИСЛЕНИЕ: ГЛИЦЕРИН + ЖИРНЫЕ МАТРИКС КИСЛОТЫ → Ацетил-Ко. А МИТОХОНДРИИ Семена масличных растений ГЛИОКСИЛАТНЫЙ ЦИКЛ: 2 CH 3 CO~S-Ko. A + 2 H 2 O + HAД → ГЛИОКСИСОМА 2 HS-Ko. A + COOH-CH 2 -COOH + HAДH +H+
ДЫХАТЕЛЬНЫЙ СУБСТРАТ: УГЛЕВОДЫ БЕЛКИ ЖИРЫ ОРГАНИЧЕСКИЕ КИСЛОТЫ ГИДРОЛИЗ: ЖИРЫ → ГЛИЦЕРИН + ЦИТОЗОЛЬ ЖИРНЫЕ КИСЛОТЫ β-ОКИСЛЕНИЕ: ГЛИЦЕРИН + ЖИРНЫЕ МАТРИКС КИСЛОТЫ → Ацетил-Ко. А МИТОХОНДРИИ Семена масличных растений ГЛИОКСИЛАТНЫЙ ЦИКЛ: 2 CH 3 CO~S-Ko. A + 2 H 2 O + HAД → ГЛИОКСИСОМА 2 HS-Ko. A + COOH-CH 2 -COOH + HAДH +H+
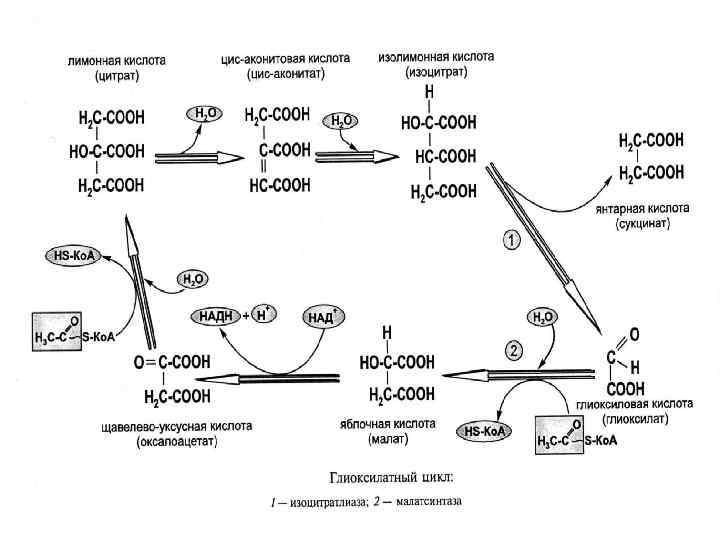 ГЛИОКСИЛАТНЫЙ ЦИКЛ
ГЛИОКСИЛАТНЫЙ ЦИКЛ
 ДЫХАТЕЛЬНЫЙ СУБСТРАТ: УГЛЕВОДЫ БЕЛКИ ЖИРЫ ОРГАНИЧЕСКИЕ КИСЛОТЫ ГИДРОЛИЗ: БЕЛКИ → АМИНОКИСЛОТЫ ДЕЗАМИНИРОВАНИЕ АМИНОКИСЛОТ ЦИКЛ КРЕБСА
ДЫХАТЕЛЬНЫЙ СУБСТРАТ: УГЛЕВОДЫ БЕЛКИ ЖИРЫ ОРГАНИЧЕСКИЕ КИСЛОТЫ ГИДРОЛИЗ: БЕЛКИ → АМИНОКИСЛОТЫ ДЕЗАМИНИРОВАНИЕ АМИНОКИСЛОТ ЦИКЛ КРЕБСА
 Методы, с помощью которых можно установить соотношение путей дыхательного обмена: применение специфических ингибиторов, метод с использованием меченых атомов и др.
Методы, с помощью которых можно установить соотношение путей дыхательного обмена: применение специфических ингибиторов, метод с использованием меченых атомов и др.
 ЛАБОРАТОРНЫЙ ПРАКТИКУМ Работа #48: Обнаружение дегидрогеназ в растении по восстановлению динитробензола Работа #50: Обнаружение пероксидазы в соке клубня картофеля Работа #52: Определение активности каталазы в растительных объектах
ЛАБОРАТОРНЫЙ ПРАКТИКУМ Работа #48: Обнаружение дегидрогеназ в растении по восстановлению динитробензола Работа #50: Обнаружение пероксидазы в соке клубня картофеля Работа #52: Определение активности каталазы в растительных объектах
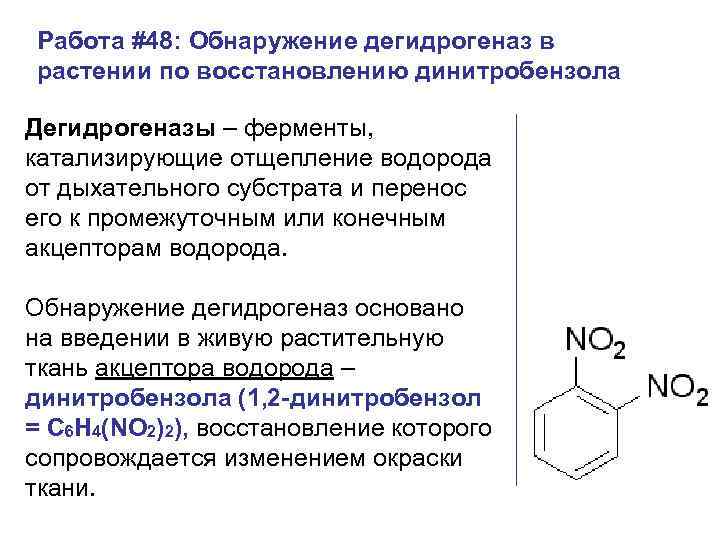 Работа #48: Обнаружение дегидрогеназ в растении по восстановлению динитробензола Дегидрогеназы – ферменты, катализирующие отщепление водорода от дыхательного субстрата и перенос его к промежуточным или конечным акцепторам водорода. Обнаружение дегидрогеназ основано на введении в живую растительную ткань акцептора водорода – динитробензола (1, 2 -динитробензол = C 6 H 4(NO 2)2), восстановление которого сопровождается изменением окраски ткани.
Работа #48: Обнаружение дегидрогеназ в растении по восстановлению динитробензола Дегидрогеназы – ферменты, катализирующие отщепление водорода от дыхательного субстрата и перенос его к промежуточным или конечным акцепторам водорода. Обнаружение дегидрогеназ основано на введении в живую растительную ткань акцептора водорода – динитробензола (1, 2 -динитробензол = C 6 H 4(NO 2)2), восстановление которого сопровождается изменением окраски ткани.
 При недостатке кислорода бесцветный орто- и парадинитробензол, присоединяя водород от восстановленных дегидрогеназ, необратимо восстанавливается в дышащих тканях в желтый орто- и пара-нитрофенилгидроксиламин и далее в орто- и паранитроанилин также желтого цвета. Орто- и паранитрофенилгидроксиламин дают в щелочной среде соответственно фиолетовое и красное окрашивание, а вместе – пурпурное. ЧРЕЗВЫЧАЙНО ТОКСИЧЕН, ИМЕЕТ НИЗКУЮ ЛЕТАЛЬНУЮ ДОЗУ! ОПАСЕН ДЛЯ ОКРУЖАЮЩЕЙ СРЕДЫ, ДАННЫЙ ВИД ВЕЩЕСТВ КАТЕГОРИЧЕСКИ ЗАПРЕЩАЕТСЯ УТИЛИЗИРОВАТЬ В ОБЩУЮ КАНАЛИЗАЦИЮ
При недостатке кислорода бесцветный орто- и парадинитробензол, присоединяя водород от восстановленных дегидрогеназ, необратимо восстанавливается в дышащих тканях в желтый орто- и пара-нитрофенилгидроксиламин и далее в орто- и паранитроанилин также желтого цвета. Орто- и паранитрофенилгидроксиламин дают в щелочной среде соответственно фиолетовое и красное окрашивание, а вместе – пурпурное. ЧРЕЗВЫЧАЙНО ТОКСИЧЕН, ИМЕЕТ НИЗКУЮ ЛЕТАЛЬНУЮ ДОЗУ! ОПАСЕН ДЛЯ ОКРУЖАЮЩЕЙ СРЕДЫ, ДАННЫЙ ВИД ВЕЩЕСТВ КАТЕГОРИЧЕСКИ ЗАПРЕЩАЕТСЯ УТИЛИЗИРОВАТЬ В ОБЩУЮ КАНАЛИЗАЦИЮ
 STEP BY STEP 1. В 2 пробирки наливают по 5 мл динитробензола (!вещество ядовито!, после работы с ним тщательно моют руки). 2. Из свежего клубня картофеля вырезают 2 одинаковых столбика длиной 3 -4 см, толщиной и шириной около 1 см. Ткани одного из них убивают кипячением в воде в течение 1 -2 мин (используют микроволновую печь). 3. В каждую пробирку с раствором динитробензола погружают по одному столбику и выдерживают 1 -3 ч при комнатной температуре или в термостате при температуре 30 -35°С. 4. В конце опыта сравнивают окраску столбиков и растворов в обеих пробирках. 5. Затем подщелачивают содержимое пробирок, добавив 10 - 15 капель 10% раствора аммиака, и через 5 -15 мин. , когда аммиак проникнет в ткани столбиков, вновь сравнивают окраску.
STEP BY STEP 1. В 2 пробирки наливают по 5 мл динитробензола (!вещество ядовито!, после работы с ним тщательно моют руки). 2. Из свежего клубня картофеля вырезают 2 одинаковых столбика длиной 3 -4 см, толщиной и шириной около 1 см. Ткани одного из них убивают кипячением в воде в течение 1 -2 мин (используют микроволновую печь). 3. В каждую пробирку с раствором динитробензола погружают по одному столбику и выдерживают 1 -3 ч при комнатной температуре или в термостате при температуре 30 -35°С. 4. В конце опыта сравнивают окраску столбиков и растворов в обеих пробирках. 5. Затем подщелачивают содержимое пробирок, добавив 10 - 15 капель 10% раствора аммиака, и через 5 -15 мин. , когда аммиак проникнет в ткани столбиков, вновь сравнивают окраску.
 Результаты опыта записывают в таблицу: Окраска ткани и раствора в конце опыта Ткань Без добавления После добавления аммиака Живая После кипячения
Результаты опыта записывают в таблицу: Окраска ткани и раствора в конце опыта Ткань Без добавления После добавления аммиака Живая После кипячения
 Работа #50: Обнаружение пероксидазы в соке клубня картофеля Пероксидаза – фермент, катализирующий окисление полифенолов и некоторых ароматических аминов при помощи O 2, Н 2 O 2 или органических перекисей. Пероксидаза образует с перекисью водорода комплексное соединение, в результате чего перекись активируется и приобретает способность действовать как акцептор водорода.
Работа #50: Обнаружение пероксидазы в соке клубня картофеля Пероксидаза – фермент, катализирующий окисление полифенолов и некоторых ароматических аминов при помощи O 2, Н 2 O 2 или органических перекисей. Пероксидаза образует с перекисью водорода комплексное соединение, в результате чего перекись активируется и приобретает способность действовать как акцептор водорода.
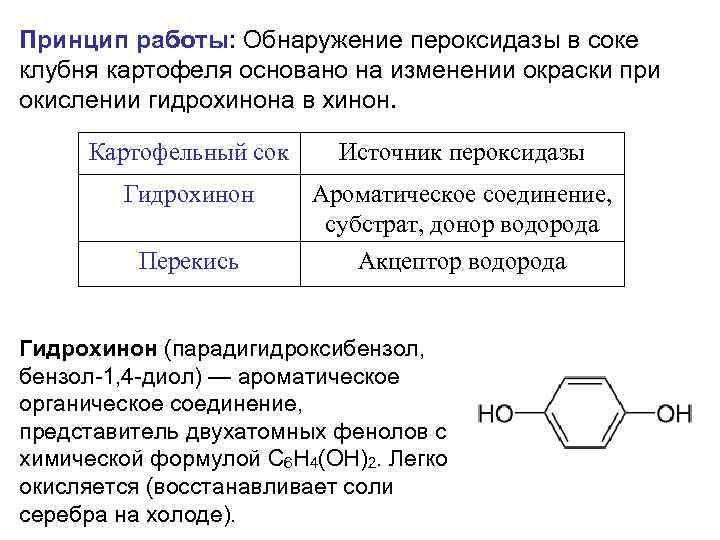 Принцип работы: Обнаружение пероксидазы в соке клубня картофеля основано на изменении окраски при окислении гидрохинона в хинон. Картофельный сок Источник пероксидазы Гидрохинон Ароматическое соединение, субстрат, донор водорода Перекись Акцептор водорода Гидрохинон (парадигидроксибензол, бензол-1, 4 -диол) — ароматическое органическое соединение, представитель двухатомных фенолов с химической формулой C 6 H 4(OH)2. Легко окисляется (восстанавливает соли серебра на холоде).
Принцип работы: Обнаружение пероксидазы в соке клубня картофеля основано на изменении окраски при окислении гидрохинона в хинон. Картофельный сок Источник пероксидазы Гидрохинон Ароматическое соединение, субстрат, донор водорода Перекись Акцептор водорода Гидрохинон (парадигидроксибензол, бензол-1, 4 -диол) — ароматическое органическое соединение, представитель двухатомных фенолов с химической формулой C 6 H 4(OH)2. Легко окисляется (восстанавливает соли серебра на холоде).
 STEP BY STEP 1. Натирают на терке очищенный клубень картофеля. Отжимают через марлю сок и собирают его в колбу. В 3 пробирки вносят по 5 мл 1% р-ра гидрохинона. 2. В первую добавляют 1 мл 3% р-ра перекиси и 1 мл картофельного сока. 3. Во вторую - 1 мл 3% р-ра перекиси. 4. В третью – 1 мл картофельного сока. 5. При окислении гидрохинона в хинон раствор буреет. Наблюдается некоторое побурение самого картофельного сока без добавления гидрохинона и перекиси, что связано с действием полифенолоксидазы, окисляющей полифенолы тканей картофеля с участием молекулярного кислорода.
STEP BY STEP 1. Натирают на терке очищенный клубень картофеля. Отжимают через марлю сок и собирают его в колбу. В 3 пробирки вносят по 5 мл 1% р-ра гидрохинона. 2. В первую добавляют 1 мл 3% р-ра перекиси и 1 мл картофельного сока. 3. Во вторую - 1 мл 3% р-ра перекиси. 4. В третью – 1 мл картофельного сока. 5. При окислении гидрохинона в хинон раствор буреет. Наблюдается некоторое побурение самого картофельного сока без добавления гидрохинона и перекиси, что связано с действием полифенолоксидазы, окисляющей полифенолы тканей картофеля с участием молекулярного кислорода.
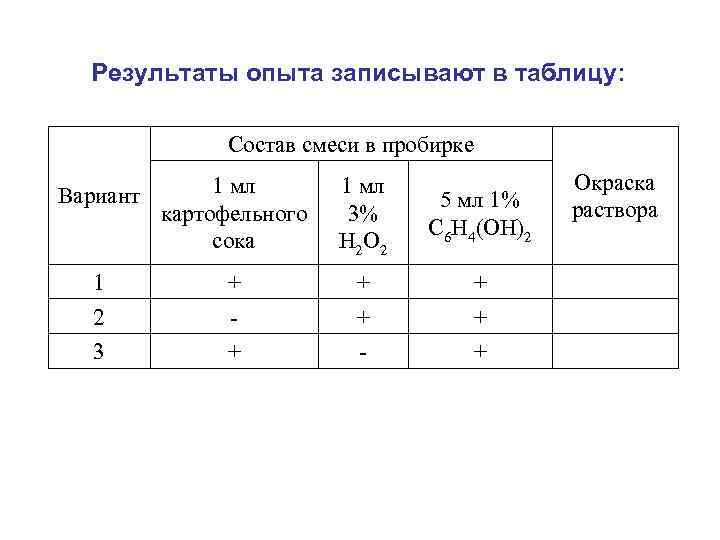 Результаты опыта записывают в таблицу: Состав смеси в пробирке 1 мл Окраска Вариант 5 мл 1% картофельного 3% раствора C 6 H 4(OH)2 сока Н 2 O 2 1 + + 2 - + 3 + - +
Результаты опыта записывают в таблицу: Состав смеси в пробирке 1 мл Окраска Вариант 5 мл 1% картофельного 3% раствора C 6 H 4(OH)2 сока Н 2 O 2 1 + + 2 - + 3 + - +
 РЕЗУЛЬТАТ
РЕЗУЛЬТАТ
 Работа #52: Определение активности каталазы в растительных объектах Каталаза – фермент, 2 Н 2 O 2 → 2 Н 2 O + O 2 нейтрализующий перекись, которая образуется в Об активности процессе дыхания в качестве каталазы судят по побочного продукта объему кислорода, окисления веществ и в выделившегося в высоких концентрациях результате оказывает токсическое разложения действие на цитоплазму. перекиси. Каталаза широко распространёна в клетках животных, растений и микроорганизмов. Специфичность каталазы в отношении к субстрату-восстановителю невелика, поэтому она может катализировать не только разложение H 2 O 2, но и окисление низших спиртов.
Работа #52: Определение активности каталазы в растительных объектах Каталаза – фермент, 2 Н 2 O 2 → 2 Н 2 O + O 2 нейтрализующий перекись, которая образуется в Об активности процессе дыхания в качестве каталазы судят по побочного продукта объему кислорода, окисления веществ и в выделившегося в высоких концентрациях результате оказывает токсическое разложения действие на цитоплазму. перекиси. Каталаза широко распространёна в клетках животных, растений и микроорганизмов. Специфичность каталазы в отношении к субстрату-восстановителю невелика, поэтому она может катализировать не только разложение H 2 O 2, но и окисление низших спиртов.
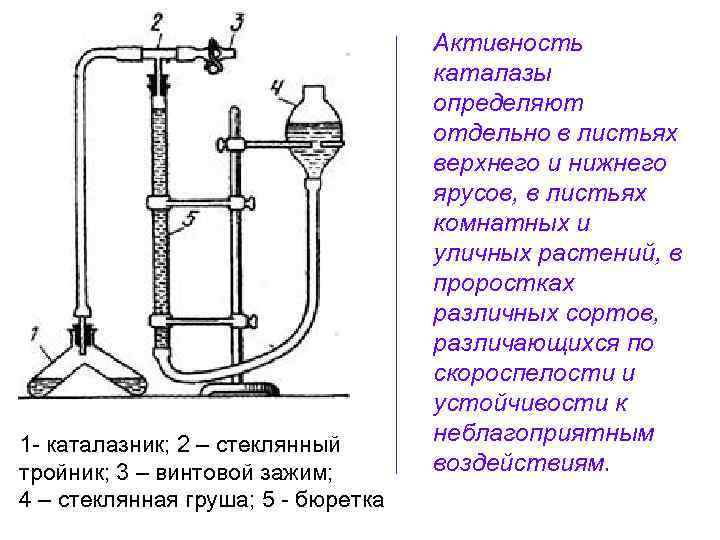 Активность каталазы определяют отдельно в листьях верхнего и нижнего ярусов, в листьях комнатных и уличных растений, в проростках различных сортов, различающихся по скороспелости и устойчивости к 1 - каталазник; 2 – стеклянный неблагоприятным тройник; 3 – винтовой зажим; воздействиям. 4 – стеклянная груша; 5 - бюретка
Активность каталазы определяют отдельно в листьях верхнего и нижнего ярусов, в листьях комнатных и уличных растений, в проростках различных сортов, различающихся по скороспелости и устойчивости к 1 - каталазник; 2 – стеклянный неблагоприятным тройник; 3 – винтовой зажим; воздействиям. 4 – стеклянная груша; 5 - бюретка
 STEP BY STEP 1. Навеску листьев 0, 5 г растирают в фарфоровой ступке с кварцевым песком и добавляют 0, 5 мела для создания щелочной реакции. Во время растирания вливают небольшими порциями 20 мл воды, смесь вносят в одно колено каталазника. В другое колено помещают 5 мл 3% раствора Н 2 O 2. Каталазник соединяют с каучуковой трубкой, не допуская смешивания жидкостей. 2. Открывают зажим и перемещением стеклянной груши устанавливают уровень воды в бюретке на ноль. При отсчете вода в стеклянной груше и бюретке должна быть на одном уровне. Закрывают зажим и быстрым изменением положения каталазника смешивают жидкость в обоих коленах в течение 3 мин. Через 3 мин. , не переставая потряхивать каталазник, в бюретке отмечают объем O 2 (мл). ! Во время опыта каталазник нельзя держать всей ладонью, т. к. при нагревании от руки воздух в колбе расширяется, что может повлиять на точность отсчета.
STEP BY STEP 1. Навеску листьев 0, 5 г растирают в фарфоровой ступке с кварцевым песком и добавляют 0, 5 мела для создания щелочной реакции. Во время растирания вливают небольшими порциями 20 мл воды, смесь вносят в одно колено каталазника. В другое колено помещают 5 мл 3% раствора Н 2 O 2. Каталазник соединяют с каучуковой трубкой, не допуская смешивания жидкостей. 2. Открывают зажим и перемещением стеклянной груши устанавливают уровень воды в бюретке на ноль. При отсчете вода в стеклянной груше и бюретке должна быть на одном уровне. Закрывают зажим и быстрым изменением положения каталазника смешивают жидкость в обоих коленах в течение 3 мин. Через 3 мин. , не переставая потряхивать каталазник, в бюретке отмечают объем O 2 (мл). ! Во время опыта каталазник нельзя держать всей ладонью, т. к. при нагревании от руки воздух в колбе расширяется, что может повлиять на точность отсчета.
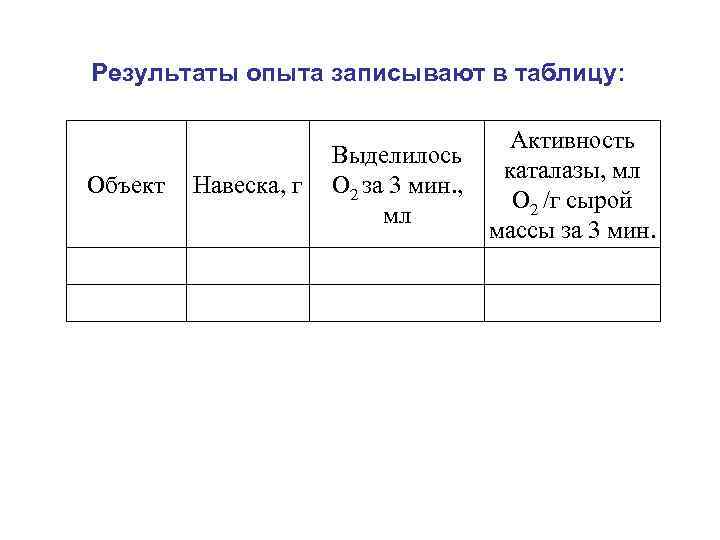 Результаты опыта записывают в таблицу: Активность Выделилось каталазы, мл Объект Навеска, г O 2 за 3 мин. , O 2 /г сырой мл массы за 3 мин.
Результаты опыта записывают в таблицу: Активность Выделилось каталазы, мл Объект Навеска, г O 2 за 3 мин. , O 2 /г сырой мл массы за 3 мин.


