лекция 25.ppt
- Количество слайдов: 15
 Движущая сила процесса кристаллизации Рост тонких пленок на подложках при кристаллизации из жидкой или парогазовой фазы обычно начинается со стадии зародышеобразования. Ростовые явления происходят на границе раздела двух фаз, следовательно процесс зародышеобразования является гетерогенным, и существенную роль при этом играют свойства поверхности подложки и межфазной границы. При Р = const, для описания процессов гомогенной кристаллизации в объеме первичной (жидкой или парогазовой) фазы следует использовать изобарный потенциал Gv, Неравновесные изобарно-изотермические процессы самопроизвольно протекают в направлении уменьшения изобарного потенциала (Gv < 0). Они идут до тех пор, пока не наступает равновесие (фазовое или химическое), при котором Gv достигает минимального при данных условиях значения, при котором Gv = 0.
Движущая сила процесса кристаллизации Рост тонких пленок на подложках при кристаллизации из жидкой или парогазовой фазы обычно начинается со стадии зародышеобразования. Ростовые явления происходят на границе раздела двух фаз, следовательно процесс зародышеобразования является гетерогенным, и существенную роль при этом играют свойства поверхности подложки и межфазной границы. При Р = const, для описания процессов гомогенной кристаллизации в объеме первичной (жидкой или парогазовой) фазы следует использовать изобарный потенциал Gv, Неравновесные изобарно-изотермические процессы самопроизвольно протекают в направлении уменьшения изобарного потенциала (Gv < 0). Они идут до тех пор, пока не наступает равновесие (фазовое или химическое), при котором Gv достигает минимального при данных условиях значения, при котором Gv = 0.
 Движущей силой фазовых и химических превращений в изобарноизотермических условиях является изменение объемного изобарного потенциала Gv, навязанное системе внешними условиями. Реальные параметрами, с помощью которых можно управлять процессами в технологических системах ci объемная концентрация частиц i-го компонента в жидкой фазе ∆ci концентрационное пересыщение Т температура ∆Т переохлаждение pi = cik. T парциальное давление в парогазовой фазе. ∆pi избыточное давление Установим связь между ∆Gv и управляемыми параметрами процесса
Движущей силой фазовых и химических превращений в изобарноизотермических условиях является изменение объемного изобарного потенциала Gv, навязанное системе внешними условиями. Реальные параметрами, с помощью которых можно управлять процессами в технологических системах ci объемная концентрация частиц i-го компонента в жидкой фазе ∆ci концентрационное пересыщение Т температура ∆Т переохлаждение pi = cik. T парциальное давление в парогазовой фазе. ∆pi избыточное давление Установим связь между ∆Gv и управляемыми параметрами процесса
 Все методы осаждения твердых веществ на подложках можно разделить на две группы: 1) физические методы осаждения, основанные на принципе нарушения условий фазового равновесия при кристаллизации из: расплава осаждаемого вещества; раствора-расплава, содержащего осаждаемое вещество; парогазовой фазы, содержащей осаждаемое вещество; 2) химические методы осаждения, основанные на принципе нарушения условий химического равновесия при кристаллизации из химически реактивной газовой фазы.
Все методы осаждения твердых веществ на подложках можно разделить на две группы: 1) физические методы осаждения, основанные на принципе нарушения условий фазового равновесия при кристаллизации из: расплава осаждаемого вещества; раствора-расплава, содержащего осаждаемое вещество; парогазовой фазы, содержащей осаждаемое вещество; 2) химические методы осаждения, основанные на принципе нарушения условий химического равновесия при кристаллизации из химически реактивной газовой фазы.
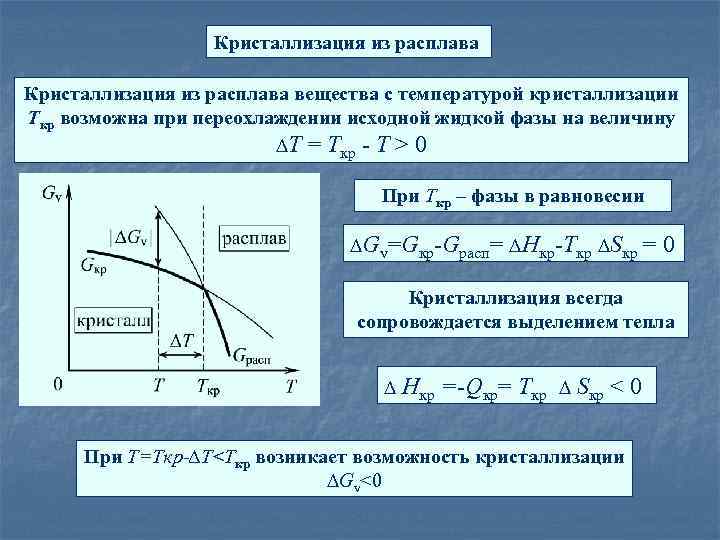 Кристаллизация из расплава вещества с температурой кристаллизации Tкр возможна при переохлаждении исходной жидкой фазы на величину ∆Т = Ткр - Т > 0 При Ткр – фазы в равновесии ∆Gv=Gкр-Gрасп= ∆Hкр-Tкр ∆Sкр = 0 Кристаллизация всегда сопровождается выделением тепла ∆ Hкр =-Qкр= Tкр ∆ Sкр < 0 При T=Tкр-∆T<Ткр возникает возможность кристаллизации ∆Gv<0
Кристаллизация из расплава вещества с температурой кристаллизации Tкр возможна при переохлаждении исходной жидкой фазы на величину ∆Т = Ткр - Т > 0 При Ткр – фазы в равновесии ∆Gv=Gкр-Gрасп= ∆Hкр-Tкр ∆Sкр = 0 Кристаллизация всегда сопровождается выделением тепла ∆ Hкр =-Qкр= Tкр ∆ Sкр < 0 При T=Tкр-∆T<Ткр возникает возможность кристаллизации ∆Gv<0
 при достаточно малом температурном интервале ∆Т можно считать, что: учтём, что:
при достаточно малом температурном интервале ∆Т можно считать, что: учтём, что:
 Кристаллизация из раствора-расплава вещества i-го сорта (при Т=const) возможна в условиях положительного концентрационного пересыщения Равновесные условия Неравновесные условия
Кристаллизация из раствора-расплава вещества i-го сорта (при Т=const) возможна в условиях положительного концентрационного пересыщения Равновесные условия Неравновесные условия
 Кристаллизация из парогазовой фазы вещества i-го сорта в изотермических условиях возможна, если парциальное давление обеспечивает в газовой фазе положительный избыток давления Равновесные условия Неравновесные условия
Кристаллизация из парогазовой фазы вещества i-го сорта в изотермических условиях возможна, если парциальное давление обеспечивает в газовой фазе положительный избыток давления Равновесные условия Неравновесные условия
 Химическое осаждение из газовой фазы осуществляется с помощью гетерогенной обратимой химической реакции Химическое пересыщение в неравновесной системе, создаваемое такой реакцией, записывается в форме уравнения изотермы Вант-Гоффа рн и рк – неравновесные давления, изменяя которые можно обеспечить нужный знак ∆Gv в равенстве, соответствующий смещению химического равновесия в сторону осаждения необходимого твердофазного продукта в реакции
Химическое осаждение из газовой фазы осуществляется с помощью гетерогенной обратимой химической реакции Химическое пересыщение в неравновесной системе, создаваемое такой реакцией, записывается в форме уравнения изотермы Вант-Гоффа рн и рк – неравновесные давления, изменяя которые можно обеспечить нужный знак ∆Gv в равенстве, соответствующий смещению химического равновесия в сторону осаждения необходимого твердофазного продукта в реакции
 Как видно из полученных выше выражений, для ∆Gv изменением внешних условий всегда термодинамически возможно обеспечить процесс кристаллизации, причем возникать он должен даже при бесконечно малом пересыщении Однако на практике, имеется определенное критическое пересыщение, ниже которого существует метастабильная пересыщенная (переохлажденная) первичная фаза, а выше — начинают образовываться зародыши новой (вторичной) фазы. Это связано с тем, что кристаллизация не является чисто объемным процессом. Она определяется в значительной степени свойствами границ раздела кристаллического зародыша с подложкой и с окружающей первичной фазой. Свойства частиц в поверхностных слоях отличается от их состояния внутри объема конденсированной фазы. Химические связи любой внутренней частицы насыщены связями ее соседей. Для поверхностных частиц симметрия силовых взаимодействий нарушается и насыщение связей уже не является всесторонним.
Как видно из полученных выше выражений, для ∆Gv изменением внешних условий всегда термодинамически возможно обеспечить процесс кристаллизации, причем возникать он должен даже при бесконечно малом пересыщении Однако на практике, имеется определенное критическое пересыщение, ниже которого существует метастабильная пересыщенная (переохлажденная) первичная фаза, а выше — начинают образовываться зародыши новой (вторичной) фазы. Это связано с тем, что кристаллизация не является чисто объемным процессом. Она определяется в значительной степени свойствами границ раздела кристаллического зародыша с подложкой и с окружающей первичной фазой. Свойства частиц в поверхностных слоях отличается от их состояния внутри объема конденсированной фазы. Химические связи любой внутренней частицы насыщены связями ее соседей. Для поверхностных частиц симметрия силовых взаимодействий нарушается и насыщение связей уже не является всесторонним.
 Нарушение симметрии силовых взаимодействий отражается в появлении избыточной поверхностной энергии ∆Gs, вводимой аналогично избыточной свободной энергии σ - удельная поверхностная энергия, имеет размерность Дж/м 2 или Н/м и выражает работу, которую необходимо совершить для увеличения границы раздела фаз на единицу площади поверхностное натяжение представляет собой силу, которую нужно приложить к единице длины линии, ограничивающей поверхность раздела фаз, для увеличения площади этой поверхности на единицу. Эта сила направлена по касательной к соответствующей границе раздела
Нарушение симметрии силовых взаимодействий отражается в появлении избыточной поверхностной энергии ∆Gs, вводимой аналогично избыточной свободной энергии σ - удельная поверхностная энергия, имеет размерность Дж/м 2 или Н/м и выражает работу, которую необходимо совершить для увеличения границы раздела фаз на единицу площади поверхностное натяжение представляет собой силу, которую нужно приложить к единице длины линии, ограничивающей поверхность раздела фаз, для увеличения площади этой поверхности на единицу. Эта сила направлена по касательной к соответствующей границе раздела
 Образование зародыша новой фазы на поверхности подложки, с одной стороны, способствует понижению энергии системы в силу уменьшения объемной свободной энергии (Gv < 0), а с другой стороны, требует затраты энергии на создание границ раздела, поскольку поверхностная свободная энергия всегда положительна (Gs > 0). знак зависит от размера зародыша – r (характерный линейный размер зародыша ) Разная степенная зависимость этих величин обеспечивает различную скорость их изменения с ростом r, а именно: при малых r быстрее нарастает квадратичная зависимость Gs , а при больших r — кубическая зависимость | Gv |.
Образование зародыша новой фазы на поверхности подложки, с одной стороны, способствует понижению энергии системы в силу уменьшения объемной свободной энергии (Gv < 0), а с другой стороны, требует затраты энергии на создание границ раздела, поскольку поверхностная свободная энергия всегда положительна (Gs > 0). знак зависит от размера зародыша – r (характерный линейный размер зародыша ) Разная степенная зависимость этих величин обеспечивает различную скорость их изменения с ростом r, а именно: при малых r быстрее нарастает квадратичная зависимость Gs , а при больших r — кубическая зависимость | Gv |.
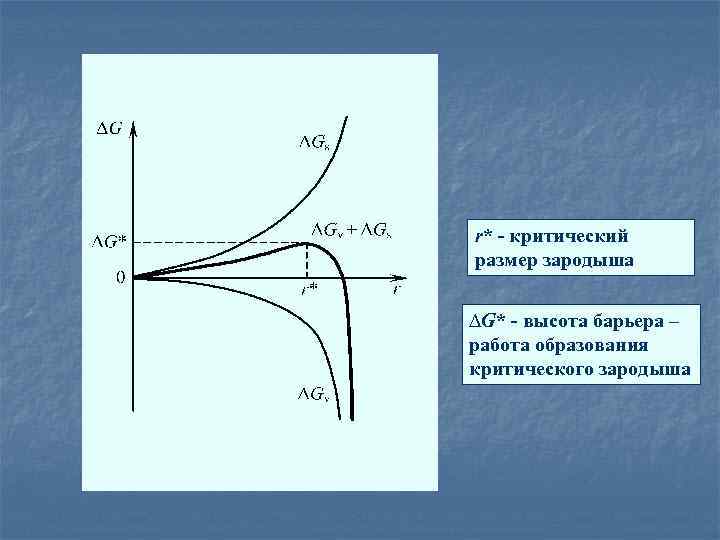 r* - критический размер зародыша ∆G* - высота барьера – работа образования критического зародыша
r* - критический размер зародыша ∆G* - высота барьера – работа образования критического зародыша
 Возникновение критических зародышей связано с преодолением барьера зародышеобразования ∆G*, т. е. относится к классу термоактивационных процессов. Высота активационного барьера ∆G* трактуется как работа образования критического зародыша. Появление критических зародышей, являющихся центрами кристаллизации, носит флуктуационный характер. Поэтому вероятность их образования определяется обычной больцмановской экспонентой: где величина ∆G* отнесена к одной частице.
Возникновение критических зародышей связано с преодолением барьера зародышеобразования ∆G*, т. е. относится к классу термоактивационных процессов. Высота активационного барьера ∆G* трактуется как работа образования критического зародыша. Появление критических зародышей, являющихся центрами кристаллизации, носит флуктуационный характер. Поэтому вероятность их образования определяется обычной больцмановской экспонентой: где величина ∆G* отнесена к одной частице.
 Теория гетерогенного зародышеобразования термодинамическая теория кинетическая теория атомно-статистическая теория Термодинамическая теория рассматривает зародыши как частицы сплошной среды только малых размеров и приписывает им термодинамические свойства массивного материала. Такая модель естественно применима только к макроскопическим зародышам, состоящим из большого числа частиц (молекул, атомов, ионов). Задачей термодинамической теории является нахождение размера критического зародыша r*, работы его образования ∆G* и скорости зародышеобразования. Экспериментально установлено, что при достаточно больших пересыщениях зародыши могут состоять из нескольких атомов. Для описания процесса их образования возможен лишь статистический подход, когда вместо свободных энергий вводятся статистические суммы и потенциальные энергии взаимодействия отдельных частиц.
Теория гетерогенного зародышеобразования термодинамическая теория кинетическая теория атомно-статистическая теория Термодинамическая теория рассматривает зародыши как частицы сплошной среды только малых размеров и приписывает им термодинамические свойства массивного материала. Такая модель естественно применима только к макроскопическим зародышам, состоящим из большого числа частиц (молекул, атомов, ионов). Задачей термодинамической теории является нахождение размера критического зародыша r*, работы его образования ∆G* и скорости зародышеобразования. Экспериментально установлено, что при достаточно больших пересыщениях зародыши могут состоять из нескольких атомов. Для описания процесса их образования возможен лишь статистический подход, когда вместо свободных энергий вводятся статистические суммы и потенциальные энергии взаимодействия отдельных частиц.
 Атомно-статистическая теория рассматривает зародыши как агрегаты, называемые кластерами, состоящие из дискретных частиц (молекул, атомов, ионов), взаимодействующих между собой и с подложкой. В этом случае зародыш характеризуется не термодинамическими свойствами осаждаемого материала, а потенциальной энергией в рамках той или иной модели взаимодействия частиц. Задачей атомно-статистической теории является не нахождение величин r* и ∆G*, а определение числа дискретных частиц в критическом зародыше и соответствующей скорости образования таких зародышей. Кинетические теории изучают развитие во времени процесса образования на подложке кластеров с различным числом частиц, учитывая при этом конкуренцию между элементарными актами адсорбции, десорбции, поверхностной диффузии, закрепления адсорбированных атомов на дефектах подложки и т. п. Детализация кинетико-статистического описания сильно усложняет анализ процесса зародышеобразования.
Атомно-статистическая теория рассматривает зародыши как агрегаты, называемые кластерами, состоящие из дискретных частиц (молекул, атомов, ионов), взаимодействующих между собой и с подложкой. В этом случае зародыш характеризуется не термодинамическими свойствами осаждаемого материала, а потенциальной энергией в рамках той или иной модели взаимодействия частиц. Задачей атомно-статистической теории является не нахождение величин r* и ∆G*, а определение числа дискретных частиц в критическом зародыше и соответствующей скорости образования таких зародышей. Кинетические теории изучают развитие во времени процесса образования на подложке кластеров с различным числом частиц, учитывая при этом конкуренцию между элементарными актами адсорбции, десорбции, поверхностной диффузии, закрепления адсорбированных атомов на дефектах подложки и т. п. Детализация кинетико-статистического описания сильно усложняет анализ процесса зародышеобразования.


