Донской государственный технический университет












Лекция 2. Периодический закон.ppt
- Количество слайдов: 18
 Донской государственный технический университет Факультет нанотехнологии и композиционные материалы Кафедра «Химия» Периодический закон Лекция 2. Д. И. Менделеева Кужаров А. А. Новикова
Донской государственный технический университет Факультет нанотехнологии и композиционные материалы Кафедра «Химия» Периодический закон Лекция 2. Д. И. Менделеева Кужаров А. А. Новикова
 Рекомендуемая литература • Кужаров А. С. Общая химия в машиностроительном ВУЗЕ. Конспект лекций для инженеров, Ростов-на- Дону, 1992. • Ахметов Н. С. Общая и неорганическая химия, М. , 2002. • Глинка Н. Л. Общая химия, М. , 2008. • Некрасов Б. В. Курс обшей химии, М. , 1962 – 2010. • Н. В. Коровин Общая химия, М. : Высшая школа, 1998 • М. И. Гельфман, В. П. Юстратов Химия, СПб. : Лань, 2000 • www. chemistry. ru • www. chem. msu. su/rus
Рекомендуемая литература • Кужаров А. С. Общая химия в машиностроительном ВУЗЕ. Конспект лекций для инженеров, Ростов-на- Дону, 1992. • Ахметов Н. С. Общая и неорганическая химия, М. , 2002. • Глинка Н. Л. Общая химия, М. , 2008. • Некрасов Б. В. Курс обшей химии, М. , 1962 – 2010. • Н. В. Коровин Общая химия, М. : Высшая школа, 1998 • М. И. Гельфман, В. П. Юстратов Химия, СПб. : Лань, 2000 • www. chemistry. ru • www. chem. msu. su/rus
 История открытия. Предшественники Правило триад Дёберейнера (1829 г. ) если расположить три сходных по химическим свойствам элемента в порядке возрастания их атомных весов, то атомный вес второго элемента будет равен среднему арифметическому атомных весов первого и третьего. Литий Li: Ar(Li) = 6, 941 а. е. м. Натрий Na: Ar(Na) = 22, 99 а. е. м. Калий K: Ar(K) = 39, 102 а. е. м Ar(Na) = ½ (Ar(Li) + Ar(K)) ≈ 23, 0 а. е. м. Иоганн Вольфганг Дёберейнер, 1780 -1849
История открытия. Предшественники Правило триад Дёберейнера (1829 г. ) если расположить три сходных по химическим свойствам элемента в порядке возрастания их атомных весов, то атомный вес второго элемента будет равен среднему арифметическому атомных весов первого и третьего. Литий Li: Ar(Li) = 6, 941 а. е. м. Натрий Na: Ar(Na) = 22, 99 а. е. м. Калий K: Ar(K) = 39, 102 а. е. м Ar(Na) = ½ (Ar(Li) + Ar(K)) ≈ 23, 0 а. е. м. Иоганн Вольфганг Дёберейнер, 1780 -1849
 Спираль Шанкуртуа «Земная спираль» Шанкуртуа (1862 г. ) На боковую поверхность цилиндра, разделенную на 16 частей, нанесена линия под углом 45°, на которой отмечены точки, соответствующие атомным весам элементов. Сходные по свойствам элементы группируются на одной вертикальной линии. Александр Эмиль Бегуйе де Шанкуртуа, 1820 -1886
Спираль Шанкуртуа «Земная спираль» Шанкуртуа (1862 г. ) На боковую поверхность цилиндра, разделенную на 16 частей, нанесена линия под углом 45°, на которой отмечены точки, соответствующие атомным весам элементов. Сходные по свойствам элементы группируются на одной вертикальной линии. Александр Эмиль Бегуйе де Шанкуртуа, 1820 -1886
 Закон октав Ньюлендса • В 1865 г. Ньюлендс опубликовал таблицу элементов, назвав её «законом октав» : «Номера аналогичных элементов, как правило, отличаются или на целое число семь, или на кратное семи; другими словами, члены одной и той же группы соотносятся друг с другом в том же отношении, как и крайние точки одной или больше октав в музыке» . Джон Александр Рейна Ньюлендс, 1837 -1898
Закон октав Ньюлендса • В 1865 г. Ньюлендс опубликовал таблицу элементов, назвав её «законом октав» : «Номера аналогичных элементов, как правило, отличаются или на целое число семь, или на кратное семи; другими словами, члены одной и той же группы соотносятся друг с другом в том же отношении, как и крайние точки одной или больше октав в музыке» . Джон Александр Рейна Ньюлендс, 1837 -1898
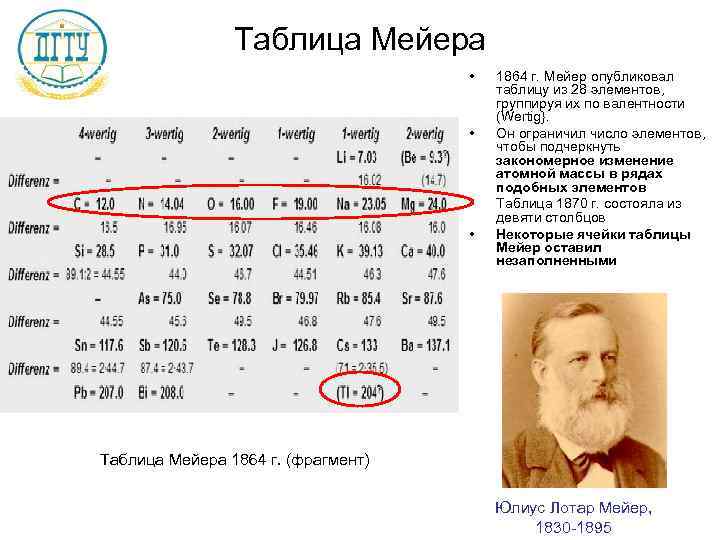
 Таблица Мейера • 1864 г. Мейер опубликовал таблицу из 28 элементов, группируя их по валентности (Wertig}. • Он ограничил число элементов, чтобы подчеркнуть закономерное изменение атомной массы в рядах подобных элементов • Таблица 1870 г. состояла из девяти столбцов • Некоторые ячейки таблицы Мейер оставил незаполненными Таблица Мейера 1864 г. (фрагмент) Юлиус Лотар Мейер, 1830 -1895
Таблица Мейера • 1864 г. Мейер опубликовал таблицу из 28 элементов, группируя их по валентности (Wertig}. • Он ограничил число элементов, чтобы подчеркнуть закономерное изменение атомной массы в рядах подобных элементов • Таблица 1870 г. состояла из девяти столбцов • Некоторые ячейки таблицы Мейер оставил незаполненными Таблица Мейера 1864 г. (фрагмент) Юлиус Лотар Мейер, 1830 -1895
 Д. И. Менделеев МЕНДЕЛЕЕВ Дмитрий Иванович (1834 -1907), (1834 -1907) российский химик, разносторонний ученый, педагог. • Открыл (1869) периодический закон химических элементов — один из основных законов естествознания. • Оставил св. 500 печатных трудов, среди которых классические «Основы химии» (ч. 1 -2, 1869 -71, 13 изд. , 1947) — первое стройное изложение неорганической химии. • Автор фундаментальных исследований по химии, химической технологии, физике, метрологии, воздухоплаванию, метеорологии, сельскому хозяйству, экономике, народному просвещению и др. • Заложил основы теории растворов, предложил промышленный способ фракционного разделения нефти, изобрел вид бездымного пороха, пропагандировал использование минеральных удобрений, орошение засушливых земель. • Один из инициаторов создания Русского химического общества (1868). Профессор Петербургского университета (1865 -90), ушел в отставку в знак протеста против притеснения студенчества. • Организатор и первый директор (1893) Главной палаты мер и весов (ныне ВНИИ метрологии им. Менделеева).
Д. И. Менделеев МЕНДЕЛЕЕВ Дмитрий Иванович (1834 -1907), (1834 -1907) российский химик, разносторонний ученый, педагог. • Открыл (1869) периодический закон химических элементов — один из основных законов естествознания. • Оставил св. 500 печатных трудов, среди которых классические «Основы химии» (ч. 1 -2, 1869 -71, 13 изд. , 1947) — первое стройное изложение неорганической химии. • Автор фундаментальных исследований по химии, химической технологии, физике, метрологии, воздухоплаванию, метеорологии, сельскому хозяйству, экономике, народному просвещению и др. • Заложил основы теории растворов, предложил промышленный способ фракционного разделения нефти, изобрел вид бездымного пороха, пропагандировал использование минеральных удобрений, орошение засушливых земель. • Один из инициаторов создания Русского химического общества (1868). Профессор Петербургского университета (1865 -90), ушел в отставку в знак протеста против притеснения студенчества. • Организатор и первый директор (1893) Главной палаты мер и весов (ныне ВНИИ метрологии им. Менделеева).
 Первая формулировка Периодического закона • 1 марта 1869 г. Д. И. Менделеев опубликовал (в Журнале Русского Химического Общества) первую статью о периодическом законе на русском и французском языках, где впервые сформулировал Периодический закон: «…Свойства элементов, а потому и свойства образуемых ими простых и сложных тел состоят в периодической зависимости от их атомного веса…»
Первая формулировка Периодического закона • 1 марта 1869 г. Д. И. Менделеев опубликовал (в Журнале Русского Химического Общества) первую статью о периодическом законе на русском и французском языках, где впервые сформулировал Периодический закон: «…Свойства элементов, а потому и свойства образуемых ими простых и сложных тел состоят в периодической зависимости от их атомного веса…»
 Сущность открытия Д. И. Менделеева • Сущность открытия Менделеева: с ростом атомной массы химических элементов их свойства меняются не монотонно, а периодически • Отличие работы Менделеева от работ предшественников: классификация всех известных к тому времени элементов на основе их атомных масс и химических свойств • Исправил атомные массы некоторых элементов (например, бериллия, индия, урана, тория, церия, титана, иттрия) • Разместил несколько элементов в своей системе вопреки принятым в то время представлениям об их сходстве с другими (например, таллий, считавшийся щелочным Первая периодическая таблица металлом, он поместил в третью группу согласно его фактической максимальной валентности), • Оставил в таблице пустые клетки, где должны были разместиться пока не открытые элементы. В 1875 -1866 гг. открыты галлий (экаалюминий), скандий (экабор) и германий (экасилиций)
Сущность открытия Д. И. Менделеева • Сущность открытия Менделеева: с ростом атомной массы химических элементов их свойства меняются не монотонно, а периодически • Отличие работы Менделеева от работ предшественников: классификация всех известных к тому времени элементов на основе их атомных масс и химических свойств • Исправил атомные массы некоторых элементов (например, бериллия, индия, урана, тория, церия, титана, иттрия) • Разместил несколько элементов в своей системе вопреки принятым в то время представлениям об их сходстве с другими (например, таллий, считавшийся щелочным Первая периодическая таблица металлом, он поместил в третью группу согласно его фактической максимальной валентности), • Оставил в таблице пустые клетки, где должны были разместиться пока не открытые элементы. В 1875 -1866 гг. открыты галлий (экаалюминий), скандий (экабор) и германий (экасилиций)
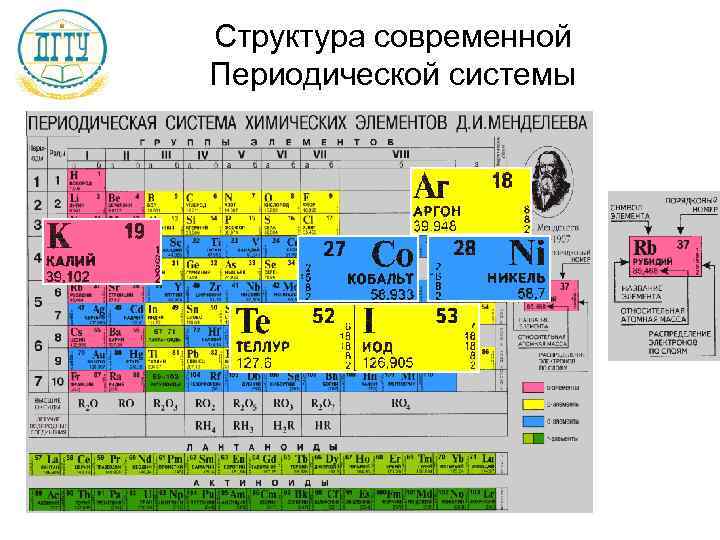
 Структура современной Периодической системы
Структура современной Периодической системы
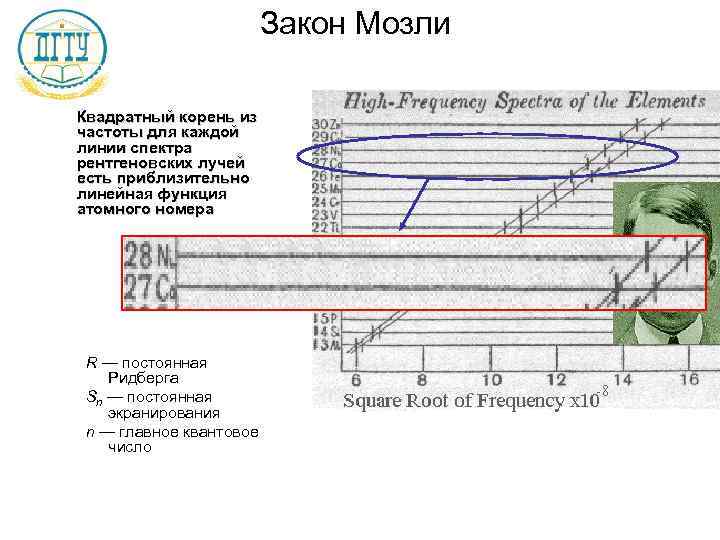
 Закон Мозли Квадратный корень из частоты для каждой линии спектра рентгеновских лучей есть приблизительно линейная функция атомного номера R — постоянная Ридберга Sn — постоянная экранирования n — главное квантовое число
Закон Мозли Квадратный корень из частоты для каждой линии спектра рентгеновских лучей есть приблизительно линейная функция атомного номера R — постоянная Ридберга Sn — постоянная экранирования n — главное квантовое число
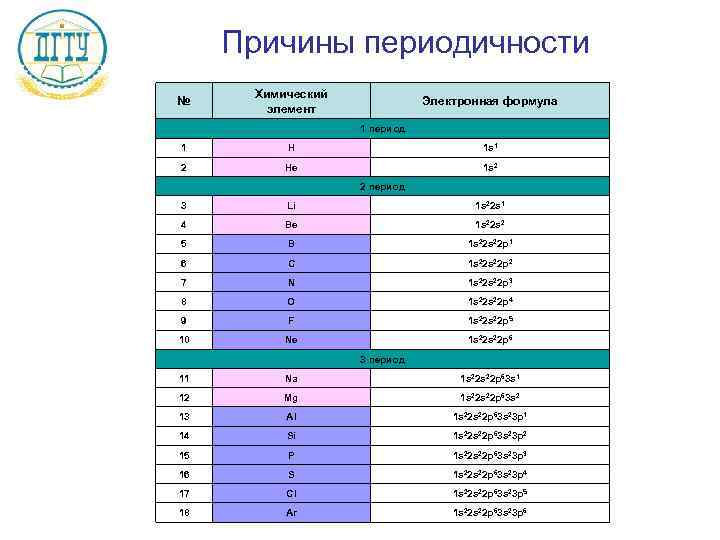
 Причины периодичности Химический № Электронная формула элемент 1 период 1 H 1 s 1 2 He 1 s 2 2 период 3 Li 1 s 22 s 1 4 Be 1 s 22 s 2 5 B 1 s 22 p 1 6 C 1 s 22 p 2 7 N 1 s 22 p 3 8 O 1 s 22 p 4 9 F 1 s 22 p 5 10 Ne 1 s 22 p 6 3 период 11 Na 1 s 22 p 63 s 1 12 Mg 1 s 22 p 63 s 2 13 Al 1 s 22 p 63 s 23 p 1 14 Si 1 s 22 p 63 s 23 p 2 15 P 1 s 22 p 63 s 23 p 3 16 S 1 s 22 p 63 s 23 p 4 17 Cl 1 s 22 p 63 s 23 p 5 18 Ar 1 s 22 p 63 s 23 p 6
Причины периодичности Химический № Электронная формула элемент 1 период 1 H 1 s 1 2 He 1 s 2 2 период 3 Li 1 s 22 s 1 4 Be 1 s 22 s 2 5 B 1 s 22 p 1 6 C 1 s 22 p 2 7 N 1 s 22 p 3 8 O 1 s 22 p 4 9 F 1 s 22 p 5 10 Ne 1 s 22 p 6 3 период 11 Na 1 s 22 p 63 s 1 12 Mg 1 s 22 p 63 s 2 13 Al 1 s 22 p 63 s 23 p 1 14 Si 1 s 22 p 63 s 23 p 2 15 P 1 s 22 p 63 s 23 p 3 16 S 1 s 22 p 63 s 23 p 4 17 Cl 1 s 22 p 63 s 23 p 5 18 Ar 1 s 22 p 63 s 23 p 6
 Современная формулировка Периодического закона Свойства химических элементов находятся в периодической зависимости от заряда ядер атомов химических элементов
Современная формулировка Периодического закона Свойства химических элементов находятся в периодической зависимости от заряда ядер атомов химических элементов
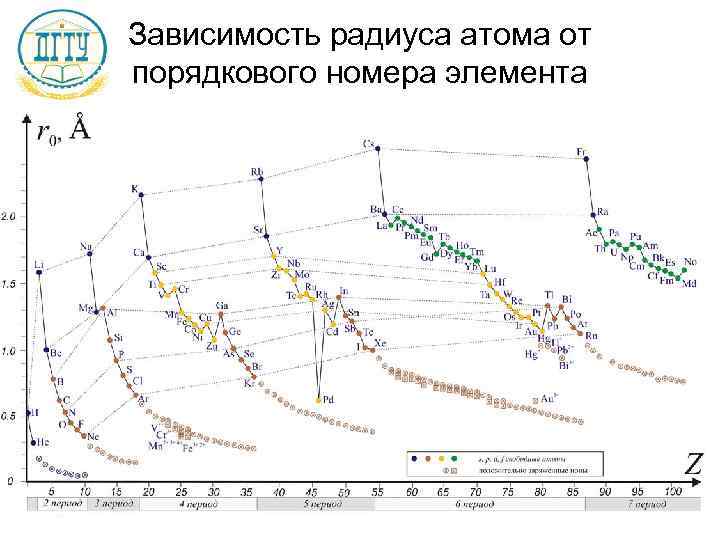
 Зависимость радиуса атома от порядкового номера элемента
Зависимость радиуса атома от порядкового номера элемента
 Энергия ионизации Энергией ионизации (потенциалом ионизации) - работа, необходимая для отрыва электрона от нейтрального атома. Э – ē = Э + Первый потенциал ионизации элементов третьего периода: Na Mg Al Si P S Cl Ar 5, 14 7, 64 6, 0 8, 15 11, 0 10, 36 13, 01 15, 80 Второй и третий потенциал ионизации значительно выше, чем первый, например: Li- ē=Li+ J 1=3, 39 эв Li+- ē=Li+2 J 2=75, 62 эв Li+2 - ē=Li+3 J 3=122, 42 эв
Энергия ионизации Энергией ионизации (потенциалом ионизации) - работа, необходимая для отрыва электрона от нейтрального атома. Э – ē = Э + Первый потенциал ионизации элементов третьего периода: Na Mg Al Si P S Cl Ar 5, 14 7, 64 6, 0 8, 15 11, 0 10, 36 13, 01 15, 80 Второй и третий потенциал ионизации значительно выше, чем первый, например: Li- ē=Li+ J 1=3, 39 эв Li+- ē=Li+2 J 2=75, 62 эв Li+2 - ē=Li+3 J 3=122, 42 эв
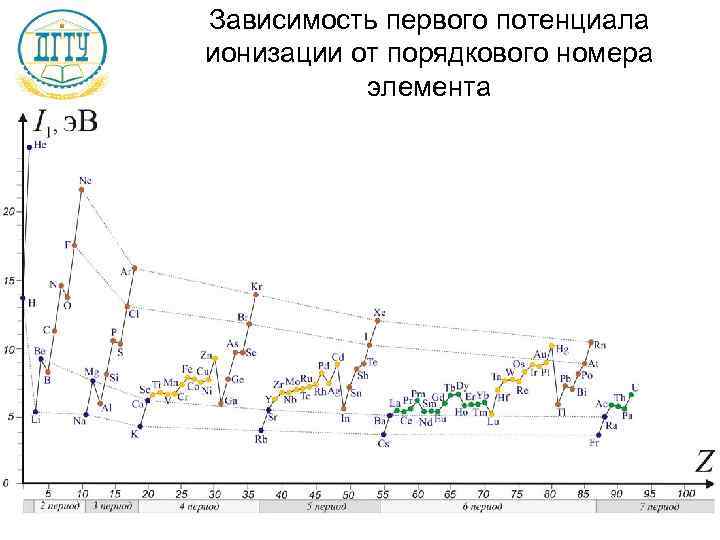
 Зависимость первого потенциала ионизации от порядкового номера элемента
Зависимость первого потенциала ионизации от порядкового номера элемента
 Энергия сродства к электрону Количество энергии, выделяемое нейтральным атомом, находящимся в состоянии с наименьшей энергией, присоединении к нему одного электрона. Э + ē = Э– Изменение сродства к электрону по периоду: Li Be B C N O F Ne Eэв 0, 34 0 0, 13 1, 13 0, 2 1, 48 3, 62 0 Изменение сродства к электрону по подгруппе, э. В: F Cl Br J 3, 62 3, 82 3, 54 3, 24
Энергия сродства к электрону Количество энергии, выделяемое нейтральным атомом, находящимся в состоянии с наименьшей энергией, присоединении к нему одного электрона. Э + ē = Э– Изменение сродства к электрону по периоду: Li Be B C N O F Ne Eэв 0, 34 0 0, 13 1, 13 0, 2 1, 48 3, 62 0 Изменение сродства к электрону по подгруппе, э. В: F Cl Br J 3, 62 3, 82 3, 54 3, 24
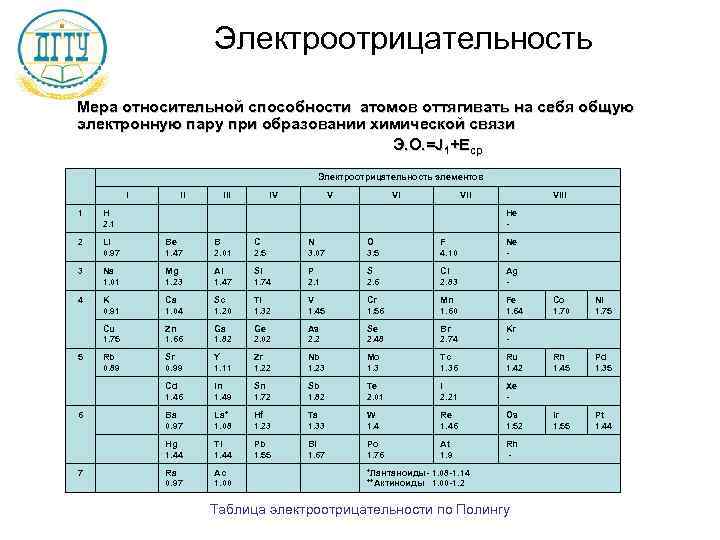
 Электроотрицательность Мера относительной способности атомов оттягивать на себя общую электронную пару при образовании химической связи Э. О. =J 1+Еср Электроотрицательность элементов I II III IV VIII 1 H He 2. 1 - 2 LI Be B C N O F Ne 0. 97 1. 47 2. 01 2. 5 3. 07 3. 5 4. 10 - 3 Na Мg Al Si P S Cl Ag 1. 01 1. 23 1. 47 1. 74 2. 1 2. 6 2. 83 - 4 K Ca Sc Ti V Cr Mn Fe Co Ni 0. 91 1. 04 1. 20 1. 32 1. 45 1. 56 1. 60 1. 64 1. 70 1. 75 Cu Zn Ga Ge As Se Br Kr 1. 75 1. 66 1. 82 2. 02 2. 48 2. 74 - 5 Rb Sr Y Zr Nb Mo Tc Ru Rh Pd 0. 89 0. 99 1. 11 1. 22 1. 23 1. 36 1. 42 1. 45 1. 35 Cd In Sn Sb Te I Xe 1. 46 1. 49 1. 72 1. 82 2. 01 2. 21 - 6 Ba La* Hf Ta W Re Os Ir Pt 0. 97 1. 08 1. 23 1. 33 1. 46 1. 52 1. 55 1. 44 Hg Tl Pb Bi Po At Rh 1. 44 1. 55 1. 67 1. 76 1. 9 - 7 Ra Ac *Лантаноиды- 1. 08 -1. 14 0. 97 1. 00 **Актиноиды 1. 00 -1. 2 Таблица электроотрицательности по Полингу
Электроотрицательность Мера относительной способности атомов оттягивать на себя общую электронную пару при образовании химической связи Э. О. =J 1+Еср Электроотрицательность элементов I II III IV VIII 1 H He 2. 1 - 2 LI Be B C N O F Ne 0. 97 1. 47 2. 01 2. 5 3. 07 3. 5 4. 10 - 3 Na Мg Al Si P S Cl Ag 1. 01 1. 23 1. 47 1. 74 2. 1 2. 6 2. 83 - 4 K Ca Sc Ti V Cr Mn Fe Co Ni 0. 91 1. 04 1. 20 1. 32 1. 45 1. 56 1. 60 1. 64 1. 70 1. 75 Cu Zn Ga Ge As Se Br Kr 1. 75 1. 66 1. 82 2. 02 2. 48 2. 74 - 5 Rb Sr Y Zr Nb Mo Tc Ru Rh Pd 0. 89 0. 99 1. 11 1. 22 1. 23 1. 36 1. 42 1. 45 1. 35 Cd In Sn Sb Te I Xe 1. 46 1. 49 1. 72 1. 82 2. 01 2. 21 - 6 Ba La* Hf Ta W Re Os Ir Pt 0. 97 1. 08 1. 23 1. 33 1. 46 1. 52 1. 55 1. 44 Hg Tl Pb Bi Po At Rh 1. 44 1. 55 1. 67 1. 76 1. 9 - 7 Ra Ac *Лантаноиды- 1. 08 -1. 14 0. 97 1. 00 **Актиноиды 1. 00 -1. 2 Таблица электроотрицательности по Полингу

