Переделанное.ppt
- Количество слайдов: 29
 ДОКЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ. Подготовили: Петрашевская Т. В. и Царенок Т. С. , 8 группа, 3 й курс.
ДОКЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ. Подготовили: Петрашевская Т. В. и Царенок Т. С. , 8 группа, 3 й курс.
 Доклинические исследования эффективности и безопасности лекарственных средств (ЛС) являются необходимым этапом разработки любого нового препарата, или расширения показаний для применения лекарственного средства, уже известного врачам. Они должны проводиться в соответствии с основополагающими этическими принципами Хельсинкской Декларации, Правилами GСP и действующими нормативными требованиями. Государственный контроль эффективности и безопасности ЛС осуществляется в виде 2 х этапов Этапы Дорегистрационный Пострегистрационный Доклинические + клинические (разные фазы) Клинические (разные виды)
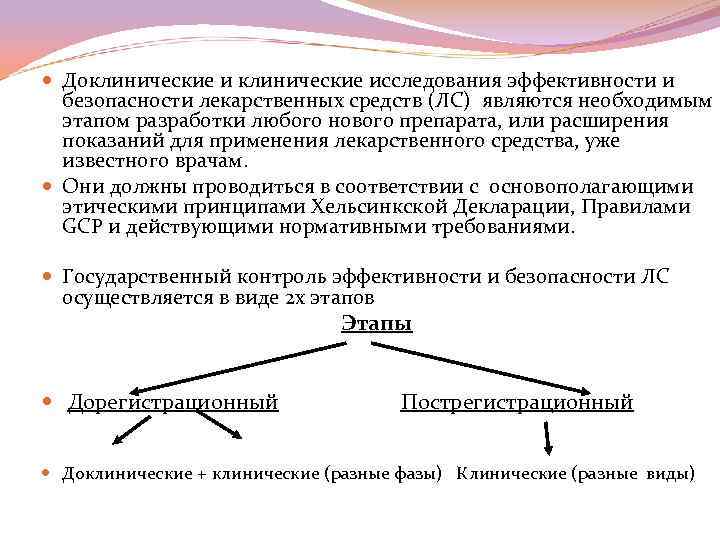
Доклинические исследования эффективности и безопасности лекарственных средств (ЛС) являются необходимым этапом разработки любого нового препарата, или расширения показаний для применения лекарственного средства, уже известного врачам. Они должны проводиться в соответствии с основополагающими этическими принципами Хельсинкской Декларации, Правилами GСP и действующими нормативными требованиями. Государственный контроль эффективности и безопасности ЛС осуществляется в виде 2 х этапов Этапы Дорегистрационный Пострегистрационный Доклинические + клинические (разные фазы) Клинические (разные виды)
 Клинические испытания лекарств имеют 3 фазы: 1) В первой фазе доказывают отсутствие или допустимость токсичности препарата на животных. 2)Во второй фазе исследования исследуют эффективность препарата на животных. Эти 2 фазы – доклинические испытания. Они включают в себя химические, физические, биологические, микробиологические, фармакологические, токсикологические и другие исследования на тканях (in vitro) или на лабораторных животных.
Клинические испытания лекарств имеют 3 фазы: 1) В первой фазе доказывают отсутствие или допустимость токсичности препарата на животных. 2)Во второй фазе исследования исследуют эффективность препарата на животных. Эти 2 фазы – доклинические испытания. Они включают в себя химические, физические, биологические, микробиологические, фармакологические, токсикологические и другие исследования на тканях (in vitro) или на лабораторных животных.
 3)В третьей фазе исследуют эффективность препарата при лечении людей. Организм лабораторных животных отличается от человеческого и по фармакокинетическим характеристикам и по реакции органов и систем на лекарства. Естественно, каждая фаза должна позитивный эффект, в противном случае исследуемый препарат не допускается до проведения следующей фазы.
3)В третьей фазе исследуют эффективность препарата при лечении людей. Организм лабораторных животных отличается от человеческого и по фармакокинетическим характеристикам и по реакции органов и систем на лекарства. Естественно, каждая фаза должна позитивный эффект, в противном случае исследуемый препарат не допускается до проведения следующей фазы.
 Виды клинических исследований Пилотное исследование предназначено для получения предварительных данных, важных для планирования дальнейших этапов исследования (определение возможности проведения исследования у большего числа испытуемых, размера выборки в будущем исследовании, необходимой мощности исследования и т. д. ). Рандомизированное клиническое исследование, в котором пациенты распределяются по группам лечения случайным образом (процедура рандомизации) и имеют одинаковую возможность получить исследуемый или контрольный препарат (препарат сравнения или плацебо). В нерандомизированном исследовании процедура рандомизации не проводится.
Виды клинических исследований Пилотное исследование предназначено для получения предварительных данных, важных для планирования дальнейших этапов исследования (определение возможности проведения исследования у большего числа испытуемых, размера выборки в будущем исследовании, необходимой мощности исследования и т. д. ). Рандомизированное клиническое исследование, в котором пациенты распределяются по группам лечения случайным образом (процедура рандомизации) и имеют одинаковую возможность получить исследуемый или контрольный препарат (препарат сравнения или плацебо). В нерандомизированном исследовании процедура рандомизации не проводится.
 Контролируемое (иногда используется синоним «сравнительное» ) клиническое исследование, в котором исследуемое лекарственное средство, эффективность и безопасность которого до конца еще не изучены, сравнивают с препаратом, эффективность и безопасность которого хорошо известны (препарат сравнения). Это может быть плацебо, стандартная терапия или отсутствие лечения вообще. В неконтролируемом(несравнительном) исследовании группа контроля / сравнения (группа испытуемых, принимающих препарат сравнения) не используется. В более широком смысле под контролируемым исследованием имеется в виду всякое исследование, в котором контролируются (по возможности минимизируются или исключаются) потенциальные источники систематических ошибок (т. е. оно проводится в строгом соответствии с протоколом, мониторируется и т. д. ).
Контролируемое (иногда используется синоним «сравнительное» ) клиническое исследование, в котором исследуемое лекарственное средство, эффективность и безопасность которого до конца еще не изучены, сравнивают с препаратом, эффективность и безопасность которого хорошо известны (препарат сравнения). Это может быть плацебо, стандартная терапия или отсутствие лечения вообще. В неконтролируемом(несравнительном) исследовании группа контроля / сравнения (группа испытуемых, принимающих препарат сравнения) не используется. В более широком смысле под контролируемым исследованием имеется в виду всякое исследование, в котором контролируются (по возможности минимизируются или исключаются) потенциальные источники систематических ошибок (т. е. оно проводится в строгом соответствии с протоколом, мониторируется и т. д. ).
 При проведении параллельных исследованиях испытуемые в различных группах получают либо только изучаемое лекарственное средство, либо только препарат сравнения / плацебо. В перекрестных исследованиях каждый пациент получает оба сравниваемых препарата, как правило, в случайной последовательности. Исследование может быть открытым, когда все участники исследования знают, какой препарат получает пациент, и слепым (замаскированным), когда одна (простое слепое исследование) или несколько сторон, принимающих участие в исследовании (двойное слепое, тройное слепое или полное слепое исследование) держатся в неведении относительно распределения пациентов по группам лечения.
При проведении параллельных исследованиях испытуемые в различных группах получают либо только изучаемое лекарственное средство, либо только препарат сравнения / плацебо. В перекрестных исследованиях каждый пациент получает оба сравниваемых препарата, как правило, в случайной последовательности. Исследование может быть открытым, когда все участники исследования знают, какой препарат получает пациент, и слепым (замаскированным), когда одна (простое слепое исследование) или несколько сторон, принимающих участие в исследовании (двойное слепое, тройное слепое или полное слепое исследование) держатся в неведении относительно распределения пациентов по группам лечения.
 Проспективное исследование проводится с делением участников на группы, которые будут или не будут получать исследуемое лекарственное средство, до того, как наступили исходы. В отличие от него, в ретроспективном (историческом) исследовании изучаются исходы проведенных ранее клинических исследований, то есть исходы наступают до того, как начато исследование.
Проспективное исследование проводится с делением участников на группы, которые будут или не будут получать исследуемое лекарственное средство, до того, как наступили исходы. В отличие от него, в ретроспективном (историческом) исследовании изучаются исходы проведенных ранее клинических исследований, то есть исходы наступают до того, как начато исследование.
 В зависимости от количества исследовательских центров, в которых проводится исследование в соответствии с единым протоколом, исследования бывают одноцентровыми и многоцентровыми. Если исследование проводится в нескольких странах, его называют международным. В параллельном исследовании сравниваются две или более группы испытуемых, одна или более из которых получают исследуемый препарат, а одна группа является контрольной. В некоторых параллельных исследованиях сравнивают различные виды лечения, без включения контрольной группы. (Такой дизайн называют дизайном независимых групп).
В зависимости от количества исследовательских центров, в которых проводится исследование в соответствии с единым протоколом, исследования бывают одноцентровыми и многоцентровыми. Если исследование проводится в нескольких странах, его называют международным. В параллельном исследовании сравниваются две или более группы испытуемых, одна или более из которых получают исследуемый препарат, а одна группа является контрольной. В некоторых параллельных исследованиях сравнивают различные виды лечения, без включения контрольной группы. (Такой дизайн называют дизайном независимых групп).
 Когортное исследование — это обсервационное исследование, в котором выделенную группу людей (когорту) наблюдают в течение некоторого времени. Исходы у испытуемых в разных подгруппах данной когорты, тех кто подвергался или не подвергался (или подвергался в разной степени) лечению исследуемым препаратом сравниваются. В проспективном когортном исследовании когорты составляют в настоящем и наблюдают их в будущем. В ретроспективном (или историческом) когортном исследовании когорту подбирают по архивным записям и прослеживают их исходы с того момента по настоящее время. Когортные исследования (cohort trials) не используются для тестирования лекарств, скорее для определения риска факторов воздеиствия, которые не возможно или не этично контролировать (курение, лишний вес и т. д).
Когортное исследование — это обсервационное исследование, в котором выделенную группу людей (когорту) наблюдают в течение некоторого времени. Исходы у испытуемых в разных подгруппах данной когорты, тех кто подвергался или не подвергался (или подвергался в разной степени) лечению исследуемым препаратом сравниваются. В проспективном когортном исследовании когорты составляют в настоящем и наблюдают их в будущем. В ретроспективном (или историческом) когортном исследовании когорту подбирают по архивным записям и прослеживают их исходы с того момента по настоящее время. Когортные исследования (cohort trials) не используются для тестирования лекарств, скорее для определения риска факторов воздеиствия, которые не возможно или не этично контролировать (курение, лишний вес и т. д).
 В исследовании случай-контроль (синоним: исследование сходных случаев) сравнивают людей с определенным заболеванием или исходами ( «случай» ) с людьми из этой же популяции, не страдающими данным заболеванием, или у которых не наблюдался данный исход ( «контроль» ), с целью выявления связи между исходом и предшествующему воздействию определенных рискфакторов. В исследовании серии случаев наблюдают несколько индивидуумов, обычно получающих одинаковое лечение, без использования контрольной группы. В описании случая (синонимы: случай из практики, история заболевания, описание единичного случая) ведется исследование лечения и исхода у одного человека.
В исследовании случай-контроль (синоним: исследование сходных случаев) сравнивают людей с определенным заболеванием или исходами ( «случай» ) с людьми из этой же популяции, не страдающими данным заболеванием, или у которых не наблюдался данный исход ( «контроль» ), с целью выявления связи между исходом и предшествующему воздействию определенных рискфакторов. В исследовании серии случаев наблюдают несколько индивидуумов, обычно получающих одинаковое лечение, без использования контрольной группы. В описании случая (синонимы: случай из практики, история заболевания, описание единичного случая) ведется исследование лечения и исхода у одного человека.
 Двойное слепое рандомизированное плацебо-контролируемое испытание — способ испытания медицинского препарата (или лечебной методики), при котором учитывается и исключается из результатов влияние на пациента как неизвестных факторов, так и факторов психологического влияния. Целью испытания является проверка действия только препарата (или методики) и больше ничего.
Двойное слепое рандомизированное плацебо-контролируемое испытание — способ испытания медицинского препарата (или лечебной методики), при котором учитывается и исключается из результатов влияние на пациента как неизвестных факторов, так и факторов психологического влияния. Целью испытания является проверка действия только препарата (или методики) и больше ничего.
 При испытании медицинского препарата или методики, экспериментаторы обычно не располагают достаточным временем и возможностями, чтобы достоверно установить, производит ли испытываемая методика достаточный эффект, поэтому используются статистические методы в ограниченном клиническом испытании. Многие болезни очень трудны в излечении и врачам приходится бороться за каждый шаг к выздоровлению. Поэтому, при испытании производится наблюдение за множеством симптомов болезни и за тем, как они изменяются при воздействии.
При испытании медицинского препарата или методики, экспериментаторы обычно не располагают достаточным временем и возможностями, чтобы достоверно установить, производит ли испытываемая методика достаточный эффект, поэтому используются статистические методы в ограниченном клиническом испытании. Многие болезни очень трудны в излечении и врачам приходится бороться за каждый шаг к выздоровлению. Поэтому, при испытании производится наблюдение за множеством симптомов болезни и за тем, как они изменяются при воздействии.
 Злую шутку может сыграть тот факт, что многие симптомы не жёстко связаны с болезнью. Они не однозначны для разных людей и подвержены влиянию со стороны психики даже отдельного человека: под воздействием добрых слов врача и/или уверенности врача, степени оптимизма пациента, симптомы и самочувствие могут улучшиться, нередко повышаются объективные показатели иммунитета. Возможен также вариант, когда реального улучшения не будет, но субъективное качество жизни повысится. На симптомы могут оказать влияние неучтённые факторы, такие, как раса пациента, его возраст, пол и др. , что также будет говорить не о действии исследуемого препарата, а о чём-то другом.
Злую шутку может сыграть тот факт, что многие симптомы не жёстко связаны с болезнью. Они не однозначны для разных людей и подвержены влиянию со стороны психики даже отдельного человека: под воздействием добрых слов врача и/или уверенности врача, степени оптимизма пациента, симптомы и самочувствие могут улучшиться, нередко повышаются объективные показатели иммунитета. Возможен также вариант, когда реального улучшения не будет, но субъективное качество жизни повысится. На симптомы могут оказать влияние неучтённые факторы, такие, как раса пациента, его возраст, пол и др. , что также будет говорить не о действии исследуемого препарата, а о чём-то другом.
 Для отсечения этих и других смазывающих влияние лечебной методики эффектов, используются следующие приёмы: • исследование делается плацебо-контролируемым. То есть пациенты делятся на две группы, одна — основная — получает исследуемое лекарство, а другой, контрольной группе даётся плацебо — пустышка. • исследование делается слепым (англ. single blind). То есть пациенты не догадываются, что некоторые из них получают не исследуемое новое лекарство, а плацебо. В результате больные из группы плацебо также думают, что проходят лечение, хотя на самом деле получают пустышку. Поэтому положительная динамика от эффекта плацебо имеет место в обеих группах и выпадает при сравнении.
Для отсечения этих и других смазывающих влияние лечебной методики эффектов, используются следующие приёмы: • исследование делается плацебо-контролируемым. То есть пациенты делятся на две группы, одна — основная — получает исследуемое лекарство, а другой, контрольной группе даётся плацебо — пустышка. • исследование делается слепым (англ. single blind). То есть пациенты не догадываются, что некоторые из них получают не исследуемое новое лекарство, а плацебо. В результате больные из группы плацебо также думают, что проходят лечение, хотя на самом деле получают пустышку. Поэтому положительная динамика от эффекта плацебо имеет место в обеих группах и выпадает при сравнении.
 В двойном слепом (double blind) исследовании не только пациенты, но и врачи и медсёстры, дающие пациентам лекарство, и даже руководство клиники, сами не знают, что они им дают — действительно ли исследуемое лекарство или плацебо. Этим исключается положительное воздействие от уверенности со стороны врачей, руководства клиники и медперсонала.
В двойном слепом (double blind) исследовании не только пациенты, но и врачи и медсёстры, дающие пациентам лекарство, и даже руководство клиники, сами не знают, что они им дают — действительно ли исследуемое лекарство или плацебо. Этим исключается положительное воздействие от уверенности со стороны врачей, руководства клиники и медперсонала.
 Фазы клинических исследований Фаза I. Первый опыт применения нового активного вещества у человека. Чаще всего исследования начинаются у добровольцев (взрослые здоровые мужчины) от 20 до 100 человек. Главная цель исследований — решить, стоит ли продолжать работу над новым препаратом, и, если удастся, установить дозы, которые будут использоваться у пациентов во время II фазы клинических исследований
Фазы клинических исследований Фаза I. Первый опыт применения нового активного вещества у человека. Чаще всего исследования начинаются у добровольцев (взрослые здоровые мужчины) от 20 до 100 человек. Главная цель исследований — решить, стоит ли продолжать работу над новым препаратом, и, если удастся, установить дозы, которые будут использоваться у пациентов во время II фазы клинических исследований
 В ходе этой фазы исследователи получают предварительные данные о безопасности нового препарата и впервые описывают его фармакокинетику и фармакодинамику у человека. Иногда невозможно провести исследования I фазы у здоровых добровольцев из-за токсичности данного препарата (лечение онкологических заболеваний, СПИДа). В этом случае проводятся нетерапевтические исследования с участием пациентов с этой патологией в специализированных учреждениях.
В ходе этой фазы исследователи получают предварительные данные о безопасности нового препарата и впервые описывают его фармакокинетику и фармакодинамику у человека. Иногда невозможно провести исследования I фазы у здоровых добровольцев из-за токсичности данного препарата (лечение онкологических заболеваний, СПИДа). В этом случае проводятся нетерапевтические исследования с участием пациентов с этой патологией в специализированных учреждениях.
 Фазы клинических исследований Фаза II. Обычно это первый опыт применения у пациентов с заболеванием, для лечения которого предполагается использовать препарат. Вторая фаза делится на IIa и IIb.
Фазы клинических исследований Фаза II. Обычно это первый опыт применения у пациентов с заболеванием, для лечения которого предполагается использовать препарат. Вторая фаза делится на IIa и IIb.
 Фаза IIa — это терапевтические пилотные исследования (pilot studies), так как полученные в них результаты обеспечивают оптимальное планирование последующих исследований. Фаза IIb — это более обширные исследования у пациентов с заболеванием, которое является основным показанием к назначению нового лекарственного средства. Главная цель — доказать эффективность и безопасность препарата. Результаты этих исследований (pivotal trial) служат основой для планирования исследований III фазы.
Фаза IIa — это терапевтические пилотные исследования (pilot studies), так как полученные в них результаты обеспечивают оптимальное планирование последующих исследований. Фаза IIb — это более обширные исследования у пациентов с заболеванием, которое является основным показанием к назначению нового лекарственного средства. Главная цель — доказать эффективность и безопасность препарата. Результаты этих исследований (pivotal trial) служат основой для планирования исследований III фазы.
 Фазы клинических исследований Фаза III. Многоцентровые испытания с участием больших (и по возможности, разнообразных) групп пациентов (в среднем 1000– 3000 человек). Основная цель — получение дополнительных данных о безопасности и эффективности различных форм препарата, о характере наиболее частых нежелательных реакций и т. п. Чаще всего клинические исследования этой фазы — двойные слепые контролируемые, рандомизированные, а условия исследований максимально приближены к обычной реальной рутинной медицинской практике. Данные, полученные в клинических исследованиях III фазы, являются основой для создания инструкций по применению препарата и для решения о его регистрации Фармакологическим комитетом.
Фазы клинических исследований Фаза III. Многоцентровые испытания с участием больших (и по возможности, разнообразных) групп пациентов (в среднем 1000– 3000 человек). Основная цель — получение дополнительных данных о безопасности и эффективности различных форм препарата, о характере наиболее частых нежелательных реакций и т. п. Чаще всего клинические исследования этой фазы — двойные слепые контролируемые, рандомизированные, а условия исследований максимально приближены к обычной реальной рутинной медицинской практике. Данные, полученные в клинических исследованиях III фазы, являются основой для создания инструкций по применению препарата и для решения о его регистрации Фармакологическим комитетом.
 Рекомендация к клиническому применению в медицинской практике считается обоснованной, если новый препарат: — более эффективен, чем известные препараты аналогичного действия; — обладает лучшей переносимостью, чем известные препараты (при одинаковой эффективности); — эффективен в тех случаях, когда лечение известными препаратами безуспешно; — более выгоден экономически, имеет более простую методику лечения или более удобную лекарственную форму; — при комбинированной терапии повышает эффективность уже существующих лекарственных средств, не увеличивая их токсичности.
Рекомендация к клиническому применению в медицинской практике считается обоснованной, если новый препарат: — более эффективен, чем известные препараты аналогичного действия; — обладает лучшей переносимостью, чем известные препараты (при одинаковой эффективности); — эффективен в тех случаях, когда лечение известными препаратами безуспешно; — более выгоден экономически, имеет более простую методику лечения или более удобную лекарственную форму; — при комбинированной терапии повышает эффективность уже существующих лекарственных средств, не увеличивая их токсичности.
 Фазы клинических исследований Фаза IV. Исследования проводятся после начала продажи препарата с целью получить более подробную информацию о длительном применении в различных группах пациентов и при различных факторах риска и т. д. и таким образом более полно оценить стратегию применения лекарственного средства. В исследовании принимает участие большое количество пациентов, это позволяет выявить ранее неизвестные и редко встречающиеся нежелательные явления.
Фазы клинических исследований Фаза IV. Исследования проводятся после начала продажи препарата с целью получить более подробную информацию о длительном применении в различных группах пациентов и при различных факторах риска и т. д. и таким образом более полно оценить стратегию применения лекарственного средства. В исследовании принимает участие большое количество пациентов, это позволяет выявить ранее неизвестные и редко встречающиеся нежелательные явления.
 Если лекарственное средство собираются применять по новому показанию, еще не зарегистрированному, то для этого проводятся дополнительные исследования, начиная с фазы II. Наиболее часто на практике проводят открытое исследование, при котором врачу и больному известен способ лечения (исследуемый препарат или препарат сравнения). При испытании простым слепым методом больной не знает, какой препарат он принимает (это может быть плацебо), а при использовании двойного слепого метода об этом не осведомлены ни больной, ни врач, а только руководитель испытания.
Если лекарственное средство собираются применять по новому показанию, еще не зарегистрированному, то для этого проводятся дополнительные исследования, начиная с фазы II. Наиболее часто на практике проводят открытое исследование, при котором врачу и больному известен способ лечения (исследуемый препарат или препарат сравнения). При испытании простым слепым методом больной не знает, какой препарат он принимает (это может быть плацебо), а при использовании двойного слепого метода об этом не осведомлены ни больной, ни врач, а только руководитель испытания.
 В современном клиническом исследовании нового лекарственного средства участвуют четыре стороны: спонсор исследования (чаще всего это фармацевтическая компания-производитель), монитор — контрактная исследовательская организация, врач-исследователь, пациент). Кроме того, возможны тройные слепые исследования, когда ни врач, ни пациент, ни те, кто организует исследование и обрабатывает его данные, не знают назначенного лечения у конкретного пациента.
В современном клиническом исследовании нового лекарственного средства участвуют четыре стороны: спонсор исследования (чаще всего это фармацевтическая компания-производитель), монитор — контрактная исследовательская организация, врач-исследователь, пациент). Кроме того, возможны тройные слепые исследования, когда ни врач, ни пациент, ни те, кто организует исследование и обрабатывает его данные, не знают назначенного лечения у конкретного пациента.
 Если врачи будут знать, какой пациент лечится каким средством, они непроизвольно могут давать оценки лечению в зависимости от своих предпочтений или объяснений. Применение слепых методов повышает достоверность результатов клинического испытания, устраняя влияние субъективных факторов. Если больной знает, что он получает новое многообещающее лекарство, то эффект лечения может быть связан с его успокоением, удовлетворенностью тем, что достигнуто самое желанное лечение из возможных.
Если врачи будут знать, какой пациент лечится каким средством, они непроизвольно могут давать оценки лечению в зависимости от своих предпочтений или объяснений. Применение слепых методов повышает достоверность результатов клинического испытания, устраняя влияние субъективных факторов. Если больной знает, что он получает новое многообещающее лекарство, то эффект лечения может быть связан с его успокоением, удовлетворенностью тем, что достигнуто самое желанное лечение из возможных.
 Плацебо (лат. placere — нравиться, цениться) обозначает препарат, заведомо не обладающий никакими целебными свойствами. Плацебо – это лекарственную форму, содержащую нейтральные вещества. Применяют для изучения роли внушения в лечебном эффекте какого-либо лекарственного вещества, в качестве контроля при исследовании эффективности новых лекарственных препаратов
Плацебо (лат. placere — нравиться, цениться) обозначает препарат, заведомо не обладающий никакими целебными свойствами. Плацебо – это лекарственную форму, содержащую нейтральные вещества. Применяют для изучения роли внушения в лечебном эффекте какого-либо лекарственного вещества, в качестве контроля при исследовании эффективности новых лекарственных препаратов
 Считается, что серьезное изучение эффектов плацебо началось в США во время Второй мировой ны. Фронтовым госпиталям очень не хватало обез боливающих и наркотических средств. Убедившись в который раз, что инъекция физиологического раствора обладает эффектом практически такой же выраженности, что и у морфина, анестезиолог Генри Бичер (Henry Beecher), вернувшись на родину, с группой коллег из Гарвардского университета приступил к изучению этого феномена. В 1955 г. он подытожил свои наблюдения в статье «Сильнодействующее плацебо» , где утверждал, что плацебо может «вызывать значительные физиологические изменения» , включая «объективные эффекты в органахмишенях, которые могут быть более выраженными, чем вследствие сильного фармакологического воздействия» .
Считается, что серьезное изучение эффектов плацебо началось в США во время Второй мировой ны. Фронтовым госпиталям очень не хватало обез боливающих и наркотических средств. Убедившись в который раз, что инъекция физиологического раствора обладает эффектом практически такой же выраженности, что и у морфина, анестезиолог Генри Бичер (Henry Beecher), вернувшись на родину, с группой коллег из Гарвардского университета приступил к изучению этого феномена. В 1955 г. он подытожил свои наблюдения в статье «Сильнодействующее плацебо» , где утверждал, что плацебо может «вызывать значительные физиологические изменения» , включая «объективные эффекты в органахмишенях, которые могут быть более выраженными, чем вследствие сильного фармакологического воздействия» .
 Спасибо за внимание! Мы ( )очень старались! =)
Спасибо за внимание! Мы ( )очень старались! =)


