de825390202fa8db823af59bf4e1a25e.ppt
- Количество слайдов: 26

Доклад «Подтверждение соответствия лекарственных средств в КР» Урмамбетова Жумакан Самыйбековна Заведующая отделом сертификации лекарственных средств Заместитель руководителя органа по сертификации лекарственных средств Департамента лекарственного обеспечения и медицинской техники

n n Главная задача государственной системы контроля качества лекарственных средств – это защита потребителя от фальсифицированных и недоброкачественных лекарственных средств. Один из рычагов оценки соответствия лекарственных средств по показателям качества эффективности и безопасности является обязательная сертификация.

Орган по сертификации лекарственных средств создан в 2004 г. на базе Департамента лекарственного обеспечения и медицинской техники при МЗ КР Аттестат аккредитации (№KG 417/01. ОСП. 002. )

Сертификация лекарственных средств n процедура подтверждения соответствия лекарственных средств, посредством которой независимая от изготовителя (продавца) и потребителя (покупателя) аккредитованная организация удостоверяет в письменной форме, что продукция соответствует установленным нормативными документами требованиям.

Основная нормативно-правовая база сертификации ЛС n n n n Закон КР «Об охране здоровья народа Кыргызской Республики» Закон КР «О лекарственных средствах» Закон КР «Об основах технического регулирования» Постановление Правительства КР № 639 от 30. 12. 05 «Об обязательном подтверждении соответствия» Постановление Правительства КР № 8 от 11. 06 «О порядке ввоза для обращения на территории Кыргызской Республики продукции, подлежащей обязательному подтверждению соответствия, и о признании результатов обязательного подтверждения соответствия продукции, полученных за пределами Кыргызской Республики» Постановление Правительства Кыргызской Республики от 23 декабря 2007 года № 512 «Об обязательном подтверждении соответствия продукции в форме принятия декларации о соответствии» . Постановление Правительства Кыргызской Республики от 18 февраля 2009 года № 128 «О внесении изменений и дополнений в некоторые решения Правительства Кыргызской Республики»

Основные цели обязательной сертификации ЛС n n n обеспечение безопасности лекарственных средств для жизни и здоровья людей, охраны окружающей среды; защита интересов потребителей в вопросах безопасности лекарственных средств; обеспечение конкурентоспособности лекарственных средств на внутреннем и внешнем рынке.

Сертификация ЛС позволяет: n n n проверить происхождение продукции; соответствие продукции наименованию, указанному в сопроводительной документации; принадлежность к данной партии и к классификационной группировке Провести анализ ввезенных ЛС на соответствие надлежащим требованиям по срокам годности полно и достоверно подтвердить соответствие ЛС требованиям, на соответствие которым производится её сертификация.
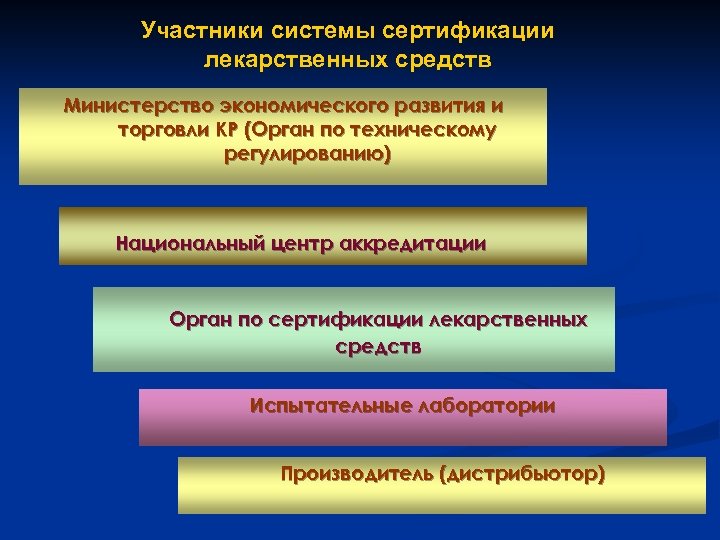
Участники системы сертификации лекарственных средств Министерство экономического развития и торговли КР (Орган по техническому регулированию) Национальный центр аккредитации Орган по сертификации лекарственных средств Испытательные лаборатории Производитель (дистрибьютор)
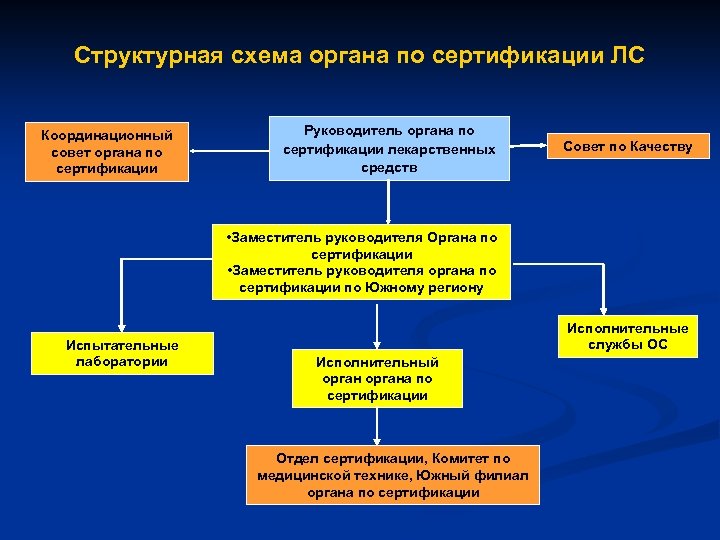
Структурная схема органа по сертификации ЛС Координационный совет органа по сертификации Руководитель органа по сертификации лекарственных средств Совет по Качеству • Заместитель руководителя Органа по сертификации • Заместитель руководителя органа по сертификации по Южному региону Испытательные лаборатории Исполнительные службы ОС Исполнительный органа по сертификации Отдел сертификации, Комитет по медицинской технике, Южный филиал органа по сертификации
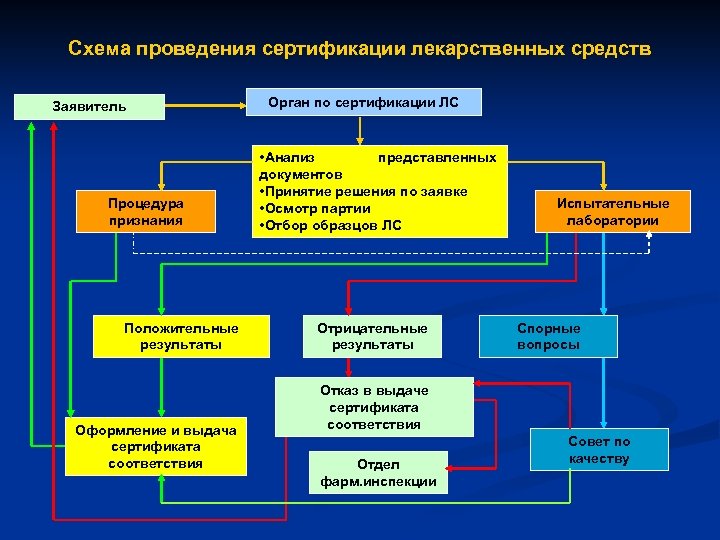
Схема проведения сертификации лекарственных средств Заявитель Процедура признания Положительные результаты Оформление и выдача сертификата соответствия Орган по сертификации ЛС • Анализ представленных документов • Принятие решения по заявке • Осмотр партии • Отбор образцов ЛС Отрицательные результаты Испытательные лаборатории Спорные вопросы Отказ в выдаче сертификата соответствия Отдел фарм. инспекции Совет по качеству
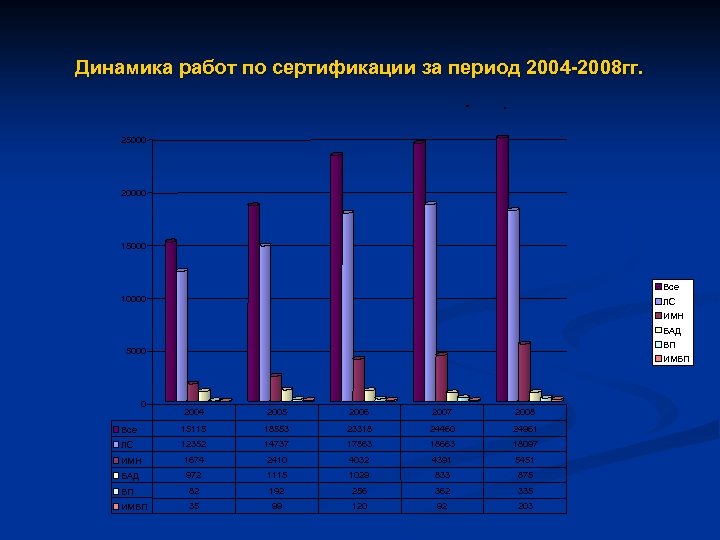
Динамика работ по сертификации за период 2004 -2008 гг. - . 25000 20000 15000 Все 10000 ЛС ИМН БАД ВП 5000 0 ИМБП 2004 2005 2006 2007 2008 Все 15115 18553 23318 24460 24961 ЛС 12352 14737 17863 18663 18097 ИМН 1674 2410 4032 4391 5451 БАД 972 1115 1029 833 875 ВП 82 192 256 362 335 ИМБП 35 99 120 92 203

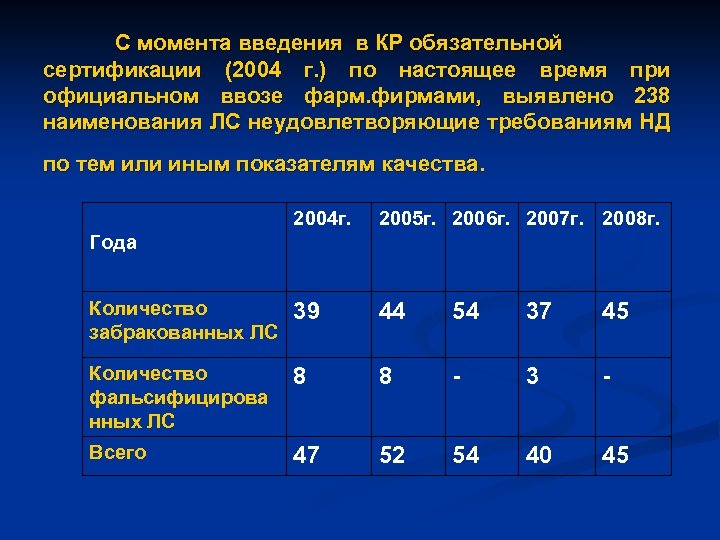
С момента введения в КР обязательной сертификации (2004 г. ) по настоящее время при официальном ввозе фарм. фирмами, выявлено 238 наименования ЛС неудовлетворяющие требованиям НД по тем или иным показателям качества. 2004 г. 2005 г. 2006 г. 2007 г. 2008 г. Количество забракованных ЛС 39 44 54 37 45 Количество фальсифицирова нных ЛС 8 8 - 3 - Всего 47 52 54 40 45 Года


Сравнительные данные по структуре забракованных ЛС по странам производителям за период 2004 -2008 гг.
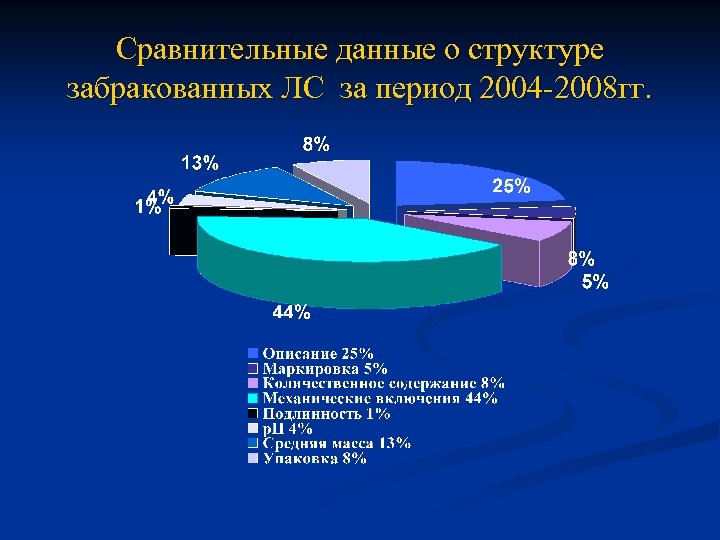
Сравнительные данные о структуре забракованных ЛС за период 2004 -2008 гг.

Автоматизированная программа по сертификации ЛС n n n сбор, систематизация и обработка данных по завозимым в республику ЛС ; оперативное формирование всех видов отчетов; мониторинг ЛС поступивших на сертификацию по различным критериям; обеспечение прозрачности проведения процедуры сертификации; упрощение процедуры сертификации (автоматизация всех этапов от подачи заявки до выдачи сертификатов соответствия)
Автоматизированная программа по сертификации 2 этап
Автоматизированная программа по сертификации 5 этап
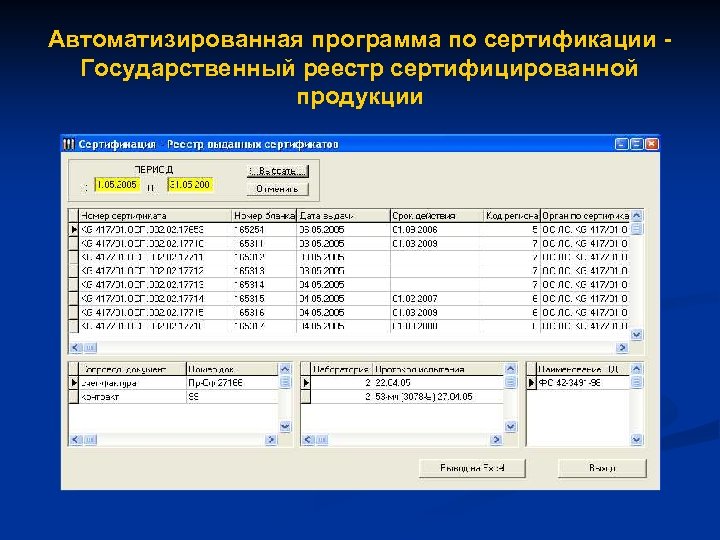
Автоматизированная программа по сертификации Государственный реестр сертифицированной продукции
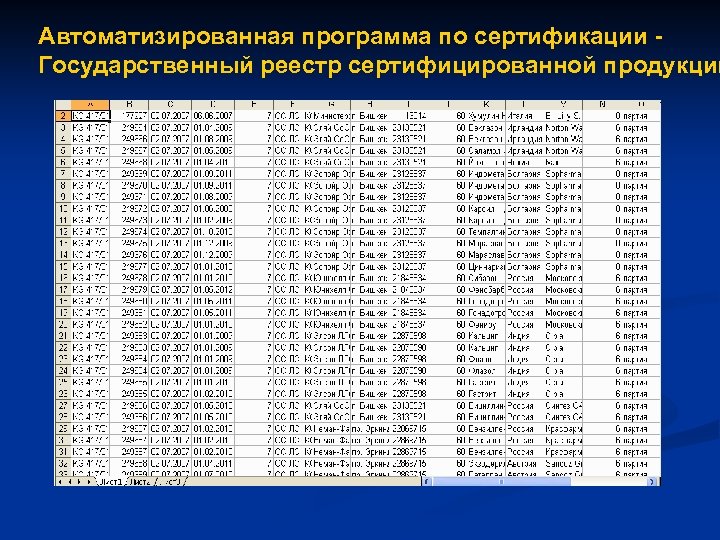
Автоматизированная программа по сертификации Государственный реестр сертифицированной продукции

Информационное обеспечение n n n Оптовым фармацевтическим фирмам регулярно предоставляется информация о забракованных ЛС ОС ДЛО и МТ, а также о забракованных и фальсифицированных ЛС России, полученные через официальные интернет-сайты: www. drugreg. ru; www. regmed. ru Проведение мониторинга сертифицированных ЛС, по разным критериям (по объемам ввоза в натуральном и стоимостном выражении, по наименованиям, по заводампроизводителям, по фармакологическим группам и др. критериям) Предоставление информации по сертифицированным ЛС по запросам компетентных учреждений для проведения мониторинга доступности жизненно-важных ЛС и др. целей.
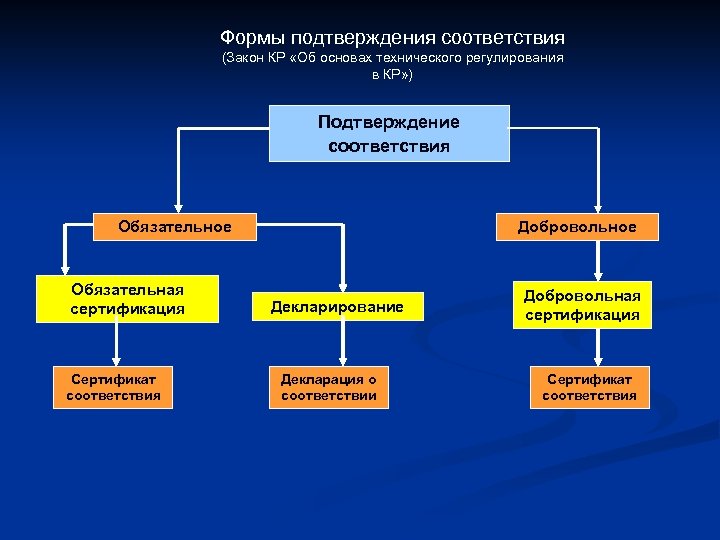
Формы подтверждения соответствия (Закон КР «Об основах технического регулирования в КР» ) Подтверждение соответствия Обязательное Обязательная сертификация Сертификат соответствия Добровольное Декларирование Декларация о соответствии Добровольная сертификация Сертификат соответствия

Декларирование соответствия n форма подтверждения соответствия, посредством которой изготовитель (поставщик) документально удостоверяет, что продукция соответствует требованиям технических регламентов

В соответствии с Постановлением Правительства КР № 512 от 23. 10. 07 «Об обязательном подтверждении соответствия продукции в форме принятия декларации о соответствии» декларация о соответствии принимается изготовителем или торговым представителем (дилер) в отношении следующих позиций: Наименование продукции Код ТН ВЭД Линзы контактные 9001 30 000 0 Тара для лекарственных средств (флаконы, банки, бутылки) емкостью не более 0, 055 литров 7010 90 790 0 3822 00 0 Реагенты диагностические или лабораторные на подложке или без нее

Благодарю за внимание!
de825390202fa8db823af59bf4e1a25e.ppt