ДОЦЕНТ КАФЕДРЫ ПАТОФИЗИОЛОГИИ РЫСПЕКОВА Н. Н





























Доклад эксперименты на животных.ppt
- Количество слайдов: 30
 ДОЦЕНТ КАФЕДРЫ ПАТОФИЗИОЛОГИИ РЫСПЕКОВА Н. Н
ДОЦЕНТ КАФЕДРЫ ПАТОФИЗИОЛОГИИ РЫСПЕКОВА Н. Н
 Исследования на животных Проводятся с целью • установления закономерностей возникновения, развития, течения, исходов различных болезней • разработки и проверки эффективности новых методов профилактики и лечения • создания новых лекарственных препаратов
Исследования на животных Проводятся с целью • установления закономерностей возникновения, развития, течения, исходов различных болезней • разработки и проверки эффективности новых методов профилактики и лечения • создания новых лекарственных препаратов
 Используются разные виды животных: собаки, кошки, кролики, морские свинки и, чаще всего, лабораторные крысы и мыши. Из всех тест-систем наиболее доступны линейные лабораторные крысы и мыши
Используются разные виды животных: собаки, кошки, кролики, морские свинки и, чаще всего, лабораторные крысы и мыши. Из всех тест-систем наиболее доступны линейные лабораторные крысы и мыши
 В настоящее время проведение исследований на лабораторных животных регламентируется следующими основными нормативными правовыми актами и методическими документами: • Приказ Министра здравоохранения Республики Казахстан от 12 ноября 2009 года № 697 • «Об утверждении Правил проведения медико- биологических экспериментов, доклинических (неклинических) и клинических исследований» • Приказ Министра здравоохранения Республики Казахстан от 14 февраля 2005 года N 51 «Об утверждении Инструкции по проведению доклинических исследований и (или) испытаний фармакологических и лекарственных средств в
В настоящее время проведение исследований на лабораторных животных регламентируется следующими основными нормативными правовыми актами и методическими документами: • Приказ Министра здравоохранения Республики Казахстан от 12 ноября 2009 года № 697 • «Об утверждении Правил проведения медико- биологических экспериментов, доклинических (неклинических) и клинических исследований» • Приказ Министра здравоохранения Республики Казахстан от 14 февраля 2005 года N 51 «Об утверждении Инструкции по проведению доклинических исследований и (или) испытаний фармакологических и лекарственных средств в
 • Госстандарт Республики Казахстан «Надлежащая лабораторная практика. Основные положения» , утвержденные приказом Министра индустрии и торговли РК от 29 декабря 2006 года № 575; • Приказ и. о. Министра здравоохранения РК от 13 января 2004 года № 19 «Санитарно- эпидемиологические требования к сбору, использованию, обезвреживанию, транспортировке, хранению и захоронению отходов медицинских организаций» , зарегистрированных в реестре государственного регистра нормативно- правовых актов под № 2674
• Госстандарт Республики Казахстан «Надлежащая лабораторная практика. Основные положения» , утвержденные приказом Министра индустрии и торговли РК от 29 декабря 2006 года № 575; • Приказ и. о. Министра здравоохранения РК от 13 января 2004 года № 19 «Санитарно- эпидемиологические требования к сбору, использованию, обезвреживанию, транспортировке, хранению и захоронению отходов медицинских организаций» , зарегистрированных в реестре государственного регистра нормативно- правовых актов под № 2674
 • Целью этих документов является создание единых требований к планированию, проведению, документальному оформлению и контролю доклинических исследований, медико- биологических экспериментов, а также обеспечение достоверности и точности получаемой в ходе исследования информации.
• Целью этих документов является создание единых требований к планированию, проведению, документальному оформлению и контролю доклинических исследований, медико- биологических экспериментов, а также обеспечение достоверности и точности получаемой в ходе исследования информации.
 • Медико-биологический эксперимент - установление закономерностей возникновения различных болезней, механизмов их развития, разработка и проверка эффективности новых методов профилактики и лечения • Доклиническое исследование лекарственных препаратов
• Медико-биологический эксперимент - установление закономерностей возникновения различных болезней, механизмов их развития, разработка и проверка эффективности новых методов профилактики и лечения • Доклиническое исследование лекарственных препаратов
 Медико-биологический эксперимент выполняет следующие основные функции: 1. выступает средством получения новых научных данных 2. является способом выделения общего в серии сходных явлений, обоснования закономерностей, формирования гипотез 3. выступает средством проверки гипотез и теорий, критерием их истинности, основой для выдвижения новых гипотез 4. является относительным гарантом перед применением новых методов диагностики и лечения болезней в клинической практике
Медико-биологический эксперимент выполняет следующие основные функции: 1. выступает средством получения новых научных данных 2. является способом выделения общего в серии сходных явлений, обоснования закономерностей, формирования гипотез 3. выступает средством проверки гипотез и теорий, критерием их истинности, основой для выдвижения новых гипотез 4. является относительным гарантом перед применением новых методов диагностики и лечения болезней в клинической практике
 Требования к модели: 1) аналогия причин и условий, вызывающих болезнь и примененных при ее моделировании 2) сходство функциональных и морфологических изменений болезни и ее модели на системном, органном, клеточном и молекулярном уровнях 3) сходство в развитии типичных осложнений 4) эффективность лечения одними и теми же воздействиями
Требования к модели: 1) аналогия причин и условий, вызывающих болезнь и примененных при ее моделировании 2) сходство функциональных и морфологических изменений болезни и ее модели на системном, органном, клеточном и молекулярном уровнях 3) сходство в развитии типичных осложнений 4) эффективность лечения одними и теми же воздействиями
 • Доклиническое исследование лекарственных препаратов (неклиническое)- комплекс биологических, токсикологических, химических, физических и других экспериментальных научных исследований, проводимых перед внедрением в клиническую практику
• Доклиническое исследование лекарственных препаратов (неклиническое)- комплекс биологических, токсикологических, химических, физических и других экспериментальных научных исследований, проводимых перед внедрением в клиническую практику
 • Доклинические испытания проходят по системе GLP - Good Laboratory Practice (надлежащая лабораторная практика) – система международных стандартов, на основе которых осуществляется планирование, проведение лабораторных исследований и написание отчётов по их итогам. Следование этим правилам обеспечивает достоверность данных и точную воспроизводимость эксперимента в будущем)
• Доклинические испытания проходят по системе GLP - Good Laboratory Practice (надлежащая лабораторная практика) – система международных стандартов, на основе которых осуществляется планирование, проведение лабораторных исследований и написание отчётов по их итогам. Следование этим правилам обеспечивает достоверность данных и точную воспроизводимость эксперимента в будущем)
 • Первый вариант международных правил GLP в 1978 г. Организация экономического сотрудничества и развития (OECD). • американские специалисты, представители девяти развитых стран, Комиссии ЕС, ВОЗ и ИСО. • В 1981 г. OECD сформулировала принципы GLP, которые в 1987 г. стали обязательными для всех стран ЕС.
• Первый вариант международных правил GLP в 1978 г. Организация экономического сотрудничества и развития (OECD). • американские специалисты, представители девяти развитых стран, Комиссии ЕС, ВОЗ и ИСО. • В 1981 г. OECD сформулировала принципы GLP, которые в 1987 г. стали обязательными для всех стран ЕС.
 • OECD подготовила также Методическое руководство по проведению инспектирования лабораторий и аудита исследований • В странах ЕС, США и Японии существуют специальные научно-исследовательские центры, осуществляющие доклинические исследования на должном техническом уровне и в соответствии со стандартами (GLP и др. ) Деятельность их контролируется не только нормативно-правовой базой отдельного государства, но и общественной международной организацией Regulatory Affairs Professional Society
• OECD подготовила также Методическое руководство по проведению инспектирования лабораторий и аудита исследований • В странах ЕС, США и Японии существуют специальные научно-исследовательские центры, осуществляющие доклинические исследования на должном техническом уровне и в соответствии со стандартами (GLP и др. ) Деятельность их контролируется не только нормативно-правовой базой отдельного государства, но и общественной международной организацией Regulatory Affairs Professional Society
 • В ЕС к проведению доклинических и научных экспериментов на животных допускаются студенты и исследователи, прошедшие обязательный курс обучения (Laboratory Animal Science) и получившие соответствующую лицензию.
• В ЕС к проведению доклинических и научных экспериментов на животных допускаются студенты и исследователи, прошедшие обязательный курс обучения (Laboratory Animal Science) и получившие соответствующую лицензию.
 Национальные стандарты GLP регулируют • обязанности руководителей лабораторий, подбор и организацию персонала • обязанности сотрудников Программы обеспечения качества • порядок проверки лабораторий на соответствие установленным требованиям • порядок записи, обработки и архивирования данных, соблюдение конфиденциальности в отношении любых данных, полученных в ходе доклинических исследований • оснащенность лаборатории приборами, аппаратурой и реактивами, соответствующими стандартам качества
Национальные стандарты GLP регулируют • обязанности руководителей лабораторий, подбор и организацию персонала • обязанности сотрудников Программы обеспечения качества • порядок проверки лабораторий на соответствие установленным требованиям • порядок записи, обработки и архивирования данных, соблюдение конфиденциальности в отношении любых данных, полученных в ходе доклинических исследований • оснащенность лаборатории приборами, аппаратурой и реактивами, соответствующими стандартам качества
 • условия передачи, хранения и учета исследуемого лекарственного вещества • этические и правовые нормы доклинического изучения вещества • вид, пол и количество животных, рекомендованных для проведения исследований • тип наркоза и гуманный способ умерщвления животных • критерии включения животных в исследование и их исключения из него • методы распределения животных по группам, размеры и материал клетки, количество содержащихся в ней животных • требования к источнику воды, температуре воздуха, влажности, условиям кондиционирования помещения и т. д.
• условия передачи, хранения и учета исследуемого лекарственного вещества • этические и правовые нормы доклинического изучения вещества • вид, пол и количество животных, рекомендованных для проведения исследований • тип наркоза и гуманный способ умерщвления животных • критерии включения животных в исследование и их исключения из него • методы распределения животных по группам, размеры и материал клетки, количество содержащихся в ней животных • требования к источнику воды, температуре воздуха, влажности, условиям кондиционирования помещения и т. д.
 Порядок проведения доклинических исследований • Уполномоченный орган выдает разрешение на проведение доклинических исследований, на основании заявления Заказчика в произвольной форме. • Доклинические исследования осуществляются на договорных условиях между Заказчиком и Исполнителем. • Договор о проведении доклинических исследований должен содержать: 1) объемы и сроки проведения доклинических исследований 2) общую стоимость программы доклинических исследований и условия оплаты.
Порядок проведения доклинических исследований • Уполномоченный орган выдает разрешение на проведение доклинических исследований, на основании заявления Заказчика в произвольной форме. • Доклинические исследования осуществляются на договорных условиях между Заказчиком и Исполнителем. • Договор о проведении доклинических исследований должен содержать: 1) объемы и сроки проведения доклинических исследований 2) общую стоимость программы доклинических исследований и условия оплаты.
 • Для проведения доклинического исследования Заказчик предоставляет Исполнителю необходимые материалы, испытываемое вещество, при необходимости, вещество для сравнения, документацию, с указанием температурного режима, условий и сроков хранения испытываемого вещества, данные по стабильности, информацию о растворителях и процедурах растворения, о мерах по обеспечению безопасности работы, а также если необходимо, устройства для введения вещества.
• Для проведения доклинического исследования Заказчик предоставляет Исполнителю необходимые материалы, испытываемое вещество, при необходимости, вещество для сравнения, документацию, с указанием температурного режима, условий и сроков хранения испытываемого вещества, данные по стабильности, информацию о растворителях и процедурах растворения, о мерах по обеспечению безопасности работы, а также если необходимо, устройства для введения вещества.
 • Руководителем исследования назначается ответственный исполнитель. • Для каждого вида (или категории) исследования до его начала, ответственный исполнитель разрабатывает протокол доклинического исследования, который согласовывается с руководителем исследования и заказчиком.
• Руководителем исследования назначается ответственный исполнитель. • Для каждого вида (или категории) исследования до его начала, ответственный исполнитель разрабатывает протокол доклинического исследования, который согласовывается с руководителем исследования и заказчиком.
 Протокол № ____ доклинического исследования безопасности лекарственного средства ____________________________ наименование Референтное вещество__________________ Заказчик________________________ ____________________________ название учреждения, адрес Исполнитель_______________________ ____________________________ название учреждения, адрес Наименование испытания_________________ Срок исполнения: дата начала испытания__________ дата завершения испытания________________ Ответственный исполнитель________________ В работе принимали участие (с указанием обязанностей): _______ _________________________________________________________ _____________________________
Протокол № ____ доклинического исследования безопасности лекарственного средства ____________________________ наименование Референтное вещество__________________ Заказчик________________________ ____________________________ название учреждения, адрес Исполнитель_______________________ ____________________________ название учреждения, адрес Наименование испытания_________________ Срок исполнения: дата начала испытания__________ дата завершения испытания________________ Ответственный исполнитель________________ В работе принимали участие (с указанием обязанностей): _______ _________________________________________________________ _____________________________
 Общая информация об исследовании 1. Название исследования. 2. Методика изучения, используемые аппаратура и реактивы. 3. Вид животных, которые использовались в исследованиях, их количество. 4. Вид наркоза. 5. Пути введения лекарственных средств, дозы. 6. Способ гуманного умерщвления животных после проведения исследований. 7. Детальный план проведения исследования, с указанием продолжительности этапов и сроков. Содержание 1. Цель исследования. 2. Задача исследования. 3. Вещество, которое изучается. 4. Вещество для сравнения. 5. Обоснование избранной схемы исследования. 6. Характеристика подопытных животных.
Общая информация об исследовании 1. Название исследования. 2. Методика изучения, используемые аппаратура и реактивы. 3. Вид животных, которые использовались в исследованиях, их количество. 4. Вид наркоза. 5. Пути введения лекарственных средств, дозы. 6. Способ гуманного умерщвления животных после проведения исследований. 7. Детальный план проведения исследования, с указанием продолжительности этапов и сроков. Содержание 1. Цель исследования. 2. Задача исследования. 3. Вещество, которое изучается. 4. Вещество для сравнения. 5. Обоснование избранной схемы исследования. 6. Характеристика подопытных животных.
 7. Материалы исследования: 1) описание препарата, которое изучается; 2) условия хранения исследуемого лекарственного средства; 3) условия передачи, учета и возвращения лекарственного средства. 8. Структура исследования: 1) общий план исследования; 2) критерии включения, исключения и выбытия животных из исследования. 9. Схема применения исследуемого вещества: 1) способ и пути введения; 2) способ и пути введения вещества для сравнения. 10. Методы, которые используются при проведении исследования. 11. Оценка эффективности исследуемого вещества. 12. Этические и правовые нормы доклинического изучения исследуемого вещества. 13. Использование полученной информации и право на публикацию результатов проведенных исследований. 14. Поправки к протоколу доклинического исследования специфической активности исследуемого вещества. 15. Обработка результатов исследования. 16. Составление отчета. 17. Использованная литература.
7. Материалы исследования: 1) описание препарата, которое изучается; 2) условия хранения исследуемого лекарственного средства; 3) условия передачи, учета и возвращения лекарственного средства. 8. Структура исследования: 1) общий план исследования; 2) критерии включения, исключения и выбытия животных из исследования. 9. Схема применения исследуемого вещества: 1) способ и пути введения; 2) способ и пути введения вещества для сравнения. 10. Методы, которые используются при проведении исследования. 11. Оценка эффективности исследуемого вещества. 12. Этические и правовые нормы доклинического изучения исследуемого вещества. 13. Использование полученной информации и право на публикацию результатов проведенных исследований. 14. Поправки к протоколу доклинического исследования специфической активности исследуемого вещества. 15. Обработка результатов исследования. 16. Составление отчета. 17. Использованная литература.
 Лабораторные животные и условия их содержания • Вид - • Порода - • Пол - • Масса тела - • Общее количество - • Источник получения - • Дата получения - • Период акклиматизации - • Индивидуальная идентификация - (СОП № ______) • Метод распределения по группам - (СОП № ______) • Количество животных в клетке - • Размеры клетки - • Материал клетки - • Основной рацион - • Источник воды - • Температура воздуха - • Влажность воздуха -
Лабораторные животные и условия их содержания • Вид - • Порода - • Пол - • Масса тела - • Общее количество - • Источник получения - • Дата получения - • Период акклиматизации - • Индивидуальная идентификация - (СОП № ______) • Метод распределения по группам - (СОП № ______) • Количество животных в клетке - • Размеры клетки - • Материал клетки - • Основной рацион - • Источник воды - • Температура воздуха - • Влажность воздуха -
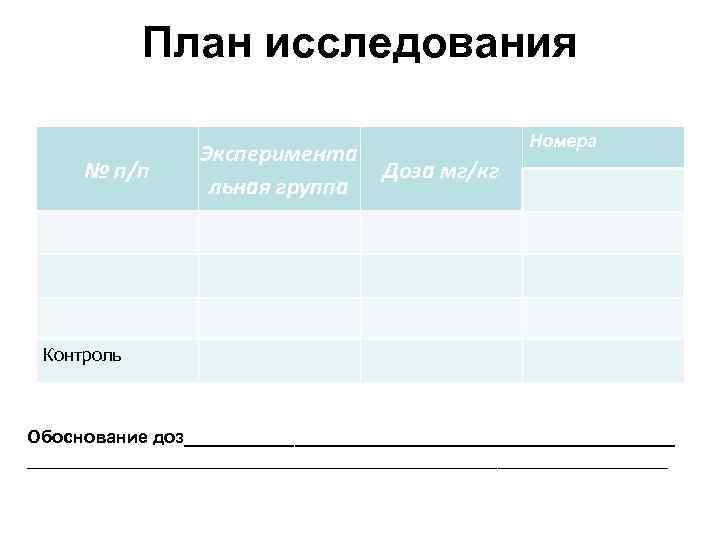
 План исследования Номера Эксперимента № п/п Доза мг/кг льная группа Контроль Обоснование доз________________________________
План исследования Номера Эксперимента № п/п Доза мг/кг льная группа Контроль Обоснование доз________________________________
 Условия эксперимента Частота введений - Путь введения - Способ введения (СОП №______) Подготовка препарата для введения - Режим дозирования - Носитель (растворитель) -
Условия эксперимента Частота введений - Путь введения - Способ введения (СОП №______) Подготовка препарата для введения - Режим дозирования - Носитель (растворитель) -
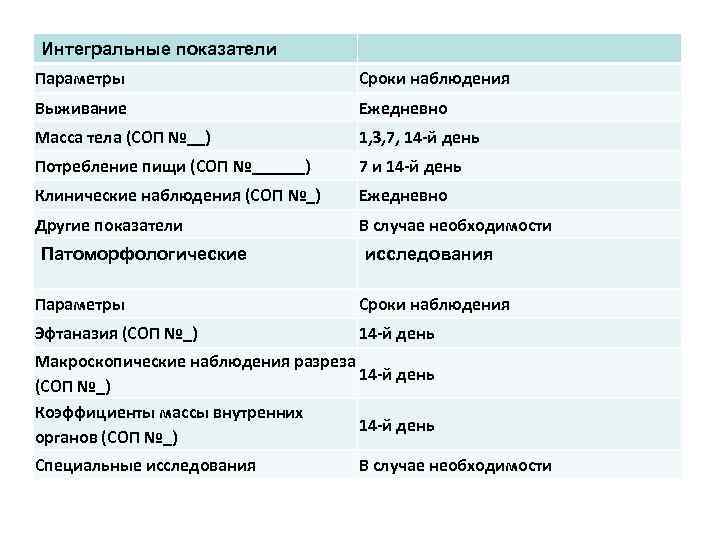
 Интегральные показатели Параметры Сроки наблюдения Выживание Ежедневно Масса тела (СОП №__) 1, 3, 7, 14 -й день Потребление пищи (СОП №______) 7 и 14 -й день Клинические наблюдения (СОП №_) Ежедневно Другие показатели В случае необходимости Патоморфологические исследования Параметры Сроки наблюдения Эфтаназия (СОП №_) 14 -й день Макроскопические наблюдения разреза 14 -й день (СОП №_) Коэффициенты массы внутренних 14 -й день органов (СОП №_) Специальные исследования В случае необходимости
Интегральные показатели Параметры Сроки наблюдения Выживание Ежедневно Масса тела (СОП №__) 1, 3, 7, 14 -й день Потребление пищи (СОП №______) 7 и 14 -й день Клинические наблюдения (СОП №_) Ежедневно Другие показатели В случае необходимости Патоморфологические исследования Параметры Сроки наблюдения Эфтаназия (СОП №_) 14 -й день Макроскопические наблюдения разреза 14 -й день (СОП №_) Коэффициенты массы внутренних 14 -й день органов (СОП №_) Специальные исследования В случае необходимости
 Статистическая обработка данных Параметры токсичности______________________ _____________________________ Масса тела________________________ Масса внутренних органов_________________ Процедура случайной выборки_______________ __________________________ Ответственные исполнители Ф. И. О. занимаемая должность, подпись
Статистическая обработка данных Параметры токсичности______________________ _____________________________ Масса тела________________________ Масса внутренних органов_________________ Процедура случайной выборки_______________ __________________________ Ответственные исполнители Ф. И. О. занимаемая должность, подпись
 • При проведении исследования исходные данные должны находится на месте проведения исследования. • Записи исходных данных должны давать возможность воспроизведения исследований, определения всех действий, которые выполнялись в ходе испытаний. • По результатам проведенного доклинического исследования, в соответствии с требованиями Инструкции ответственный исполнитель составляет отчет о результатах доклинических исследований согласно форме Инструкции, и передает их Заказчику.
• При проведении исследования исходные данные должны находится на месте проведения исследования. • Записи исходных данных должны давать возможность воспроизведения исследований, определения всех действий, которые выполнялись в ходе испытаний. • По результатам проведенного доклинического исследования, в соответствии с требованиями Инструкции ответственный исполнитель составляет отчет о результатах доклинических исследований согласно форме Инструкции, и передает их Заказчику.
 • Отчет о результатах доклинических исследований формируется по каждому проведенному исследованию. В отчете должно быть представлено заключение о безопасности исследуемого вещества (лекарственного средства) и отображены все возможные стороны потенциального действия исследуемого вещества (лекарственного средства), основанные на данных проведенных исследований. • Отчеты ответственного исполнителя о проведении исследований должны быть подписаны и датированы им. • .
• Отчет о результатах доклинических исследований формируется по каждому проведенному исследованию. В отчете должно быть представлено заключение о безопасности исследуемого вещества (лекарственного средства) и отображены все возможные стороны потенциального действия исследуемого вещества (лекарственного средства), основанные на данных проведенных исследований. • Отчеты ответственного исполнителя о проведении исследований должны быть подписаны и датированы им. • .
 • Исполнителем формируется два идентичных пакета документов по проведенным исследованиям, состоящих из: 1) договора между Заказчиком и Исполнителем 2) протоколов доклинических исследований и поправок к ним 3) образцов исследуемого вещества 4) образцов упаковки лекарственного средства, которое исследуется 5) актов проверок проведения доклинического исследования Заказчиком (если такие проверки проводились) 6) исходных данных 7) отчетов о результатах испытаний. • Документы хранятся у Исполнителя и у Заказчика в течение 15 лет с даты подачи заявки на регистрацию.
• Исполнителем формируется два идентичных пакета документов по проведенным исследованиям, состоящих из: 1) договора между Заказчиком и Исполнителем 2) протоколов доклинических исследований и поправок к ним 3) образцов исследуемого вещества 4) образцов упаковки лекарственного средства, которое исследуется 5) актов проверок проведения доклинического исследования Заказчиком (если такие проверки проводились) 6) исходных данных 7) отчетов о результатах испытаний. • Документы хранятся у Исполнителя и у Заказчика в течение 15 лет с даты подачи заявки на регистрацию.

