Презентация Арины Коптяевой. ДНК в медицине.pptx
- Количество слайдов: 13
 ДНК-технологии в медицине
ДНК-технологии в медицине
 Презентацию подготовила Студентка ЛПФ, 3 курса, 31 группы Арина Коптяева
Презентацию подготовила Студентка ЛПФ, 3 курса, 31 группы Арина Коптяева
 В настоящее время стало очевидным, что достижения в области молекулярной биологии способны сильно изменить практическую медицину. Они не только углубили наши знания об экспрессии генов и причинах многих болезней, но способствовали разработке новых подходов к их диагностике и лечению. Было установлено, что полиморфизм генов широко распространён в популяции людей, показана взаимосвязь между изменениями в структуре ДНК и многими болезнями. Идентификация генов, нарушение работы которых приводит к развитию наследственных заболеваний, создала предпосылки для подробного анализа генетических и биохимических основ патогенеза этих заболеваний и разработки наиболее эффективных методов лечения. Методами молекулярной медицины были созданы: • вакцины для предотвращения гепатитов, • инсулин человека - для лечения сахарного диабета, • фактор VIII - для восстановления нормального свёртывания крови и лечения гемофилии и многие другие препараты.
В настоящее время стало очевидным, что достижения в области молекулярной биологии способны сильно изменить практическую медицину. Они не только углубили наши знания об экспрессии генов и причинах многих болезней, но способствовали разработке новых подходов к их диагностике и лечению. Было установлено, что полиморфизм генов широко распространён в популяции людей, показана взаимосвязь между изменениями в структуре ДНК и многими болезнями. Идентификация генов, нарушение работы которых приводит к развитию наследственных заболеваний, создала предпосылки для подробного анализа генетических и биохимических основ патогенеза этих заболеваний и разработки наиболее эффективных методов лечения. Методами молекулярной медицины были созданы: • вакцины для предотвращения гепатитов, • инсулин человека - для лечения сахарного диабета, • фактор VIII - для восстановления нормального свёртывания крови и лечения гемофилии и многие другие препараты.
 С помощью генной терапии оказалось возможным вводить в организм больного полноценно работающие гены и таким образом восстанавливать метаболические нарушения, вызванные мутантными генами. Таким путём осуществляется лечение детей с иммунодефицитом, вызванным дефектом аденозиндезаминазы, в стадии клинических испытаний находятся методы гено-коррекции таких наследственных болезней, как: • семейная гиперхолестеринемия, • гемофилия В, • муковисцидоз и некоторые другие. Для выявления дефектов в структуре ДНК она должна быть выделена из соответствующего источника (биологической жидкости, биоптата, культуры клеток и т. д. ) и "наработана" в количествах, достаточных для исследования. Для геннотерапевтических работ необходимы выделение нормальных генов и введение их в дефектные клетки таким образом, чтобы они экспрессировались, позволяя восстановить здоровье пациента.
С помощью генной терапии оказалось возможным вводить в организм больного полноценно работающие гены и таким образом восстанавливать метаболические нарушения, вызванные мутантными генами. Таким путём осуществляется лечение детей с иммунодефицитом, вызванным дефектом аденозиндезаминазы, в стадии клинических испытаний находятся методы гено-коррекции таких наследственных болезней, как: • семейная гиперхолестеринемия, • гемофилия В, • муковисцидоз и некоторые другие. Для выявления дефектов в структуре ДНК она должна быть выделена из соответствующего источника (биологической жидкости, биоптата, культуры клеток и т. д. ) и "наработана" в количествах, достаточных для исследования. Для геннотерапевтических работ необходимы выделение нормальных генов и введение их в дефектные клетки таким образом, чтобы они экспрессировались, позволяя восстановить здоровье пациента.
 ДНК-диагностика заболеваний • Используя технику рекомбинантных ДНК, удаётся исследовать варианты генов, ответственных за развитие многих заболеваний. Этим способом идентифицированы точечные мутации, вызванные заменой одного азотистого основания, делениями или вставками, приводящими к появлению аллелей, кодирующих функционально неактивные белки. Дефектные "полиморфы" возникают как за счёт изменений в кодирующих участках гена, так и в результате мутаций в некодирующих областях, тесно примыкающих к генам и вызывающих нарушение их работы. • Разработанные технологии позволяют вести целенаправленное картирование генов человека в рамках международного проекта "Геном человека". Официально эта научная программа с участием ведущих молекулярно-генетических лабораторий США, стран Западной Европы, а также России и Японии оформилась в 1990 г. В ходе работы над проектом картированы 923 гена, вызывающих развитие моногенных заболеваний. К концу 2001 г. работами лабораторий США, Великобритании, Японии и ряда европейских стран с точностью до 90% завершена расшифровка генома. Ожидается, что вскоре будут изучены все гены, ответственные за развитие патологических процессов у человека. Это позволит вывести диагностику и лечение многих болезней на новый уровень.
ДНК-диагностика заболеваний • Используя технику рекомбинантных ДНК, удаётся исследовать варианты генов, ответственных за развитие многих заболеваний. Этим способом идентифицированы точечные мутации, вызванные заменой одного азотистого основания, делениями или вставками, приводящими к появлению аллелей, кодирующих функционально неактивные белки. Дефектные "полиморфы" возникают как за счёт изменений в кодирующих участках гена, так и в результате мутаций в некодирующих областях, тесно примыкающих к генам и вызывающих нарушение их работы. • Разработанные технологии позволяют вести целенаправленное картирование генов человека в рамках международного проекта "Геном человека". Официально эта научная программа с участием ведущих молекулярно-генетических лабораторий США, стран Западной Европы, а также России и Японии оформилась в 1990 г. В ходе работы над проектом картированы 923 гена, вызывающих развитие моногенных заболеваний. К концу 2001 г. работами лабораторий США, Великобритании, Японии и ряда европейских стран с точностью до 90% завершена расшифровка генома. Ожидается, что вскоре будут изучены все гены, ответственные за развитие патологических процессов у человека. Это позволит вывести диагностику и лечение многих болезней на новый уровень.
 Использование ДНК-технологий для получения лекарственных препаратов. Вакцины - очищенные белки, антигенные детерминанты ряда возбудителей вирусных и бактериальных инфекций. В последнее время их получают, пользуясь техникой рекомбинантных ДНК. Первой вакциной, синтезированной этим способом, была вакцина против вируса гепатита В. Белки, имеющие терапевтическое значение, получают с использованием этой технологии во многих странах мира. Так, одним из первых синтезирован инсулин человека. В клетках Е. coli, трансформированных плазмидами, содержащими ДНК, которая кодировала А- и В-цепи инсулина, нарабатывают белковые продукты А- и В-цепей. После очистки их подвергают фолдингу и окислению, которое обеспечивает образование соответствующих дисульфидных мостиков.
Использование ДНК-технологий для получения лекарственных препаратов. Вакцины - очищенные белки, антигенные детерминанты ряда возбудителей вирусных и бактериальных инфекций. В последнее время их получают, пользуясь техникой рекомбинантных ДНК. Первой вакциной, синтезированной этим способом, была вакцина против вируса гепатита В. Белки, имеющие терапевтическое значение, получают с использованием этой технологии во многих странах мира. Так, одним из первых синтезирован инсулин человека. В клетках Е. coli, трансформированных плазмидами, содержащими ДНК, которая кодировала А- и В-цепи инсулина, нарабатывают белковые продукты А- и В-цепей. После очистки их подвергают фолдингу и окислению, которое обеспечивает образование соответствующих дисульфидных мостиков.
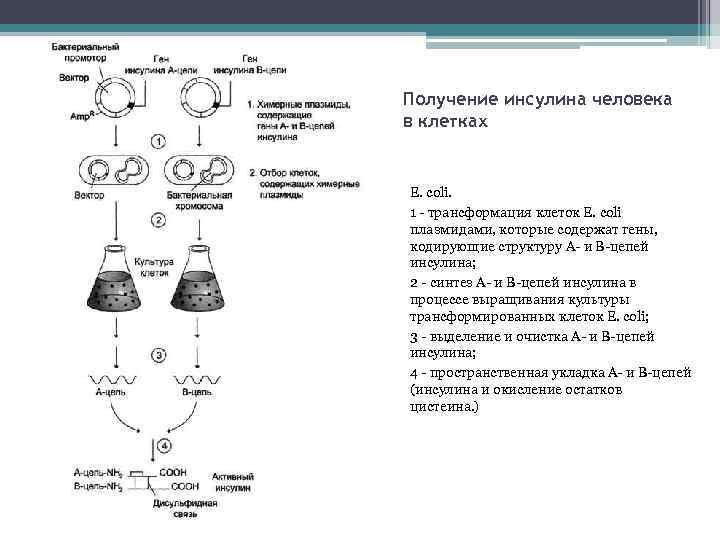 Получение инсулина человека в клетках Е. coli. 1 - трансформация клеток Е. coli плазмидами, которые содержат гены, кодирующие структуру А- и В-цепей инсулина; 2 - синтез А- и В-цепей инсулина в процессе выращивания культуры трансформированных клеток Е. coli; 3 - выделение и очистка А- и В-цепей инсулина; 4 - пространственная укладка А- и В-цепей (инсулина и окисление остатков цистеина. )
Получение инсулина человека в клетках Е. coli. 1 - трансформация клеток Е. coli плазмидами, которые содержат гены, кодирующие структуру А- и В-цепей инсулина; 2 - синтез А- и В-цепей инсулина в процессе выращивания культуры трансформированных клеток Е. coli; 3 - выделение и очистка А- и В-цепей инсулина; 4 - пространственная укладка А- и В-цепей (инсулина и окисление остатков цистеина. )
 Аналогичным способом получен гормон роста, используемый для лечения детей с недостаточностью этого гормона. Более сложные белки получены в культуре клеток млекопитающих. Так, дефекты в гене фактора VIII, кодирующего один из белков - участников свёртывающей системы крови, ответственны за возникновение гемофилии. До того как фактор VIII был получен методами генной инженерии, большое количество больных погибало от СПИДа или гепатита, которыми они заражались в результате введения выделенного из крови фактора VIII или переливания крови от доноров, являвшихся носителями этих болезней.
Аналогичным способом получен гормон роста, используемый для лечения детей с недостаточностью этого гормона. Более сложные белки получены в культуре клеток млекопитающих. Так, дефекты в гене фактора VIII, кодирующего один из белков - участников свёртывающей системы крови, ответственны за возникновение гемофилии. До того как фактор VIII был получен методами генной инженерии, большое количество больных погибало от СПИДа или гепатита, которыми они заражались в результате введения выделенного из крови фактора VIII или переливания крови от доноров, являвшихся носителями этих болезней.
 Тканевый активатор плазминогена (ТАЛ) - протеаза, участвующая в процессе фибринолиза и предотвращающая образование тромбов в кровеносном русле; получена с помощью рекомбинантных ДНК. ТАЛ назначают больным с ишемической болезнью сердца для ускорения растворения тромбов, которые могут вызвать закупорку коронарных артерий и нарушить поступление кислорода в миокард. Осуществлено получение рекомбинантных факторов роста, обеспечивающих восстановление гемостаза: эритропоэтина, интерлейкинов, колоний-стимулирующих факторов. Эти препараты используют в лечении больных анемией, после трансплантации костного мозга или химиотерапии, чтобы стимулировать образование клеток крови и снизить риск иммунодефицита. Разработаны методы получения белков человека с использованием трансгенных животных; эти белки получают в результате искусственного введения чужеродного гена в оплодотворённую яйцеклетку или в ранние зародыши млекопитающих. Генноинженерные мероприятия можно провести таким образом, чтобы интересующий нас белок человека секретировался с белками молока.
Тканевый активатор плазминогена (ТАЛ) - протеаза, участвующая в процессе фибринолиза и предотвращающая образование тромбов в кровеносном русле; получена с помощью рекомбинантных ДНК. ТАЛ назначают больным с ишемической болезнью сердца для ускорения растворения тромбов, которые могут вызвать закупорку коронарных артерий и нарушить поступление кислорода в миокард. Осуществлено получение рекомбинантных факторов роста, обеспечивающих восстановление гемостаза: эритропоэтина, интерлейкинов, колоний-стимулирующих факторов. Эти препараты используют в лечении больных анемией, после трансплантации костного мозга или химиотерапии, чтобы стимулировать образование клеток крови и снизить риск иммунодефицита. Разработаны методы получения белков человека с использованием трансгенных животных; эти белки получают в результате искусственного введения чужеродного гена в оплодотворённую яйцеклетку или в ранние зародыши млекопитающих. Генноинженерные мероприятия можно провести таким образом, чтобы интересующий нас белок человека секретировался с белками молока.
 Генная терапия - лечение наследственных, многофакторных и инфекционных заболеваний путём введения в соматические клетки пациентов генов, которые обеспечивают исправление генных дефектов или придают клеткам новые функции. Первый клинический опыт применения генной терапии был осуществлён в 1990 г. в США на четырёхлетней девочке, страдавшей наследственным иммунодефицитом, вызванным мутацией в гене аденозиндезаминазы (ADA. ) Ребёнку были введены её собственные лимфоциты, предварительно трансформированные вне организма генной конструкцией. Лечебный эффект наблюдался в течение нескольких месяцев, после чего процедуру введения гена повторяли многократно без видимых неблагоприятных эффектов. Для успешной генотерапии необходимо: • обеспечить эффективную доставку чужеродного гена в клеткимишени; • создать условия длительной экспрессии гена в этих клетках.
Генная терапия - лечение наследственных, многофакторных и инфекционных заболеваний путём введения в соматические клетки пациентов генов, которые обеспечивают исправление генных дефектов или придают клеткам новые функции. Первый клинический опыт применения генной терапии был осуществлён в 1990 г. в США на четырёхлетней девочке, страдавшей наследственным иммунодефицитом, вызванным мутацией в гене аденозиндезаминазы (ADA. ) Ребёнку были введены её собственные лимфоциты, предварительно трансформированные вне организма генной конструкцией. Лечебный эффект наблюдался в течение нескольких месяцев, после чего процедуру введения гена повторяли многократно без видимых неблагоприятных эффектов. Для успешной генотерапии необходимо: • обеспечить эффективную доставку чужеродного гена в клеткимишени; • создать условия длительной экспрессии гена в этих клетках.
 В геном пациента чужеродная ДНК может вводиться либо в культуре клеток (ex vivo), либо непосредственно в организм больного (in vivo). При осуществлении первого способа выделяют и культивируют специфический тип клеток пациента, вводят в него чужеродный ген, отбирают трансформированные клетки и реинфузируют их тому же больному. Генная терапия in vivo основана на прямом введении в специализированные ткани больного клонированных и определённым образом упакованных последовательностей ДНК, поступающих с помощью рецепторов в определённые типы клеток. В этом способе гены вводят, как правило, в виде аэрозольных и инъецируемых форм. Наиболее часто аэрозольную генотерапию используют при лечении болезней лёгких (например, раке лёгких) и муковисцидоза.
В геном пациента чужеродная ДНК может вводиться либо в культуре клеток (ex vivo), либо непосредственно в организм больного (in vivo). При осуществлении первого способа выделяют и культивируют специфический тип клеток пациента, вводят в него чужеродный ген, отбирают трансформированные клетки и реинфузируют их тому же больному. Генная терапия in vivo основана на прямом введении в специализированные ткани больного клонированных и определённым образом упакованных последовательностей ДНК, поступающих с помощью рецепторов в определённые типы клеток. В этом способе гены вводят, как правило, в виде аэрозольных и инъецируемых форм. Наиболее часто аэрозольную генотерапию используют при лечении болезней лёгких (например, раке лёгких) и муковисцидоза.
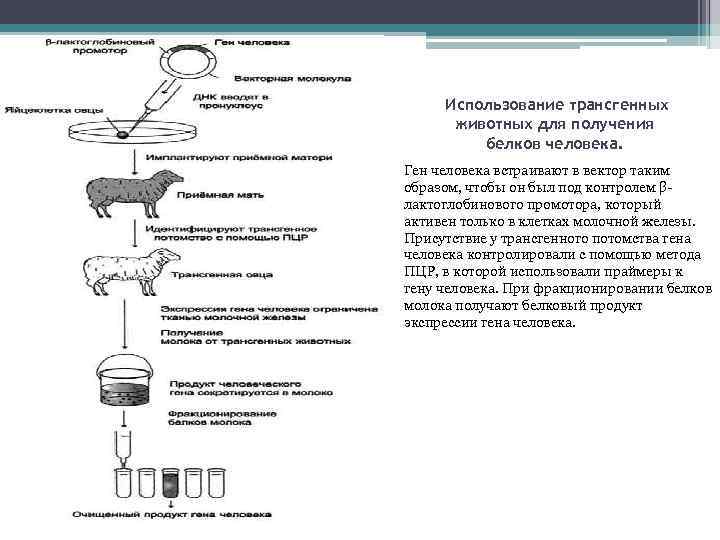 Использование трансгенных животных для получения белков человека. Ген человека встраивают в вектор таким образом, чтобы он был под контролем βлактоглобинового промотора, который активен только в клетках молочной железы. Присутствие у трансгенного потомства гена человека контролировали с помощью метода ПЦР, в которой использовали праймеры к гену человека. При фракционировании белков молока получают белковый продукт экспрессии гена человека.
Использование трансгенных животных для получения белков человека. Ген человека встраивают в вектор таким образом, чтобы он был под контролем βлактоглобинового промотора, который активен только в клетках молочной железы. Присутствие у трансгенного потомства гена человека контролировали с помощью метода ПЦР, в которой использовали праймеры к гену человека. При фракционировании белков молока получают белковый продукт экспрессии гена человека.
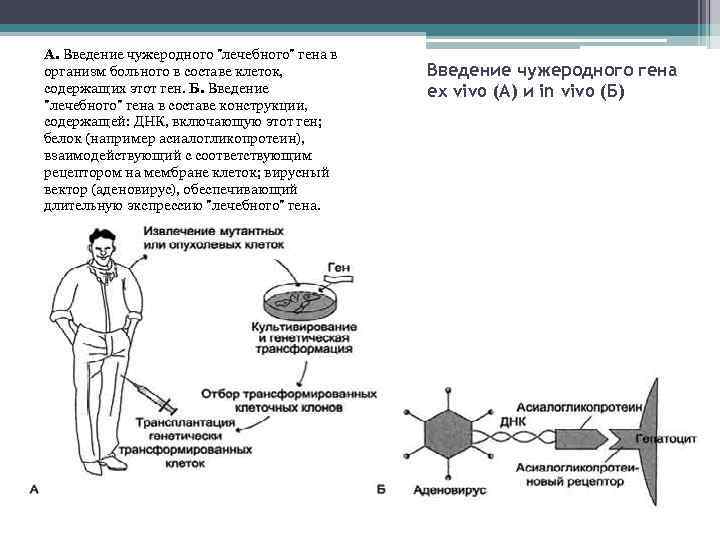 А. Введение чужеродного "лечебного" гена в организм больного в составе клеток, содержащих этот ген. Б. Введение "лечебного" гена в составе конструкции, содержащей: ДНК, включающую этот ген; белок (например асиалогликопротеин), взаимодействующий с соответствующим рецептором на мембране клеток; вирусный вектор (аденовирус), обеспечивающий длительную экспрессию "лечебного" гена. Введение чужеродного гена ex vivo (А) и in vivo (Б)
А. Введение чужеродного "лечебного" гена в организм больного в составе клеток, содержащих этот ген. Б. Введение "лечебного" гена в составе конструкции, содержащей: ДНК, включающую этот ген; белок (например асиалогликопротеин), взаимодействующий с соответствующим рецептором на мембране клеток; вирусный вектор (аденовирус), обеспечивающий длительную экспрессию "лечебного" гена. Введение чужеродного гена ex vivo (А) и in vivo (Б)


