Lektsiya_6_-_Transplantatsiya_embrioniv.ppt
- Количество слайдов: 149
 ДНІПРОПЕТРОВСЬКИЙ ДЕРЖАВНИЙ АГРАРНО-ЕКОНОМІЧНИЙ УНІВЕРСИТЕТ ФАКУЛЬТЕТ ВЕТЕРИНАРНОЇ МЕДИЦИНИ Кафедра хірургії і акушерства с. -г. тварин ТРАНСПЛАНТАЦІЯ ЕМБРІОНІВ Лектор: проф. Скляров П. М. © Скляров П. М. © кафедра хірургії і с. -г. тварин © Дніпропетровський державний аграрно-, економічний університет
ДНІПРОПЕТРОВСЬКИЙ ДЕРЖАВНИЙ АГРАРНО-ЕКОНОМІЧНИЙ УНІВЕРСИТЕТ ФАКУЛЬТЕТ ВЕТЕРИНАРНОЇ МЕДИЦИНИ Кафедра хірургії і акушерства с. -г. тварин ТРАНСПЛАНТАЦІЯ ЕМБРІОНІВ Лектор: проф. Скляров П. М. © Скляров П. М. © кафедра хірургії і с. -г. тварин © Дніпропетровський державний аграрно-, економічний університет
 План лекції l Історія розвитку технології трансплантації ембріонів, значення для тваринництва. l Загальна характеристика основних етапів трансплантації ембріонів. l Добір та підготовка донорів і реципієнтів для трансплантації ембріонів. l Складання схеми гормональної обробки корів. l Методи пересадки ембріонів.
План лекції l Історія розвитку технології трансплантації ембріонів, значення для тваринництва. l Загальна характеристика основних етапів трансплантації ембріонів. l Добір та підготовка донорів і реципієнтів для трансплантації ембріонів. l Складання схеми гормональної обробки корів. l Методи пересадки ембріонів.
![Трансплантація ембріонів тварин (animal embryo transplantation) [лат. transplantare пересаджувати; грец. embryon - зародок] ‒ Трансплантація ембріонів тварин (animal embryo transplantation) [лат. transplantare пересаджувати; грец. embryon - зародок] ‒](https://present5.com/presentation/-101445357_437140696/image-3.jpg) Трансплантація ембріонів тварин (animal embryo transplantation) [лат. transplantare пересаджувати; грец. embryon - зародок] ‒ метод прискореного відтворення високопродуктивних тварин шляхом отримання та пересадки їх ембріонів менш цінним тваринам
Трансплантація ембріонів тварин (animal embryo transplantation) [лат. transplantare пересаджувати; грец. embryon - зародок] ‒ метод прискореного відтворення високопродуктивних тварин шляхом отримання та пересадки їх ембріонів менш цінним тваринам
 Під трансплантацією ембріонів (ТЕ) розуміють вилучення ембріонів із статевих органів однієї самки (тварини-донора) і пересадку їх в статеві органи іншої (тварини-реципієнта)
Під трансплантацією ембріонів (ТЕ) розуміють вилучення ембріонів із статевих органів однієї самки (тварини-донора) і пересадку їх в статеві органи іншої (тварини-реципієнта)
 ТЕ проводиться у більшості лаб. та с. -г. тварин і приматів. Найбільш поширена ТЕ у скотарстві.
ТЕ проводиться у більшості лаб. та с. -г. тварин і приматів. Найбільш поширена ТЕ у скотарстві.
 n Метод ТЕ дозволяє більш ефективно використовувати генетичний потенціал самки, у 1, 5 рази прискорити селекційний процес і добитись щорічного підвищення продуктивності стад на 15. . . 20%.
n Метод ТЕ дозволяє більш ефективно використовувати генетичний потенціал самки, у 1, 5 рази прискорити селекційний процес і добитись щорічного підвищення продуктивності стад на 15. . . 20%.
 ІСТОРІЯ РОЗВИТКУ, СУЧАСНИЙ СТАН ТА ПЕРСПЕКТИВИ • 1881 р. ‒ В. Хіпп (Walter Heape) (Кембриджський ун-т, Англія) вперше в історії біології одержав вагітність після пересадки 2 ембріонів 32 -год. віку від кролиці ангорської породи кролиці породи бельгійський чемпіон.
ІСТОРІЯ РОЗВИТКУ, СУЧАСНИЙ СТАН ТА ПЕРСПЕКТИВИ • 1881 р. ‒ В. Хіпп (Walter Heape) (Кембриджський ун-т, Англія) вперше в історії біології одержав вагітність після пересадки 2 ембріонів 32 -год. віку від кролиці ангорської породи кролиці породи бельгійський чемпіон.
 1897 р. : В. С. Груздєв – • перші спроби по заплідненню яйцеклітин й інкубації зародків ссавців поза організмом.
1897 р. : В. С. Груздєв – • перші спроби по заплідненню яйцеклітин й інкубації зародків ссавців поза організмом.
 Головна причина попередніх невдач ТЕ – недотримання принципу синхронності СЦ донорів і реципієнтів.
Головна причина попередніх невдач ТЕ – недотримання принципу синхронності СЦ донорів і реципієнтів.
 • 1930 р. – виявлення у крові жеребних кобил гонадотропінів, здатних викликати СО фолікулів → реальна можливість практичного використання ТЕ (Н. Colе та співавт. , Девіс, Каліфорнія)
• 1930 р. – виявлення у крові жеребних кобил гонадотропінів, здатних викликати СО фолікулів → реальна можливість практичного використання ТЕ (Н. Colе та співавт. , Девіс, Каліфорнія)
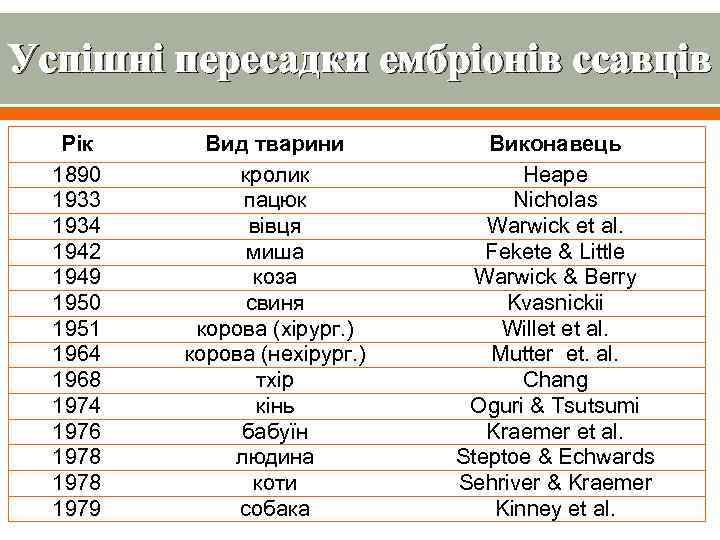 Успішні пересадки ембріонів ссавців Рік 1890 1933 1934 1942 1949 1950 1951 1964 1968 1974 1976 1978 1979 Вид тварини кролик пацюк вівця миша коза свиня корова (хірург. ) корова (нехірург. ) тхір кінь бабуїн людина коти собака Виконавець Heape Nicholas Warwick et al. Fekete & Little Warwick & Berry Kvasnickii Willet et al. Mutter et. al. Chang Oguri & Tsutsumi Kraemer et al. Steptoe & Echwards Sehriver & Kraemer Kinney et al.
Успішні пересадки ембріонів ссавців Рік 1890 1933 1934 1942 1949 1950 1951 1964 1968 1974 1976 1978 1979 Вид тварини кролик пацюк вівця миша коза свиня корова (хірург. ) корова (нехірург. ) тхір кінь бабуїн людина коти собака Виконавець Heape Nicholas Warwick et al. Fekete & Little Warwick & Berry Kvasnickii Willet et al. Mutter et. al. Chang Oguri & Tsutsumi Kraemer et al. Steptoe & Echwards Sehriver & Kraemer Kinney et al.
 1951 р. – успішна хірургічна пересадка ембріону корови (Willet E. L. та ін. , ун-т шт. Вісконсин). 1964 р. – народилося перше у світі теля після «безкровної трансплантації» (Mutter L. R. та ін. , ун-т шт. Вісконсин).
1951 р. – успішна хірургічна пересадка ембріону корови (Willet E. L. та ін. , ун-т шт. Вісконсин). 1964 р. – народилося перше у світі теля після «безкровної трансплантації» (Mutter L. R. та ін. , ун-т шт. Вісконсин).
 q 1971 р. – японським дослідникам вдалося отримати жеребність кобили після пересадки ембріону (Oguri & Tsutsumi). q 1971 р. – успішні досліди по заморожуванню і відтаванню зародків мишей (Whittingham D. G. та ін. )
q 1971 р. – японським дослідникам вдалося отримати жеребність кобили після пересадки ембріону (Oguri & Tsutsumi). q 1971 р. – успішні досліди по заморожуванню і відтаванню зародків мишей (Whittingham D. G. та ін. )
 q 1973 р. – народження першого теляти після пересадки корові заморожено-відтанутого зародку. q 1974 р. – народження химерних ягнят, отриманих від 4 батьків (Tucker I. M. та ін. , Кембрідж, Англія)
q 1973 р. – народження першого теляти після пересадки корові заморожено-відтанутого зародку. q 1974 р. – народження химерних ягнят, отриманих від 4 батьків (Tucker I. M. та ін. , Кембрідж, Англія)
 q 1978 р. – розділення на дві половинки зародка миші на стадії морули і вдала пересадка їх реципієнтам. q 1979 р. – народження монозиготної пари ягнят методом ембріонального клонування (S. W. Willadsen – Кембрідж, Англія).
q 1978 р. – розділення на дві половинки зародка миші на стадії морули і вдала пересадка їх реципієнтам. q 1979 р. – народження монозиготної пари ягнят методом ембріонального клонування (S. W. Willadsen – Кембрідж, Англія).
 q 1981 р. – народження першого ембріонального клону телят (S. W. Willadsen та С. Polge – Кембрідж, Англія ). q 1984 р. – отримання міжвидових химер вівці та кози (Кембрідж, Англія) та першого ембріонального клону коней (W. Allen та R. Pashen, США)
q 1981 р. – народження першого ембріонального клону телят (S. W. Willadsen та С. Polge – Кембрідж, Англія ). q 1984 р. – отримання міжвидових химер вівці та кози (Кембрідж, Англія) та першого ембріонального клону коней (W. Allen та R. Pashen, США)
 Бурхливий розвиток наукових досліджень, поліпшення техніки ТЕ → суттєве покращення результатів: - у 1974 р. після обробки однієї тварини-донора одержували 1, 6 вагітності у реципієнта, через 67 років – по 4 вагітності на донора.
Бурхливий розвиток наукових досліджень, поліпшення техніки ТЕ → суттєве покращення результатів: - у 1974 р. після обробки однієї тварини-донора одержували 1, 6 вагітності у реципієнта, через 67 років – по 4 вагітності на донора.
 До початку 70 -х рр. – розробка теоретичних основ і технології хірургічної ТЕ у корів (Кембріджський ун-т, Англія)
До початку 70 -х рр. – розробка теоретичних основ і технології хірургічної ТЕ у корів (Кембріджський ун-т, Англія)
 • До середини 70 -хх рр. – переміщення центру досліджень до країн Півн. Америки: створення інструментів та нехірургічного способу вилучення та пересадки ембріонів → спрощення і здешевлення техніки ТЕ.
• До середини 70 -хх рр. – переміщення центру досліджень до країн Півн. Америки: створення інструментів та нехірургічного способу вилучення та пересадки ембріонів → спрощення і здешевлення техніки ТЕ.
 За 1973 -1982 рр. у Канаді одержано 5413 теляттрансплантатів На кінець 80 -х рр. у країнах Півн. Америки здійснювалося ~200 тис. щорічних ембріопересадок. В СРСР за 1984 -1987 рр. – ~17 тис. пересадок → ~ 3 тис. телят, до 1990 р. – 12 тис.
За 1973 -1982 рр. у Канаді одержано 5413 теляттрансплантатів На кінець 80 -х рр. у країнах Півн. Америки здійснювалося ~200 тис. щорічних ембріопересадок. В СРСР за 1984 -1987 рр. – ~17 тис. пересадок → ~ 3 тис. телят, до 1990 р. – 12 тис.
 До середини 90 -х в області ТЕ досягнуто рекордних результатів: у США від корови-донора за рік одержано 136 телят, у Франції – 80, у Німеччині – 57, в Україні – від 6 донорів 71 теля.
До середини 90 -х в області ТЕ досягнуто рекордних результатів: у США від корови-донора за рік одержано 136 телят, у Франції – 80, у Німеччині – 57, в Україні – від 6 донорів 71 теля.
 У 2003 р. було пересаджено понад півмільйона ембріонів, 40% з них після заморозки і відтавання і 18% ‒ вирощених in vitro. Півн. Америка займає лідируюче положення (45% пересадок), а Європа і Півд. Америка – по 20%
У 2003 р. було пересаджено понад півмільйона ембріонів, 40% з них після заморозки і відтавання і 18% ‒ вирощених in vitro. Півн. Америка займає лідируюче положення (45% пересадок), а Європа і Півд. Америка – по 20%
 ІН ВІТРО (IVF) ТУБАЛЬНИХ ООЦИТІВ І НАСТУПНОЇ ПЕРЕСАДКИ ЇХ РЕЦИПІЄНТАМ: - у 1978 р. народилася дівчинка у 30 -річної жінки; - у 1982 р. вперше одержано теля.
ІН ВІТРО (IVF) ТУБАЛЬНИХ ООЦИТІВ І НАСТУПНОЇ ПЕРЕСАДКИ ЇХ РЕЦИПІЄНТАМ: - у 1978 р. народилася дівчинка у 30 -річної жінки; - у 1982 р. вперше одержано теля.
 У СРСР роботи з ТЕ розпочалися у 1936 р. , але були спрямовані на отримання експериментальних даних, що спростовують основи «формально-генетичної» теорії генів.
У СРСР роботи з ТЕ розпочалися у 1936 р. , але були спрямовані на отримання експериментальних даних, що спростовують основи «формально-генетичної» теорії генів.
 Перше «радянське» теля-трансплантант хірургічним шляхом отримано у 1977 р. , нехірургічним – у 1978 р.
Перше «радянське» теля-трансплантант хірургічним шляхом отримано у 1977 р. , нехірургічним – у 1978 р.
 У 80 -90 -х рр. на базі інститутів, дослідних станцій, племпідприємств та племзаводів було організовано центри овотрансплантації, провідні – Харківський (при Інті тваринництва УААН) та Київський (при Ін-ті розведення і генетики тварин УААН).
У 80 -90 -х рр. на базі інститутів, дослідних станцій, племпідприємств та племзаводів було організовано центри овотрансплантації, провідні – Харківський (при Інті тваринництва УААН) та Київський (при Ін-ті розведення і генетики тварин УААН).
 У ряді областей (Сумській – Охтирка, Харківській – д/г ІТ УААН «Українка» та «Кутузівка» , п/з «Червоний Велетень» та ін. ) реалізовано проект виробничої лабораторії овотрансплантації.
У ряді областей (Сумській – Охтирка, Харківській – д/г ІТ УААН «Українка» та «Кутузівка» , п/з «Червоний Велетень» та ін. ) реалізовано проект виробничої лабораторії овотрансплантації.
 ТЕОРЕТИЧНІ ПЕРЕДУМОВИ ТЕ можливість використання біологічних резервів репродуктивних органів самок – телички народжуються, маючи 50 -100 і більше тис. ЯК, тоді як фактично використовується лише близько 10 -20.
ТЕОРЕТИЧНІ ПЕРЕДУМОВИ ТЕ можливість використання біологічних резервів репродуктивних органів самок – телички народжуються, маючи 50 -100 і більше тис. ЯК, тоді як фактично використовується лише близько 10 -20.
 Сучасні методи СО дозволяють збільшити в 10 -20 раз число ЯК, що овулювали: корів та овець – до 25, у свиней – до 40 -45, у коней – до 5, у гризунів – до 90.
Сучасні методи СО дозволяють збільшити в 10 -20 раз число ЯК, що овулювали: корів та овець – до 25, у свиней – до 40 -45, у коней – до 5, у гризунів – до 90.
 1975 р. – народження 22 телят в результаті хірургічної ТЕ, отриманих від однієї СО у донора (Baker R. D. , Макдональдський центр ТЕ, Канада) 1977 р. – одержання тільності у 51 реципієнта в результаті пересадки їм ембріонів одного донора після 6 -кратного вимивання (генет. центр шт. Техас, США).
1975 р. – народження 22 телят в результаті хірургічної ТЕ, отриманих від однієї СО у донора (Baker R. D. , Макдональдський центр ТЕ, Канада) 1977 р. – одержання тільності у 51 реципієнта в результаті пересадки їм ембріонів одного донора після 6 -кратного вимивання (генет. центр шт. Техас, США).
 В Англії у 1983 р. від корови за один раз вимили 27 зародків і, пересадивши їх реципієнтам, одержали 19 телят (нехірургічна трансплантація). 1988 р. (P. Rommel, НДР) отримав 57 телят від однієї корови.
В Англії у 1983 р. від корови за один раз вимили 27 зародків і, пересадивши їх реципієнтам, одержали 19 телят (нехірургічна трансплантація). 1988 р. (P. Rommel, НДР) отримав 57 телят від однієї корови.
 • На практиці однократно вдається отримати 5 -6 ембріонів за одну СО, а за 6 -8 вимиваннях за рік можна отримати від одного донора 30 -40 нащадків. • З урахуванням реальних масових можливостей використання донора можна в середньому отримувати 12 телят за рік (Жебровський Л. С. та ін. , 1983).
• На практиці однократно вдається отримати 5 -6 ембріонів за одну СО, а за 6 -8 вимиваннях за рік можна отримати від одного донора 30 -40 нащадків. • З урахуванням реальних масових можливостей використання донора можна в середньому отримувати 12 телят за рік (Жебровський Л. С. та ін. , 1983).
 Прикладом успішної реалізації програми з ТЕ є Канада l У 2002 р. тут від 14, 5 тис. корівдонорів було отримано біля 100 тис. ембріонів (6, 6 ‒ за вимивання). Щорічний запас ембріобанку становив більше 65 тис. кріоконсервованих ембріонів.
Прикладом успішної реалізації програми з ТЕ є Канада l У 2002 р. тут від 14, 5 тис. корівдонорів було отримано біля 100 тис. ембріонів (6, 6 ‒ за вимивання). Щорічний запас ембріобанку становив більше 65 тис. кріоконсервованих ембріонів.
 Канада також є лідером за кількістю: l пересаджених ембріонів з попередньо визначеною статтю, l пересадок ембріонів, отриманих in vitro, l пересадок частин ембріонів з метою отримання ідентичних близнюків l програм клонування телят із соматичних клітин донора.
Канада також є лідером за кількістю: l пересаджених ембріонів з попередньо визначеною статтю, l пересадок ембріонів, отриманих in vitro, l пересадок частин ембріонів з метою отримання ідентичних близнюків l програм клонування телят із соматичних клітин донора.
 Значення та переваги методу ТЕ: q q Одержання від генетично цінних маток більшої кількості нащадків і тим самим більш швидке підвищення якості стада (одержання від однієї корови до 30. . . 50 телят на рік). У молочному скотарстві – прискорення і більш точна оцінка корів за якістю їх дочок. Створення нових ліній, типів, порід тварин більш швидкими темпами. У м’ясному скотарстві – підвищення продуктивності стад шляхом збільшення народження двієнь (до 20% і більше).
Значення та переваги методу ТЕ: q q Одержання від генетично цінних маток більшої кількості нащадків і тим самим більш швидке підвищення якості стада (одержання від однієї корови до 30. . . 50 телят на рік). У молочному скотарстві – прискорення і більш точна оцінка корів за якістю їх дочок. Створення нових ліній, типів, порід тварин більш швидкими темпами. У м’ясному скотарстві – підвищення продуктивності стад шляхом збільшення народження двієнь (до 20% і більше).
 q q Рання ідентифікація статі → попередження народження теличокфримартинів. Усунення неплідності за непрохідності яйцепроводів, спайок яєчників, порушення умов у матці внаслідок старіння та ін. випадків. Одержання ідентичних близнюків (шляхом поділу морули чи ранньої бластоцисти, перенесення ядер соматичних клітин). Розвиток генної інженерії: одержання трансгенних, химерних тварин і т. і.
q q Рання ідентифікація статі → попередження народження теличокфримартинів. Усунення неплідності за непрохідності яйцепроводів, спайок яєчників, порушення умов у матці внаслідок старіння та ін. випадків. Одержання ідентичних близнюків (шляхом поділу морули чи ранньої бластоцисти, перенесення ядер соматичних клітин). Розвиток генної інженерії: одержання трансгенних, химерних тварин і т. і.
 За даними Міжнародного товариства з пересадки ембріонів (International Embryo Transfer Society) у 2002 р. у світі було здійснено більше півмільйона пересадок ембріонів ВРХ, 83000 з них ‒ методом запліднення in vitro.
За даними Міжнародного товариства з пересадки ембріонів (International Embryo Transfer Society) у 2002 р. у світі було здійснено більше півмільйона пересадок ембріонів ВРХ, 83000 з них ‒ методом запліднення in vitro.
 q Вивчення питань фізіології і патології вагітності, міжвидової гібридизації. q Тривале зберігання зародків дозволяє створювати запаси (банки зародків) цінного зародків високопродуктивних і рідких порід тварин і можливість більш вигідного експортування чи імпортування генетичного матеріалу. q Можливість одержувати цінний в племінному відношенні приплід від корів місцевих порід, що мають імунітет до різних хвороб.
q Вивчення питань фізіології і патології вагітності, міжвидової гібридизації. q Тривале зберігання зародків дозволяє створювати запаси (банки зародків) цінного зародків високопродуктивних і рідких порід тварин і можливість більш вигідного експортування чи імпортування генетичного матеріалу. q Можливість одержувати цінний в племінному відношенні приплід від корів місцевих порід, що мають імунітет до різних хвороб.
 Переваги при ТЕ в умовах господарства досягається лише за чіткого повсякденного здійснення комплексу агрозооветорганізаційних заходів: ◘ наявність здорових, конституційно кріпких донорів та реципієнтів, забезпечених повноцінною годівлею, відповідним утриманням і правильною експлуатацією; ◘ висококваліфікованих акушерівгінекологів і спеціального центру (пункту) ТЕ з необхідним обладнанням та оснащенням. {
Переваги при ТЕ в умовах господарства досягається лише за чіткого повсякденного здійснення комплексу агрозооветорганізаційних заходів: ◘ наявність здорових, конституційно кріпких донорів та реципієнтів, забезпечених повноцінною годівлею, відповідним утриманням і правильною експлуатацією; ◘ висококваліфікованих акушерівгінекологів і спеціального центру (пункту) ТЕ з необхідним обладнанням та оснащенням. {
 Схема приміщення лабораторії трансплантації ембріонів: 1 – манеж для санітарної обробки і сушки тварин; 2 – тамбур з дезбар’єром (ножна ванна); 3 – коридор з дезкилимком; 4 – мийкова; 5 – щитова кубової; 6 – автоклавна ; 7 – манеж для вимивання; 8 – пошукова; 9 – душова; 10 – роздягальня; 11 – туалет; 12 – передбоксник; 13 – стерильний передбоксник; 14 – склад; 15 – ветаптека; 16 – кімната для заморожування ембріонів; 17 – ембріобанк; 18 – кімната для спеціалістів; 19 – кабінет завідуючого; 20 – тамбур з дезбар’єром
Схема приміщення лабораторії трансплантації ембріонів: 1 – манеж для санітарної обробки і сушки тварин; 2 – тамбур з дезбар’єром (ножна ванна); 3 – коридор з дезкилимком; 4 – мийкова; 5 – щитова кубової; 6 – автоклавна ; 7 – манеж для вимивання; 8 – пошукова; 9 – душова; 10 – роздягальня; 11 – туалет; 12 – передбоксник; 13 – стерильний передбоксник; 14 – склад; 15 – ветаптека; 16 – кімната для заморожування ембріонів; 17 – ембріобанк; 18 – кімната для спеціалістів; 19 – кабінет завідуючого; 20 – тамбур з дезбар’єром
 ГОЛОВНІ ЕТАПИ ТРАНСПЛАНТАЦІЇ ЕМБРІОНІВ q добір донорів і реципієнтів; q викликання множинної овуляції (СО) у донорів та їх осіменіння; q одержання зародків від донорів; q оцінка, культивування та зберігання зародків; q синхронізація статевого циклу реципієнтів зі статевим циклом донорів; q пересадка зародків на стадії морули чи бластули реципієнтам.
ГОЛОВНІ ЕТАПИ ТРАНСПЛАНТАЦІЇ ЕМБРІОНІВ q добір донорів і реципієнтів; q викликання множинної овуляції (СО) у донорів та їх осіменіння; q одержання зародків від донорів; q оцінка, культивування та зберігання зародків; q синхронізація статевого циклу реципієнтів зі статевим циклом донорів; q пересадка зародків на стадії морули чи бластули реципієнтам.
 ПРАКТИКА ПІДБОРУ ДОНОРІВ ТА РЕЦИПІЄНТІВ Добір донорів Донор – цінна у генетичному відношенні тварина, від якої після гормонального викликання поліовуляції і осіменіння спермою перевіреного плідникаполіпшувача одержують декілька зародків з метою наступної пересадки реципієнтам.
ПРАКТИКА ПІДБОРУ ДОНОРІВ ТА РЕЦИПІЄНТІВ Добір донорів Донор – цінна у генетичному відношенні тварина, від якої після гормонального викликання поліовуляції і осіменіння спермою перевіреного плідникаполіпшувача одержують декілька зародків з метою наступної пересадки реципієнтам.
 Вимоги для донорів : l Молочна продуктивність вище стандарту даної породи в середньому на 50 -60% (не менше 220% стандарту по породі) при жирності молока не нижче стандарту породи. l Використовують зазвичай корів, що мають не менше 2 -3 -х лактацій, у віці не більше 8 -9 років.
Вимоги для донорів : l Молочна продуктивність вище стандарту даної породи в середньому на 50 -60% (не менше 220% стандарту по породі) при жирності молока не нижче стандарту породи. l Використовують зазвичай корів, що мають не менше 2 -3 -х лактацій, у віці не більше 8 -9 років.
 Вимоги для донорів : l Після родів тварина повинна проявити мінімум 2 -3 повноцінних синхронних природних СЦ з яскраво вираженими феноменами, мати хороший стан статевих органів і нормальний відтворний статус у попередній репродуктивний період.
Вимоги для донорів : l Після родів тварина повинна проявити мінімум 2 -3 повноцінних синхронних природних СЦ з яскраво вираженими феноменами, мати хороший стан статевих органів і нормальний відтворний статус у попередній репродуктивний період.
 l Враховують такі селекційні ознаки як породність, екстер’єр, конституція, морфофункціональні властивості вим’я, життєздатність приплоду.
l Враховують такі селекційні ознаки як породність, екстер’єр, конституція, морфофункціональні властивості вим’я, життєздатність приплоду.
 Заключний добір донорів проводять після встановлення реакції яєчників на введення гонадотропних препаратів і пробного вилучення ембріонів: l не менше 5 ЖТ і не менше 4 повноцінних ембріонів, придатних для заморожування і трансплантації).
Заключний добір донорів проводять після встановлення реакції яєчників на введення гонадотропних препаратів і пробного вилучення ембріонів: l не менше 5 ЖТ і не менше 4 повноцінних ембріонів, придатних для заморожування і трансплантації).
 l l Тварини-донори добираються з господарств, благополучних за інфекційними та інвазійними захворюваннями. Тварини, що ввозяться, повинні мати ветеринарні свідоцтва і пройти відповідні ветеринарно-карантинні обробки.
l l Тварини-донори добираються з господарств, благополучних за інфекційними та інвазійними захворюваннями. Тварини, що ввозяться, повинні мати ветеринарні свідоцтва і пройти відповідні ветеринарно-карантинні обробки.
 Добір реципієнтів Реципієнт – тварина, якій трансплантують (пересаджують) у матку одного чи двох зародків на ранній стадії їх розвитку (сурогатна мати, гестаційний кур'єр). Після пересадки в організмі реципієнта повинні бути забезпечені оптимальні умови для подальшого розвитку зародку і народження життєздатного плода.
Добір реципієнтів Реципієнт – тварина, якій трансплантують (пересаджують) у матку одного чи двох зародків на ранній стадії їх розвитку (сурогатна мати, гестаційний кур'єр). Після пересадки в організмі реципієнта повинні бути забезпечені оптимальні умови для подальшого розвитку зародку і народження життєздатного плода.
 В якості реципієнтів використовують інтактних телиць чи молодих корів з перевіреною здатністю до запліднення (ті ж вимоги, що й до донорів, за виключенням племінної цінності): o o o Тварини повинні бути добре розвиненими, ж. м. телиць – не менше 350. . . 380 кг у віці 16. . . 18 міс. чи корів не ст. 7 років. Не можна використовувати дрібні породи для трансплантації їм зародків, одержаних від донорів крупних порід. Тварини повинні бути здоровими, без ознак порушення обміну речовин, з хорошим фізичним розвитком, у стані середньої вгодованості, мати крупний, правильної форми таз. СЦ повинні бути регулярними і повноцінними, з синхронним формуванням стадії збудження; яєчники і матка – нормально розвинені, без пат. змін. Пересадка зародків реципієнтам проводиться при наявності функціонуючого ЖТ розміром 1. . . 1, 5 см.
В якості реципієнтів використовують інтактних телиць чи молодих корів з перевіреною здатністю до запліднення (ті ж вимоги, що й до донорів, за виключенням племінної цінності): o o o Тварини повинні бути добре розвиненими, ж. м. телиць – не менше 350. . . 380 кг у віці 16. . . 18 міс. чи корів не ст. 7 років. Не можна використовувати дрібні породи для трансплантації їм зародків, одержаних від донорів крупних порід. Тварини повинні бути здоровими, без ознак порушення обміну речовин, з хорошим фізичним розвитком, у стані середньої вгодованості, мати крупний, правильної форми таз. СЦ повинні бути регулярними і повноцінними, з синхронним формуванням стадії збудження; яєчники і матка – нормально розвинені, без пат. змін. Пересадка зародків реципієнтам проводиться при наявності функціонуючого ЖТ розміром 1. . . 1, 5 см.

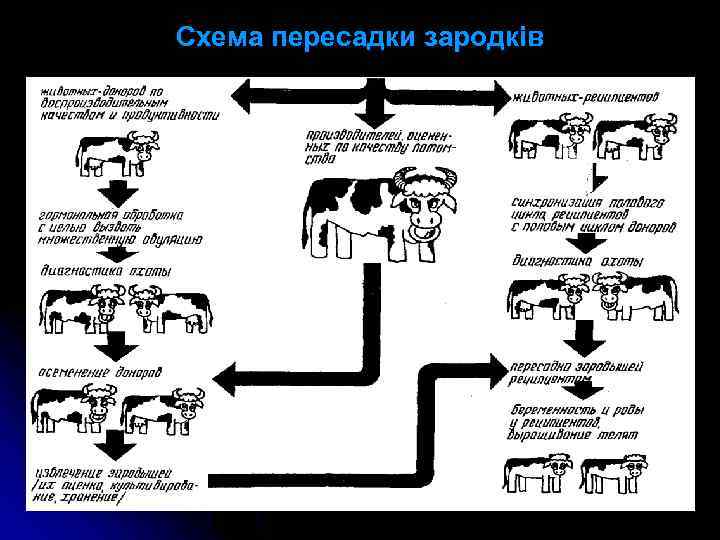 Схема пересадки зародків
Схема пересадки зародків
 Процес трансплантації ембріонів Дата Донори Реципієнти 13. 09 Огляд донора Ін’єкція простагландином Огляд реципієнта Ін'єкція простагландином 16. 09 Охота 28. 09 Обробка гормонами для викликання СО починається 29. 09 Обробка гормонами для викликання СО 2 рази Ін'єкція простагландином 30. 09 Обробка гормонами для викликання СО 2 рази та ін'єкція простагландином 1. 10 Обробка гормонами для викликання СО 2 рази 2. 10 Охота Осіменіння 2 рази Охота 8. 10 Дослідження ЖТ 9. 10 Вимивання зародків 16. 10 Ін'єкція простагландином Пересадка зародків
Процес трансплантації ембріонів Дата Донори Реципієнти 13. 09 Огляд донора Ін’єкція простагландином Огляд реципієнта Ін'єкція простагландином 16. 09 Охота 28. 09 Обробка гормонами для викликання СО починається 29. 09 Обробка гормонами для викликання СО 2 рази Ін'єкція простагландином 30. 09 Обробка гормонами для викликання СО 2 рази та ін'єкція простагландином 1. 10 Обробка гормонами для викликання СО 2 рази 2. 10 Охота Осіменіння 2 рази Охота 8. 10 Дослідження ЖТ 9. 10 Вимивання зародків 16. 10 Ін'єкція простагландином Пересадка зародків
 Викликання суперовуляції (СО) Обробці підлягають лише тварини, що позитивно реагують на введення горм. преп. , які вводяться суворо в середині ЕЦ (лютеальній фазі, тобто за наявності функц. ЖТ розміром ~1 см), зберігаються і використовуються у відповідності до вимог інструкції. СО вважають досягнутою, якщо відбулося виділення не менше 3 ЯК, однак основна мета – 10 -20 ЯК.
Викликання суперовуляції (СО) Обробці підлягають лише тварини, що позитивно реагують на введення горм. преп. , які вводяться суворо в середині ЕЦ (лютеальній фазі, тобто за наявності функц. ЖТ розміром ~1 см), зберігаються і використовуються у відповідності до вимог інструкції. СО вважають досягнутою, якщо відбулося виділення не менше 3 ЯК, однак основна мета – 10 -20 ЯК.
 Для ініціювання СО у ВРХ використовуються різні типи гонадотропінів: l Гн. РГ з витяжки гіпофіза свиней або ін. домашніх тварин (ФСГ); l кінський хоріонічний гонадотропін (e. CG) / ГСЖК; l людський менопаузальний гонадотропін (МГЛ).
Для ініціювання СО у ВРХ використовуються різні типи гонадотропінів: l Гн. РГ з витяжки гіпофіза свиней або ін. домашніх тварин (ФСГ); l кінський хоріонічний гонадотропін (e. CG) / ГСЖК; l людський менопаузальний гонадотропін (МГЛ).
 Найбільш широко застосовуються ГСЖК і ФСГ, окремо чи в компл. з Гн. РГ, PG, естрогенами, ХГ. ГСЖК одержують з сироватки вагітних кобил в період з 40 -го по 130 -й дні жеребності. Він має довгий (50. . . 120 год) період напіврозпаду, завдяки чому для викликання СО достатньо однократного введення (скорочення витрат праці і зменшення стресової дії на тварин).
Найбільш широко застосовуються ГСЖК і ФСГ, окремо чи в компл. з Гн. РГ, PG, естрогенами, ХГ. ГСЖК одержують з сироватки вагітних кобил в період з 40 -го по 130 -й дні жеребності. Він має довгий (50. . . 120 год) період напіврозпаду, завдяки чому для викликання СО достатньо однократного введення (скорочення витрат праці і зменшення стресової дії на тварин).
 Активність ГСЖК виражають в ОД інтернаціональних (ІО) або мишачих (м. о. ) (одна ІО = 2. . . 2, 5 м. о. ). Звична доза ГСЖК для індукції СО = 1500. . . 3000 ІО. Фірми-виготовлювачі нерідко дають ГСЖК власну назву (фоллігон, інтергонан, маротропін та ін. ).
Активність ГСЖК виражають в ОД інтернаціональних (ІО) або мишачих (м. о. ) (одна ІО = 2. . . 2, 5 м. о. ). Звична доза ГСЖК для індукції СО = 1500. . . 3000 ІО. Фірми-виготовлювачі нерідко дають ГСЖК власну назву (фоллігон, інтергонан, маротропін та ін. ).
 Головний недолік – lвисокі антигенні властивості, що імунізує оброблених тварин і робить проблематичним повторне використання донорів.
Головний недолік – lвисокі антигенні властивості, що імунізує оброблених тварин і робить проблематичним повторне використання донорів.
 Препарати ФСГ за більш стабільних результатів дають таку ж ефективність, але менш доступні (їх одержують з гіпофізу тварин або сечі клімактеричних жінок). ФСГ має нетривалий (біля 6 год) період напіврозпаду, у зв’язку з чим, для підтримки необхідної для СО конц. у крові, його вводять в організм протягом 4. . . 5 діб з інт. 12 год.
Препарати ФСГ за більш стабільних результатів дають таку ж ефективність, але менш доступні (їх одержують з гіпофізу тварин або сечі клімактеричних жінок). ФСГ має нетривалий (біля 6 год) період напіврозпаду, у зв’язку з чим, для підтримки необхідної для СО конц. у крові, його вводять в організм протягом 4. . . 5 діб з інт. 12 год.
 Препарати ФСГ також мають різні назви в залежності від фірми-виробника: ФСГ-П (США), l фоллітропін (Литва), l "ФСГ-СУПЕР" (Росія), l фоллікотропін (Чехія) та ін. l
Препарати ФСГ також мають різні назви в залежності від фірми-виробника: ФСГ-П (США), l фоллітропін (Литва), l "ФСГ-СУПЕР" (Росія), l фоллікотропін (Чехія) та ін. l
 Загальноприйняті методики викликання СО: обробка гонадотропінами → ч/з 48. . . 56 год PG F 2α (0, 5. . . 1 мг) чи його аналоги: Естрофан (Чехія), Ремофан (Спофа), Аніпрост (Росія), Ензапрост (Угорщина), Еструмат (Англія), Простін (США).
Загальноприйняті методики викликання СО: обробка гонадотропінами → ч/з 48. . . 56 год PG F 2α (0, 5. . . 1 мг) чи його аналоги: Естрофан (Чехія), Ремофан (Спофа), Аніпрост (Росія), Ензапрост (Угорщина), Еструмат (Англія), Простін (США).
 l Естрогени вводяться для підвищення заплідненості, а ХГ – для прискорення овуляції.
l Естрогени вводяться для підвищення заплідненості, а ХГ – для прискорення овуляції.
 В оброблених тварин число овуляцій варіює від 0 до 50, частіше – 10 -15, що залежить від дози і якості горм. преп. , інд. особл. тварин та ряду ін. факторів (порода, вік тварин, сезон року, лактація та ін. )
В оброблених тварин число овуляцій варіює від 0 до 50, частіше – 10 -15, що залежить від дози і якості горм. преп. , інд. особл. тварин та ряду ін. факторів (порода, вік тварин, сезон року, лактація та ін. )
 Ірландський спосіб Дні циклу: 16 -17 -й 19 -20 -й 21 -й 2 -й 5 -й 6 -8 -й 1500 -3000 ОД ГСЖК внутрішньом’язево 10 мг естрадіол-бензоату внутрішньом’язево Статева охота (0 день). 1500 -3000 ОД хоріонічного гонадотропіну внутрішньовенно Перше осіменіння Друге осіменіння Хірургічне вилучення зародків Нехірургічне вилучення зародків
Ірландський спосіб Дні циклу: 16 -17 -й 19 -20 -й 21 -й 2 -й 5 -й 6 -8 -й 1500 -3000 ОД ГСЖК внутрішньом’язево 10 мг естрадіол-бензоату внутрішньом’язево Статева охота (0 день). 1500 -3000 ОД хоріонічного гонадотропіну внутрішньовенно Перше осіменіння Друге осіменіння Хірургічне вилучення зародків Нехірургічне вилучення зародків
 Датський спосіб Дні циклу: 8 -12 -й 10 -14 -й Через 48 год. 0 1 -й 2 -й 6 -8 -й 1500 -3000 ОД ГСЖК внутрішньом’язево 25 мг ПГ-Ф 2α чи 500 мкг клопростенолу внутрішньом’язево Статева охота Перше осіменіння Друге осіменіння Нехірургічне вилучення зародків
Датський спосіб Дні циклу: 8 -12 -й 10 -14 -й Через 48 год. 0 1 -й 2 -й 6 -8 -й 1500 -3000 ОД ГСЖК внутрішньом’язево 25 мг ПГ-Ф 2α чи 500 мкг клопростенолу внутрішньом’язево Статева охота Перше осіменіння Друге осіменіння Нехірургічне вилучення зародків
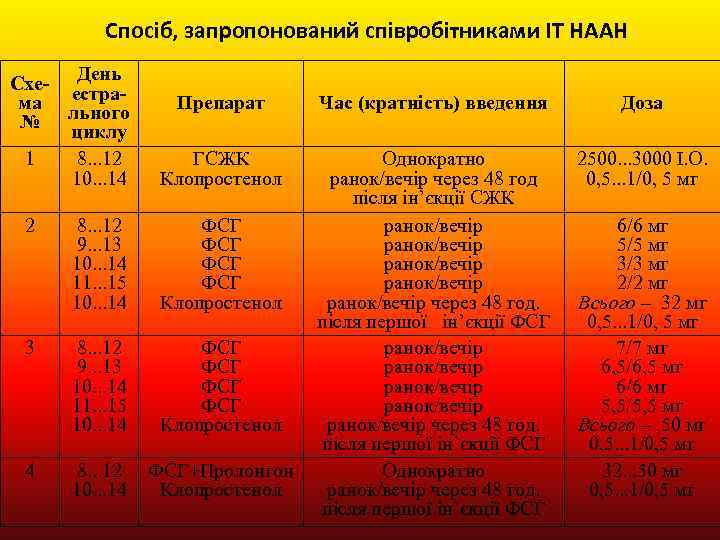 Спосіб, запропонований співробітниками ІТ НААН День Схе- естрама льного № циклу 1 8. . . 12 10. . . 14 Препарат Час (кратність) введення Доза ГСЖК Клопростенол Однократно ранок/вечір через 48 год після ін’єкції СЖК ранок/вечір ранок/вечір ранок/вечір через 48 год. після першої ін’єкції ФСГ Однократно ранок/вечір через 48 год. після першої ін’єкції ФСГ 2500. . . 3000 І. О. 0, 5. . . 1/0, 5 мг 2 8. . . 12 9. . . 13 10. . . 14 11. . . 15 10. . . 14 ФСГ ФСГ Клопростенол 3 8. . . 12 9. . . 13 10. . . 14 11. . . 15 10. . . 14 ФСГ ФСГ Клопростенол 4 8. . . 12 10. . . 14 ФСГ+Пролонгон Клопростенол 6/6 мг 5/5 мг 3/3 мг 2/2 мг Всього – 32 мг 0, 5. . . 1/0, 5 мг 7/7 мг 6, 5/6, 5 мг 6/6 мг 5, 5/5, 5 мг Всього – 50 мг 0, 5. . . 1/0, 5 мг 32. . . 50 мг 0, 5. . . 1/0, 5 мг
Спосіб, запропонований співробітниками ІТ НААН День Схе- естрама льного № циклу 1 8. . . 12 10. . . 14 Препарат Час (кратність) введення Доза ГСЖК Клопростенол Однократно ранок/вечір через 48 год після ін’єкції СЖК ранок/вечір ранок/вечір ранок/вечір через 48 год. після першої ін’єкції ФСГ Однократно ранок/вечір через 48 год. після першої ін’єкції ФСГ 2500. . . 3000 І. О. 0, 5. . . 1/0, 5 мг 2 8. . . 12 9. . . 13 10. . . 14 11. . . 15 10. . . 14 ФСГ ФСГ Клопростенол 3 8. . . 12 9. . . 13 10. . . 14 11. . . 15 10. . . 14 ФСГ ФСГ Клопростенол 4 8. . . 12 10. . . 14 ФСГ+Пролонгон Клопростенол 6/6 мг 5/5 мг 3/3 мг 2/2 мг Всього – 32 мг 0, 5. . . 1/0, 5 мг 7/7 мг 6, 5/6, 5 мг 6/6 мг 5, 5/5, 5 мг Всього – 50 мг 0, 5. . . 1/0, 5 мг 32. . . 50 мг 0, 5. . . 1/0, 5 мг
 Фактори, що впливають на вилучення та пересадку ембріонів • З боку тварин - Стадія циклу. Кращі результати можливі, якщо СО ініціюється в середині лютеїнової фази (9 -13 -й дні циклу). - Фолікулярний статус на момент СО. Присутність великого домінантного фолікула на момент СО чинить негативний вплив на реакцію. - Загальний стан здоров'я і вгодованість. - Фаза лактації.
Фактори, що впливають на вилучення та пересадку ембріонів • З боку тварин - Стадія циклу. Кращі результати можливі, якщо СО ініціюється в середині лютеїнової фази (9 -13 -й дні циклу). - Фолікулярний статус на момент СО. Присутність великого домінантного фолікула на момент СО чинить негативний вплив на реакцію. - Загальний стан здоров'я і вгодованість. - Фаза лактації.
 З погляду управління та утримання - Загальне управління тваринами (відсутність стресу, адекватне утримання). - Зовнішня температура і відносна вологість середовища.
З погляду управління та утримання - Загальне управління тваринами (відсутність стресу, адекватне утримання). - Зовнішня температура і відносна вологість середовища.
 З погляду процедури Обрана програма синхронізації і індукції (тип програми і відповідність). - Сперма / осіменіння. Використання високоякісної сперми під час осіменіння через 12 -24 год після початку прихованої статевої охоти. Повторне осіменіння не покращує показники заплідненості. Існують відмінності між биками. - Пересадка ембріона і техніка пересадки.
З погляду процедури Обрана програма синхронізації і індукції (тип програми і відповідність). - Сперма / осіменіння. Використання високоякісної сперми під час осіменіння через 12 -24 год після початку прихованої статевої охоти. Повторне осіменіння не покращує показники заплідненості. Існують відмінності між биками. - Пересадка ембріона і техніка пересадки.
 Осіменіння донорів В оброблених донорів охота настає ч/з 3 -5 діб, при комбінованій обробці гонадотропінами та ПГФ 2 а – ч/з 75 год. після введення простагландину. Однак у 10 -12% тварин ознаки стадії збудження СЦ не проявляються → тому осіменяють ч/з 48. . . 54 год. після введення PG.
Осіменіння донорів В оброблених донорів охота настає ч/з 3 -5 діб, при комбінованій обробці гонадотропінами та ПГФ 2 а – ч/з 75 год. після введення простагландину. Однак у 10 -12% тварин ознаки стадії збудження СЦ не проявляються → тому осіменяють ч/з 48. . . 54 год. після введення PG.
 l Осіменяють цервікально з ректальною фіксацією шийки матки декілька разів з 10 -12 год. інтервалами до закінчення охоти (іноді 3 -4 рази) збільшеною дозою сперми (10. . . 15 млн. акт. сперміїв, а загальна доза – не менше 50 млн. ).
l Осіменяють цервікально з ректальною фіксацією шийки матки декілька разів з 10 -12 год. інтервалами до закінчення охоти (іноді 3 -4 рази) збільшеною дозою сперми (10. . . 15 млн. акт. сперміїв, а загальна доза – не менше 50 млн. ).
 l Для осіменіння беруть сперму видатних бугаїв-плідників, перевірених за якістю потомства і визнаних поліпшувачами продуктивності. Добір бугаїв, роботу зі спермою та ШО проводять з дотриманням вет. -сан. правил у відповідності до діючої інструкції.
l Для осіменіння беруть сперму видатних бугаїв-плідників, перевірених за якістю потомства і визнаних поліпшувачами продуктивності. Добір бугаїв, роботу зі спермою та ШО проводять з дотриманням вет. -сан. правил у відповідності до діючої інструкції.
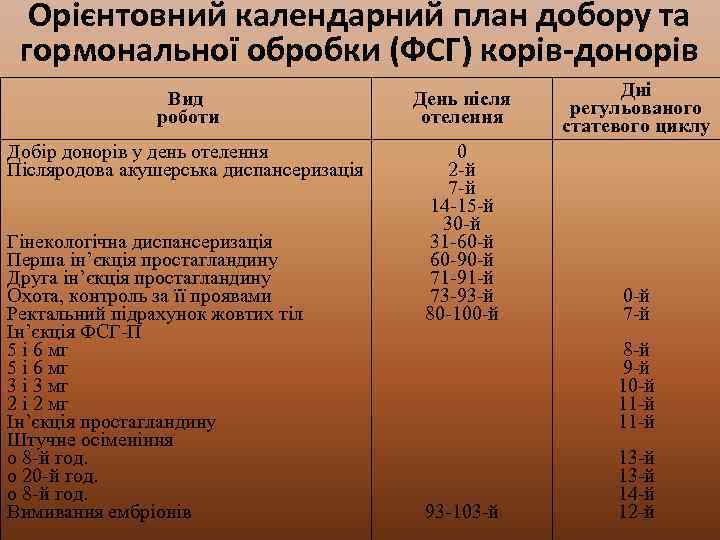 Орієнтовний календарний план добору та гормональної обробки (ФСГ) корів-донорів Вид роботи День після отелення Дні регульованого статевого циклу Добір донорів у день отелення Післяродова акушерська диспансеризація 0 2 -й 7 -й 14 -15 -й 30 -й 31 -60 -й 60 -90 -й 71 -91 -й 73 -93 -й 80 -100 -й 7 -й Гінекологічна диспансеризація Перша ін’єкція простагландину Друга ін’єкція простагландину Охота, контроль за її проявами Ректальний підрахунок жовтих тіл Ін’єкція ФСГ-П 5 і 6 мг 3 і 3 мг 2 і 2 мг Ін’єкція простагландину Штучне осіменіння о 8 -й год. о 20 -й год. о 8 -й год. Вимивання ембріонів 8 -й 9 -й 10 -й 11 -й 93 -103 -й 13 -й 14 -й 12 -й
Орієнтовний календарний план добору та гормональної обробки (ФСГ) корів-донорів Вид роботи День після отелення Дні регульованого статевого циклу Добір донорів у день отелення Післяродова акушерська диспансеризація 0 2 -й 7 -й 14 -15 -й 30 -й 31 -60 -й 60 -90 -й 71 -91 -й 73 -93 -й 80 -100 -й 7 -й Гінекологічна диспансеризація Перша ін’єкція простагландину Друга ін’єкція простагландину Охота, контроль за її проявами Ректальний підрахунок жовтих тіл Ін’єкція ФСГ-П 5 і 6 мг 3 і 3 мг 2 і 2 мг Ін’єкція простагландину Штучне осіменіння о 8 -й год. о 20 -й год. о 8 -й год. Вимивання ембріонів 8 -й 9 -й 10 -й 11 -й 93 -103 -й 13 -й 14 -й 12 -й
 ОДЕРЖАННЯ ЗАРОДКІВ Ціни на ембріони різні, в межах 350 $ -2000 $ і залежать в основному від 3 -х причин: q корови q кількості отриманих ембріонів q якості вимитих ембріонів
ОДЕРЖАННЯ ЗАРОДКІВ Ціни на ембріони різні, в межах 350 $ -2000 $ і залежать в основному від 3 -х причин: q корови q кількості отриманих ембріонів q якості вимитих ембріонів
 Для пересадки можуть використовуватися ембріони двох видів: - ембріони, вирощені в природних умовах і вилучені з репродуктивного тракту корови -донора; - ембріони, отримані шляхом дозрівання і запліднення яйцеклітини in vitro
Для пересадки можуть використовуватися ембріони двох видів: - ембріони, вирощені в природних умовах і вилучені з репродуктивного тракту корови -донора; - ембріони, отримані шляхом дозрівання і запліднення яйцеклітини in vitro
 • Близько 48% усіх ембріонів пересаджують свіжими, а 52% — попередньо замороженими. При цьому експерти відмічають, у середньому, досить високий рівень приживлення, що становить, відповідно, — 63% та 60%.
• Близько 48% усіх ембріонів пересаджують свіжими, а 52% — попередньо замороженими. При цьому експерти відмічають, у середньому, досить високий рівень приживлення, що становить, відповідно, — 63% та 60%.
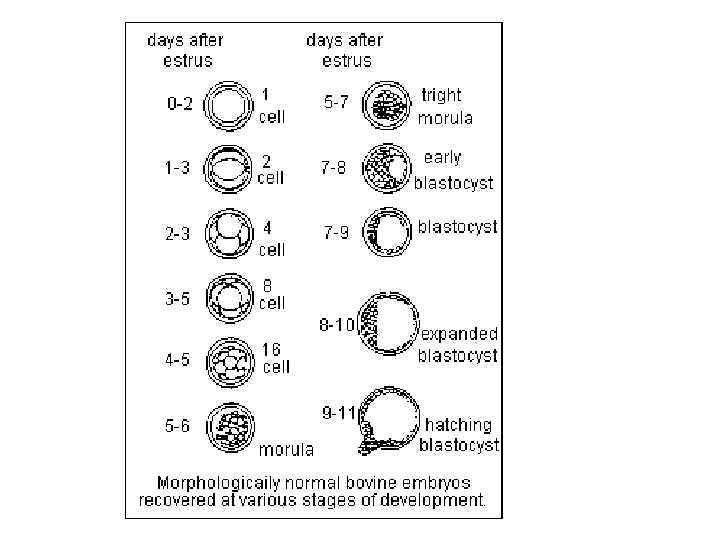
 Зародки доцільно вилучати у корів на 7 -8 -й день, а у овець – на 5 -6 -й день після першого осіменіння (до звільнення зародку з прозорої оболонки).
Зародки доцільно вилучати у корів на 7 -8 -й день, а у овець – на 5 -6 -й день після першого осіменіння (до звільнення зародку з прозорої оболонки).
 Для вилучення зародків використовують два способи: нехірургічний хірургічний.
Для вилучення зародків використовують два способи: нехірургічний хірургічний.
 l За нехірургічного способу частіше використовують 2 - чи 3 ходові катетери (типу Фоллея) з латексної гуми з пружним мандреном і надувним балончиком чи телескопічний комбінований триходовий інструмент з внутрішнім еластичним катетером французької фірми IMV.
l За нехірургічного способу частіше використовують 2 - чи 3 ходові катетери (типу Фоллея) з латексної гуми з пружним мандреном і надувним балончиком чи телескопічний комбінований триходовий інструмент з внутрішнім еластичним катетером французької фірми IMV.
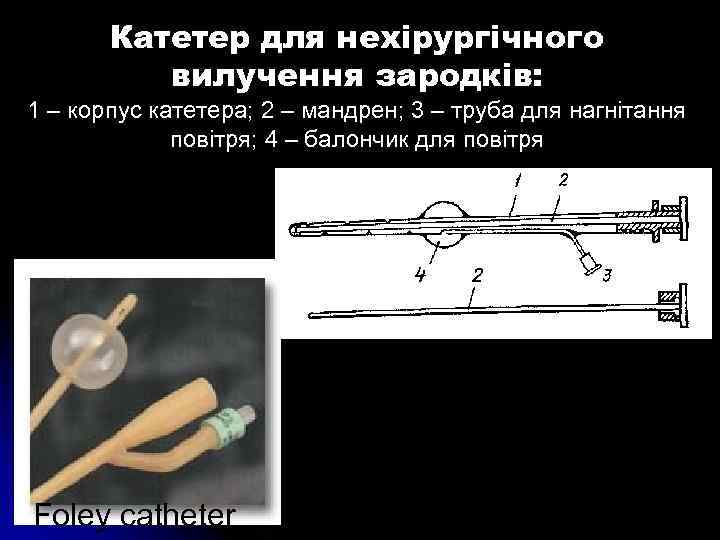 Катетер для нехірургічного вилучення зародків: 1 – корпус катетера; 2 – мандрен; 3 – труба для нагнітання повітря; 4 – балончик для повітря Foley catheter
Катетер для нехірургічного вилучення зародків: 1 – корпус катетера; 2 – мандрен; 3 – труба для нагнітання повітря; 4 – балончик для повітря Foley catheter
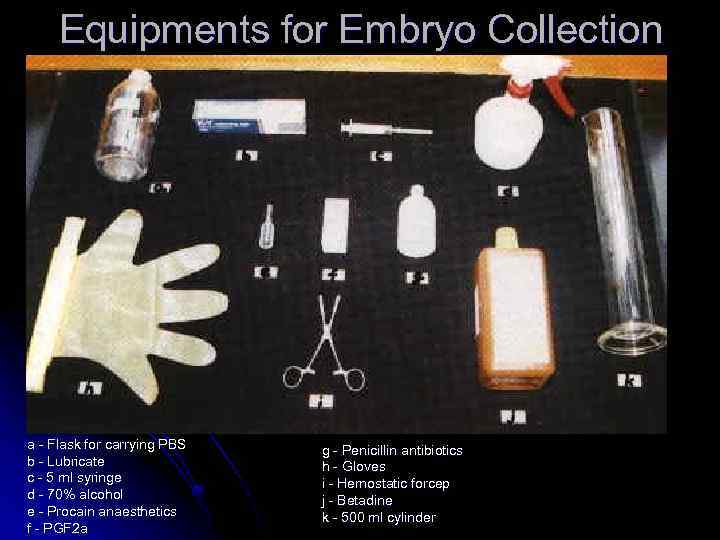 Equipments for Embryo Collection a - Flask for carrying PBS b - Lubricate c - 5 ml syringe d - 70% alcohol e - Procain anaesthetics f - PGF 2 a g - Penicillin antibiotics h - Gloves i - Hemostatic forcep j - Betadine k - 500 ml cylinder
Equipments for Embryo Collection a - Flask for carrying PBS b - Lubricate c - 5 ml syringe d - 70% alcohol e - Procain anaesthetics f - PGF 2 a g - Penicillin antibiotics h - Gloves i - Hemostatic forcep j - Betadine k - 500 ml cylinder
 Foley Catheter : a - catheter b - steel pole for insertion into the uterine horn c - upper left-inlet for inflation of air bubble cuff d - inlet for flushing and collecting embryo e - inflatable cuff
Foley Catheter : a - catheter b - steel pole for insertion into the uterine horn c - upper left-inlet for inflation of air bubble cuff d - inlet for flushing and collecting embryo e - inflatable cuff
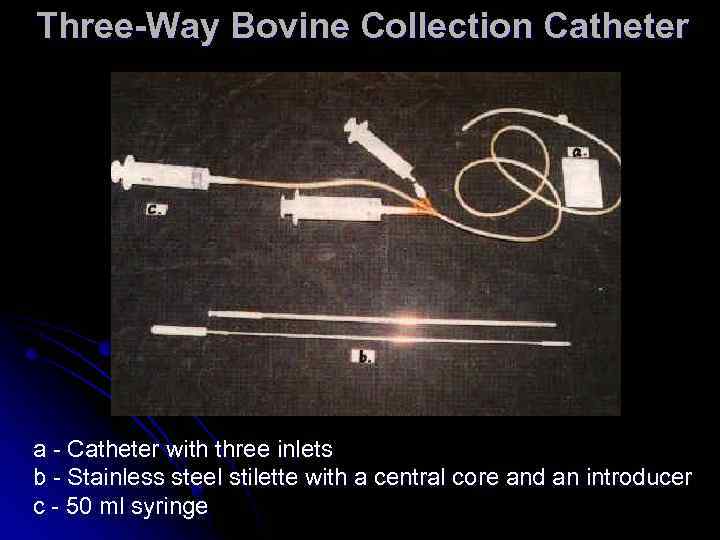 Three-Way Bovine Collection Catheter a - Catheter with three inlets b - Stainless steel stilette with a central core and an introducer c - 50 ml syringe
Three-Way Bovine Collection Catheter a - Catheter with three inlets b - Stainless steel stilette with a central core and an introducer c - 50 ml syringe
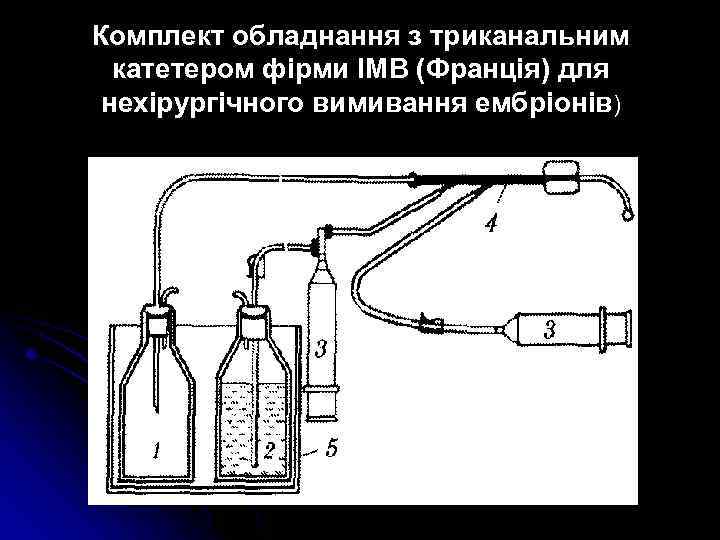 Комплект обладнання з триканальним катетером фірми ІМВ (Франція) для нехірургічного вимивання ембріонів)
Комплект обладнання з триканальним катетером фірми ІМВ (Франція) для нехірургічного вимивання ембріонів)
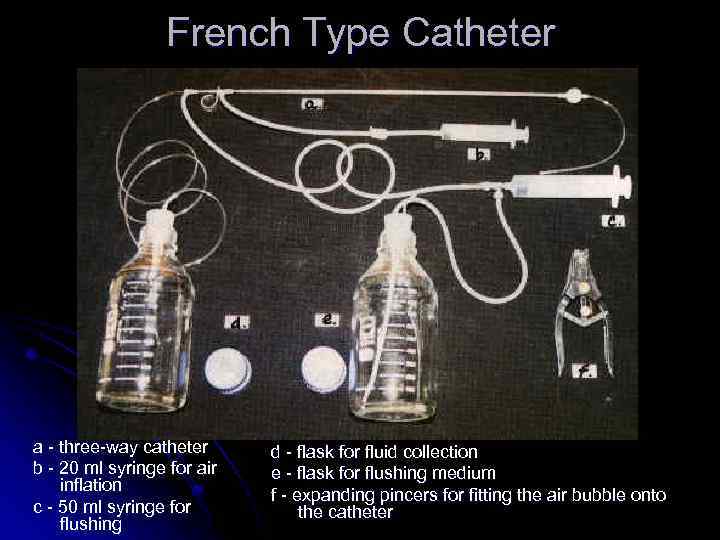 French Type Catheter a - three-way catheter b - 20 ml syringe for air inflation c - 50 ml syringe for flushing d - flask for fluid collection e - flask for flushing medium f - expanding pincers for fitting the air bubble onto the catheter
French Type Catheter a - three-way catheter b - 20 ml syringe for air inflation c - 50 ml syringe for flushing d - flask for fluid collection e - flask for flushing medium f - expanding pincers for fitting the air bubble onto the catheter


 1. Підрахунок жовтих тіл в яєчниках корови-донора (ректально): 10 чи більше – хороша реакція, менше 5 – слабка). 2. Фіксація корови: у станку в положенні стоячи так, щоб тазові кінцівки знаходилися дещо вище передніх. 3. Сакральна анестезія (для попередження частої дефекації і зняття м’язової напруги: епідурально 5 мл 2%-ного розчину новокаїну); норовливим коровам – в/м міорелаксант (рампун) 0, 5 -0, 7 мл чи маточний релаксант комбілен 0, 7 -1, 0 мл, іліханегіф 10 мл чи аміназин 5 мл. 4. Сан. обробка: теплою водою з милом миють зовнішні статеві органи і корінь хвоста, витирають паперовими серветками чи ватними тампонами.
1. Підрахунок жовтих тіл в яєчниках корови-донора (ректально): 10 чи більше – хороша реакція, менше 5 – слабка). 2. Фіксація корови: у станку в положенні стоячи так, щоб тазові кінцівки знаходилися дещо вище передніх. 3. Сакральна анестезія (для попередження частої дефекації і зняття м’язової напруги: епідурально 5 мл 2%-ного розчину новокаїну); норовливим коровам – в/м міорелаксант (рампун) 0, 5 -0, 7 мл чи маточний релаксант комбілен 0, 7 -1, 0 мл, іліханегіф 10 мл чи аміназин 5 мл. 4. Сан. обробка: теплою водою з милом миють зовнішні статеві органи і корінь хвоста, витирають паперовими серветками чи ватними тампонами.
 5. Підготовка інструментів: - стерилізація (металеві – кип’ятінням, латексні – у 96%-ному спирті); - промивання фосфатно-буферним середовищем; - вставка металевого стилета (для латексного катетера); - змазування катетера вазеліновим маслом; - поміщення катетера в захисний поліетиленовий чохол. 6. Введення катетера: у піхву (по верхньому її склепінню), далі – у канал шийки матки → зсовування поліетиленового чохла назад → введення катетера проводять через канал шийки матки в один з рогів матки (під ректальним контролем ).
5. Підготовка інструментів: - стерилізація (металеві – кип’ятінням, латексні – у 96%-ному спирті); - промивання фосфатно-буферним середовищем; - вставка металевого стилета (для латексного катетера); - змазування катетера вазеліновим маслом; - поміщення катетера в захисний поліетиленовий чохол. 6. Введення катетера: у піхву (по верхньому її склепінню), далі – у канал шийки матки → зсовування поліетиленового чохла назад → введення катетера проводять через канал шийки матки в один з рогів матки (під ректальним контролем ).
 7. Фіксація катетера у розі матки (щоб промивна рідина не витікала мимо нього): видалення мандрена, нагнітання повітря (10 -15 мл) в балончик катетера. 8. Промивання порожнини рогу (під ректальним контролем з легким масажем): 40 -60 мл промивної рідини (загалом не більше 500 мл). 9. Та ж сама процедура і в іншому розі (випускання повітря з балончика, видалення катетера з одного рогу та введення в інший. 10. Санація матки (ч/з катетер в матку вводять пеніцилін та стрептоміцин по 500 тис. ОД і тетрациклин 200 тис. ОД. В якості середовища для промивання матки використовують фосфатно-сольовий буфер (ФСБ) Дюльбекко.
7. Фіксація катетера у розі матки (щоб промивна рідина не витікала мимо нього): видалення мандрена, нагнітання повітря (10 -15 мл) в балончик катетера. 8. Промивання порожнини рогу (під ректальним контролем з легким масажем): 40 -60 мл промивної рідини (загалом не більше 500 мл). 9. Та ж сама процедура і в іншому розі (випускання повітря з балончика, видалення катетера з одного рогу та введення в інший. 10. Санація матки (ч/з катетер в матку вводять пеніцилін та стрептоміцин по 500 тис. ОД і тетрациклин 200 тис. ОД. В якості середовища для промивання матки використовують фосфатно-сольовий буфер (ФСБ) Дюльбекко.
 Вилучення зародків нехірургічним способом: 1 – катетер для вилучення зародків; 2 – шийка та 3 – ріг матки; 4 – надувний балончик; 5 – яєчники
Вилучення зародків нехірургічним способом: 1 – катетер для вилучення зародків; 2 – шийка та 3 – ріг матки; 4 – надувний балончик; 5 – яєчники


 - - За хірургічного вилучення: тварину не годують 1 -1, 5 доби і не поять 56 год. ; використовують двоканальний з надувною кулькою катетер Фолея № 14 (з латексної гуми) зі та спец. тупою голкою або двоканальний катетер західнонімецької фірми «Руш Нейштадт» чи триканальний катетер франц. фірми ІMB; загальне чи місцеве знеболення → розріз черевної стінки по білій лінії чи (частіше) в області голодної ямки справа чи зліва → підрахунок кількості ЖТ → підтягування і розріз одного з рогів матки → введення в його порожнину катетера.
- - За хірургічного вилучення: тварину не годують 1 -1, 5 доби і не поять 56 год. ; використовують двоканальний з надувною кулькою катетер Фолея № 14 (з латексної гуми) зі та спец. тупою голкою або двоканальний катетер західнонімецької фірми «Руш Нейштадт» чи триканальний катетер франц. фірми ІMB; загальне чи місцеве знеболення → розріз черевної стінки по білій лінії чи (частіше) в області голодної ямки справа чи зліва → підрахунок кількості ЖТ → підтягування і розріз одного з рогів матки → введення в його порожнину катетера.
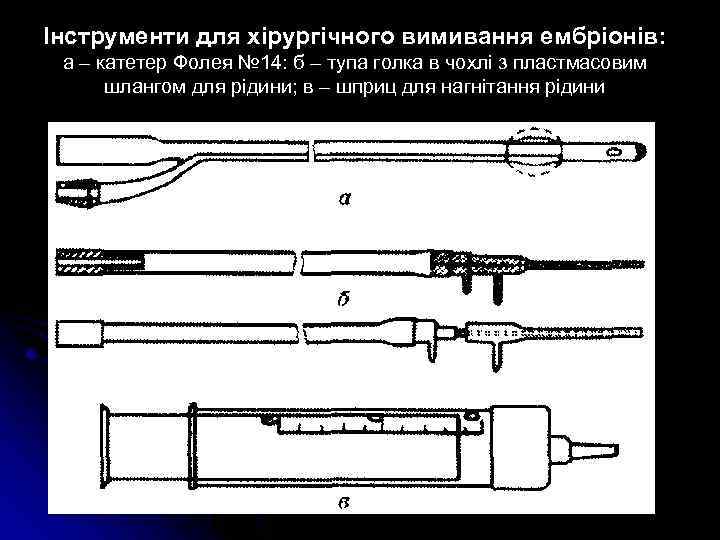 Інструменти для хірургічного вимивання ембріонів: а – катетер Фолея № 14: б – тупа голка в чохлі з пластмасовим шлангом для рідини; в – шприц для нагнітання рідини
Інструменти для хірургічного вимивання ембріонів: а – катетер Фолея № 14: б – тупа голка в чохлі з пластмасовим шлангом для рідини; в – шприц для нагнітання рідини
 Хірургічний спосіб: ü ü ü складний працемісткий потребує великих витрат після операції у тварини значно знижується рівень молочної продуктивності мається ризик втрати високоцінного донора при загальному знеболенні його не можна часто повторювати (у післяопераційний період утворюються спайки)
Хірургічний спосіб: ü ü ü складний працемісткий потребує великих витрат після операції у тварини значно знижується рівень молочної продуктивності мається ризик втрати високоцінного донора при загальному знеболенні його не можна часто повторювати (у післяопераційний період утворюються спайки)
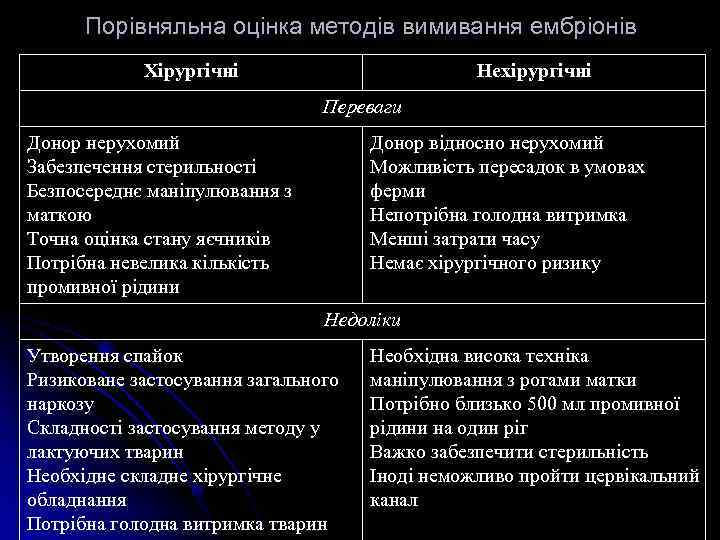 Порівняльна оцінка методів вимивання ембріонів Хірургічні Нехірургічні Переваги Донор нерухомий Забезпечення стерильності Безпосереднє маніпулювання з маткою Точна оцінка стану яєчників Потрібна невелика кількість промивної рідини Донор відносно нерухомий Можливість пересадок в умовах ферми Непотрібна голодна витримка Менші затрати часу Немає хірургічного ризику Недоліки Утворення спайок Ризиковане застосування загального наркозу Складності застосування методу у лактуючих тварин Необхідне складне хірургічне обладнання Потрібна голодна витримка тварин Необхідна висока техніка маніпулювання з рогами матки Потрібно близько 500 мл промивної рідини на один ріг Важко забезпечити стерильність Іноді неможливо пройти цервікальний канал
Порівняльна оцінка методів вимивання ембріонів Хірургічні Нехірургічні Переваги Донор нерухомий Забезпечення стерильності Безпосереднє маніпулювання з маткою Точна оцінка стану яєчників Потрібна невелика кількість промивної рідини Донор відносно нерухомий Можливість пересадок в умовах ферми Непотрібна голодна витримка Менші затрати часу Немає хірургічного ризику Недоліки Утворення спайок Ризиковане застосування загального наркозу Складності застосування методу у лактуючих тварин Необхідне складне хірургічне обладнання Потрібна голодна витримка тварин Необхідна висока техніка маніпулювання з рогами матки Потрібно близько 500 мл промивної рідини на один ріг Важко забезпечити стерильність Іноді неможливо пройти цервікальний канал
 Пошук, оцінка, культивування і зберігання зародків t 0 в лабораторії = 20. . . 25°С За 3 год. до початку роботи приміщення обробляють УФпроменями 15. . . 20 хв. Верхній шар рідини видаляють, нижній порційно (по 20 -30 мл) для виявлення зародків досліджують у великих годинникових стеклах чи чашках Петрі під бінокулярною лупою при 10 -50 -кратному збільшенні; знайдені зародки за допомогою пастерівської піпетки переносять в середовище для короткотривалого зберігання (середовище Дюльбекко з додаванням 20 % фетальної сироватки теля). Оцінка якості та життєздатності зародків за морфологічними ознаками та результатами їх культивування: враховують відповідність стадії розвитку зародку його віку, цілісність і форму прозорої оболонки; рівномірність дроблення бластомерів і стан їх цитоплазми; величину і прозорість перивітелінового простору – зародки з ознаками дегенерації, виродливостей та недорозвитку для пересадок непридатні.
Пошук, оцінка, культивування і зберігання зародків t 0 в лабораторії = 20. . . 25°С За 3 год. до початку роботи приміщення обробляють УФпроменями 15. . . 20 хв. Верхній шар рідини видаляють, нижній порційно (по 20 -30 мл) для виявлення зародків досліджують у великих годинникових стеклах чи чашках Петрі під бінокулярною лупою при 10 -50 -кратному збільшенні; знайдені зародки за допомогою пастерівської піпетки переносять в середовище для короткотривалого зберігання (середовище Дюльбекко з додаванням 20 % фетальної сироватки теля). Оцінка якості та життєздатності зародків за морфологічними ознаками та результатами їх культивування: враховують відповідність стадії розвитку зародку його віку, цілісність і форму прозорої оболонки; рівномірність дроблення бластомерів і стан їх цитоплазми; величину і прозорість перивітелінового простору – зародки з ознаками дегенерації, виродливостей та недорозвитку для пересадок непридатні.
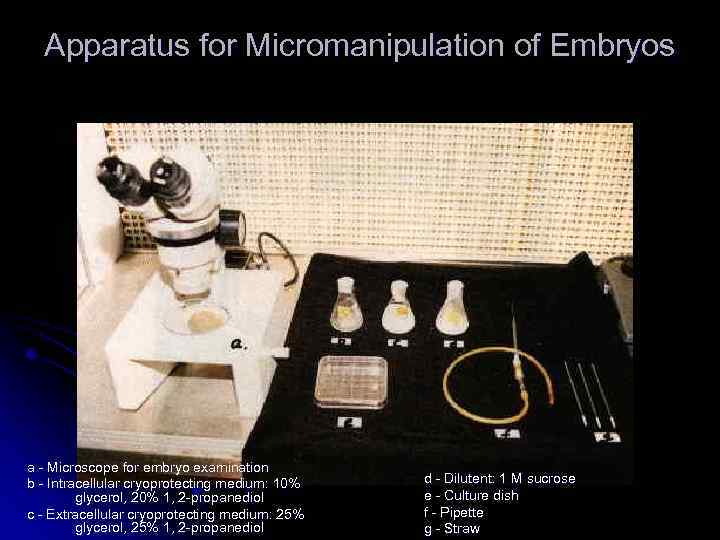 Apparatus for Micromanipulation of Embryos a - Microscope for embryo examination b - Intracellular cryoprotecting medium: 10% glycerol, 20% 1, 2 -propanediol c - Extracellular cryoprotecting medium: 25% glycerol, 25% 1, 2 -propanediol d - Dilutent: 1 M sucrose e - Culture dish f - Pipette g - Straw
Apparatus for Micromanipulation of Embryos a - Microscope for embryo examination b - Intracellular cryoprotecting medium: 10% glycerol, 20% 1, 2 -propanediol c - Extracellular cryoprotecting medium: 25% glycerol, 25% 1, 2 -propanediol d - Dilutent: 1 M sucrose e - Culture dish f - Pipette g - Straw
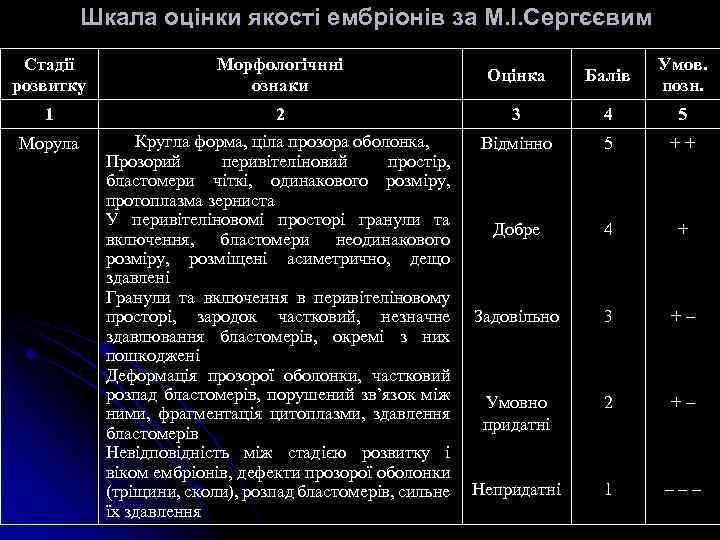 Шкала оцінки якості ембріонів за М. І. Сергєєвим Стадії розвитку Морфологічнні ознаки Оцінка Балів Умов. позн. 1 2 3 4 5 Морула Кругла форма, ціла прозора оболонка, Прозорий перивітеліновий простір, бластомери чіткі, одинакового розміру, протоплазма зерниста У перивітеліновомі просторі гранули та включення, бластомери неодинакового розміру, розміщені асиметрично, дещо здавлені Гранули та включення в перивітеліновому просторі, зародок частковий, незначне здавлювання бластомерів, окремі з них пошкоджені Деформація прозорої оболонки, частковий розпад бластомерів, порушений зв’язок між ними, фрагментація цитоплазми, здавлення бластомерів Невідповідність між стадією розвитку і віком ембріонів, дефекти прозорої оболонки (тріщини, сколи), розпад бластомерів, сильне їх здавлення Відмінно 5 ++ Добре 4 + Задовільно 3 +– Умовно придатні 2 +– Непридатні 1 –––
Шкала оцінки якості ембріонів за М. І. Сергєєвим Стадії розвитку Морфологічнні ознаки Оцінка Балів Умов. позн. 1 2 3 4 5 Морула Кругла форма, ціла прозора оболонка, Прозорий перивітеліновий простір, бластомери чіткі, одинакового розміру, протоплазма зерниста У перивітеліновомі просторі гранули та включення, бластомери неодинакового розміру, розміщені асиметрично, дещо здавлені Гранули та включення в перивітеліновому просторі, зародок частковий, незначне здавлювання бластомерів, окремі з них пошкоджені Деформація прозорої оболонки, частковий розпад бластомерів, порушений зв’язок між ними, фрагментація цитоплазми, здавлення бластомерів Невідповідність між стадією розвитку і віком ембріонів, дефекти прозорої оболонки (тріщини, сколи), розпад бластомерів, сильне їх здавлення Відмінно 5 ++ Добре 4 + Задовільно 3 +– Умовно придатні 2 +– Непридатні 1 –––
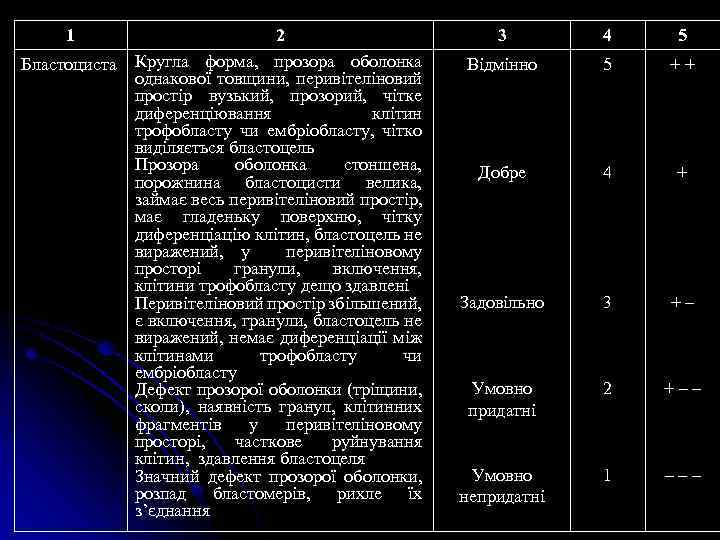 1 Бластоциста 2 Кругла форма, прозора оболонка однакової товщини, перивітеліновий простір вузький, прозорий, чітке диференціювання клітин трофобласту чи ембріобласту, чітко виділяється бластоцель Прозора оболонка стоншена, порожнина бластоцисти велика, займає весь перивітеліновий простір, має гладеньку поверхню, чітку диференціацію клітин, бластоцель не виражений, у перивітеліновому просторі гранули, включення, клітини трофобласту дещо здавлені Перивітеліновий простір збільшений, є включення, гранули, бластоцель не виражений, немає диференціації між клітинами трофобласту чи ембріобласту Дефект прозорої оболонки (тріщини, сколи), наявність гранул, клітинних фрагментів у перивітеліновому просторі, часткове руйнування клітин, здавлення бластоцеля Значний дефект прозорої оболонки, розпад бластомерів, рихле їх з’єднання 3 4 5 Відмінно 5 ++ Добре 4 + Задовільно 3 +– Умовно придатні 2 +–– Умовно непридатні 1 –––
1 Бластоциста 2 Кругла форма, прозора оболонка однакової товщини, перивітеліновий простір вузький, прозорий, чітке диференціювання клітин трофобласту чи ембріобласту, чітко виділяється бластоцель Прозора оболонка стоншена, порожнина бластоцисти велика, займає весь перивітеліновий простір, має гладеньку поверхню, чітку диференціацію клітин, бластоцель не виражений, у перивітеліновому просторі гранули, включення, клітини трофобласту дещо здавлені Перивітеліновий простір збільшений, є включення, гранули, бластоцель не виражений, немає диференціації між клітинами трофобласту чи ембріобласту Дефект прозорої оболонки (тріщини, сколи), наявність гранул, клітинних фрагментів у перивітеліновому просторі, часткове руйнування клітин, здавлення бластоцеля Значний дефект прозорої оболонки, розпад бластомерів, рихле їх з’єднання 3 4 5 Відмінно 5 ++ Добре 4 + Задовільно 3 +– Умовно придатні 2 +–– Умовно непридатні 1 –––
 Після оцінки зародків їх культивують при 370 С до моменту пересадки чи залишають для зберігання. Для заморожування зародків готують середовище (в г/л): натрію хлорид 8, 0; калію хлорид 0, 2; гідроортофосфат (дінатрійфосфат) безводний 1, 15; дигідроортофосфат (монокалійфосфат) однозаміщений 0, 2; магнію хлорид, що містить 6 молекул води, 0, 1; калію хлорид безводний 0, 1; натрію піруват – 376; глюкоза – 1, 0 + 20% фетальної сироватки крові теляти і 100 тис. ОД/л пеніциліну (калієвої солі). Потім готують серію розчинів з різною концентрацією гліцерину за методикою, викладеною в інструкції, і насичують зародок гліцерином одно- чи багатоступеневим способом, контролюючи під мікроскопом при t = 20°С.
Після оцінки зародків їх культивують при 370 С до моменту пересадки чи залишають для зберігання. Для заморожування зародків готують середовище (в г/л): натрію хлорид 8, 0; калію хлорид 0, 2; гідроортофосфат (дінатрійфосфат) безводний 1, 15; дигідроортофосфат (монокалійфосфат) однозаміщений 0, 2; магнію хлорид, що містить 6 молекул води, 0, 1; калію хлорид безводний 0, 1; натрію піруват – 376; глюкоза – 1, 0 + 20% фетальної сироватки крові теляти і 100 тис. ОД/л пеніциліну (калієвої солі). Потім готують серію розчинів з різною концентрацією гліцерину за методикою, викладеною в інструкції, і насичують зародок гліцерином одно- чи багатоступеневим способом, контролюючи під мікроскопом при t = 20°С.
 Насичені гліцерином зародки розфасовують в пайети у наступному порядку: 0, 75 М розчин сахарози в 20 % розчині ФС в ФСБ, повітряна кулька 2. . . 3 мм; ембріон в 1 М розчину гліцерину в 20% розчині ФС в ФСБ, повітряна кулька 3. . . 5 мм; простір пайети, що залишився заповнюють 0, 75 М розчином сахарози в 20 % розчині ФС в ФСБ. Установка для заморожування ембріоном складається з посудини Дьюара, контейнера для пайет, штатива для кріплення контейнера на горловині посудини Дьюара і термопар для установки програми охолодження. Охолодження проводять в декілька етапів: 1) знижують температуру від 200 С до -5. . . -7°С зі швидкістю 1 -10°С за 1 хв. ; 2) при -6. . . -70 С штучна кристалізація; 3) охолодження зі швидкістю 0, 3°С за 1 хв. до -36°С; 4) занурення в рідкий азот для швидкого охолодження до -196°С. Зберігають заморожені ембріони в посудинах Дьюара.
Насичені гліцерином зародки розфасовують в пайети у наступному порядку: 0, 75 М розчин сахарози в 20 % розчині ФС в ФСБ, повітряна кулька 2. . . 3 мм; ембріон в 1 М розчину гліцерину в 20% розчині ФС в ФСБ, повітряна кулька 3. . . 5 мм; простір пайети, що залишився заповнюють 0, 75 М розчином сахарози в 20 % розчині ФС в ФСБ. Установка для заморожування ембріоном складається з посудини Дьюара, контейнера для пайет, штатива для кріплення контейнера на горловині посудини Дьюара і термопар для установки програми охолодження. Охолодження проводять в декілька етапів: 1) знижують температуру від 200 С до -5. . . -7°С зі швидкістю 1 -10°С за 1 хв. ; 2) при -6. . . -70 С штучна кристалізація; 3) охолодження зі швидкістю 0, 3°С за 1 хв. до -36°С; 4) занурення в рідкий азот для швидкого охолодження до -196°С. Зберігають заморожені ембріони в посудинах Дьюара.
 Порядок заправки ембріону в пайету для заморожування: 1 – пробка пайети; 2 – 0, 75 М розчин сахарози; 3 – повітряна кулька; 4 – 1 М розчин гліцерину в 20% розчині ФС в ФСБ; 5 - ембріон
Порядок заправки ембріону в пайету для заморожування: 1 – пробка пайети; 2 – 0, 75 М розчин сахарози; 3 – повітряна кулька; 4 – 1 М розчин гліцерину в 20% розчині ФС в ФСБ; 5 - ембріон

 Відтавання: переносять пайету з каністри посудини Дьюара у водяну баню кімн. t 0 = 20. . . 22°С (після відтавання ембріони необхідно використати на протязі 2 год. ). Оцінка ембріонів мікроскопічно. Для пересадки придатні непошкоджені ембріони, що мають нормальну морфологічну структуру.
Відтавання: переносять пайету з каністри посудини Дьюара у водяну баню кімн. t 0 = 20. . . 22°С (після відтавання ембріони необхідно використати на протязі 2 год. ). Оцінка ембріонів мікроскопічно. Для пересадки придатні непошкоджені ембріони, що мають нормальну морфологічну структуру.
 Короткочасне зберігання ембріонів (доцільне, якщо розсинхронізація між стадію розвитку ембріона і СЦ реципієнта не перевищує 1, 5 доби): ембріон заправляють в пайету (20% розчин ФС в ФСБ чи СФСБ на довжину 30. . . 45 мм, повітряна кулька на 5. . . 10 мм, 20% розчин ФС в ФСБ (на 20. . . 30 мм) з ембріоном, знову повітряна кулька – 5. . . 10 мм і простір, що залишився, заповнюють 20 % розчином ФС в ФСБ.
Короткочасне зберігання ембріонів (доцільне, якщо розсинхронізація між стадію розвитку ембріона і СЦ реципієнта не перевищує 1, 5 доби): ембріон заправляють в пайету (20% розчин ФС в ФСБ чи СФСБ на довжину 30. . . 45 мм, повітряна кулька на 5. . . 10 мм, 20% розчин ФС в ФСБ (на 20. . . 30 мм) з ембріоном, знову повітряна кулька – 5. . . 10 мм і простір, що залишився, заповнюють 20 % розчином ФС в ФСБ.
 Для зберігання ембріонів при 0°С використовують льодяну баню (можливе зберігання зародків протягом 2 діб, з часу вилучення пайети з льодяної бані до пересадки не повинно пройти більше 2 год. ). До 4 -7 днів зберігати зародки можна в перев’язаному яйцепроводі кролика. Інтервал часу між одержанням зародку і початком наступного технологічного етапу (короткочасного зберігання, кріоконсервації) не повинен перевищувати 2 год.
Для зберігання ембріонів при 0°С використовують льодяну баню (можливе зберігання зародків протягом 2 діб, з часу вилучення пайети з льодяної бані до пересадки не повинно пройти більше 2 год. ). До 4 -7 днів зберігати зародки можна в перев’язаному яйцепроводі кролика. Інтервал часу між одержанням зародку і початком наступного технологічного етапу (короткочасного зберігання, кріоконсервації) не повинен перевищувати 2 год.
 Синхронізація СЦ реципієнтів і донорів При пересадці зародків стан всього організму і статевої системи реципієнта повинні відповідати стадії розвитку зародків. Якщо різниця в строках прояву СЦ між донором та реципієнтом складає більше 24 год. , то частота вагітностей після пересадок різко знижується.
Синхронізація СЦ реципієнтів і донорів При пересадці зародків стан всього організму і статевої системи реципієнта повинні відповідати стадії розвитку зародків. Якщо різниця в строках прояву СЦ між донором та реципієнтом складає більше 24 год. , то частота вагітностей після пересадок різко знижується.
 При незначній кількості тваринреципієнтів виникає необхідність у синхронізації СЦ у реципієнтів і донорів шляхом використання простагландина Ф 2α (Естрофан, Ремофан, Аніпрост) – двічі з інтервалом 11 днів, вводячи по одній ампулі (0, 5 мг клопростенолу); другу ін’єкцію роблять одночасно донору і реципієнтам
При незначній кількості тваринреципієнтів виникає необхідність у синхронізації СЦ у реципієнтів і донорів шляхом використання простагландина Ф 2α (Естрофан, Ремофан, Аніпрост) – двічі з інтервалом 11 днів, вводячи по одній ампулі (0, 5 мг клопростенолу); другу ін’єкцію роблять одночасно донору і реципієнтам
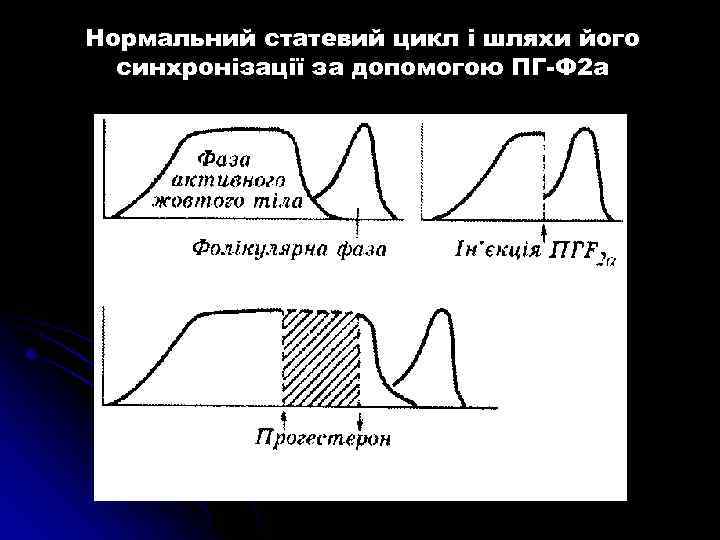 Нормальний статевий цикл і шляхи його синхронізації за допомогою ПГ-Ф 2 а
Нормальний статевий цикл і шляхи його синхронізації за допомогою ПГ-Ф 2 а
 Схема синхронізації донора і реципієнта
Схема синхронізації донора і реципієнта
 Пересадка зародків q Здійснюють хірургічним і нехірургічним способами. q Безпосередньо перед пересадкою ще раз обслідують стан здоров’я і статевої системи реципієнтів, визначають, в якому яєчнику знаходиться ЖТ, чи відповідає його величина і консистенція строкам СЦ; найкращим місцем пересадки – верхівка рогу матки, що прилягає до яєчника з ЖТ.
Пересадка зародків q Здійснюють хірургічним і нехірургічним способами. q Безпосередньо перед пересадкою ще раз обслідують стан здоров’я і статевої системи реципієнтів, визначають, в якому яєчнику знаходиться ЖТ, чи відповідає його величина і консистенція строкам СЦ; найкращим місцем пересадки – верхівка рогу матки, що прилягає до яєчника з ЖТ.
 Хірургічний спосіб: l можна використовувати оперативний доступ з розрізом по білій лінії черева – підготовка і техніка операції такі ж, як і при вилученні зародків.
Хірургічний спосіб: l можна використовувати оперативний доступ з розрізом по білій лінії черева – підготовка і техніка операції такі ж, як і при вилученні зародків.
 Нехірургічний спосіб більш придатний для використання його у виробничих умовах. Для цього застосовують різні катетери – часто використовують прибор для ШО Касу у модифікованій формі
Нехірургічний спосіб більш придатний для використання його у виробничих умовах. Для цього застосовують різні катетери – часто використовують прибор для ШО Касу у модифікованій формі
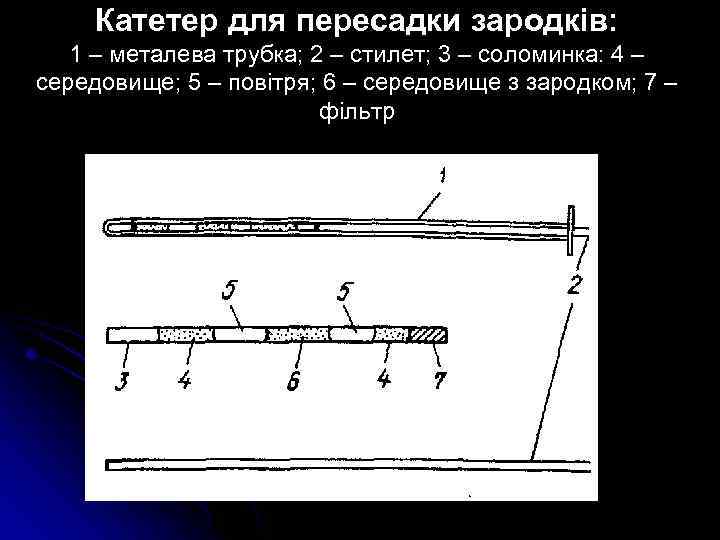 Катетер для пересадки зародків: 1 – металева трубка; 2 – стилет; 3 – соломинка: 4 – середовище; 5 – повітря; 6 – середовище з зародком; 7 – фільтр
Катетер для пересадки зародків: 1 – металева трубка; 2 – стилет; 3 – соломинка: 4 – середовище; 5 – повітря; 6 – середовище з зародком; 7 – фільтр

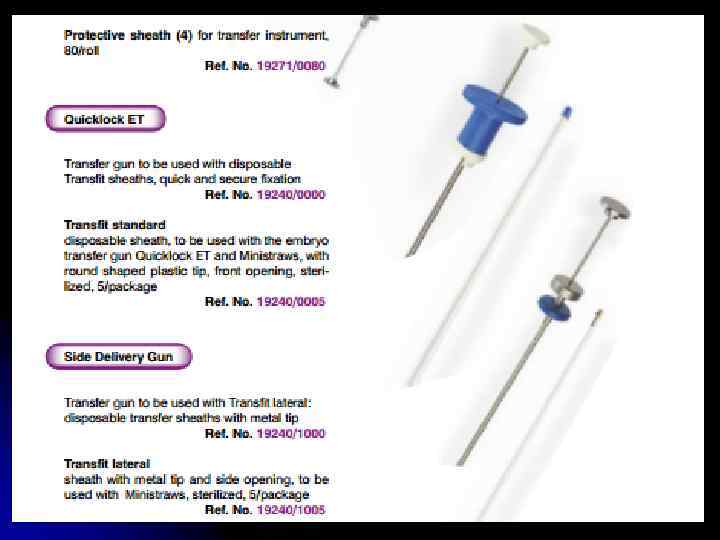
 Реципієнтів до пересадки зародків готують так же, як і донорів при нехірургічному вилученні. Для зменшення скорочень матки, зниження можливості пошкодження ендометрію → матковий релаксант. Прибор вводять у піхву, при досягненні шийки матки знімають тонку оболонку, просувають під ректальним контролем через канал шийки матки далі у ріг матки, виштовхують вміст пайети і обережно видаляють з матки. Приживленість зародків складає 50%.
Реципієнтів до пересадки зародків готують так же, як і донорів при нехірургічному вилученні. Для зменшення скорочень матки, зниження можливості пошкодження ендометрію → матковий релаксант. Прибор вводять у піхву, при досягненні шийки матки знімають тонку оболонку, просувають під ректальним контролем через канал шийки матки далі у ріг матки, виштовхують вміст пайети і обережно видаляють з матки. Приживленість зародків складає 50%.
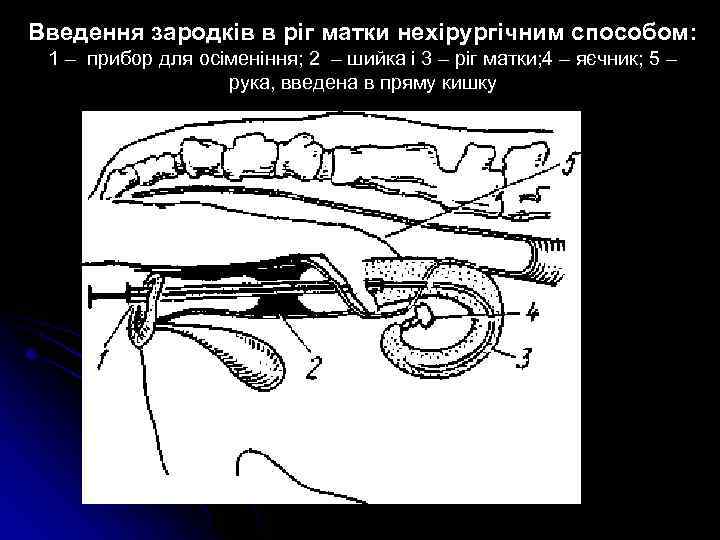 Введення зародків в ріг матки нехірургічним способом: 1 – прибор для осіменіння; 2 – шийка і 3 – ріг матки; 4 – яєчник; 5 – рука, введена в пряму кишку
Введення зародків в ріг матки нехірургічним способом: 1 – прибор для осіменіння; 2 – шийка і 3 – ріг матки; 4 – яєчник; 5 – рука, введена в пряму кишку
 Після підсадки тваринам створюють умови годівлі і утримання у відповідності до зоогігієнічних вимог, не допускають травмування і сильних негативних стресових впливів. Організовують ранню рефлексологічну діагностику вагітності, що виключає можливість пропуску повторної охоти. Через 2 міс. після пересадки проводять діагностику вагітності і неплідності ректальним способом.
Після підсадки тваринам створюють умови годівлі і утримання у відповідності до зоогігієнічних вимог, не допускають травмування і сильних негативних стресових впливів. Організовують ранню рефлексологічну діагностику вагітності, що виключає можливість пропуску повторної охоти. Через 2 міс. після пересадки проводять діагностику вагітності і неплідності ректальним способом.
 Використовують зародки протягом перших 3 год. з моменту їх одержання. Зберігають в стерильній сироватці на годинникових стеклах при 35°С. Успіх трансплантації залежить від того, в який ріг поміщена зигота: в іпсилатеральний чи контрлатеральний (протилежний) яєчнику з ЖТ. У першому випадку приживленість зародків значно вище (85% проти 35%).
Використовують зародки протягом перших 3 год. з моменту їх одержання. Зберігають в стерильній сироватці на годинникових стеклах при 35°С. Успіх трансплантації залежить від того, в який ріг поміщена зигота: в іпсилатеральний чи контрлатеральний (протилежний) яєчнику з ЖТ. У першому випадку приживленість зародків значно вище (85% проти 35%).
 Серед факторів, що впливають на успіх пересадки ембріонів у реципієнтів, найважливішими є наступні - якість ембріона і відповідна техніка пересадки; - вибраний час пересадки по відношенню до СЦ реципієнта; - адекватна концентрація прогестерону в організмі під час пересадки; - управління чинниками, що викликають стрес (управління, годівля, утримання і т. д. ).
Серед факторів, що впливають на успіх пересадки ембріонів у реципієнтів, найважливішими є наступні - якість ембріона і відповідна техніка пересадки; - вибраний час пересадки по відношенню до СЦ реципієнта; - адекватна концентрація прогестерону в організмі під час пересадки; - управління чинниками, що викликають стрес (управління, годівля, утримання і т. д. ).
 Фактори, що впливають на життєздатність ембріонів при пересадці їх реципієнтам l - Пересадка ембріонів ближче до початкової частини входу в ріг матки дає порівняно нижчі результати їх приживлюваності у реципієнтів, ніж при пересадці в верхівку. Основною причиною цього може бути велика забезпеченість прогестероном цій області матки через кровоносне судини, що сприяє посиленню секреції маткових залоз і, тим самим, забезпечує краще живлення ембріона в перші тижні життя
Фактори, що впливають на життєздатність ембріонів при пересадці їх реципієнтам l - Пересадка ембріонів ближче до початкової частини входу в ріг матки дає порівняно нижчі результати їх приживлюваності у реципієнтів, ніж при пересадці в верхівку. Основною причиною цього може бути велика забезпеченість прогестероном цій області матки через кровоносне судини, що сприяє посиленню секреції маткових залоз і, тим самим, забезпечує краще живлення ембріона в перші тижні життя
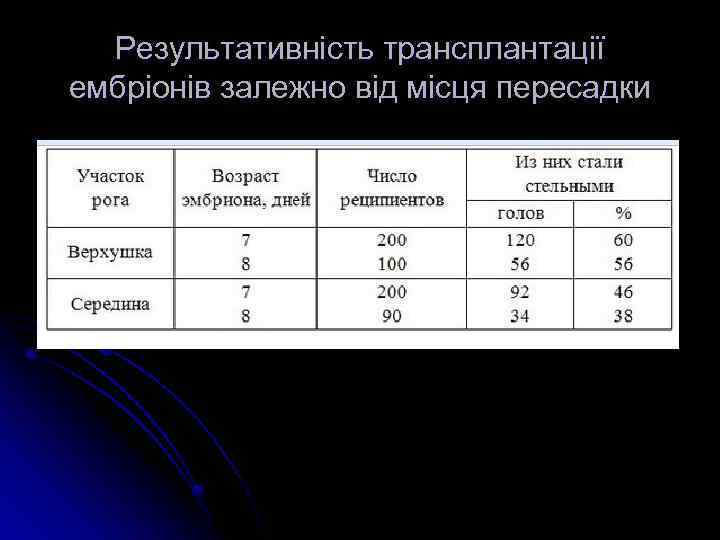 Результативність трансплантації ембріонів залежно від місця пересадки
Результативність трансплантації ембріонів залежно від місця пересадки
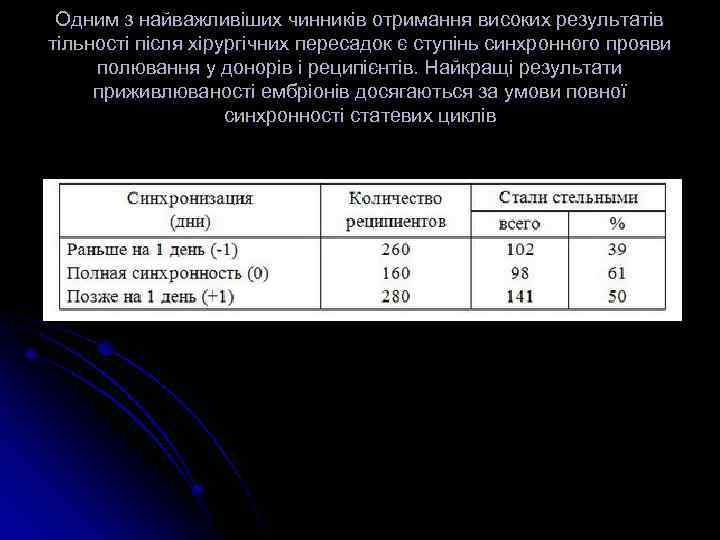 Одним з найважливіших чинників отримання високих результатів тільності після хірургічних пересадок є ступінь синхронного прояви полювання у донорів і реципієнтів. Найкращі результати приживлюваності ембріонів досягаються за умови повної синхронності статевих циклів
Одним з найважливіших чинників отримання високих результатів тільності після хірургічних пересадок є ступінь синхронного прояви полювання у донорів і реципієнтів. Найкращі результати приживлюваності ембріонів досягаються за умови повної синхронності статевих циклів
 ОСОБЛИВОСТІ ГОДІВЛІ І УТРИМАННЯ КОРІВ-ДОНОРІВ ТА ТЕЛИЦЬ-РЕЦИПІЄНТІВ Годують тварин у відповідності до нормативів і зоотехнічних вимог по годівлі племінної худоби. Раціон повинен бути забезпеченим різноманітними якісними кормами з вмістом всіх поживних речовин не нижче встановлених норм. Щоквартально корма повинні підлягати дослідженню на їх повноцінність і токсичність в ветеринарних лабораторіях. Перевагу слід надавати злакобобовим сумішам. Раціони повинні бути збалансовані за всіма показникаи, особливу увагу слід приділити вмісту в них вітамінів. Не можна допускати білкового перекорму. Кількість концентрованих кормів не перевищувати допустимих норм. При зниженні кількості концентратів до 70. . . 80 % норми необхідно збільшити кількість сіна. Тварин донорів і реципієнтів слід утримувати в чистих, сухих, добре вентильованих приміщеннях при температурі і вологості повітря, що відповідають вимогам. В літній час їх необхідно випасати на пасовищі, а на території для утриманні худоби слід виконувати всі ветеринарні вимоги, що пред’являються до тваринницьких підприємств закритого типу.
ОСОБЛИВОСТІ ГОДІВЛІ І УТРИМАННЯ КОРІВ-ДОНОРІВ ТА ТЕЛИЦЬ-РЕЦИПІЄНТІВ Годують тварин у відповідності до нормативів і зоотехнічних вимог по годівлі племінної худоби. Раціон повинен бути забезпеченим різноманітними якісними кормами з вмістом всіх поживних речовин не нижче встановлених норм. Щоквартально корма повинні підлягати дослідженню на їх повноцінність і токсичність в ветеринарних лабораторіях. Перевагу слід надавати злакобобовим сумішам. Раціони повинні бути збалансовані за всіма показникаи, особливу увагу слід приділити вмісту в них вітамінів. Не можна допускати білкового перекорму. Кількість концентрованих кормів не перевищувати допустимих норм. При зниженні кількості концентратів до 70. . . 80 % норми необхідно збільшити кількість сіна. Тварин донорів і реципієнтів слід утримувати в чистих, сухих, добре вентильованих приміщеннях при температурі і вологості повітря, що відповідають вимогам. В літній час їх необхідно випасати на пасовищі, а на території для утриманні худоби слід виконувати всі ветеринарні вимоги, що пред’являються до тваринницьких підприємств закритого типу.
 ТЕ коней l За нинішніх засобах розмноження коней, заснованих на природному перебігу процесу, без істотного втручання людини, за все життя від кобили можна отримати лише 12 -14 лошат. У той же час сотні продукованих в яєчниках кобили яйцеклітин гинуть. Тобто генетично обумовлені можливості розмноження кобил використовуються лише на 5 -7%. Головна причина такої невідповідності - тривала жеребність. На жеребність доводиться 80 -90% часу племінного використання кобили. Як показують розрахунки, застосовуючи метод ТЕ від однієї кобили-донора, можна отримувати щорічно 10 і більше нащадків.
ТЕ коней l За нинішніх засобах розмноження коней, заснованих на природному перебігу процесу, без істотного втручання людини, за все життя від кобили можна отримати лише 12 -14 лошат. У той же час сотні продукованих в яєчниках кобили яйцеклітин гинуть. Тобто генетично обумовлені можливості розмноження кобил використовуються лише на 5 -7%. Головна причина такої невідповідності - тривала жеребність. На жеребність доводиться 80 -90% часу племінного використання кобили. Як показують розрахунки, застосовуючи метод ТЕ від однієї кобили-донора, можна отримувати щорічно 10 і більше нащадків.
 l проводиться з метою вивчення причин ембріональної смертності, особливо у чистокровних кобил, отримання приплоду від старих тварин з патологіями матки та одержання генетично ідентичних цінних лошат. l Здійснюють хірургічним і нехірургічним методами. l Ембріони вимивають на 6 -9 -й день
l проводиться з метою вивчення причин ембріональної смертності, особливо у чистокровних кобил, отримання приплоду від старих тварин з патологіями матки та одержання генетично ідентичних цінних лошат. l Здійснюють хірургічним і нехірургічним методами. l Ембріони вимивають на 6 -9 -й день
 l СО у кобил-донорів викликається, як правило, введенням екстракту гіпофізу коней, оскільки застосування СЖК, КЖК та ін. гонадотропних препаратів не завжди призводить до СО. Розробку методики ТЕ гальмує те, що не завжди вдається викликати СО у непарувальний сезон.
l СО у кобил-донорів викликається, як правило, введенням екстракту гіпофізу коней, оскільки застосування СЖК, КЖК та ін. гонадотропних препаратів не завжди призводить до СО. Розробку методики ТЕ гальмує те, що не завжди вдається викликати СО у непарувальний сезон.
 l У кобил реєструється затримання ембріонів у яйцепроводах. Вони мігрують у матку лише на 2 -4 клітинній стадії розвитку. В цей період ембріони виділяють невідому речовину, що дозволяє їм рухатись через істмус (перешийок яйцеводу) в матку. Тому рекомендується вимивати ембріони не тільки з рогів матки, а й з яйцеводів.
l У кобил реєструється затримання ембріонів у яйцепроводах. Вони мігрують у матку лише на 2 -4 клітинній стадії розвитку. В цей період ембріони виділяють невідому речовину, що дозволяє їм рухатись через істмус (перешийок яйцеводу) в матку. Тому рекомендується вимивати ембріони не тільки з рогів матки, а й з яйцеводів.
 l Зберігаються ембріони у яйцепроводі кролиць протягом 48 год. Німецькою фірмою “Minitііb” розроблений метод кріоконсервації ембріонів. Вони заморожуються за допомогою приладу Gryomat 2000 P і зберігаються в рідкому азоті в соломинках, об’ємом 0, 25 і 0, 5 мл.
l Зберігаються ембріони у яйцепроводі кролиць протягом 48 год. Німецькою фірмою “Minitііb” розроблений метод кріоконсервації ембріонів. Вони заморожуються за допомогою приладу Gryomat 2000 P і зберігаються в рідкому азоті в соломинках, об’ємом 0, 25 і 0, 5 мл.
 ТЕ овець проводять хірургічним способом. Внаслідок утворень спайок рогів матки та яйцепроводів після хірургічного втручання, донорів і реципієнтів використовують не більше 3 разів за сезон. l Здійснюють у парувальний сезон, коли яєчники реагують СО на введення СЖК і ФСГ. Рівень овуляції в середньому складає 6 -10 на донора. l
ТЕ овець проводять хірургічним способом. Внаслідок утворень спайок рогів матки та яйцепроводів після хірургічного втручання, донорів і реципієнтів використовують не більше 3 разів за сезон. l Здійснюють у парувальний сезон, коли яєчники реагують СО на введення СЖК і ФСГ. Рівень овуляції в середньому складає 6 -10 на донора. l
 l Осіменіння овець проводиться природньо 3 -4 рази протягом статевої охоти, з інтервалом 10 -12 годин. l Для трансплантації використовують ембріони 4 -7 -денного віку, які знаходяться на стадії морули або бластоцисти. Асинхронність між статевим циклом донора і реципієнта може складати ± 2 дні.
l Осіменіння овець проводиться природньо 3 -4 рази протягом статевої охоти, з інтервалом 10 -12 годин. l Для трансплантації використовують ембріони 4 -7 -денного віку, які знаходяться на стадії морули або бластоцисти. Асинхронність між статевим циклом донора і реципієнта може складати ± 2 дні.
 У овець вилучення зародків хірургічним способом проводять через 40 -80 год. після прояву перших ознак статевої охоти. У залежності від строків виконання процедури промивають різні ділянки статевих шляхів. В перші три доби промивання підлягають яйцепроводи, а іноді і кінцеву частину рогів матки; на 5 -7 -й день роблять змиви з великої частини рогів матки, а після 9 -го дня – промивають всю матку.
У овець вилучення зародків хірургічним способом проводять через 40 -80 год. після прояву перших ознак статевої охоти. У залежності від строків виконання процедури промивають різні ділянки статевих шляхів. В перші три доби промивання підлягають яйцепроводи, а іноді і кінцеву частину рогів матки; на 5 -7 -й день роблять змиви з великої частини рогів матки, а після 9 -го дня – промивають всю матку.
 Вівцям-реципієнтам після лапаротомії по білій лінії живота зародки трансплантують в яйцепровід чи матку. Зиготи у стані від 2 до 6 бластомерів вводять піпеткою Пастера в яйцепровід на глибину 2 -3 см. Зародки з 8 -16 бластомерами чи бластоцисти вводять в матку піпеткою через отвір, пророблений тупою голкою в стінці матки на межі з широкою матковою зв’язкою.
Вівцям-реципієнтам після лапаротомії по білій лінії живота зародки трансплантують в яйцепровід чи матку. Зиготи у стані від 2 до 6 бластомерів вводять піпеткою Пастера в яйцепровід на глибину 2 -3 см. Зародки з 8 -16 бластомерами чи бластоцисти вводять в матку піпеткою через отвір, пророблений тупою голкою в стінці матки на межі з широкою матковою зв’язкою.
 l Приживлення ембріонів вище при пересаджуванні їх у яйцепроводи, ніж у матку. l Ембріони можуть зберігатися у яйцепроводі кролиці протягом 5 ти діб. Розроблений метод тривалого зберігання ембріонів овець у середовищах, які у своєму складі мають кріопротектор — гліцерин.
l Приживлення ембріонів вище при пересаджуванні їх у яйцепроводи, ніж у матку. l Ембріони можуть зберігатися у яйцепроводі кролиці протягом 5 ти діб. Розроблений метод тривалого зберігання ембріонів овець у середовищах, які у своєму складі мають кріопротектор — гліцерин.
 ТЕ свиней добре відпрацьована, але на практиці застосовується обмежено, що зумовлено їхньою багатоплідністю. l Протягом статевої охоти у свиней відбувається численна овуляція в середньому 20 фолікулів. З метою викликання овуляції більшої кількості фолікулів, донорів обробляють на 15 -16 -й день СЦ СЖК. Внаслідок цього овулює в середньому на 10 фолікулів більше. l
ТЕ свиней добре відпрацьована, але на практиці застосовується обмежено, що зумовлено їхньою багатоплідністю. l Протягом статевої охоти у свиней відбувається численна овуляція в середньому 20 фолікулів. З метою викликання овуляції більшої кількості фолікулів, донорів обробляють на 15 -16 -й день СЦ СЖК. Внаслідок цього овулює в середньому на 10 фолікулів більше. l
 l Вимивання і пересадка ембріонів у свиней здійснюється хірургічним методом. У донорів і реципієнтів майже не реєструється ускладнень після хірургічного втручання. l Для зберігання ембріонів протягом 24 -х годин використовують середовище Брінстера, 199, Хемса і Дюльбекко. В яйцепроводі кролиці або вівці вони можуть зберігатися протягом двох діб.
l Вимивання і пересадка ембріонів у свиней здійснюється хірургічним методом. У донорів і реципієнтів майже не реєструється ускладнень після хірургічного втручання. l Для зберігання ембріонів протягом 24 -х годин використовують середовище Брінстера, 199, Хемса і Дюльбекко. В яйцепроводі кролиці або вівці вони можуть зберігатися протягом двох діб.
 l. Ембріони (6 -8 -денні бластоцисти) пересаджують лише в один ріг, внаслідок міграції вони розподіляються в обох рогах матки. l. Супоросність може не настати, якщо пересаджено менше, ніж чотири ембріони.
l. Ембріони (6 -8 -денні бластоцисти) пересаджують лише в один ріг, внаслідок міграції вони розподіляються в обох рогах матки. l. Супоросність може не настати, якщо пересаджено менше, ніж чотири ембріони.
 ТЕ кролів l проводять хірургічним способом. l Синхронізації досягають шляхом одночасно осіменінням донора і провокуючим овуляцію коїтусом реципієнтів з вазектомованим кролем.
ТЕ кролів l проводять хірургічним способом. l Синхронізації досягають шляхом одночасно осіменінням донора і провокуючим овуляцію коїтусом реципієнтів з вазектомованим кролем.
 l Вимивання ембріонів проводять через 3 дні після осіменіння. Тварину фіксують на спині у станку. Лапаротомію проводять за білою лінією черевної стінки. Перед цим готують операційне поле: видаляють шерстний покрив, мильним розчином миють черевну стінку і обробляють 70°-ним спиртом. Після цього роблять розріз довжиною 5 -7 см, знаходять матку, підраховують кількість ЖТ в яєчниках і вимивають з матки ембріони.
l Вимивання ембріонів проводять через 3 дні після осіменіння. Тварину фіксують на спині у станку. Лапаротомію проводять за білою лінією черевної стінки. Перед цим готують операційне поле: видаляють шерстний покрив, мильним розчином миють черевну стінку і обробляють 70°-ним спиртом. Після цього роблять розріз довжиною 5 -7 см, знаходять матку, підраховують кількість ЖТ в яєчниках і вимивають з матки ембріони.
 Після вимивання ембріонів матку донора промивають розчином антибіотика і закривають розріз швами, а рану обробляють 70°-ним спиртом. Для попередження післяопераційних ускладнень внутрішньочеревно вводять розчин антибіотика. l Одночасно проводять лапаротомію у реципієнта і оцінюють ембріони. Знайдені і оцінені ембріони в 1 -1, 5 мл промивальної рідини, вводять у верхівку рогів матки, після чого черевну порожнину зашивають. l
Після вимивання ембріонів матку донора промивають розчином антибіотика і закривають розріз швами, а рану обробляють 70°-ним спиртом. Для попередження післяопераційних ускладнень внутрішньочеревно вводять розчин антибіотика. l Одночасно проводять лапаротомію у реципієнта і оцінюють ембріони. Знайдені і оцінені ембріони в 1 -1, 5 мл промивальної рідини, вводять у верхівку рогів матки, після чого черевну порожнину зашивають. l
 l Після трансплантації вагітність визначають через 5 -6 днів рефлексологічним методом, ефективність якого складає 76 %. Методом ультрасонографії вагітність встановлюють на 7 -8 -й день, враховуючи наявність ембріональних міхурів. Точність метода складає майже 100 %. У більш пізні строки застосовують пальпацію плодів через черевну стінку. l Після окролу за кількістю новонароджених визначають ефективність трансплантації.
l Після трансплантації вагітність визначають через 5 -6 днів рефлексологічним методом, ефективність якого складає 76 %. Методом ультрасонографії вагітність встановлюють на 7 -8 -й день, враховуючи наявність ембріональних міхурів. Точність метода складає майже 100 %. У більш пізні строки застосовують пальпацію плодів через черевну стінку. l Після окролу за кількістю новонароджених визначають ефективність трансплантації.
 Вимоги до обліку та звітності 1. При поступанні на пункт трансплантації на кожного донора і реципієнта заводиться картка племінного обліку встановленої форми. 2. Характеристика відтворювальної здатності тварини та ін. показники, перераховані у вимогах при відборі корів-донорів, а також причина вибракування (при використанні вибракуваних з основного стада тварин), вказуються в племінній картці. 3. На використовуваних бугаїв-плідників також заводиться картка плем. обліку або племсвідоцтво. У правому верхньому куті картки племінного обліку відзначають тип крові тварини для генетичного контролю походження потомства. 4. На кожного отриманого методом ТЕ теляти, в день його народження складають всі необхідні документи: а) акт на оприбуткування приплоду (форма № 95 Сільгоспоблік); б) журнал приплоду та вирощування молодняку великої рогатої худоби (. 5. Генетичний контроль походження телят-трансплантантів проводять у віці 11, 5 міс. на підставі експертизи груп крові батьків і потомства. На кожного бичка чи теличку заповнюють відповідні картки племінного обліку. 6. На пунктах ТЕ ведуться спеціальні журнали для реєстрації і безпосереднього обліку робіт фахівців. 7. За підсумками робіт за рік складається звіт.
Вимоги до обліку та звітності 1. При поступанні на пункт трансплантації на кожного донора і реципієнта заводиться картка племінного обліку встановленої форми. 2. Характеристика відтворювальної здатності тварини та ін. показники, перераховані у вимогах при відборі корів-донорів, а також причина вибракування (при використанні вибракуваних з основного стада тварин), вказуються в племінній картці. 3. На використовуваних бугаїв-плідників також заводиться картка плем. обліку або племсвідоцтво. У правому верхньому куті картки племінного обліку відзначають тип крові тварини для генетичного контролю походження потомства. 4. На кожного отриманого методом ТЕ теляти, в день його народження складають всі необхідні документи: а) акт на оприбуткування приплоду (форма № 95 Сільгоспоблік); б) журнал приплоду та вирощування молодняку великої рогатої худоби (. 5. Генетичний контроль походження телят-трансплантантів проводять у віці 11, 5 міс. на підставі експертизи груп крові батьків і потомства. На кожного бичка чи теличку заповнюють відповідні картки племінного обліку. 6. На пунктах ТЕ ведуться спеціальні журнали для реєстрації і безпосереднього обліку робіт фахівців. 7. За підсумками робіт за рік складається звіт.
 РЕКОМЕНДОВАНА ЛІТЕРАТУРА • Валюшкин К. Д. Акушерство, гинекология и биотехника размножения животных / К. Д. Валюшкин, Г. Ф. Медведев. – 2 -е изд. , перераб. и доп. – Минск: Ураджай, 2001. – 869 с. • Ветеринарне акушерство, гінекологія та біотехнологія відтворення тварин з основами андрології: підруч. / за ред. В. А. Яблонського та С. П. Хомина. – Вінниця: Нова Книга, 2006. – 592 с. • Ветеринарное акушерство, гинекология и биотехника размножения / [А. П. Студенцов, В. С. Шипилов, В. Я. Никитин и др. ]; под ред. В. Я. Никитина и М. Г. Миролюбова. – 7 -е изд. , перераб. и доп. – М. : Колос, 1999. – 495 с.
РЕКОМЕНДОВАНА ЛІТЕРАТУРА • Валюшкин К. Д. Акушерство, гинекология и биотехника размножения животных / К. Д. Валюшкин, Г. Ф. Медведев. – 2 -е изд. , перераб. и доп. – Минск: Ураджай, 2001. – 869 с. • Ветеринарне акушерство, гінекологія та біотехнологія відтворення тварин з основами андрології: підруч. / за ред. В. А. Яблонського та С. П. Хомина. – Вінниця: Нова Книга, 2006. – 592 с. • Ветеринарное акушерство, гинекология и биотехника размножения / [А. П. Студенцов, В. С. Шипилов, В. Я. Никитин и др. ]; под ред. В. Я. Никитина и М. Г. Миролюбова. – 7 -е изд. , перераб. и доп. – М. : Колос, 1999. – 495 с.
 РЕКОМЕНДОВАНА ЛІТЕРАТУРА • Гончаров В. П. Акушерство, гинекология и биотехника размножения животных / В. П. Гончаров, Д. А. Черепахин. – М. : Колос С, 2004. – 328 с. • Полянцев Н. И. Ветеринарное акушерство и биотехника репродукции животных: учеб. пос. / Н. И. Полянцев, В. В. Подберезный. – Ростов н/Д: Феникс, 2001. – 480 с. • Козел А. А. Курс лекций по дисциплине: “Биотехнология репродукции сельскохозяйственных животных и птицы” / А. А. Козел. – Гродно, 2013. – 99 с. • Краткое руководство по репродукции животных: крупный рогатый скот. – Ч. 1 и 2. – MSD Animal Health, 2009. – 10 -е изд. , исправл. и доп. – 176 с.
РЕКОМЕНДОВАНА ЛІТЕРАТУРА • Гончаров В. П. Акушерство, гинекология и биотехника размножения животных / В. П. Гончаров, Д. А. Черепахин. – М. : Колос С, 2004. – 328 с. • Полянцев Н. И. Ветеринарное акушерство и биотехника репродукции животных: учеб. пос. / Н. И. Полянцев, В. В. Подберезный. – Ростов н/Д: Феникс, 2001. – 480 с. • Козел А. А. Курс лекций по дисциплине: “Биотехнология репродукции сельскохозяйственных животных и птицы” / А. А. Козел. – Гродно, 2013. – 99 с. • Краткое руководство по репродукции животных: крупный рогатый скот. – Ч. 1 и 2. – MSD Animal Health, 2009. – 10 -е изд. , исправл. и доп. – 176 с.
 РЕКОМЕНДОВАНА ЛІТЕРАТУРА • Мадисон В. В. Трансплантация эмбрионов в практике разведения молочного скотоводства / В. В. Мадисон, В. Л. Мадисон. – М. : Агропромиздат, 1988. – 128 с. • Осташко Ф. И. Биотехнология воспроизводства крупного рогатого скота / Осташко Ф. И. – К. : Аграрна наука, 1995. – 183 с. • Эрнст Л. К. Трансплантация эмбрионов сельскохозяйственных животных / Л. К. Эрнст, Н. И. Сергеев. – М. : Агропромиздат, 1989. – 302 с. • Яблонський В. А. Біотехнологія відтворення тварин / Яблонський В. А. – К. : Аристей, 2004. – 296 с.
РЕКОМЕНДОВАНА ЛІТЕРАТУРА • Мадисон В. В. Трансплантация эмбрионов в практике разведения молочного скотоводства / В. В. Мадисон, В. Л. Мадисон. – М. : Агропромиздат, 1988. – 128 с. • Осташко Ф. И. Биотехнология воспроизводства крупного рогатого скота / Осташко Ф. И. – К. : Аграрна наука, 1995. – 183 с. • Эрнст Л. К. Трансплантация эмбрионов сельскохозяйственных животных / Л. К. Эрнст, Н. И. Сергеев. – М. : Агропромиздат, 1989. – 302 с. • Яблонський В. А. Біотехнологія відтворення тварин / Яблонський В. А. – К. : Аристей, 2004. – 296 с.
 Дякую за увагу! Лекцію закінчено!!!
Дякую за увагу! Лекцію закінчено!!!


