белки 10 класс.ppt
- Количество слайдов: 17
Для понимания и объяснения процессов, происходящих в клетке, выявить особенности строения, свойства и функции белков. На основании полученных знаний уметь проводить взаимосвязь между функциями и строением ЦЕЛЬ.

• 1838 г Жерар Мюльдер – открыл существование белковых тел и сформулировал теорию протеина • 1888 г. Данилевский и Херт предложили строение белковой молекулы, но они считали, что "мономеры" представляют собой очень сложные образования пептоны или "углеазотные комплексы". • 1903 г Фишер открыл пептидную связь и сформулировал пептидную теорию 30% Б – мыщцы 20% - в костях и сухожилиях 10% в коже 100. 000 белков в организме человека

Элементарный химический состав белков Белки, или протеины (от греч. протос – основной, первичный) занимают первое место по количеству и значению в клетке Белки составляют 10– 18%, т. е. половину сухого веса клетки. В состав белков входят атомы С, Н, О, N, S, Р, иногда Fe, Сu, Zn. Формула гемоглобина – C 3032 Н 4816 О 872 S 8 Fe 4 Белки – это высокомолекулярные полимеры (макромолекулы) По своей химической природе белки являются непериодическими полимерами. Мономерами являются аминокислоты
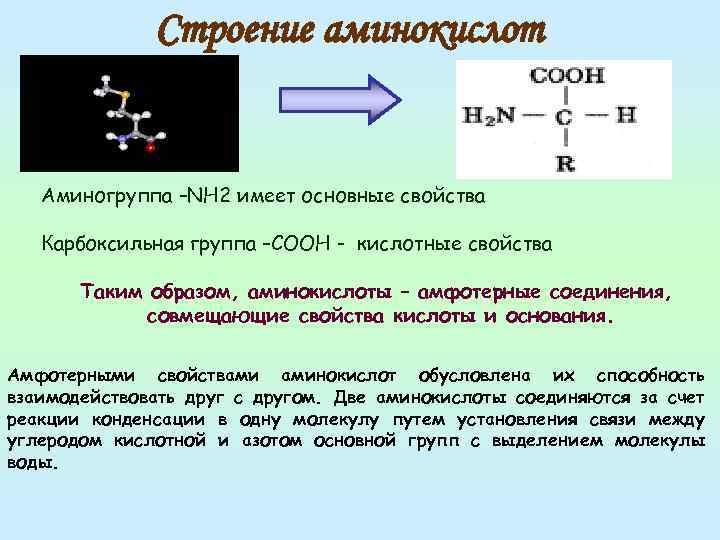
Строение аминокислот Аминогруппа –NH 2 имеет основные свойства Карбоксильная группа –СООН - кислотные свойства Таким образом, аминокислоты – амфотерные соединения, совмещающие свойства кислоты и основания. Амфотерными свойствами аминокислот обусловлена их способность взаимодействовать друг с другом. Две аминокислоты соединяются за счет реакции конденсации в одну молекулу путем установления связи между углеродом кислотной и азотом основной групп с выделением молекулы воды.
Аминокислот очень много (170) НО : белки образуют только 20 так называемых золотых или стандартных, аминокислот 8 незаменимыми 12 заменимых т. к. не синтезируются в организмах животных и человека • Лизин • Лейцин • Изолейцин Именно сочетание • Фенилаланин этих 20 аминокислот • Метианин • Валин и дает все многообразие • Трианин белков • триптофан Свойства А. К. 1. Бесцветные кристал в –ва 2. Растворяются в воде 3. Сладковатый вкус АМИНОКИСЛОТЫ Неполноценные
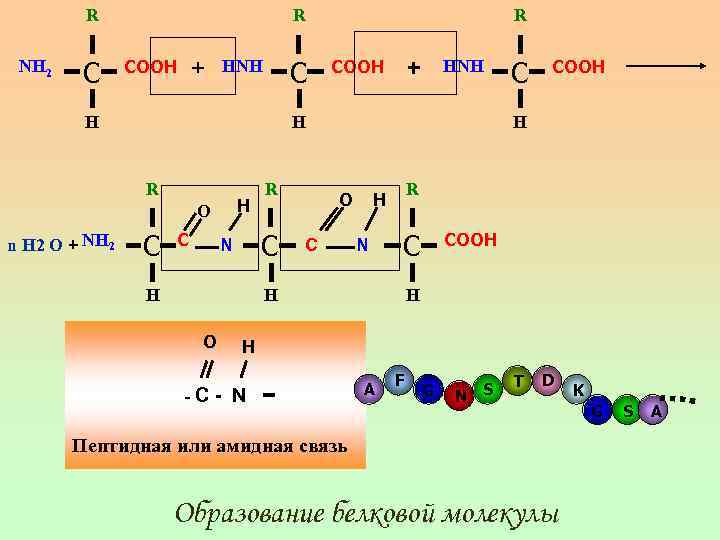
R NH 2 C R + COOH C HNH H + COOH HNH H R H O n H 2 O + NH 2 R C C R C N H COOH H O C R H N C H O C COOH H H -C- N A F G N S T D Пептидная или амидная связь Образование белковой молекулы K G S A
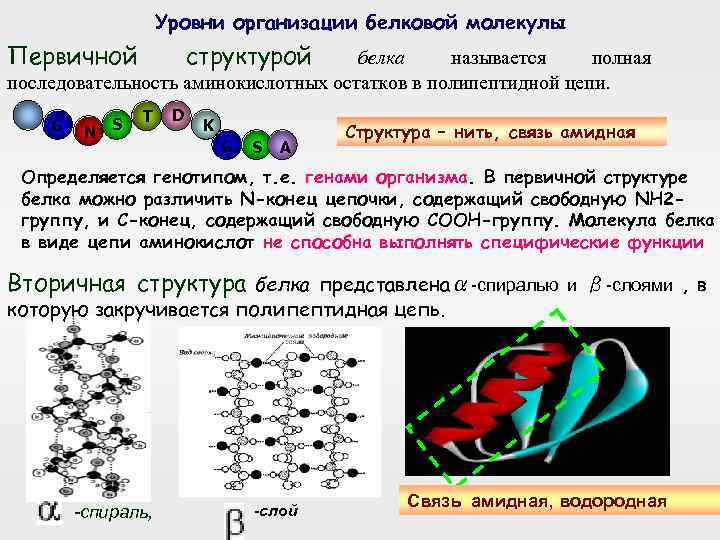
Уровни организации белковой молекулы Первичной структурой белка называется полная последовательность аминокислотных остатков в полипептидной цепи. G N S T D K G S A Структура – нить, связь амидная Определяется генотипом, т. е. генами организма. В первичной структуре белка можно различить N-конец цепочки, содержащий свободную NH 2 группу, и С-конец, содержащий свободную СООН-группу. Молекула белка в виде цепи аминокислот не способна выполнять специфические функции Вторичная структура белка представленаα-спиралью которую закручивается полипептидная цепь. -спираль, -слой и β-слоями , в Связь амидная, водородная

Структура – глобула Третичная структура белка представляет собой сложную трехмерную пространственную упаковку α-спиралей иβ -слоев. Эта трехмерная структура устанавливается за счет взаимодействия радикалов аминокислот, между которыми могут возникнуть связи несколько типов ионные, гидрофобные, дисульфидные : Четвертичная структура представлена структурой, состоящей из нескольких полипептидных цепей Агрегат из нескольких глобул. Свойственна лишь белкам с особо сложной структурой В основном силы межмолек притяж, в меньшей степени – водородные, ионные и ковалентные Пространственная конфигурация белка т. е. третичная и четвертичная структуры называется конформацией. Конформация белка определяется его первичной структурой
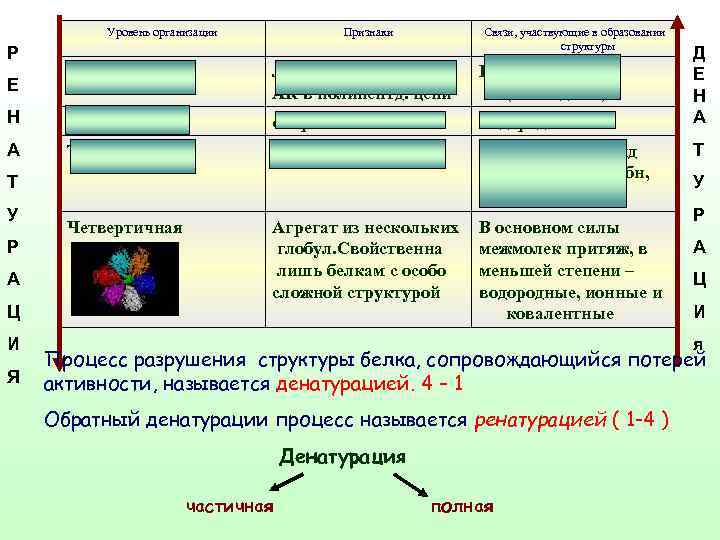
Уровень организации Р Признаки Связи, участвующие в образовании структуры Первичная Линейная последоват АК в полипептд. цепи Ковалентные (пептидные) Н Вторичная спираль Водородные А Третичная Глобула, Ионные, дисульфид мостики, гидрофобн, водородные Е Т У Р А Четвертичная Агрегат из нескольких глобул. Свойственна лишь белкам с особо сложной структурой Ц И Я В основном силы межмолек притяж, в меньшей степени – водородные, ионные и ковалентные Д Е Н А Т У Р А Ц И я Процесс разрушения структуры белка, сопровождающийся потерей активности, называется денатурацией. 4 – 1 Обратный денатурации процесс называется ренатурацией ( 1 -4 ) Денатурация частичная полная

Классификация белков по составу Простые белки (протеины) состоят только из аминокислот • Альбумины • Глобулины • Гистоны • склеропротеины Сложные белки (протеиды) состоят из глобулярных белков и небелкового материала. Небелковую часть называют простетической группой • фосфопротеиды • гликопротеиды • нуклеопротеиды • хромопротеиды • липопротеиды • металлопротеиды

Классификация белков по их структуре Фибриллярные – образуют длинные волокна или слоистые структуры (коллаген, миозин, фиброин, кератин). Они нерастворимы в воде. Глобулярные – их полипептидные цепи свернуты в компактные глобулы (ферменты, антитела, гормон инсулин). Промежуточные – фибриллярной природы, но растворяются в воде (фибриноген).

Классификация белков по функциям. Структурные – входят в различные структуры клетки и организма. Ферменты – являются биологическими катализаторами. Гормоны – являются регуляторами биологических функций. Транспортные – переносят различные вещества. Защитные – обеспечивают иммунные реакции организма. Сократительные – участвуют в сокращении мышечных волокон. Запасные – служат резервными веществами клетки и организма. Токсины – являются ядами, используемыми живыми существами в целях защиты

Свойства белков 1. Есть белки растворимые (например, фибриноген) и нерастворимые (например, фибрин) в воде. 2. Есть белки очень устойчивые (например, кератин) и неустойчивые (например, фермент каталаза с легко изменяющейся структурой). 3. У белков встречается разнообразная форма молекул – от нитей (миозин – белок мышечных волокон) до шариков (гемоглобин) и т. д. 4 Ренатурация и денатурация. 5. Высокий поверхностный заряд 6. Все белки строго специфичны ! СПЕЦИФИЧНОСТЬ ЗАВИСИТ ОТ: * от количества аминокислот * от их расположения * от конфигурации белковой молекулы

ФУНКЦИИ БЕЛКОВ 1. Структурная (строительная). Белки входят в состав всех клеточных мембран и органоидов клетки, а также внеклеточных структур. 2. Например; кератин. Из этого белка состоят волосы, шерсть, рога, копыта, верхний отмерший слой кожи. В более глубоких слоях кожи расположены прокладки из белков коллагена и эластина. Именно эти белки обеспечивают прочность и упругость кожи. Они же содержатся в связках, соединяющих мышцы с суставами и суставы между собой. 2. Ферментативная. Белки являются биологическими катализаторами. Например, пепсин, трипсин и др. 3. Двигательная. Особые сократительные белки участвуют во всех видах движения клетки и организма: образовании псевдоподий, мерцании ресничек и биении жгутиков у простейших, сокращении мышц у многоклеточных животных, движении листьев у растений и др. Так, сокращение мышц обеспечивают мышечные белки актин и миозин. Функции Особенност и Примеры

4. Транспортная. В крови, в наружных клеточных мембранах, в цитоплазме и ядрах клеток есть различные транспортные белки. В крови имеются белки-транспортеры, которые узнают и связывают определенные гормоны и несут их к клеткам-мишеням. Известны белки, например гемоглобин и гемоцианин, переносящие кислород, и миоглобин, удерживающий кислород в мышцах. 5. Защитная. В ответ на проникновение в организм чужеродных белков или микроорганизмов, обладающих антигенными свойствами, лимфоциты крови образуют особые белки – антитела, способные связывать и обезвреживать их. В слюне и слезах содержится белок лизоцим – фермент, разрушающий клеточные стенки бактерий. Фибрин и тромбин способствуют остановке кровотечений. 6. Энергетическая (питательная). Белки можно расщепить, окислить и получить энергию, необходимую для жизни. Правда, это не очень выгодно: энергетическая ценность белков по сравнению с жирами невысока и составляет 17, 6 к. Дж (4, 1 ккал) энергии на 1 г белка. Обычно белки расходуются на энергетические нужды в крайних случаях, когда исчерпаны запасы жиров и углеводов.

7. Регуляторная. Многие (хотя далеко не все) гормоны являются белками – например все гормоны гипофиза, гипоталамуса, поджелудочной железы (инсулин, глюкагон) и др. Гормоны действуют на клетку, связываясь со специфическими рецепторами. Каждый рецептор узнает только один гормон. 8. Сигнальная (рецепторная). В поверхностную мембрану клетки встроены молекулы белков, способных изменять свою третичную структуру в ответ на действие факторов внешней среды. Так происходит прием сигналов из внешней среды и передача команд в клетку. 9. Запасающая. Благодаря белкам в организме могут откладываться в запас некоторые вещества. Яичный альбумин служит водозапасающим белком в яичном «белке» , казеин молока является источником энергии, а белок ферритин удерживает железо в яичном желтке, селезенке и печени. 10. Токсическая. Некоторые белки являются токсинами: яд кобры содержит нейротоксин ! Белки многофункциональны, так как специфичны.

ДОМАШНЕЕ ЗАДАНИЕ • записи в тетради учить • Приготовить устный ответ • заполнить таблицу «Функции белков» • Подготовиться к тесту. Заполните пропуски в тексте: «В результате взаимодействия различных. . . и образования. . . связей спирализованная молекула белка образует. . . структуру, которая, в свою очередь, зависит от. . . структуры белка, то есть от. . . аминокислот в молекуле полипептида. Субъединицы некоторых белков образуют. . . структуру. Примером такого белка является. . . » . УСПЕХОВ !
белки 10 класс.ppt