Дисперсные системы.Коллоиды.ppt
- Количество слайдов: 31
 Дисперсные системы Коллоидные растворы
Дисперсные системы Коллоидные растворы
 • Дисперсными системами называются вещества, раздробленные до частиц большей или меньшей величины и распределенные в другом веществе. • Измельченное (раздробленное) вещество называют дисперсной фазой. • Вещество, в котором распределена дисперсная фаза, называют дисперсионной средой.
• Дисперсными системами называются вещества, раздробленные до частиц большей или меньшей величины и распределенные в другом веществе. • Измельченное (раздробленное) вещество называют дисперсной фазой. • Вещество, в котором распределена дисперсная фаза, называют дисперсионной средой.
 Характеристики дисперсных систем • степень дисперсности: где а – линейный размер частицы • удельная поверхность: где Sуд – удельная поверхность, S – общая поверхность частиц, V – объем вещества дисперсной фазы.
Характеристики дисперсных систем • степень дисперсности: где а – линейный размер частицы • удельная поверхность: где Sуд – удельная поверхность, S – общая поверхность частиц, V – объем вещества дисперсной фазы.
 Степень дисперсности и удельная поверхность взаимосвязаны: Длина грани, мм Число кубиков Удельная поверхность, см 2 1 1 6 10– 1 103 60 10– 3 109 6· 103 10– 5 1015 6· 105 (60 м 2) 10– 7 1021 6· 107 (6000 м 2)
Степень дисперсности и удельная поверхность взаимосвязаны: Длина грани, мм Число кубиков Удельная поверхность, см 2 1 1 6 10– 1 103 60 10– 3 109 6· 103 10– 5 1015 6· 105 (60 м 2) 10– 7 1021 6· 107 (6000 м 2)
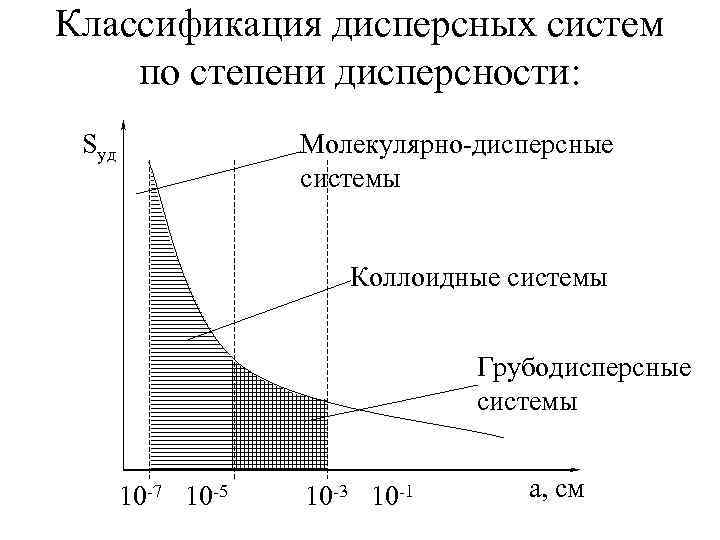 Классификация дисперсных систем по степени дисперсности: Sуд Молекулярно-дисперсные системы Коллоидные системы Грубодисперсные системы 10 -7 10 -5 10 -3 10 -1 а, см
Классификация дисперсных систем по степени дисперсности: Sуд Молекулярно-дисперсные системы Коллоидные системы Грубодисперсные системы 10 -7 10 -5 10 -3 10 -1 а, см
 Примеры коллоидных систем: Грубодисперсных систем: • Пены: суспензии, эмульсии, пены (мыльная пена, муссы). • Суспензии: известковое молоко (Ca(OH)2) взвесь в воде), напитки кофе и какао. • Эмульсии: молоко, маргарин, майонез.
Примеры коллоидных систем: Грубодисперсных систем: • Пены: суспензии, эмульсии, пены (мыльная пена, муссы). • Суспензии: известковое молоко (Ca(OH)2) взвесь в воде), напитки кофе и какао. • Эмульсии: молоко, маргарин, майонез.
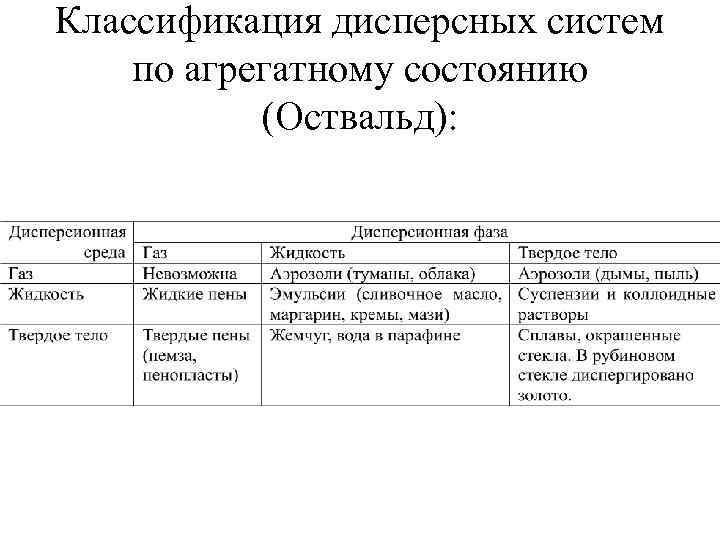 Классификация дисперсных систем по агрегатному состоянию (Оствальд):
Классификация дисперсных систем по агрегатному состоянию (Оствальд):
 Физико-химические особенности коллоидных систем • Молекулы поверхностного слоя коллоидных частиц имеют часть ненасыщенных, некомпенсированных сил взаимодействия, которые представляют собой избыточную энергию. Избыточная энергия называется свободной поверхностной энергией. • Коллоидные системы неустойчивые стремятся к избавлению от избыточной энергии - к само-укрупнению – коагуляции.
Физико-химические особенности коллоидных систем • Молекулы поверхностного слоя коллоидных частиц имеют часть ненасыщенных, некомпенсированных сил взаимодействия, которые представляют собой избыточную энергию. Избыточная энергия называется свободной поверхностной энергией. • Коллоидные системы неустойчивые стремятся к избавлению от избыточной энергии - к само-укрупнению – коагуляции.
 Получение, строение и коагуляция коллоидных частиц. Получение: 1 – дробление более крупных частиц до коллоидной степени дисперсности (методы диспергирования). 2 – укрупнение частиц в результате объединения атомов или молекул в агрегаты коллоидной степени дисперсности (методы конденсации).
Получение, строение и коагуляция коллоидных частиц. Получение: 1 – дробление более крупных частиц до коллоидной степени дисперсности (методы диспергирования). 2 – укрупнение частиц в результате объединения атомов или молекул в агрегаты коллоидной степени дисперсности (методы конденсации).
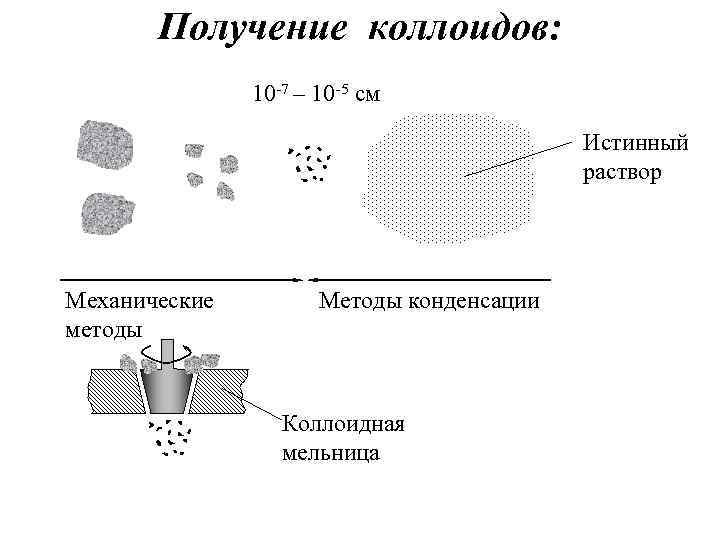 Получение коллоидов: 10 -7 – 10 -5 см Истинный раствор Механические методы Методы конденсации Коллоидная мельница
Получение коллоидов: 10 -7 – 10 -5 см Истинный раствор Механические методы Методы конденсации Коллоидная мельница
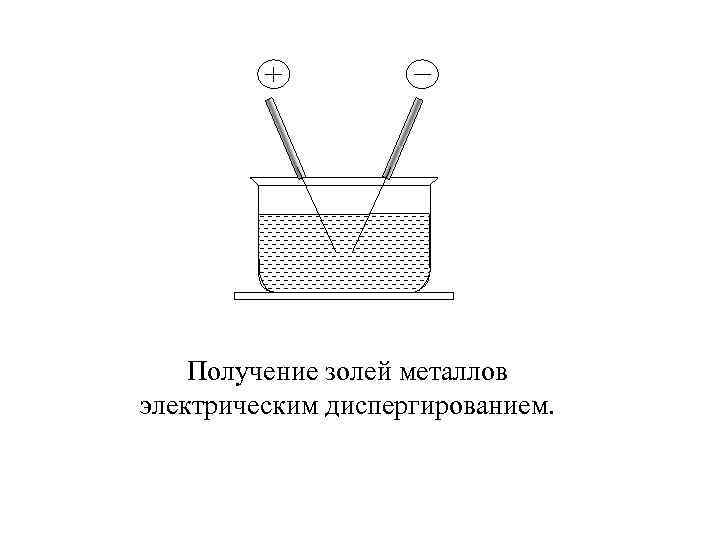 Получение золей металлов электрическим диспергированием.
Получение золей металлов электрическим диспергированием.
 Химические методы конденсации основаны на принципе создания концентраций превышающих равновесные:
Химические методы конденсации основаны на принципе создания концентраций превышающих равновесные:
![Строение коллоидной частицы m[Ag. I]. В случаи избытка в растворе KJ: {m[Ag. I] n. Строение коллоидной частицы m[Ag. I]. В случаи избытка в растворе KJ: {m[Ag. I] n.](https://present5.com/presentation/3/31647411_132731086.pdf-img/31647411_132731086.pdf-13.jpg) Строение коллоидной частицы m[Ag. I]. В случаи избытка в растворе KJ: {m[Ag. I] n. I–(n–x)K+}x– x. K+ агрегат ядро m[Ag. I] гранула мицелла
Строение коллоидной частицы m[Ag. I]. В случаи избытка в растворе KJ: {m[Ag. I] n. I–(n–x)K+}x– x. K+ агрегат ядро m[Ag. I] гранула мицелла
![Строение коллоидной частицы m[Ag. I]. В случаи избытка в растворе Ag. NO 3 : Строение коллоидной частицы m[Ag. I]. В случаи избытка в растворе Ag. NO 3 :](https://present5.com/presentation/3/31647411_132731086.pdf-img/31647411_132731086.pdf-14.jpg) Строение коллоидной частицы m[Ag. I]. В случаи избытка в растворе Ag. NO 3 : Диффузионный слой Адсорбционный слой m[Ag. I] Гранула Ядро Агрегат Двойной электрический слой
Строение коллоидной частицы m[Ag. I]. В случаи избытка в растворе Ag. NO 3 : Диффузионный слой Адсорбционный слой m[Ag. I] Гранула Ядро Агрегат Двойной электрический слой
![Одноимённый заряд препятствует слипанию, укрупнению коллоидных частиц, тем самым обуславливает устойчивость частиц: m[Ag. I] Одноимённый заряд препятствует слипанию, укрупнению коллоидных частиц, тем самым обуславливает устойчивость частиц: m[Ag. I]](https://present5.com/presentation/3/31647411_132731086.pdf-img/31647411_132731086.pdf-15.jpg) Одноимённый заряд препятствует слипанию, укрупнению коллоидных частиц, тем самым обуславливает устойчивость частиц: m[Ag. I]
Одноимённый заряд препятствует слипанию, укрупнению коллоидных частиц, тем самым обуславливает устойчивость частиц: m[Ag. I]
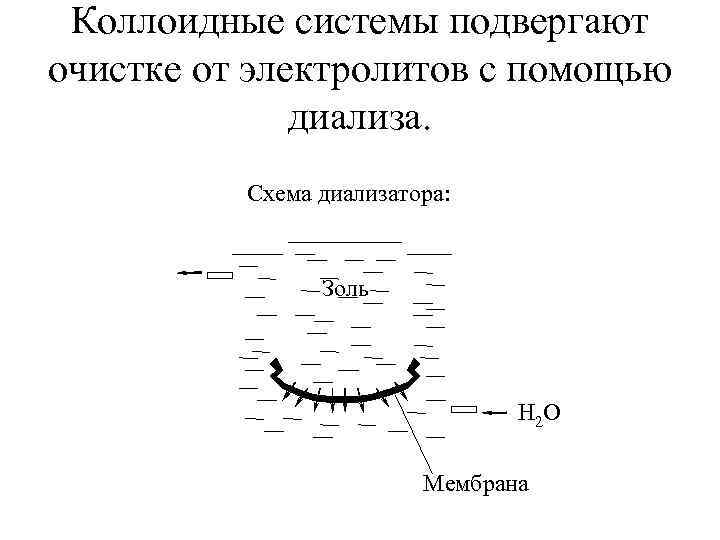 Коллоидные системы подвергают очистке от электролитов с помощью диализа. Схема диализатора: Золь H 2 O Мембрана
Коллоидные системы подвергают очистке от электролитов с помощью диализа. Схема диализатора: Золь H 2 O Мембрана
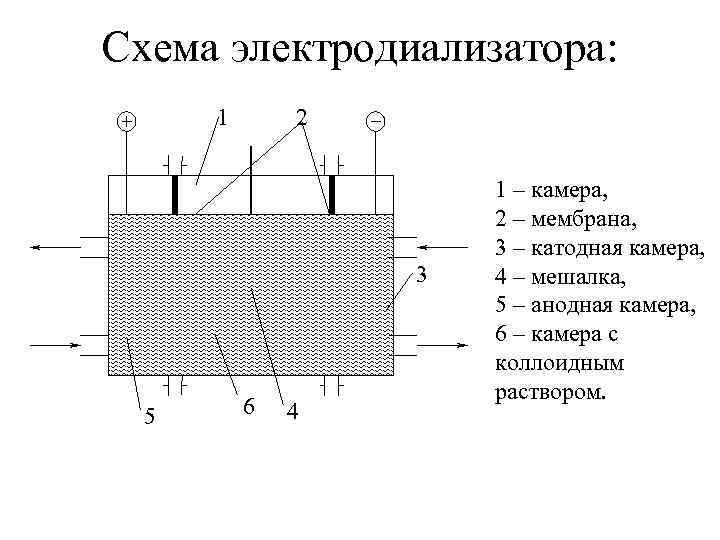 Схема электродиализатора: 1 2 3 5 6 4 1 – камера, 2 – мембрана, 3 – катодная камера, 4 – мешалка, 5 – анодная камера, 6 – камера с коллоидным раствором.
Схема электродиализатора: 1 2 3 5 6 4 1 – камера, 2 – мембрана, 3 – катодная камера, 4 – мешалка, 5 – анодная камера, 6 – камера с коллоидным раствором.
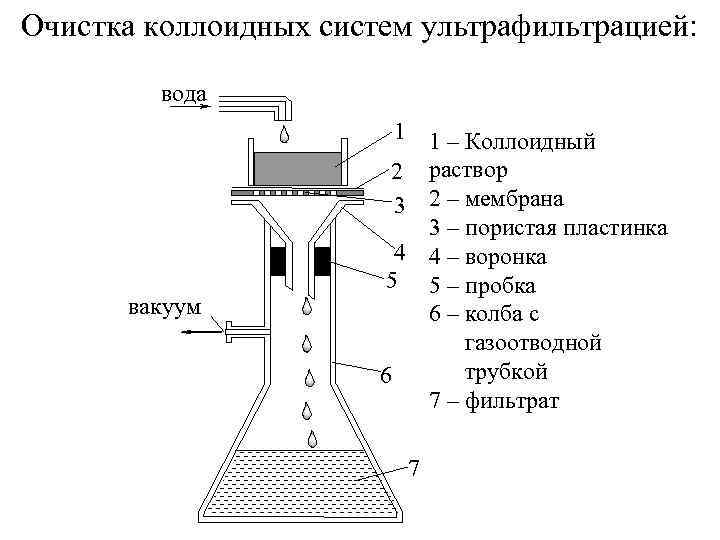 Очистка коллоидных систем ультрафильтрацией: вода вакуум 1 1 – Коллоидный 2 раствор 3 2 – мембрана 3 – пористая пластинка 4 4 – воронка 5 5 – пробка 6 – колба с газоотводной трубкой 6 7 – фильтрат 7
Очистка коллоидных систем ультрафильтрацией: вода вакуум 1 1 – Коллоидный 2 раствор 3 2 – мембрана 3 – пористая пластинка 4 4 – воронка 5 5 – пробка 6 – колба с газоотводной трубкой 6 7 – фильтрат 7
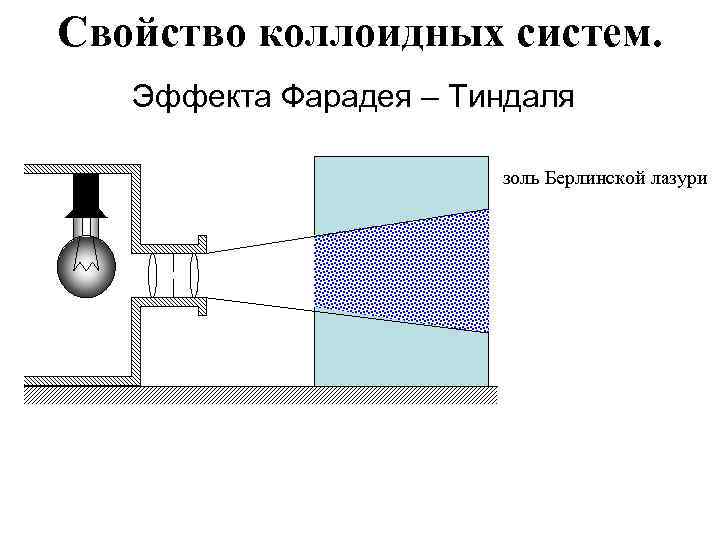 Свойство коллоидных систем. Эффекта Фарадея – Тиндаля золь Берлинской лазури
Свойство коллоидных систем. Эффекта Фарадея – Тиндаля золь Берлинской лазури
 Для коллоидных растворов, как и для истинных растворов работают законы Рауля и Вант-Гоффа. • осмотическое давление 1% раствора сахара достигает 509 мм. рт. ст. • осмотическое давление 1% золя сульфида мышьяка – 0, 026 мм. рт. ст.
Для коллоидных растворов, как и для истинных растворов работают законы Рауля и Вант-Гоффа. • осмотическое давление 1% раствора сахара достигает 509 мм. рт. ст. • осмотическое давление 1% золя сульфида мышьяка – 0, 026 мм. рт. ст.
 Электро-кинетические явления. • явления электрофореза и электроосмоса впервые были обнаружены в 1808 году профессором Московского университета Ф. Ф. Рейсом. 1 – вода; 2 – песок; 3 – суспензия глины; Осмос 4 – кусок глины; 5 – перенос частиц глины (электрофоре 6 – перенос воды (электроосмос). 1 3 2 4 5 6
Электро-кинетические явления. • явления электрофореза и электроосмоса впервые были обнаружены в 1808 году профессором Московского университета Ф. Ф. Рейсом. 1 – вода; 2 – песок; 3 – суспензия глины; Осмос 4 – кусок глины; 5 – перенос частиц глины (электрофоре 6 – перенос воды (электроосмос). 1 3 2 4 5 6
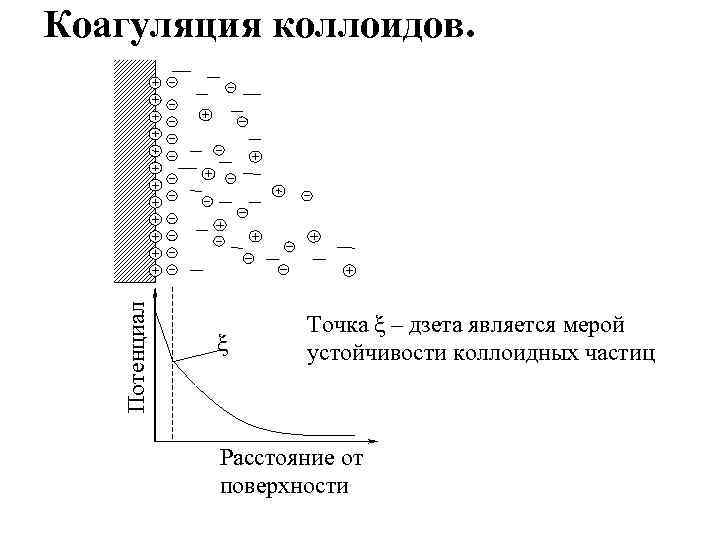 Потенциал Коагуляция коллоидов. ξ Точка ξ – дзета является мерой устойчивости коллоидных частиц Расстояние от поверхности
Потенциал Коагуляция коллоидов. ξ Точка ξ – дзета является мерой устойчивости коллоидных частиц Расстояние от поверхности
 Коагулирующим действием обладает лишь тот ион электролита, который несет заряд противоположный заряд коллоидной частицы. Такой ион называется коагулирующим.
Коагулирующим действием обладает лишь тот ион электролита, который несет заряд противоположный заряд коллоидной частицы. Такой ион называется коагулирующим.
 Правило коагуляции Шульца – Гарди • Порог коагуляции (минимальная концентрация электролита): где Z - валентность коагулирующего иона
Правило коагуляции Шульца – Гарди • Порог коагуляции (минимальная концентрация электролита): где Z - валентность коагулирующего иона
 Значение порогов коагуляции для одно-, двух - и трех-валентных ионов относятся, как:
Значение порогов коагуляции для одно-, двух - и трех-валентных ионов относятся, как:
 φ, скорость коагуляции Зависимость скорости коагуляции от концентрации коагулирующего электролита: 0 Рис. 1 Участок 0 – A коллоидная система устойчива, на участке A – B скорость коагуляции резко возрастает. A B С, моль/л
φ, скорость коагуляции Зависимость скорости коагуляции от концентрации коагулирующего электролита: 0 Рис. 1 Участок 0 – A коллоидная система устойчива, на участке A – B скорость коагуляции резко возрастает. A B С, моль/л
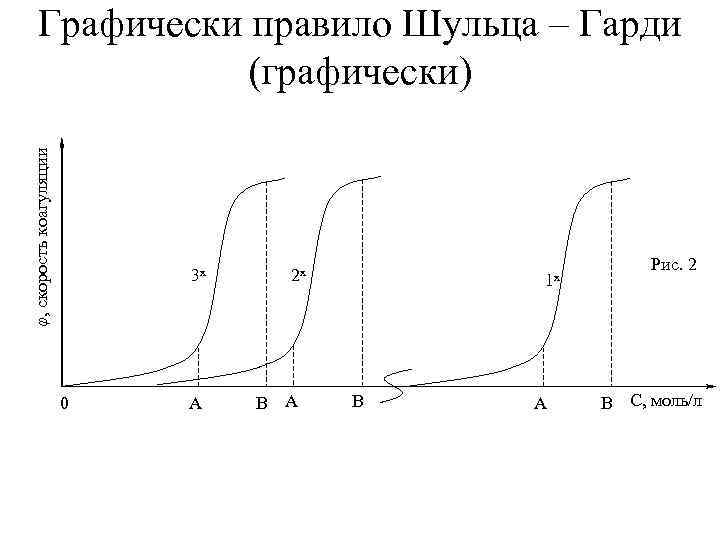 φ, скорость коагуляции Графически правило Шульца – Гарди (графически) 3 x 0 A 2 x B A 1 x B A Рис. 2 B С, моль/л
φ, скорость коагуляции Графически правило Шульца – Гарди (графически) 3 x 0 A 2 x B A 1 x B A Рис. 2 B С, моль/л
 Выводы и правила коагуляции. • Коагуляцию вызывают любые электролиты, но с заметной скоростью она происходит только при определенной концентрацией, которая называется порогом коагуляции. • Коагулирующим действием обладает лишь тот ион электролита, заряд которого противоположен заряду коллоидной частицы. При этом его коагулирующая способность выражается тем сильнее, чем выше заряд (правило Шульце – Гарди). • В ряду органических ионов коагулирующее действие возрастает с повышением адсорбционной способности. • В ряду неорганических ионов с одинаковым зарядом их коагулирующая активность возрастает с уменьшением гидратации. В ряду катионов Li+, Na+, K+, Rb+ коагулирующая активность возрастает, а степень гидратации уменьшается. В ряду Cl–, Br–, J–, CNS– коагулирующая активность возрастает, а степень гидратации уменьшается.
Выводы и правила коагуляции. • Коагуляцию вызывают любые электролиты, но с заметной скоростью она происходит только при определенной концентрацией, которая называется порогом коагуляции. • Коагулирующим действием обладает лишь тот ион электролита, заряд которого противоположен заряду коллоидной частицы. При этом его коагулирующая способность выражается тем сильнее, чем выше заряд (правило Шульце – Гарди). • В ряду органических ионов коагулирующее действие возрастает с повышением адсорбционной способности. • В ряду неорганических ионов с одинаковым зарядом их коагулирующая активность возрастает с уменьшением гидратации. В ряду катионов Li+, Na+, K+, Rb+ коагулирующая активность возрастает, а степень гидратации уменьшается. В ряду Cl–, Br–, J–, CNS– коагулирующая активность возрастает, а степень гидратации уменьшается.
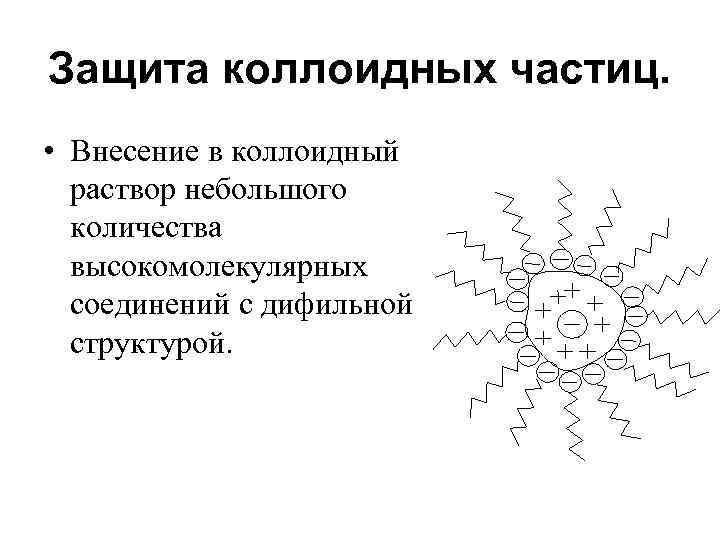 Защита коллоидных частиц. • Внесение в коллоидный раствор небольшого количества высокомолекулярных соединений с дифильной структурой.
Защита коллоидных частиц. • Внесение в коллоидный раствор небольшого количества высокомолекулярных соединений с дифильной структурой.
 Золь↔гель обратимые процессы. • Если механически перемешать студень то система переходит в подвижный золь. Через некоторое время золь станет гелем. • Желатин удерживает до 90% воды. • Золь оксида ванадия, имеющий винтовидные частицы образуют гель, содержащий до 99, 9% воды.
Золь↔гель обратимые процессы. • Если механически перемешать студень то система переходит в подвижный золь. Через некоторое время золь станет гелем. • Желатин удерживает до 90% воды. • Золь оксида ванадия, имеющий винтовидные частицы образуют гель, содержащий до 99, 9% воды.
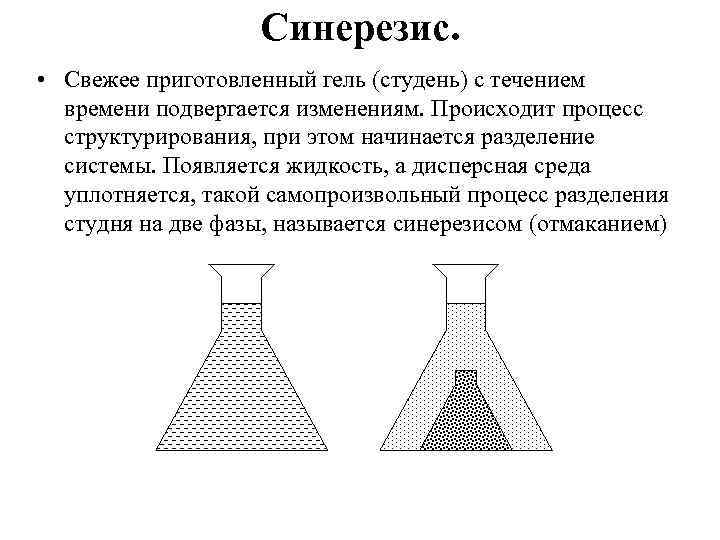 Синерезис. • Свежее приготовленный гель (студень) с течением времени подвергается изменениям. Происходит процесс структурирования, при этом начинается разделение системы. Появляется жидкость, а дисперсная среда уплотняется, такой самопроизвольный процесс разделения студня на две фазы, называется синерезисом (отмаканием)
Синерезис. • Свежее приготовленный гель (студень) с течением времени подвергается изменениям. Происходит процесс структурирования, при этом начинается разделение системы. Появляется жидкость, а дисперсная среда уплотняется, такой самопроизвольный процесс разделения студня на две фазы, называется синерезисом (отмаканием)


