Дисперсные системы и растворы.ppt
- Количество слайдов: 11
 Дисперсные системы и растворы
Дисперсные системы и растворы
 Дисперсные системы • Дисперсными называют гетерогенные системы, в которых одно вещество в виде очень мелких частиц равномерно распределено в объёме другого. • То вещество, которое присутствует в меньшем количестве и распределено в объёме другого, называют дисперсной фазой. • Вещество, присутствующее в большем количестве, в объёме которого распределена дисперсная фаза , называют дисперсионной средой.
Дисперсные системы • Дисперсными называют гетерогенные системы, в которых одно вещество в виде очень мелких частиц равномерно распределено в объёме другого. • То вещество, которое присутствует в меньшем количестве и распределено в объёме другого, называют дисперсной фазой. • Вещество, присутствующее в большем количестве, в объёме которого распределена дисперсная фаза , называют дисперсионной средой.
 Примеры дисперсных систем Дисперсионная среда Дисперсная фаза жидкость Газ Твердое вещество газ жидкость Твердое вещество Примеры Туман, аэрозоли, попутный газ с капельками нефти, капельки бензина в воздухе пыль в воздухе, дым, смог, самумы Шипучие напитки, пены Эмульсии, жидкие среды организма, жидкое содержимое клеток Золи, гели, пасты, речной и морской ил, строительные растворы Снежный наст с пузырьками воздуха, почва, текстильные ткани, кирпич, керамика, поролон, порошки. Влажная почва, медицинские и косметические средства Горные породы, цветные стекла, некоторые сплавы
Примеры дисперсных систем Дисперсионная среда Дисперсная фаза жидкость Газ Твердое вещество газ жидкость Твердое вещество Примеры Туман, аэрозоли, попутный газ с капельками нефти, капельки бензина в воздухе пыль в воздухе, дым, смог, самумы Шипучие напитки, пены Эмульсии, жидкие среды организма, жидкое содержимое клеток Золи, гели, пасты, речной и морской ил, строительные растворы Снежный наст с пузырьками воздуха, почва, текстильные ткани, кирпич, керамика, поролон, порошки. Влажная почва, медицинские и косметические средства Горные породы, цветные стекла, некоторые сплавы
 Классификация дисперсных систем и растворов Дисперсные системы Растворы эмульсии взвеси суспензии молекулярные аэрозоли Коллоидные системы гели золи Молекулярноионные Ионные
Классификация дисперсных систем и растворов Дисперсные системы Растворы эмульсии взвеси суспензии молекулярные аэрозоли Коллоидные системы гели золи Молекулярноионные Ионные
 Взвеси 1. Взвеси – это дисперсные системы, в которых размер частиц фазы более 100 нм. Это непрозрачные системы, отдельные частицы которых можно заметить невооруженным глазом. Дисперсная фаза и дисперсионная среда легко разделяется отстаиванием. Такие системы разделяют на три группы: Эмульсии (молоко, лимфа, водоэмульсионные краски) 2. Суспензии (планктон, взвешенный в воде речной и морской ил) 3. Аэрозоли (пыли, дымы, туманы, смог)
Взвеси 1. Взвеси – это дисперсные системы, в которых размер частиц фазы более 100 нм. Это непрозрачные системы, отдельные частицы которых можно заметить невооруженным глазом. Дисперсная фаза и дисперсионная среда легко разделяется отстаиванием. Такие системы разделяют на три группы: Эмульсии (молоко, лимфа, водоэмульсионные краски) 2. Суспензии (планктон, взвешенный в воде речной и морской ил) 3. Аэрозоли (пыли, дымы, туманы, смог)
 Коллоидные системы • Коллоидные системы – это такие дисперсные системы, в которых размер частиц фазы от 100 до 1 нм. Эти частицы не видны невооруженным глазом, и дисперсная фаза и дисперсионная среда в таких системах отстаиванием разделяются с трудом. • Их подразделяют на золи(коллоидные растворы) и гели (студни). • Коллоидные растворы могут быть получены в результате химических реакций. Золь образуется при гидролизе хлорида железа в горячей воде.
Коллоидные системы • Коллоидные системы – это такие дисперсные системы, в которых размер частиц фазы от 100 до 1 нм. Эти частицы не видны невооруженным глазом, и дисперсная фаза и дисперсионная среда в таких системах отстаиванием разделяются с трудом. • Их подразделяют на золи(коллоидные растворы) и гели (студни). • Коллоидные растворы могут быть получены в результате химических реакций. Золь образуется при гидролизе хлорида железа в горячей воде.
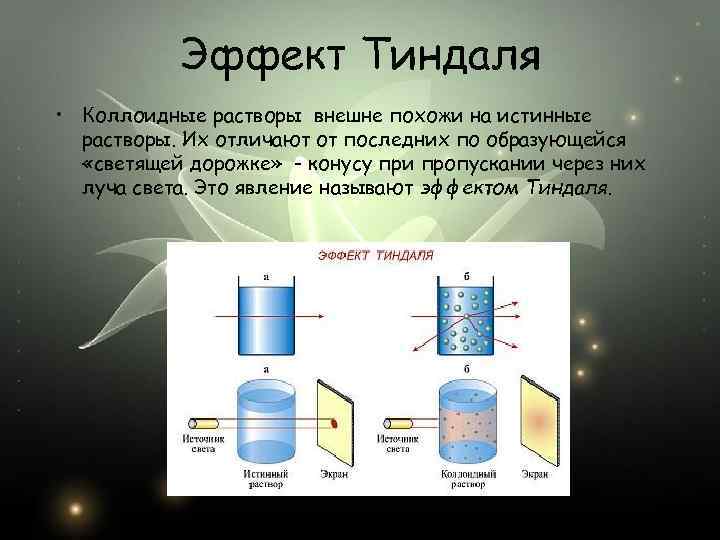 Эффект Тиндаля • Коллоидные растворы внешне похожи на истинные растворы. Их отличают от последних по образующейся «светящей дорожке» - конусу при пропускании через них луча света. Это явление называют эффектом Тиндаля.
Эффект Тиндаля • Коллоидные растворы внешне похожи на истинные растворы. Их отличают от последних по образующейся «светящей дорожке» - конусу при пропускании через них луча света. Это явление называют эффектом Тиндаля.
 Коагуляция • Коагуляция – явление слипания коллоидных частиц и выпадения их в осадок– наблюдается при нейтрализации зарядов этих частиц, когда в коллоидный раствор добавляют электролит. При этом раствор превращается в суспензию или гель. • Некоторые органические коллоиды коагулируют при нагревании или при изменении кислотно-щелочной среды раствора.
Коагуляция • Коагуляция – явление слипания коллоидных частиц и выпадения их в осадок– наблюдается при нейтрализации зарядов этих частиц, когда в коллоидный раствор добавляют электролит. При этом раствор превращается в суспензию или гель. • Некоторые органические коллоиды коагулируют при нагревании или при изменении кислотно-щелочной среды раствора.
 Гели (студни) • гели представляют собой студенистые осадки, образующиеся при коагуляции золей. • К ним относят большое количество полимерных гелей : косметические, медицинские и кондитерские(желатин, холодец, желе, мармелад) и природные гели (минералы, тела медуз, хрящи, сухожилия, волосы) • Со временем структура гелей нарушается – из них выделяется вода. Это явление называется синерезисом.
Гели (студни) • гели представляют собой студенистые осадки, образующиеся при коагуляции золей. • К ним относят большое количество полимерных гелей : косметические, медицинские и кондитерские(желатин, холодец, желе, мармелад) и природные гели (минералы, тела медуз, хрящи, сухожилия, волосы) • Со временем структура гелей нарушается – из них выделяется вода. Это явление называется синерезисом.
 Растворы • Раствором называют гомогенную систему, состоящую из двух и более веществ. • Растворы всегда однофазны, т. е. представляют собой однородный газ, жидкость или твердое вещество. • Растворы называют истинными, если требуется подчеркнуть их отличие от коллоидных растворов. • Растворителем считают вещество, агрегатное состояние которого не изменяется при образовании раствора. • Наибольшее значение имеют водные растворы. Природная вода всегда содержит растворенные вещества. Природные водные растворы участвуют в процессах почвообразования. Процессы жизнедеятельности, проходящие в организмах человека и животных, также протекают в растворах.
Растворы • Раствором называют гомогенную систему, состоящую из двух и более веществ. • Растворы всегда однофазны, т. е. представляют собой однородный газ, жидкость или твердое вещество. • Растворы называют истинными, если требуется подчеркнуть их отличие от коллоидных растворов. • Растворителем считают вещество, агрегатное состояние которого не изменяется при образовании раствора. • Наибольшее значение имеют водные растворы. Природная вода всегда содержит растворенные вещества. Природные водные растворы участвуют в процессах почвообразования. Процессы жизнедеятельности, проходящие в организмах человека и животных, также протекают в растворах.
 Растворы подразделяются на три группы: • Молекулярные – это водные растворы неэлектролитов – органических веществ (спирта, глюкозы, сахарозы). • Молекулярно-ионные – это растворы слабых электролитов (азотистой, сероводородной кислот). • Ионные – это растворы сильных электролитов (щелочей, солей, кислот).
Растворы подразделяются на три группы: • Молекулярные – это водные растворы неэлектролитов – органических веществ (спирта, глюкозы, сахарозы). • Молекулярно-ионные – это растворы слабых электролитов (азотистой, сероводородной кислот). • Ионные – это растворы сильных электролитов (щелочей, солей, кислот).


