22. Дисперсные системы.ppt
- Количество слайдов: 89

Дисперсное состояние вещества

ОБЩАЯ ХАРАКТЕРИСТИКА ДИСПЕРСНЫХ СИСТЕМ

Общая характеристика дисперсных систем Химия дисперсных систем изучает поведение вещества в сильно раздробленном, высокодисперсном состоянии, характеризующемся очень высоким отношением общей площади поверхности всех частиц к их общему объему или массе (степень дисперсности). От названия коллоидных систем произошло название отдельной области химии — коллоидной. Коллоидная химия — традиционное название химии дисперсных систем и поверхностных явлений. Раньше коллоидами называли клееподобные вещества, теперь это высокодисперсные системы с сильно развитой поверхностью раздела фаз. Ниже мы будем использовать старые традиционные термины, понимая их современный смысл. Например, под выражением «коллоидный раствор» будем иметь в виду высокодисперсное состояние вещества в воде в качестве дисперсионной среды.

Общая характеристика дисперсных систем Дисперсные системы — это системы, в которых мелкие частицы вещества, или дисперсная фаза, распределены в однородной среде (жидкость, газ, кристалл), или дисперсионной среде.
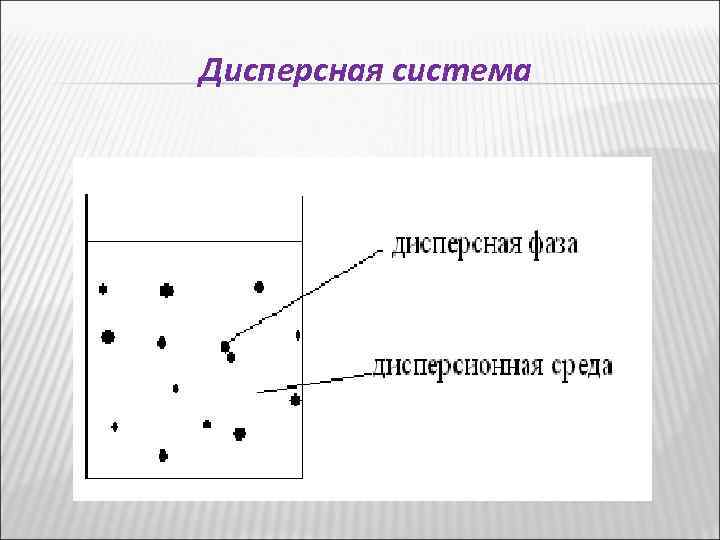
Дисперсная система

Общая характеристика дисперсных систем Размер частиц дисперсной фазы характеризуется дисперсностью. В зависимости от нее дисперсные системы бывают: высокодисперсные, или собственно коллоидные (размер частиц составляет 10 -3 мм и меньше), 10 -6 -10 -4 мм (от 1 до 100 нм), что, как минимум, на порядок больше, чем в истинных растворах (=10 - 7 мм) низкодисперсные или грубодисперсные (в интервале (больше 1. 10 -3 мм)

Общая характеристика дисперсных систем Важнейшая особенность дисперсного состояния вещества состоит в том, что энергия системы главным образом сосредоточена на поверхности раздела фаз. При диспергировании, или измельчении, вещества происходит значительное увеличение площади поверхности частиц (при постоянном суммарном их объеме). При этом энергия, затрачиваемая на измельчение и на преодоление сил притяжения между образующимися частицами, переходит в энергию поверхностного слоя — поверхностную энергию. Чем выше степень измельчения, тем больше поверхностная энергия. Поэтому область химии дисперсных систем (и коллоидных растворов) считают химией поверхностных явлений.

Общая характеристика дисперсных систем Коллоидные частицы очень малы (содержат 103 — 109 атомов), и не задерживаются обычными фильтрами, не видны в обычный микроскоп, не оседают под действием силы тяжести. Их устойчивость со временем снижается, т. е. они подвержены «старению» . Дисперсные системы термодинамически неустойчивы и стремятся к состоянию с наименьшей энергией, когда поверхностная энергия частиц становится минимальной. Это достигается за счет уменьшения общей площади поверхности при укрупнении частиц (что может также происходить при адсорбции на поверхности частиц других веществ).

Общая характеристика дисперсных систем В связи с тем, что поверхностная энергия маленькой частицы выше, чем более крупной, термодинамические свойства их различны. Так, растворимость мельчайших кристалликов выше, чем больших, и происходит перенос вещества из высоко дисперсной фазы в менее дисперсную, т. е. крупные кристаллы растут за счет растворения мелких. В этом самопроизвольном процессе ΔG < 0. Давление пара над маленькой каплей выше, чем над большой, и большие капли вырастают за счет испарения маленьких. Поэтому в облаках образуются капли дождя, точно так же растут снежинки
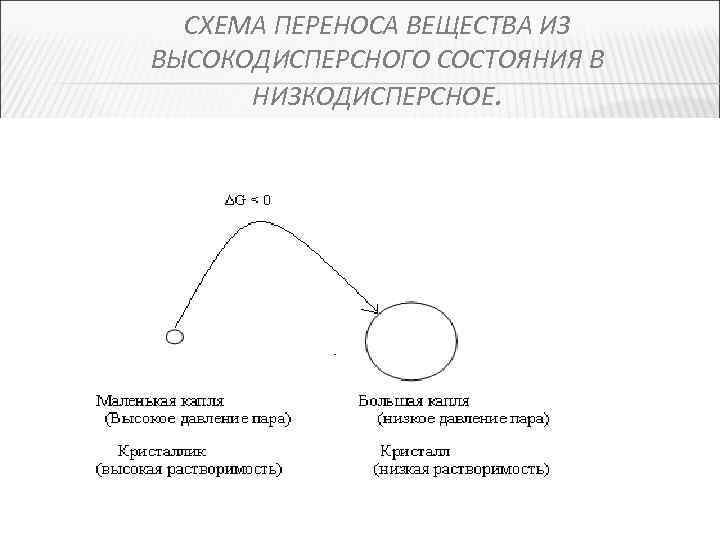
СХЕМА ПЕРЕНОСА ВЕЩЕСТВА ИЗ ВЫСОКОДИСПЕРСНОГО СОСТОЯНИЯ В НИЗКОДИСПЕРСНОЕ.

Общая характеристика дисперсных систем Вещество в дисперсном состоянии стремится поглотить другие вещества. Растворимость газов в каплях выше, чем в жидкости большого объема. Например, из-за того, что растворимость кислорода в капле воды высока, коррозия железа проходит даже без примесей в железе других веществ. Под каплей воды на поверхности железа коррозия проявляется в первую очередь у краев капли, где растворимость кислорода больше.

КЛАССИФИКАЦИЯ ДИСПЕРСНЫХ СИСТЕМ

Классификация дисперсных систем Существует несколько различных классификаций дисперсных систем: - по размеру частиц, -по фазовому состоянию дисперсной фазы и дисперсионной среды, -по характеру взаимодействия частиц дисперсной фазы с веществом дисперсионной среды, -по термодинамической и кинетической устойчивости дисперсных систем и т. п.
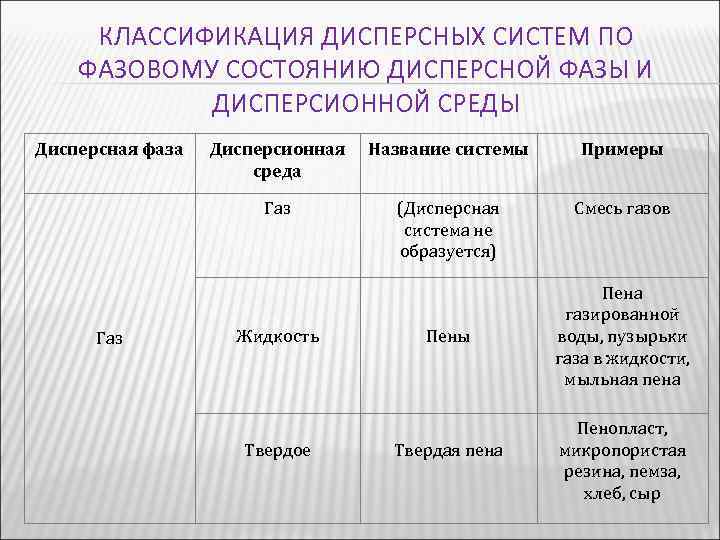
КЛАССИФИКАЦИЯ ДИСПЕРСНЫХ СИСТЕМ ПО ФАЗОВОМУ СОСТОЯНИЮ ДИСПЕРСНОЙ ФАЗЫ И ДИСПЕРСИОННОЙ СРЕДЫ Дисперсная фаза Название системы Примеры Газ Дисперсионная среда (Дисперсная система не образуется) Смесь газов Жидкость Твердое Пены Твердая пена Пена газированной воды, пузырьки газа в жидкости, мыльная пена Пенопласт, микропористая резина, пемза, хлеб, сыр

КЛАССИФИКАЦИЯ ДИСПЕРСНЫХ СИСТЕМ ПО ФАЗОВОМУ СОСТОЯНИЮ ДИСПЕРСНОЙ ФАЗЫ И ДИСПЕРСИОННОЙ СРЕДЫ Дисперсная фаза Дисперсионная среда Газ Название системы Аэрозоль Примеры Туман, облака, струя из аэрозольного баллона Жидкость Эмульсия Твердое тело Твердая эмульсия - суспензии Молоко, сливочное масло, майонез, крем, мазь Жемчуг, опал
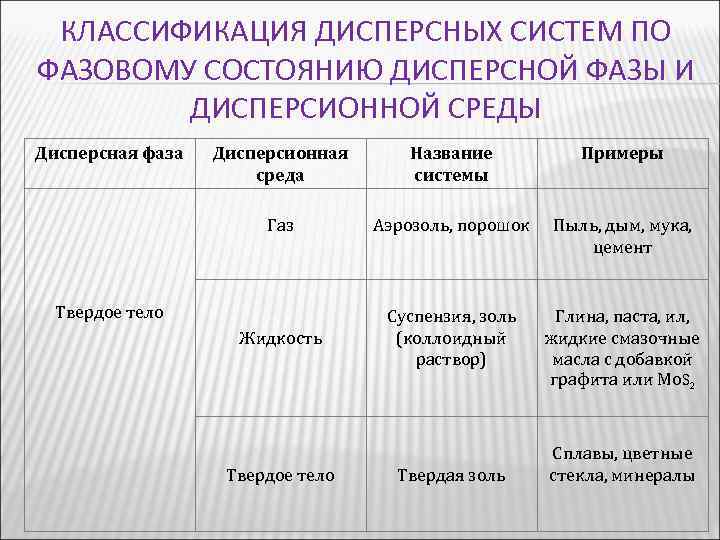
КЛАССИФИКАЦИЯ ДИСПЕРСНЫХ СИСТЕМ ПО ФАЗОВОМУ СОСТОЯНИЮ ДИСПЕРСНОЙ ФАЗЫ И ДИСПЕРСИОННОЙ СРЕДЫ Дисперсная фаза Дисперсионная среда Название системы Примеры Газ Аэрозоль, порошок Пыль, дым, мука, цемент Жидкость Суспензия, золь (коллоидный раствор) Глина, паста, ил, жидкие смазочные масла с добавкой графита или Мо. S 2 Твердое тело Твердая золь Сплавы, цветные стекла, минералы

ЛИОФИЛЬНЫЕ И ЛИОФОБНЫЕ ДИСПЕРСНЫЕ СИСТЕМЫ

ЛИОФИЛЬНЫЕ И ЛИОФОБНЫЕ ДИСПЕРСНЫЕ СИСТЕМЫ По силе взаимодействия дисперсной фазы с дисперсионной средой коллоидные системы разделяют на - лиофильные (от греч. 1 уо — растворяю, phileo — люблю) - лиофобные (от греч. phobos — страх). Эти названия указывают на то, что в лиофильных коллоидных системах взаимодействие частиц с веществом дисперсионной среды сильнее, чем в лиофобных.

Лиофильные дисперсные системы характеризуются сильным притяжением молекул дисперсионной среды к частицам дисперсной фазы. Вокруг частиц самопроизвольно образуются плотные и сравнительно устойчивые сольватные оболочки. При взаимодействии с молекулами воды говорят о гидрофильности дисперсной фазы и образовании гидратных оболочек. Если частицы распределены в маслоподобных органических веществах и окружены такими оболочками, говорят об олеофильности частиц.

Свойства лиофильных дисперсных систем Лиофильные вещества (тела) растворяются в данной жидкости, набухают в ней или хорошо смачиваются. В лиофильных коллоидах поверхность частиц сильно сольватирована и поверхностная энергия (поверхностное натяжение) на границе раздела фаз мала. Лиофильные коллоиды образуются в результате самопроизвольного диспергирования крупных частиц твердого вещества или капель жидкости на мельчайшие коллоидные частицы (или мицеллы). Лиофильные коллоиды термодинамически устойчивы и поэтому почти не разрушаются при постоянстве условий их образования. Лиофильные системы самопроизвольно образуются в жидкостях без участия электролитов или поверхностноактивных веществ. К лиофильным коллоидным системам относятся растворы обычного мыла в воде.

Свойства лиофильных дисперсных систем Важнейшая характеристика дисперсных систем — знак и величина заряда частиц. У частиц лиофильных коллоидов заряд или очень мал, или вообще отсутствует. Заряд на частице лиофильного коллоида изменяется очень легко прибавлении небольших количеств электролитов. Изменение концентрации ионов водорода в растворе (р. Н) приводит к перезарядке частиц коллоидного раствора. В электрическом поле лиофильные коллоиды или не перемещаются, или перемещаются в любом направлении.

Лиофобные дисперсные системы Слабое взаимодействие молекул дисперсионной среды с частицами дисперсной фазы приводит к образованию лиофобных систем. Если дисперсионной средой является вода, говорят о гидрофобности системы, если органические маслоподобные вещества — об ее олеофобности. Частицы лиофобных веществ (тела) не растворяются, плохо смачиваются и не набухают в веществе дисперсионной среды. Лиофобные системы с концентрацией дисперсной фазы выше 1% получить не удается, а лиофильные коллоидные системы могут быть очень концентрированными.

Свойства лиофильных и лиофобных систем Ø Ø Ø О лиофильности или лиофобности системы можно судить по количеству теплоты, выделяющейся при растворении, набухании и смачивании: у лиофильных систем теплота взаимодействия намного больше, чем у лиофобных. На гладкой поверхности лиофильного вещества капля жидкости растекается, образуя тонкий слой (пленку), а на лиофобной поверхности капля не растекается, образуя линзу или сплющенный шар. Количественной мерой лиофобности может служить величина угла между поверхностями капли и смачиваемого тела (краевой угол, или угол смачивания). Лиофобные коллоидные системы по вязкости близки к дисперсионной среде, лиофильные системы имеют более высокую вязкость. Лиофильные коллоидные растворы рассеивают свет слабее лиофобных.

Свойства лиофильных и лиофобных систем Ø Ø Ø Лиофобные системы — гетерогенные, и в этом отношении их нельзя относить к истинным растворам. Лиофильные системы — однофазные, гомогенные, обладающие многими свойствами истинных растворов. Вследствие высокой поверхностной энергии лиофобные системы термодинамически и кинетически неустойчивы. Лиофильные системы термодинамически устойчивы. При распаде лиофобные коллоидов происходит укрупнение коллоидных частиц, которое сопровождается уменьшением энергии системы. Способность противостоять укрупнению частиц (агрегативная устойчивость) у лиофобной системы имеет временный характер и часто обусловлена наличием веществ (стабилизаторов), адсорбирующихся на поверхности частиц и препятствующих их слипанию (или слиянию).

СУСПЕНЗИИ

СУСПЕНЗИИ Суспензии (или взвеси) - грубодисперсные системы типа «твердое вещество-жидкость» со сравнительно крупными (больше 1. 10 -3 мм) частицами. Частицы суспензий не обнаруживают броуновского движения. Суспензии с плотностью больше, чем плотность дисперсионной среды, выпадают в осадок; если же их плотность меньше, частицы всплывают.

Суспензии Глина — тонкодисперсная осадочная горная порода, в составе которой 30 -70% Si. O 2, 10 -30% Al 2 O 3 и 5 -10% H 2 O. Ø Размер частиц глины не превышает 0, 01 мм (при более крупных частицах глины переходят в песок). Суспензия глины в воде под названием «глинистый раствор» используется как промывная жидкость при бурении и как смазочное средство для уменьшения трения при вращении труб в скважинах. Ø Крайне концентрированная суспензия глины образует с водой тесто, которому можно придать желаемую форму и после высушивания и обжига получить кирпич или другое изделие. Ø Фарфор изготавливают из смеси порошков каолинита Al 4[Si 40 IO](OH), кварца Si. O 2, полевого шпата (алюмосиликаты калия, натрия, кальция, бария). Порошок смешивают с водой до образования густой пластичной массы, которой придают желаемую форму, высушивают и обжигают. Ø Порошок цемента, полученный обжигом силикатов и алюминатов кальция, при смешении с водой через некоторое время затвердевает в прочное камнеподобное тело.

СУСПЕНЗИИ Кровь — важнейшая для жизни человека и многих животных суспензия эритроцитов, лейкоцитов и тромбоцитов в физиологическом растворе (лимфе). Эритроциты — красные кровяные тельца — переносят кислород и углекислый газ, имеют диаметр (7, 2 -7, 5). 10 мм 3. В крови их содержится 4, 5— 5 млн.

Суспензии Поскольку размеры частиц относительно велики, суспензии кинетически неустойчивы, и при отстаивании частицы выпадают в осадок. Седиментация или осаждение - процесс выделения суспензированных частиц, происходящий под действием силы тяжести.

ЗОЛИ

Общая характеристика золей Золи — высокодисперсные системы с частицами (размер 10 -3— 10 -5 мм)из твердого вещества, находящимися в броуновском движении. Чаще всего золями называют системы с жидкой дисперсионной средой. Золи — типичные коллоидные системы, которые наиболее ярко проявляют свойства, присущие веществу в высокодисперсном состоянии.
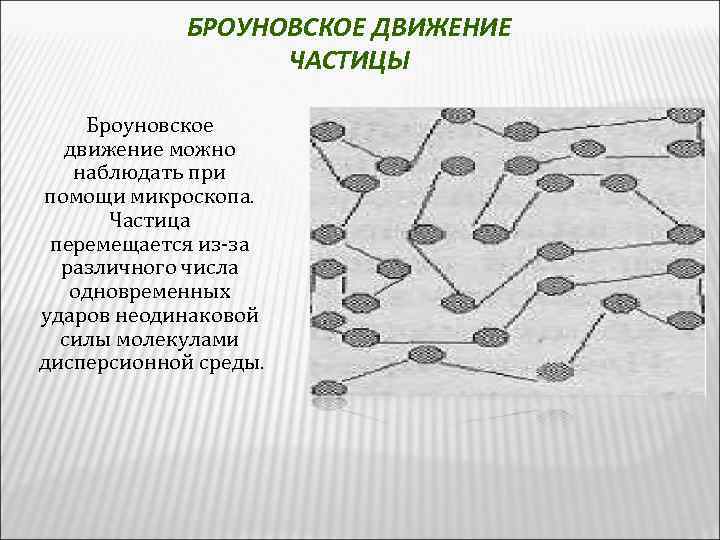
БРОУНОВСКОЕ ДВИЖЕНИЕ ЧАСТИЦЫ Броуновское движение можно наблюдать при помощи микроскопа. Частица перемещается из-за различного числа одновременных ударов неодинаковой силы молекулами дисперсионной среды.

ЛИОФИЛЬНЫЕ И ЛИОФОБНЫЕ ЗОЛИ Лиофильные золи образуются золи самопроизвольно и не разрушаются со временем. Лиофобные золи постепенно разрушаются золи вследствие самопроизвольного слипания твердых частиц (коагуляция) или слияния жидких частиц (коалесценция), хотя при наличии стабилизатора эти процессы могут быть очень длительными.

ПОЛУЧЕНИЕ КОЛЛОИДНЫХ СИСТЕМ 1. Конденсационный метод - образованиие нерастворимых веществ в химической реакции. Например, при окислении сероводорода сера выделяется в коллоидном состоянии: H 2 S + O 2 =2 S + 2 H 2 O 2 H 2 S + SO 2 = 3 S + 2 H 2 O 2 H 2 S + SO 32 - + 2 H+ = 3 S +3 H 2 O

Получение коллоидных систем Распад тиосульфат иона в кислотной среде также приводит к образованию золя серы: S 2 O 32 - = S + SO 32 При гидролизе ионов Fe 3+ образуется золь гидроксида железа: Fe 3+ + ЗН 2 О = Fe(OH)3 + ЗН+ Эти и подобные им реакции проходят в природе при слиянии природных вод различных составов и кислотности.

Получение коллоидных систем Дисперсные вещества получают в лаборатории растиранием в ступках пестиком или в мельницах с шарами. В природе подобное случается при трении камней в быстрых потоках воды или на камере (вспомните форму гальки).

ОБРАЗОВАНИЕ ЧАСТИЦ ДИСПЕРСНОЙ ФАЗЫ Процесс химического образования частиц дисперсной фазы очень сложен, но упрощенно его можно описать следующим образом. Рассмотрим образование золя и строение его частиц на примере хлорида серебра Ag. Cl. Этот золь образуется при медленном приливании водного раствора хлорида натрия Na. Cl к водному раствору нитрата серебра Ag. NO 3, взятому в избытке. Реакция протекает по уравнению: Ag. NO 3 + Na. Cl = Na. NO 3+ Ag. Cl Ag+ + Сl- = Ag. Cl

ОБРАЗОВАНИЕ ЧАСТИЦ ДИСПЕРСНОЙ ФАЗЫ При постепенном приливании раствора Na. Cl в раствор Ag. NO 3 в первый момент из ионов Ag+ и С 1 - образуется агрегат (Ag. Cl)n , в котором ионы расположены в том же порядке, что и в кристаллической решетке Ag. Cl. Далее агрегат (Ag. Cl)n адсорбирует на своей поверхности преимущественно те ионы, которые входят в его состав (или изоморфны по типу кристаллической решетки) и находятся в растворе в избытке. Этим условиям в данном случае отвечают ионы серебра. В результате адсорбции ионов Ag+ агрегат из хлорида серебра со слоем ионов серебра приобретает положительный заряд.

ОБРАЗОВАНИЕ ЧАСТИЦ ДИСПЕРСНОЙ ФАЗЫ Ионы, адсорбирующиеся на поверхности агрегата, придают частице заряд и называются потенциалопределяющими. Наличие одноименных зарядов потенциалопределяющими на агрегатах препятствует их объединению и росту кристалла Ag. Cl. Таким образом, агрегаты Ag. Cl с адсорбированными на них ионами приобретают состояние агрегативной устойчивости. Агрегат (Ag. Cl)n вместе с потенциалопределяющими ионами Ag+ составляет ядро. К заряженному ядру притягиваются ионы ядро противоположного заряда — противоионы. В данном случае такими ионами будут ионы, содержащиеся в растворе (но не входящие в состав агрегата), — нитрат ионы NO 3 -. Противоионы, непосредственно примыкающие к ядру, образуют адсорбционный слой противоионов
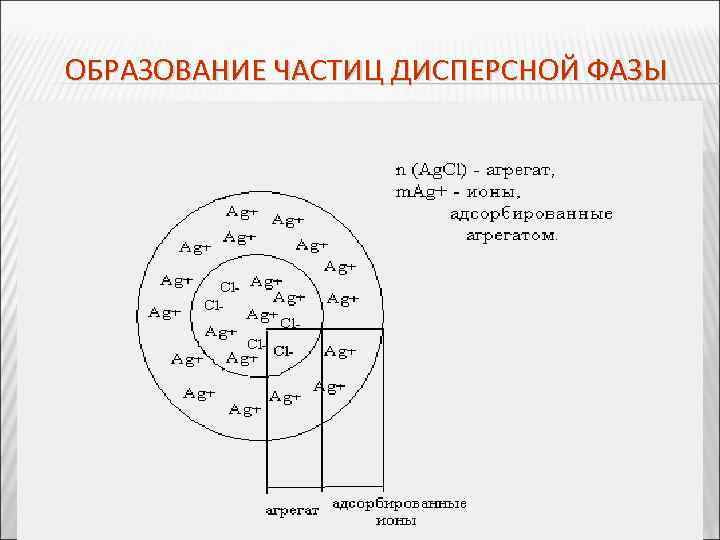
ОБРАЗОВАНИЕ ЧАСТИЦ ДИСПЕРСНОЙ ФАЗЫ

ОБРАЗОВАНИЕ ЧАСТИЦ ДИСПЕРСНОЙ ФАЗЫ За адсорбционным слоем противоионов следует диффузный слой тех же противоионов. Количество противоионов диффузного слоя постепенно понижается по мере удаления от ядра. Противоионы диффузного слоя ориентируют вокруг себя полярные молекулы растворителя, создавая дополнительную сольватную (гидратную) оболочку. Противоионы диффузного слоя удерживаются под действием двух факторов: - электростатического притяжения ионами противоположного заряда, которое удерживает их вблизи ядра, - броуновского движения, стремящегося распределить их в дисперсионной среде.

ОБРАЗОВАНИЕ ЧАСТИЦ ДИСПЕРСНОЙ ФАЗЫ Ядро вместе с противоионами адсорбционного слоя составляет коллоидную частицу, или гранулу. коллоидную частицу, Гранула с противоионами диффузного слоя называется мицеллой. Следует иметь в виду, что знак мицеллой. заряда гранулы соответствует знаку заряда потенциал определяющих ионов. Мицелла в отличие от гранулы электронейтральна. Формулу мицеллы гидрозоля хлорида серебра записывают так: {n (Ag. Cl), m. Ag+, (m - x)NO 3 -}x+ x. NO 3 В фигурные скобки гидрозоля заключена гранула. Ионы, указанные за фигурными скобками, составляют внешнюю часть мицеллы.
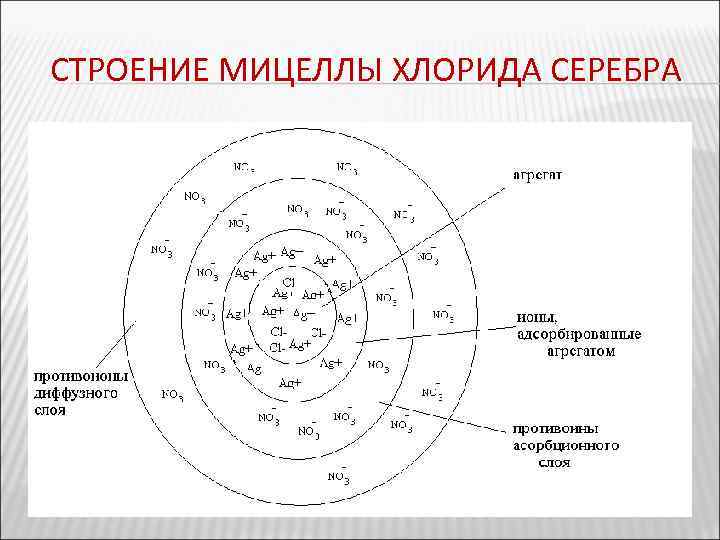
СТРОЕНИЕ МИЦЕЛЛЫ ХЛОРИДА СЕРЕБРА

ЭЛЕКТРОКИНЕТИЧЕСКИЕ ЯВЛЕНИЯ: ЭЛЕКТРОФОРЕЗ, ЭЛЕКТРООСМОС

ЭЛЕКТРОКИНЕТИЧЕСКИЕ ЯВЛЕНИЯ: ЭЛЕКТРОФОРЕЗ, ЭЛЕКТРООСМОС Явления смещения диффузного слоя в мицелле и даже его отрыва или, наоборот, возникновения разности потенциалов при движении мицеллы называют электрокинетическими явлениями. Все электрокинетические явления связаны с наличием двойного электрического слоя и определяются электрокинетическим потенциалом. Эти явления наблюдаются в дисперсных системах и в капиллярах и связаны с подвижностью диффузного слоя ионов. На электрокинетических явлениях основаны некоторые методы очистки воды.

ЭЛЕКТРОКИНЕТИЧЕСКИЕ ЯВЛЕНИЯ: ЭЛЕКТРОФОРЕЗ, ЭЛЕКТРООСМОС В плоскую чашку положим влажную глину и воткнем в нее две стеклянные трубки, в которые нальем воду с добавкой небольшого количества электролита для увеличения электропроводности. В воду опустим электроды и соединим их с источником постоянного тока. Через некоторое время жидкость в трубке с положительным электродом становится мутной из-за подъема частиц глины к электроду. Одновременно уровень жидкости в этой трубке понизится, а в другой поднимется. Этот опыт показывает, что частицы глины имеют отрицательный заряд и перемещаются в электрическом поле.

ЭЛЕКТРОФОРЕЗ Электрофорез - движение дисперсных Электрофорез частиц относительно дисперсионной среды (жидкой и газообразной) под действием электрического поля. В водной среде частица движется к электроду, знак заряда которого противоположен знаку электрокинетического потенциала.

СХЕМА ЭЛЕКТРОФОРЕЗА Диффузный слой ионов мицеллы непрочен, при перемещении мицеллы происходит его частичное разделение, при этом дисперсная фаза и дисперсионная среда приобретают противоположные заряды. В электрическом поле гранула перемещается к одному полюсу, а часть противоионов диффузного слоя отрывается от мицеллы и передвигается к противоположному полюсу.

ПРИМЕНЕНИЕ ЭЛЕКТРОФОРЕЗА На электрофорезе основаны: § очистка воды, § улавливание частиц дыма или пыли, § выделение белков, аминокислот, витаминов и т. п. , § поскольку вместе с гранулами передвигаются молекулы жидкости, составляющие их сольватные оболочки, электрофорезом производят частичное обезвоживание различных материалов (глины, почвы, мокрого торфа), § в медицине электрофорезом через кожу или слизистые оболочки вводят лекарственные вещества. § при электрофорезе частицы могут перезаряжаться и заряжаться. Например, хотя частицы белка электронейтральны, в кислотной среде белок передвигается к катоду, а в щелочной — к аноду.

ЭЛЕКТРООСМОС Если вместо глины взять пористую диафрагму (мембрану) или перегородку из пористого фарфора или стекла, плотной или смерзшейся почвы, то через мембрану в электрическом поле будет проходить жидкость без дисперсных частиц. Это явление называется электроосмосом. Электроосмос — перемещение дисперсионной Электроосмос среды под действием электрического поля: противоионы диффузного слоя притягиваются к соответствующему электроду и увлекают за собой жидкость дисперсионной среды.

ЭЛЕКТРООСМОС. ПРИМЕНЕНИЕ Электроосмос проявляется также при движении жидкости дисперсной системы через капилляры или поры диафрагмы под действием электрического тока. Электроосмосом можно объяснить некоторые природные процессы. Электроосмос используют для обезвоживания древесины, грунта, торфа и других материалов.

ЭЛЕКТРОКИНЕТИЧЕСКИЕ ЯВЛЕНИЯ: ЭЛЕКТРОФОРЕЗ, ЭЛЕКТРООСМОС Электрокинетические явления осуществимы только в том случае, если частицы заряжены. Благодаря электрокинетическим явлениям, может быть определен знак заряда коллоидной частицы, величина электрокинетического потенциала и изучены другие свойства дисперсных систем.

ЭМУЛЬСИИ

ЭМУЛЬСИИ. ТИПЫ И СВОЙСТВА Эмульсии – это высокодисперсные системы, в которых дисперсионная среда и дисперсная фаза находятся в жидком состоянии, т. е. состоят из мелких капель жидкости, распределенных в другой жидкости. Эмульсии образуются, если жидкости нерастворимы или ограниченно растворимы друг в друге. Например: эмульсии масла, бензина или нефти в воде, но не в спирте. Эмульсии могут образоваться при замене растворителя, например при введении, в воду раствора масла в органическом веществе, растворимом в воде.

Эмульсии. Типы и свойства В эмульсиях из двух (и более) взаимно нерастворимых жидкостей одна из них может быть либо дисперсионной средой, либо дисперсной фазой. Например, из масла и воды могут быть получены эмульсии «масло в воде» и «вода в масле» . При механическом диспергировании жидкостей могут образовываться одновременно оба вида эмульсий, но различной стойкости, и дольше сохраняется та эмульсия, капельки которой прочнее связаны со средой.

Эмульсии. Типы и свойства Тип эмульсии можно определить по следующим признакам: 1) эмульсии «масло в воде» легко смешиваются с водой, а «вода в масле» - с маслом; 2) эмульсии «масло в воде» окрашиваются водорастворимыми красителями, а «вода в масле» — маслорастворимыми.

Эмульсии. Типы и свойства Эмульсии, как и золи, разделяются на: ü лиофильные, термодинамически устойчивые (размер капель не больше 10 -3 мм), ü лиофобные, термодинамически неустойчивые, для стабилизации которых необходимы эмульгаторы (размер капель от 10 -3 до 1 мм).

Эмульсии. Типы и свойства Большинство эмульсий - лиофобные системы. Они самопроизвольно не образуются, термодинамически неустойчивы, и сразу же после образования эмульсии начинается обратный процесс слияния капель при их столкновении – коалесценция. Вслед за коалесценцией в зависимости от соотношения плотностей жидкостей дисперсной и дисперсионной фаз происходит всплывание больших капель (в бутылке с молоком образуется верхний жирный слой сливок) или их осаждение — седиментация. Чем больше размер капель и различие в плотностях, тем быстрее происходит разделение фаз.
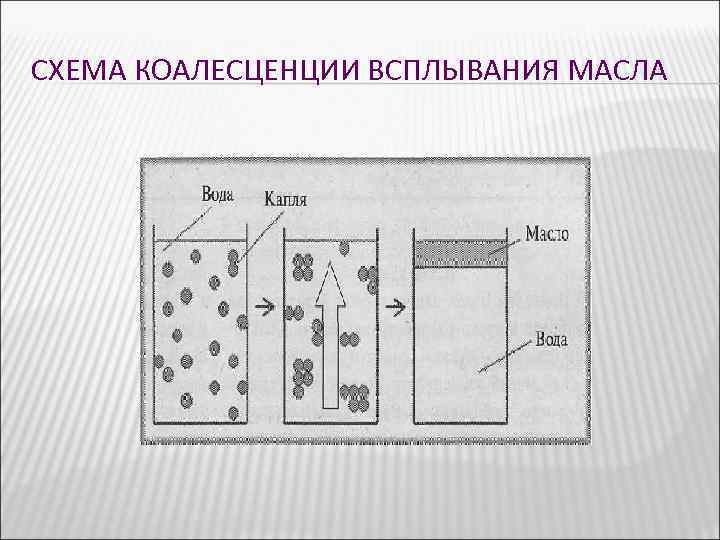
СХЕМА КОАЛЕСЦЕНЦИИ ВСПЛЫВАНИЯ МАСЛА

ЭМУЛЬГАТОРЫ Для сохранения эмульсии в течение некоторого интервала времени пользуются эмульгаторами. Эмульгаторы - молекулы которых Эмульгаторы адсорбируются на поверхности капель и препятствуют их слиянию. Наиболее эффективны в качестве эмульгаторов поверхностно-активные вещества (ПАВ), молекулы которых состоят из полярной (лиофильной) и неполярной (лиофобной) частей.
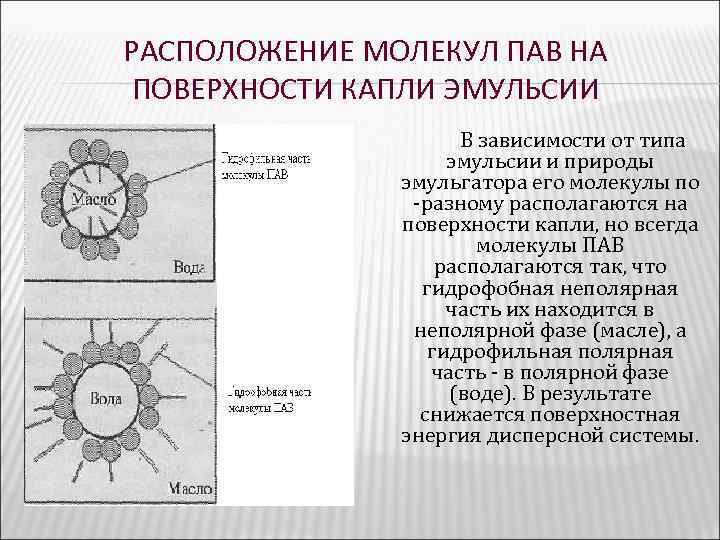
РАСПОЛОЖЕНИЕ МОЛЕКУЛ ПАВ НА ПОВЕРХНОСТИ КАПЛИ ЭМУЛЬСИИ В зависимости от типа эмульсии и природы эмульгатора его молекулы по -разному располагаются на поверхности капли, но всегда молекулы ПАВ располагаются так, что гидрофобная неполярная часть их находится в неполярной фазе (масле), а гидрофильная полярная часть - в полярной фазе (воде). В результате снижается поверхностная энергия дисперсной системы.

МЫЛА Мыла относятся к ПАВ. Стабилизирующее действие мыла на эмульсии и золи объясняется тем, что мыло представляет собой натриевые или калиевые соли стеариновой, пальмитиновой и олеиновой кислот: C 17 H 35 COONa, C 15 H 31 COONa и C 17 H 33 COONa, или CH 3(CH 2)7 CH=CH(CH 2)7 COONa.

Получение мыла Вспомним, как получают мыло. Оно образуется в процессе омыления (взаимодействия с гидроксид-ионами раствора щелочи) жира, т. е. сложного эфира глицерина и жирной кислоты: О СН 2 – О – С 17 Н 35 СН 2 ОН О СН - О – С 17 Н 35 + 3 ОН- = СНОН + 3 С 17 Н 35 СОО О СН 2 ОН СН 2 – О – С 17 Н 35 Жир глицерин стеарат-ион Образовавшаяся смесь содержит очень много воды, глицерина и избыток щелочи. Для выделения мыла в раствор добавляют поваренную соль (хлорид натрия), и в результате образуются соли кислот, например стеарат натрия C 17 H 35 COONa.

Моющее действие мыла объясняется гидролизом, например: CH 3(CH 2)16 COONa = СН 3(СН 2)16 СОО- + Na+, стеарат натрия стеарат-ион СН 3(СН 2)]6 СОО- + Н 2 О = СН 3(СН 2)16 СООН + ОН-. стеариновая кислота Грязь прикрепляется к ткани тонким слоем жира, который удаляется мылом. Моющее действие мыла включает смачивание поверхности, пептизацию загрязнения и его стабилизацию в растворе. Молекулы образовавшейся при гидролизе кислоты длинной гидрофобной частью окружают каплю или частицу жирового загрязнения или входят в нее ( «растворяются» ), а гидрофильные группы СООН обращены в воду. Так загрязнение переходит в воду.

ПРИМЕНЕНИЕ ЭМУЛЬСИЙ Эмульсии широко применяются при производстве пластмасс, красок, мыла, косметических средств, пищевых продуктов. Молоко - сложная эмульсия жира в воде, Молоко содержащая белки, сахар, минеральные вещества, витамины, ферменты, микроорганизмы. Жир находится в виде шариков диаметром от 0, 5 до 20 мкм (около 3 млрд в 1 мл). Каждый шарик окружен оболочкой из белков (и фосфолипидов), играющих роль стабилизаторов. Капли жира поднимаются на поверхность, и образуются сливки - очень концентрированные эмульсии. После молочнокислого брожения сливки превращаются в сметану - также высококонцентрированную эмульсию.

Применение эмульсий Сливочное масло - это концентрированная эмульсия, в которой большую часть составляет эмульсия типа «масло в воде» и меньшую - «вода в масле» . Яичный желток также может быть отнесен к эмульсиям. Мороженое - продукт из молока, сливок, масла, сахара. Это сложная дисперсная система, состоящая из мельчайших кристалликов льда, пузырьков воздуха, капелек жира. Для приготовления мороженого готовится эмульсия из смеси веществ, которую гомогенизируют с эмульгаторами (моно- и диглицеридами) и загустителями (желатином и крахмалом). Затем через эмульсию при охлаждении и непрерывном перемешивании пропускается воздух, что приводит к понижению плотности смеси почти в два раза.

Применение эмульсий Водоэмульсионные краски - это суспензии пигментов (красителей) в водных эмульсиях полимерных веществ (полиакрилаты, поливинилацетаты, сополимеры стирола с бутадиеном и т. п. ), играющих роль пленкообразующих. Их содержание доходит до 55%. Водоэмульсионные краски могут наноситься на влажные поверхности и образуют матовые покрытия. Нефть и нефтепродукты попадают в сточные воды из нефтедобывающих установок, нефтеперерабатывающих заводов и др. Они загрязняют природные воды также при промывке и авариях нефтеналивных танкеров и барж. Особенно опасен для живой природы слой нефти на поверхности воды (гибель рыбы, птиц и других животных). ПАВ способствуют образованию устойчивых эмульсий нефти и нефтепродуктов.

ПЕНЫ

ПЕНЫ Пены представляют собой пузырьки газа, разделенные пленками жидкости. Размер пузырьков, составляющих дисперсную фазу, лежит в пределах от долей миллиметра до нескольких сантиметров. По размеру пузырьков пены относятся к грубодисперсным системам. Общий объем заключенного в них газа может в сотни раз превосходить объем жидкости, находящейся в прослойках.

ПРИМЕНЕНИЕ ПЕН Пены широко используются в быту и производстве: ü вспенивание жидких и полужидких продуктов с последующим отверждением имеет важное значение при производстве хлеба, кондитерских изделий, кремов, ü брожение теста (молочнокислое брожение) сопровождается выделением углекислого газа, который поднимает тесто, после выпекания хлеба в нем сохраняются маленькие и большие пузырьки, ü приготовлении пива используют природные пенообразователи - хмель, некоторые белки, крахмал и др. ü в стиральных порошках запрещено использование пенообразователей. Они создают пену в барабане стиральной машины, и она выбрасывается наружу при стирке. Но еще вреднее попадание пенообразователей в сточные и природные воды. Описаны случаи превращения рек в пенный поток. ü устойчивые и обильные пены с углекислым газом используются как средство тушения пожаров, ü пены применяются при обогащении полезных ископаемых пенной флотацией.

ПЕНЫ Каждый знает про пемзу - пористую легкую вулканическую горную породу (60 -70% оксида кремния). Пемза образуется из жидкой лавы, насыщенной вулканическими газами, при выделении из-за понижения давления в ней пузырьков и быстром застывании пенообразной лавы. Пемза не тонет в воде, т. к. ее пористость свыше 60%, а плотность 0, 2 -0, 3 г/см 3. Пемзу используют как абразивный материал и наполнитель бетонов (пемзобетон). По аналогии с природным процессом образования пемзы получают вспениванием (растворов, жидких расплавов, суспензий и т. п. ) самые различные материалы: строительные и конструкционные ячеистые материалы, пеностекло, пеношлаки, пенопласты, пористую резину и т. п. Пенокерамика (керамика с ячеистой структурой) изготавливается из пен оксидов алюминия, магния, циркония. Пеностекло получают спеканием стеклянного порошка с мелом как порообразователем. Применяется как теплоизолирующий материал. Из пеностекла с открытыми порами изготавливают фильтры.

ПЕНЫ Для получения пенометаллов (алюминий, магний и др. ) в расплавленный металл добавляют гидриды титана, циркония и других элементов. Выделяющийся водород вспенивает металл. Пеноалюминий - прекрасный конструкционный материал - имеет низкую теплопроводность и низкую плотность (-0, 23 г/см 3). Пористую резину получают вулканизацией каучука в смеси с порообразователями. Используется как материал, уменьшающий вибрацию, для подошв обуви, сидений автомобилей. Из вспененных при помощи порообразователей пластмасс (полиуретан, полистирол, поливинилхлорид) получают пенопласты с закрытыми порами и поропласты с сообщающимися порами. Используются для теплоизоляции холодильников, электроизоляции, изготовления плавучих средств, фильтров и т. п.

АЭРОЗОЛИ

АЭРОЗОЛИ Аэрозоли - дисперсные системы, состоящие из мельчайших частиц твердого тела или жидкости, равномерно распределенных в газовой (воздушной) среде. Пыль - типичный и постоянно нас окружающий аэрозоль, представляющая большую опасность для человека. Пыль - это твердые частицы, взвешенные в воздухе, размером от микроскопических до видимых невооруженным глазом (10 -4 - 10 -1 мм). Пыль неустойчива - ее частицы соединяются в броуновском движении или при оседании (седиментация). Пыль усиливает рассеяние и поглощение света атмосферой и влияет на ее тепловой режим, отдельных местностей и даже планеты.

ГЕЛИ (СТУДНИ)

ГЕЛИ (СТУДНИ) Гели (студни) - гидрофильные коллоиды при осаждении увлекают за собой жидкую фазу (иногда даже полностью), образуя с водой общую массу. Примеры бытовых гелей — желе, мармелад, яичный белок, студень. Гели образуются при высаливании, испарении растворителя, увеличении концентрации лиофильного коллоида и под действием других факторов. Влияние температуры на гелеобразование может быть различным: в некоторых случаях с понижением температуры образуется гель, в других — гель разрушается.

ХРУПКИЕ И ЭЛАСТИЧНЫЕ ГЕЛИ Хрупкие гели — это двухфазные гетерогенные системы. К хрупким гелям относится, например, гель кремниевой кислоты H 2 Si 03. Благодаря жесткости каркаса хрупкого геля его объем при высушивании или обезвоживании мало изменяется. После высушивания образуются хрупкие гели, имеющие сильнопористую структуру с множеством капилляров и пор. Так получают распространенные сорбенты: алюмогель из геля гидроксида алюминия и силикагель из кремниевой кислоты. Сухой торф также можно отнести к аэрогелям, он обладает высокими сорбционными свойствами.

ХРУПКИЕ И ЭЛАСТИЧНЫЕ ГЕЛИ Эластичные гели образуются из некоторых гидрофильных неорганических веществ и высокомолекулярных соединений и в отличие от хрупких гелей являются однофазными системами. Эластичные гели способны к набуханию с увеличением объема в десятки раз по сравнению с собственным объемом полимера. Эти гели обладают малой прочностью. Таковы, например, гели мыл, гидроксидов алюминия и железа.

ОБРАЗОВАНИЕ ГЕЛЕЙ Процесс образования геля из золя обратим. При встряхивании геля может образоваться золь, но после прекращения воздействия снова образуется гель. Тиксотропия - явление обратимости в системе «гель - золь» . Тиксотропия проявляется при определенной концентрации коллоидных частиц (или концентрации полимера). Понятие тиксотропии применяют не только к дисперсным системам. Тиксотропия объясняется разрушением и образованием химических связей. Состояние жидкости в гелях непрочное. Они сравнительно легко изменяют свой объем при поглощении или отдаче дисперсионной среды. С течением времени из геля самопроизвольно выделяется жидкая фаза и объем геля уменьшается. Это явление называется синерезисом, или старением геля.

ГЕЛИ В ПРИРОДЕ Гели, как и золи, очень распространены в природе. Свежеобразованные природные гели богаты водой и напоминают студенистые или хлопьевидные массы. Эти гели весьма реакционноспособны, на их свойствах сказывается даже незначительное изменение р. Н, они легко реагируют с компонентами растворов. Постепенно гели теряют воду и становятся малореакционноспособными. Аморфные минералы, образовавшиеся в водных растворах и содержащие переменное количество воды, также относятся к твердым гелям.

ПРИРОДНЫЕ ДИСПЕРСНЫЕ СИСТЕМЫ Почва - сложнейшая система из мельчайших частиц с размерами 2. 10 -5 - 1. 10 -7 см и более крупных. Основную часть органических веществ почвы представляют углеводы, жиры и гуминовые кислоты. Компоненты почвы обладают лиофобными и лиофильными свойствами, и мельчайшие частицы почвы с почвенной водой образуют гели, золи и эмульсии. Эти дисперсные системы поглощают из почвенных растворов ионы аммония, кальция, магния, вещества вносимых удобрений и переносят их из одного слоя почвы в другой. Гели способствуют образованию структуры почв. В состав природных коллоидов почв входят нерастворимые в воде алюмосиликатные соединения (глина) и органические соединения, гумус.

ПРИРОДНЫЕ ДИСПЕРСНЫЕ СИСТЕМЫ Гумус - это перегной, органическая темноокрашенная часть почвы, образующаяся в результате биохимического превращения растительных и животных остатков, а также при воздействии кислорода атмосферы или грунтовых вод на органические вещества почвы. В состав гумуса входят наиболее важные для плодородия почв гуминовые кислоты - это высокомолекулярные темноокрашенные органические вещества. Они образуются при конденсации ароматических соединений типа фенола с аминокислотами и имеют кислотные группы -СООН. Гуминовые кислоты могут образовывать истинные и коллоидные растворы, состоящие из мицелл с относительной массой 3700 -8300. Разрушение почвенных дисперсных систем нежелательно, т. к. при этом снижается адсорбционная способность почвы и из нее вымываются необходимые для растений вещества (в частности, ионы кальция и магния).

НАУЧНЫЕ ОСНОВЫ УЧЕНИЯ ОБ УСТОЙЧИВОСТИ ДИСПЕРСНЫХ СИСТЕМ

УСТОЙЧИВОСТЬ ДИСПЕРСНЫХ СИСТЕМ Устойчивость коллоидных систем зависит от многих факторов: при повышении температуры из-за роста кинетической энергии частиц уменьшается диффузный слой ионов частиц, и при их соударении слипаются; при замораживании раствора вода из защитных гидратных оболочек частиц переходит в лед, и происходит концентрирование золя и электролита; при последующем размораживании дисперсная система может не восстановиться; сильное повышение давления также способствует слипанию частиц.

СТАБИЛИЗАТОРЫ Сохранение коллоидных систем и их стабилизация имеют большое значение в природе и в производстве. Стабилизаторы — это вещества ионного или молекульного строения. Ионные стабилизаторы усиливают ионные слои, которые затрудняют объединение частиц. Молекульные стабилизаторы создают вокруг частиц сольватные оболочки из молекул дисперсионной среды, также затрудняющие их объединение.

ПЕПТИЗАЦИЯ Пептизация — самопроизвольный распад слипшихся коллоидных частиц на частицы меньших размеров. Пептизация проходит благодаря образованию двойного электрического слоя, адсорбции ионов и гидратации частиц. Пептизация протекает с выделением энергии (ΔН < 0) и связана как с увеличением порядка вследствие сольватации частиц, так и с уменьшением их размеров вследствие раздробления вещества. Пептизации способствуют повышение температуры, перемешивание, удаление коагулянтов и введение пептизаторов (электролитов, ПАВ). Пептизаторы — вещества, вызывающие пептизацию, — изменяют состав и структуру двойного электрического слоя, увеличивают диффузный слой и этим защищают частицы от слипания.

СПОСОБЫ ОЧИСТКИ Диализ - основан на диффузии и прохождении ионов и молекул через полупроницаемые мембраны (перегородки из пленок). Мембраны пропускают молекулы и ионы, но задерживают частицы дисперсной фазы. Фильтрование: золь промывают водой, а затем фильтруют через специальные фильтры с очень малыми размерами пор. Для ускорения фильтрации процесс проводят при повышенном давлении над фильтром или при разрежении за фильтром. Центрифугирование - разделением центробежной силой фаз, имеющих различные плотности. Высаливание - коагулирование гидрофильных коллоидов (например, высаливание мыла из водного щелочного раствора). Происходит из-за нарушения адсорбционных слоев частицы и разрушения ее гидратной оболочки (при добавлении дегидратирующих веществ).

ВЫВОДЫ Вы ознакомились с самыми основными понятиями химии дисперсного состояния веществ и увидели, насколько широко дисперсное состояние вещества встречается в природе, нашей повседневной жизни и в промышленных процессах. В дисперсном состоянии может находиться любое вещество. Поэтому коллоидная химия представляет собой науку, связывающую многие разделы химии, физики и другие области знания.

Спасибо за внимание!
22. Дисперсные системы.ppt