MedChem_2-4.ppt
- Количество слайдов: 22

ДИСПЕРСНІ ВЛАСТИВОСТІ СИСТЕМИ. РОЗЧИНІВ БІОПОЛІМЕРІВ
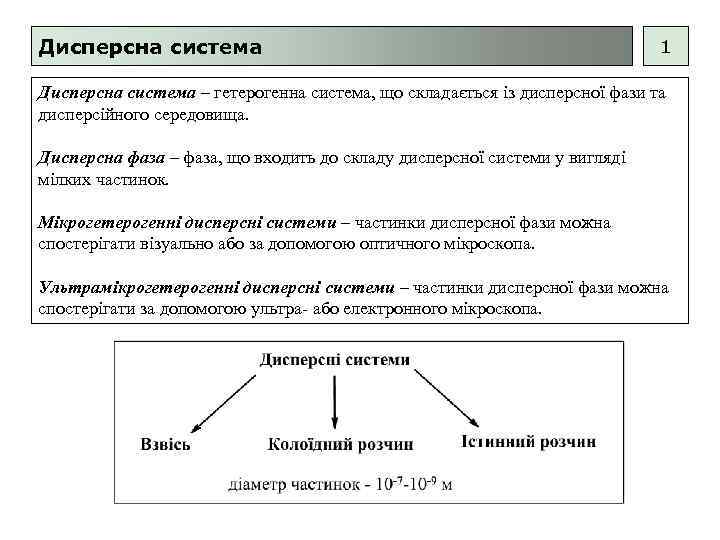
Дисперсна система 1 Дисперсна система – гетерогенна система, що складається із дисперсної фази та дисперсійного середовища. Дисперсна фаза – фаза, що входить до складу дисперсної системи у вигляді мілких частинок. Мікрогетерогенні дисперсні системи – частинки дисперсної фази можна спостерігати візуально або за допомогою оптичного мікроскопа. Ультрамікрогетерогенні дисперсні системи – частинки дисперсної фази можна спостерігати за допомогою ультра- або електронного мікроскопа.

Дисперсна система 2 Класифікація дисперсних систем за фізичним станом: Назва Дисперсне середовище Дисперсна фаза Розмір частинок: грубодисперсні – 10 -5 -10 -7 м, колоїдно-дисперсні – 10 -7 -10 -9 м Туман газ рідина грубодисперсна система Аерозоль газ рідина, тверда речовина колоїдно-дисперсна система Піна рідина газ грубо- та колоїдно-дисперсна система Емульсія рідина грубо- та колоїдно-дисперсна система Суспензія рідина тверда речовина грубодисперсна система Золь рідина тверда речовина колоїдно-дисперсна система Тверда піна тверда речовина газ грубо- та колоїдно-дисперсна система Золями прийнято називати усі системи колоїдної дисперсності.

Дисперсна система 3 Класифікація дисперсних систем за термодинамічною стабільністю та характером утворення: • ліофобні (гідрофобні) – утворюються шляхом подрібнення більш крупних об’єктів і є нестабільними; • ліофільні (гідрофільні) – утворюються самовільно та термодинамічно стабільні. Ефект Тіндаля – ефект розсіювання світла при пропусканні його через колоїдний розчин. Нефелометрія – метод вивчення колоїдних систем (розміру часточок) шляхом вимірювання розсіювання ними світла.
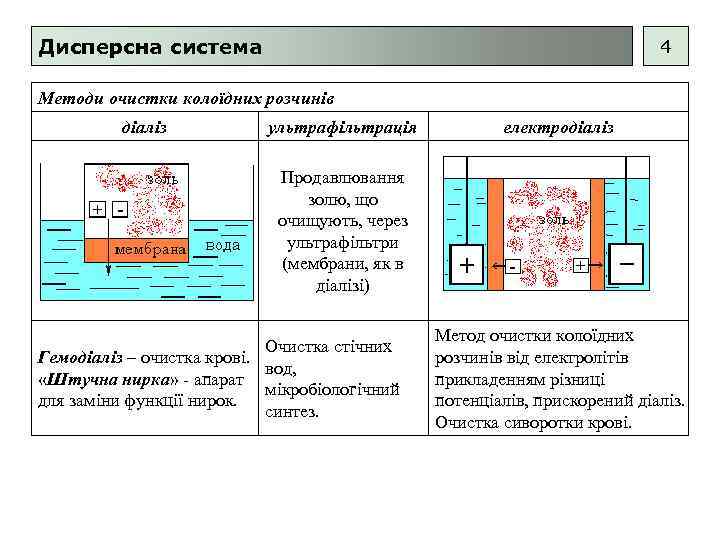
Дисперсна система 4 Методи очистки колоїдних розчинів діаліз ультрафільтрація електродіаліз Продавлювання золю, що очищують, через ультрафільтри (мембрани, як в діалізі) Очистка стічних Гемодіаліз – очистка крові. вод, «Штучна нирка» - апарат мікробіологічний для заміни функції нирок. синтез. Метод очистки колоїдних розчинів від електролітів прикладенням різниці потенціалів, прискорений діаліз. Очистка сиворотки крові.

Дисперсна система. Міцели 5 Міцела – комплекс, що утворює кристалик дисперсної фази та його ПЕШ. Подвійний електричний шар (ПЕШ) – два близьких за значенням, але різнойменні заряди, що виникають на контактуючих поверхнях. Причини появи: • обмін йонами з водою (для металів); • адсорбція переважно йонів одного знаку (для іонітів та колоїдних часток); • орієнтація полярних молекул певним чином на поверхні. Гель (ліогель) – структурована міцелярна система, утворюється із колоїдних розчинів внаслідок втрати ними стійкості. Однорідна система, в якій зв’язані міжмолекулярними силами міцели утворюють рівномірну, заповнену дисперсійним середовищем, сітку.
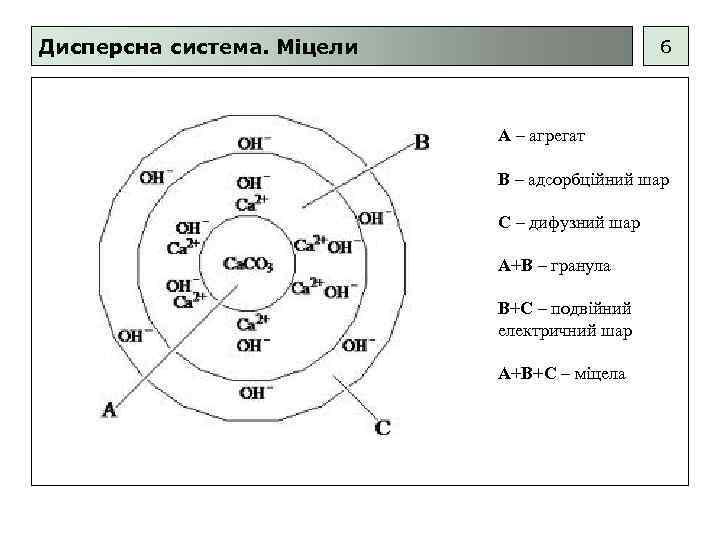
Дисперсна система. Міцели 6 А – агрегат В – адсорбційний шар С – дифузний шар А+В – гранула В+С – подвійний електричний шар А+В+С – міцела

Дисперсна система. Електро-кінетичні явища 7 Електро-кінетичні явища – переміщення двох фаз під дією електричного поля або виникнення різниці потенціалів при переміщенні двої фаз одна відносно іншої. Електрофорез - переміщення частинок дисперсної фази в дисперсних системах під дією електричного поля. Застосовується: • очистка колоїдних розчинів; • електрофоретичні методи аналізу та розділення природних біополімерів; • введення в організм ліків під дією зовнішнього електричного поля. Електроосмос - переміщення рідини в пористих тілах та дисперсних системах під дією електричного поля. Застосовується: зневоднення фармацевтичної сировини. Осмос - однобічна дифузія молекул розчинника через напівпроникну перегородку (мембрану), яка відокремлює розчин від чистого розчинника або розчину меншої концентрації. Зумовлений прагненням системи до вирівнювання концентрацій розчину з обох боків мембрани. Характеризується осмотичним тиском, що дорівнює надлишковому зовнішньому тискові, який треба докласти, щоб припинити осмос. Відіграє важливу роль у фізіологічних процесах, використовується при дослідженні полімерів, біологічних структур.
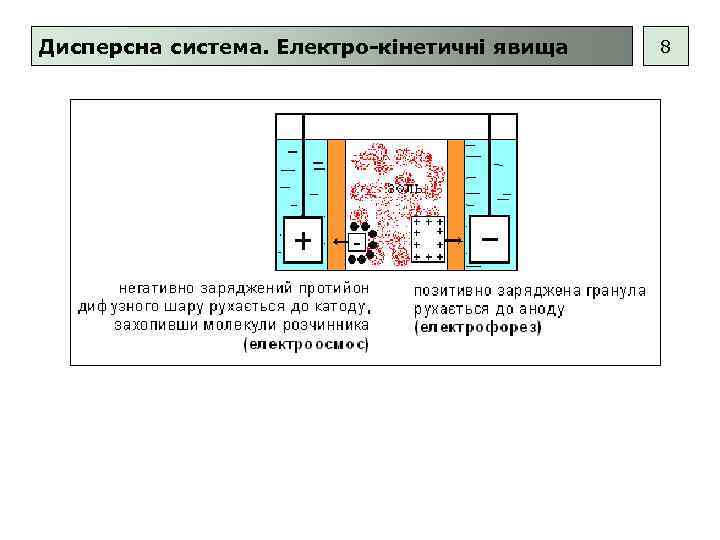
Дисперсна система. Електро-кінетичні явища 8

Дисперсна система. Електро-кінетичні явища 9 Швидкість руху частинок дисперсної фази в електричному полі визначає дзетапотенціал (електро-кінетичний потенціал), який розраховують за рівнянням Гельмгольца- Смолуховського: = / 0 Н, де - дзета-потенціал; - коефіцієнт, що враховує форму частинок; - в’язкість середовища; - швидкість електрофорезу, м/с; - діелектрична проникність середовища; 0 – діелектрична стала, 8, 85 10 -12 Ф/м; Н – градієнт зовнішнього електричного поля, В/м Потенціал седиментації (ефект Дорна) – різниця потенціалів між верхньою та нижньою частинами посуду, в якому осідають колоїдні частинки. Потенціал перебігу (явище, зворотнє електроосмосу) – різниця потенціалів між кінцями капілярів або на поверхнях діафрагми, що виникають внаслідок протікання (продавлювання) через них колоїдного розчину.

Коагуляція 10 Стійкість золів: • седиментаційна – здатність зберігати однорідний розподіл частинок у всьому об’ємі; • термодинамічна – характерна для золів, що утворились із зменшенням поверхневої енергії (ліофільних); ліофобні дисперсні системи термодинамічно нестійкі; • агрегаційна – здатність зберігати ступінь дисперсності. Коагуляція – явище злипання частинок дисперсної фази. Гідрозолі руйнуються при додаванні електролітів. В осадах, що отримані при коагуляції золів електролітами, завжди присутні йони, що викликали коагуляцію. При коагуляції золів сумішами електролітів рідко спостерігається їх незалежна (адитивна) дія; зазвичай має місце взаємне посилення або ослаблення коагулюючої дії (синергізм або антагонізм йонів).

Коагуляція Правила коагуляції: коагуляцію викликають будь-які електроліти, але з помітною швидкістю вона виникає лише за певної концентрації, яку називають «порогом коагуляції» ; правило Шульца – Гарді: коагулюючу дію спричиняє лише той йон електроліта, заряд якого протилежний заряду дисперсної частинки, при чому коагулююча дія зростає при збільшенні величини заряду; в ряду неорганічних йонів з однаковим зарядом максимальну коагулюючу дію буде мати найменш сольватований йон; в ряду органічних сполук коагулююча активність зростає з підвищенням адсорбційної здатності. 11

Коагуляція 12 Теорія коагуляції колоїдних систем електролітами ДЛФО (Дерягін, 1941, Ландау, Фервей, Овербек) базується на загальних принципах статистичної фізики, теорії розчинів і теорії дії міжмолекулярних сил Ван-дер-Ваальса. Теорія ДЛФО розглядає процес коагуляції як результат спільної дії молекулярної енергії притягання UM та електростатичної енергії відштовхування UE. Залежно від балансу цих енергій в тонкому шарі рідини між будь-якими частинками при їх наближенні виникає розклинюючий тиск рідкого прошарку. Розклинюючий тиск - сумарний параметр, який враховує енергію притягання UM і енергію відштовхування UE частинок золю. При додаванні електролітів заряджена частинка дисперсної фази адсорбує протийон, внаслідок чого зменшується заряд цієй частинки, товщина ПЕШ і, відповідно, розклинюючий тиск.

Коагуляція 13 Звикання золів до дії електролітів: при поступовому введенні електроліту в колоїдну систему остання втрачає стійкість при концентраціях, що істотно перевищують такі, коли б електроліти вводилися одноразово, але у великих кількостях. Захист золей – стабілізація шляхом додавання антикоагулянтів (ПАР, біополімери тощо). Захист золей в медицині – антикоагулянти крові; стабілізатори емульсій, які використовують в медичній практиці. Пептизація – явище протилежне коагуляції, розщеплення коагуляту з утворенням золю. Можлива лише коли диперсні частинки в коагуляті не зв’язались хімічно. Коагуляти для очистки стічних вод: вапняне молоко, солі алюмінію, заліза, магнію, цинку, сірчанокислого кальцію, карбонати тощо. Швидкість осідання еритроцитів (ШОЕ) [або Реакція осідання еритроцитів, РОЕ]неспецифічний лабораторний показник крові, що відображає співвідношення фракцій білків плазми; зміна ШОЕ може служити непрямою ознакою запального або іншого патологічного процесу. В нормі еритроцити несуть негативний заряд, який перешоджає їх злипанню (коагуляції). Патологічний процес зменшує заряд оболонки еритроцита, тому швидкість коагуляції та осідання суттєво зростає.
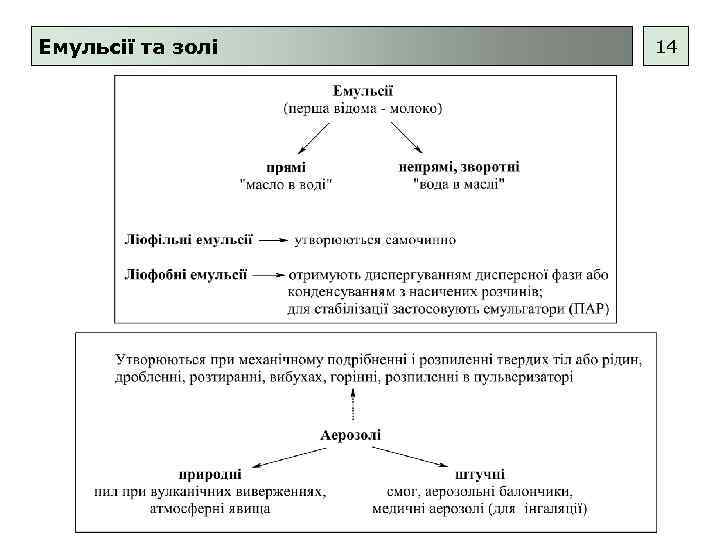
Емульсії та золі 14

Високомолекулярні сполуки 15 Біополімери мають дифільний характер, оскільки містять полярні (-COOH, -NH 2, OH) і неполярні (-CH 3, -CH 2, -C 6 H 5) функціональні групи. Розчинність ВМС у воді: кількість полярних груп; форма молекули.
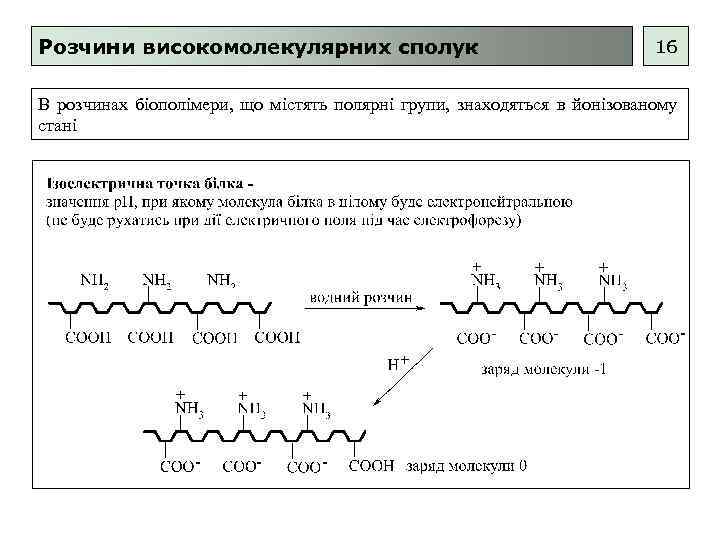
Розчини високомолекулярних сполук 16 В розчинах біополімери, що містять полярні групи, знаходяться в йонізованому стані

Розчини високомолекулярних сполук 17 Процес розчинення ВМС відбувається в 2 стадії: 1. Набухання - самовільний процес поглинання ВМС великих обсягів низькомолекулярної рідини, що супроводжується значним збільшенням полімеру Необмежене набухання: процес переходу від набухання до розчинення відбувається плавно та самовільно Обмежене набухання: процес переходу від набухання до розчинення відбувається при певних факторах (підвищення температури) 2. Розчинення - дифузія молекул ВМС у розчинник
Розчини високомолекулярних сполук Властивості розчинів ВМС, що об'єднують їх з істинними розчинами: 1. речовина диспергують до стану молекул; 2. при розчиненні ВМС розчин утворюється самовільно; 3. розчини ВМС - гомогенні системи (немає межі розділу між речовиною, що розчиняється і розчинником); 4. розчини ВМС - термодинамічно рівноважні системи; 5. для розчинів ВМС характерно: - Броунівський рух; - Відсутність явища Тіндаля 18 Властивості розчинів ВМС, відрізняють їх від істинних розчинів: 1. великий розмір молекул; 2. низький осмотичний тиск; 3. мала дифузійна здатність; 4. розчини ВМС не здатні до діалізу; 5. розчини ВМС можуть змінюватися під впливом зовнішніх факторів (додавання електролітів, зміну температури та ін. )
Розчини високомолекулярних сполук 19 Чинники, що викликають порушення стійкості розчинів ВМС: висока концентрація ВМС в розчині; зміна р. Н; низька температура; додавання електролітів. Види нестійкості розчинів ВМС: висолювання - процес виділення ВМС із розчину у вигляді аморфного осаду в результаті дегідратації молекул; коацервація - утворення нової фази у вигляді дрібних крапель; драглюваня - особлива проміжна форма існування системи (драглі або гель), що характеризується повною втратою рідкої фази; синерезис - явище драглюваня, що відбувається в самих драглях, та призводить до поділу системи на 2 фази: концентровані граглі та розчин ВМС

В'язкість розчинів ВМС 20 В'язкість розчинів ВМС залежить від: концентрації речовини у розчині. На відміну від істинних та колоїдних розчинів незначна концентрація ВМС інколи приводить до значного збільшення в'язкості розчину; умов визначення, зокрема, від тиску. Макромолекули можуть перебувати в різних конформаційних станах (лінійні, глобули), тому в'язкість розчинів ВМС може бути неоднакова в різних напрямках. Якщо в'язкий полімер або його розчин продавити через капіляр, то молекули будуть випрямлятися, а в'язкість - знижуватися. Тиксотропія (тиксотропність) - здатність субстанції зменшувати в'язкість (розріджуватися) від механічної дії та збільшувати в'язкість (згущуватися) в стані спокою; властивостей і температури розчинника. Прилад для вимірювання в’язкості: віскозиметр.

В'язкість крові Кров - суспензія клітин в рідині. У 1972 р. Г. Б. Фарстон вперше виміряв в'язкоеластичні властивості крові, які контролюють пульсуючий струм крові та залежать від багатьох параметрів: в'язкість плазми, деформація червоних кров'яних тіл, коагуляції еритроцитів та білків крові та ін. В'язкість води - 1 м. Па·c (20 °С). В’язкість крові в нормі - 4 -5 м. Па·c. При різних патологіях значення в'язкості крові можуть змінюватися від 1, 7 до 22, 9 м. Па·c 21
MedChem_2-4.ppt