
Дисциплина «Химия» Лекция № 6 Тема: α – аминокислоты. Пептиды. Белки. Для студентов 1 курса специальности: “Общая медицина”, “Стоматология” Лектор: ст. преподаватель кафедры биохимии и химических дисциплин, кандидат химических наук Болысбекова Салтанат Манарбековна

Цель и задачи: • Сформировать знания о α-аминокислотах как важнейшего класса органических соединений и основы белков живых организмов.

Актуальность: • Белки играют исключительно важную роль в живой природе. Жизнь немыслима без различных по строению и функциям белков. Белки – обязательная составная часть всех живых клеток.

План лекции: 1. 2. 3. 4. 5. Аминокислоты. Классификация АМК. Химические свойства. Пептиды. Белки.

Аминокислоты (АМК) – это производные карбоновых кислот, в радикале которых один или несколько атомов водорода замещены на аминогруппы.
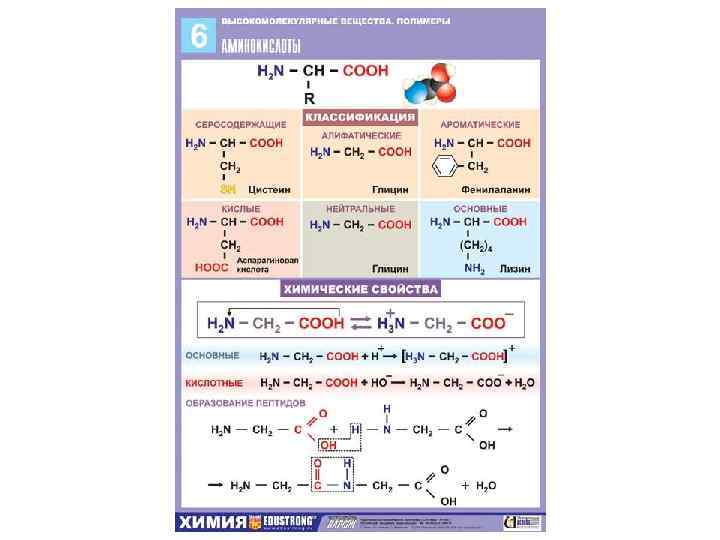

Классификация альфааминокислот. 1. По числу амино- и карбоксильных груп; 2. По наличию функциональных групп в радикале; 3. По природе радикала.
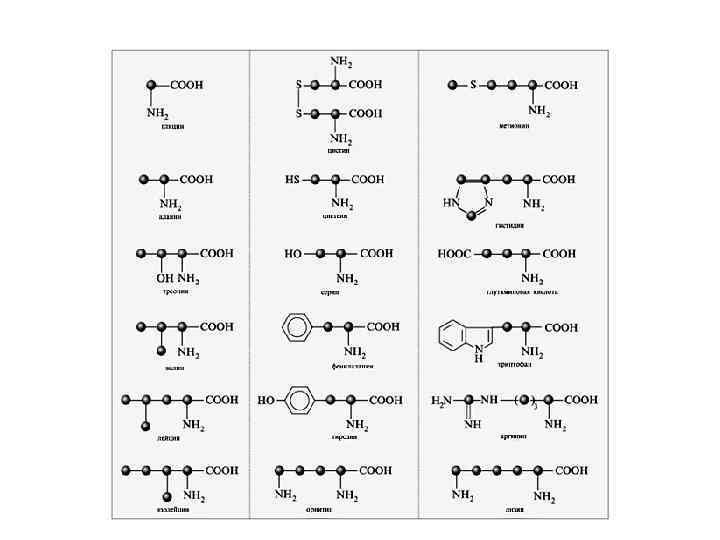
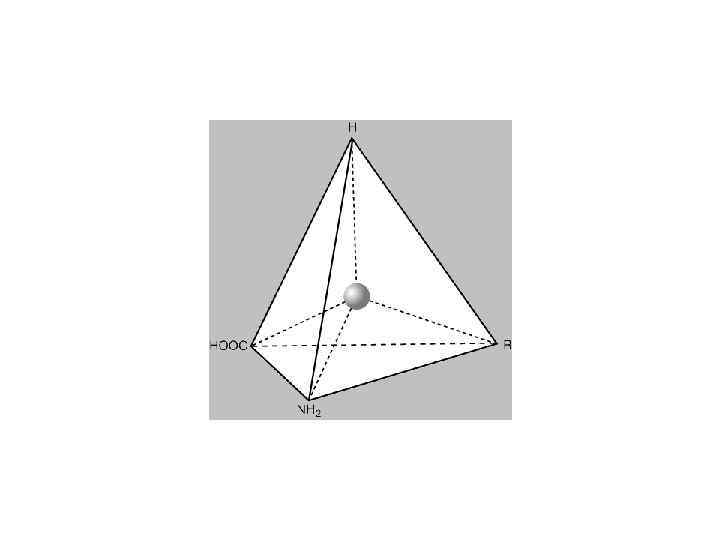
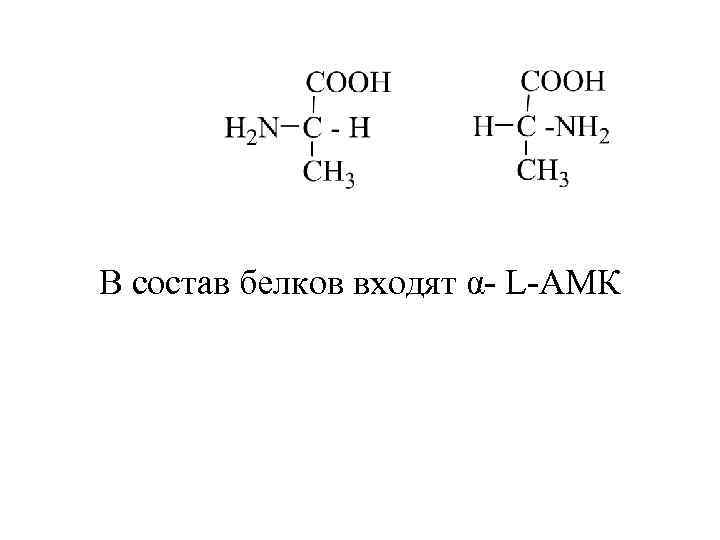
В состав белков входят α- L-АМК
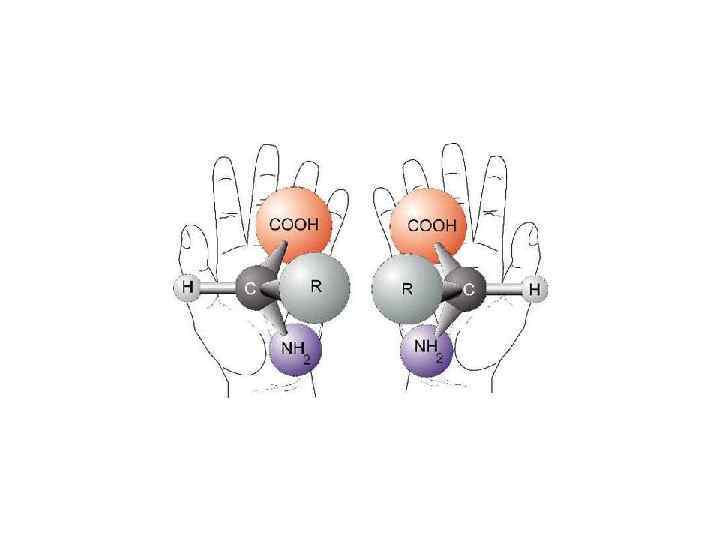

Химические свойства аминокислот • I. Амфотерные свойства аминокислот. • R-CH-COOH + HCl R-CH-COOH | | • NH 2 NH 3+Сl- • R-CH(NH 2)-COOH + Na. OH R-CH(NH 2)-COONa + H 2 O

II. Реакции аминокислот по карбоксильной группе 1. Образование внутрикомплексных солей –хелатов с катионами металлов

2. Образование сложных эфиров: АМК + спирт сложный эфир аминокислоты (катализатор сухой НСl). 3. Образование галогенангидридов: используется в синтезе пептидов как метод активации карбоксильной группы АМК + РOСl 3 галогенангидрид аминокислоты;

4. Реакции декарбоксилирования (триптофан→триптамин)

III. Реакции аминокислот по аминогруппе: 1. Взаимодействие с формальдегидом (альдегидами) R-CH-COOH + H 2 C=О NH 2 R-CH-COOH NH- CH 2 ОН карбиноламин данная реакция используется для количественного определения аминокислот (метод Серенсена).

2. Дезаминирование в организме-ферментативным путем, вне организма эта реакция применяется для количественного определения аминокислот (метод Ван–Слайка): R-CH-COOH + HNO 2 NH 2 R-CH-COOH + N 2 + H 2 O ОН

3. Ацилирование аминокислот ацетил-α-аминопропионовая кислота. Ацильные производные АМК широко используются при изучении последовательности их в белках и в синтезе пептидов (защита аминогруппы).

IV. Реакции, связанные с наличием и взаимным влиянием амино- и карбоксильной групп.
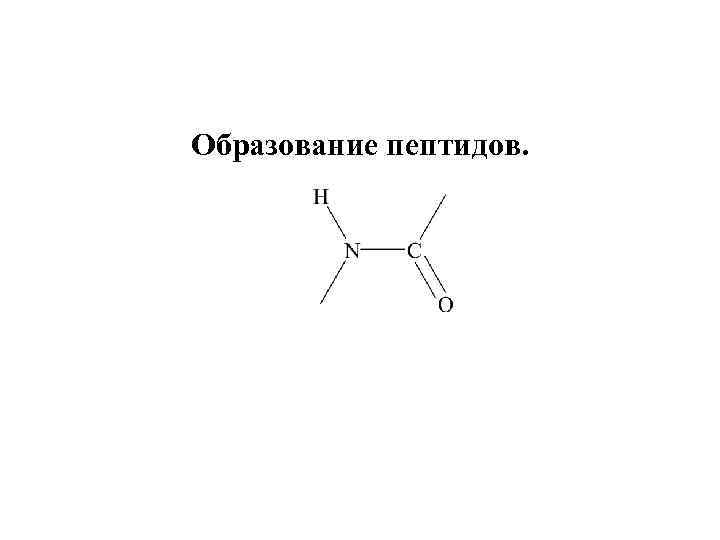
Образование пептидов.

Пептидная группа относится к р-, -сопряженной системе, в составе которой атомы С, О и N образуют -связи, которые лежат в одной плоскости. За счет образования единого делокализованного 4 -электронного облака вращение вокруг С-N связи затруднено. При этом -углеродные звенья находятся в выгодном транс-положении.
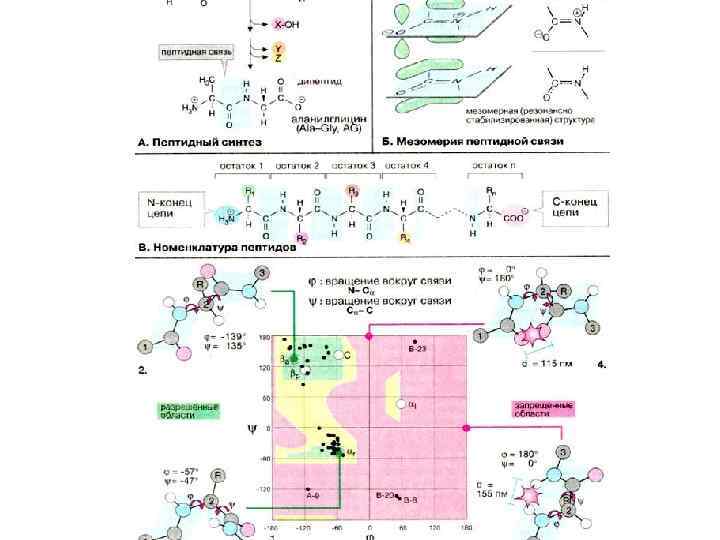

В зависимости от числа аминокислотных остатков в молекуле различают ди-, три-, тетрапептиды и т. д. вплоть до полипептидов (до 100 остатков АМК). Олигопептиды содержат от 2 до 10 остатков АМК, белки - более 100 остатков АМК.
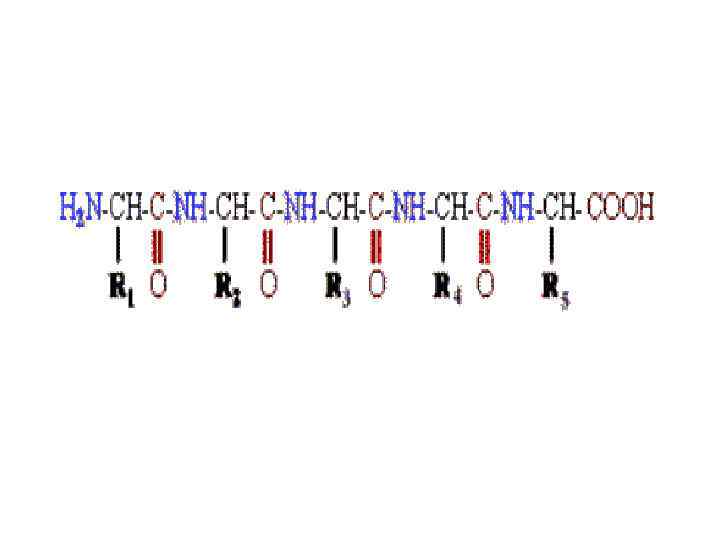

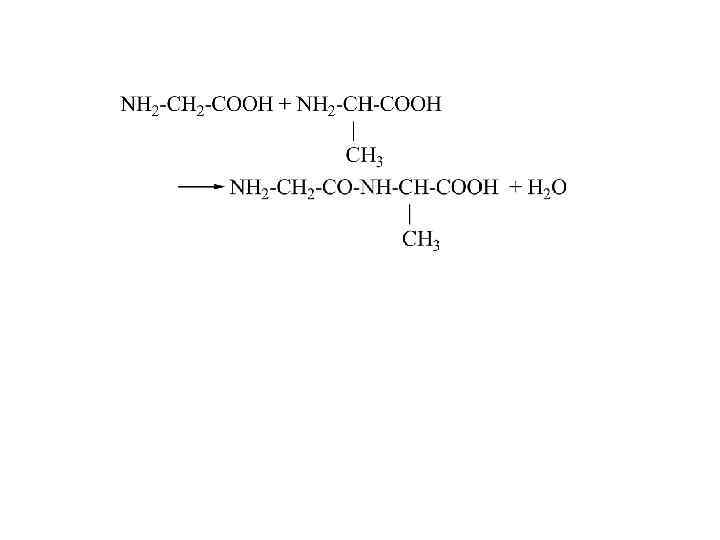
На концах аминокислотной цепочки находятся свободные амино- и карбоксильные группы, эти концы наз. N- и С-концами (нумеруют с N- конца). Из двух α-АМК глицина и аланина образуется дипептид глицилаланин (гли-ала):
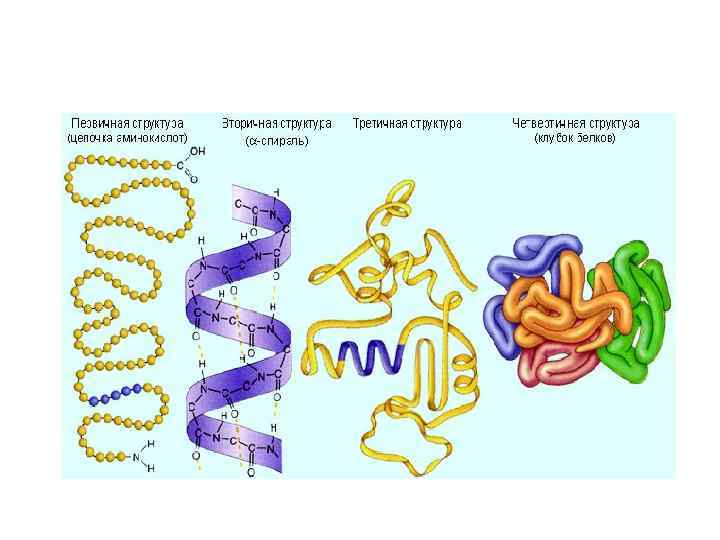
β-Структура полипептидных цепей.

В 1950 г. Полинг и Корни показали, что наиболее выгодной конформацией полипептидной цепи является правозакрученная -спираль. Основной вклад в закрепление этой конформации цепи вносят водородные связи, формирующиеся между параллельными участками пептидных групп. Известна другая вторичная структура белка: структура в виде складчатого листа.

Третичная структура — пространственное строение полипептидной цепи — взаимное расположение элементов вторичной структуры, стабилизированное взаимодействием между боковыми цепями аминокислотных остатков.

В стабилизации третичной структуры принимают участие: - ковалентные связи (между двумя цистеинами — дисульфидные мостики); - ионные (электростатические) взаимодействия (между противоположно заряженными аминокислотными остатками); - водородные связи; - гидрофобные взаимодействия.

По третичной структуре белки делят на: - глобулярные - для них характерна спиральная структура, уложенная в пространстве в виде сферы – глобулы (пр. яичный белок, фермент - глобин в составе гемоглобина); -фибриллярные - для них характерна структура. Как правило, эти белки имеют волокнистое строение и к ним относятся белки мышц, ткани - миоинозин, бетта - кератин волос.

Четвертичная структура – субъединичная структура белка. Взаимное расположение нескольких полипептидных цепей в составе единого белкового комплекса.

Слово «протеин» (белок) происходит от греческого «протейос» , что означает «занимающий первое место» . Все живое на земле содержит белки. Они составляют ≈50% сухого веса тела всех организмов. Белки - это биополимеры сложного строения, макромолекулы которых, состоят из остатков аминокислот, соединенных между собой амидной (пептидной) связью.

Роль белков в организме: 1. Строительная функция – создание опорных структур – важные структурные белки: коллаген в соединительной ткани, кератин в волосах, ногтях, коже, эластин в сосудистой стенке, мембраны клеток в комплексе с липидами. 2. Транспортная функция: белки крови переносят кислород, липиды и др.

3. Защитная функция: специфические белки иммуноглобулины синтезируются в ответ на поступление в организм бактерий, токсинов, вирусов. 4. Каталитическая функция: многие биологические катализаторы – ферменты по своей природе белки или полипептиды. 5. Гормональная функция: белки или полипептиды как гормоны выполняют функции регуляторов обмена веществ, регуляторов биологических функций.

6. Питательная функция: белки – один из источников энергии, резервные белки – источник питания для развития плода (белки яйца, белок молока – казеин), белки – источник АМК в организме.