Дисахариди.ppt
- Количество слайдов: 34
 ДИСАХАРИДИ Це вуглеводи, що під час гідролізу утворюють два однакових або неоднакових моносахариди Мальтоза + Н 2 О → 2α-D-глюкоза Лактоза + Н 2 О → β- D -галактоза + α-D-глюкоза Целобіоза + Н 2 О → 2 β-D-глюкоза Сахароза + Н 2 О → α-D-глюкоза +β-D-фруктоза Трегалоза + Н 2 О → 2α-D-глюкоза
ДИСАХАРИДИ Це вуглеводи, що під час гідролізу утворюють два однакових або неоднакових моносахариди Мальтоза + Н 2 О → 2α-D-глюкоза Лактоза + Н 2 О → β- D -галактоза + α-D-глюкоза Целобіоза + Н 2 О → 2 β-D-глюкоза Сахароза + Н 2 О → α-D-глюкоза +β-D-фруктоза Трегалоза + Н 2 О → 2α-D-глюкоза
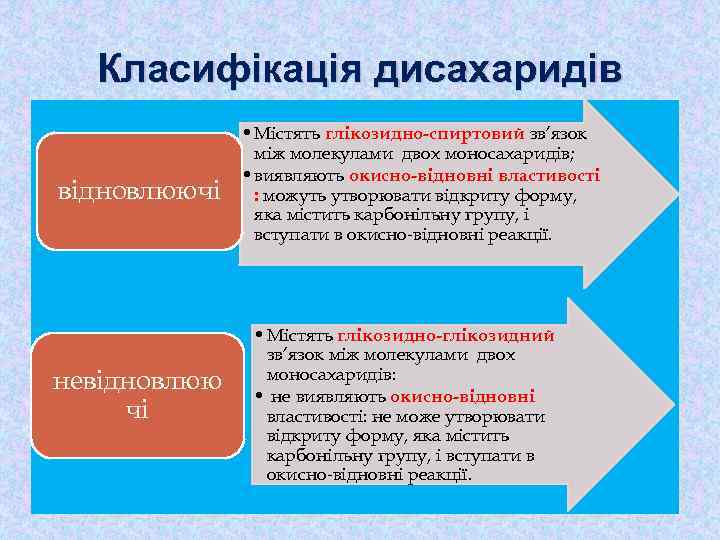 Класифікація дисахаридів відновлюючі невідновлюю чі • Містять глікозидно-спиртовий зв’язок між молекулами двох моносахаридів; • виявляють окисно-відновні властивості : можуть утворювати відкриту форму, яка містить карбонільну групу, і вступати в окисно-відновні реакції. • Містять глікозидно-глікозидний зв’язок між молекулами двох моносахаридів: • не виявляють окисно-відновні властивості: не може утворювати відкриту форму, яка містить карбонільну групу, і вступати в окисно-відновні реакції.
Класифікація дисахаридів відновлюючі невідновлюю чі • Містять глікозидно-спиртовий зв’язок між молекулами двох моносахаридів; • виявляють окисно-відновні властивості : можуть утворювати відкриту форму, яка містить карбонільну групу, і вступати в окисно-відновні реакції. • Містять глікозидно-глікозидний зв’язок між молекулами двох моносахаридів: • не виявляють окисно-відновні властивості: не може утворювати відкриту форму, яка містить карбонільну групу, і вступати в окисно-відновні реакції.
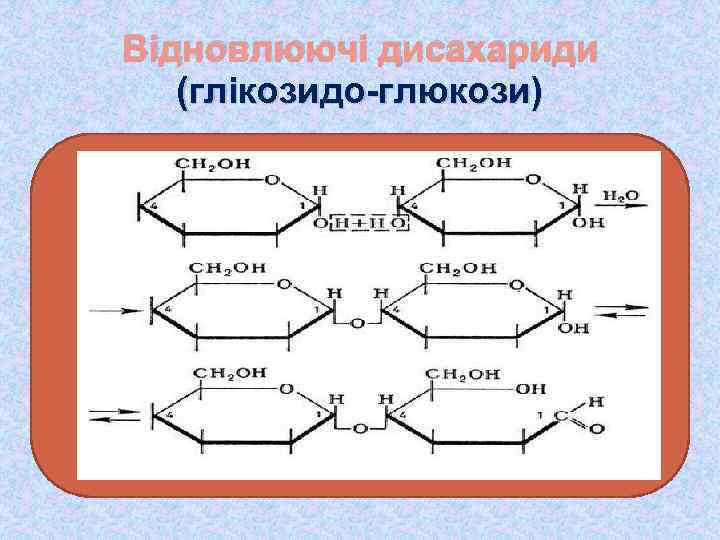 Відновлюючі дисахариди (глікозидо-глюкози)
Відновлюючі дисахариди (глікозидо-глюкози)
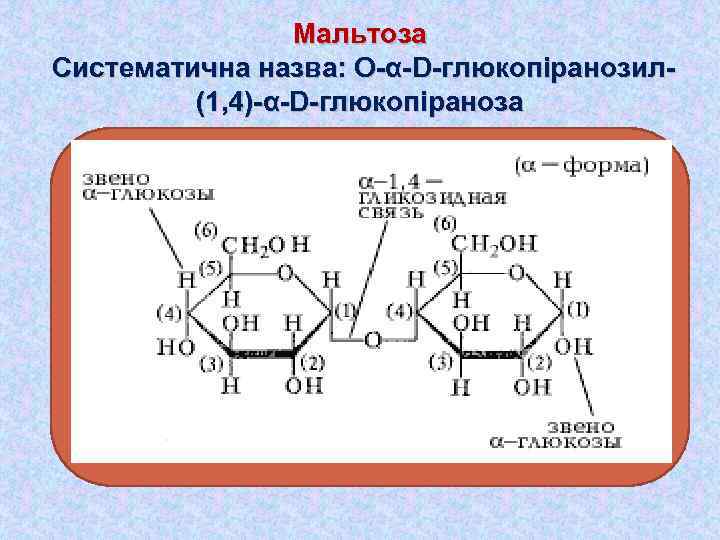 Мальтоза Систематична назва: О-α-D-глюкопіранозил(1, 4)-α-D-глюкопіраноза
Мальтоза Систематична назва: О-α-D-глюкопіранозил(1, 4)-α-D-глюкопіраноза
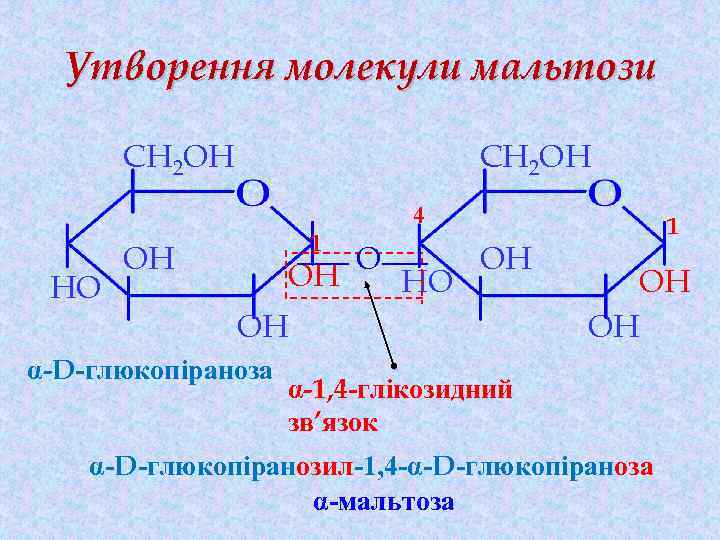 Утворення молекули мальтози CH 2 OH 4 HO 1 OH OH O HO OH OH α-D-глюкопіраноза 1 OH OH α-1, 4 -глікозидний зв’язок α-D-глюкопіранозил-1, 4 -α-D-глюкопіраноза α-мальтоза
Утворення молекули мальтози CH 2 OH 4 HO 1 OH OH O HO OH OH α-D-глюкопіраноза 1 OH OH α-1, 4 -глікозидний зв’язок α-D-глюкопіранозил-1, 4 -α-D-глюкопіраноза α-мальтоза
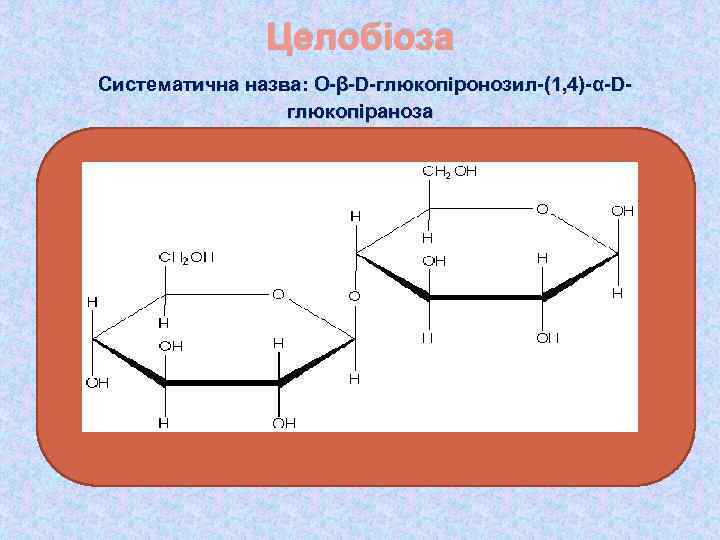 Целобіоза Систематична назва: О-β-D-глюкопіронозил-(1, 4)-α-Dглюкопіраноза
Целобіоза Систематична назва: О-β-D-глюкопіронозил-(1, 4)-α-Dглюкопіраноза
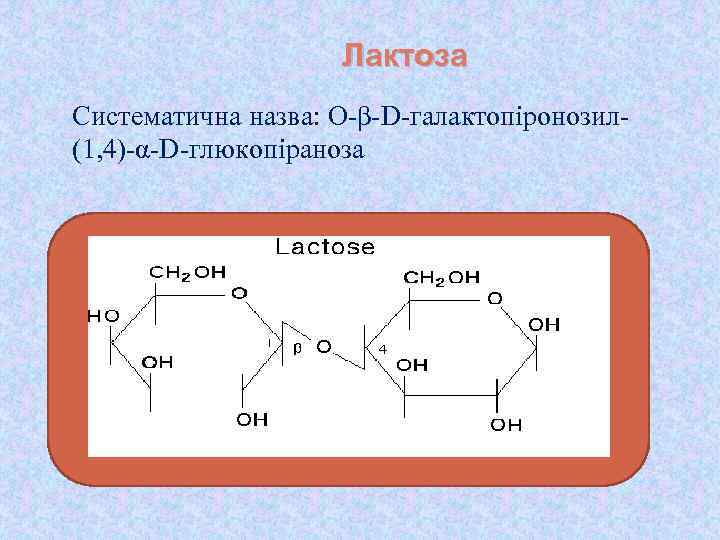 Лактоза Систематична назва: О-β-D-галактопіронозил(1, 4)-α-D-глюкопіраноза
Лактоза Систематична назва: О-β-D-галактопіронозил(1, 4)-α-D-глюкопіраноза
 Хімічні властивості відновлюючих дисахаридів 1. Реакція у воді : - утворення відкритого ланцюга, - встановлення рівноваги оксо-циклічної таутомерії між (α-)альфа- і (β-)бета-аномерами; - з’явлення вільної альдегідної групи
Хімічні властивості відновлюючих дисахаридів 1. Реакція у воді : - утворення відкритого ланцюга, - встановлення рівноваги оксо-циклічної таутомерії між (α-)альфа- і (β-)бета-аномерами; - з’явлення вільної альдегідної групи
 CH 2 OH O HO H O OH OH α-мальтоза OH OH оксо-таутомер мальтози
CH 2 OH O HO H O OH OH α-мальтоза OH OH оксо-таутомер мальтози
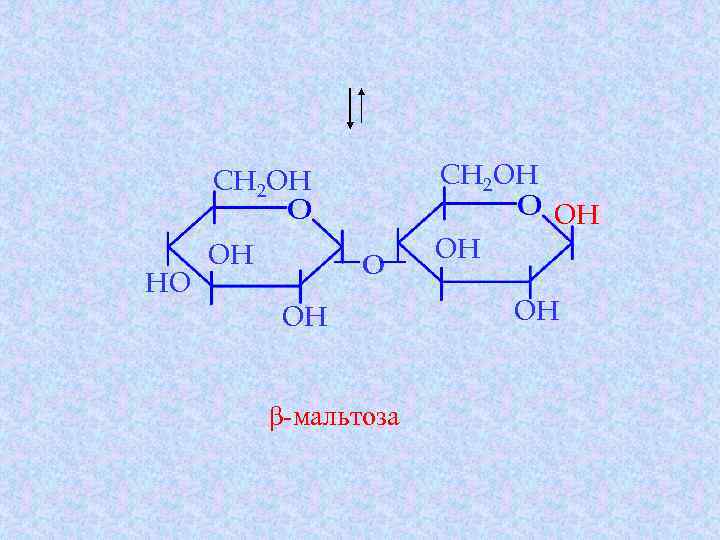 CH 2 OH HO CH 2 OH OH OH O OH β-мальтоза OH OH
CH 2 OH HO CH 2 OH OH OH O OH β-мальтоза OH OH
 Хімічні властивості відновлюючих дисахаридів 2. Реакції окиснення з реактивом Толенса та реактивом Фелінга : перебігають за вільною альдегідною групою з утворенням продукта окиснення – глікобіонових кислот –
Хімічні властивості відновлюючих дисахаридів 2. Реакції окиснення з реактивом Толенса та реактивом Фелінга : перебігають за вільною альдегідною групою з утворенням продукта окиснення – глікобіонових кислот –
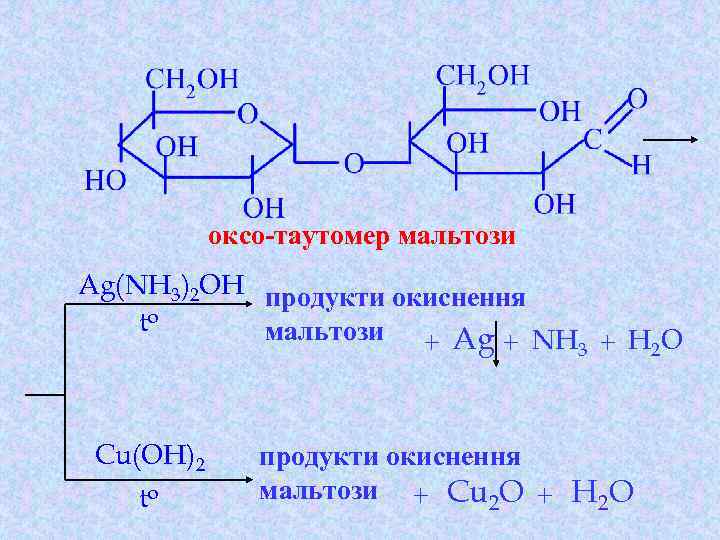 оксо-таутомер мальтози Ag(NH 3)2 OH продукти окиснення to мальтози + Ag + NH + H O 3 2 Cu(OH)2 to продукти окиснення мальтози + Cu 2 O + H 2 O
оксо-таутомер мальтози Ag(NH 3)2 OH продукти окиснення to мальтози + Ag + NH + H O 3 2 Cu(OH)2 to продукти окиснення мальтози + Cu 2 O + H 2 O
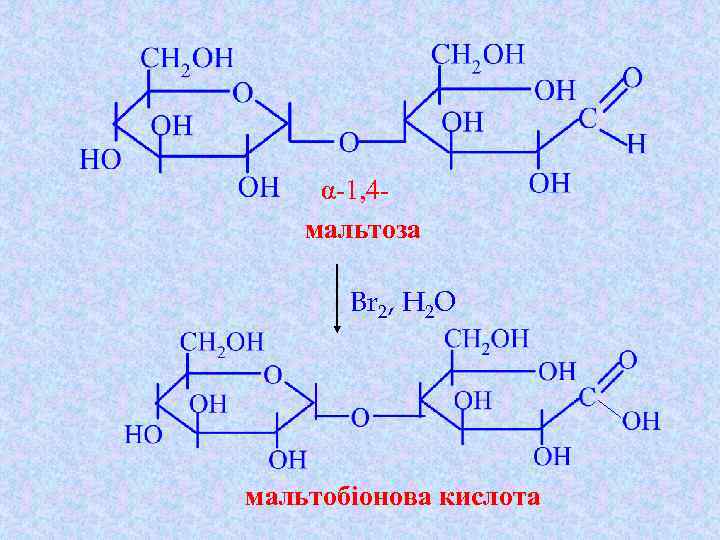 α-1, 4 мальтоза Br 2, H 2 O мальтобіонова кислота
α-1, 4 мальтоза Br 2, H 2 O мальтобіонова кислота
 Хімічні властивості відновлюючих дисахаридів 3. Утворення глікозидів за участю напівацетального гідроксилу дисахариду: метилювання у кислому середовищі
Хімічні властивості відновлюючих дисахаридів 3. Утворення глікозидів за участю напівацетального гідроксилу дисахариду: метилювання у кислому середовищі
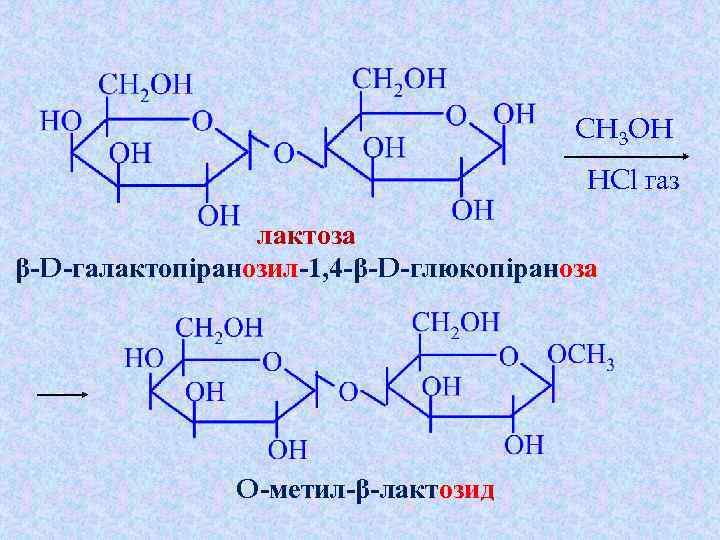 CH 3 OH HCl газ лактоза β-D-галактопіранозил-1, 4 -β-D-глюкопіраноза O-метил-β-лактозид
CH 3 OH HCl газ лактоза β-D-галактопіранозил-1, 4 -β-D-глюкопіраноза O-метил-β-лактозид
 Хімічні властивості відновлюючих дисахаридів 4. Реакція алкілювання (синтез поліетерів): Утворення простих і складних ефірів за участю всіх гідроксильних груп циклічних форм дисахариду, аналогічно моносахаридам
Хімічні властивості відновлюючих дисахаридів 4. Реакція алкілювання (синтез поліетерів): Утворення простих і складних ефірів за участю всіх гідроксильних груп циклічних форм дисахариду, аналогічно моносахаридам
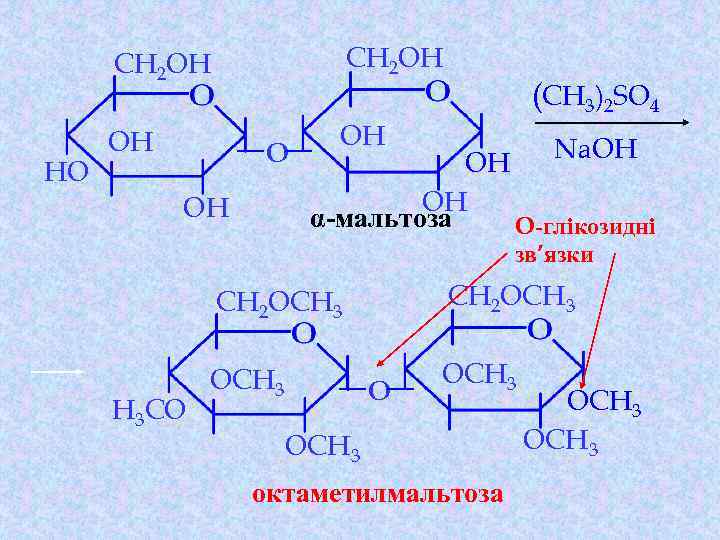 CH 2 OH HO CH 2 OH OH OH O OH (CH 3)2 SO 4 Na. OH OH OH α-мальтоза O-глікозидні зв’язки CH 2 OCH 3 H 3 CO CH 2 OCH 3 O OCH 3 октаметилмальтоза OCH 3
CH 2 OH HO CH 2 OH OH OH O OH (CH 3)2 SO 4 Na. OH OH OH α-мальтоза O-глікозидні зв’язки CH 2 OCH 3 H 3 CO CH 2 OCH 3 O OCH 3 октаметилмальтоза OCH 3
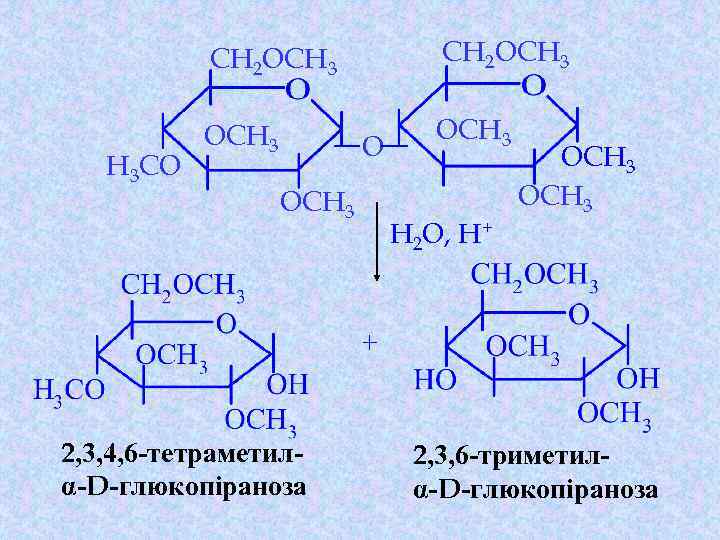 CH 2 OCH 3 H 3 CO CH 2 OCH 3 O OCH 3 H 2 O, H+ OCH 3 + 2, 3, 4, 6 -тетраметилα-D-глюкопіраноза 2, 3, 6 -триметилα-D-глюкопіраноза
CH 2 OCH 3 H 3 CO CH 2 OCH 3 O OCH 3 H 2 O, H+ OCH 3 + 2, 3, 4, 6 -тетраметилα-D-глюкопіраноза 2, 3, 6 -триметилα-D-глюкопіраноза
 Хімічні властивості відновлюючих дисахаридів 5. Реакція ацилювання (синтез поліестерів):
Хімічні властивості відновлюючих дисахаридів 5. Реакція ацилювання (синтез поліестерів):
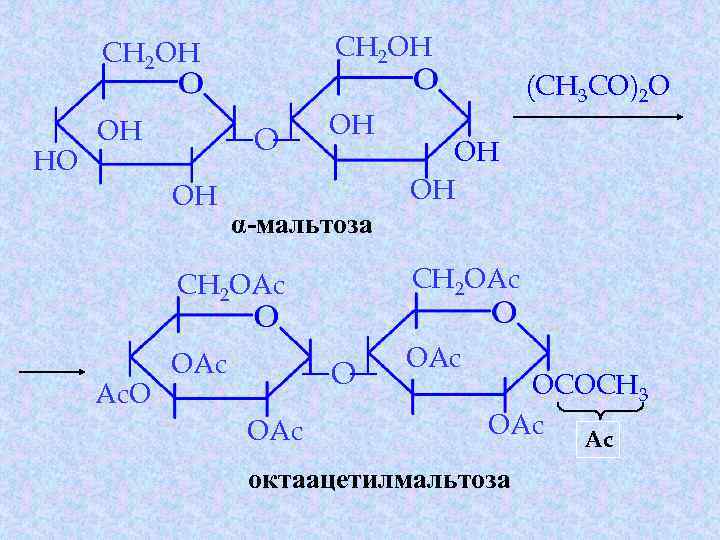 CH 2 OH HO CH 2 OH OH OH O OH (CH 3 CO)2 O OH OH α-мальтоза CH 2 OAc Ac. O CH 2 OAc OAc OCOCH 3 OAc Ac октаацетилмальтоза
CH 2 OH HO CH 2 OH OH OH O OH (CH 3 CO)2 O OH OH α-мальтоза CH 2 OAc Ac. O CH 2 OAc OAc OCOCH 3 OAc Ac октаацетилмальтоза
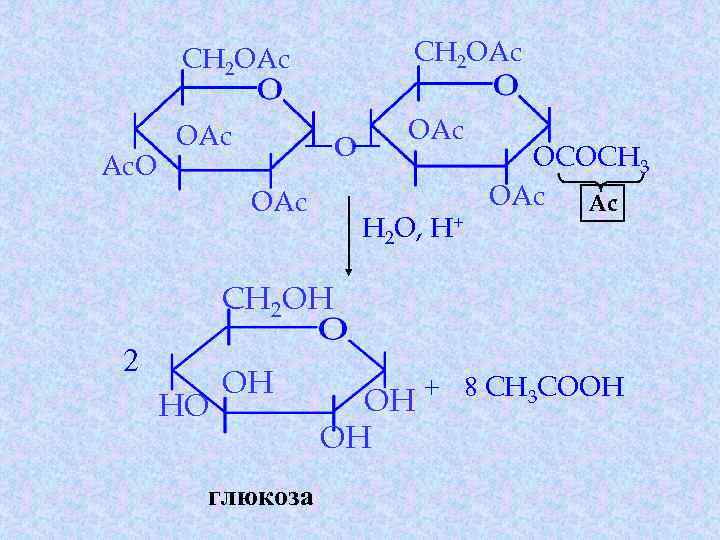 CH 2 OAc Ac. O CH 2 OAc OAc O OAc H 2 O, H+ OCOCH 3 OAc Ac CH 2 OH 2 HO OH глюкоза OH OH + 8 CH 3 COOH
CH 2 OAc Ac. O CH 2 OAc OAc O OAc H 2 O, H+ OCOCH 3 OAc Ac CH 2 OH 2 HO OH глюкоза OH OH + 8 CH 3 COOH
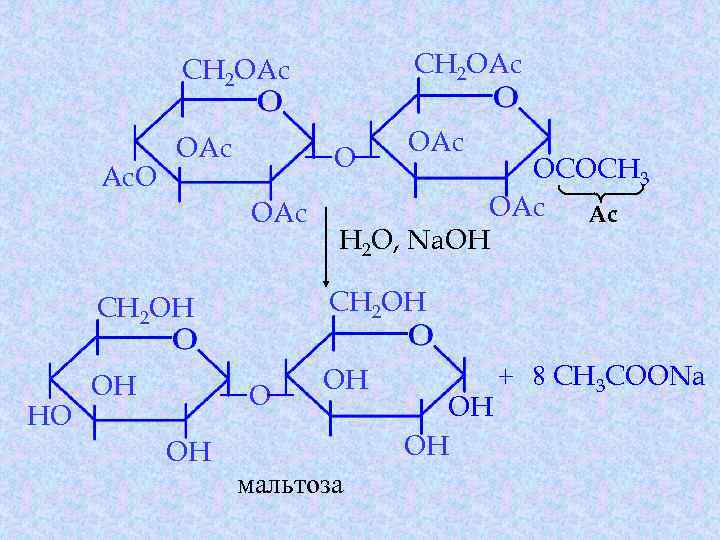 CH 2 OAc Ac. O CH 2 OAc OAc OCOCH 3 OAc Ac H 2 O, Na. OH CH 2 OH HO CH 2 OH OH OH O OH мальтоза OH OH + 8 CH 3 COONa
CH 2 OAc Ac. O CH 2 OAc OAc OCOCH 3 OAc Ac H 2 O, Na. OH CH 2 OH HO CH 2 OH OH OH O OH мальтоза OH OH + 8 CH 3 COONa
 Хімічні властивості відновлюючих дисахаридів 6. Гідроліз за наявності кислотних каталізаторів
Хімічні властивості відновлюючих дисахаридів 6. Гідроліз за наявності кислотних каталізаторів
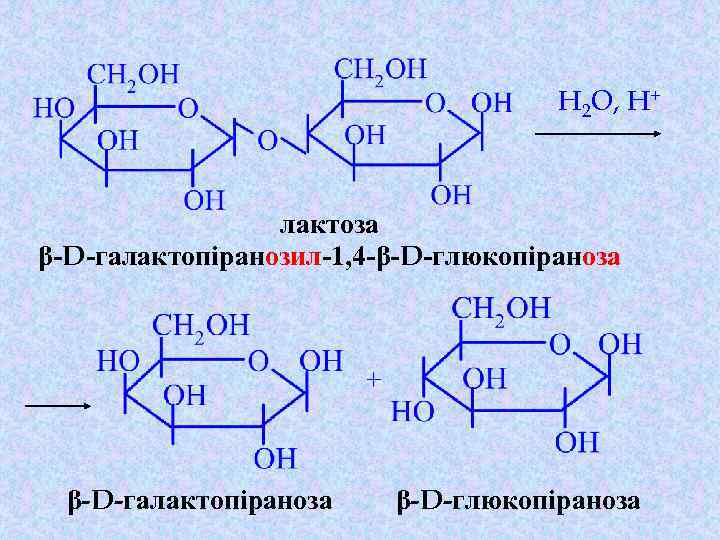 H 2 O, H+ лактоза β-D-галактопіранозил-1, 4 -β-D-глюкопіраноза + β-D-галактопіраноза β-D-глюкопіраноза
H 2 O, H+ лактоза β-D-галактопіранозил-1, 4 -β-D-глюкопіраноза + β-D-галактопіраноза β-D-глюкопіраноза
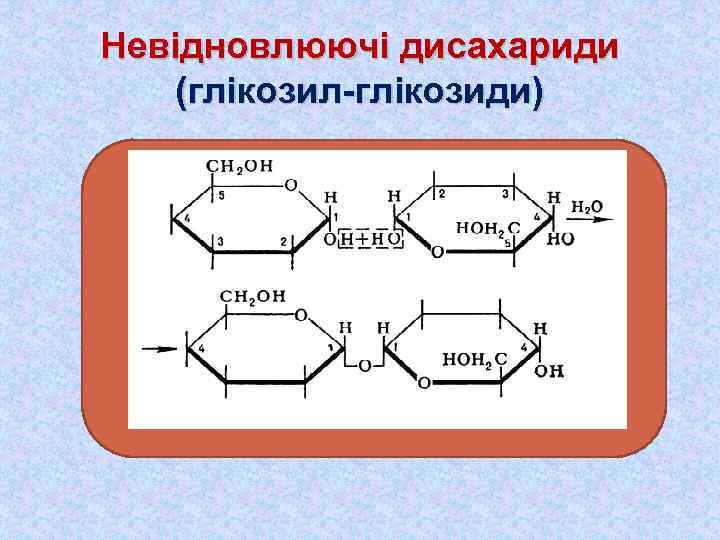 Невідновлюючі дисахариди (глікозил-глікозиди) Фізичні властивості
Невідновлюючі дисахариди (глікозил-глікозиди) Фізичні властивості
 Невідновлюючі дисахариди Не утворюють відкриту форму, тому не проявляють властивостей альдегідів і кетонів. Не проявляють відновлювальних властивостей — не реагують з реактивом Толенса і реактивом Фелінга. (Альдегідної групи в молекулі немає: при нагріванні з аміачним розчином Аргентум (І) оксиду не дають «срібного дзеркала» , при нагріванні з Купрум (II) гідроксидом не утворюють червоного оксиду Купруму (I). Наявність гідроксильних груп підтверджується реакцією з Купрум (ІІ) гідроксидом : (утворюється яскраво-синій розчин цукриту Купруму (ІІ)).
Невідновлюючі дисахариди Не утворюють відкриту форму, тому не проявляють властивостей альдегідів і кетонів. Не проявляють відновлювальних властивостей — не реагують з реактивом Толенса і реактивом Фелінга. (Альдегідної групи в молекулі немає: при нагріванні з аміачним розчином Аргентум (І) оксиду не дають «срібного дзеркала» , при нагріванні з Купрум (II) гідроксидом не утворюють червоного оксиду Купруму (I). Наявність гідроксильних груп підтверджується реакцією з Купрум (ІІ) гідроксидом : (утворюється яскраво-синій розчин цукриту Купруму (ІІ)).
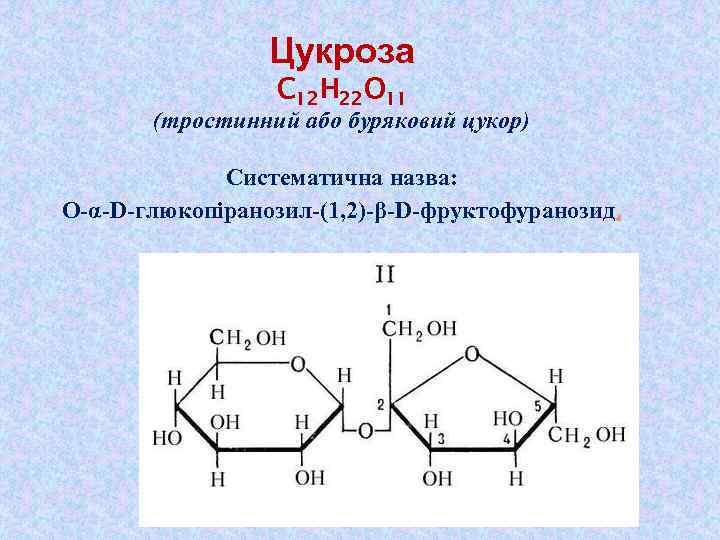 Цукроза C 12 H 22 O 11 (тростинний або буряковий цукор) Систематична назва: О-α-D-глюкопіранозил-(1, 2)-β-D-фруктофуранозид.
Цукроза C 12 H 22 O 11 (тростинний або буряковий цукор) Систематична назва: О-α-D-глюкопіранозил-(1, 2)-β-D-фруктофуранозид.
 Поширення Утворюється у клітинах зелених рослин під час фотосинтезу Нагромаджується в стеблах, насінні, плодах і коренях рослин Не синтезується в організмах тварин та людей Вміст в цукровому буряку складає 15 -22%, в цукровій тростині — 12 -15%. У кукурудзі — 1, 4 -1, 8%, картоплі — 0, 6 %, цибулі — 6, 5, моркві — 3, 5, дині — 5, 9 %, персиках і абрикосах — 6, 0, апельсинах — 3, 5 %, винограді — 0, 5%. Багато її в кленовому, пальмовому, березовому соку та в соку фруктів.
Поширення Утворюється у клітинах зелених рослин під час фотосинтезу Нагромаджується в стеблах, насінні, плодах і коренях рослин Не синтезується в організмах тварин та людей Вміст в цукровому буряку складає 15 -22%, в цукровій тростині — 12 -15%. У кукурудзі — 1, 4 -1, 8%, картоплі — 0, 6 %, цибулі — 6, 5, моркві — 3, 5, дині — 5, 9 %, персиках і абрикосах — 6, 0, апельсинах — 3, 5 %, винограді — 0, 5%. Багато її в кленовому, пальмовому, березовому соку та в соку фруктів.
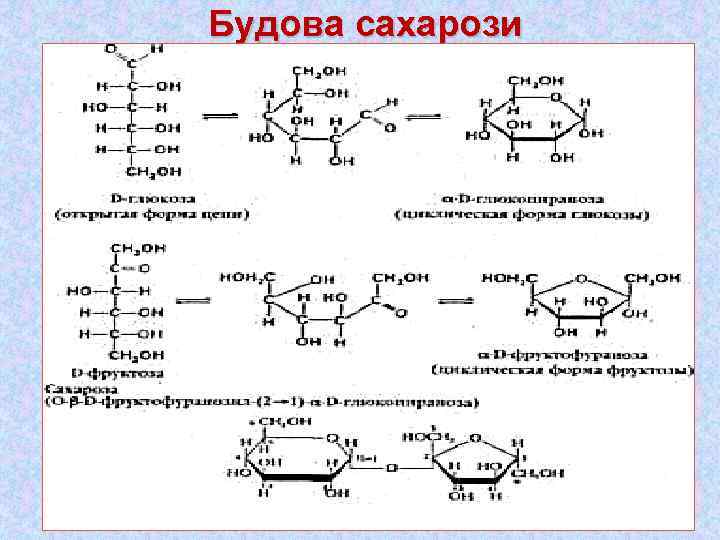 Будова сахарози Назва:
Будова сахарози Назва:
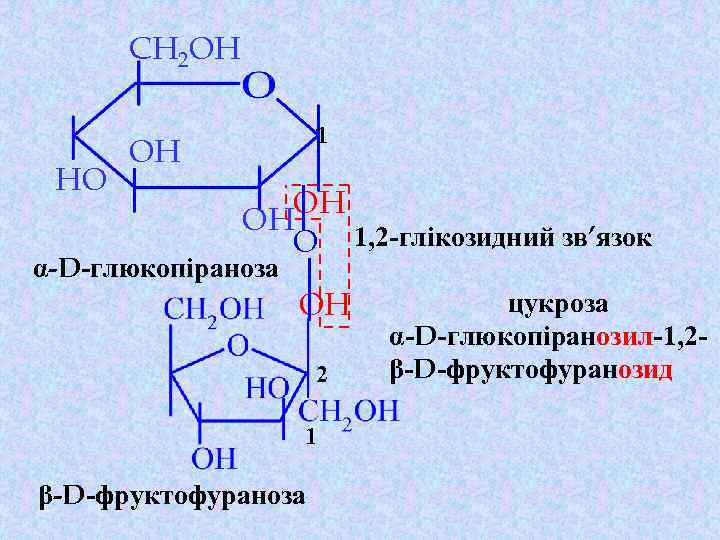 CH 2 OH HO 1 OH OH OH O 1, 2 -глікозидний зв’язок α-D-глюкопіраноза OH 2 1 β-D-фруктофураноза цукроза α-D-глюкопіранозил-1, 2β-D-фруктофуранозид
CH 2 OH HO 1 OH OH OH O 1, 2 -глікозидний зв’язок α-D-глюкопіраноза OH 2 1 β-D-фруктофураноза цукроза α-D-глюкопіранозил-1, 2β-D-фруктофуранозид
 Фізичні властивості Білий, без запаху, кристалічний порошок; Смак солодкуватий ; Кристали цукрози добре розчинні у воді, погано — у спиртах; При охолодженні рідким повітрям, після висвітлення яскравим світлом кристал цукрози фосфоресціює.
Фізичні властивості Білий, без запаху, кристалічний порошок; Смак солодкуватий ; Кристали цукрози добре розчинні у воді, погано — у спиртах; При охолодженні рідким повітрям, після висвітлення яскравим світлом кристал цукрози фосфоресціює.
 Кристалізується без води у вигляді великих моноклінічних кристалів; Вище температури плавлення карамелізується, перетворюючись у суміш складних продуктів: карамелана С 24 Н 36 О 18, карамелена С 36 Н 50 О 25 і інших, втрачаючи при цьому воду
Кристалізується без води у вигляді великих моноклінічних кристалів; Вище температури плавлення карамелізується, перетворюючись у суміш складних продуктів: карамелана С 24 Н 36 О 18, карамелена С 36 Н 50 О 25 і інших, втрачаючи при цьому воду
 Гідроліз сахарози Можливий під дією кислот (НCl, H 2 SO 4) і ферменту сахарази; З утворенням молекул глюкози і фруктози. Гідроліз цукрози отримав назву інверсії, а суміш утворюваних рівних кількостей глюкози і фруктози — інвертним цукром.
Гідроліз сахарози Можливий під дією кислот (НCl, H 2 SO 4) і ферменту сахарази; З утворенням молекул глюкози і фруктози. Гідроліз цукрози отримав назву інверсії, а суміш утворюваних рівних кількостей глюкози і фруктози — інвертним цукром.
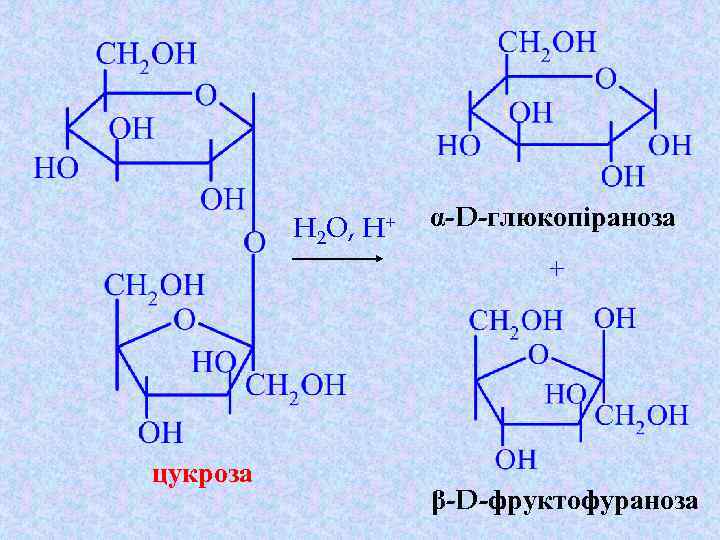 H 2 O, H+ α-D-глюкопіраноза + цукроза β-D-фруктофураноза
H 2 O, H+ α-D-глюкопіраноза + цукроза β-D-фруктофураноза


