Diferentsiyna_diagnostika_leykoizv_u_ditey.pptx
- Количество слайдов: 14
 Диференційна діагностика лейкозів у діетй ПІДГОТУВАВ СТУДЕНТ 31 ГР. VI КУРСКУ ЛОЗИНСЬКИЙ А.
Диференційна діагностика лейкозів у діетй ПІДГОТУВАВ СТУДЕНТ 31 ГР. VI КУРСКУ ЛОЗИНСЬКИЙ А.
 Лейкоз - онкологічне захворювання клітин крові, що уражає кістковий мозок і інші кровотворні органи. Основною ознакою лейкемії є велика пропорція лейкоцитів. Ці клітини, що дегенерували і втратили захисні функції нормальних лейкоцитів, знищують здорові клітини, після чого жертва стає беззахисною перед будь-якою інфекцією. Лікування проводиться за допомогою опромінення і цитотоксичних препаратів для придушення розмноження клітин, що дегенерували, або трансплантацією кісткового мозку. Критерієм діагнозу гострого лейкозу є визначення бластних клітин в кістковому мозку та, у певної кількості хворих, у крові. Діагноз встановлюється при наявності 30% і більше бластних клітин в мієлограмі. При знаходженні в мієлограмі менш ніж 30% (5 -30%) бластних клітин (виключенням є бластний криз хронічного мієлопроліферативного процесу та метастази гематосаркоми в кістковий мозок) виставляють діагноз гострого малопроцентного лейкозу, що згідно міжнародної FAB-класифікації гострих лейкозів, відповідає двом варіантам мієлодиспластичного синдрому (МДС). В цих випадках необхідно повторне неодноразове дослідження кісткового мозку, бажано з каріологічним аналізом, який дозволяє довести пухлинну природу проліферації. Ідентифікація основних форм гострого лейкозу базується на використанні як морфологічного методу, так і цитохімічних маркерних реакцій першого діагностиченого пунктату кісткового мозку. Морфологічні і цитохімічні особливості бластних клітин покладені в основу сучасної класифікації гострих лейкозів, яку запропонували групи французьких, американських та британських гематологів і яку коротко позначають як FAB-класифікація.
Лейкоз - онкологічне захворювання клітин крові, що уражає кістковий мозок і інші кровотворні органи. Основною ознакою лейкемії є велика пропорція лейкоцитів. Ці клітини, що дегенерували і втратили захисні функції нормальних лейкоцитів, знищують здорові клітини, після чого жертва стає беззахисною перед будь-якою інфекцією. Лікування проводиться за допомогою опромінення і цитотоксичних препаратів для придушення розмноження клітин, що дегенерували, або трансплантацією кісткового мозку. Критерієм діагнозу гострого лейкозу є визначення бластних клітин в кістковому мозку та, у певної кількості хворих, у крові. Діагноз встановлюється при наявності 30% і більше бластних клітин в мієлограмі. При знаходженні в мієлограмі менш ніж 30% (5 -30%) бластних клітин (виключенням є бластний криз хронічного мієлопроліферативного процесу та метастази гематосаркоми в кістковий мозок) виставляють діагноз гострого малопроцентного лейкозу, що згідно міжнародної FAB-класифікації гострих лейкозів, відповідає двом варіантам мієлодиспластичного синдрому (МДС). В цих випадках необхідно повторне неодноразове дослідження кісткового мозку, бажано з каріологічним аналізом, який дозволяє довести пухлинну природу проліферації. Ідентифікація основних форм гострого лейкозу базується на використанні як морфологічного методу, так і цитохімічних маркерних реакцій першого діагностиченого пунктату кісткового мозку. Морфологічні і цитохімічні особливості бластних клітин покладені в основу сучасної класифікації гострих лейкозів, яку запропонували групи французьких, американських та британських гематологів і яку коротко позначають як FAB-класифікація.
 FAB -КЛАСИФІКАЦІЯ ГОСТРИХ ЛЕЙКОЗІВ (1980) Група І – нелімфобластні мієлогенні (мієлоїдні) лейкози, що поділяються на 6 типів. Група ІІ – лімфобластні лейкози – 3 типи. Група ІІІ – мієлопоетичні дисплазії або мієлодиспластичний синдром (МДС) – 4 типи. Нелімфобластні гострі лейкози (ГНЛЛ) включають: М 1 – гострий мієлобластний лейкоз без ознак визрівання клітин – 20% випадків; М 2 – гострий мієлобластний лейкоз з ознаками визрівання клітин – 30% випадків; М 3 – гострий промієлоцитарний лейкоз – 8% випадків; М 3 м (підтип) – мікрогранулярний промієлоцитарний лейкоз – може бути ідентифікований тільки за допомогою електронної мікроскопії; М 4 - гострий мієлобластний (мієломоноцитарний) лейкоз – 28% випадків. М 5 – гострий монобластний (моноцитарний) лейкоз; М 5 А (підтип) – без дозрівання клітин; М 5 Б (підтип) – з частковим дозріванням клітин – 10% випадків; М 6 – гострий еритромієлоз (еритролейкемія, еритролейкоз) – 4% випадків; До цієї групи включений також гострий недиференційований лейкоз під індексом М о. Деякі автори доповнюють класифікацію варіантом М 7 – мегакаріобластним гострим лейкозом.
FAB -КЛАСИФІКАЦІЯ ГОСТРИХ ЛЕЙКОЗІВ (1980) Група І – нелімфобластні мієлогенні (мієлоїдні) лейкози, що поділяються на 6 типів. Група ІІ – лімфобластні лейкози – 3 типи. Група ІІІ – мієлопоетичні дисплазії або мієлодиспластичний синдром (МДС) – 4 типи. Нелімфобластні гострі лейкози (ГНЛЛ) включають: М 1 – гострий мієлобластний лейкоз без ознак визрівання клітин – 20% випадків; М 2 – гострий мієлобластний лейкоз з ознаками визрівання клітин – 30% випадків; М 3 – гострий промієлоцитарний лейкоз – 8% випадків; М 3 м (підтип) – мікрогранулярний промієлоцитарний лейкоз – може бути ідентифікований тільки за допомогою електронної мікроскопії; М 4 - гострий мієлобластний (мієломоноцитарний) лейкоз – 28% випадків. М 5 – гострий монобластний (моноцитарний) лейкоз; М 5 А (підтип) – без дозрівання клітин; М 5 Б (підтип) – з частковим дозріванням клітин – 10% випадків; М 6 – гострий еритромієлоз (еритролейкемія, еритролейкоз) – 4% випадків; До цієї групи включений також гострий недиференційований лейкоз під індексом М о. Деякі автори доповнюють класифікацію варіантом М 7 – мегакаріобластним гострим лейкозом.
 Лімфобластні гострі лейкози (ГЛЛ): Л 1 – гострий мікролімфобластний лейкоз (85% - у дітей, 5 -10% - у дорослих); Л 2 – гострий лімфобластний лейкоз (з типовими лімфобластами), частіше у дорослих; Л 3 – гострий макро- або пролімфобластний лейкоз (великі бласти з базофільною цитоплазмою); Найбільш благоприємним в прогностичному відношенні є Л 1 (найбльш високі показники частоти отримуваних ремісій і тривалості безрецидивної виживаємості). Цитохімічно всі ГЛЛ є негативними на мієлопероксидазу, судан чорний (покраска на ліпіди), хлорацетатестеразу і альфа-нафтилестеразу. Найбільш характерною для ГЛЛ є виражена реакція на глікоген у вигляді концентрованих накопичень навколо ядра лімфобласту його грубих гранул PAS-реакція в глибчатій формі. Імунологічні варіанти гострого лімфобластного лейкозу: Гострий Т-бластний лейкоз (Т-ГЛЛ); Гострий О-бластний лейкоз (О-ГЛЛ); Гострий В-бластний лейкоз (В-ГЛЛ). ГНЛ- гострий недиференційований лейкоз подібний до ГЛЛ. Стадії перебігу гострого лейкозу (ГЛ): І стадія – перша атака ГЛ; ІІ стадія – ремісія ГЛ; ІІІ стадія – рецидив ГЛ; IV стадія – термінальна.
Лімфобластні гострі лейкози (ГЛЛ): Л 1 – гострий мікролімфобластний лейкоз (85% - у дітей, 5 -10% - у дорослих); Л 2 – гострий лімфобластний лейкоз (з типовими лімфобластами), частіше у дорослих; Л 3 – гострий макро- або пролімфобластний лейкоз (великі бласти з базофільною цитоплазмою); Найбільш благоприємним в прогностичному відношенні є Л 1 (найбльш високі показники частоти отримуваних ремісій і тривалості безрецидивної виживаємості). Цитохімічно всі ГЛЛ є негативними на мієлопероксидазу, судан чорний (покраска на ліпіди), хлорацетатестеразу і альфа-нафтилестеразу. Найбільш характерною для ГЛЛ є виражена реакція на глікоген у вигляді концентрованих накопичень навколо ядра лімфобласту його грубих гранул PAS-реакція в глибчатій формі. Імунологічні варіанти гострого лімфобластного лейкозу: Гострий Т-бластний лейкоз (Т-ГЛЛ); Гострий О-бластний лейкоз (О-ГЛЛ); Гострий В-бластний лейкоз (В-ГЛЛ). ГНЛ- гострий недиференційований лейкоз подібний до ГЛЛ. Стадії перебігу гострого лейкозу (ГЛ): І стадія – перша атака ГЛ; ІІ стадія – ремісія ГЛ; ІІІ стадія – рецидив ГЛ; IV стадія – термінальна.
 КЛІНІКО-МОРФОЛОГІЧНА ДИФЕРЕНЦІАЦІЯ ГОСТРИХ ЛЕЙКОЗІВ
КЛІНІКО-МОРФОЛОГІЧНА ДИФЕРЕНЦІАЦІЯ ГОСТРИХ ЛЕЙКОЗІВ
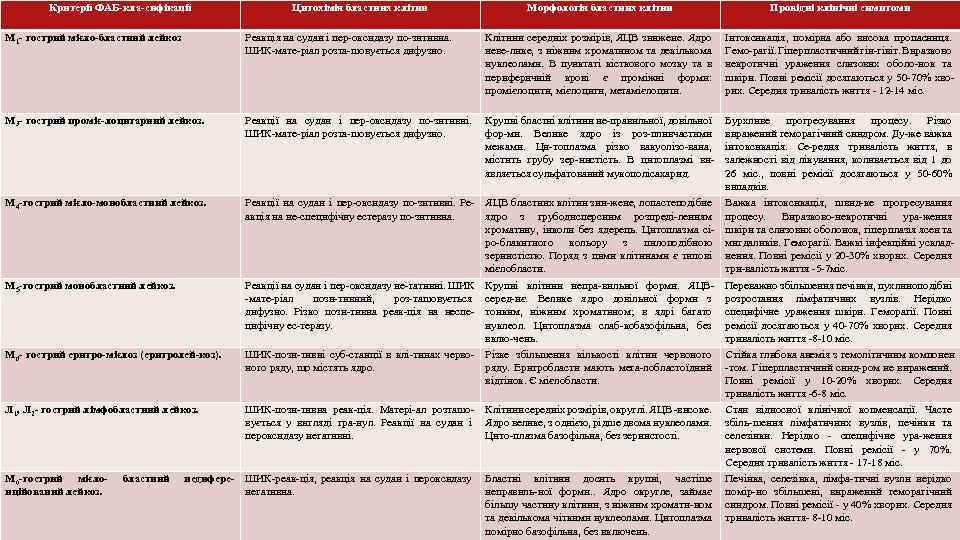 Критерії ФАБ-кла-сифікації Цитохімія бластних клітин Морфологія бластних клітин Провідні клінічні симптоми Клітини середніх розмірів, ЯЦВ знижене. Ядро неве-лике, з ніжним хроматином та декількома нуклеолами. В пунктаті кісткового мозку та в периферичній крові є проміжні форми: промієлоцити, метамієлоцити. Інтоксикація, помірна або висока пропасниця. Гемо-рагії. Гіперпластичний гін-гівіт. Виразково некротичні ураження слизових оболо-нок та шкіри. Повні ремісії досягаються у 50 -70% хворих. Середня тривалість життя - 12 -14 міс. М 1 - гострий мієло-бластний лейкоз Реакція на судан і пер-оксидазу по-зитивна. ШИК-мате-ріал розта-шовується дифузно. М 3 - гострий проміє-лоцитарний лейкоз. Реакції на судан і пер-оксидазу по-зитивні. Крупні бластні клітини не-правильної, довільної Бурхливе прогресування процесу. Різко ШИК-мате-ріал розта-шовується дифузно. фор-ми. Велике ядро із роз-пливчастими виражений геморагічний синдром. Ду-же важка межами. Ци-топлазма різко вакуолізо-вана, інтоксикація. Се-редня тривалість життя, в містить грубу зер-нистість. В цитоплазмі ви- залежності від лікування, коливається від 1 до являється сульфатований мукополісахарид. 26 міс. , повні ремісії досягаються у 50 -60% випадків. М 4 -гострий мієло-монобластний лейкоз. Реакції на судан і пер-оксидазу по-зитивні. Ре- ЯЦВ бластних клітин зни-жене, лопастеподібне Важка інтоксикація, швид-ке прогресування акція на не-специфічну естеразу по-зитивна. ядро з грубодисперсним розпреді-ленням процесу. Виразково-некротичні ура-ження хроматину, інколи без ядерець. Цитоплазма сі- шкіри та слизових оболонок, гіперплазія ясен та ро-блакитного кольору з пилоподібною мигдаликів. Геморагії. Важкі інфекційні ускладзернистістю. Поряд з цими клітинами є типові нення. Повні ремісії у 20 -30% хворих. Середня мієлобласти. три-валість життя -5 -7 міс. М 5 -гострий монобластний лейкоз. Реакції на судан і пер-оксидазу не-гативні. ШИК -мате-ріал пози-тивний, роз-ташовується дифузно. Різко пози-тивна реак-ція на неспецифічну ес-теразу. М 6 - гострий еритро-мієлоз (еритролей-коз). Л 1, Л 2 - гострий лімфобластний лейкоз. М 0 -гострий мієло- нційований лейкоз. бластний Крупні клітини непра-вильної форми. ЯЦВсеред-нє. Велике ядро довільної форми з тонким, ніжним хроматином; в ядрі багато нуклеол. Цитоплазма слаб-кобазофільна, без вклю-чень. ШИК-пози-тивні суб-станції в клі-тинах черво- Різке збільшення кількості клітин червоного ряду, що містять ядро. ряду. Еритробласти мають мега-лобластоїдний відтінок. Є мієлобласти. ШИК-пози-тивна реак-ція. Матері-ал розташо- Клітини середніх розмірів, округлі. ЯЦВ -високе. вується у вигляді гра-нул. Реакції на судан і Ядро велике, з однією, рідше двома нуклеолами. пероксидазу негативні. Цито-плазма базофільна, без зернистості. недифере- ШИК-реак-ція, реакція на судан і пероксидазу Бластні клітини досить крупні, частіше негативна. неправиль-ної форми. . Ядро округле, займає більшу частину клітини, з ніжним хромати-ном та декількома чіткими нуклеолами. Цитоплазма помірно базофільна, без включень. Переважно збільшення печінки, пухлиноподібні розростання лімфатичних вузлів. Нерідко специфічне ураження шкіри. Геморагії. Повні ремісії досягаються у 40 -70% хворих. Середня тривалість життя -8 -10 міс. Стійка глибока анемія з гемолітичним компонен -том. Гіперпластичний синд-ром не виражений. Повні ремісії у 10 -20% хворих. Середня тривалість життя -6 -8 міс. Стан відносної клінічної копменсації. Часте збіль-шення лімфатичних вузлів, печінки та селезінки. Нерідко - специфічне ура-ження нервової системи. Повні ремісії - у 70%. Середня тривалість життя - 17 -18 міс. Печінка, селезінка, лімфа-тичні вузли нерідко помір-но збільшені, виражений геморагічний синдром. Повні ремісії - у 40% хворих. Середня тривалість життя- 8 -10 міс.
Критерії ФАБ-кла-сифікації Цитохімія бластних клітин Морфологія бластних клітин Провідні клінічні симптоми Клітини середніх розмірів, ЯЦВ знижене. Ядро неве-лике, з ніжним хроматином та декількома нуклеолами. В пунктаті кісткового мозку та в периферичній крові є проміжні форми: промієлоцити, метамієлоцити. Інтоксикація, помірна або висока пропасниця. Гемо-рагії. Гіперпластичний гін-гівіт. Виразково некротичні ураження слизових оболо-нок та шкіри. Повні ремісії досягаються у 50 -70% хворих. Середня тривалість життя - 12 -14 міс. М 1 - гострий мієло-бластний лейкоз Реакція на судан і пер-оксидазу по-зитивна. ШИК-мате-ріал розта-шовується дифузно. М 3 - гострий проміє-лоцитарний лейкоз. Реакції на судан і пер-оксидазу по-зитивні. Крупні бластні клітини не-правильної, довільної Бурхливе прогресування процесу. Різко ШИК-мате-ріал розта-шовується дифузно. фор-ми. Велике ядро із роз-пливчастими виражений геморагічний синдром. Ду-же важка межами. Ци-топлазма різко вакуолізо-вана, інтоксикація. Се-редня тривалість життя, в містить грубу зер-нистість. В цитоплазмі ви- залежності від лікування, коливається від 1 до являється сульфатований мукополісахарид. 26 міс. , повні ремісії досягаються у 50 -60% випадків. М 4 -гострий мієло-монобластний лейкоз. Реакції на судан і пер-оксидазу по-зитивні. Ре- ЯЦВ бластних клітин зни-жене, лопастеподібне Важка інтоксикація, швид-ке прогресування акція на не-специфічну естеразу по-зитивна. ядро з грубодисперсним розпреді-ленням процесу. Виразково-некротичні ура-ження хроматину, інколи без ядерець. Цитоплазма сі- шкіри та слизових оболонок, гіперплазія ясен та ро-блакитного кольору з пилоподібною мигдаликів. Геморагії. Важкі інфекційні ускладзернистістю. Поряд з цими клітинами є типові нення. Повні ремісії у 20 -30% хворих. Середня мієлобласти. три-валість життя -5 -7 міс. М 5 -гострий монобластний лейкоз. Реакції на судан і пер-оксидазу не-гативні. ШИК -мате-ріал пози-тивний, роз-ташовується дифузно. Різко пози-тивна реак-ція на неспецифічну ес-теразу. М 6 - гострий еритро-мієлоз (еритролей-коз). Л 1, Л 2 - гострий лімфобластний лейкоз. М 0 -гострий мієло- нційований лейкоз. бластний Крупні клітини непра-вильної форми. ЯЦВсеред-нє. Велике ядро довільної форми з тонким, ніжним хроматином; в ядрі багато нуклеол. Цитоплазма слаб-кобазофільна, без вклю-чень. ШИК-пози-тивні суб-станції в клі-тинах черво- Різке збільшення кількості клітин червоного ряду, що містять ядро. ряду. Еритробласти мають мега-лобластоїдний відтінок. Є мієлобласти. ШИК-пози-тивна реак-ція. Матері-ал розташо- Клітини середніх розмірів, округлі. ЯЦВ -високе. вується у вигляді гра-нул. Реакції на судан і Ядро велике, з однією, рідше двома нуклеолами. пероксидазу негативні. Цито-плазма базофільна, без зернистості. недифере- ШИК-реак-ція, реакція на судан і пероксидазу Бластні клітини досить крупні, частіше негативна. неправиль-ної форми. . Ядро округле, займає більшу частину клітини, з ніжним хромати-ном та декількома чіткими нуклеолами. Цитоплазма помірно базофільна, без включень. Переважно збільшення печінки, пухлиноподібні розростання лімфатичних вузлів. Нерідко специфічне ураження шкіри. Геморагії. Повні ремісії досягаються у 40 -70% хворих. Середня тривалість життя -8 -10 міс. Стійка глибока анемія з гемолітичним компонен -том. Гіперпластичний синд-ром не виражений. Повні ремісії у 10 -20% хворих. Середня тривалість життя -6 -8 міс. Стан відносної клінічної копменсації. Часте збіль-шення лімфатичних вузлів, печінки та селезінки. Нерідко - специфічне ура-ження нервової системи. Повні ремісії - у 70%. Середня тривалість життя - 17 -18 міс. Печінка, селезінка, лімфа-тичні вузли нерідко помір-но збільшені, виражений геморагічний синдром. Повні ремісії - у 40% хворих. Середня тривалість життя- 8 -10 міс.
 Лікування гострого нелімфобластного лейкозу Програма “ 7+3” Індукція ремісії. Для індукції ремісії використовується цитозар у дозі 100 мг/м 2 в день (при інфузійному безперервному введенні) протягом 7 днів чи у дозі 100 мг/м 2 кожні 12 годин протягом 7 днів; рубоміцин у дозі 45 мг/м 2 (для осіб молодше 60 років) чи 30 мг/м 2 (для осіб старше 60 років) внутрішньовенно протягом 3 днів. За курсами індукції ремісії (не менше 2 курсів) слідує курс консолідації ремісії. Консолідація ремісії проводиться трьома курсами. Перший курс консолідації проводиться по тій же схемі, що і курс індукції ремісії. Другий курс консолідації проводиться за допомогою цитозара, що вводиться у дозі 3 г/м 2 кожні 12 годин для осіб молодше 50 років і 2 г/м 2 кожні 12 годин в день для осіб старше 50 років протягом 3 днів. Третій курс консолідації ремісії проводиться так як перший. Інтервал між курсами консолідації залежить відновлення гранулоцитів до 1 х10 9/л і тромбоцитів до 100 х109/л. Терапія підтримання ремісії проводиться по загальній для всіх програм схемі. Профілактика і лікування нейролейкемії обов’язкова при всіх варіантах гострого лейкозу. В один з перших днів діагностики гострого лейкозу проводиться перша діагностична люмбальна пункція, під час якої вводиться внутрішньолюмбально метотрексат у дозі 12, 5 мг/м 2 (не більше 15 мг). Якщо спиномозкова рідина нормальна (цитоз не більше 10 клітин в 1 мм 3, , немає бластів), то через кожні 2 тижні в період індукції ремісії повторюють внутрішньолюмбальне введення метотрексату в дозі 12, 5 мг/м 2. Після досягнення ремісії проводиться другий етап профілактики нейролейкемії: 1. Опромінення голови в дозі 24 гр за 15 -18 сеансів по 1, 5 Гр за сеанс з обох латеральних полів. Паралельно опроміненню вводиться 5 доз (пятикратно) метотрексат інтралюмбально в дозі 12, 5 мг/м 2, при цьому метотрексат вводиться 3 рази у дні вільні від опромінення, і 2 рази – через 6 годин після опромінення.
Лікування гострого нелімфобластного лейкозу Програма “ 7+3” Індукція ремісії. Для індукції ремісії використовується цитозар у дозі 100 мг/м 2 в день (при інфузійному безперервному введенні) протягом 7 днів чи у дозі 100 мг/м 2 кожні 12 годин протягом 7 днів; рубоміцин у дозі 45 мг/м 2 (для осіб молодше 60 років) чи 30 мг/м 2 (для осіб старше 60 років) внутрішньовенно протягом 3 днів. За курсами індукції ремісії (не менше 2 курсів) слідує курс консолідації ремісії. Консолідація ремісії проводиться трьома курсами. Перший курс консолідації проводиться по тій же схемі, що і курс індукції ремісії. Другий курс консолідації проводиться за допомогою цитозара, що вводиться у дозі 3 г/м 2 кожні 12 годин для осіб молодше 50 років і 2 г/м 2 кожні 12 годин в день для осіб старше 50 років протягом 3 днів. Третій курс консолідації ремісії проводиться так як перший. Інтервал між курсами консолідації залежить відновлення гранулоцитів до 1 х10 9/л і тромбоцитів до 100 х109/л. Терапія підтримання ремісії проводиться по загальній для всіх програм схемі. Профілактика і лікування нейролейкемії обов’язкова при всіх варіантах гострого лейкозу. В один з перших днів діагностики гострого лейкозу проводиться перша діагностична люмбальна пункція, під час якої вводиться внутрішньолюмбально метотрексат у дозі 12, 5 мг/м 2 (не більше 15 мг). Якщо спиномозкова рідина нормальна (цитоз не більше 10 клітин в 1 мм 3, , немає бластів), то через кожні 2 тижні в період індукції ремісії повторюють внутрішньолюмбальне введення метотрексату в дозі 12, 5 мг/м 2. Після досягнення ремісії проводиться другий етап профілактики нейролейкемії: 1. Опромінення голови в дозі 24 гр за 15 -18 сеансів по 1, 5 Гр за сеанс з обох латеральних полів. Паралельно опроміненню вводиться 5 доз (пятикратно) метотрексат інтралюмбально в дозі 12, 5 мг/м 2, при цьому метотрексат вводиться 3 рази у дні вільні від опромінення, і 2 рази – через 6 годин після опромінення.
 КЛАСИФІКАЦІЯ ХРОНІЧНИХ ЛЕЙКОЗІВ С 92. 1 Хронічний мієлолейкоз (варіанти з Ph - хромосомою у дорослих та варіант без Ph - хромосоми). С 92. 1 Ювенільний хронічний мієлолейкоз з Ph -хромосомою. С 92. 1 Дитяча форма хронічного мієлолейкозу з Ph -хромосомою. С 94. 7 Сублейкемічний мієлоз (власно сублейкемічний мієлоз, мієлофіброз, остеомієлосклероз). С 94. 1 Еритремія. С 93. 1 Хронічний моноцитарний і мієломоноцитарний лейкоз. С 94. 3 Хронічний тучноклітинний лейкоз. С 91. 1 Хронічний лімфолейкоз (кістково-мозкова форма, основна прогресуюча, доброякісна, пухлинна, Т-форма, проліфоцитарна, із секрецією парапротеїну). С 91. 4 Волосатоклітинний лейкоз. С 84. 1 Хвороба Сезарі. Парапротеїнемічні гемобластози: С 88. 0 макроглобулінемія Вальденстрема; С 90. 0 мієломна хвороба; С 88. 1 хвороба важких ланцюгів; С 88. 7 хвороба легких ланцюгів.
КЛАСИФІКАЦІЯ ХРОНІЧНИХ ЛЕЙКОЗІВ С 92. 1 Хронічний мієлолейкоз (варіанти з Ph - хромосомою у дорослих та варіант без Ph - хромосоми). С 92. 1 Ювенільний хронічний мієлолейкоз з Ph -хромосомою. С 92. 1 Дитяча форма хронічного мієлолейкозу з Ph -хромосомою. С 94. 7 Сублейкемічний мієлоз (власно сублейкемічний мієлоз, мієлофіброз, остеомієлосклероз). С 94. 1 Еритремія. С 93. 1 Хронічний моноцитарний і мієломоноцитарний лейкоз. С 94. 3 Хронічний тучноклітинний лейкоз. С 91. 1 Хронічний лімфолейкоз (кістково-мозкова форма, основна прогресуюча, доброякісна, пухлинна, Т-форма, проліфоцитарна, із секрецією парапротеїну). С 91. 4 Волосатоклітинний лейкоз. С 84. 1 Хвороба Сезарі. Парапротеїнемічні гемобластози: С 88. 0 макроглобулінемія Вальденстрема; С 90. 0 мієломна хвороба; С 88. 1 хвороба важких ланцюгів; С 88. 7 хвороба легких ланцюгів.
 ЗА СТАДІЯМИ: Початкова. Розгорнута: а) соматично компенсована; б) соматично декомпенсована. Термінальна. УСКЛАДНЕННЯ: Анемія (в тому числі аутоімунна). Тромбоцитопенія та геморагічний синдром. Виразково-некротичні ускладнення (ангіни, пневмонії, шлунковокишкові та шкірні ураження та ін. ). Інфаркт селезінки. Ексудативний плеврит. Гнійні ускладнення (фурункули, флегмони, сепсис та ін. ).
ЗА СТАДІЯМИ: Початкова. Розгорнута: а) соматично компенсована; б) соматично декомпенсована. Термінальна. УСКЛАДНЕННЯ: Анемія (в тому числі аутоімунна). Тромбоцитопенія та геморагічний синдром. Виразково-некротичні ускладнення (ангіни, пневмонії, шлунковокишкові та шкірні ураження та ін. ). Інфаркт селезінки. Ексудативний плеврит. Гнійні ускладнення (фурункули, флегмони, сепсис та ін. ).
 Хронічний мієлолейкоз (ХМЛ) є одним з мієлопроліферативних захворювань та характеризується клональною проліферацією ранньої стовбурової клітини, що зазвичай призводить до збільшення кількості гранулоцитів. Число еритроїдних попередників та мегакаріоцитів може бути також підвищеним. Клінічно відрізнити ХМЛ від інших мієлопроліферативних захворювань (есенціального тромбоцитозу, поліцитемії та мієлоїдної метаплазії) часто буває дуже важко. ХМЛ можна відрізнити цитогенетично – завдяки виявленню в лейкемічних клітинах “філадельфійської хромосоми”, яка присутня у 90 -95% хворих на ХМЛ. “Філадельфійська хромосома” утворюється внаслідок делеції (відриву) довгого плеча 22 пари хромосом та транслокації (переносу) його на довге плече 9 -ї пари хромосом. При цій транслокації відбувається перенос протоонкогену, т. з. c-abl, зі звичайного положення на хромосомі 9 на нове місце на 22 хромосомі, що називається bcr. В результаті утворюється новий химерний ген bcr/abl. Білок – продукт цього химерного гену – функціонує як тирозинкіназа, ідентична продукту гену cabl, але з підвищеною ферментативною активністю. В експерименті даний ген був поміщений в клітини кісткового мозку, надалі введений опроміненій миші. Після того, як клітини заселили територію вбитого кісткового мозку миші, у неї виникли клінічні порушення, що відповідають ХМЛ. Ці важливі спостереження заставляють припустити не тільки те, що ген bcr/abl викликає ХМЛ, але і те, що це єдина генетична подія, необхідна для розвитку ХМЛ. Клінічні прояви ХМЛ різні. Захворювання може розвиватися як в 15, так і в 80 років. Близько 40% хворих в момент постановки діагнозу не мають ніяких клінічних симптомів. У 20% хворих спостерігається гепатоспленомегалія, у 54% - тільки спленомегалія. Приблизно у 50% хворих захворювання починається з анемії (Нв < 120 г/л), майже у 60% - з гіперлейкоцитозу (кількість лейкоцитів > 100 х109/л). Іноді захворювання починається зі значної втрати маси тіла, лихоманки, пропасниці, зниження апетиту та кволості. В перебігу хвороби розрізняють початкову (повільну, хронічну), розгорнуту (фаза акселерації) та термінальну стадії. Хронічна фаза ХМЛ триває, як правило, близько 3 років. Фаза акселерації – 1. 1. 5 роки. При відповідному лікуванні можна повернути захворювання в хронічну фазу. Термінальна фаза – фаза швидкої акселерації (3 -6 місяців), закінчується, як правило, смертю. Тривалість захворювання складає близько 7 років. Початкова стадія часто має субклінічний перебіг. Хворі можуть скаржитися на кволість, підвищену втомлюваність, зумовлену підвищенням клітинного розпаду. У периферичній крові у цей час відзначається помірний нейтрофільний лейкоцитоз із зсувом до незрілих форм: мієлоцитів, промієлоцитів та метамієлоцитів, підвищений відсоток базофілів та еозинофілів (базофільноеозинофільна асоціація). Розгорнута стадія характеризується зростанням симптомів інтоксикації, подальшим збільшенням селезінки та печінки внаслідок мієлоїдної метаплазії останніх. В периферичній крові - значний лейкоцитоз із зсувом до мієлоцитів, можуть з’являтися поодинокі бластні клітини. У 20 -30% випадків - тромбоцитоз, незначна нормохромна анемія. На певному етапі розвитку хвороби моноклонова пухлина трансформується у поліклонову, тобто процес вступає у термінальну стадію. Клінічні прояви термінальної стадії: швидке зростання селезінки, геморагічний синдром (внаслідок тромбоцитопенії), біль у кістках, немотивоване підвищення температури тіла, ураження шкіри та лімфатичних вузлів, відсутність ефекту від попереджувальної терапії, розвиток рефрактерності до мієлосану. Гематологічна картина термінальної стадії представлена бластним кризом, тобто значним зростанням у периферичній крові бластних клітин (до 50 -80% і більше). При проведенні диференційної діагностики між іншими мієлопроліферативними захворюваннями треба згадати про визначення вмісту лужної фосфатази у нейтрофілах. При хронічному мієлолейкозі специфічним є зменшення вмісту її до нуля. Лікування: при початковій та розгорнутій стадії основним препаратом є мієлосан (таб. по 2 мг, добова доза - 2 -3 таб. , діє на рівні стовбурової клітини, може викликати пластичний стан кровотворення); використовуються також мієлобромол (таб. по 250 мг, ефективність нижча, ніж у мієлосана), гідреа (капсули по 500 мг). Ця терапія давала до 80% ремісій, якщо її починали застосовувати в хронічну фазу. Проте жоден з медикаментів не може попередити трансформацію в бластну фазу. Останнім часом для лікування ХМЛ використовується -інтерферон (IFN ): застосування цього препарату дає таку ж гематологічну відповідь та кращу відповідь на цитогенетичному рівні. При трансформації хвороби у термінальну фазу монохіміотерапія неефективна. Тому при наявності бластного кризу проводиться цитохімічна реакція на встановлення варіанту бластного кризу (лімфобластний чи нелімфобластний) та в залежності від цього проводиться поліхіміотерапія як при гострому лейкозі. Симптоматична терапія: трансфузії еритроцитраної маси, тромбомаси, антибіотики при необхідності, знеболюючі, при підвищенні рівня сечової кислоти - алопуринол 0. 3 х 3 р. Ознаки ХМЛ, що пов’язані з поганим прогнозом: більш старший вік, втрата маси тіла, гепатоспленомегалія, поганий загальний стан та наявність симптомів на момент постановки діагнозу. Певні лабораторні ознаки також розцінюються як погіршуючі прогноз: анемія, збільшення або зменшення кількості тромбоцитів, більш високий процент бластних клітин в крові або кістковому мозку.
Хронічний мієлолейкоз (ХМЛ) є одним з мієлопроліферативних захворювань та характеризується клональною проліферацією ранньої стовбурової клітини, що зазвичай призводить до збільшення кількості гранулоцитів. Число еритроїдних попередників та мегакаріоцитів може бути також підвищеним. Клінічно відрізнити ХМЛ від інших мієлопроліферативних захворювань (есенціального тромбоцитозу, поліцитемії та мієлоїдної метаплазії) часто буває дуже важко. ХМЛ можна відрізнити цитогенетично – завдяки виявленню в лейкемічних клітинах “філадельфійської хромосоми”, яка присутня у 90 -95% хворих на ХМЛ. “Філадельфійська хромосома” утворюється внаслідок делеції (відриву) довгого плеча 22 пари хромосом та транслокації (переносу) його на довге плече 9 -ї пари хромосом. При цій транслокації відбувається перенос протоонкогену, т. з. c-abl, зі звичайного положення на хромосомі 9 на нове місце на 22 хромосомі, що називається bcr. В результаті утворюється новий химерний ген bcr/abl. Білок – продукт цього химерного гену – функціонує як тирозинкіназа, ідентична продукту гену cabl, але з підвищеною ферментативною активністю. В експерименті даний ген був поміщений в клітини кісткового мозку, надалі введений опроміненій миші. Після того, як клітини заселили територію вбитого кісткового мозку миші, у неї виникли клінічні порушення, що відповідають ХМЛ. Ці важливі спостереження заставляють припустити не тільки те, що ген bcr/abl викликає ХМЛ, але і те, що це єдина генетична подія, необхідна для розвитку ХМЛ. Клінічні прояви ХМЛ різні. Захворювання може розвиватися як в 15, так і в 80 років. Близько 40% хворих в момент постановки діагнозу не мають ніяких клінічних симптомів. У 20% хворих спостерігається гепатоспленомегалія, у 54% - тільки спленомегалія. Приблизно у 50% хворих захворювання починається з анемії (Нв < 120 г/л), майже у 60% - з гіперлейкоцитозу (кількість лейкоцитів > 100 х109/л). Іноді захворювання починається зі значної втрати маси тіла, лихоманки, пропасниці, зниження апетиту та кволості. В перебігу хвороби розрізняють початкову (повільну, хронічну), розгорнуту (фаза акселерації) та термінальну стадії. Хронічна фаза ХМЛ триває, як правило, близько 3 років. Фаза акселерації – 1. 1. 5 роки. При відповідному лікуванні можна повернути захворювання в хронічну фазу. Термінальна фаза – фаза швидкої акселерації (3 -6 місяців), закінчується, як правило, смертю. Тривалість захворювання складає близько 7 років. Початкова стадія часто має субклінічний перебіг. Хворі можуть скаржитися на кволість, підвищену втомлюваність, зумовлену підвищенням клітинного розпаду. У периферичній крові у цей час відзначається помірний нейтрофільний лейкоцитоз із зсувом до незрілих форм: мієлоцитів, промієлоцитів та метамієлоцитів, підвищений відсоток базофілів та еозинофілів (базофільноеозинофільна асоціація). Розгорнута стадія характеризується зростанням симптомів інтоксикації, подальшим збільшенням селезінки та печінки внаслідок мієлоїдної метаплазії останніх. В периферичній крові - значний лейкоцитоз із зсувом до мієлоцитів, можуть з’являтися поодинокі бластні клітини. У 20 -30% випадків - тромбоцитоз, незначна нормохромна анемія. На певному етапі розвитку хвороби моноклонова пухлина трансформується у поліклонову, тобто процес вступає у термінальну стадію. Клінічні прояви термінальної стадії: швидке зростання селезінки, геморагічний синдром (внаслідок тромбоцитопенії), біль у кістках, немотивоване підвищення температури тіла, ураження шкіри та лімфатичних вузлів, відсутність ефекту від попереджувальної терапії, розвиток рефрактерності до мієлосану. Гематологічна картина термінальної стадії представлена бластним кризом, тобто значним зростанням у периферичній крові бластних клітин (до 50 -80% і більше). При проведенні диференційної діагностики між іншими мієлопроліферативними захворюваннями треба згадати про визначення вмісту лужної фосфатази у нейтрофілах. При хронічному мієлолейкозі специфічним є зменшення вмісту її до нуля. Лікування: при початковій та розгорнутій стадії основним препаратом є мієлосан (таб. по 2 мг, добова доза - 2 -3 таб. , діє на рівні стовбурової клітини, може викликати пластичний стан кровотворення); використовуються також мієлобромол (таб. по 250 мг, ефективність нижча, ніж у мієлосана), гідреа (капсули по 500 мг). Ця терапія давала до 80% ремісій, якщо її починали застосовувати в хронічну фазу. Проте жоден з медикаментів не може попередити трансформацію в бластну фазу. Останнім часом для лікування ХМЛ використовується -інтерферон (IFN ): застосування цього препарату дає таку ж гематологічну відповідь та кращу відповідь на цитогенетичному рівні. При трансформації хвороби у термінальну фазу монохіміотерапія неефективна. Тому при наявності бластного кризу проводиться цитохімічна реакція на встановлення варіанту бластного кризу (лімфобластний чи нелімфобластний) та в залежності від цього проводиться поліхіміотерапія як при гострому лейкозі. Симптоматична терапія: трансфузії еритроцитраної маси, тромбомаси, антибіотики при необхідності, знеболюючі, при підвищенні рівня сечової кислоти - алопуринол 0. 3 х 3 р. Ознаки ХМЛ, що пов’язані з поганим прогнозом: більш старший вік, втрата маси тіла, гепатоспленомегалія, поганий загальний стан та наявність симптомів на момент постановки діагнозу. Певні лабораторні ознаки також розцінюються як погіршуючі прогноз: анемія, збільшення або зменшення кількості тромбоцитів, більш високий процент бластних клітин в крові або кістковому мозку.
 Хронічний лімфолейкоз. Приблизно у 95% хворих на ХЛЛ пухлинний клон має Вклітинну природу і лише 5% лейкозні клітини мають Т-фенотип. Основні зовнішні ознаки хронічного лімфолейкозу: лімфатичний лейкоцитоз, збільшення периферичних лімфовузлів, а також селезінки та печінки. Клінічні прояви хронічного лімфолейкозу залежать від стадії та форми хвороби. Класифікація K. Rai, T. Han та співавт. (1975): 0 – кількість лімфоцитів в периферичній крові більше 15 х109/л, в кістковому мозку – більше 40%, органомегалія відсутня. 1 – всі перераховані вище ознаки, гіперплазія лімфатичних вузлів. 2 – лімфоцитоз, гепатомегалія і/або спленомегалія (лімфовузли можуть бути збільшеними, але не обов'язково). 3 – лімофцитоз та анемія (Нв < 110 г/л), лімфовузли, печінка, селезінка можуть бути збільшені, але необов'язково. 4 - лімфоцитоз та тромбоцитопенія (тромбоцити < 100 х10 9/л), анемія та органомегалія можуть бути, але не обов'язково.
Хронічний лімфолейкоз. Приблизно у 95% хворих на ХЛЛ пухлинний клон має Вклітинну природу і лише 5% лейкозні клітини мають Т-фенотип. Основні зовнішні ознаки хронічного лімфолейкозу: лімфатичний лейкоцитоз, збільшення периферичних лімфовузлів, а також селезінки та печінки. Клінічні прояви хронічного лімфолейкозу залежать від стадії та форми хвороби. Класифікація K. Rai, T. Han та співавт. (1975): 0 – кількість лімфоцитів в периферичній крові більше 15 х109/л, в кістковому мозку – більше 40%, органомегалія відсутня. 1 – всі перераховані вище ознаки, гіперплазія лімфатичних вузлів. 2 – лімфоцитоз, гепатомегалія і/або спленомегалія (лімфовузли можуть бути збільшеними, але не обов'язково). 3 – лімофцитоз та анемія (Нв < 110 г/л), лімфовузли, печінка, селезінка можуть бути збільшені, але необов'язково. 4 - лімфоцитоз та тромбоцитопенія (тромбоцити < 100 х10 9/л), анемія та органомегалія можуть бути, але не обов'язково.
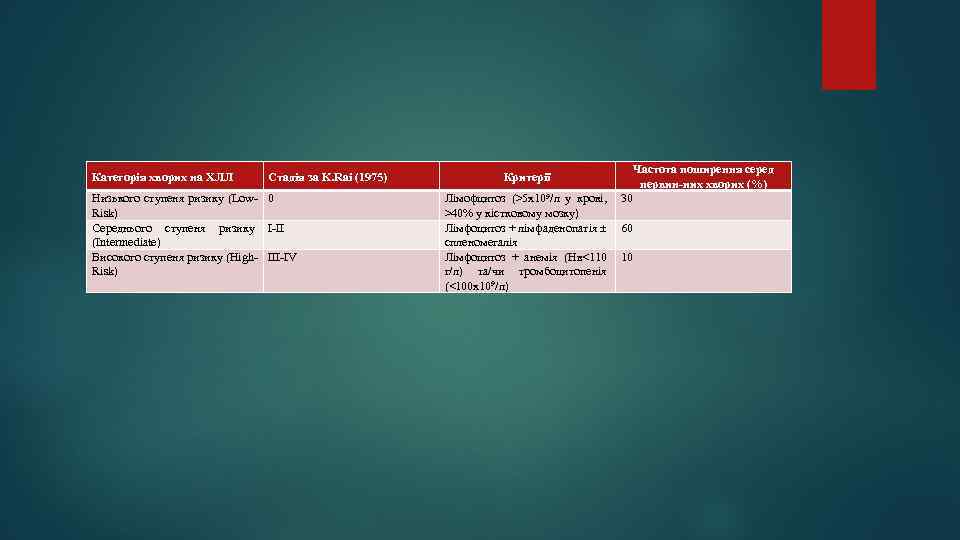 Категорія хворих на ХЛЛ Стадія за K. Rai (1975) Низького ступеня ризику (Low- 0 Risk) Середнього ступеня ризику I-II (Intermediate) Високого ступеня ризику (High- III-IV Risk) Критерії Лімофцитоз (>5 х109/л у крові, 30 >40% у кістковому мозку) Лімфоцитоз + лімфаденопатія 60 спленомегалія Лімфоцитоз + анемія (Нв<110 10 г/л) та/чи тромбоцитопенія (<100 х109/л) Частота поширення серед первин-них хворих (%)
Категорія хворих на ХЛЛ Стадія за K. Rai (1975) Низького ступеня ризику (Low- 0 Risk) Середнього ступеня ризику I-II (Intermediate) Високого ступеня ризику (High- III-IV Risk) Критерії Лімофцитоз (>5 х109/л у крові, 30 >40% у кістковому мозку) Лімфоцитоз + лімфаденопатія 60 спленомегалія Лімфоцитоз + анемія (Нв<110 10 г/л) та/чи тромбоцитопенія (<100 х109/л) Частота поширення серед первин-них хворих (%)
 Класифікація ХЛЛ J. Binet та співавт. (1981) більш придатна для прогнозування та лікування. Виділяють три стадії захворювання: А – кількість лімфоцитів в периферичній крові більше 15 х109/л, в кістковому мозку – більше 40%; анемія та тромбоцитопенія відсутні, в процес залучаються менше трьох груп лімфовузлів. В – перераховані вище ознаки, залучення трьох та більше груп лімфовузлів, збільшення селезінки та печінки; анемія та тромбоцитопенія відсутні. С – перераховані вище ознаки, анемія (Нв < 110 г/л у чоловіків та 100 г/л у жінок) або тромбоцитопенія незалежно від кількості збільшених лімфовузлів. В даний час рекомендують комбінування обидві класифікації, виділяючи А (0), А (1), А (2), В (1), В (2), С (3), С (4). Особливу увагу слід звернути на характерне збільшення лімфовузлів та їх характеристику на різних етапах хвороби. Спочатку вони м’якої, тістуватої консистенції, рухомі, неболючі, неспаяні. Надалі - більш щільні, в термінальній стадії - можуть бути кам’янистої щільності та стискувати оточуючі тканини.
Класифікація ХЛЛ J. Binet та співавт. (1981) більш придатна для прогнозування та лікування. Виділяють три стадії захворювання: А – кількість лімфоцитів в периферичній крові більше 15 х109/л, в кістковому мозку – більше 40%; анемія та тромбоцитопенія відсутні, в процес залучаються менше трьох груп лімфовузлів. В – перераховані вище ознаки, залучення трьох та більше груп лімфовузлів, збільшення селезінки та печінки; анемія та тромбоцитопенія відсутні. С – перераховані вище ознаки, анемія (Нв < 110 г/л у чоловіків та 100 г/л у жінок) або тромбоцитопенія незалежно від кількості збільшених лімфовузлів. В даний час рекомендують комбінування обидві класифікації, виділяючи А (0), А (1), А (2), В (1), В (2), С (3), С (4). Особливу увагу слід звернути на характерне збільшення лімфовузлів та їх характеристику на різних етапах хвороби. Спочатку вони м’якої, тістуватої консистенції, рухомі, неболючі, неспаяні. Надалі - більш щільні, в термінальній стадії - можуть бути кам’янистої щільності та стискувати оточуючі тканини.
 Лікування Лікування: В початковій фазі хвороби специфічна терапія непотрібна. Загальні моменти рекомендацій: запобігати інсоляції та перехолодження. При зростанні лейкоцитів до 60 -70 тис. у мкл і наявності інтоксикації проводиться хіміотерапія. З цією метою застосовують: хлорбутин таб. 2 та 5 мг. Добова доза 3 -10 мг; циклофосфан по 200 -400 мг через день в/в; вінбластин 10 мг 1 раз на 7 -10 днів в/в. При кістковомозковій формі використовують схему VAMP. Застосовується також променева терапія на лімфовузли та селезінку. Разова доза 1, 5 -2 Гр, сумарна доза - до 25 Гр. Можливе застосування лейкаферезу та плазмаферезу. У комплекс лікувальних заходів включають спленектомію, після якої прояви автоімунного цитолізу значно зменшуються. При наявності автоімунних ускладнень можливе застосування глюкокортикоїдів. У термінальній стадій хвороби застосовують схеми поліхіміотерапії, COPP, CVPP тощо.
Лікування Лікування: В початковій фазі хвороби специфічна терапія непотрібна. Загальні моменти рекомендацій: запобігати інсоляції та перехолодження. При зростанні лейкоцитів до 60 -70 тис. у мкл і наявності інтоксикації проводиться хіміотерапія. З цією метою застосовують: хлорбутин таб. 2 та 5 мг. Добова доза 3 -10 мг; циклофосфан по 200 -400 мг через день в/в; вінбластин 10 мг 1 раз на 7 -10 днів в/в. При кістковомозковій формі використовують схему VAMP. Застосовується також променева терапія на лімфовузли та селезінку. Разова доза 1, 5 -2 Гр, сумарна доза - до 25 Гр. Можливе застосування лейкаферезу та плазмаферезу. У комплекс лікувальних заходів включають спленектомію, після якої прояви автоімунного цитолізу значно зменшуються. При наявності автоімунних ускладнень можливе застосування глюкокортикоїдів. У термінальній стадій хвороби застосовують схеми поліхіміотерапії, COPP, CVPP тощо.


