ДИАЗО-И АЗОСОЕДИНЕНИЯ РЕАКЦИОННАЯ СПОСОБНОСТЬ АРОМАТИЧЕСКИХ


ДИАЗО-И АЗОСОЕДИНЕНИЯ РЕАКЦИОННАЯ СПОСОБНОСТЬ АРОМАТИЧЕСКИХ СОЛЕЙ ДИАЗОНИЯ 1

Азогруппа - группировка из двух атомов азота, соединенных двойной или тройной связью 2

АЗОСОЕДИНЕНИЯ Азосоединениями называются вещества, содержащие в молекуле азогруппу —N=N—, связанную с двумя углеводородными радикалами 3
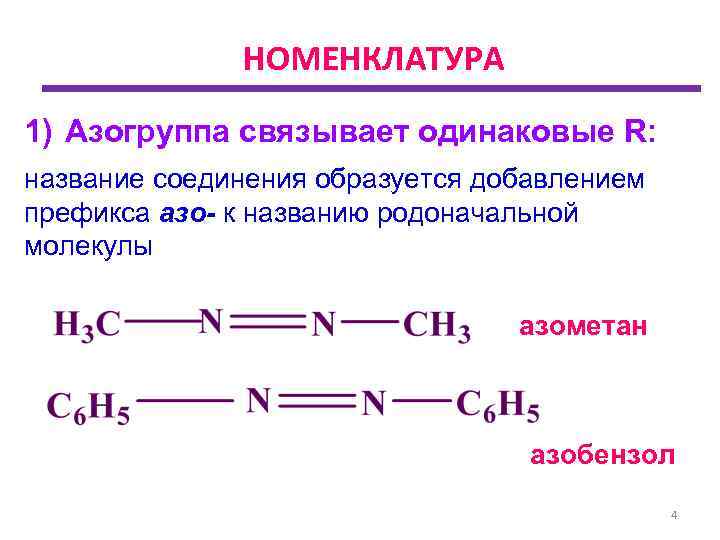
НОМЕНКЛАТУРА 1) Азогруппа связывает одинаковые R: название соединения образуется добавлением префикса азо- к названию родоначальной молекулы азометан азобензол 4
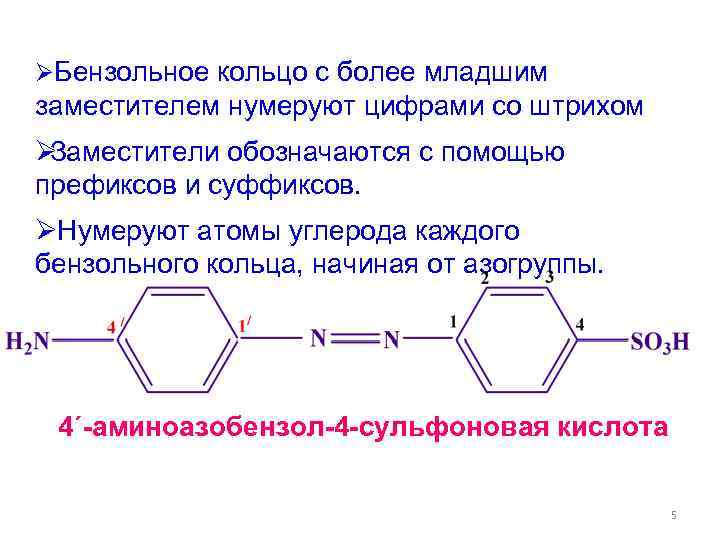
ØБензольное кольцо с более младшим заместителем нумеруют цифрами со штрихом ØЗаместители обозначаются с помощью префиксов и суффиксов. ØНумеруют атомы углерода каждого бензольного кольца, начиная от азогруппы. 4´-аминоазобензол-4 -сульфоновая кислота 5

2) Азогруппа связывает различные радикалы: в названии частицу азо- помещают между полными наименованиями родоначальных молекул. ØПервой указывается более сложная родоначальная молекула. 6
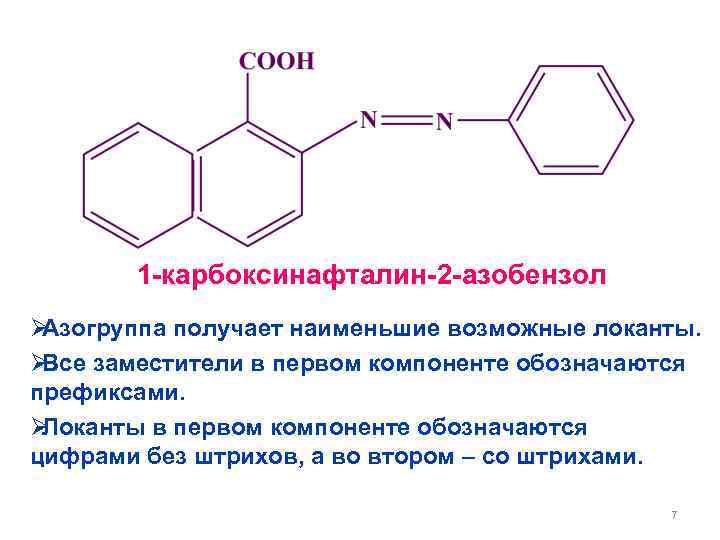
1 -карбоксинафталин-2 -азобензол ØАзогруппа получает наименьшие возможные локанты. ØВсе заместители в первом компоненте обозначаются префиксами. ØЛоканты в первом компоненте обозначаются цифрами без штрихов, а во втором – со штрихами. 7

3) RN = NR' RN = N─ заместитель в родоначальной структуре RН' – молекула, которая имеет большее число старших характеристических групп RN = N─ называют R-азо Суффикс должен получить наименьший локант, следующие, насколько возможные низкие номера должна иметь азогруппа 8
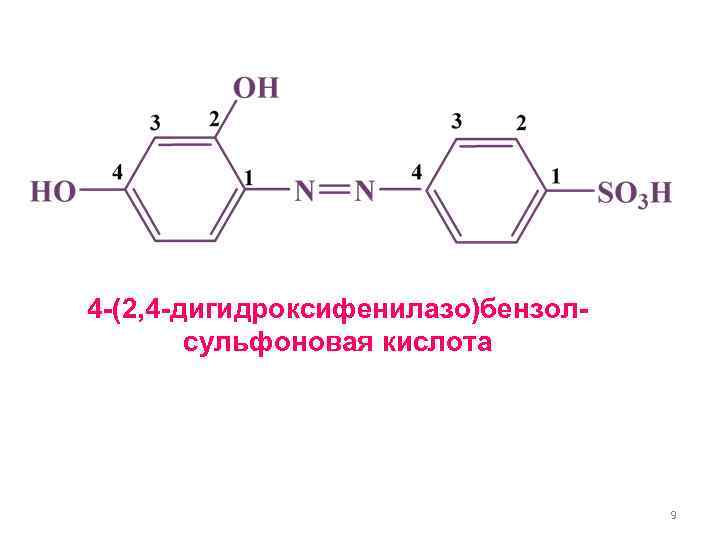
4 -(2, 4 -дигидроксифенилазо)бензол- сульфоновая кислота 9

ДИАЗОСОЕДИНЕНИЯ Диазосоединениями называются вещества, в молекуле которых азогруппа соединена с одним углеводородным радикалом R—N 2 X Х — ковалентносвязанная группа, например ОН или анион сильной кислоты. Если Х, анион сильной кислоты – соль диазония (ионное строение) 10
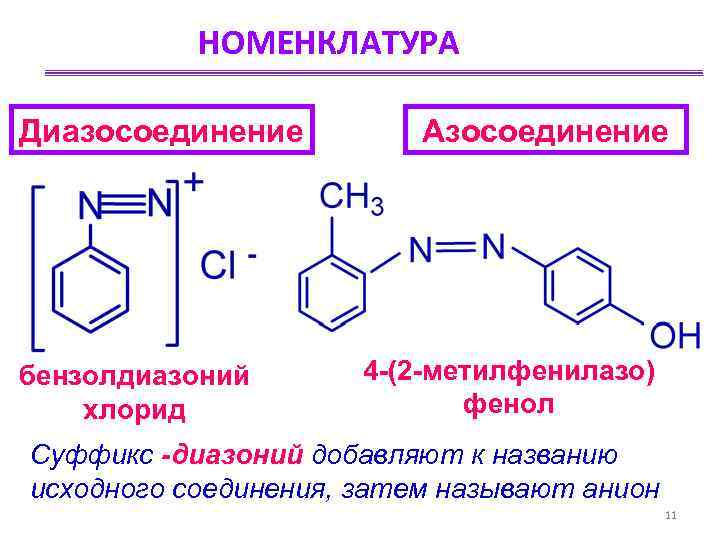
НОМЕНКЛАТУРА Диазосоединение Азосоединение бензолдиазоний 4 -(2 -метилфенилазо) хлорид фенол Суффикс -диазоний добавляют к названию исходного соединения, затем называют анион 11
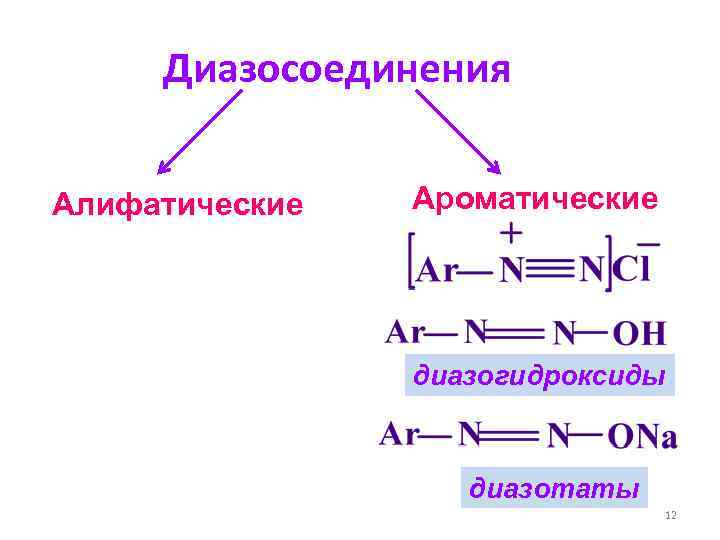
Диазосоединения Алифатические Ароматические диазогидроксиды диазотаты 12
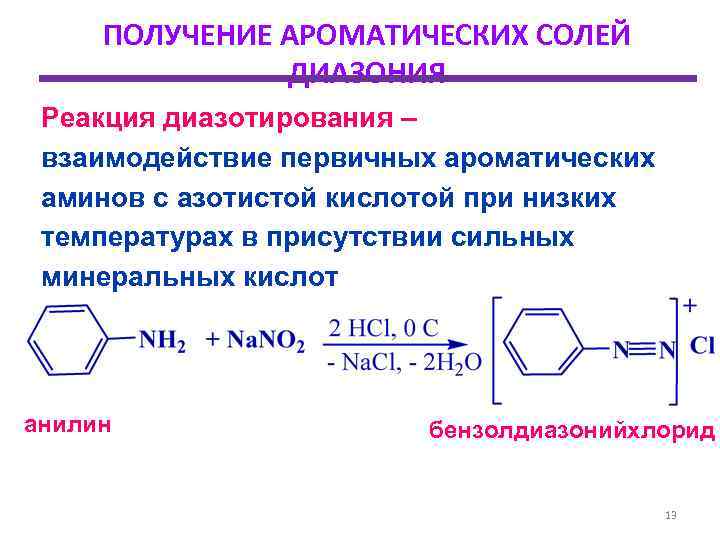
ПОЛУЧЕНИЕ АРОМАТИЧЕСКИХ СОЛЕЙ ДИАЗОНИЯ Реакция диазотирования – взаимодействие первичных ароматических аминов с азотистой кислотой при низких температурах в присутствии сильных минеральных кислот анилин бензолдиазонийхлорид 13
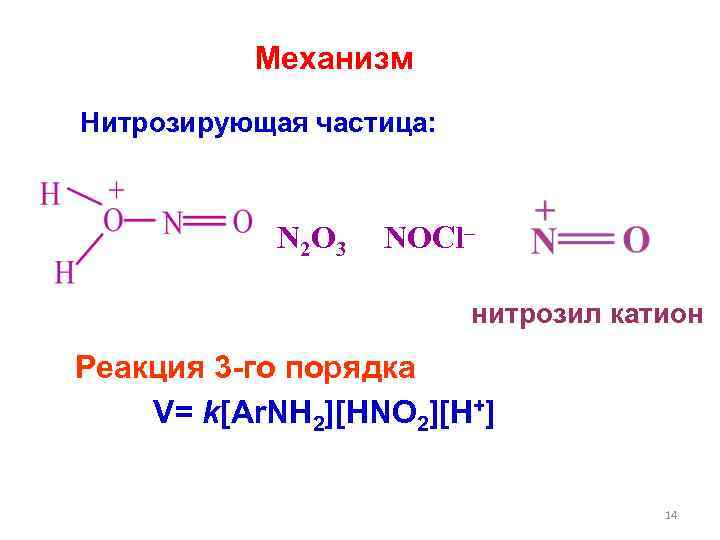
Механизм Нитрозирующая частица: N 2 O 3 NOCl– нитрозил катион Реакция 3 -го порядка V= k[Ar. NH 2][HNO 2][H+] 14
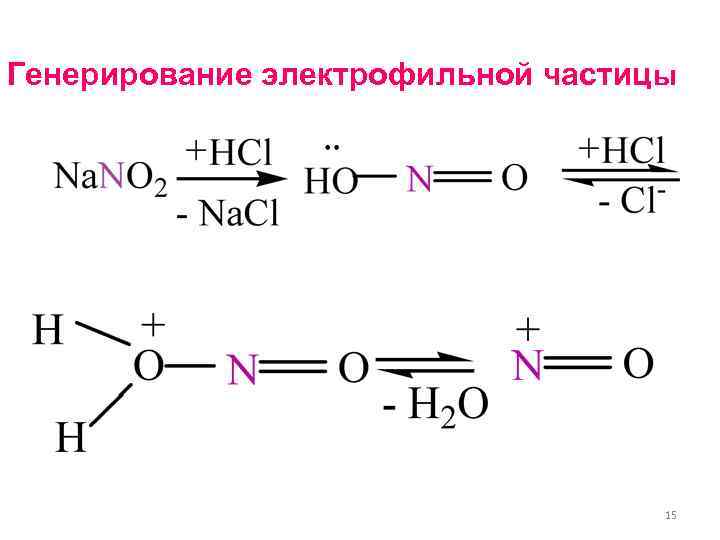
Генерирование электрофильной частицы 15
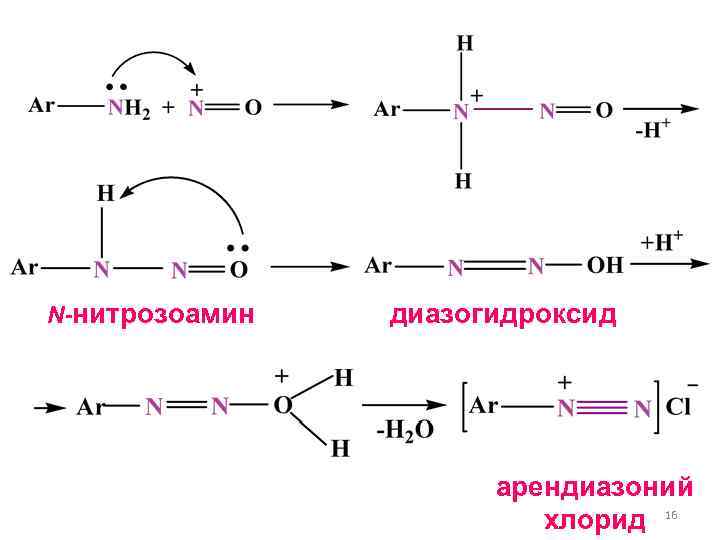
N-нитрозоамин диазогидроксид арендиазоний хлорид 16
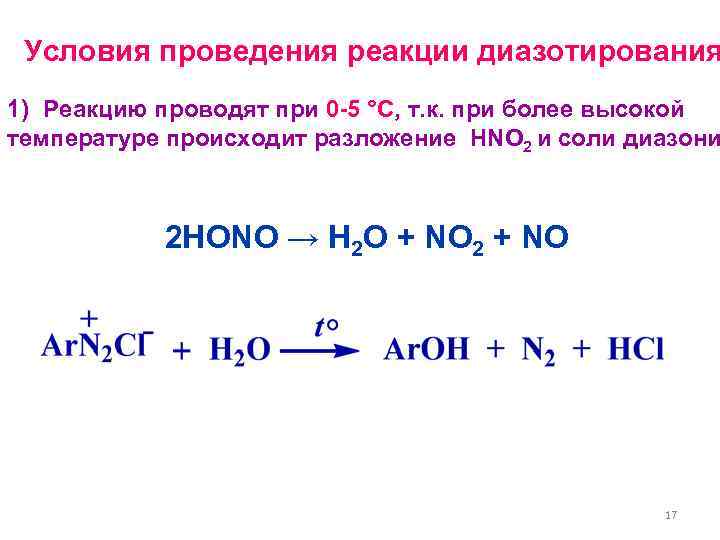
Условия проведения реакции диазотирования 1) Реакцию проводят при 0 -5 °С, т. к. при более высокой температуре происходит разложение HNO 2 и соли диазони 2 HONO → H 2 O + NO 2 + NO 17

2) избыток минеральной кислоты (2, 5 -3 моль на 1 моль амина), при недостатке кислоты наблюдается азосочетание соли диазония с исходным ароматическим амином; В кислой среде амин утрачивает Nu свойства 3) окончание диазотирования определяется по наличию Избытка HNO 2 с помощью йодкрахмальной бумаги. 2 KI(крахмал)+ 2 HNO 2 + 2 HCl → 2 KCl + I 2 + 2 H 2 O +2 NO 18

Избыток азотистой кислоты мешает проведению дальнейших реакциий с солями диазония (окисление азосоставляющей, нитрозирование и др. ). Избыток азотистой кислоты перед азосочетанием необходимо удалить с помощью мочевины. 19

Значение реакции диазотирования - синтетическое (препаративное); - аналитическое – для количественного определения лекарственных препаратов с ароматической аминогруппой (нитритометрия) 20
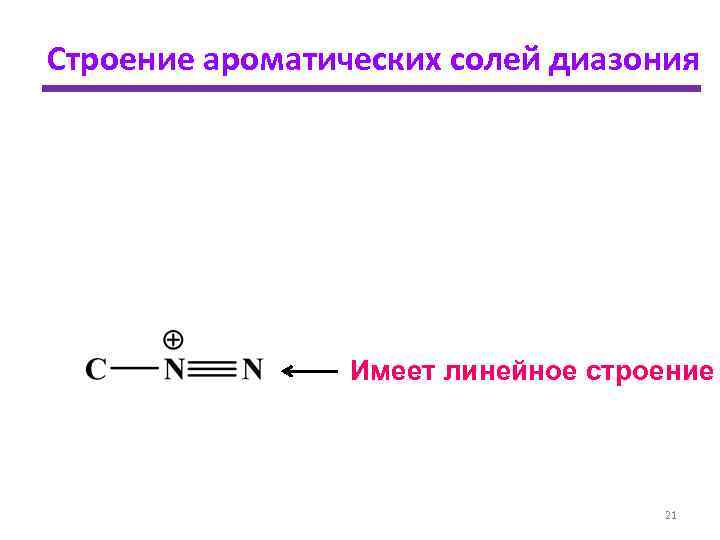
Строение ароматических солей диазония Имеет линейное строение 21
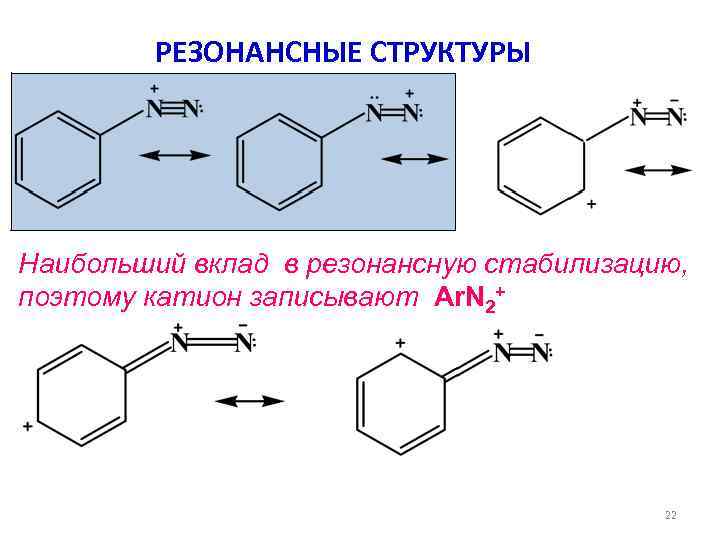
РЕЗОНАНСНЫЕ СТРУКТУРЫ Наибольший вклад в резонансную стабилизацию, поэтому катион записывают Ar. N 2+ 22

Строение диазосоединений зависит от р. Н среды. В кислой среде - соль диазония бензолдиазоний бензолдиазо- бензолдиазотат хлорид гидроксид натрия кислота соль При добавлении щелочи соли даазония последовательно переходят в диазогидроксиды и диазотаты. В нейтральной, слабокислой и слабощелочной среде в равновесии находятся все формы. 23
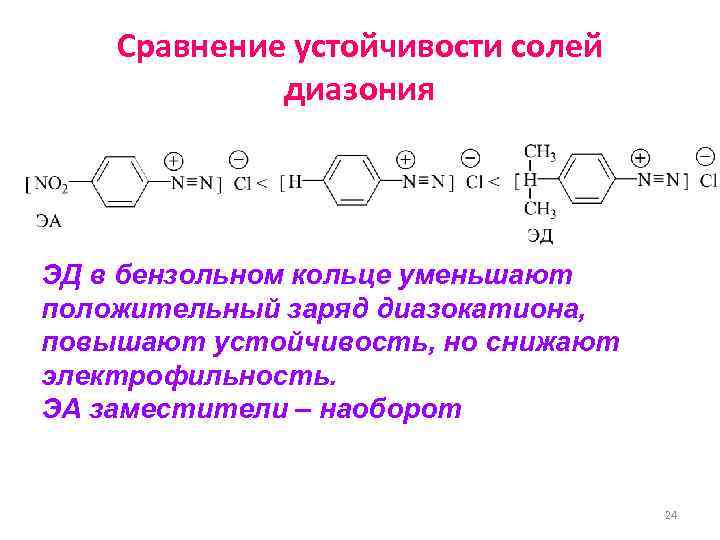
Сравнение устойчивости солей диазония ЭД в бензольном кольце уменьшают положительный заряд диазокатиона, повышают устойчивость, но снижают электрофильность. ЭА заместители – наоборот 24
Реакции солей диазония С выделением азота Без выделения азота 25

Реакции ароматических солей диазония с выделением азота Замещение диазогруппы на –ОН группу Механизм SN 1 Ar V= k [С 6 Н 5 N 2+HSO 4 -] Гидросульфат-ион более слабый Nu и не может конкурировать с водой в реакции с фенил-катионом 26
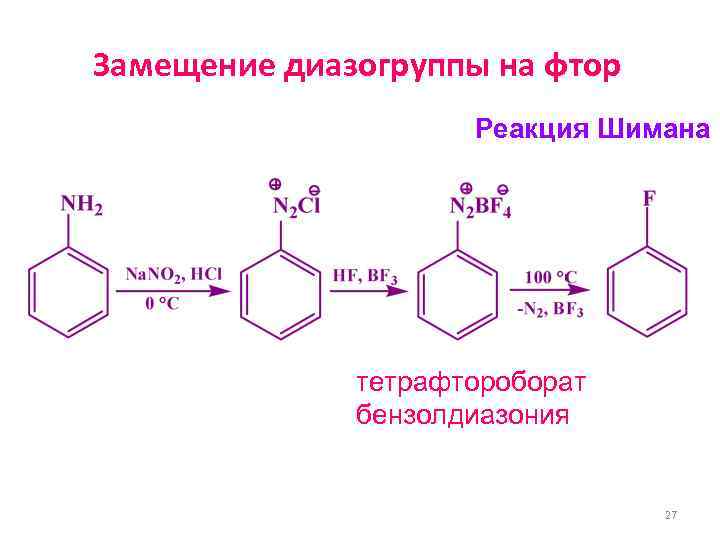
Замещение диазогруппы на фтор Реакция Шимана тетрафтороборат бензолдиазония 27
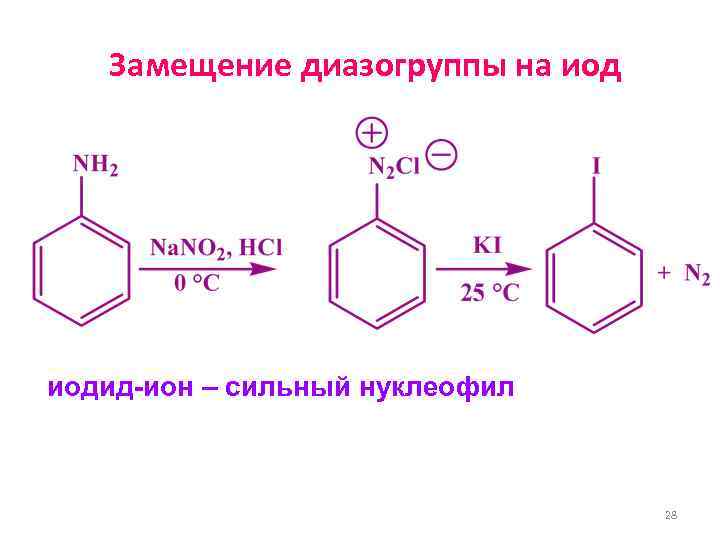
Замещение диазогруппы на иодид-ион – сильный нуклеофил 28
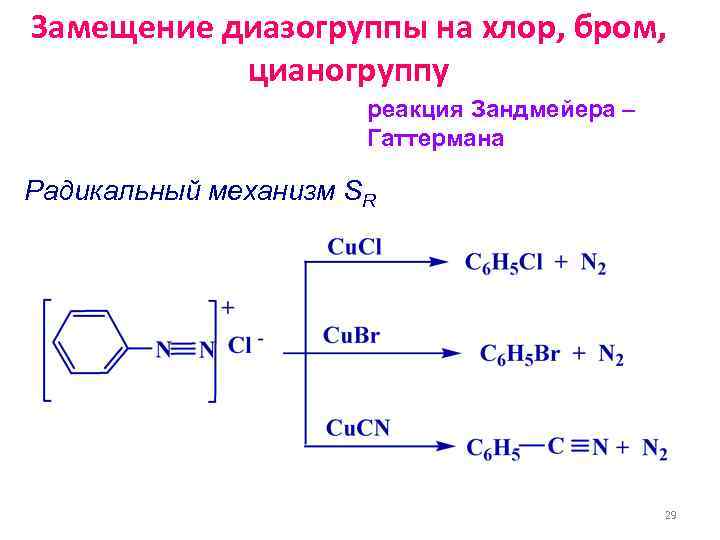
Замещение диазогруппы на хлор, бром, цианогруппу реакция Зандмейера – Гаттермана Радикальный механизм SR 29
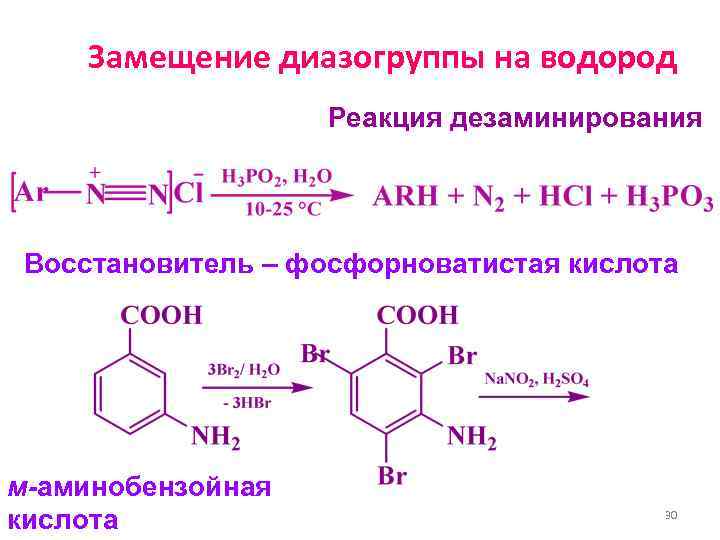
Замещение диазогруппы на водород Реакция дезаминирования Восстановитель – фосфорноватистая кислота м-аминобензойная кислота 30
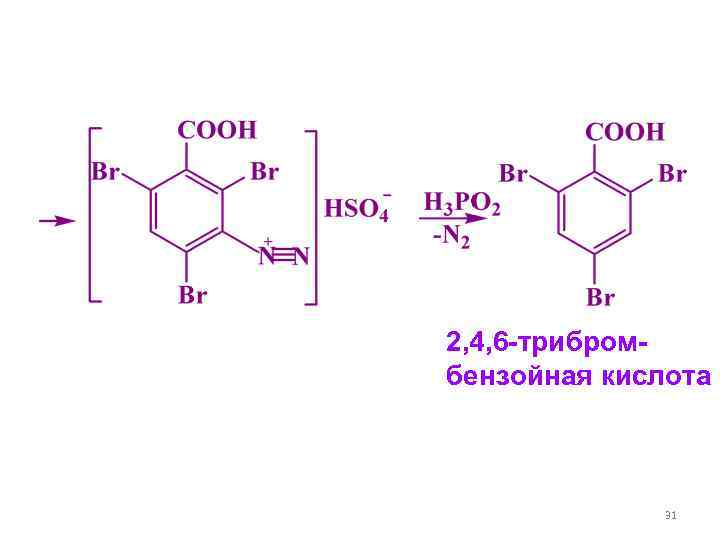
2, 4, 6 -трибром- бензойная кислота 31
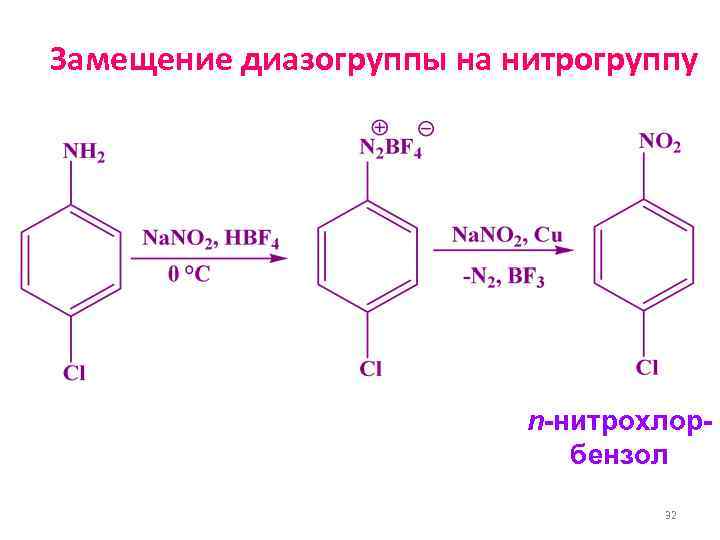
Замещение диазогруппы на нитрогруппу n-нитрохлор- бензол 32
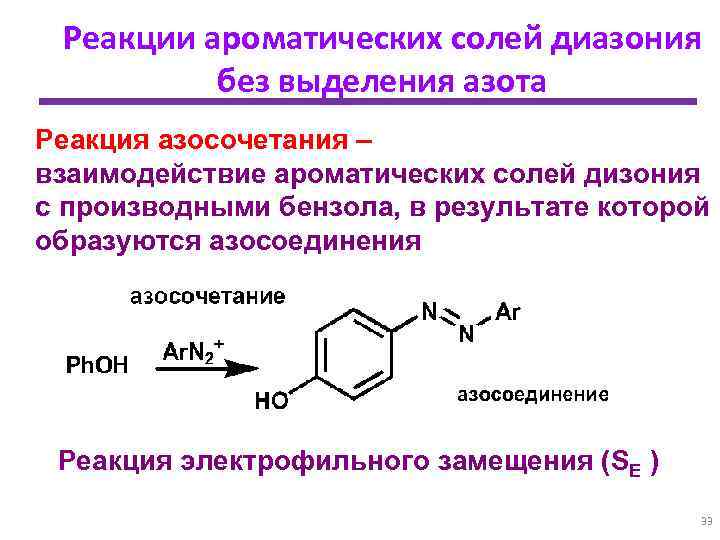
Реакции ароматических солей диазония без выделения азота Реакция азосочетания – взаимодействие ароматических солей дизония с производными бензола, в результате которой образуются азосоединения Реакция электрофильного замещения (SE ) 33
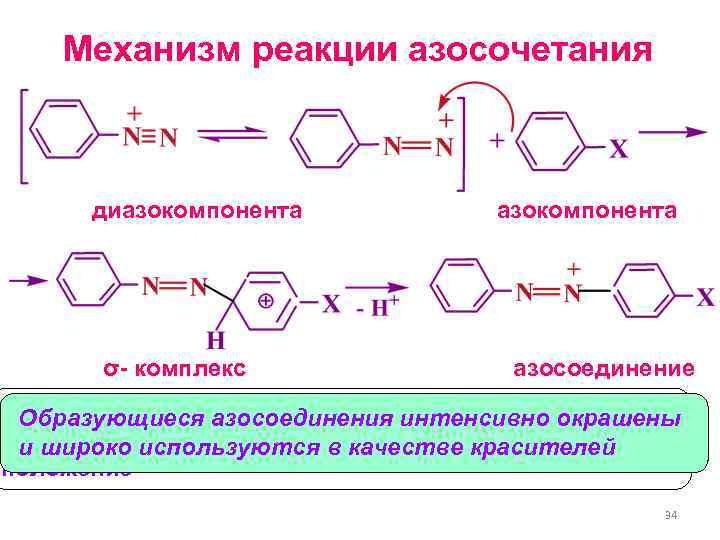
Механизм реакции азосочетания диазокомпонента азокомпонента σ- комплекс азосоединение Реакция происходит в пара-положение (из-за большого Образующиеся азосоединения интенсивно окрашены объема диазокатиона); если качестве красителей и широко используются в оно занято, то в орто- положение 34

Субстрат (азокомпонента, азосотавляющая) – ароматическое кольцо, содержащее сильные ЭД заместители O– > NR 2 > NHR > NH 2 > OH Электрофильный реагент (диазокомпонента, диазосотавляющая ) – катион диазония. ЭА заместители увеличивают, а ЭД уменьшают электрофильные свойства катиона диазония. 35

Бензол, его гомологи, простые эфиры, а также ароматические соединения с ЭА-заместителями не вступают в реакцию азосочетания. 36
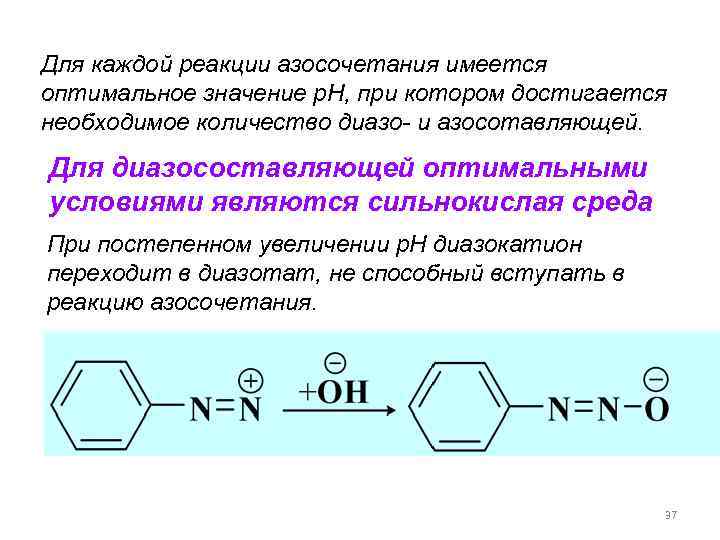
Для каждой реакции азосочетания имеется оптимальное значение р. Н, при котором достигается необходимое количество диазо- и азосотавляющей. Для диазосоставляющей оптимальными условиями являются сильнокислая среда При постепенном увеличении р. Н диазокатион переходит в диазотат, не способный вступать в реакцию азосочетания. 37
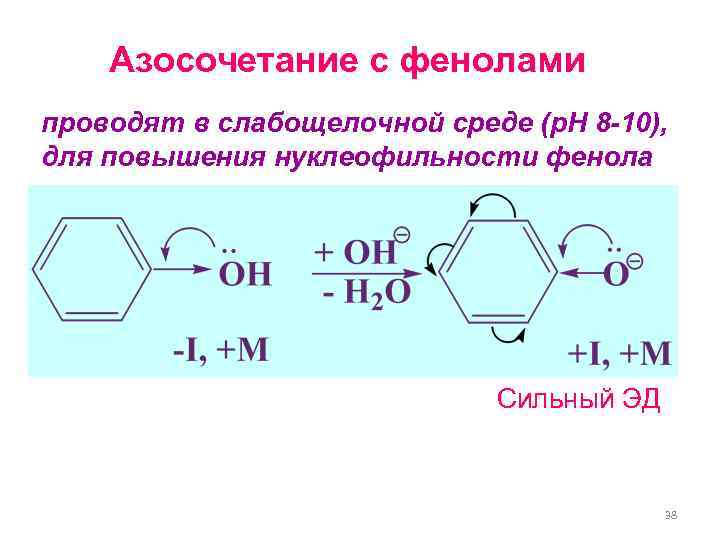
Азосочетание с фенолами проводят в слабощелочной среде (р. Н 8 -10), для повышения нуклеофильности фенола Сильный ЭД 38
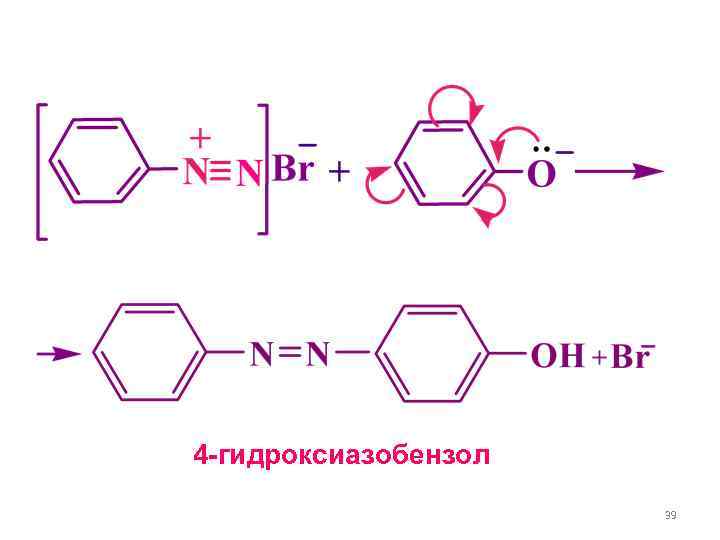
4 -гидроксиазобензол 39
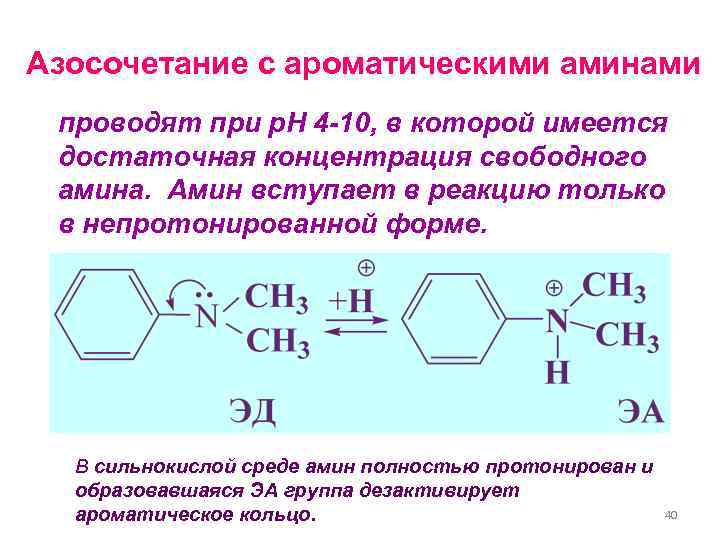
Азосочетание с ароматическими аминами проводят при р. Н 4 -10, в которой имеется достаточная концентрация свободного амина. Амин вступает в реакцию только в непротонированной форме. В сильнокислой среде амин полностью протонирован и образовавшаяся ЭА группа дезактивирует ароматическое кольцо. 40

41

Значение реакции азосочетания 1. Идентификация фенолов, первичных, вторичных и третичных ароматических аминов, а также лекарственных препаратов на их основе. 2. Получение азокрасителей, кислотно-основных индикаторов. 42
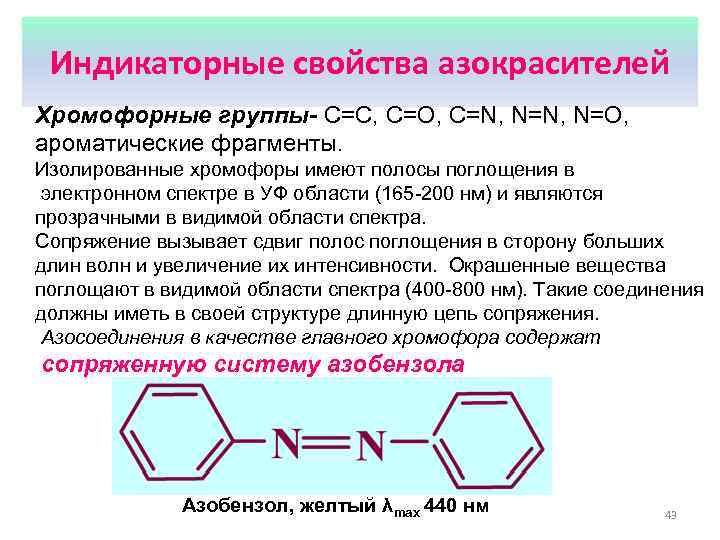
Индикаторные свойства азокрасителей Хромофорные группы- С=С, С=О, C=N, N=O, ароматические фрагменты. Изолированные хромофоры имеют полосы поглощения в электронном спектре в УФ области (165 -200 нм) и являются прозрачными в видимой области спектра. Сопряжение вызывает сдвиг полос поглощения в сторону больших длин волн и увеличение их интенсивности. Окрашенные вещества поглощают в видимой области спектра (400 -800 нм). Такие соединения должны иметь в своей структуре длинную цепь сопряжения. Азосоединения в качестве главного хромофора содержат сопряженную систему азобензола Азобензол, желтый λmax 440 нм 43

В зависимости от длины сопряженной системы азосоединения могут быть окрашены в желтый, оранжевый, красный, синий и зеленый цвета. Углублению окраски способствует наличие в структуре ауксохромов – атомов или групп атомов, вступающи в р, π- и π, π-сопряжение -NH 2, -N(CH 3)2, -OH, -SO 3 H, COOH Наиболее интенсивную окраску имеют те соединения, в которых с главным хромофором сопряжены одновременно ЭД и ЭА группы, находящиеся в пара- или орто-положении по отношению друг к другу Многие ароматические азосоединения при действии кислот и щелочей изменяют свою окраску в определенном интервал р. Н среды и используются как индикаторы 44

N, N-диметил диазотированная анилин сульфаниловая кислота 45

МЕТИЛОВЫЙ ОРАНЖЕВЫЙ – n-(n-диметиламинофенилазо)-бензолсульфонат натрия 46

АЛИФАТИЧЕСКИЕ ДИАЗОСОЕДИНЕНИЯ Диазометан, СН 2 N 2 Резонансные структуры Диазометан имеет линейное строение Газ желтого цвета, токсичен, взрывоопасен. Используют в растворе диэтилового эфира 47
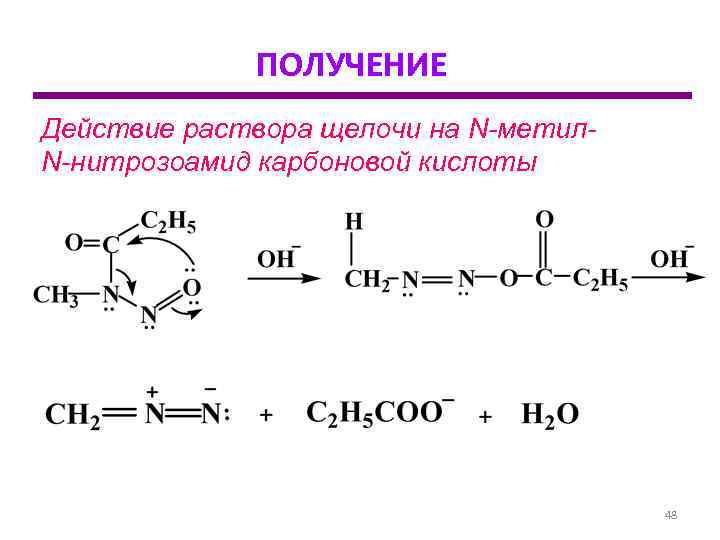
ПОЛУЧЕНИЕ Действие раствора щелочи на N-метил- N-нитрозоамид карбоновой кислоты 48

Алкилирующие свойства диазометана Метилирование соединений кислотного характера (карбоновые, сульфоновые кислоты, фенолы) 49
Диазосоединения.ppt
- Количество слайдов: 49

