7 Диаграммы.ppt
- Количество слайдов: 15

Диаграммы состояния

Энергией Гиббса (или потенциалом Гиббса, или просто термодинамическим потенциалом в узком смысле) называют термодинамический потенциал следующего вида: Внутренняя энергия тела (обозначается как E или U) — полная энергия этого тела за вычетом кинетической энергии тела как целого и потенциальной энергии тела во внешнем поле сил. Следовательно, внутренняя энергия складывается из кинетической энергии хаотического движения молекул, потенциальной энергии взаимодействия между ними и внутримолекулярной энергии. Для квазистатических процессов выполняется следующее соотношение: μ — химический потенциал, который можно определить как энергию, которую необходимо затратить, чтобы добавить в систему ещё одну частицу. Дифференциал энергии Гиббса для системы с постоянным числом частиц: Для системы с переменным числом частиц Химический потенциал применяется при анализе систем с переменным числом частиц, а также при изучении фазовых переходов.

Фазой называется совокупность всех гомогенных частей системы, одинаковых во всех точках по составу и по всем химическим и физическим свойствам (не зависящим от количества вещества) и ограниченных от других частей некоторой поверхностью (поверхностью раздела). Составляющие вещества, концентрации которых в рассматриваемой системе могут быть выбраны произвольно без изменения числа фаз системы, называются независимыми составляющими веществами или компонентами. Число компонентов или совпадает с числом составляющих веществ или меньше его. Число компонентов равняется числу составляющих веществ системы минус число уравнений, связывающих концентрации этих веществ в момент равновесия. Число компонентов есть наименьшее число составляющих веществ, достаточное для определения состава любой фазы системы. Условием равенства в гетерогенной системе, состоящей из нескольких компонентов, является равенство факторов интенсивности, характеризующих состояние каждой из фаз. Факторами интенсивности многокомпонентной системы являются температура, давление и химические потенциалы каждого из компонентов.

Рассмотрим случай, когда гетерогенная система состоит из фаз, в каждую из которых входят все компоненты без исключения. Верхними индексами обозначим фазы, а нижними компоненты системы. Для равновесия при наличии n компонентов и k фаз можно записать следующие равенства: Ряд уравнений, составленных на основании первой и второй строк представляют собой ряды тождеств, Поскольку давление и температура являются независимыми переменными, определяющими состояние системы. Уравнения, составленные на основании равенства химических потенциалов не представляют собой ряд тождеств, так как химический потенциал одного и того же компонента в разных фазах описывается различными функциями концентраций. температуры и давления. Химические компоненты отдельных компонентов каждой из фаз реальных систем представляют собой функции температуры, давления и концентраций всех компонентов, входящих в рассматриваемую фазу 1) 2) 3) 4) Каждая строка в системе 3 состоит из (к-1) независимых уравнений. Число строк в системе 3 равно n. Следовательно общее число уравнений равно n(k-1)

Число независимых концентраций в каждой фазе равно (n-1), а общее число независимых концентраций во всех k фазах - k(n-1). Независимыми переменными являются температура и давление. Поэтому общее число независимых переменных, охватываемое системой уравнений 3), равно k (n-1) + 2 Если число независимых переменных равно числу уравнений, их связывающих n(k-1) = k (n-1) + 2, 5) то каждое независимое переменное принимает некоторое строго определенное значение, и вся система может существовать только при этом единственно возможном сочетании значений температуры, давления и концентраций компонентов во всех фазах. Если число уравнений меньше числа независимых переменных f = k(n-1) + 2 – n(k-1) 6) f – число переменных, которым можно придавать произвольные значения пр имеющемся числе Уравнений, а следовательно и при данном числе фаз. f– число термодинамических степеней свободы системы. f+k=n+2 7) Уравнение 7) называется правилом фаз. Число степеней свободы равновесной термодинамической системы, на которую из внешних факторов влияют только давление и температура, равно числ Независимых компонентов системы плюс два минус число фаз. f=n+2 -k
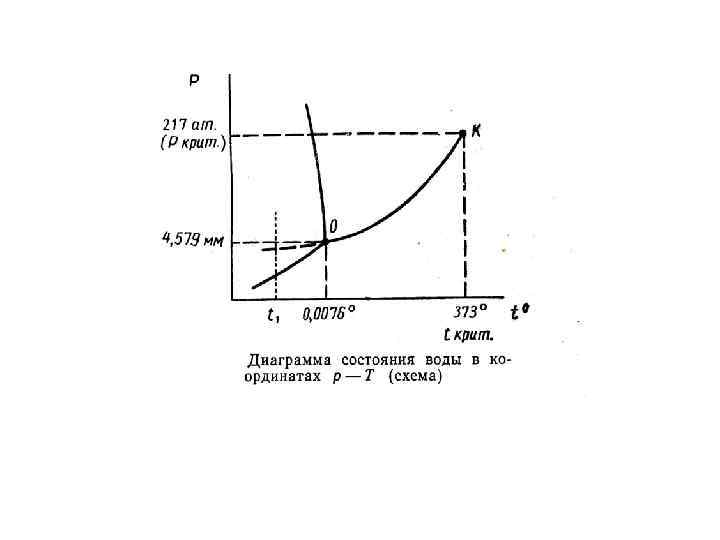
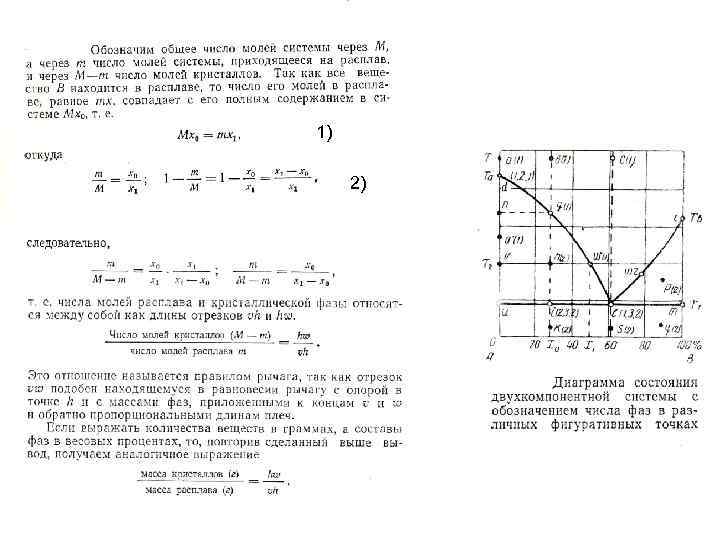
1) 2) 3) 4)
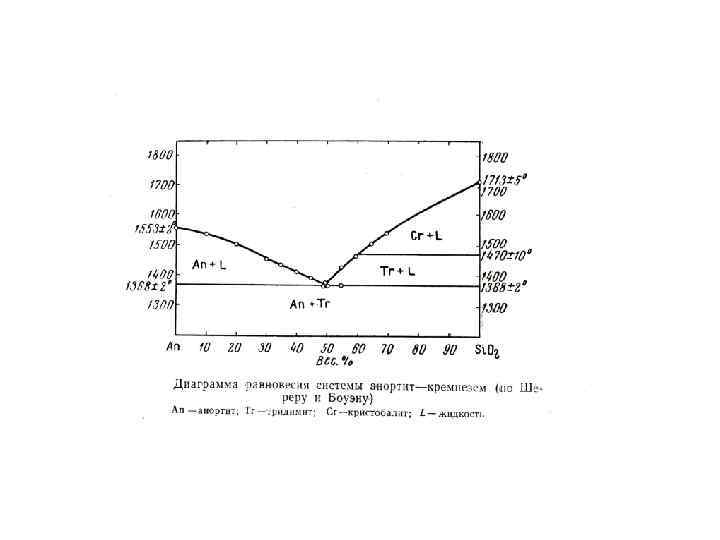
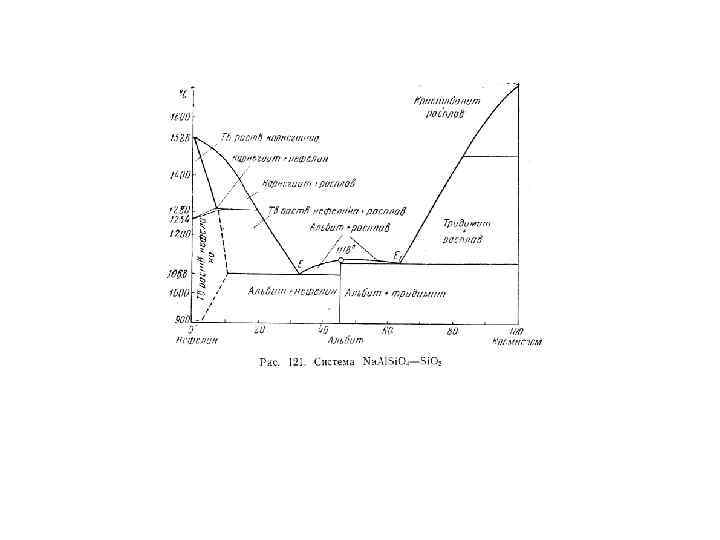
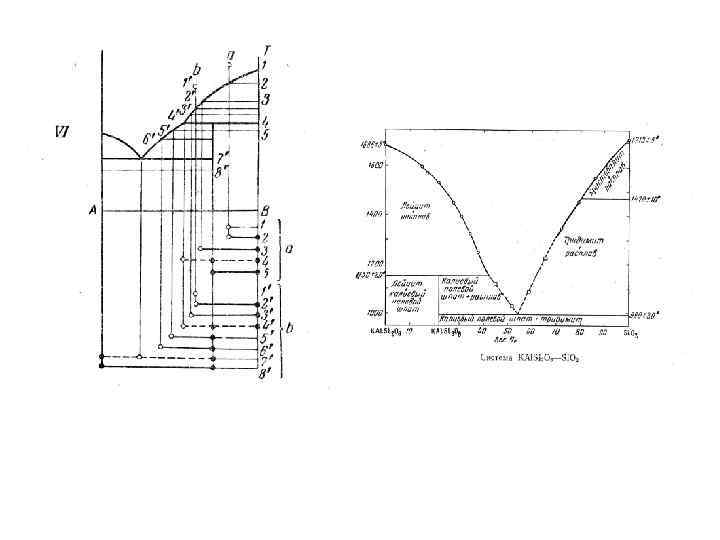
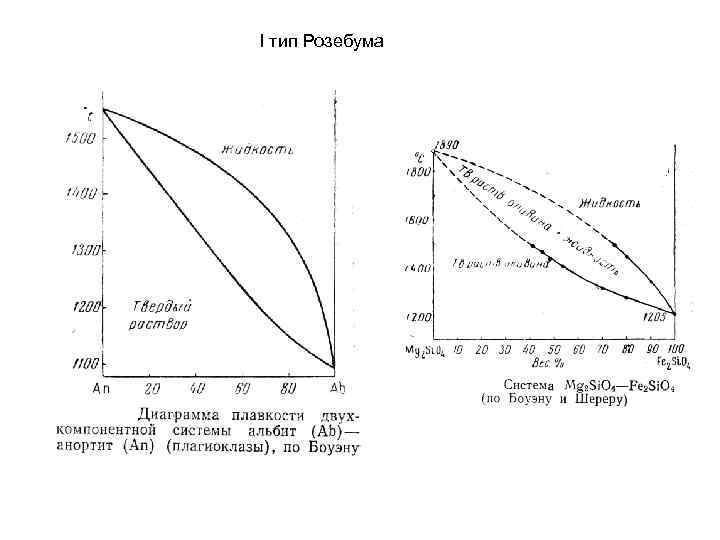
I тип Розебума
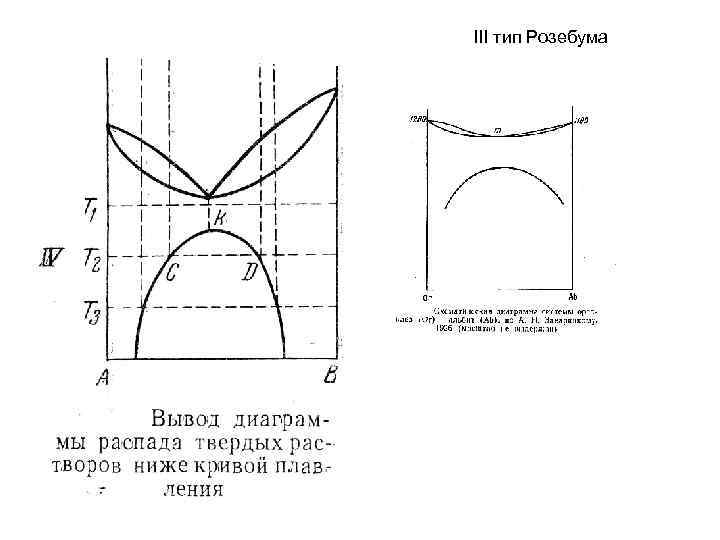
III тип Розебума
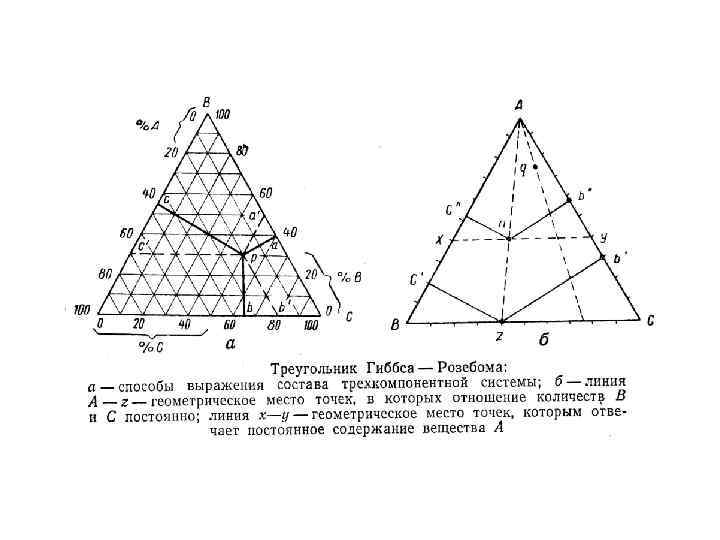
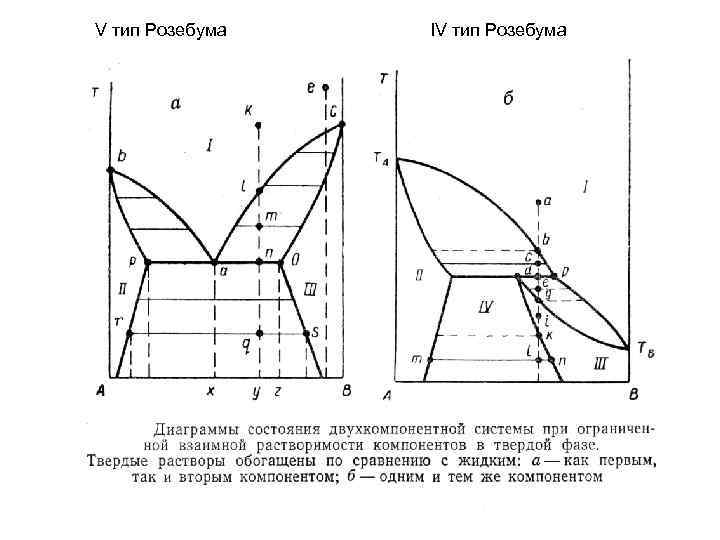
V тип Розебума IV тип Розебума

7 Диаграммы.ppt