Диаграммы равновесия двухкомпонентных











Диаграммы равновесия двухкомпонентных систем.ppt
- Количество слайдов: 23
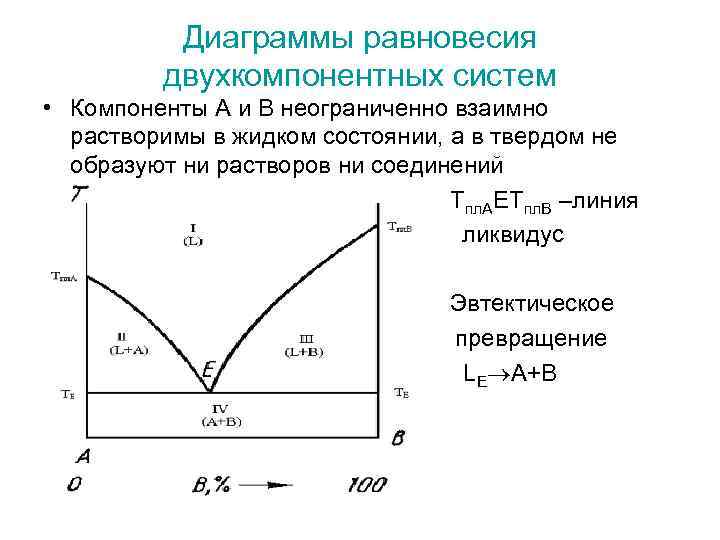
 Диаграммы равновесия двухкомпонентных систем • Компоненты А и В неограниченно взаимно растворимы в жидком состоянии, а в твердом не образуют ни растворов ни соединений Тпл. АЕТпл. В –линия ликвидус Эвтектическое превращение LE A+B
Диаграммы равновесия двухкомпонентных систем • Компоненты А и В неограниченно взаимно растворимы в жидком состоянии, а в твердом не образуют ни растворов ни соединений Тпл. АЕТпл. В –линия ликвидус Эвтектическое превращение LE A+B
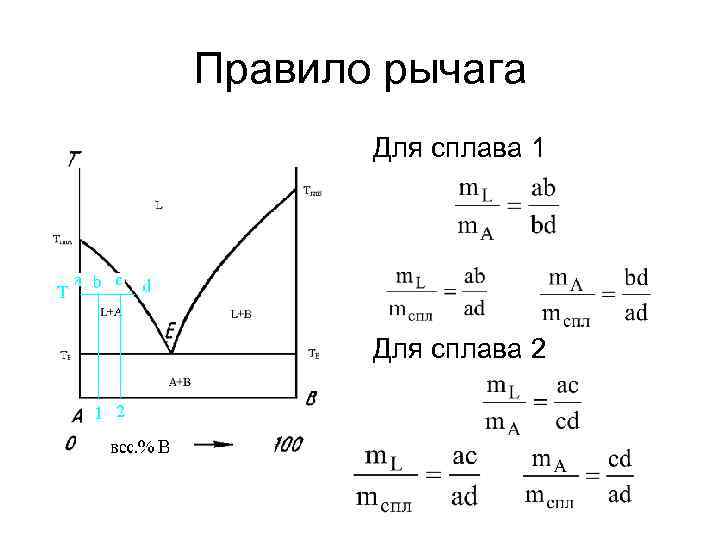
 Правило рычага Для сплава 1 Для сплава 2
Правило рычага Для сплава 1 Для сплава 2
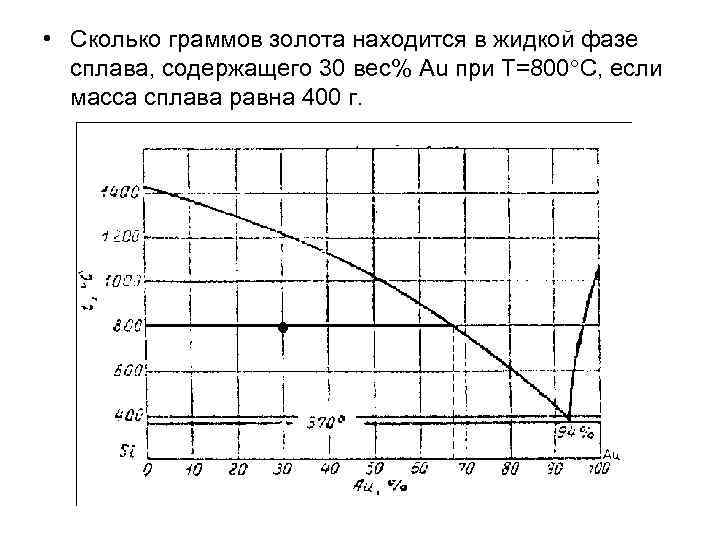
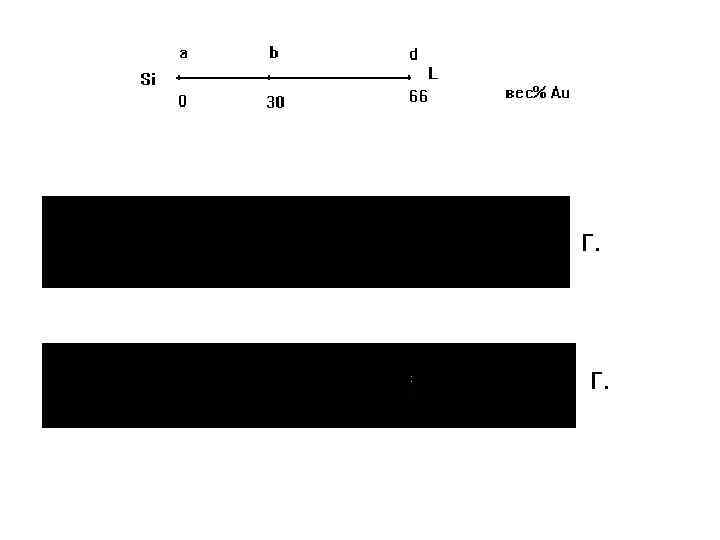
 • Сколько граммов золота находится в жидкой фазе сплава, содержащего 30 вес% Au при Т=800 С, если масса сплава равна 400 г.
• Сколько граммов золота находится в жидкой фазе сплава, содержащего 30 вес% Au при Т=800 С, если масса сплава равна 400 г.
 г. г.
г. г.
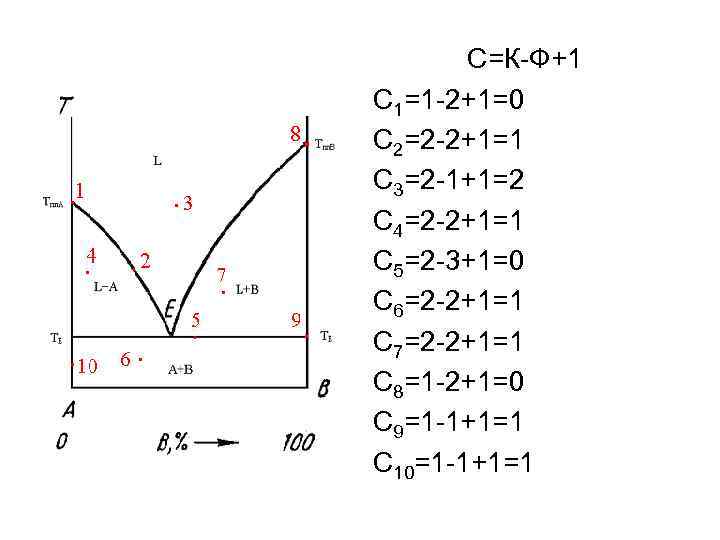
 С=К-Ф+1 С 1=1 -2+1=0 С 2=2 -2+1=1 С 3=2 -1+1=2 С 4=2 -2+1=1 С 5=2 -3+1=0 С 6=2 -2+1=1 С 7=2 -2+1=1 С 8=1 -2+1=0 С 9=1 -1+1=1 С 10=1 -1+1=1
С=К-Ф+1 С 1=1 -2+1=0 С 2=2 -2+1=1 С 3=2 -1+1=2 С 4=2 -2+1=1 С 5=2 -3+1=0 С 6=2 -2+1=1 С 7=2 -2+1=1 С 8=1 -2+1=0 С 9=1 -1+1=1 С 10=1 -1+1=1
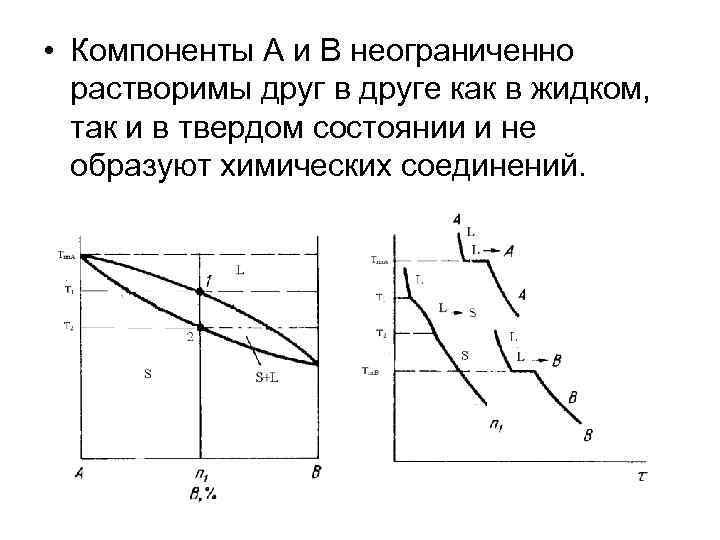
 • Компоненты А и В неограниченно растворимы друг в друге как в жидком, так и в твердом состоянии и не образуют химических соединений.
• Компоненты А и В неограниченно растворимы друг в друге как в жидком, так и в твердом состоянии и не образуют химических соединений.
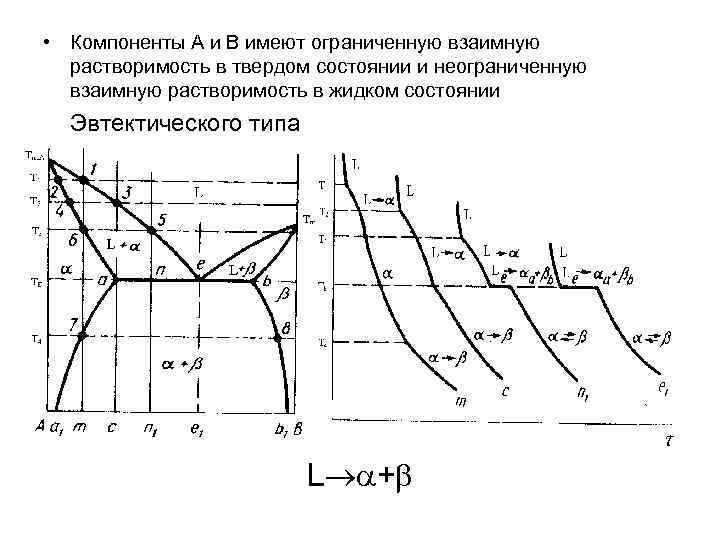
 • Компоненты А и В имеют ограниченную взаимную растворимость в твердом состоянии и неограниченную взаимную растворимость в жидком состоянии Эвтектического типа L +
• Компоненты А и В имеют ограниченную взаимную растворимость в твердом состоянии и неограниченную взаимную растворимость в жидком состоянии Эвтектического типа L +
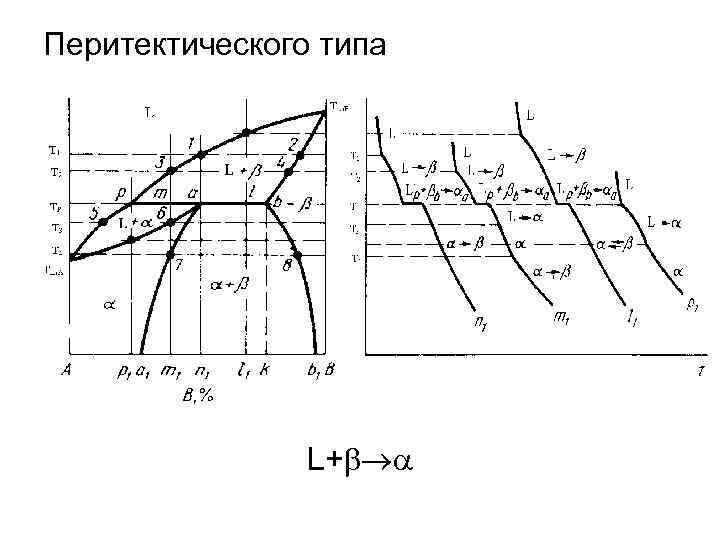
 Перитектического типа L+
Перитектического типа L+
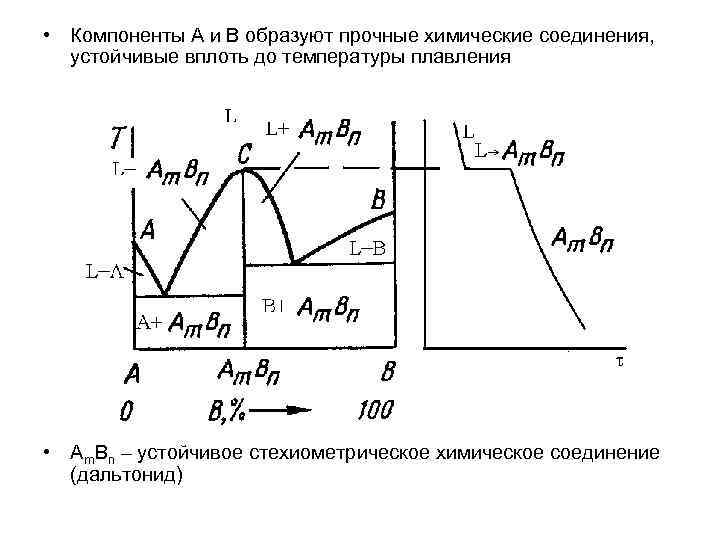
 • Компоненты А и В образуют прочные химические соединения, устойчивые вплоть до температуры плавления • Аm. Bn – устойчивое стехиометрическое химическое соединение (дальтонид)
• Компоненты А и В образуют прочные химические соединения, устойчивые вплоть до температуры плавления • Аm. Bn – устойчивое стехиометрическое химическое соединение (дальтонид)
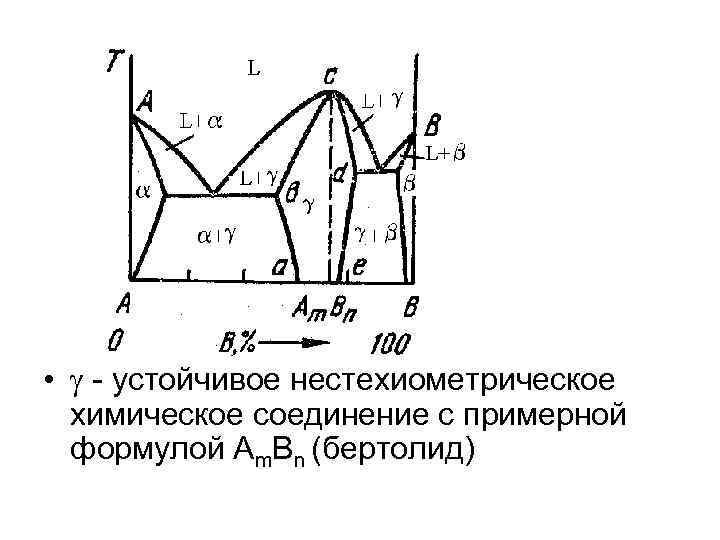
 • - устойчивое нестехиометрическое химическое соединение с примерной формулой Аm. Bn (бертолид)
• - устойчивое нестехиометрическое химическое соединение с примерной формулой Аm. Bn (бертолид)
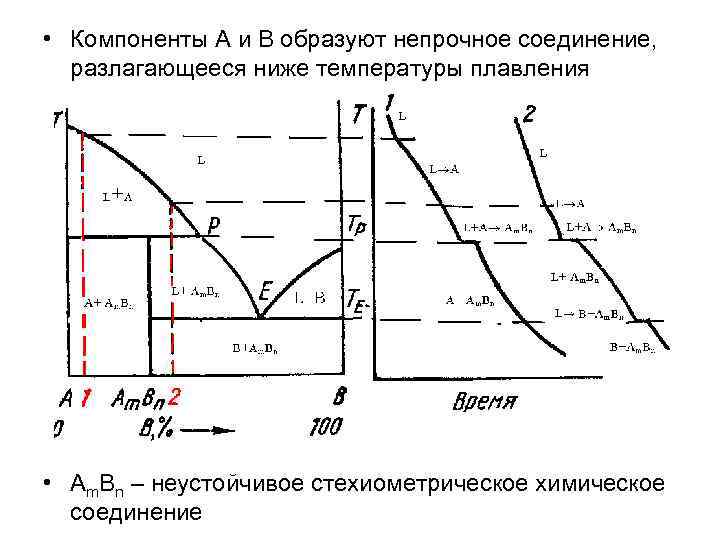
 • Компоненты А и В образуют непрочное соединение, разлагающееся ниже температуры плавления • Аm. Bn – неустойчивое стехиометрическое химическое соединение
• Компоненты А и В образуют непрочное соединение, разлагающееся ниже температуры плавления • Аm. Bn – неустойчивое стехиометрическое химическое соединение
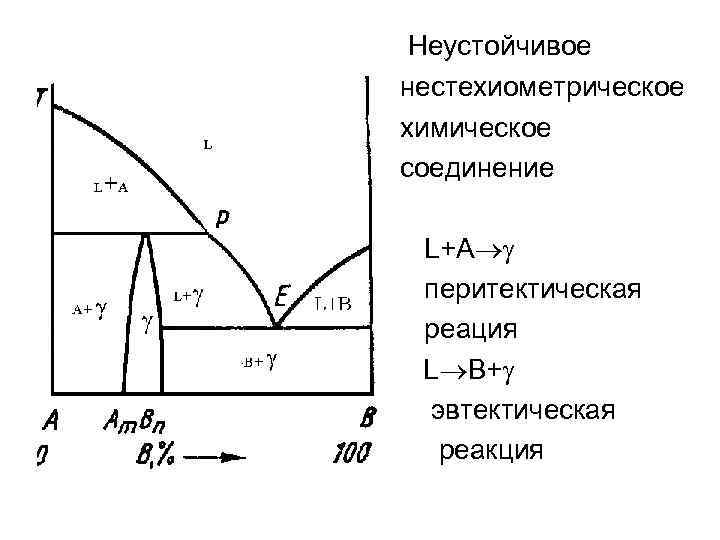
 Неустойчивое нестехиометрическое химическое соединение L+A перитектическая реация L B+ эвтектическая реакция
Неустойчивое нестехиометрическое химическое соединение L+A перитектическая реация L B+ эвтектическая реакция
 • L тв 1 + тв 2 Эвтектическая р-ция • тв 1 + тв 2 Эвтектоидная р-ция L+тв Аm. Bn или Перитектическая р-ция тв 1+тв 2 Аm. Bn или Перитектоидная р-ция
• L тв 1 + тв 2 Эвтектическая р-ция • тв 1 + тв 2 Эвтектоидная р-ция L+тв Аm. Bn или Перитектическая р-ция тв 1+тв 2 Аm. Bn или Перитектоидная р-ция
 • Число компонентов (K) 1 – на любой ординате (чистого компонента или химического соединения) 2 – на всей остальной диаграмме
• Число компонентов (K) 1 – на любой ординате (чистого компонента или химического соединения) 2 – на всей остальной диаграмме
 • Число фаз (Ф) 1 – однофазные области ординаты чистых компонентов и химических соединений исключая Тпл, Тполим. превр. , Тразл. неуст. х. с. 2 – двухфазные области Тпл, Тполим. Превр 3 – любая горизонталь, исключая крайние точки
• Число фаз (Ф) 1 – однофазные области ординаты чистых компонентов и химических соединений исключая Тпл, Тполим. превр. , Тразл. неуст. х. с. 2 – двухфазные области Тпл, Тполим. Превр 3 – любая горизонталь, исключая крайние точки
 2. Определите концентрации (в атомных процентах) каждого компонента в сосуществующих фазах для системы, содержащей 20 ат. % V при температурах 1800, 1400, 1230, 1000, 777 и 400 С. Т=1500 С T=1000 С L: 20 ат% V; 80 ат% Zr : 12 ат% V; 88 ат% Zr T=1400 С Zr. V 2: 67 ат% V; 33 ат% Zr L: 35 ат% V; 65 ат% Zr T=777 С : 11 ат% V; 89 ат% Zr -Zr: 0 ат% V; 100 ат% Zr T=1230 С : 8, 6 ат% V; 91, 4 ат% Zr L: 43, 5 ат% V; 56, 5 ат% Zr Zr. V 2: 67 ат% V; 33 ат% Zr : 16, 5 ат% V; 83, 5 ат% Zr T=400 С Zr. V 2: 67 ат% V; 33 ат% Zr -Zr: 0 ат% V; 100 ат% Zr Zr. V 2: 67 ат% V; 33 ат% Zr
2. Определите концентрации (в атомных процентах) каждого компонента в сосуществующих фазах для системы, содержащей 20 ат. % V при температурах 1800, 1400, 1230, 1000, 777 и 400 С. Т=1500 С T=1000 С L: 20 ат% V; 80 ат% Zr : 12 ат% V; 88 ат% Zr T=1400 С Zr. V 2: 67 ат% V; 33 ат% Zr L: 35 ат% V; 65 ат% Zr T=777 С : 11 ат% V; 89 ат% Zr -Zr: 0 ат% V; 100 ат% Zr T=1230 С : 8, 6 ат% V; 91, 4 ат% Zr L: 43, 5 ат% V; 56, 5 ат% Zr Zr. V 2: 67 ат% V; 33 ат% Zr : 16, 5 ат% V; 83, 5 ат% Zr T=400 С Zr. V 2: 67 ат% V; 33 ат% Zr -Zr: 0 ат% V; 100 ат% Zr Zr. V 2: 67 ат% V; 33 ат% Zr
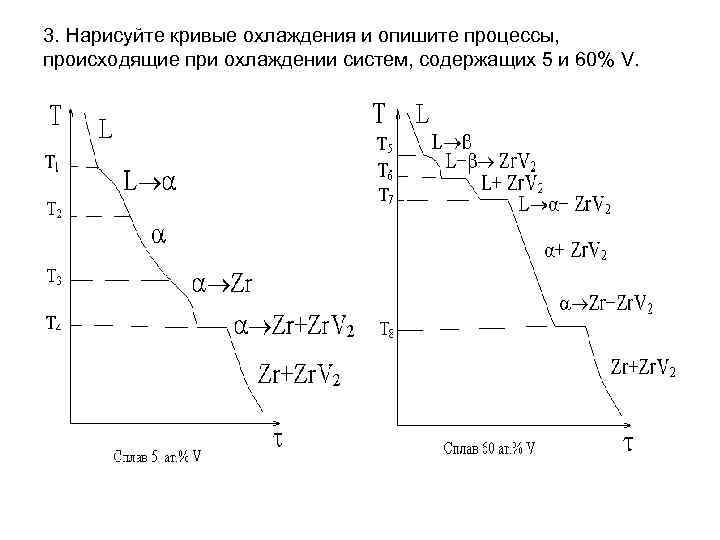
 3. Нарисуйте кривые охлаждения и опишите процессы, происходящие при охлаждении систем, содержащих 5 и 60% V.
3. Нарисуйте кривые охлаждения и опишите процессы, происходящие при охлаждении систем, содержащих 5 и 60% V.
 4. Рассчитайте массу каждой фазы и массу каждого компонента в каждой фазе для системы, содержащей 20 ат. % V при температуре 1000 С, если общая масса системы 100 грамм. гр.
4. Рассчитайте массу каждой фазы и массу каждого компонента в каждой фазе для системы, содержащей 20 ат. % V при температуре 1000 С, если общая масса системы 100 грамм. гр.
 гр. гр.
гр. гр.
 5. Рассчитайте сколько грамм и какого компонента в минимальном количестве необходимо добавить в систему, содержащую 10 ат. % Zr при температуре 1600 С, чтобы она из двухфазной превратилась в однофазную при той же температуре, если масса всей системы равна 200 г.
5. Рассчитайте сколько грамм и какого компонента в минимальном количестве необходимо добавить в систему, содержащую 10 ат. % Zr при температуре 1600 С, чтобы она из двухфазной превратилась в однофазную при той же температуре, если масса всей системы равна 200 г.
 • Добавляем V 83 гр. V в 100 гр. раствора 166 гр. V в 200 гр. раствора 166+Х - 200+Х 94 - 100 (166+Х). 100= (200+Х). 94 16600+100 Х=18800+94 Х 6 Х=2200 Х=366, 7 гр.
• Добавляем V 83 гр. V в 100 гр. раствора 166 гр. V в 200 гр. раствора 166+Х - 200+Х 94 - 100 (166+Х). 100= (200+Х). 94 16600+100 Х=18800+94 Х 6 Х=2200 Х=366, 7 гр.
 • Добавляем Zr 17 гр. Zr в 100 гр. раствора 34 гр. Zr в 200 гр. раствора 34+Y - 200+Y 38 - 100 (34+Y). 100= (200+Y). 38 3400+100 Y=7600+38 Y 62 Y=4200 Y=67, 7 гр.
• Добавляем Zr 17 гр. Zr в 100 гр. раствора 34 гр. Zr в 200 гр. раствора 34+Y - 200+Y 38 - 100 (34+Y). 100= (200+Y). 38 3400+100 Y=7600+38 Y 62 Y=4200 Y=67, 7 гр.
 6. Определите число термодинамических степеней свободы в точках, указанных преподавателем. • Точка 1. К=1 (Zr), Ф=2 (Zr-твердый, Zr-жидкий), С=1 - 2+1=0. • Точка 2. К=1 (Zr), Ф=2 ( -Zr, -Zr), С=1 -2+1=0. • Точка 3. К=1 (Zr), Ф=1 (Zr-твердый), С=1 -1+1=1. • Точка 4. К=2 (Zr, V), Ф=2 (L, ), С=2 -2+1=1. • Точка 5. К=2 (Zr, V), Ф=3 (L, , Zr. V 2), С=2 -3+1=0. • Точка 6. К=2 (Zr, V), Ф=3 (Zr, , Zr. V 2), С=2 -3+1=0. • Точка 7. К=1 (Zr. V 2), Ф=1 (Zr. V 2 - твердый), С=1 -1+1=1. • Точка 8. К=2 (Zr, V), Ф=3 (L, , Zr. V 2), С=2 -3+1=0. • Точка 9. К=2 (Zr, V), Ф=2 ( , Zr. V 2), С=2 -2+1=1. • Точка 10. К=2 (Zr, V), Ф=1 ( ), С=2 -1+1=2. • Точка 11. К=2 (Zr, V), Ф=1 (L), С=2 -1+1=2.
6. Определите число термодинамических степеней свободы в точках, указанных преподавателем. • Точка 1. К=1 (Zr), Ф=2 (Zr-твердый, Zr-жидкий), С=1 - 2+1=0. • Точка 2. К=1 (Zr), Ф=2 ( -Zr, -Zr), С=1 -2+1=0. • Точка 3. К=1 (Zr), Ф=1 (Zr-твердый), С=1 -1+1=1. • Точка 4. К=2 (Zr, V), Ф=2 (L, ), С=2 -2+1=1. • Точка 5. К=2 (Zr, V), Ф=3 (L, , Zr. V 2), С=2 -3+1=0. • Точка 6. К=2 (Zr, V), Ф=3 (Zr, , Zr. V 2), С=2 -3+1=0. • Точка 7. К=1 (Zr. V 2), Ф=1 (Zr. V 2 - твердый), С=1 -1+1=1. • Точка 8. К=2 (Zr, V), Ф=3 (L, , Zr. V 2), С=2 -3+1=0. • Точка 9. К=2 (Zr, V), Ф=2 ( , Zr. V 2), С=2 -2+1=1. • Точка 10. К=2 (Zr, V), Ф=1 ( ), С=2 -1+1=2. • Точка 11. К=2 (Zr, V), Ф=1 (L), С=2 -1+1=2.

