ДИАГНОСТИКА НАНОСТРУКТУРИРОВАННЫХ МАТЕРИ!.ppt
- Количество слайдов: 32
 ДИАГНОСТИКА НАНОСТРУКТУРИРОВАННЫХ МАТЕРИАЛОВ НА ОСНОВЕ ФАЗ ПЕРЕМЕННОГО СОСТАВА В. А. Мошников 10 сентября 2012 г.
ДИАГНОСТИКА НАНОСТРУКТУРИРОВАННЫХ МАТЕРИАЛОВ НА ОСНОВЕ ФАЗ ПЕРЕМЕННОГО СОСТАВА В. А. Мошников 10 сентября 2012 г.
 Джон Дальтон (6 сентября 1766 — 27 июля 1844) — английский провинциальный учитель-самоучка, химик, метеоролог и естествоиспытатель. Один из самых знаменитых и уважаемых учёных своего времени Он впервые (1794) провёл исследования и описал дефект зрения, которым страдал сам, — цветовая слепота, позже названный в его честь дальтонизмом; открыл закон парциальных давлений (закон Дальтона) (1801), закон равномерного расширения газов при нагревании (1802), закон растворимости газов в жидкостях (закон Генри-Дальтона). Установил закон кратных отношений (1803), обнаружил явление полимерии (на примере этилена и бутилена), ввёл понятие «атомный вес» , первым расчитал атомные веса (массы) ряда элементов и составил первую таблицу их относительных атомных весов, заложив тем самым основу атомной теории строения вещества.
Джон Дальтон (6 сентября 1766 — 27 июля 1844) — английский провинциальный учитель-самоучка, химик, метеоролог и естествоиспытатель. Один из самых знаменитых и уважаемых учёных своего времени Он впервые (1794) провёл исследования и описал дефект зрения, которым страдал сам, — цветовая слепота, позже названный в его честь дальтонизмом; открыл закон парциальных давлений (закон Дальтона) (1801), закон равномерного расширения газов при нагревании (1802), закон растворимости газов в жидкостях (закон Генри-Дальтона). Установил закон кратных отношений (1803), обнаружил явление полимерии (на примере этилена и бутилена), ввёл понятие «атомный вес» , первым расчитал атомные веса (массы) ряда элементов и составил первую таблицу их относительных атомных весов, заложив тем самым основу атомной теории строения вещества.
 Жозеф Луи Пруст Из ВИКИПЕДИИ: Жозеф Луи Пруст (фр. Joseph Louis Proust, 26 сентября 1754, Анжер — 5 июля 1826, Анжер) — французский химик Самым выдающимся научным достижением Пруста стало открытие закона постоянства состава. Занимаясь исследованием свойств и состава соединений различных металлов, он доказал, что при определении состава оксидов металлов многие его современники допускали ошибки, считая гидроксиды оксидами. Пруст показал также, что различные оксиды одного и того же металла имеют вполне определённый состав, который меняется скачкообразно. Исследование состава различных оксидов металлов, а также их хлоридов и сульфидов, выполненное в 1797— 1809, послужило основой для открытия им закона постоянных отношений. Оппонентом Пруста в возникшей дискуссии о постоянстве состава химических соединений выступил его соотечественник — известный химик Клод Луи Бертолле. Полемика этих двух учёных продолжалась с 1801 по 1808. Благодаря тому, что измерения Пруста были исключительно точными для своего времени, дискуссия закончилась в пользу Пруста и закон постоянства состава получил признание большинства химиков, став одним из краеугольных камней химической теории
Жозеф Луи Пруст Из ВИКИПЕДИИ: Жозеф Луи Пруст (фр. Joseph Louis Proust, 26 сентября 1754, Анжер — 5 июля 1826, Анжер) — французский химик Самым выдающимся научным достижением Пруста стало открытие закона постоянства состава. Занимаясь исследованием свойств и состава соединений различных металлов, он доказал, что при определении состава оксидов металлов многие его современники допускали ошибки, считая гидроксиды оксидами. Пруст показал также, что различные оксиды одного и того же металла имеют вполне определённый состав, который меняется скачкообразно. Исследование состава различных оксидов металлов, а также их хлоридов и сульфидов, выполненное в 1797— 1809, послужило основой для открытия им закона постоянных отношений. Оппонентом Пруста в возникшей дискуссии о постоянстве состава химических соединений выступил его соотечественник — известный химик Клод Луи Бертолле. Полемика этих двух учёных продолжалась с 1801 по 1808. Благодаря тому, что измерения Пруста были исключительно точными для своего времени, дискуссия закончилась в пользу Пруста и закон постоянства состава получил признание большинства химиков, став одним из краеугольных камней химической теории
 Клод Луи Бертолле (фр. Claude Louis Berthollet, 9 декабря 1748, Таллуар (Савойя) — 6 ноября 1822, Аркёй) — французский химик На основании наблюдений за процессами выпадения осадков из растворов Бертолле пришёл в выводу о зависимости направления реакций и состава образующихся соединений от массы реагентов и условий протекания реакций. Эти взгляды он высказал в своем «Опыте химической статики» (1803), в котором утверждал, что элементы могут соединяться друг с другом в любых пропорциях в зависимости от массы реагирующих веществ. По вопросу о непостоянстве состава соединений и изменчивости сил химического сродства Бертолле вёл длительную полемику с Ж. Л. Прустом. В начале XIX в. эта дискуссия завершилась в пользу Пруста и закон постоянства состава получил признание большинства химиков
Клод Луи Бертолле (фр. Claude Louis Berthollet, 9 декабря 1748, Таллуар (Савойя) — 6 ноября 1822, Аркёй) — французский химик На основании наблюдений за процессами выпадения осадков из растворов Бертолле пришёл в выводу о зависимости направления реакций и состава образующихся соединений от массы реагентов и условий протекания реакций. Эти взгляды он высказал в своем «Опыте химической статики» (1803), в котором утверждал, что элементы могут соединяться друг с другом в любых пропорциях в зависимости от массы реагирующих веществ. По вопросу о непостоянстве состава соединений и изменчивости сил химического сродства Бертолле вёл длительную полемику с Ж. Л. Прустом. В начале XIX в. эта дискуссия завершилась в пользу Пруста и закон постоянства состава получил признание большинства химиков
 Никола й Семёнович Курнако в (24 ноября (6 декабря) 1860, Нолинск — 19 марта 1941, Барвиха) — выдающийся русский физикохимик, профессор (1893), заслуженный профессор (1907), доктор химических наук (1909), академик Петербургской академии наук (1913) и АН СССР, лауреат Сталинской премии, создатель физико-химического анализа Изучая состав сплавов, Курнаков (совместно с С. Ф. Жемчужиным) обнаружил в них образование фаз (соединений) переменного свойства, существование которых допускал К. Бертолле. Эти соединения он предложил называть бертоллидами в отличие от дальтонидов, подчиняющихся закону постоянства состава Пруста и закону кратных отношений Дальтона. Учение Курнакова о бертоллидах легло в основу современной химии твердого и жидкого состояний. Построение диаграмм «состав – свойство» нашло широкое распространение при исследовании не только металлических сплавов, но и солей, органических веществ, руд, грязей и солевых отложений.
Никола й Семёнович Курнако в (24 ноября (6 декабря) 1860, Нолинск — 19 марта 1941, Барвиха) — выдающийся русский физикохимик, профессор (1893), заслуженный профессор (1907), доктор химических наук (1909), академик Петербургской академии наук (1913) и АН СССР, лауреат Сталинской премии, создатель физико-химического анализа Изучая состав сплавов, Курнаков (совместно с С. Ф. Жемчужиным) обнаружил в них образование фаз (соединений) переменного свойства, существование которых допускал К. Бертолле. Эти соединения он предложил называть бертоллидами в отличие от дальтонидов, подчиняющихся закону постоянства состава Пруста и закону кратных отношений Дальтона. Учение Курнакова о бертоллидах легло в основу современной химии твердого и жидкого состояний. Построение диаграмм «состав – свойство» нашло широкое распространение при исследовании не только металлических сплавов, но и солей, органических веществ, руд, грязей и солевых отложений.
 Фазы переменного состава Промежуточная фаза является фазой переменного состава. На диаграмме существует область гомогенности (область g ). Составы, расположенные в области левее Аm. Вn, принято рассматривать как твердый раствор компонента А в химическом соединении, а составы, расположенные правее – как раствор компонента В в этом же соединении. При заданных значениях давления и температуры равновесной является атомная структура, отвечающая минимуму свободной энергии Гиббса G: G = Н – ТS. Равновесии состоянию с неизменной свободной энергией Гиббса G соответствует состав кристалла с некоторой степенью отклонения от стехиометрии. Полностью упорядоченный идеальный кристалл может существовать только при Т = 0 К. Энтропийный член S, отражающий роль природного разупорядочения в кристаллах с повышением значения температуры Т, приобретает все большее значение и при равновесии состоянию с неизменной свободной энергией Гиббса G соответствует состав кристалла с некоторой степенью отклонения от
Фазы переменного состава Промежуточная фаза является фазой переменного состава. На диаграмме существует область гомогенности (область g ). Составы, расположенные в области левее Аm. Вn, принято рассматривать как твердый раствор компонента А в химическом соединении, а составы, расположенные правее – как раствор компонента В в этом же соединении. При заданных значениях давления и температуры равновесной является атомная структура, отвечающая минимуму свободной энергии Гиббса G: G = Н – ТS. Равновесии состоянию с неизменной свободной энергией Гиббса G соответствует состав кристалла с некоторой степенью отклонения от стехиометрии. Полностью упорядоченный идеальный кристалл может существовать только при Т = 0 К. Энтропийный член S, отражающий роль природного разупорядочения в кристаллах с повышением значения температуры Т, приобретает все большее значение и при равновесии состоянию с неизменной свободной энергией Гиббса G соответствует состав кристалла с некоторой степенью отклонения от
 Дальтониды и бертоллиды Георгий Борисович Бокий (6. 09(9. 10). 1909, Санкт-Петербург - 4. 09. 2001, Москва) Всемирно-известный ученый, профессор, член-корреспондент Академии Наук, создатель и организатор отечественной кристаллохимии, родился 9 октября 1909 г. в Санкт-Петербурге в семье выдающегося потомственного горного инженера , профессора Горного института Б. И. Бокия. Это термины, введённые Н. С. Курнаковым в 1912 -14 для обозначения химических соединений постоянного состава (дальтониды) и переменного состава (бертоллиды). Термин "дальтониды" предложен в память Дж. Дальтона, а термин "бертоллиды" - в память К. Л. Бертолле. Большинство обычных химических соединений является дальтонидами; их состав удовлетворяет законам постоянства состава и кратных отношений. Многочисленные случаи образования бертоллидов открыты в металлических системах, а также среди окислов, сульфидов, карбидов, гидридов и др.
Дальтониды и бертоллиды Георгий Борисович Бокий (6. 09(9. 10). 1909, Санкт-Петербург - 4. 09. 2001, Москва) Всемирно-известный ученый, профессор, член-корреспондент Академии Наук, создатель и организатор отечественной кристаллохимии, родился 9 октября 1909 г. в Санкт-Петербурге в семье выдающегося потомственного горного инженера , профессора Горного института Б. И. Бокия. Это термины, введённые Н. С. Курнаковым в 1912 -14 для обозначения химических соединений постоянного состава (дальтониды) и переменного состава (бертоллиды). Термин "дальтониды" предложен в память Дж. Дальтона, а термин "бертоллиды" - в память К. Л. Бертолле. Большинство обычных химических соединений является дальтонидами; их состав удовлетворяет законам постоянства состава и кратных отношений. Многочисленные случаи образования бертоллидов открыты в металлических системах, а также среди окислов, сульфидов, карбидов, гидридов и др.
 Из книги Г. Б. Бокия «Кристаллохимия» . Н. С. Курнаков, следуя определению Бертолле, писал, что ввиду невозможности приписать бертоллидам какойлибо постоянный и рациональный состав, их следует рассматривать в целом как химическое соединение переменного состава. Это первое по времени определение бертоллидов, в котором сделана попытка проникнуть в сущность понятия. Однако это определение весьма несовершенно Ширина области гомогенности фаз не является признаком, характеризующим принадлежность ее к дальтони-дам или бертоллидам. Эта область может быть очень узка, и тем не менее фаза не обязательно будет при этом дальтопидом. С 1913 по 1928 г. Н. С. Курнаков с учениками продолжал интенсивно разрабатывать высказанные ранее идеи. Для этого он сделал несколько попыток проникнуть в сущность понятия бертоллид как понятие менее ясное, чем дальтонид, и в известном смысле ему противопоставляемое. соединения в состоянии диссоциации или же как твердые растворы определенных соединений или полиморфных модификаций компонентов, которые являются неустойчивыми в свободном состоянии, —так называемые «мнимые соединения»
Из книги Г. Б. Бокия «Кристаллохимия» . Н. С. Курнаков, следуя определению Бертолле, писал, что ввиду невозможности приписать бертоллидам какойлибо постоянный и рациональный состав, их следует рассматривать в целом как химическое соединение переменного состава. Это первое по времени определение бертоллидов, в котором сделана попытка проникнуть в сущность понятия. Однако это определение весьма несовершенно Ширина области гомогенности фаз не является признаком, характеризующим принадлежность ее к дальтони-дам или бертоллидам. Эта область может быть очень узка, и тем не менее фаза не обязательно будет при этом дальтопидом. С 1913 по 1928 г. Н. С. Курнаков с учениками продолжал интенсивно разрабатывать высказанные ранее идеи. Для этого он сделал несколько попыток проникнуть в сущность понятия бертоллид как понятие менее ясное, чем дальтонид, и в известном смысле ему противопоставляемое. соединения в состоянии диссоциации или же как твердые растворы определенных соединений или полиморфных модификаций компонентов, которые являются неустойчивыми в свободном состоянии, —так называемые «мнимые соединения»
 Борис Филиппович Ормонт Материал из Википедии — свободной энциклопедии Борис Филиппович Ормонт (29 января 1900 — 27 марта 1978, Ленинград) — известный специалист в области кристаллохимии и физикохимии твёрдых веществ, доктор химических наук (1939), профессор (1940), создатель термодинамической шкалы твёрдости
Борис Филиппович Ормонт Материал из Википедии — свободной энциклопедии Борис Филиппович Ормонт (29 января 1900 — 27 марта 1978, Ленинград) — известный специалист в области кристаллохимии и физикохимии твёрдых веществ, доктор химических наук (1939), профессор (1940), создатель термодинамической шкалы твёрдости
 Б. Ф. Ормонт
Б. Ф. Ормонт
 Кристаллохимическое приближение фаз переменного состава. Отклонение от стехиометрии. Все вещества в парообразном или газообразном состоянии существуют в виде молекул или атомов, но не все вещества состоят из молекул в твердом состоянии. В немолекулярных кристаллах электронная плотность существенно перераспределена по сравнению с молекулой. Таким образом, за свойства кристаллов отвечает фаза, а не молекула. Фазой обычно называют гомогенную часть гетерогенной системы, отделенную от других ее частей поверхностью раздела. Более строгое определение фазы заключается в том, что каждая фаза должна отличаться от других фаз системы строением и видом зависимости свойств от параметров состояния, т. е. иметь собственное уравнение состояния: , где G – энергия Гиббса, S – энтропия, V – объем фазы, ni – число молей i-го компонента.
Кристаллохимическое приближение фаз переменного состава. Отклонение от стехиометрии. Все вещества в парообразном или газообразном состоянии существуют в виде молекул или атомов, но не все вещества состоят из молекул в твердом состоянии. В немолекулярных кристаллах электронная плотность существенно перераспределена по сравнению с молекулой. Таким образом, за свойства кристаллов отвечает фаза, а не молекула. Фазой обычно называют гомогенную часть гетерогенной системы, отделенную от других ее частей поверхностью раздела. Более строгое определение фазы заключается в том, что каждая фаза должна отличаться от других фаз системы строением и видом зависимости свойств от параметров состояния, т. е. иметь собственное уравнение состояния: , где G – энергия Гиббса, S – энтропия, V – объем фазы, ni – число молей i-го компонента.
 В. Б. Алесковский Валентин Борисович Алесковский (1912 -2006) – выдающийся ученый в области химии твердого тела и технологии неорганических материалов, автор более 450 научных публикаций, в том числе 12 монографий и учебников и более 150 изобретений. Основным направлением исследований В. Б. Алесковского является изучение природы и химических превращений твердых веществ, в том числе высокоорганизованных веществ. Он – основатель и руководитель ведущей научной школы России "Химия высокоорганизованных веществ". Широко известны его работы по созданию (в 1960 -х годах) по некоторой аналогии с репликацией ДНК процесса химической сборки (ХС) и одновременно метода синтеза твердых соединений воспроизводимого состава методом молекулярного наслаивания (химической сборки). Этот метод получил развитие за рубежом спустя 20 лет и известен под названием атомной послойной эпитаксии (ALE) и в настоящее время является одним из основных методов синтеза материалов для микроэлектроники.
В. Б. Алесковский Валентин Борисович Алесковский (1912 -2006) – выдающийся ученый в области химии твердого тела и технологии неорганических материалов, автор более 450 научных публикаций, в том числе 12 монографий и учебников и более 150 изобретений. Основным направлением исследований В. Б. Алесковского является изучение природы и химических превращений твердых веществ, в том числе высокоорганизованных веществ. Он – основатель и руководитель ведущей научной школы России "Химия высокоорганизованных веществ". Широко известны его работы по созданию (в 1960 -х годах) по некоторой аналогии с репликацией ДНК процесса химической сборки (ХС) и одновременно метода синтеза твердых соединений воспроизводимого состава методом молекулярного наслаивания (химической сборки). Этот метод получил развитие за рубежом спустя 20 лет и известен под названием атомной послойной эпитаксии (ALE) и в настоящее время является одним из основных методов синтеза материалов для микроэлектроники.
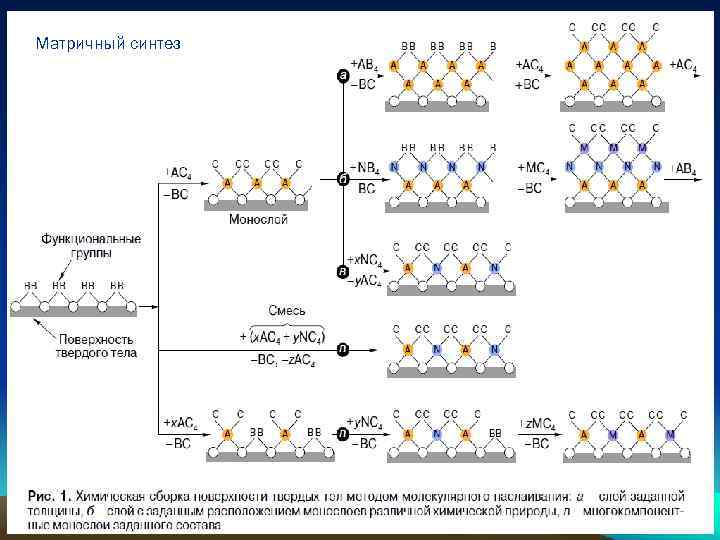 Матричный синтез
Матричный синтез
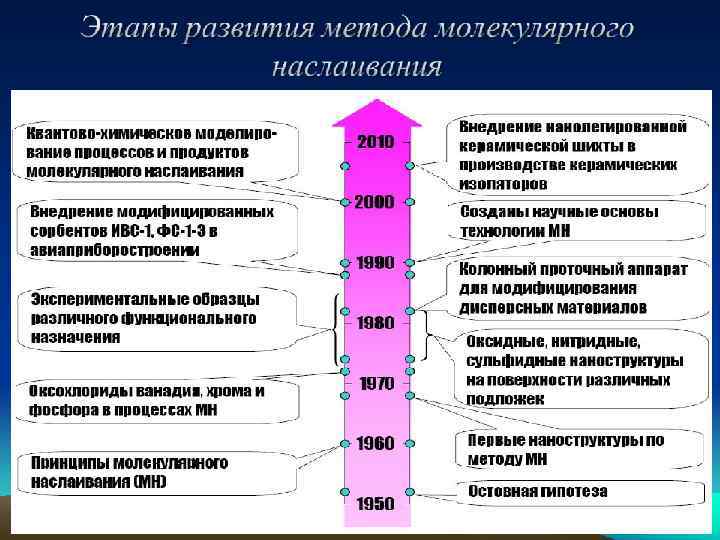
 Цитаты: "Долгое время химия имела дело только с низкомолекулярными химическими индивидами – соединениями постоянного состава, так как вместо высокомолекулярных и надмолекулярных высокоорганизованных индивидов в химических реакциях получаются смеси их аналогов, изомеров и гомологов. Последние, тем не менее, принимают за индивидуальные вещества переменного состава – нестехиометрические соединения. Тем самым всякая мысль о существовании высокоорганизованных химических индивидов (ВХИ) полностью отвергается. Но в начале 1960 -х годов, как высокомолекулярные, так и низкомолекулярные химические индивиды были получены". . «Подставляя в формулу известные значения N, узнаем, как и ожидалось, вероятность образования низкомолекулярных индивидов близка к единице, а высокомолекулярных и надмолекулярных крайне мала, » н. «В то же время вероятность образования смесей всех возможных высоко- и надмолекулярных соединений данных элементов Рс равна единице: » . » Это и порождает феномен нестехиометрических соединений" [ с. 10… 11]. »
Цитаты: "Долгое время химия имела дело только с низкомолекулярными химическими индивидами – соединениями постоянного состава, так как вместо высокомолекулярных и надмолекулярных высокоорганизованных индивидов в химических реакциях получаются смеси их аналогов, изомеров и гомологов. Последние, тем не менее, принимают за индивидуальные вещества переменного состава – нестехиометрические соединения. Тем самым всякая мысль о существовании высокоорганизованных химических индивидов (ВХИ) полностью отвергается. Но в начале 1960 -х годов, как высокомолекулярные, так и низкомолекулярные химические индивиды были получены". . «Подставляя в формулу известные значения N, узнаем, как и ожидалось, вероятность образования низкомолекулярных индивидов близка к единице, а высокомолекулярных и надмолекулярных крайне мала, » н. «В то же время вероятность образования смесей всех возможных высоко- и надмолекулярных соединений данных элементов Рс равна единице: » . » Это и порождает феномен нестехиометрических соединений" [ с. 10… 11]. »
 Приближение Ф. Крёгера Обозначения точечных дефектов: Прописная буква – тип дефекта: A, B, … – атомы, V – вакансия (h – дырка, e – электрон). Нижний индекс – в какой позиции находится дефект: AA – атом в регулярном узле, AB – атом в «чужой» подрешетке, Ai – атом в междоузлии, Vi – свободное междоузлие. Верхний индекс – (эффективный) заряд – заряд атомов или вакансий по отношению к нормальным составляющим решетки: x – нейтральный, • - положительный, ‘ – отрицательный (количество надстрочных индексов соответствует величине заряда) Дефекты рассматриваются как квазичастицы, к которым применимы законы сохранения заряда, вещества и количества окружающих данную позицию «противо» узлов (образование вакансии катиона должно автоматически привести к эквивалентным изменениям в анионной подрешетке и наоборот). Дефекты Шоттки – вакансии (в катионной и анионной подрешктке), дефекты Френкеля – переход атома в междоузлие, антиструктурные дефекты – обмен эквивалентного атомов/ионов между подрешетками.
Приближение Ф. Крёгера Обозначения точечных дефектов: Прописная буква – тип дефекта: A, B, … – атомы, V – вакансия (h – дырка, e – электрон). Нижний индекс – в какой позиции находится дефект: AA – атом в регулярном узле, AB – атом в «чужой» подрешетке, Ai – атом в междоузлии, Vi – свободное междоузлие. Верхний индекс – (эффективный) заряд – заряд атомов или вакансий по отношению к нормальным составляющим решетки: x – нейтральный, • - положительный, ‘ – отрицательный (количество надстрочных индексов соответствует величине заряда) Дефекты рассматриваются как квазичастицы, к которым применимы законы сохранения заряда, вещества и количества окружающих данную позицию «противо» узлов (образование вакансии катиона должно автоматически привести к эквивалентным изменениям в анионной подрешетке и наоборот). Дефекты Шоттки – вакансии (в катионной и анионной подрешктке), дефекты Френкеля – переход атома в междоузлие, антиструктурные дефекты – обмен эквивалентного атомов/ионов между подрешетками.
 Фазы переменного состава Промежуточная фаза является фазой переменного состава. На диаграмме существует область гомогенности (область g ). Составы, расположенные в области левее Аm. Вn, принято рассматривать как твердый раствор компонента А в химическом соединении, а составы, расположенные правее – как раствор компонента В в этом же соединении.
Фазы переменного состава Промежуточная фаза является фазой переменного состава. На диаграмме существует область гомогенности (область g ). Составы, расположенные в области левее Аm. Вn, принято рассматривать как твердый раствор компонента А в химическом соединении, а составы, расположенные правее – как раствор компонента В в этом же соединении.
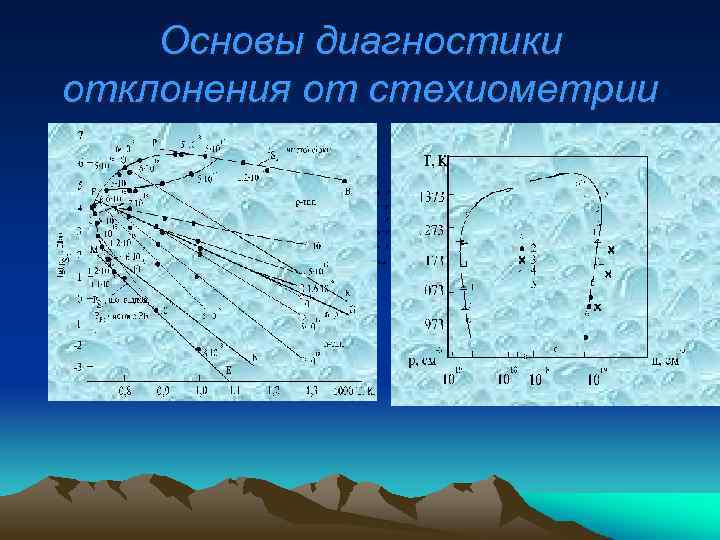 Основы диагностики отклонения от стехиометрии
Основы диагностики отклонения от стехиометрии
 Зломанов В. П. , Новоселова А. В. P-T-x-диаграммы состояния систем металл-халькоген— М. : Наука, 1987. — 207 Алекса ндра Васи льевна Новосё лова (10 (23) марта 1900, деревня Верезино, ныне Леушинского сельского поселения Кашинского района Тверской области — 27 сентября 1986, Москва) — советский химик-неорганик, действительный член Академии наук СССР (1970), лауреат Сталинской (1948) и Государственной (1981) премий СССР, Герой Социалистического Труда (1980). Проф. Зломанов Владимир. Павлович, МГУ, химфак
Зломанов В. П. , Новоселова А. В. P-T-x-диаграммы состояния систем металл-халькоген— М. : Наука, 1987. — 207 Алекса ндра Васи льевна Новосё лова (10 (23) марта 1900, деревня Верезино, ныне Леушинского сельского поселения Кашинского района Тверской области — 27 сентября 1986, Москва) — советский химик-неорганик, действительный член Академии наук СССР (1970), лауреат Сталинской (1948) и Государственной (1981) премий СССР, Герой Социалистического Труда (1980). Проф. Зломанов Владимир. Павлович, МГУ, химфак
 Основы физико-химического анализа C H h. B O h. A h. C A а . B C a T 2 T T 4 3 T T 6 5 AС T 6 T 5 T T 3 4 T 2 x 1 T 1 A b BС O x 2 x 3 x 4 B В основе ФХА лежат правило фаз Гиббса и принципы непрерывности и соответствия. Принцип непрерывности. При непрерывных изменениях параметров состояния свойства системы изменяются также непрерывно (при условии, что число фаз в системе остается постоянным). При изменении числа фаз некоторые свойства системы меняются скачком. Принцип соответствия. Каждой фазе или совокупности фаз системы соответствует определенный геометрический образ (точка, линия, поверхность, объем) на диаграмме "состав – свойство".
Основы физико-химического анализа C H h. B O h. A h. C A а . B C a T 2 T T 4 3 T T 6 5 AС T 6 T 5 T T 3 4 T 2 x 1 T 1 A b BС O x 2 x 3 x 4 B В основе ФХА лежат правило фаз Гиббса и принципы непрерывности и соответствия. Принцип непрерывности. При непрерывных изменениях параметров состояния свойства системы изменяются также непрерывно (при условии, что число фаз в системе остается постоянным). При изменении числа фаз некоторые свойства системы меняются скачком. Принцип соответствия. Каждой фазе или совокупности фаз системы соответствует определенный геометрический образ (точка, линия, поверхность, объем) на диаграмме "состав – свойство".
 Прогнозирование тройных полупроводниковых соединений Нина Александровна Горюнова (1916− 1971) Разрез Cu 2 Se 3 – In 2 Se в концентрационном треугольнике Cu – In – Se соответствует геометрическому образу составов в системе Cu – In – Se, в которых на каждый атом приходится в среднем 4 электрона. Условие "8" удовлетворяет фигуративным точкам In 2 Se 3 и Cu 2 Se на сторонах концентрационного треугольника и разрезу In 2 Se 3 – Cu 2 Se Точка пересечения составов Cu 2 Se 3 и In 2 Se 3 и Cu 2 Se соответствует геометрическому образу состава тройного соединения, для которого удовлетворяются оба условия "4" и "8": Cu 2 Se 3 + In 2 Se = In 2 Se 3 + Cu 2 Se. Этой точке соответствует тройное соединение Cu. In. Se.
Прогнозирование тройных полупроводниковых соединений Нина Александровна Горюнова (1916− 1971) Разрез Cu 2 Se 3 – In 2 Se в концентрационном треугольнике Cu – In – Se соответствует геометрическому образу составов в системе Cu – In – Se, в которых на каждый атом приходится в среднем 4 электрона. Условие "8" удовлетворяет фигуративным точкам In 2 Se 3 и Cu 2 Se на сторонах концентрационного треугольника и разрезу In 2 Se 3 – Cu 2 Se Точка пересечения составов Cu 2 Se 3 и In 2 Se 3 и Cu 2 Se соответствует геометрическому образу состава тройного соединения, для которого удовлетворяются оба условия "4" и "8": Cu 2 Se 3 + In 2 Se = In 2 Se 3 + Cu 2 Se. Этой точке соответствует тройное соединение Cu. In. Se.
 Кристаллохимическое приближение фаз переменного состава. Отклонение от стехиометрии. Все вещества в парообразном или газообразном состоянии существуют в виде молекул или атомов, но не все вещества состоят из молекул в твердом состоянии. В немолекулярных кристаллах электронная плотность существенно перераспределена по сравнению с молекулой. Таким образом, за свойства кристаллов отвечает фаза, а не молекула. Фазой обычно называют гомогенную часть гетерогенной системы, отделенную от других ее частей поверхностью раздела. Более строгое определение фазы заключается в том, что каждая фаза должна отличаться от других фаз системы строением и видом зависимости свойств от параметров состояния, т. е. иметь собственное уравнение состояния: , где G – энергия Гиббса, S – энтропия, V – объем фазы, ni – число молей i-го компонента.
Кристаллохимическое приближение фаз переменного состава. Отклонение от стехиометрии. Все вещества в парообразном или газообразном состоянии существуют в виде молекул или атомов, но не все вещества состоят из молекул в твердом состоянии. В немолекулярных кристаллах электронная плотность существенно перераспределена по сравнению с молекулой. Таким образом, за свойства кристаллов отвечает фаза, а не молекула. Фазой обычно называют гомогенную часть гетерогенной системы, отделенную от других ее частей поверхностью раздела. Более строгое определение фазы заключается в том, что каждая фаза должна отличаться от других фаз системы строением и видом зависимости свойств от параметров состояния, т. е. иметь собственное уравнение состояния: , где G – энергия Гиббса, S – энтропия, V – объем фазы, ni – число молей i-го компонента.
 Аллотропия форм углерода Полиморфизмом называют способность твердого тела, в том числе соединений, существовать в виде двух или нескольких кристаллических структур (полиморфных модификаций). Аллотропия – способность одного и того же элемента образовывать несколько разных типов простых веществ. Различают аллотропию состава (изменение состава молекул простого вещества) и аллотропию формы (изменение способа размещения молекул или атомов в кристаллах).
Аллотропия форм углерода Полиморфизмом называют способность твердого тела, в том числе соединений, существовать в виде двух или нескольких кристаллических структур (полиморфных модификаций). Аллотропия – способность одного и того же элемента образовывать несколько разных типов простых веществ. Различают аллотропию состава (изменение состава молекул простого вещества) и аллотропию формы (изменение способа размещения молекул или атомов в кристаллах).
 Границы применимости модельных представлений sp 3 ta-С GLCH sp 2 Основные представители семейства аморфных углеродных материалов: ta-C: H алмазоподобный аморфный углерод (ta-C), полимероподобный аморфный DLCH гидрогенизированный углерод (PLCH), алмазоподобный аморфный PLCH гидрогенизированный углерод (DLCH), аморфный гидрогенизированный Нет пленок углерод с жесткими тетраэдральными H связями (ta-C: H), графитоподобный аморфный гидрогенизированный углерод (GLCH). Все эти материалы существенно отличаются по механическим свойствам. Например в графите величина энергетического зазора Eg равна 0, в материалах GLCH Eg возрастает до 1 э. В, в слоях PLCH, как правило, Eg = 2… 4 э. В.
Границы применимости модельных представлений sp 3 ta-С GLCH sp 2 Основные представители семейства аморфных углеродных материалов: ta-C: H алмазоподобный аморфный углерод (ta-C), полимероподобный аморфный DLCH гидрогенизированный углерод (PLCH), алмазоподобный аморфный PLCH гидрогенизированный углерод (DLCH), аморфный гидрогенизированный Нет пленок углерод с жесткими тетраэдральными H связями (ta-C: H), графитоподобный аморфный гидрогенизированный углерод (GLCH). Все эти материалы существенно отличаются по механическим свойствам. Например в графите величина энергетического зазора Eg равна 0, в материалах GLCH Eg возрастает до 1 э. В, в слоях PLCH, как правило, Eg = 2… 4 э. В.
 Диагностика наноструктурированных слоев
Диагностика наноструктурированных слоев
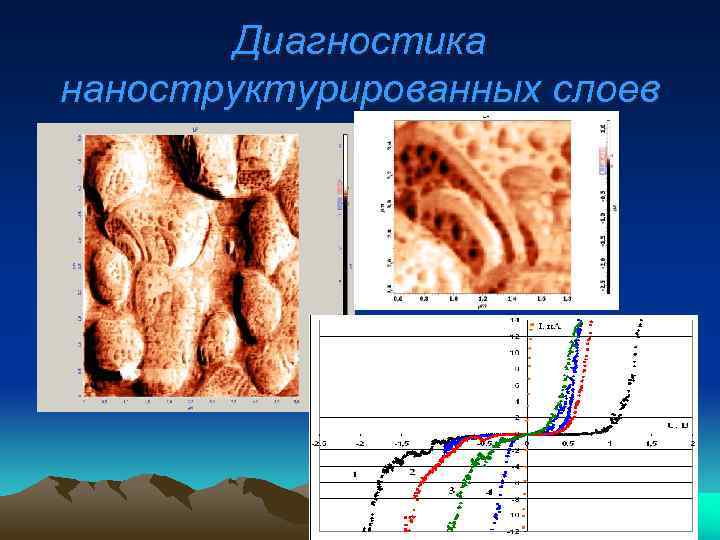 Диагностика наноструктурированных слоев
Диагностика наноструктурированных слоев
 Диагностика наноструктурированных слоев 1 2 p n 3 4
Диагностика наноструктурированных слоев 1 2 p n 3 4
 Диагностика наноструктурированных слоев
Диагностика наноструктурированных слоев
 Диагностика наноструктурированных слоев а) б)
Диагностика наноструктурированных слоев а) б)
 Выводы Любые модельные представления имеют границы применимости. Последовательное использование схемы физико-химического анализа, сформулированное в предыдущем разделе, приводит к следующим выводам: 1. Продукты метода молекулярной химической сборки и фазы переменного состава – совершенно различные объекты ( даже если у них близкие составы). Эти объекты находятся в разных местах по координатам "дисперсность – размер" и "структура". Равновесная фаза в твердом агрегатном состоянии имеет кристаллическую решетку, а отклонение от стехиометрии обусловлено образованием точечных дефектов. 2. Распространение принципов химической сборки на любое твердое тело неправомочно, также как применение термина "фаза переменного состава" на продукты химической сборки. Это не всегда учитывается при внедрении химических методов нанотехнологии для получения слоев с полупроводниковыми свойствами
Выводы Любые модельные представления имеют границы применимости. Последовательное использование схемы физико-химического анализа, сформулированное в предыдущем разделе, приводит к следующим выводам: 1. Продукты метода молекулярной химической сборки и фазы переменного состава – совершенно различные объекты ( даже если у них близкие составы). Эти объекты находятся в разных местах по координатам "дисперсность – размер" и "структура". Равновесная фаза в твердом агрегатном состоянии имеет кристаллическую решетку, а отклонение от стехиометрии обусловлено образованием точечных дефектов. 2. Распространение принципов химической сборки на любое твердое тело неправомочно, также как применение термина "фаза переменного состава" на продукты химической сборки. Это не всегда учитывается при внедрении химических методов нанотехнологии для получения слоев с полупроводниковыми свойствами
 Литература Книги и учебные пособия доступны для бесплатного скачивания. см www. twirpx. com/files
Литература Книги и учебные пособия доступны для бесплатного скачивания. см www. twirpx. com/files
 Спасибо за внимание !
Спасибо за внимание !


