Дегидрирование н-бутана.pptx
- Количество слайдов: 16

Дегидрирование н-бутана

Бутадиен-1, 3 может быть получен: • 1. Выделением из С 4 -фракции продуктов пиролиза жидких нефтепродуктов, содержащей 20— 30% бутадиена-1, 3; • 2. Каталитическим дегидрированием н-бутиленовой фракции, выделенной из продуктов пиролиза нефтепродуктов • 3. Каталитическим дегидрированием н-бутана, выделенного из попутного нефтяного газа • 4. Каталитическим расщеплением этанола (С. В. Лебедев) 2 С 2 Н 5 ОН → 2 Н 2 О + Н 2 + С 4 Н 6 • 5. Взаимодействием ацетилена с формальдегидом через бутандиол-1, 3 и бутандиол-1, 3 (В. Реппе) • 6. Из ацеталъдегида через альдоль и бутандиол-1, 3 (Н. Н. Остромысленский)

Термохимическое уравнение CH 3 -CH 2 -CH 3 ↔ CH 3 -CH 2 -CH=CH 2 + H 2 - Q 1; • Q 1 = 30 ккал/моль = 125, 4 к. Дж/моль • • где: I – интенсивность процесса, • B – выход продукта, • t – время пребывания реагентов.

Термодинамика количественно

Влияние давления и концентрации • • Pбутилена =Xбутилена*Pобщ. Pводорода=Xводорода*Pобщ. Pбутана =Xбутана *Pобщ. , где Xбутилена, Xводорода, Xбутана - мольные доли бутилена, водорода и бутана в реакционной смеси. • Pобщ. – общее давление в системе.

Кинетика • Основная реакция CH 3 – CH - CH 3 ↔CH 2 = CH – CH 2 – CH 3 + H 2 - Q 1 • Побочные реакции CH 3 - CH 2 –CH 3 →CH 3 – CH 3 + CH 2 = CH 2 - Q 2 CH 3 – CH 2 - CH 2 – CH 3 → CH 3 – CH 3 + CH 4 + C - Q 3

• W 1 =k 1*Pбутана, где: k 1 – константа скорости прямой реакции, Pбутана – парциальное давление бутана. • Pбут. = Xбут. *Po. Xбут. – мольная доля бутана в реакционной смеси Po – общее давление газовой смеси • W 1 = k 1*Xбут. Po По Аррениусу: W = k X P F 1 1 бут. o

Регенерация катализатора • C + O 2 →CO 2 + Qэкзо. При этом одновременно идет окисление трехвалентной окиси хрома до шестивалентной окиси хрома по уравнению: • Cr 2 O 3 + 1, 5 O 2 → 2 Cr. O 3 Шестивалентная окись хрома не активна в реакции дегидрирования, поэтому ее восстанавливают в активное состояние реакцией: • 2 Cr. O 3 + 3 H 2 →Cr 2 O 3 + 3 H 2 O
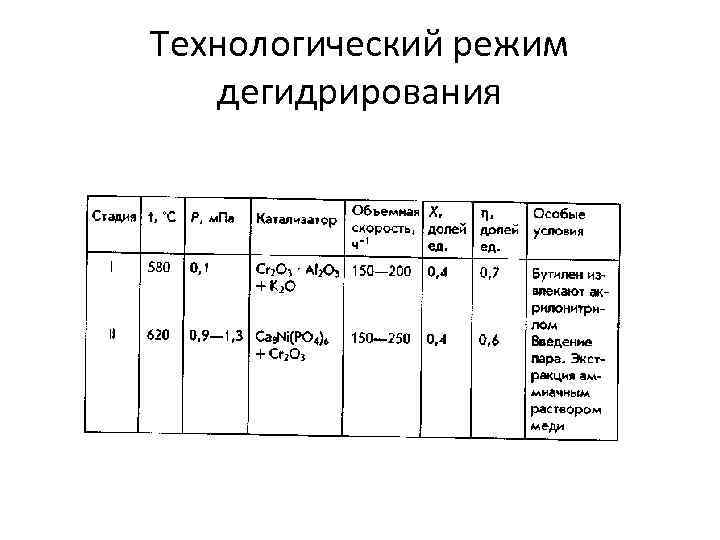
Технологический режим дегидрирования


Дегидирование бутилена • CH 2 = CH – CH 2 – CH 3 ↔ CH 2 = CH – CH = CH 2 + H 2 - Q 1 = 27 kkal/mol = 112 kkal/mol

Pdiwinil– парциальное давление дивинила, Pwodor. – парциальное давление водорода, Pbuten - парциальное давление бутена. • Pdiwinil = Xdiwinil Po; Pwodor= Xwodor Po ; Pbuten = Xbuten Po. Xdiwinil, Xwodor, Xbuten - мольные доли в реакционной смеси дивинила, водорода, бутена. Po – Общее давление газовой смеси. При t = Const, KP = Const.

кинетика • CH 2 = CH – CH 2 – CH 3 ↔ CH 2 = CH – CH = CH 2 + H 2 - Q 1 Основная реакция – 1 сопровождается рядом побочных реакций: Реакцией полимеризации с образованием смолистых продуктов: • n ( CH 2=CH-CH=CH 2 ) → − [ CH 2=CH-CH=CH 2 ] – [ CH 2=CH-CH=CH 2 ]n-1 Реакцией распада с образованием кокса – углистых отложений: • CH 2 = CH – CH = CH 2 → CH 4 + C 2 H 2 + C – Q 3 W 1 = k 1 Pbuten W 2 =k 2 Pdiwinil W 3 = k Pdiwinil W 1 = k 1 Pbutena F , где: k –консанта скорости дегидрирования бутена, Pbuteha – парциальное давление бутена, F – удельная поверхность катализатора, м 2/г. Pbut = Xbut Po. Xbut – мольная доля бутена в реакционной смеси, Po - общее давление реакционной смеси. • W 1 = k 1 Xbut Po F

Регенерация катализатора Ca 8 Ni (PO 4 )6 C + O 2 → CO 2 + Q экзо C + HOH ↔ CO 2 + H 2 − Q

Принципиальная схема двухстадийного процесса дегидрирования н-бутана • Сu 2(NН 3)4(СН 3 СОО)2+С 4 Н 6 ↔ С 4 Нб(NН 3)3 Сu 2(СН 3 СОО)2+NН 3

Дегидрирование н-бутана.pptx