Дефекты в твердом теле Многие важнейшие

























































































Дефекты в твердом теле.ppt лекц..ppt
- Количество слайдов: 89
 Дефекты в твердом теле Многие важнейшие свойства твердого тела объясняются наличием в нем нарушений или дефектов. Эти термины являются синонимами и используются для того, чтобы определить какую либо химическую примесь или нарушение структуры, приводящее к отличию твердого вещества от химически чистого и совершенного кристалла
Дефекты в твердом теле Многие важнейшие свойства твердого тела объясняются наличием в нем нарушений или дефектов. Эти термины являются синонимами и используются для того, чтобы определить какую либо химическую примесь или нарушение структуры, приводящее к отличию твердого вещества от химически чистого и совершенного кристалла
 • Дефекты могут быть собственными, если они образуются вследствие теплового движения в кристалле, находящимся в условиях теплового равновесия при температуре выше 0 0 К. Другие дефекты, такие как химические примеси, могут появится в твердом веществе случайно или в результате преднамеренного введения добавок
• Дефекты могут быть собственными, если они образуются вследствие теплового движения в кристалле, находящимся в условиях теплового равновесия при температуре выше 0 0 К. Другие дефекты, такие как химические примеси, могут появится в твердом веществе случайно или в результате преднамеренного введения добавок
 • Собственные дефекты могут присутствовать в концентрациях, отличных от тех, которые можно ожидать в чистых кристаллах в состоянии равновесия. Это может быть результатом случайного или преднамеренного введения в кристалл различного рода дефектов, взаимодействия между дефектами или следствием неравновесных условий.
• Собственные дефекты могут присутствовать в концентрациях, отличных от тех, которые можно ожидать в чистых кристаллах в состоянии равновесия. Это может быть результатом случайного или преднамеренного введения в кристалл различного рода дефектов, взаимодействия между дефектами или следствием неравновесных условий.
 Электроны и дырки • В идеальном кристалл при 0 0 К, согласно распределению Ферми-Дирака, все электроны должны располагаться на наинизших из возможных разрешенных энергетических уровней . При температурах выше 0 0 К за счет энергии теплового движения определенное число электронов может возбуждаться на более высокие энергетические уровни, что определяется энергией разрешенных состояний и температурой
Электроны и дырки • В идеальном кристалл при 0 0 К, согласно распределению Ферми-Дирака, все электроны должны располагаться на наинизших из возможных разрешенных энергетических уровней . При температурах выше 0 0 К за счет энергии теплового движения определенное число электронов может возбуждаться на более высокие энергетические уровни, что определяется энергией разрешенных состояний и температурой
 • Так, в кристалле кремния атомы связаны ковалентными связями. При 0 К все валентные электроны находятся в целиком заполненной зоне, а следующая за ней энергетическая зона не заполнена. Согласно теории валентных связей, можно считать, что пара валентных электронов, обеспечивающих ковалентную связь между атомами кремния, одновременно принадлежат двум соседним атомам кремния.
• Так, в кристалле кремния атомы связаны ковалентными связями. При 0 К все валентные электроны находятся в целиком заполненной зоне, а следующая за ней энергетическая зона не заполнена. Согласно теории валентных связей, можно считать, что пара валентных электронов, обеспечивающих ковалентную связь между атомами кремния, одновременно принадлежат двум соседним атомам кремния.
 • При температурах выше 0 0 К некоторые из этих электронов возбуждаются термически и приобретают способность перемещаться по кристаллу. Такие электроны называются электронами проводимости. Термически возбужденные электроны обуславливают электропроводимость многих твердых тел, которые обычно являются диэлектриками из-за наличия полностью заполненной и пустой зон.
• При температурах выше 0 0 К некоторые из этих электронов возбуждаются термически и приобретают способность перемещаться по кристаллу. Такие электроны называются электронами проводимости. Термически возбужденные электроны обуславливают электропроводимость многих твердых тел, которые обычно являются диэлектриками из-за наличия полностью заполненной и пустой зон.
 • Вакантное место, возникающее в системе с ковалентной связью после удаления электрона, называют положительной дыркой. Наличие дырок, как и наличие электронов, может обуславливать механизм электропроводимости. Это описание иллюстрирует рис. 24.
• Вакантное место, возникающее в системе с ковалентной связью после удаления электрона, называют положительной дыркой. Наличие дырок, как и наличие электронов, может обуславливать механизм электропроводимости. Это описание иллюстрирует рис. 24.
 • Последовательный переход валентных электронов на вакантные места можно рассматривать как движение дырок в направлении обратном движению электрона в электрическом поле. Поэтому термин положительная дырка можно рассматривать как движение в электрическом поле эффективного положительного заряда, несмотря на то, что в действительности имеет место перемещение валентного электрона в противоположном направлении.
• Последовательный переход валентных электронов на вакантные места можно рассматривать как движение дырок в направлении обратном движению электрона в электрическом поле. Поэтому термин положительная дырка можно рассматривать как движение в электрическом поле эффективного положительного заряда, несмотря на то, что в действительности имеет место перемещение валентного электрона в противоположном направлении.
 • При определенных условиях (например при поглощении света) концентрации электронов и дырок могут в течение короткого периода отличаться от равновесных значений. Кроме того, концентрации электронов и дырок не обязательно равны между собой.
• При определенных условиях (например при поглощении света) концентрации электронов и дырок могут в течение короткого периода отличаться от равновесных значений. Кроме того, концентрации электронов и дырок не обязательно равны между собой.
 • У большинства ионных солей валентные электроны сосредоточены на определенных ионах, но в случае металлов это весьма неточно. Строение ионных и ковалентных кристаллов можно рассматривать в рамках представлений о электронах и дырках. Рассмотрим окись никеля, в которой ионы никеля двухвалентны.
• У большинства ионных солей валентные электроны сосредоточены на определенных ионах, но в случае металлов это весьма неточно. Строение ионных и ковалентных кристаллов можно рассматривать в рамках представлений о электронах и дырках. Рассмотрим окись никеля, в которой ионы никеля двухвалентны.
 • В решетку окиси легко ввести небольшое количество ионов трехвалентного никеля. В результате большинство катионных узлов будет занять Ni +2 , но некоторые катионные узлы будут заняты Ni +3 это эквивалентно введению в кристалл положительных дырок, поскольку можно считать, что в этих местах отсутствуют валентные электроны.
• В решетку окиси легко ввести небольшое количество ионов трехвалентного никеля. В результате большинство катионных узлов будет занять Ni +2 , но некоторые катионные узлы будут заняты Ni +3 это эквивалентно введению в кристалл положительных дырок, поскольку можно считать, что в этих местах отсутствуют валентные электроны.
 • Различие между ковалентными кристаллами типа кремния и кристаллами типа закиси никеля состоит в том, что электроны и дырки в Ni. O локализованы в гораздо большей степени. Другими словами. электроны и дырки находятся длительное время на отдельных катионах, прежде чем перескочить на соседнее место и такой перескок возможен всякий раз, когда ионы в разных валентных состояниях находятся по-соседству.
• Различие между ковалентными кристаллами типа кремния и кристаллами типа закиси никеля состоит в том, что электроны и дырки в Ni. O локализованы в гораздо большей степени. Другими словами. электроны и дырки находятся длительное время на отдельных катионах, прежде чем перескочить на соседнее место и такой перескок возможен всякий раз, когда ионы в разных валентных состояниях находятся по-соседству.
 • Переходы такого рода изменяют порядок расположения ионов: • …Ni+2 Ni+3 Ni+2 … → …Ni+2 Ni+3 Ni+2… • Этот механизм обуславливает электронную проводимость в таких веществах, заметим, что при этом не происходит движения ионов.
• Переходы такого рода изменяют порядок расположения ионов: • …Ni+2 Ni+3 Ni+2 … → …Ni+2 Ni+3 Ni+2… • Этот механизм обуславливает электронную проводимость в таких веществах, заметим, что при этом не происходит движения ионов.
 • В то же время двухвалентный ион, находящийся среди трехвалентных, соответствует иону проводимости. Этот вид проводимости характерен для соединений переходных металлов, например окислов переходных элементов 3 d-ряда.
• В то же время двухвалентный ион, находящийся среди трехвалентных, соответствует иону проводимости. Этот вид проводимости характерен для соединений переходных металлов, например окислов переходных элементов 3 d-ряда.
 • Электропроводимость их пропорциональна подвижности электронов или дырок, а подвижность локализованных электронов или дырок обычно невелика, порядок 1 см 2 в -1 сек - или даже значительно меньше, тогда как для ковалентных полупроводников типичны величины порядка сотен или десятков тысяч
• Электропроводимость их пропорциональна подвижности электронов или дырок, а подвижность локализованных электронов или дырок обычно невелика, порядок 1 см 2 в -1 сек - или даже значительно меньше, тогда как для ковалентных полупроводников типичны величины порядка сотен или десятков тысяч
 Точечные дефекты • Простейшие структурные дефекты, роль которых играют единичные примесные атомы или нарушения в узлах решетки, называют точечными дефектами. Они бывают трех видов. Во-первых это атомы, находящиеся в междоузлиях. (рис. 25)
Точечные дефекты • Простейшие структурные дефекты, роль которых играют единичные примесные атомы или нарушения в узлах решетки, называют точечными дефектами. Они бывают трех видов. Во-первых это атомы, находящиеся в междоузлиях. (рис. 25)
 • В решетках с большими пустотами между узлами междоузельные дефекты образуются легче, чем в тех решетках, где междоузельное пространство мало. Соответственно малые по размерам атомы или ионы могут легче, чем крупные, занимать междоузлия
• В решетках с большими пустотами между узлами междоузельные дефекты образуются легче, чем в тех решетках, где междоузельное пространство мало. Соответственно малые по размерам атомы или ионы могут легче, чем крупные, занимать междоузлия
 • Во-вторых, в узлах решетки, которые в идеальном кристалле заполнены, атомы могут отсутствовать. Точечные дефекты такого вида называются вакансиями. В элементарной ковалентной решетке отсутствие одного атома (электрически нейтрального) не вызывает существенных нарушений в общем балансе электрических зарядов в кристалле.
• Во-вторых, в узлах решетки, которые в идеальном кристалле заполнены, атомы могут отсутствовать. Точечные дефекты такого вида называются вакансиями. В элементарной ковалентной решетке отсутствие одного атома (электрически нейтрального) не вызывает существенных нарушений в общем балансе электрических зарядов в кристалле.
 • Однако в ионном кристалле (если рассматривать его в целом) вакансии в катионной или анионной подрешетке должны быть каким то образом электрически скомпенсированы. Это условие выполняется, если имеется эквивалентное количество катионных и анионных вакансий или если на каждую ионную вакансию приходится такое же число ионов того же знака в междоузлиях
• Однако в ионном кристалле (если рассматривать его в целом) вакансии в катионной или анионной подрешетке должны быть каким то образом электрически скомпенсированы. Это условие выполняется, если имеется эквивалентное количество катионных и анионных вакансий или если на каждую ионную вакансию приходится такое же число ионов того же знака в междоузлиях
 • Комбинацию вакансии и иона в междоузлиях называют жефектом по Френкелю, а комбинацию анионной и катионной вакансий – дефектом по Шоттки. Требования комбинации заряда может быть также удовлетворено, если в кристалле содержится примесь атомов с валентностью, отличной от валентности атомов в самой решетки.
• Комбинацию вакансии и иона в междоузлиях называют жефектом по Френкелю, а комбинацию анионной и катионной вакансий – дефектом по Шоттки. Требования комбинации заряда может быть также удовлетворено, если в кристалле содержится примесь атомов с валентностью, отличной от валентности атомов в самой решетки.
 • Наконец, компенсации можно достичь простым введением избыточных электронов или наоборот удалением их из кристалла. Если вакансия образуется в металле, то происходит одновременное удаление положительно заряженного иона и компенсирующего электрона.
• Наконец, компенсации можно достичь простым введением избыточных электронов или наоборот удалением их из кристалла. Если вакансия образуется в металле, то происходит одновременное удаление положительно заряженного иона и компенсирующего электрона.
 • Считают, что в кристаллах галогенидов щелочных металлов катионные и анионные вакансии присутствуют в равных количествах, а дефекты по Френкелю, образующиеся за счет смещения катионов в междоузлиях, можно обнаружить, например в галогенидах серебра.
• Считают, что в кристаллах галогенидов щелочных металлов катионные и анионные вакансии присутствуют в равных количествах, а дефекты по Френкелю, образующиеся за счет смещения катионов в междоузлиях, можно обнаружить, например в галогенидах серебра.
 • Определенное количество дефектов по Шоттки и Френкелю может возникнуть при температуре выше 00 К в результате термического возбуждения в любом реальном кристалле, который находится в состоянии равновесия. Дефекты по Шоттки обычно снижают плотность кристалла вследствие наличия катионных и анионных вакансий.
• Определенное количество дефектов по Шоттки и Френкелю может возникнуть при температуре выше 00 К в результате термического возбуждения в любом реальном кристалле, который находится в состоянии равновесия. Дефекты по Шоттки обычно снижают плотность кристалла вследствие наличия катионных и анионных вакансий.
 • Дефекты по Френкелю существенно плотность не изменяют. • Другим видом локальных дефектов кристалла является антиструктурное разупорядочение: в кристаллической решетке соединения типа АВ некоторое количество атомов А занимают места атомов В, а равное количество атомов В занимают места атомов А.
• Дефекты по Френкелю существенно плотность не изменяют. • Другим видом локальных дефектов кристалла является антиструктурное разупорядочение: в кристаллической решетке соединения типа АВ некоторое количество атомов А занимают места атомов В, а равное количество атомов В занимают места атомов А.
 • Обмен местами между атомами А и В более вероятен в металлических сплавах, а не ионных соединениях, где для этого необходимо преодолеть большие энергетические барьеры, обусловленные электрическими силами. Этот вид дефектов наблюдается в Bi 2 Te 3 и Mg 2 Sn.
• Обмен местами между атомами А и В более вероятен в металлических сплавах, а не ионных соединениях, где для этого необходимо преодолеть большие энергетические барьеры, обусловленные электрическими силами. Этот вид дефектов наблюдается в Bi 2 Te 3 и Mg 2 Sn.
 • Возможны также промежуточные типы нарушений, например комбинации дефектов по Шоттки и антиструктурного разупорядочению. Так, в Ni. Al никель занимает часть мест, обычно занимаемых атомами алюминия, что приводит к образованию никелевых вакансий.
• Возможны также промежуточные типы нарушений, например комбинации дефектов по Шоттки и антиструктурного разупорядочению. Так, в Ni. Al никель занимает часть мест, обычно занимаемых атомами алюминия, что приводит к образованию никелевых вакансий.
 Примесные атомы • Другой важный вид нарушений структуры кристалла возникает при введении в кристалл приместных атомов. Они могут располагаться в междоузлиях, либо в узлах решетки, в последнем случае они замещают атомы исходного кристалла.
Примесные атомы • Другой важный вид нарушений структуры кристалла возникает при введении в кристалл приместных атомов. Они могут располагаться в междоузлиях, либо в узлах решетки, в последнем случае они замещают атомы исходного кристалла.
 • Для образования междоузельных примесных включений обычно имеет большое значение соотношение между размерами иона и размерами междоузлий. При замещении большое значение имеет электронное строение примесных атомов. Замещение проходит легче, если примесные атомы принадлежат к той же самой или соседним группам периодической системы, что и замещающие атомы.
• Для образования междоузельных примесных включений обычно имеет большое значение соотношение между размерами иона и размерами междоузлий. При замещении большое значение имеет электронное строение примесных атомов. Замещение проходит легче, если примесные атомы принадлежат к той же самой или соседним группам периодической системы, что и замещающие атомы.
 Заряженные и незаряженные дефекты • Во многих местах дефекты могут существовать либо в нейтральном, либо в заряженном состоянии, что является результатом улавливания дефектом избыточного электрона, либо удаления одного из электронов, в нормальном состоянии связанного с дефектом.
Заряженные и незаряженные дефекты • Во многих местах дефекты могут существовать либо в нейтральном, либо в заряженном состоянии, что является результатом улавливания дефектом избыточного электрона, либо удаления одного из электронов, в нормальном состоянии связанного с дефектом.
 • Например, анионная вакансия в кристалле галогенида щелочного металла (хлористого натрия). Удаление иона хлора из узла решетки приводит к тому , что область решетки в непосредственной близости от вакансии приобретает положительный заряд, который может быть нейтрализован путем захвата электрона на дефекте.
• Например, анионная вакансия в кристалле галогенида щелочного металла (хлористого натрия). Удаление иона хлора из узла решетки приводит к тому , что область решетки в непосредственной близости от вакансии приобретает положительный заряд, который может быть нейтрализован путем захвата электрона на дефекте.
 • Другое возможное образование заряда на центре образуется просто при удалении электрона. Этот особый вид центров в галогенидах щелочных металлов носит название F-центров или центров окрашивания, поскольку именно они ответственны за окрашивание, соответствующее поглощению в видимой части спектра.
• Другое возможное образование заряда на центре образуется просто при удалении электрона. Этот особый вид центров в галогенидах щелочных металлов носит название F-центров или центров окрашивания, поскольку именно они ответственны за окрашивание, соответствующее поглощению в видимой части спектра.
 • Аналогичным образом можно рассматривать те атомы в междоузлиях, в отношении которых можно ожидать, что они будут ионизироваться или до положительно заряженного иона за счет потери электрона, или до отрицательно заряженного иона в результате захвата электрона.
• Аналогичным образом можно рассматривать те атомы в междоузлиях, в отношении которых можно ожидать, что они будут ионизироваться или до положительно заряженного иона за счет потери электрона, или до отрицательно заряженного иона в результате захвата электрона.
 • Примесные атомы также могут ионизироваться. Например примесные атомы элементов III и V групп в кристаллах элементов IV группы, таких как кремний (рис. 26). Примесные атомы элементов III и V замещают атомы кремния в кристаллической решетке, но атомы III группы, такие как алюминий, имеют только три валентных электрона. Это приводит к дефициту одного электрона в тетраэдрических ковалентных связях с четырьмя ближними атомами кремния
• Примесные атомы также могут ионизироваться. Например примесные атомы элементов III и V групп в кристаллах элементов IV группы, таких как кремний (рис. 26). Примесные атомы элементов III и V замещают атомы кремния в кристаллической решетке, но атомы III группы, такие как алюминий, имеют только три валентных электрона. Это приводит к дефициту одного электрона в тетраэдрических ковалентных связях с четырьмя ближними атомами кремния
 • Элементы V группы, например фосфор имеют пять валентных электронов и после завершения построения ими четырех ковалентных связей имеют еще один лишний электрон. В каждом из рассмотренных случаев будет происходить образование электрически нейтрального центра. Но такой центр может ионизироваться.
• Элементы V группы, например фосфор имеют пять валентных электронов и после завершения построения ими четырех ковалентных связей имеют еще один лишний электрон. В каждом из рассмотренных случаев будет происходить образование электрически нейтрального центра. Но такой центр может ионизироваться.
 • Примесный атом алюминия может присоединить еще один электрон к центру, в результате чего он будет заряжен отрицательно. Образовавшаяся при этом дырка будет перемещаться в объеме кристалла, являясь носителем положительного заряда.
• Примесный атом алюминия может присоединить еще один электрон к центру, в результате чего он будет заряжен отрицательно. Образовавшаяся при этом дырка будет перемещаться в объеме кристалла, являясь носителем положительного заряда.
 • Тем самым обеспечивается сохранение нейтральности кристалла в целом, но положительные и отрицательные заряды теперь оказываются разделенными внутри твердого тела на значительные расстояния.
• Тем самым обеспечивается сохранение нейтральности кристалла в целом, но положительные и отрицательные заряды теперь оказываются разделенными внутри твердого тела на значительные расстояния.
 • Аналогичным образом примесный атом V группы может потерять избыточный электрон, и положительный заряд образовавшегося центра компенсируется в кристалле как в целом образованием электрона проводимости, несущего отрицательный заряд
• Аналогичным образом примесный атом V группы может потерять избыточный электрон, и положительный заряд образовавшегося центра компенсируется в кристалле как в целом образованием электрона проводимости, несущего отрицательный заряд
 • Дефекты, которые могут ионизироваться (с отрывом электрона), такие, как атомы P в Si или вакансии свинца Pb. S , называют акцепторами. Энергия, необходимая для осуществления подобной ионизации, часто довольно незначительна, поэтому ионизация является достаточно полной даже при комнатной температуре.
• Дефекты, которые могут ионизироваться (с отрывом электрона), такие, как атомы P в Si или вакансии свинца Pb. S , называют акцепторами. Энергия, необходимая для осуществления подобной ионизации, часто довольно незначительна, поэтому ионизация является достаточно полной даже при комнатной температуре.
 • При более низких температурах носители заряда замораживаются на примесных центрах. • Подобным же образом примеси в веществах могут находиться в двух заряженных состояниях. Так, цинк в решетке арсенида галлия занимает узлы галлия и действует как акцептор, тогда как сера занимает узлы мышьяка и проявляет донорные свойства.
• При более низких температурах носители заряда замораживаются на примесных центрах. • Подобным же образом примеси в веществах могут находиться в двух заряженных состояниях. Так, цинк в решетке арсенида галлия занимает узлы галлия и действует как акцептор, тогда как сера занимает узлы мышьяка и проявляет донорные свойства.
 • Кремний может занимать узлы и галлия и мышьяка, на первые он действует как донор, а на вторые - как акцептор. • Иногда может иметь место многократная ионизация дефектных центров. Так, донорный центр может потерять два электрона, в результате чего образуется центр с двумя положительными зарядами, а акцептор может присоединить больше одного электрона.
• Кремний может занимать узлы и галлия и мышьяка, на первые он действует как донор, а на вторые - как акцептор. • Иногда может иметь место многократная ионизация дефектных центров. Так, донорный центр может потерять два электрона, в результате чего образуется центр с двумя положительными зарядами, а акцептор может присоединить больше одного электрона.
 • Примеси могут быть в равной степени и донорами, и акцепторами, как, например, золото и медь в полупроводниковых элементах IV группы. • Не все дефектные центры способны ионизироваться. Иногда требуемая для этого энергия превышает энергию электронного перехода из валентной зоны в зону проводимости, так что ионизацию подобного центра наблюдать не удается, поскольку до нее происходит ионизация самого кристалла.
• Примеси могут быть в равной степени и донорами, и акцепторами, как, например, золото и медь в полупроводниковых элементах IV группы. • Не все дефектные центры способны ионизироваться. Иногда требуемая для этого энергия превышает энергию электронного перехода из валентной зоны в зону проводимости, так что ионизацию подобного центра наблюдать не удается, поскольку до нее происходит ионизация самого кристалла.
 Нестехиометричность • Состав многих соединений, как правило, отклоняется от стехиометрического и добиться их строго стехиометрического состава бывает очень трудно. Примером тому служат соединения II – IV групп типа Cd. S и Zn. O. Бинарные соединения могут быть нестехиометрическими по разным причинам.
Нестехиометричность • Состав многих соединений, как правило, отклоняется от стехиометрического и добиться их строго стехиометрического состава бывает очень трудно. Примером тому служат соединения II – IV групп типа Cd. S и Zn. O. Бинарные соединения могут быть нестехиометрическими по разным причинам.
 • Так, избыток элементами А или В в соединения АВ может объясняться тем, что этот элемент находится в междоузлиях. Кроме того, избыток какого-либо элемента может быть связан с наличием в решетке различного рода вакансий. Например, если хлористый натрий нагреть в атмосфере паров натрия, в кристалл попадает избыточное количество атомов натрия.
• Так, избыток элементами А или В в соединения АВ может объясняться тем, что этот элемент находится в междоузлиях. Кроме того, избыток какого-либо элемента может быть связан с наличием в решетке различного рода вакансий. Например, если хлористый натрий нагреть в атмосфере паров натрия, в кристалл попадает избыточное количество атомов натрия.
 • Избыточные атомы натрия занимают нормальные катионные узлы, при этом образуется равное количество анионных вакансий и поскольку электронейтральность при этом сохраняется, образовавшиеся анионные вакансии связаны с электронами.
• Избыточные атомы натрия занимают нормальные катионные узлы, при этом образуется равное количество анионных вакансий и поскольку электронейтральность при этом сохраняется, образовавшиеся анионные вакансии связаны с электронами.
 • Это и есть так называемые F- центры, в результате их образования кристалл окрашивается в голубой цвет. В качестве другого примера приведем окись титана, которая в зависимости от давления кислорода в окружающей среде, находящейся в равновесии с веществом, может иметь состав от Ti. O 1, 35 до Ti. O 0, 60.
• Это и есть так называемые F- центры, в результате их образования кристалл окрашивается в голубой цвет. В качестве другого примера приведем окись титана, которая в зависимости от давления кислорода в окружающей среде, находящейся в равновесии с веществом, может иметь состав от Ti. O 1, 35 до Ti. O 0, 60.
 • При избытке атомов кислорода имеется соответствующая концентрация вакансий титана, а при избытке атомов титана появляются кислородные вакансии. К числу соединений нестехиометричность которых объясняется наличием междоузельных включения, относится Zn. O, где в междоузлиях имеется избыток атомов цинка.
• При избытке атомов кислорода имеется соответствующая концентрация вакансий титана, а при избытке атомов титана появляются кислородные вакансии. К числу соединений нестехиометричность которых объясняется наличием междоузельных включения, относится Zn. O, где в междоузлиях имеется избыток атомов цинка.
 • Нестехиометричность состава, связанная с образованием вакансий, наблюдается гораздо чаще, чем нестехиометричность, вызванная наличием избытка одного из элементов в междоузлиях.
• Нестехиометричность состава, связанная с образованием вакансий, наблюдается гораздо чаще, чем нестехиометричность, вызванная наличием избытка одного из элементов в междоузлиях.
 • Обычный способ контролирования числа дефектов, обусловленных нестехиометричностью состава, состоит в том, чтобы привести кристалл в равновесие с окружающей средой, состояние которой можно регулировать.
• Обычный способ контролирования числа дефектов, обусловленных нестехиометричностью состава, состоит в том, чтобы привести кристалл в равновесие с окружающей средой, состояние которой можно регулировать.
 Образование вакансий при введении примесных атомов • Другим важным методом введения вакансий в кристалл, является добавление примесных атомов с валентностью, отличающейся от валентности соответствующих атомов самого кристалла. Эта система представляет собой твердый раствор двух соединений
Образование вакансий при введении примесных атомов • Другим важным методом введения вакансий в кристалл, является добавление примесных атомов с валентностью, отличающейся от валентности соответствующих атомов самого кристалла. Эта система представляет собой твердый раствор двух соединений
 • Смешанные кристаллы Ag. Cl и Cd. Cl 2 с малым количеством Cd. Cl 2 показана на рис. 27. В этой системе ионы Cd +2 занимают катионные узлы в решетке, но на каждый ион Cd +2 в кристалле должна приходится одна катионная вакансия (отсутствие в решетке одного иона Ag + ), чтобы электронейтральность кристалла в целом сохранилась.
• Смешанные кристаллы Ag. Cl и Cd. Cl 2 с малым количеством Cd. Cl 2 показана на рис. 27. В этой системе ионы Cd +2 занимают катионные узлы в решетке, но на каждый ион Cd +2 в кристалле должна приходится одна катионная вакансия (отсутствие в решетке одного иона Ag + ), чтобы электронейтральность кристалла в целом сохранилась.
 • Образование вакансий при добавлении примесных атомов можно легко показать с помощью измерения плотности кристаллов. Так, Ca. Cl 2 , введенный в KCl уменьшает плотность кристаллов.
• Образование вакансий при добавлении примесных атомов можно легко показать с помощью измерения плотности кристаллов. Так, Ca. Cl 2 , введенный в KCl уменьшает плотность кристаллов.
 • Экспериментальные данные довольно хорошо согласуются с расчетными значениями уменьшения плотности, вычисленными на основании предположения, что ион калия замещен на ион кальция плюс катионную вакансию. Предполагается, что объем кристалла при этом не изменяется.
• Экспериментальные данные довольно хорошо согласуются с расчетными значениями уменьшения плотности, вычисленными на основании предположения, что ион калия замещен на ион кальция плюс катионную вакансию. Предполагается, что объем кристалла при этом не изменяется.
 • Если бы плотность изменялась аддитивно, а вакансии не образовывались, появление смешанных кристаллов должно было бы приводить к росту плотности.
• Если бы плотность изменялась аддитивно, а вакансии не образовывались, появление смешанных кристаллов должно было бы приводить к росту плотности.
 • Экспериментальные данные довольно хорошо согласуются с расчетными значениями уменьшения плотности, вычисленными из расчета, что ион калия замещается на ион кальция и катионную вакансию.
• Экспериментальные данные довольно хорошо согласуются с расчетными значениями уменьшения плотности, вычисленными из расчета, что ион калия замещается на ион кальция и катионную вакансию.
 • Если бы плотность изменялась аддитивно, а вакансии не образовывались, появление смешанных кристаллов должно было сопровождаться увеличением плотности.
• Если бы плотность изменялась аддитивно, а вакансии не образовывались, появление смешанных кристаллов должно было сопровождаться увеличением плотности.
 Контролируемая валентность • Мы видели, что вакансии могут образовываться при введении в кристалл примесных атомов. Такие добавки могут также вызывать изменения валентности контролируемого числа ионов в решетке самого кристалла, если химическая природа этого кристалла такова, что возможны по крайней мере два валентных состояния.
Контролируемая валентность • Мы видели, что вакансии могут образовываться при введении в кристалл примесных атомов. Такие добавки могут также вызывать изменения валентности контролируемого числа ионов в решетке самого кристалла, если химическая природа этого кристалла такова, что возможны по крайней мере два валентных состояния.
 • Это очень часто имеет место в соединениях переходных металлов, например Ni. O. Если в решетку Ni. O ввести небольшое количество Li 2 O, ионы лития займут часть катионных узлов, как это показано на рис. 28.
• Это очень часто имеет место в соединениях переходных металлов, например Ni. O. Если в решетку Ni. O ввести небольшое количество Li 2 O, ионы лития займут часть катионных узлов, как это показано на рис. 28.
 • Общая электронейтральность кристалла может сохраняться при условии, что в структуре Ni. O образуются анионные вакансии, и концентрация их должна быть равна половине концентрации введенных ионов лития. В рассматриваемом случае, однако, избыточный заряд компенсируется за счет изменения валентности ионов никеля.
• Общая электронейтральность кристалла может сохраняться при условии, что в структуре Ni. O образуются анионные вакансии, и концентрация их должна быть равна половине концентрации введенных ионов лития. В рассматриваемом случае, однако, избыточный заряд компенсируется за счет изменения валентности ионов никеля.
 • Двухвалентные ионы никеля в количестве, равном количеству введенных ионов лития, переходят в трехвалентное состояние. • Метод контролируемой валентности позволяет получать заданную концентрацию атомов с измененной валентностью в исходном кристалле и увеличивать электропроводность оксида никеля, который в обычном состоянии является диэлектриком.
• Двухвалентные ионы никеля в количестве, равном количеству введенных ионов лития, переходят в трехвалентное состояние. • Метод контролируемой валентности позволяет получать заданную концентрацию атомов с измененной валентностью в исходном кристалле и увеличивать электропроводность оксида никеля, который в обычном состоянии является диэлектриком.
 • Метод контролируемой валентности имеет также большое значение при определении магнитных свойств соединений переходных металлов, поскольку эти свойства определяются степенью заполнения d-электронных оболочек в атомах переходных металлов.
• Метод контролируемой валентности имеет также большое значение при определении магнитных свойств соединений переходных металлов, поскольку эти свойства определяются степенью заполнения d-электронных оболочек в атомах переходных металлов.
 Компенсация заряда • Условия сохранения электронейтральности кристалла играет важную роль в кристаллохимии. Принцип компенсации заряда позволяет выдвинуть общий метод получения вакансий или мест с аномальной валентностью путем введения заранее подобранных примесей.
Компенсация заряда • Условия сохранения электронейтральности кристалла играет важную роль в кристаллохимии. Принцип компенсации заряда позволяет выдвинуть общий метод получения вакансий или мест с аномальной валентностью путем введения заранее подобранных примесей.
 • Введение примесей можно также использовать для осуществления взаимодействия их с другими примесными ионами. Так, если трехвалентные ионы Ni +3 замещают ионы Ca +2 в Ca. WO 4 , компенсация заряда может быть осуществлена тремя способами:
• Введение примесей можно также использовать для осуществления взаимодействия их с другими примесными ионами. Так, если трехвалентные ионы Ni +3 замещают ионы Ca +2 в Ca. WO 4 , компенсация заряда может быть осуществлена тремя способами:
 Комплексные центры; ассоциированные дефекты • В твердом теле имеется много дефектных центров, которые состоят из двух или нескольких атомных дефектов, находящихся в состоянии тесной связи. По мере того как возрастает сложность центров, затрудняется идентификация и изучение их.
Комплексные центры; ассоциированные дефекты • В твердом теле имеется много дефектных центров, которые состоят из двух или нескольких атомных дефектов, находящихся в состоянии тесной связи. По мере того как возрастает сложность центров, затрудняется идентификация и изучение их.
 • Среди дефектных центров такого рода особенно хорошо изучены те, которые образуются в галогенидах щелочных металлов. Оптические исследования таких систем позволили обнаружить их сложный характер.
• Среди дефектных центров такого рода особенно хорошо изучены те, которые образуются в галогенидах щелочных металлов. Оптические исследования таких систем позволили обнаружить их сложный характер.
 • Различная химическая обработка или облучение кристалла при различных длинах волн вызывает появление или, наоборот, исчезновение хорошо вызванных полос в спектрах поглощения, которые можно связать с отдельными типами дефектов.
• Различная химическая обработка или облучение кристалла при различных длинах волн вызывает появление или, наоборот, исчезновение хорошо вызванных полос в спектрах поглощения, которые можно связать с отдельными типами дефектов.
 • Кроме F- центров, идентифицированы центры, образующиеся в результате ассоциации вакансий: пара катионных вакансий, пара анионных вакансий, центры, состоящие из одной катионной и пары анионных вакансий и т. д. • Избыточные электроны и дырки могут захватываться на некоторых из этих дефектах. Модели некоторых из этих центров приведены на рис. 29.
• Кроме F- центров, идентифицированы центры, образующиеся в результате ассоциации вакансий: пара катионных вакансий, пара анионных вакансий, центры, состоящие из одной катионной и пары анионных вакансий и т. д. • Избыточные электроны и дырки могут захватываться на некоторых из этих дефектах. Модели некоторых из этих центров приведены на рис. 29.
 • Два различных дефекта в твердом теле могут образовывать ионную пару. Некоторые примесные атомы одного и того же вида могут образовывать небольшие агрегаты (кластеры). Если такой кластер содержит достаточное число атомов, его следует рассматривать уже не как дефектный центр, а как участок новой фазы
• Два различных дефекта в твердом теле могут образовывать ионную пару. Некоторые примесные атомы одного и того же вида могут образовывать небольшие агрегаты (кластеры). Если такой кластер содержит достаточное число атомов, его следует рассматривать уже не как дефектный центр, а как участок новой фазы
 Обозначения • Для обозначения нарушений в твердом теле предложено несколько схем. Такие схемы обычно сложны из-за разнообразия информации, которую пытаются с их помощью выразить. Так символы должны обозначать вид дефекта, его место в решетке, заряд центра и для сложных центров – природу каждого из компонентов.
Обозначения • Для обозначения нарушений в твердом теле предложено несколько схем. Такие схемы обычно сложны из-за разнообразия информации, которую пытаются с их помощью выразить. Так символы должны обозначать вид дефекта, его место в решетке, заряд центра и для сложных центров – природу каждого из компонентов.
 • Символом V обозначают вакансию, символом I –междоузлия, а положение в решетке – подстрочным символом. Так, V Pb обозначает вакансию в узле решетки, обычно занятым атомом свинца, Li i – междоузельный литий и Se As – селен в узле решетки, который в обчном состоянии занят мышьяком. Электроны и дырки обозначаются e- и h+.
• Символом V обозначают вакансию, символом I –междоузлия, а положение в решетке – подстрочным символом. Так, V Pb обозначает вакансию в узле решетки, обычно занятым атомом свинца, Li i – междоузельный литий и Se As – селен в узле решетки, который в обчном состоянии занят мышьяком. Электроны и дырки обозначаются e- и h+.
 Линейные и плоские дефекты • Кристаллы могут отличаться от идеального состояния не только в точках, соответствующих узлам решетки, но и вдоль линий и плоскостей. • Дислокации • Линейные дефекты называются дислокациями, различают два основных типа
Линейные и плоские дефекты • Кристаллы могут отличаться от идеального состояния не только в точках, соответствующих узлам решетки, но и вдоль линий и плоскостей. • Дислокации • Линейные дефекты называются дислокациями, различают два основных типа
 • Один из них – краевая дислокация, это дополнительная неполная атомная плоскость, расположенная в решетке так, как это показано на рис. 30. Плоскость в кристалле ниже и выше некоторой плоскости, показанной на рисунке, имеют одну и ту же степень сдвига, так что дислокация распространяется вдоль линии, перпендикулярной плоскости бумаги.
• Один из них – краевая дислокация, это дополнительная неполная атомная плоскость, расположенная в решетке так, как это показано на рис. 30. Плоскость в кристалле ниже и выше некоторой плоскости, показанной на рисунке, имеют одну и ту же степень сдвига, так что дислокация распространяется вдоль линии, перпендикулярной плоскости бумаги.
 • Очевидно, что кристалл в непосредственной близости от дислокации должен находится в напряженном состоянии, так как в нем должно разместится дополнительное число атомов. Нормальный порядок атомов восстанавливается в обоих направлениях на расстоянии нескольких постоянных решетки от дислокации.
• Очевидно, что кристалл в непосредственной близости от дислокации должен находится в напряженном состоянии, так как в нем должно разместится дополнительное число атомов. Нормальный порядок атомов восстанавливается в обоих направлениях на расстоянии нескольких постоянных решетки от дислокации.
 • Краевые дислокации могут двигаться в кристалле, и это движение приводит к скольжению. Деформация кристалла обычно совершается не за счет одновременного разрыва всех связей между двумя плоскостями нормального кристалла при их сдвиге относительно друга.
• Краевые дислокации могут двигаться в кристалле, и это движение приводит к скольжению. Деформация кристалла обычно совершается не за счет одновременного разрыва всех связей между двумя плоскостями нормального кристалла при их сдвиге относительно друга.
 • Расчеты силы, необходимой для осуществления такого рода процессов, показывают. Что она должна быть намного больше экспериментально наблюдаемой величины критического напряжения, при котором происходит сдвиг. В действительности сдвиг происходит чаще всего за счет движения дислокаций, как показано на рис. 31.
• Расчеты силы, необходимой для осуществления такого рода процессов, показывают. Что она должна быть намного больше экспериментально наблюдаемой величины критического напряжения, при котором происходит сдвиг. В действительности сдвиг происходит чаще всего за счет движения дислокаций, как показано на рис. 31.
 • Если кристалл подвергается деформации сдвига, смещение атомов в плоскости скольжения происходит таким образом, что атомы, находящиеся на одной стороне плоскости скольжения, постепенно сдвигаются относительно другой плоскости. Таким образом, появляется дислокация, которая движется через кристалл до его противолежащей плоскости. В результате происходит смещение верхней половины кристалла относительно нижней.
• Если кристалл подвергается деформации сдвига, смещение атомов в плоскости скольжения происходит таким образом, что атомы, находящиеся на одной стороне плоскости скольжения, постепенно сдвигаются относительно другой плоскости. Таким образом, появляется дислокация, которая движется через кристалл до его противолежащей плоскости. В результате происходит смещение верхней половины кристалла относительно нижней.
 • Так как силы, необходимые для отрыва ряда атомов от ближних соседей, расположенных с одной стороны от дислокации при ее движении, компенсируются силами притяжения со стороны соседних атомов, расстояние до которых чуть больше, и которые расположены с другой стороны, то чтобы движение могло происходить требуется приложить извне лишь очень небольшую силу.
• Так как силы, необходимые для отрыва ряда атомов от ближних соседей, расположенных с одной стороны от дислокации при ее движении, компенсируются силами притяжения со стороны соседних атомов, расстояние до которых чуть больше, и которые расположены с другой стороны, то чтобы движение могло происходить требуется приложить извне лишь очень небольшую силу.
 • Этот вид движения, повторяющийся многократно, обуславливает пластичность кристаллов. • Дислокации могут возникнуть не только при деформации сдвига, но и, например, вследствие образования различных дефектов во время роста кристалла.
• Этот вид движения, повторяющийся многократно, обуславливает пластичность кристаллов. • Дислокации могут возникнуть не только при деформации сдвига, но и, например, вследствие образования различных дефектов во время роста кристалла.
 • Сгибая кристалл, в него за счет деформации сдвига можно ввести известное число краевых дислокаций. Используя известные значения постоянных решетки, и радиуса кривизны сдвига. С помощью простых геометрических соотношений можно определить число таких дислокаций.
• Сгибая кристалл, в него за счет деформации сдвига можно ввести известное число краевых дислокаций. Используя известные значения постоянных решетки, и радиуса кривизны сдвига. С помощью простых геометрических соотношений можно определить число таких дислокаций.
 • Плотность краевых дислокаций обычно из меряется числом дислокационных линий, проходящих через единицу поверхности в кристалле. В обычных кристаллах содержится 10 6 см -2 дислокаций. Другой способ выражения числа дислокаций в кристалле состоит в оценке общей длины всех дислокаций в кристалле, отнесенной к единице его объема.
• Плотность краевых дислокаций обычно из меряется числом дислокационных линий, проходящих через единицу поверхности в кристалле. В обычных кристаллах содержится 10 6 см -2 дислокаций. Другой способ выражения числа дислокаций в кристалле состоит в оценке общей длины всех дислокаций в кристалле, отнесенной к единице его объема.
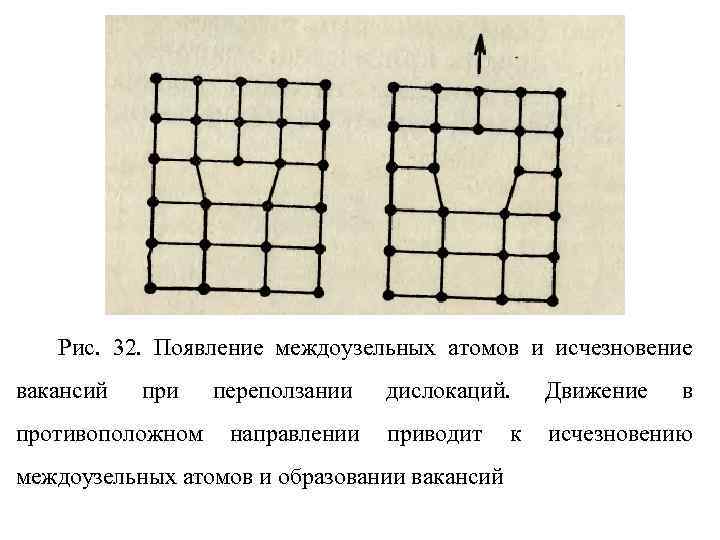
 • Если краевая дислокация движется не в направлении плоскости скольжения, а перпендикулярно этой плоскости, такой вид движения называется переползанием (рис. 32).
• Если краевая дислокация движется не в направлении плоскости скольжения, а перпендикулярно этой плоскости, такой вид движения называется переползанием (рис. 32).
 Рис. 32. Появление междоузельных атомов и исчезновение вакансий при переползании дислокаций. Движение в противоположном направлении приводит к исчезновению междоузельных атомов и образовании вакансий
Рис. 32. Появление междоузельных атомов и исчезновение вакансий при переползании дислокаций. Движение в противоположном направлении приводит к исчезновению междоузельных атомов и образовании вакансий
 • Результатом такого движения является образование или исчезновение вакансий или ионов в междоузлиях (в зависимости от характера движения дислокации), поскольку чтобы продолжить или сократить неполную атомную плоскость, образующую дислокацию (на один ряд атомов), требуется присоединить к ней или удалить определенное число атомов.
• Результатом такого движения является образование или исчезновение вакансий или ионов в междоузлиях (в зависимости от характера движения дислокации), поскольку чтобы продолжить или сократить неполную атомную плоскость, образующую дислокацию (на один ряд атомов), требуется присоединить к ней или удалить определенное число атомов.
 • Другой вид дислокации представляют так называемые винтовые дислокации, показанные на рис. 33. Они образуются в результате смещения атомов в одной части кристалла по отношению к оставшейся части кристалла, в результате которого вокруг линии дислокации образуется наклонная плоскость в виде спирали.
• Другой вид дислокации представляют так называемые винтовые дислокации, показанные на рис. 33. Они образуются в результате смещения атомов в одной части кристалла по отношению к оставшейся части кристалла, в результате которого вокруг линии дислокации образуется наклонная плоскость в виде спирали.
 • В отличие от краевой дислокации, где край неполной атомной плоскости наблюдается внутри кристалла, при образовании винтовой дислокации смещение элементарных ячеек происходит только лишь в непосредственной близости от дислокации. Направление смещения для краевой дислокации перпендикулярно дислокационной линии, а для винтовой дислокации смещение параллельно этой линии.
• В отличие от краевой дислокации, где край неполной атомной плоскости наблюдается внутри кристалла, при образовании винтовой дислокации смещение элементарных ячеек происходит только лишь в непосредственной близости от дислокации. Направление смещения для краевой дислокации перпендикулярно дислокационной линии, а для винтовой дислокации смещение параллельно этой линии.
 • Линейные дефекты не обязательно должны представлять собой прямые линии, на них должны быть пороги или ступеньки. Реально существующие дислокации обычно представляют комбинацию краевых и винтовых дислокаций
• Линейные дефекты не обязательно должны представлять собой прямые линии, на них должны быть пороги или ступеньки. Реально существующие дислокации обычно представляют комбинацию краевых и винтовых дислокаций
 Плоские дефекты • Многие структурные дефекты представляют собой атомные плоскости или чаще поверхности. • Наиболее очевидным проявлением геометрических дефектов в виде поверхностей является наличие зерен или границ зерен в поликристаллическом материале.
Плоские дефекты • Многие структурные дефекты представляют собой атомные плоскости или чаще поверхности. • Наиболее очевидным проявлением геометрических дефектов в виде поверхностей является наличие зерен или границ зерен в поликристаллическом материале.
 • Типичное поликристаллическое твердое вещество состоит из определенного числа небольших соединенных между собой кристаллов или зерен, ориентированных произвольным образом. Углы между направлениями главных осей кристалла в соседних зернах очень часто велики, а структура границы раздела фаз достаточно сложна в соответствии с особенностями ориентации и вида двух соседних кристаллов.
• Типичное поликристаллическое твердое вещество состоит из определенного числа небольших соединенных между собой кристаллов или зерен, ориентированных произвольным образом. Углы между направлениями главных осей кристалла в соседних зернах очень часто велики, а структура границы раздела фаз достаточно сложна в соответствии с особенностями ориентации и вида двух соседних кристаллов.
 • Это показано на рис. 34. Слой атомов на границе между зернами представляет собой область нарушенной решетки. Эта область имеет ширину в несколько атомных слоев и обеспечивает переход между соседними разориентированными областями. • Обычно зерна в поликристалле не соответствуют по форме и структуре кристаллу.
• Это показано на рис. 34. Слой атомов на границе между зернами представляет собой область нарушенной решетки. Эта область имеет ширину в несколько атомных слоев и обеспечивает переход между соседними разориентированными областями. • Обычно зерна в поликристалле не соответствуют по форме и структуре кристаллу.
 • Они огранены поверхностями, которые имеют скорее случайную форму, нежели соответствуют хорошо выраженным граням кристалла. При повышенных температурах подвижность атомов увеличивается и некоторые зерна начинают расти за счет других (этот процесс называют вторичной рекристаллизацией).
• Они огранены поверхностями, которые имеют скорее случайную форму, нежели соответствуют хорошо выраженным граням кристалла. При повышенных температурах подвижность атомов увеличивается и некоторые зерна начинают расти за счет других (этот процесс называют вторичной рекристаллизацией).

