АХ-растворы.ppt
- Количество слайдов: 42
 ДЕДКОВ ЮРИЙ МАРКОВИЧ Доктор химических наук Профессор Заслуженный деятель науки РФ (Московский государственный областной университет) 16. 02. 2018 1
ДЕДКОВ ЮРИЙ МАРКОВИЧ Доктор химических наук Профессор Заслуженный деятель науки РФ (Московский государственный областной университет) 16. 02. 2018 1
 АНАЛИТИЧЕСКАЯ ХИМИЯ (РАСТВОРЫ} 16. 02. 2018 2
АНАЛИТИЧЕСКАЯ ХИМИЯ (РАСТВОРЫ} 16. 02. 2018 2
 • • 1. Понятие о растворах 2. Силы, действующие в растворах 3. Структура молекулы воды 4. Гидратация ионов металлов 5. Ионная сила растворов и активность ионов 6. Факторы, влияющие на активность ионов 7. Протолитические равновесия 8. Гетерогенные системы. Произведение растворимости 16. 02. 2018 3
• • 1. Понятие о растворах 2. Силы, действующие в растворах 3. Структура молекулы воды 4. Гидратация ионов металлов 5. Ионная сила растворов и активность ионов 6. Факторы, влияющие на активность ионов 7. Протолитические равновесия 8. Гетерогенные системы. Произведение растворимости 16. 02. 2018 3
 • Жидкости — промежуточное положение между газами и твердыми веществами. Характерна упорядочненость ближней сферы. Раствор — гомогенная смесь двух или более соединений и продуктов их взаимодействия. • Истинный раствор - термодинамически устойчивая гомогенная система переменного состава, образованная двумя или бόльшим числом индивидуальных соединений. • Сольватация - взаимодействие растворенного вещества с растворителем. • Гидратация: • Сl 2∙ 8 Н 2 О; Хе∙ 6 Н 2 О; С 2 Н 6∙ 6 Н 2 О; С 3 Н 8∙ 17 Н 2 О 16. 02. 2018 4
• Жидкости — промежуточное положение между газами и твердыми веществами. Характерна упорядочненость ближней сферы. Раствор — гомогенная смесь двух или более соединений и продуктов их взаимодействия. • Истинный раствор - термодинамически устойчивая гомогенная система переменного состава, образованная двумя или бόльшим числом индивидуальных соединений. • Сольватация - взаимодействие растворенного вещества с растворителем. • Гидратация: • Сl 2∙ 8 Н 2 О; Хе∙ 6 Н 2 О; С 2 Н 6∙ 6 Н 2 О; С 3 Н 8∙ 17 Н 2 О 16. 02. 2018 4
 • Концентрация - количество растворенного вещества, содержащееся в единице раствора или растворителя. • Молярность раствора - число молей вещества в 1 дм 3 раствора. • Нормальность раствора - число молей эквивалента вещества в 1 дм 3 раствора. • Процентность раствора - число граммов вещества в 100 г. раствора или число см 3 вещества в 100 см 3 раствора. • Титр раствора - масса растворенного вещества в 1 см 3 раствора. 16. 02. 2018 5
• Концентрация - количество растворенного вещества, содержащееся в единице раствора или растворителя. • Молярность раствора - число молей вещества в 1 дм 3 раствора. • Нормальность раствора - число молей эквивалента вещества в 1 дм 3 раствора. • Процентность раствора - число граммов вещества в 100 г. раствора или число см 3 вещества в 100 см 3 раствора. • Титр раствора - масса растворенного вещества в 1 см 3 раствора. 16. 02. 2018 5
 Взаимодействие «вещество растворитель» • Силы Ван-дер-Ваальса (0, 5 -1 к. Дж/моль); • - дисперсионные (нейтральные молекулы, взаимодействие мгновенных электрических диполей, возникающих при движении электронов; растворение неполярных веществ); • - индукционные (поляризация молекулы вещества под действием молекулы растворителя); • - ориентационные (взаимодействие постоянных диполей). • • 16. 02. 2018 6
Взаимодействие «вещество растворитель» • Силы Ван-дер-Ваальса (0, 5 -1 к. Дж/моль); • - дисперсионные (нейтральные молекулы, взаимодействие мгновенных электрических диполей, возникающих при движении электронов; растворение неполярных веществ); • - индукционные (поляризация молекулы вещества под действием молекулы растворителя); • - ориентационные (взаимодействие постоянных диполей). • • 16. 02. 2018 6
 • Химические взаимодействия (5 – 50 к. Дж/моль): • - ион-дипольное взаимодействие; • - водородные связи: R-H ←: OR 2, СН 3 ОН ← : ОН 2 Причины образования ВС малый радиус иона Н+ и высокая электронная плотность ( «Li-связь» ); - поляризация связи Н-Х и стремление атома Н отдать электрон: • С 6 Н 6∙Н+; СНСl 3 16. 02. 2018 7
• Химические взаимодействия (5 – 50 к. Дж/моль): • - ион-дипольное взаимодействие; • - водородные связи: R-H ←: OR 2, СН 3 ОН ← : ОН 2 Причины образования ВС малый радиус иона Н+ и высокая электронная плотность ( «Li-связь» ); - поляризация связи Н-Х и стремление атома Н отдать электрон: • С 6 Н 6∙Н+; СНСl 3 16. 02. 2018 7
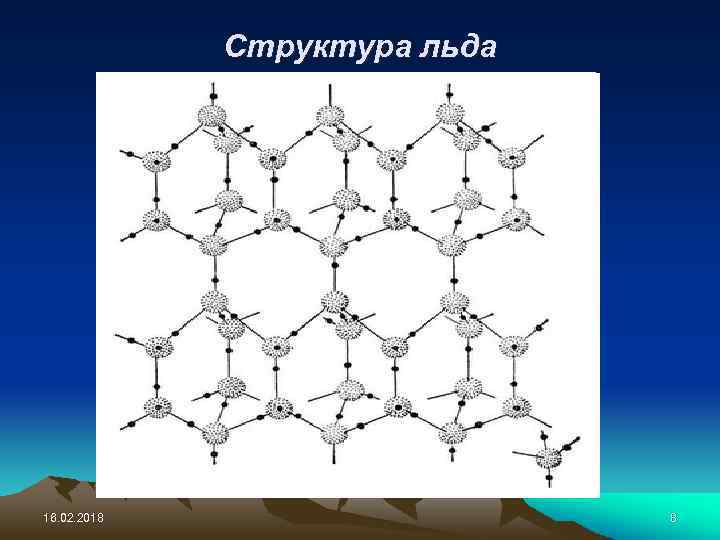 Структура льда 16. 02. 2018 8
Структура льда 16. 02. 2018 8
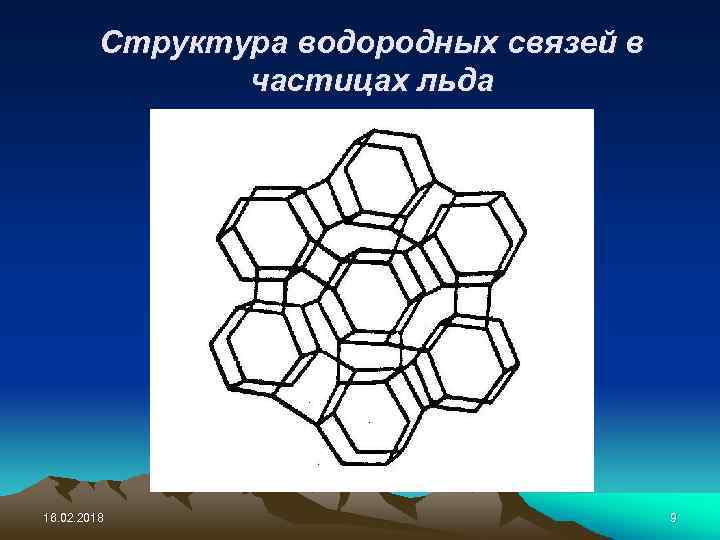 Структура водородных связей в частицах льда 16. 02. 2018 9
Структура водородных связей в частицах льда 16. 02. 2018 9
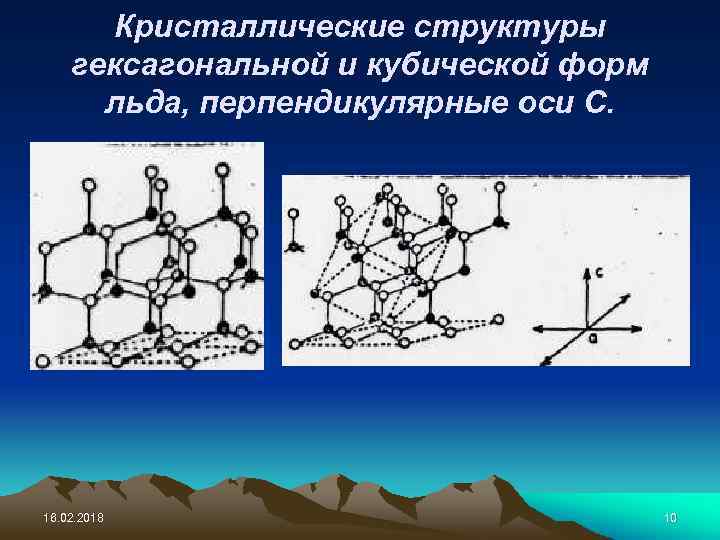 Кристаллические структуры гексагональной и кубической форм льда, перпендикулярные оси С. 16. 02. 2018 10
Кристаллические структуры гексагональной и кубической форм льда, перпендикулярные оси С. 16. 02. 2018 10
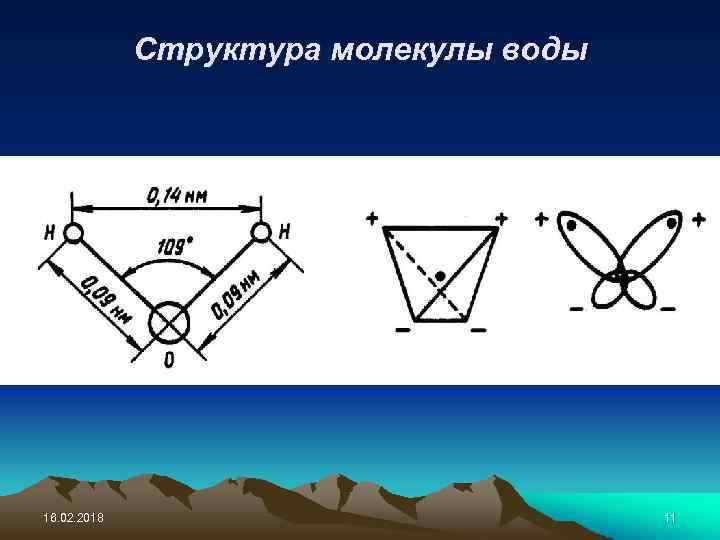 Структура молекулы воды 16. 02. 2018 11
Структура молекулы воды 16. 02. 2018 11
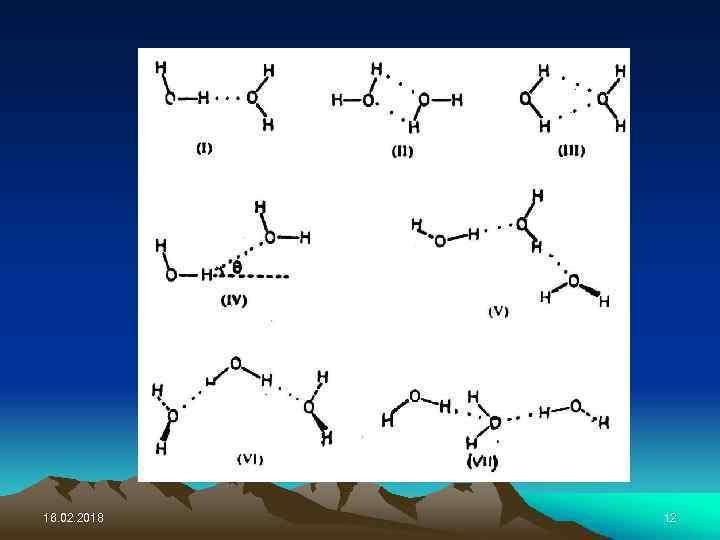 16. 02. 2018 12
16. 02. 2018 12
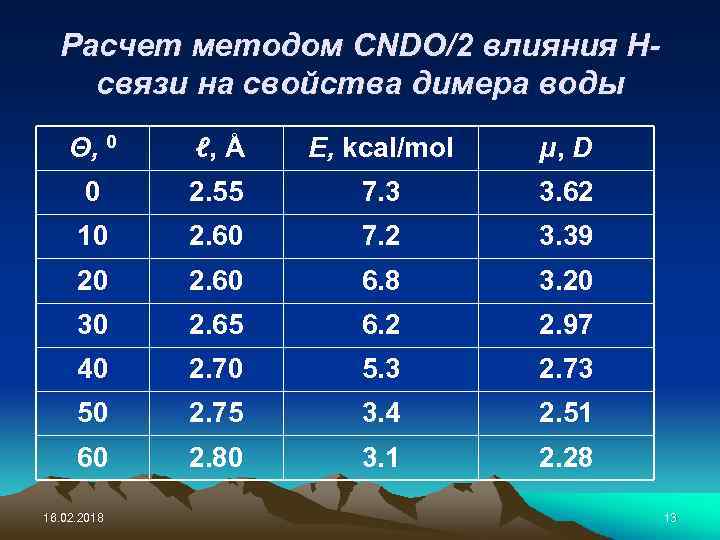 Расчет методом CNDO/2 влияния Нсвязи на свойства димера воды Θ, 0 ℓ, Å E, kcal/mol µ, D 0 2. 55 7. 3 3. 62 10 2. 60 7. 2 3. 39 20 2. 60 6. 8 3. 20 30 2. 65 6. 2 2. 97 40 2. 70 5. 3 2. 73 50 2. 75 3. 4 2. 51 60 2. 80 3. 1 2. 28 16. 02. 2018 13
Расчет методом CNDO/2 влияния Нсвязи на свойства димера воды Θ, 0 ℓ, Å E, kcal/mol µ, D 0 2. 55 7. 3 3. 62 10 2. 60 7. 2 3. 39 20 2. 60 6. 8 3. 20 30 2. 65 6. 2 2. 97 40 2. 70 5. 3 2. 73 50 2. 75 3. 4 2. 51 60 2. 80 3. 1 2. 28 16. 02. 2018 13
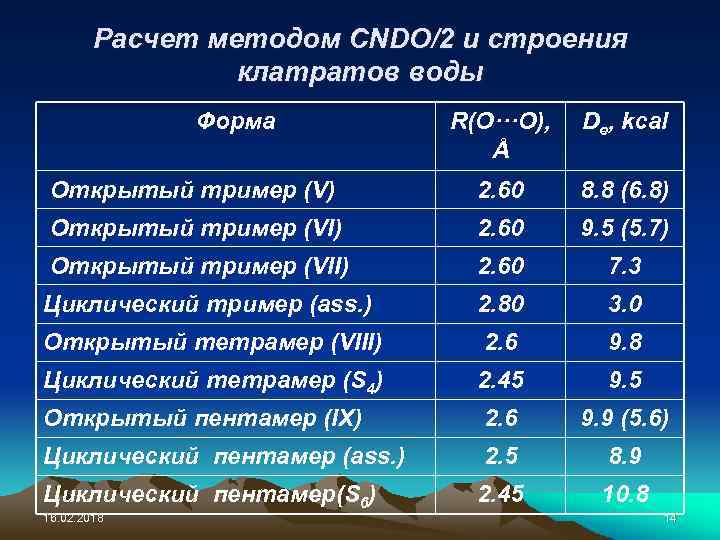 Расчет методом CNDO/2 и строения клатратов воды Форма R(O···O), Å De, kcal Открытый тример (V) 2. 60 8. 8 (6. 8) Открытый тример (VI) 2. 60 9. 5 (5. 7) Открытый тример (VII) 2. 60 7. 3 Циклический тример (ass. ) 2. 80 3. 0 Открытый тетрамер (VIII) 2. 6 9. 8 Циклический тетрамер (S 4) 2. 45 9. 5 Открытый пентамер (IX) 2. 6 9. 9 (5. 6) Циклический пентамер (ass. ) 2. 5 8. 9 Циклический пентамер(S 6) 2. 45 10. 8 16. 02. 2018 14
Расчет методом CNDO/2 и строения клатратов воды Форма R(O···O), Å De, kcal Открытый тример (V) 2. 60 8. 8 (6. 8) Открытый тример (VI) 2. 60 9. 5 (5. 7) Открытый тример (VII) 2. 60 7. 3 Циклический тример (ass. ) 2. 80 3. 0 Открытый тетрамер (VIII) 2. 6 9. 8 Циклический тетрамер (S 4) 2. 45 9. 5 Открытый пентамер (IX) 2. 6 9. 9 (5. 6) Циклический пентамер (ass. ) 2. 5 8. 9 Циклический пентамер(S 6) 2. 45 10. 8 16. 02. 2018 14
 Радиусы гидратированных ионов щелочных металлов 16. 02. 2018 15
Радиусы гидратированных ионов щелочных металлов 16. 02. 2018 15
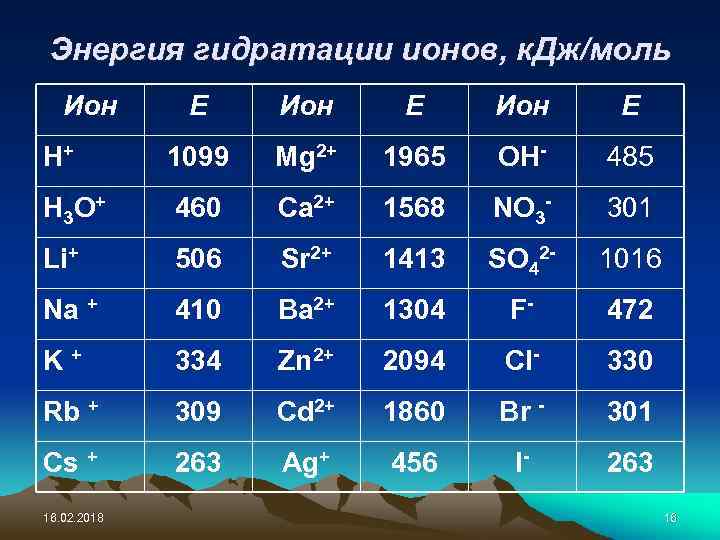 Энергия гидратации ионов, к. Дж/моль Ион Е H+ 1099 Mg 2+ 1965 OH- 485 H 3 O + 460 Ca 2+ 1568 NO 3 - 301 Li+ 506 Sr 2+ 1413 SO 42 - 1016 Na + 410 Ba 2+ 1304 F- 472 K+ 334 Zn 2+ 2094 Cl- 330 Rb + 309 Cd 2+ 1860 Br - 301 Cs + 263 Ag+ 456 I- 263 16. 02. 2018 16
Энергия гидратации ионов, к. Дж/моль Ион Е H+ 1099 Mg 2+ 1965 OH- 485 H 3 O + 460 Ca 2+ 1568 NO 3 - 301 Li+ 506 Sr 2+ 1413 SO 42 - 1016 Na + 410 Ba 2+ 1304 F- 472 K+ 334 Zn 2+ 2094 Cl- 330 Rb + 309 Cd 2+ 1860 Br - 301 Cs + 263 Ag+ 456 I- 263 16. 02. 2018 16
 Сольватация в аналитике 16. 02. 2018 17
Сольватация в аналитике 16. 02. 2018 17
 Степень ионизации α – доля ионизованных молекул • • • 16. 02. 2018 D ↔ A+ + BαΑ+= αB- = C∙α; αD = C∙(1 – α); K 0 равн = (αA+∙αB-)/αD = C∙{α 2/(1 – α)}; __________ α << 1; K 0 равн ≈ α 2∙C; α = √K 0 равн /C 18
Степень ионизации α – доля ионизованных молекул • • • 16. 02. 2018 D ↔ A+ + BαΑ+= αB- = C∙α; αD = C∙(1 – α); K 0 равн = (αA+∙αB-)/αD = C∙{α 2/(1 – α)}; __________ α << 1; K 0 равн ≈ α 2∙C; α = √K 0 равн /C 18
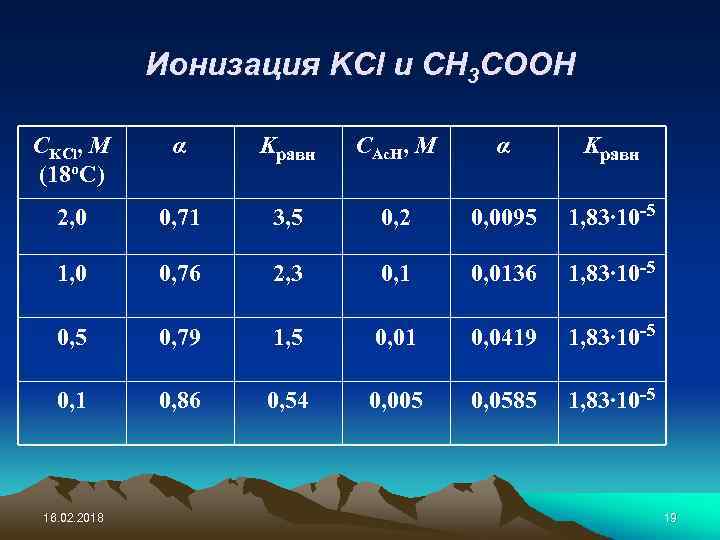 Ионизация KCl и CH 3 COOH CKCl, M (18 o. C) α Kравн CAc. H, M α Kравн 2, 0 0, 71 3, 5 0, 2 0, 0095 1, 83∙ 10 -5 1, 0 0, 76 2, 3 0, 1 0, 0136 1, 83∙ 10 -5 0, 79 1, 5 0, 01 0, 0419 1, 83∙ 10 -5 0, 1 0, 86 0, 54 0, 005 0, 0585 1, 83∙ 10 -5 16. 02. 2018 19
Ионизация KCl и CH 3 COOH CKCl, M (18 o. C) α Kравн CAc. H, M α Kравн 2, 0 0, 71 3, 5 0, 2 0, 0095 1, 83∙ 10 -5 1, 0 0, 76 2, 3 0, 1 0, 0136 1, 83∙ 10 -5 0, 79 1, 5 0, 01 0, 0419 1, 83∙ 10 -5 0, 1 0, 86 0, 54 0, 005 0, 0585 1, 83∙ 10 -5 16. 02. 2018 19
 Активность частиц в растворе • Активность - кажущаяся концентрация заряженной час-тицы, в соответствии с которой та проявляет себя в химических реакциях (Льюис, 1907 г. ): α = γ∙[В]; γ <1 • Зависимость α от I (Льюис, Рэндел, 1921 г. ). • Ионная сила раствора I - мера интенсивности электрического поля, создаваемого ионами в растворе, характеристика числа заряженных частиц: • n • I = 0, 5∙Σ (Cj∙Zj 2) • j=1 Дебай, Хюккель (1923 г. ) 16. 02. 2018 20
Активность частиц в растворе • Активность - кажущаяся концентрация заряженной час-тицы, в соответствии с которой та проявляет себя в химических реакциях (Льюис, 1907 г. ): α = γ∙[В]; γ <1 • Зависимость α от I (Льюис, Рэндел, 1921 г. ). • Ионная сила раствора I - мера интенсивности электрического поля, создаваемого ионами в растворе, характеристика числа заряженных частиц: • n • I = 0, 5∙Σ (Cj∙Zj 2) • j=1 Дебай, Хюккель (1923 г. ) 16. 02. 2018 20
 • Во всех разбавленных растворах сильных электролитов с одинаковой ионной силой катионы и анионы с равными численными значениями зарядов имеют одинаковые коэффициенты активности. • Предельный закон (частица - точечный заряд): _ lgγ = - 0, 511∙Z 2√I (I ≤ 0, 01 М) ____ ------------------------- -- ___ lgγ = - 0, 511∙Z 2√I ·(1 + k√I) -1 • • • - (I = 0, 1 -0, 5 М) Уравнение Дэвиса: lg γ = - 0, 511∙Z 2√I·(1 + k√I) -1 - 0, 1 Z 2∙I (I = 0, 5 -1, 0 М) lg γ = - 0, 511∙Z 2√I·(1 + k√I) -1 - Сz∙I (I = 0, 5 -1, 0 М) k = a. В (а ≈ 3 Å, В ≈ 0, 33) _ ------------------------------------------------------------------ ___________________ __ m+n _______ Для Аm. Bn 16. 02. 2018 lgγ = √γAm∙γBn 21
• Во всех разбавленных растворах сильных электролитов с одинаковой ионной силой катионы и анионы с равными численными значениями зарядов имеют одинаковые коэффициенты активности. • Предельный закон (частица - точечный заряд): _ lgγ = - 0, 511∙Z 2√I (I ≤ 0, 01 М) ____ ------------------------- -- ___ lgγ = - 0, 511∙Z 2√I ·(1 + k√I) -1 • • • - (I = 0, 1 -0, 5 М) Уравнение Дэвиса: lg γ = - 0, 511∙Z 2√I·(1 + k√I) -1 - 0, 1 Z 2∙I (I = 0, 5 -1, 0 М) lg γ = - 0, 511∙Z 2√I·(1 + k√I) -1 - Сz∙I (I = 0, 5 -1, 0 М) k = a. В (а ≈ 3 Å, В ≈ 0, 33) _ ------------------------------------------------------------------ ___________________ __ m+n _______ Для Аm. Bn 16. 02. 2018 lgγ = √γAm∙γBn 21
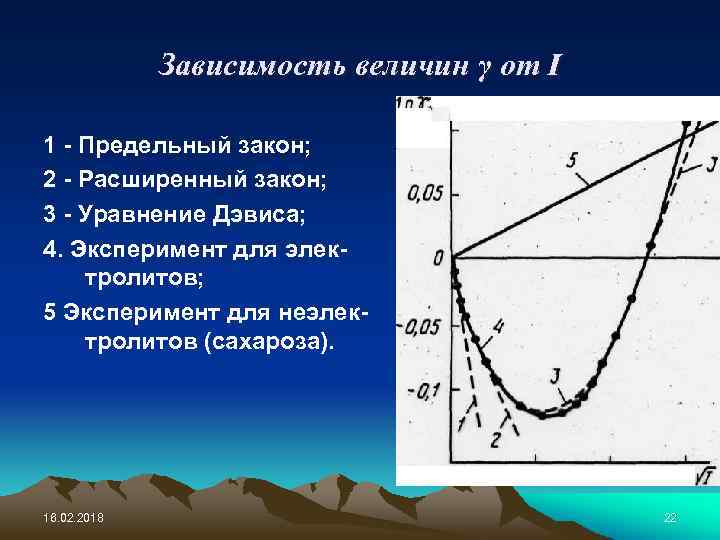 Зависимость величин γ от I 1 - Предельный закон; 2 - Расширенный закон; 3 - Уравнение Дэвиса; 4. Эксперимент для электролитов; 5 Эксперимент для неэлектролитов (сахароза). 16. 02. 2018 22
Зависимость величин γ от I 1 - Предельный закон; 2 - Расширенный закон; 3 - Уравнение Дэвиса; 4. Эксперимент для электролитов; 5 Эксперимент для неэлектролитов (сахароза). 16. 02. 2018 22
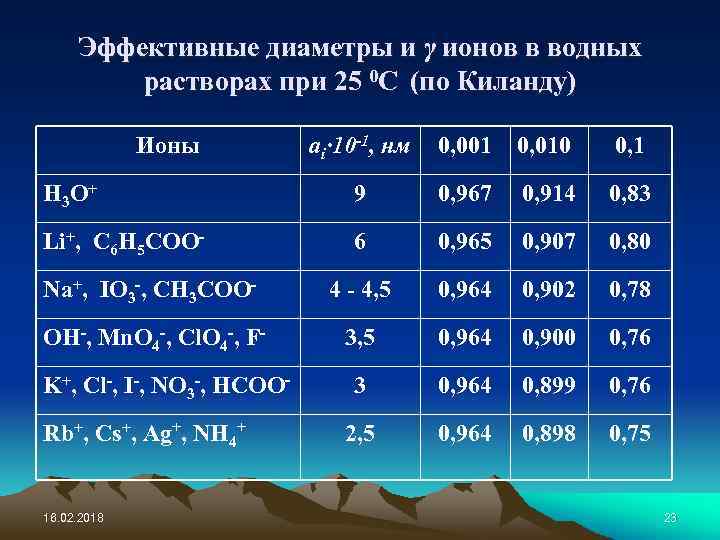 Эффективные диаметры и γ ионов в водных растворах при 25 0 C (по Киланду) Ионы ai∙ 10 -1, нм 0, 001 0, 010 0, 1 H 3 O + 9 0, 967 0, 914 0, 83 Li+, C 6 H 5 COO- 6 0, 965 0, 907 0, 80 Na+, IO 3 -, CH 3 COO- 4 - 4, 5 0, 964 0, 902 0, 78 OH-, Mn. O 4 -, Cl. O 4 -, F- 3, 5 0, 964 0, 900 0, 76 3 0, 964 0, 899 0, 76 2, 5 0, 964 0, 898 0, 75 K+, Cl-, I-, NO 3 -, HCOORb+, Cs+, Ag+, NH 4+ 16. 02. 2018 23
Эффективные диаметры и γ ионов в водных растворах при 25 0 C (по Киланду) Ионы ai∙ 10 -1, нм 0, 001 0, 010 0, 1 H 3 O + 9 0, 967 0, 914 0, 83 Li+, C 6 H 5 COO- 6 0, 965 0, 907 0, 80 Na+, IO 3 -, CH 3 COO- 4 - 4, 5 0, 964 0, 902 0, 78 OH-, Mn. O 4 -, Cl. O 4 -, F- 3, 5 0, 964 0, 900 0, 76 3 0, 964 0, 899 0, 76 2, 5 0, 964 0, 898 0, 75 K+, Cl-, I-, NO 3 -, HCOORb+, Cs+, Ag+, NH 4+ 16. 02. 2018 23
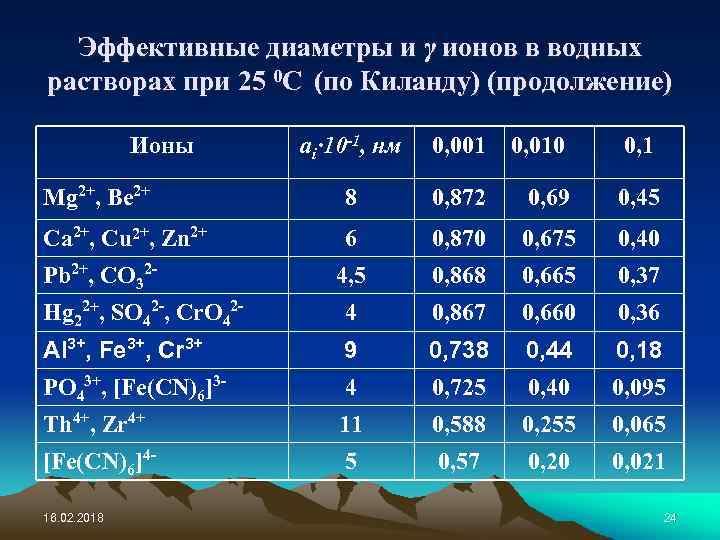 Эффективные диаметры и γ ионов в водных растворах при 25 0 C (по Киланду) (продолжение) Ионы ai∙ 10 -1, нм 0, 001 0, 010 0, 1 Mg 2+, Be 2+ 8 0, 872 0, 69 0, 45 Ca 2+, Cu 2+, Zn 2+ 6 0, 870 0, 675 0, 40 4, 5 0, 868 0, 665 0, 37 Hg 22+, SO 42 -, Cr. O 42 - 4 0, 867 0, 660 0, 36 Al 3+, Fe 3+, Cr 3+ 9 0, 738 0, 44 0, 18 PO 43+, [Fe(CN)6]3 - 4 0, 725 0, 40 0, 095 Th 4+, Zr 4+ 11 0, 588 0, 255 0, 065 [Fe(CN)6]4 - 5 0, 57 0, 20 0, 021 Pb 2+, CO 32 - 16. 02. 2018 24
Эффективные диаметры и γ ионов в водных растворах при 25 0 C (по Киланду) (продолжение) Ионы ai∙ 10 -1, нм 0, 001 0, 010 0, 1 Mg 2+, Be 2+ 8 0, 872 0, 69 0, 45 Ca 2+, Cu 2+, Zn 2+ 6 0, 870 0, 675 0, 40 4, 5 0, 868 0, 665 0, 37 Hg 22+, SO 42 -, Cr. O 42 - 4 0, 867 0, 660 0, 36 Al 3+, Fe 3+, Cr 3+ 9 0, 738 0, 44 0, 18 PO 43+, [Fe(CN)6]3 - 4 0, 725 0, 40 0, 095 Th 4+, Zr 4+ 11 0, 588 0, 255 0, 065 [Fe(CN)6]4 - 5 0, 57 0, 20 0, 021 Pb 2+, CO 32 - 16. 02. 2018 24
 Протолитические равновесия (Н 2 О)2 ↔ Н 3 О+ + ОНУпрощение: Н 2 О ↔ Н+ + ОНКравн = α(Н+)·α(ОН-)/α(Н 2 О) = 1000/18 = 55, 6 моль/дм 3 Кравн ·α(Н 2 О) = α(н+)· α(он-) = = 55, 6· 1, 8· 10 -16 ~ 10 -14 = Кw α(н+) = α(ОН-) = (Kw)½ = 1· 10 -7 16. 02. 2018 25
Протолитические равновесия (Н 2 О)2 ↔ Н 3 О+ + ОНУпрощение: Н 2 О ↔ Н+ + ОНКравн = α(Н+)·α(ОН-)/α(Н 2 О) = 1000/18 = 55, 6 моль/дм 3 Кравн ·α(Н 2 О) = α(н+)· α(он-) = = 55, 6· 1, 8· 10 -16 ~ 10 -14 = Кw α(н+) = α(ОН-) = (Kw)½ = 1· 10 -7 16. 02. 2018 25
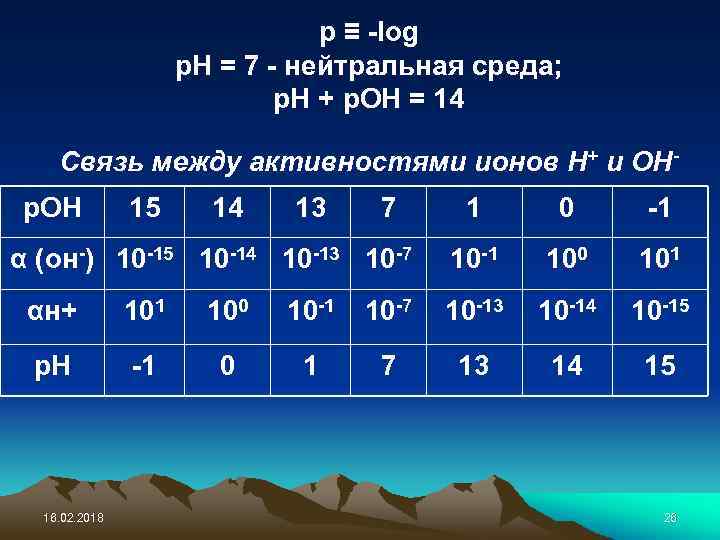 р ≡ -log р. Н = 7 - нейтральная среда; р. Н + р. ОН = 14 Связь между активностями ионов Н+ и ОНр. ОН 15 14 13 7 α (он-) 10 -15 10 -14 10 -13 10 -7 1 0 -1 100 101 αн+ 101 100 10 -1 10 -7 10 -13 10 -14 10 -15 р. Н -1 0 1 7 13 14 15 16. 02. 2018 26
р ≡ -log р. Н = 7 - нейтральная среда; р. Н + р. ОН = 14 Связь между активностями ионов Н+ и ОНр. ОН 15 14 13 7 α (он-) 10 -15 10 -14 10 -13 10 -7 1 0 -1 100 101 αн+ 101 100 10 -1 10 -7 10 -13 10 -14 10 -15 р. Н -1 0 1 7 13 14 15 16. 02. 2018 26
 • Шкала Гамметта: СНСl = 12, 0 М, Но- -3, 2 CH 2 SO 4 = 18 M Ho = -12, 8. • 16. 02. 2018 27
• Шкала Гамметта: СНСl = 12, 0 М, Но- -3, 2 CH 2 SO 4 = 18 M Ho = -12, 8. • 16. 02. 2018 27
 • Гидролиз соли - взаимодействие ионов соли с водой, приводящее к образованию слабой кислоты и слабого основания. СН 3 СОО- + Н 2 О ↔ СН 3 СООН + ОН • NH 4+ + Н 2 О ↔ NH 4 OH + Н+ • CH 3 COONH 4 +H 2 O ↔ CH 3 COOH+NH 4 OH+OH-+ Н+ • Кравн = ([СНз. СООН] [ОН-])/([СНз. СОО-][Н 2 О]); • Кравн·[Н 2 О] = ([СНз. СООН] [ОН-])/([СН 3 СОО-] = Кг • Слабая кислота: Кг = Kw /Ka • Слабое основание: Кг = Кw /Кb • Слабые кислота и основание: Кг = Кw /(Ка. Кb) 16. 02. 2018 28
• Гидролиз соли - взаимодействие ионов соли с водой, приводящее к образованию слабой кислоты и слабого основания. СН 3 СОО- + Н 2 О ↔ СН 3 СООН + ОН • NH 4+ + Н 2 О ↔ NH 4 OH + Н+ • CH 3 COONH 4 +H 2 O ↔ CH 3 COOH+NH 4 OH+OH-+ Н+ • Кравн = ([СНз. СООН] [ОН-])/([СНз. СОО-][Н 2 О]); • Кравн·[Н 2 О] = ([СНз. СООН] [ОН-])/([СН 3 СОО-] = Кг • Слабая кислота: Кг = Kw /Ka • Слабое основание: Кг = Кw /Кb • Слабые кислота и основание: Кг = Кw /(Ка. Кb) 16. 02. 2018 28
 • Буферные системы - растворы слабой кислоты и ее соли или слабого основания и его соли с определенной концентрацией ионов водорода, незначительно меняющие значения р. Н при разбавлении или концентрировании раствора или же введении в него небольших количеств кислоты или основания. 16. 02. 2018 29
• Буферные системы - растворы слабой кислоты и ее соли или слабого основания и его соли с определенной концентрацией ионов водорода, незначительно меняющие значения р. Н при разбавлении или концентрировании раствора или же введении в него небольших количеств кислоты или основания. 16. 02. 2018 29
 • • СН 3 СООН ↔ СН 3 СОО- + Н+ • СН 3 СООNа ↔ СНз. СОО- + Na+ • Ка = ([СНз. СОО-] [Н+])/[СН 3 СООН]; • [СНз. СООН] ~ Са; [СН 3 СОО-] ~ Cсоль • Ка ~ (Ссоль/Са)·[H+] • [H+] ~ Ка·(Сa/Ссоль); • р. Н = р. Ка - lg(Ссоль/Са) Смеси: Формиатная р. Н 3, 8 ± 0, 5 Ацетатная р. Н 4, 7 ± 0, 5 КН 2 РО 4 + Na 2 HPO 4 р. Н 6, 6 ± 0, 5 Аммиачная р. Н 9, 3 ± 0, 5 Бифталатная р. Н 4, 01 16. 02. 2018 30
• • СН 3 СООН ↔ СН 3 СОО- + Н+ • СН 3 СООNа ↔ СНз. СОО- + Na+ • Ка = ([СНз. СОО-] [Н+])/[СН 3 СООН]; • [СНз. СООН] ~ Са; [СН 3 СОО-] ~ Cсоль • Ка ~ (Ссоль/Са)·[H+] • [H+] ~ Ка·(Сa/Ссоль); • р. Н = р. Ка - lg(Ссоль/Са) Смеси: Формиатная р. Н 3, 8 ± 0, 5 Ацетатная р. Н 4, 7 ± 0, 5 КН 2 РО 4 + Na 2 HPO 4 р. Н 6, 6 ± 0, 5 Аммиачная р. Н 9, 3 ± 0, 5 Бифталатная р. Н 4, 01 16. 02. 2018 30
 Гетерогенные системы • Гетерогенная система – система, состоящая из нескольких фаз, различающихся по своим свойствам и соприкасающихся поверхностями раздела. 16. 02. 2018 31
Гетерогенные системы • Гетерогенная система – система, состоящая из нескольких фаз, различающихся по своим свойствам и соприкасающихся поверхностями раздела. 16. 02. 2018 31
 Стадия (1) – неэлектролиты; Все стадии – малополярные соединения; Стадии (1) и (2) – полярные или ионные соединения; в растворителях с высокой диэлектрической проницаемостью могут не учитываться 16. 02. 2018 m+n ----So = √Кs 32
Стадия (1) – неэлектролиты; Все стадии – малополярные соединения; Стадии (1) и (2) – полярные или ионные соединения; в растворителях с высокой диэлектрической проницаемостью могут не учитываться 16. 02. 2018 m+n ----So = √Кs 32
 Правило произведения растворимости • Произведение активностей ионов малорастворимого хорощо диссоциирующего вещества над осадком, взятых в стехиометрических степенях, есть величина постоянная (Кso)Am. Bn (тв. ) ↔ Am. Bn (в. ) • Am. Bn (в. ) ↔ m. A+ +n. B • Am. Bn (тв. ) ↔ m. A+ +n. B • K∑ = {(a. A+)m(a. B-)n} / {a. Am. Bn (тв. )}; • a. Am. Bn (тв. ) ~ const. • Kso = K∑ a. Am. Bn (тв. ) = (a. A+)m(a. B-)n ; • Kso = [m. S]m·[n. S]n; • S 16. 02. 2018 m+n -----------------= √ Kso / [S]m·[S]n 33
Правило произведения растворимости • Произведение активностей ионов малорастворимого хорощо диссоциирующего вещества над осадком, взятых в стехиометрических степенях, есть величина постоянная (Кso)Am. Bn (тв. ) ↔ Am. Bn (в. ) • Am. Bn (в. ) ↔ m. A+ +n. B • Am. Bn (тв. ) ↔ m. A+ +n. B • K∑ = {(a. A+)m(a. B-)n} / {a. Am. Bn (тв. )}; • a. Am. Bn (тв. ) ~ const. • Kso = K∑ a. Am. Bn (тв. ) = (a. A+)m(a. B-)n ; • Kso = [m. S]m·[n. S]n; • S 16. 02. 2018 m+n -----------------= √ Kso / [S]m·[S]n 33
 • Что дает правило произведения растворимости: • - возможность подбора условий осаждения; • - возможность расчета оптимального избытка осадителя; • - возможность расчета концентрации осаждаемой соли в насыщенном растворе в условиях осаждения. 16. 02. 2018 34
• Что дает правило произведения растворимости: • - возможность подбора условий осаждения; • - возможность расчета оптимального избытка осадителя; • - возможность расчета концентрации осаждаемой соли в насыщенном растворе в условиях осаждения. 16. 02. 2018 34
 Влияние одноименного иона Ba(IO 3)2 (насыщенный водный раствор) Ks 0{Ba(IO 3)2}= 1, 5· 10 -9 3 ---------- S = [Ba 2+] = ½ [IO 3 -] =√Ks 0/(22· 12)= 7, 2· 10 -4 М Ba(IO 3)2 (насыщенный водный раствор, 0, 10 н по Na. IO 3, без учета ионной силы ) [IO 3 -] ~ CNa. IO 3 = 0, 10 M S = [Ba 2+] = Ks /[IO 3 -]2 S = 1, 5· 10 -7 M 16. 02. 2018 35
Влияние одноименного иона Ba(IO 3)2 (насыщенный водный раствор) Ks 0{Ba(IO 3)2}= 1, 5· 10 -9 3 ---------- S = [Ba 2+] = ½ [IO 3 -] =√Ks 0/(22· 12)= 7, 2· 10 -4 М Ba(IO 3)2 (насыщенный водный раствор, 0, 10 н по Na. IO 3, без учета ионной силы ) [IO 3 -] ~ CNa. IO 3 = 0, 10 M S = [Ba 2+] = Ks /[IO 3 -]2 S = 1, 5· 10 -7 M 16. 02. 2018 35
 Ba(IO 3)2 (насыщенный водный раствор, 0, 1 н. по Na. IO 3, с учетом ионной силы) S = [Ba 2+] = Ks /[IO 3 -]2 [IO 3 -] ≈ C(Na. IO 3)= 0, 10 M I = ½ (0, 1· 12 + 0, 1· 12) =0, 10 γ(Ba 2+) = 0, 44; γ(IO 3 -) = 0, 81 Ks=Ks 0 / {γ(Ba 2+)· γ(IO 3 -)2} = 5, 2· 10 -9 S = [Ba 2+] = Ks /[IO 3 -]2 = 5, 2· 10 -7 16. 02. 2018 36
Ba(IO 3)2 (насыщенный водный раствор, 0, 1 н. по Na. IO 3, с учетом ионной силы) S = [Ba 2+] = Ks /[IO 3 -]2 [IO 3 -] ≈ C(Na. IO 3)= 0, 10 M I = ½ (0, 1· 12 + 0, 1· 12) =0, 10 γ(Ba 2+) = 0, 44; γ(IO 3 -) = 0, 81 Ks=Ks 0 / {γ(Ba 2+)· γ(IO 3 -)2} = 5, 2· 10 -9 S = [Ba 2+] = Ks /[IO 3 -]2 = 5, 2· 10 -7 16. 02. 2018 36
![Влияние комплексообразования • Комплексы Аm. Bn • Молекулярная растворимость So = [Аm. Bn] • Влияние комплексообразования • Комплексы Аm. Bn • Молекулярная растворимость So = [Аm. Bn] •](https://present5.com/presentation/21878719_151569255/image-37.jpg) Влияние комплексообразования • Комплексы Аm. Bn • Молекулярная растворимость So = [Аm. Bn] • Для комплекса АВ: β = [AB]/[A][B] • Ks = [A][B]; So = β·Ks ----- • S = β·Ks + √Ks • S = [A] + [AB 2] + …+[ABn] • А + В ↔ АВ (р-р) β 1 = S o / Ks • АB + В ↔ АВ 2 (р-р) Kуст2 = [AB 2] / So [B] • АB 2 + В ↔ АВ 3 (р-р) Kуст3 = [AB 3] / [AB 2][B] • S = Ks / [B] + So· Kуст2· Кs·[B]2 +…= • = Ks( 1 / [B] + β[B]2…) = • = Ks/[B] + Ks∑β[B]i-1 16. 02. 2018 37
Влияние комплексообразования • Комплексы Аm. Bn • Молекулярная растворимость So = [Аm. Bn] • Для комплекса АВ: β = [AB]/[A][B] • Ks = [A][B]; So = β·Ks ----- • S = β·Ks + √Ks • S = [A] + [AB 2] + …+[ABn] • А + В ↔ АВ (р-р) β 1 = S o / Ks • АB + В ↔ АВ 2 (р-р) Kуст2 = [AB 2] / So [B] • АB 2 + В ↔ АВ 3 (р-р) Kуст3 = [AB 3] / [AB 2][B] • S = Ks / [B] + So· Kуст2· Кs·[B]2 +…= • = Ks( 1 / [B] + β[B]2…) = • = Ks/[B] + Ks∑β[B]i-1 16. 02. 2018 37
 • Ag. Cℓ (тв. ) ↔ Ag+ + Cℓ- Ks = 1, 8· 10 -10 • В насыщенном растворе без учета побочных процессов: • S = [Ag+] = [Cℓ-] = √ Ks = 1, 34· 10 -5 M • C учетом возможного комплексообразования: • (β = 5, 0· 102) • S = [Ag. Cℓ] + [Ag +] = [Ag. Cℓ] + [Cℓ-] • β = [Ag. Cℓ] / [Ag +]· [Cℓ-] • S =β· Ks = 9, 0· 10 -8 M « 1, 34· 10 -5 M 16. 02. 2018 38
• Ag. Cℓ (тв. ) ↔ Ag+ + Cℓ- Ks = 1, 8· 10 -10 • В насыщенном растворе без учета побочных процессов: • S = [Ag+] = [Cℓ-] = √ Ks = 1, 34· 10 -5 M • C учетом возможного комплексообразования: • (β = 5, 0· 102) • S = [Ag. Cℓ] + [Ag +] = [Ag. Cℓ] + [Cℓ-] • β = [Ag. Cℓ] / [Ag +]· [Cℓ-] • S =β· Ks = 9, 0· 10 -8 M « 1, 34· 10 -5 M 16. 02. 2018 38
 • В насыщенном растворе Ag. Cℓ, 0, 010 н. по Na. Cℓ , без учета комплексообразования • S = [Ag +]; ССℓ ~ [Cℓ-] = 0, 01 М • [Ag +] = 0, 01 Ks = 1, 8· 10 -8 М • С учетом образования комплексов • Ag. Cℓ (Kуст1 = 5, 0· 102), Ag. Cℓ 21 - (Kуст2 = 1, 7· 105) и • Ag. Cℓ 32 - (Kуст3 = 1, 1· 105): • S = [Ag +] + [Ag. Cℓ] + [Ag. Сℓ 2 -] + [Ag. Cℓ 32 -] = • = Ks( 1 / [Cℓ-] + Kуст1 + Kуст2[Cℓ-] + Kуст3[Cℓ-]2 = • = 4, 2· 10 -7 M 16. 02. 2018 39
• В насыщенном растворе Ag. Cℓ, 0, 010 н. по Na. Cℓ , без учета комплексообразования • S = [Ag +]; ССℓ ~ [Cℓ-] = 0, 01 М • [Ag +] = 0, 01 Ks = 1, 8· 10 -8 М • С учетом образования комплексов • Ag. Cℓ (Kуст1 = 5, 0· 102), Ag. Cℓ 21 - (Kуст2 = 1, 7· 105) и • Ag. Cℓ 32 - (Kуст3 = 1, 1· 105): • S = [Ag +] + [Ag. Cℓ] + [Ag. Сℓ 2 -] + [Ag. Cℓ 32 -] = • = Ks( 1 / [Cℓ-] + Kуст1 + Kуст2[Cℓ-] + Kуст3[Cℓ-]2 = • = 4, 2· 10 -7 M 16. 02. 2018 39
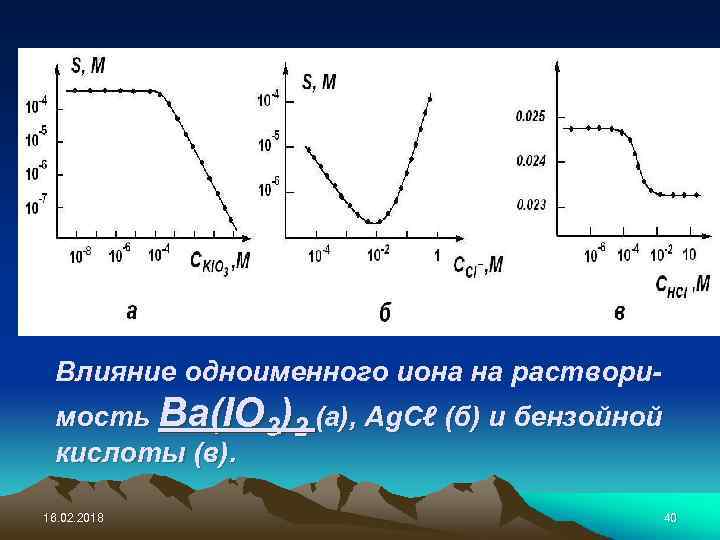 Влияние одноименного иона на растворимость Ba(IO 3)2 (а), Ag. Cℓ (б) и бензойной кислоты (в). 16. 02. 2018 40
Влияние одноименного иона на растворимость Ba(IO 3)2 (а), Ag. Cℓ (б) и бензойной кислоты (в). 16. 02. 2018 40
 • Рекомендуемая литература: • Любой учебник по аналитической химии 16. 02. 2018 41
• Рекомендуемая литература: • Любой учебник по аналитической химии 16. 02. 2018 41
 • Спасибо за внимание! 16. 02. 2018 42
• Спасибо за внимание! 16. 02. 2018 42


