 Д/з - конспект, подготовиться к С/р: - уметь устанавливать окислитель и восстановитель в реакциях конспекта; - уметь определять с. о.
Д/з - конспект, подготовиться к С/р: - уметь устанавливать окислитель и восстановитель в реакциях конспекта; - уметь определять с. о.
 СЕРА 1. Получение в промышленности: - самородная; - выделение из руд, нефти и т. п. . пирит Fe. S 2 – «золото дураков» , железный колчедан
СЕРА 1. Получение в промышленности: - самородная; - выделение из руд, нефти и т. п. . пирит Fe. S 2 – «золото дураков» , железный колчедан
 в лаборатории: Na 2 S 2 O 3 + 2 HCl = 2 Na. Cl + S↓ + SO 2↑ + H 2 O Тиосульфат натрия
в лаборатории: Na 2 S 2 O 3 + 2 HCl = 2 Na. Cl + S↓ + SO 2↑ + H 2 O Тиосульфат натрия
 2. Физические свойства У серы есть три аллотропные модификации (видоизменения): S 8 или α-S 8 – ромбическая; S 8 или β-S 8 – моноклинная; Sn – пластическая. Наиболее устойчивой является первая!
2. Физические свойства У серы есть три аллотропные модификации (видоизменения): S 8 или α-S 8 – ромбическая; S 8 или β-S 8 – моноклинная; Sn – пластическая. Наиболее устойчивой является первая!
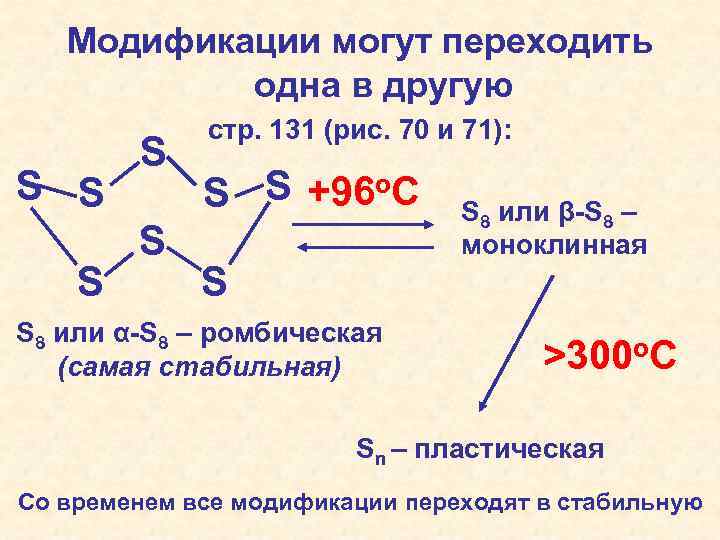 Модификации могут переходить одна в другую S S S стр. 131 (рис. 70 и 71): S S +96 o. C S S 8 или α-S 8 – ромбическая (самая стабильная) S 8 или β-S 8 – моноклинная >300 o. C Sn – пластическая Со временем все модификации переходят в стабильную
Модификации могут переходить одна в другую S S S стр. 131 (рис. 70 и 71): S S +96 o. C S S 8 или α-S 8 – ромбическая (самая стабильная) S 8 или β-S 8 – моноклинная >300 o. C Sn – пластическая Со временем все модификации переходят в стабильную
 α-S 8 ромбическая сера
α-S 8 ромбическая сера

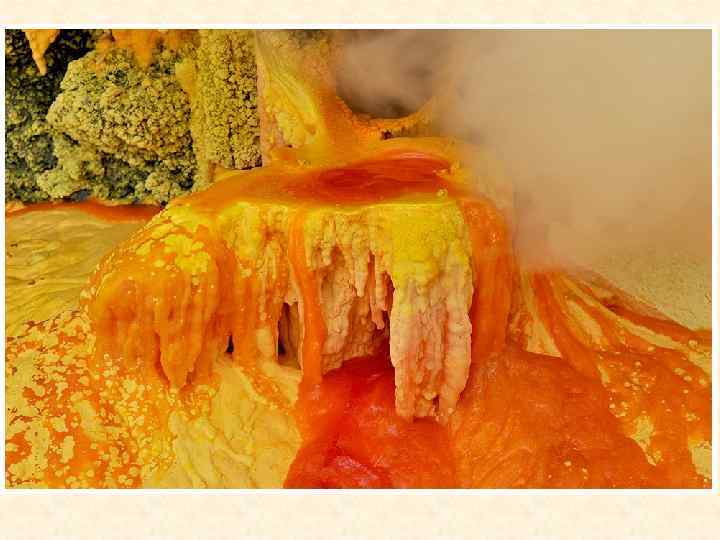

 α-S 8 тв. ; октаэдрические кристаллы, ц – лимонно-жёлтый; з – у чистой; в; не растворима в воде, малорастворима в спирте, ацетоне, диэтиловом эфире, толуоле, но лучше всего: в сероуглероде CS 2. tпл. = +112, 8 о. С, хрупкая строение – «корона»
α-S 8 тв. ; октаэдрические кристаллы, ц – лимонно-жёлтый; з – у чистой; в; не растворима в воде, малорастворима в спирте, ацетоне, диэтиловом эфире, толуоле, но лучше всего: в сероуглероде CS 2. tпл. = +112, 8 о. С, хрупкая строение – «корона»
 β-S 8 моноклинная сера
β-S 8 моноклинная сера
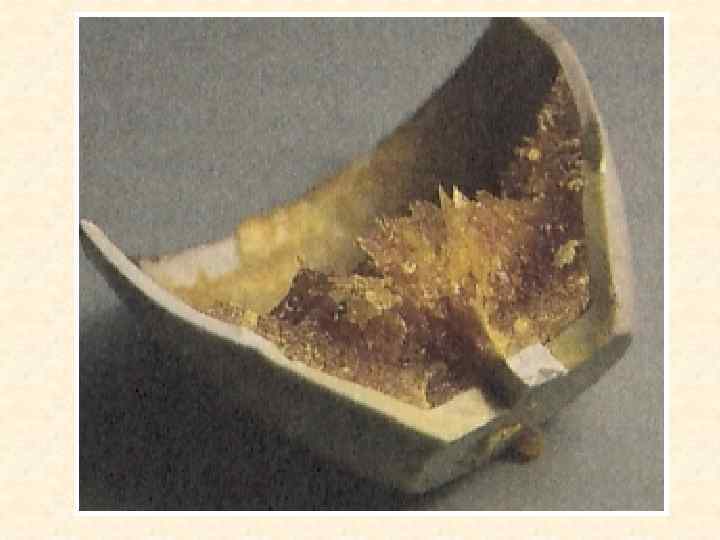

 β-S 8 тв. ; игольчатые кристаллы; ц – медово-жёлтый; з – у чистой; в; не растворима в воде, малорастворима в спирте, ацетоне, диэтиловом эфире, толуоле, но лучше всего: в сероуглероде CS 2. tпл. = +119, 3 о. С, хрупкая
β-S 8 тв. ; игольчатые кристаллы; ц – медово-жёлтый; з – у чистой; в; не растворима в воде, малорастворима в спирте, ацетоне, диэтиловом эфире, толуоле, но лучше всего: в сероуглероде CS 2. tпл. = +119, 3 о. С, хрупкая
 Sn пластическая сера
Sn пластическая сера


 Sn тв. ; прозрачная резиноподобная масса жёлтого или тёмножёлтого цвета;
Sn тв. ; прозрачная резиноподобная масса жёлтого или тёмножёлтого цвета;
 3. Химические свойства При обычных условиях сера реагирует фтором (только он окисляет серу сразу в +6 – SF 6), с щ. , щ/з металлами, медью, ртутью, серебром. Демеркуризация – стр. 132
3. Химические свойства При обычных условиях сера реагирует фтором (только он окисляет серу сразу в +6 – SF 6), с щ. , щ/з металлами, медью, ртутью, серебром. Демеркуризация – стр. 132
 При нагревании сера реагирует с остальными металлами, кроме золота и платины. Металлы образуют сульфиды: 2 Na + S = Na 2 S Hg + S = Hg. S t C Zn + S = Zn. S o
При нагревании сера реагирует с остальными металлами, кроме золота и платины. Металлы образуют сульфиды: 2 Na + S = Na 2 S Hg + S = Hg. S t C Zn + S = Zn. S o
 При нагревании сера реагирует с неметаллами: to C H 2 + S = H 2 S - сероводород t C S + O 2 = SO 2 – сернистый газ o Сера не реагирует с азотом, иодом и инертными газами.
При нагревании сера реагирует с неметаллами: to C H 2 + S = H 2 S - сероводород t C S + O 2 = SO 2 – сернистый газ o Сера не реагирует с азотом, иодом и инертными газами.
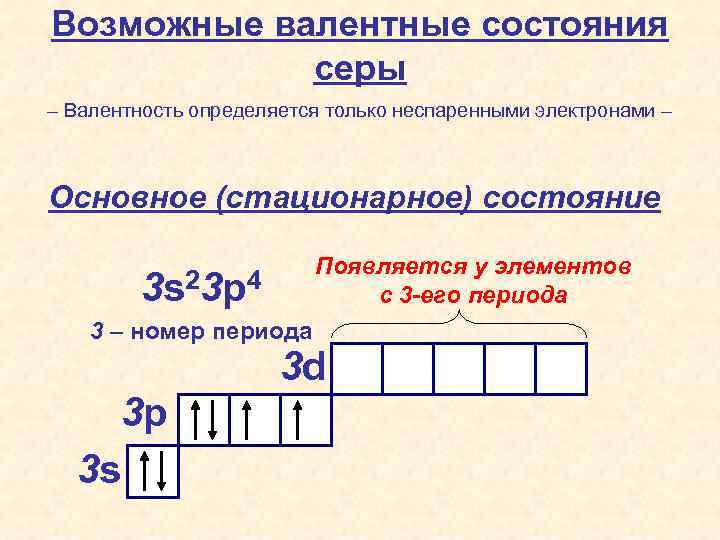 Возможные валентные состояния серы – Валентность определяется только неспаренными электронами – Основное (стационарное) состояние Появляется у элементов с 3 -его периода 3 s 23 p 4 3 – номер периода 3 d 3 p 3 s
Возможные валентные состояния серы – Валентность определяется только неспаренными электронами – Основное (стационарное) состояние Появляется у элементов с 3 -его периода 3 s 23 p 4 3 – номер периода 3 d 3 p 3 s
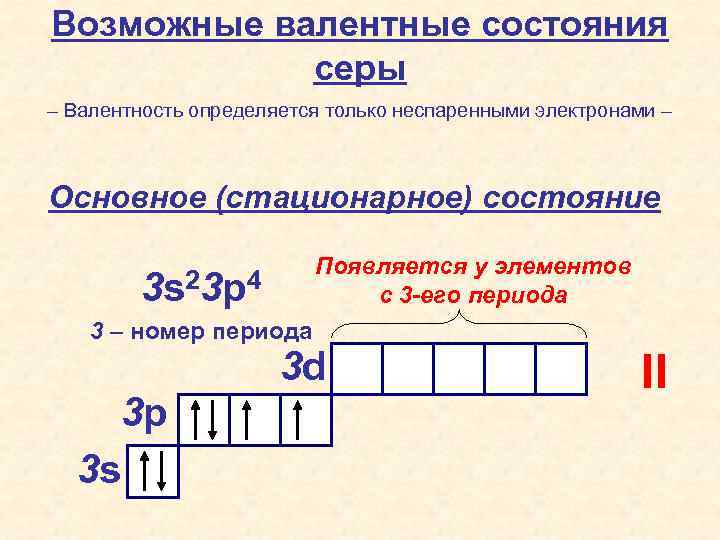 Возможные валентные состояния серы – Валентность определяется только неспаренными электронами – Основное (стационарное) состояние Появляется у элементов с 3 -его периода 3 s 23 p 4 3 – номер периода 3 d 3 p 3 s II
Возможные валентные состояния серы – Валентность определяется только неспаренными электронами – Основное (стационарное) состояние Появляется у элементов с 3 -его периода 3 s 23 p 4 3 – номер периода 3 d 3 p 3 s II
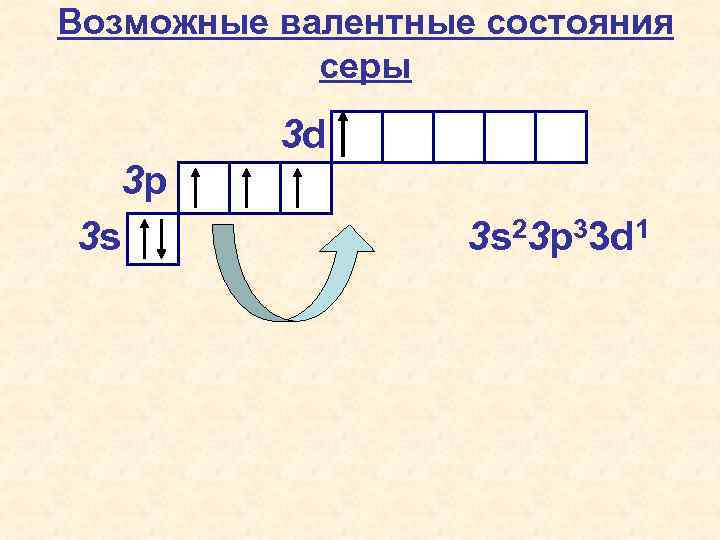 Возможные валентные состояния серы 3 d 3 p 3 s 3 s 23 p 33 d 1
Возможные валентные состояния серы 3 d 3 p 3 s 3 s 23 p 33 d 1
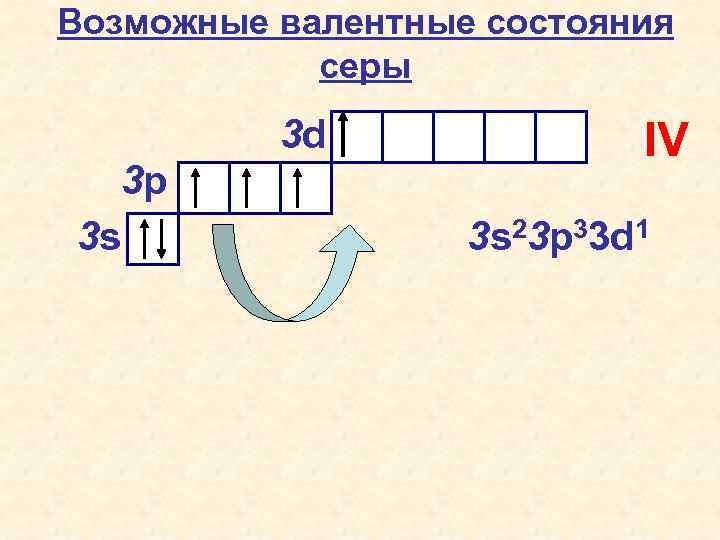 Возможные валентные состояния серы 3 d 3 p 3 s IV 3 s 23 p 33 d 1
Возможные валентные состояния серы 3 d 3 p 3 s IV 3 s 23 p 33 d 1
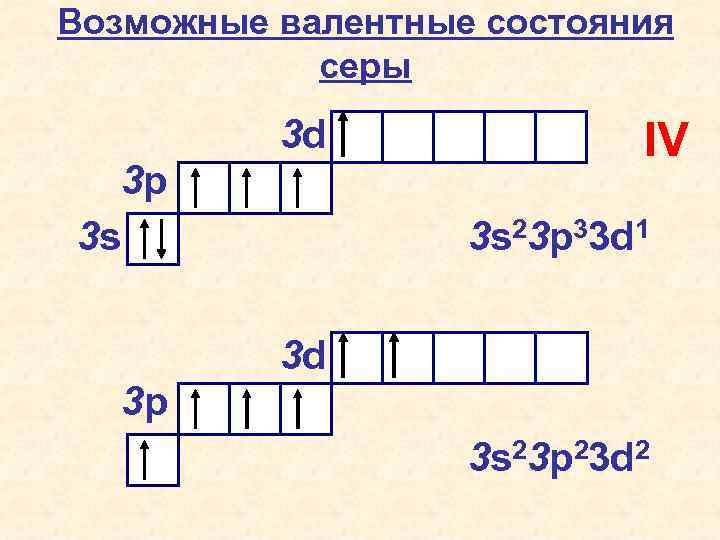 Возможные валентные состояния серы 3 d 3 p 3 s IV 3 s 23 p 33 d 1 3 d 3 p 3 s 23 p 23 d 2
Возможные валентные состояния серы 3 d 3 p 3 s IV 3 s 23 p 33 d 1 3 d 3 p 3 s 23 p 23 d 2
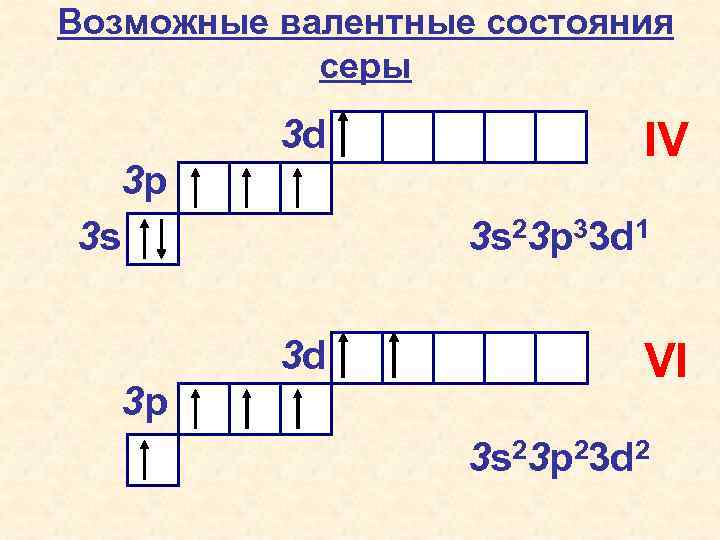 Возможные валентные состояния серы 3 d 3 p 3 s 3 s 23 p 33 d 1 3 d 3 p IV VI 3 s 23 p 23 d 2
Возможные валентные состояния серы 3 d 3 p 3 s 3 s 23 p 33 d 1 3 d 3 p IV VI 3 s 23 p 23 d 2
 Т. о. в ходе химических реакций сера проявляет следующие с. о. согласно «правилу чётности» : -2 0 сульфиды, S (S 8) гидросульфиды, H 2 S +2 SCl 2 +4 +6 SO 2 SF 6 H 2 SO 3 сульфиты, H 2 SO 4 гидро- сульфаты, сульфиты гидросульфаты
Т. о. в ходе химических реакций сера проявляет следующие с. о. согласно «правилу чётности» : -2 0 сульфиды, S (S 8) гидросульфиды, H 2 S +2 SCl 2 +4 +6 SO 2 SF 6 H 2 SO 3 сульфиты, H 2 SO 4 гидро- сульфаты, сульфиты гидросульфаты
 СЕРА. СОЕДИНЕНИЯ СЕРЫ Основные соединения: - сероводород, сероводородная кислота и её соли; - сернистый газ, сернистая кислота и её соли; - серный ангидрид, серная кислота и её соли.
СЕРА. СОЕДИНЕНИЯ СЕРЫ Основные соединения: - сероводород, сероводородная кислота и её соли; - сернистый газ, сернистая кислота и её соли; - серный ангидрид, серная кислота и её соли.


